PDF (Bab I)
advertisement

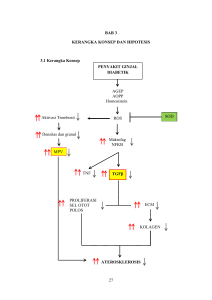
BAB I PENDAHULUAN A. Latar Belakang Masalah Radikal bebas merupakan suatu molekul yang memiliki elektron-elektron yang tidak berpasangan (unpaired), hal itu dapat menyebabkan radikal bebas menjadi senyawa yang sangat reaktif terhadap sel-sel tubuh dengan cara mengikat elektron molekul pada sel dan dapat menyebabkan oksidasi yang berlebihan (Umayah & Amrun, 2007). Menurut Sholihah & Widodo (2008), secara sederhana, radikal bebas sering disebut produk oksigen yang tereduksi secara parsial, karena berpotensi untuk menghasilkan reaksi radikal dalam sistem biologis. Radikal bebas dalam kadar yang normal sangat diperlukan oleh tubuh untuk kelangsungan beberapa proses fisiologis, terutama untuk transportasi elektron, namun radikal bebas yang berlebihan dapat membahayakan tubuh karena oksidasi yang berlebihan terhadap asam nukleat, protein, lemak dan sel DNA, sehingga dapat memicu terjadinya penyakit degeneratif seperti jantung koroner, katarak, gangguan kognisi, kanker, dan kerusakan makromolekul yang mengakibatkan terjadinya kematian sel (Wresdiyati et al, 2007). Secara normal tubuh manusia memiliki sistem pelindung yang luas berupa antioksidan alamiah yang berfungsi dalam mengendalikan radikal bebas. Bila pengendalian gagal karena terjadi kelebihan radikal bebas dan kekurangan relatif dari antioksidansia, maka dapat menyebabkan stres oksidatif sehingga berdampak pada kerusakan sel dan organ (Tjay & Rahardja, 2002). Kelebihan radikal bebas dapat disebabkan dua faktor, yaitu faktor dari dalam (internal) dan faktor dari luar (eksternal). Faktor dari dalam timbul dari tubuh manusia yang disebabkan karena stres dan penyakit yang diderita seperti diabetes mellitus dan hiperkolesterolemia (Wresdiyati et al, 2007), sedangkan faktor dari luar timbul karena aktivitas manusia dalam kehidupan sehari-hari, yaitu asap rokok, makanan yang digoreng dan dibakar, paparan sinar matahari berlebih, obat-obatan tertentu, racun, dan polusi (Umayah & Amrun, 2007). Menurut Gomes et al (2005), malondialdehida (MDA) merupakan suatu radikal bebas hasil dari metabolit lipid 1 2 peroksida yang secara luas digunakan sebagai biomarker biologis untuk menilai stress oksidatif. Lipid peroksida terbentuk karena kelebihan produk ROS (reactive oxygen species) yang menyerang komponen sel (membran lipid dan protein) dengan melibatkan residu asam lemak ganda dari fosfolipid yang sangat sensitif terhadap oksigen. Setelah terbentuk, radikal peroksil (ROO•) disusun kembali melalui reaksi siklikisasi pada endoperoksida (perkursor malondialdehid) dengan produk akhir dari proses peroksidasi menjadi MDA (Valko et a.l, 2007). Kerusakan akibat adanya radikal bebas dapat dicegah oleh senyawa antioksidan, karena mempunyai potensi untuk menanggulangi proses oksidatif sebagai dampak negatif adanya radikal bebas (Desminarti et al, 2012). Antioksidan merupakan senyawa penting bagi tubuh manusia karena berfungsi dalam menangkap radikal bebas yang banyak terbentuk dalam tubuh. Sebagian besar sumber antioksidan alami yaitu tanaman yang mengandung senyawa fenolik yang tersebar diseluruh bagian tanaman, baik di kayu, biji, daun, buah, akar, dan bunga. Senyawa fenolik dan flavonoid memiliki kemampuan untuk merubah atau mereduksi radikal bebas (Marliana, 2012). Buah kurma mengandung senyawa yang memiliki aktivitas antioksidan. Adapun jenis kurma yang dipakai dalam percobaan kali ini yaitu kurma Ajwah yang memiliki bentuk elips, berwarna merah saat belum matang kemudian berubah menjadi sawo matang. Ajwah merupakan salah satu jenis kurma yang terkenal di Madinah (Hammad, 2011). Menurut Vyawahre et al. (2009), kurma diketahui memiliki beragam aktivitas biologis seperti antiulkus, antikanker, antidiare, efek pada gastrointestinal, hepatoprotektif, antimutagenik, antioksidan, efek pada sistem reproduksi, antiinflamasi, antivirus, antihemolitik, antihiperlidemik, dan nefroprotektif. Senyawa dalam kurma yang memiliki aktivitas antioksidan meliputi senyawa fenolik, flavonoid, dan procyanidin. Kurma jenis Deglet Nour yang diekstraksi dengan aquadest terbukti memiliki efek yang sama dengan vitamin C yaitu secara signifikan dapat menurunkan MDA tikus yang telah diinduksi dengan dimetoat (Saafi et al., 2011). Kandungan vitamin C dan E, β-karoten, dan retinol yang tinggi pada ekstrak metanol kurma Zaghlool dapat menurunkan kadar MDA tikus yang mengalami stress oksidatif (Mohamed & Al-Okbi, 2004). 3 Salah satu penyebab meningkatnya radikal bebas pada tubuh manusia yaitu karena hepatotoksisitas atau kerusakan hati yang disebabkan oleh obatobatan tertentu. Shenoy et al (2012), menyatakan pemberian parasetamol dengan dosis yang berlebihan (overdose) dapat menyebabkan hepatotoksisitas dan meningkatkan MDA pada hati yang signifikan dibandingkan dengan kontrol normal yang diberi Gom acacia. Hepatotoksisitas disebabkan produk dari reaksi reaktif N-asetil-p-benzoquinon imina (NAPQI) yang dihasilkan oleh sistem sitokrom P450 pada hati yang berlebihan (overdose). Secara normal NAPQI akan didetoksifikasi oleh glutathione menjadi senyawa non toksik yang kemudian diekskresikan oleh ginjal (Knight et al, 2003). Sejauh pengetahuan penulis belum pernah ada penelitian tentang aktivitas antioksidan pada kurma Ajwah dengan melihat penurunan profil kadar MDA karena krusakan hati yang diinduksi dengan parasetamol. B. Perumusan Masalah Berdasarkan latar belakang di atas maka dapat disusun perumusan masalah, apakah pemberian ekstrak etanol buah kurma Ajwah dapat menurunkan kadar malondialdehida (MDA) pada tikus putih yang diinduksi dengan parasetamol 2,5 g/kgBB? C. Tujuan Penelitian Tujuan dilakukan penelitian ini yaitu mengetahui pemberian ekstrak etanol buah kurma Ajwah untuk menurunkan kadar malondialdehida (MDA) pada tikus putih yang diinduksi dengan parasetamol 2,5 g/kgBB. D. Tinjauan Pustaka 1. Kurma (Phoenix dactylifera) a. Klasifikasi Klasifikasi kurma sebagai berikut: Kingdom : Plantae Divisi : Magnoliophyta 4 Kelas : Liliopsida Ordo : Arecales Keluarga : Arecaceae Genus : Phoenix Spesies : P. Dactylifera Linn Nama ilmiah : Phoenix dactylifera (Vyawahare et al., 2009) b. Kandungan Kimia Kurma memiliki kandungan kimia karbohidrat, alkaloid, steroid, flavonoid, tanin esterterpen, asam fenolik (Onuh et al., 2012). Profil fenolik pada tanaman menunjukkan adanya asam sinamat (ferulat, sinapik dan asam kumarat beserta turunannya, seperti asam 5-O-kaffeoylshikimik yang juga disebut dengan asam dactyliferic), glikosida flavonoid (luteolin, metil luteolin, kuersetin, dan metil kuersetin), dan flavonol (katekin dan epikatekin). Kandungan sari kurma juga menunjukkan adanya α-amirin, triterpenoid saponin dan zat mentah gonadotropik. Terdapat juga kandungan kimia terisolasi, seperti α-D glukan, heteroksilon, dan galaktomannan (Vyawahare et al., 2009). Selain itu kurma juga mengandung sterol, prosianidin, karotenoid, antosianin, serat, vitamin seperti riboflavin, biotin, tiamin, asam askorbat dan asam folat, dan mineral seperti kalsium, besi, tembaga, kobalt, magnesium, sulfur, zinc, dan selenium (Ismail dan Radzi, 2013). c. Khasiat Kurma memiliki beberapa aktivitas yang bermanfaat diantaranya antiulkus, antikanker, anti-diare, hepatoprotektif, antimutagenik, antioksidan, antiinflamasi, antivirus, antihemolitik, nefroprotektif, antihiperlidemik, dan memiliki efek baik terhadap gastrointestinal, cisplatin dan sistem reproduksi (Vyawahare et al., 2009). d. Keamanan Menurut Agbon et al. (2014), penggunaan ekstrak kurma pada dosis 5000 mg/kgBB masih terbilang relatif aman. Pemakaian ekstrak kurma akan 5 mengakibatkan LD50 semu pada penggunaan dosis 6000 mg/kgBB (Okwuosa et al., 2014) e. Senyawa yang berperan pada aktivitas antioksidan Senyawa fenolik yang terkandung pada buah kurma memiliki aktivitas antioksidan, karena terbukti dapat menghambat kenaikan signifikan lipid peroksida dan protein oksida, ekstrak aquadest buah kurma juga memiliki potensi untuk membersihkan superperoksid dan radikal hidroksil (Vyawahare et al, 2009). Asam ferulat dan kumarat pada buah kurma bertanggung jawab sebagai senyawa yang mempunyai aktivitas antioksidan (Ismail dan Radzi, 2013). Selain senyawa fenolik, kandungan senyawa flavonoid dan procyanidin juga memiliki potensi antioksidan yang dapat menghambat lipid peroksida (Saafi et al, 2011). Tingginya kandungan vitamin dan β-karoten menjadi pendukung aktivitas antioksidan yang dimiliki buah kurma (Mohamed & Al-Okbi, 2004) b a (Vyawahare et al, 2009) Gambar 1. Struktur dari (a) senyawa fenolik yaitu asam ferulat; (b) senyawa flavonoid yaitu kuersetin 2. Antioksidan Aktivitas antioksidan dalam buah kurma secara efektif dapat mereduksi radikal bebas dalam tubuh dengan cara mengikat elektron bebas yang berlebihan, karena kaya dengan antioksidan hidrofilik yang umumnya terkait dengan adanya senyawa polifenol khususnya flavanol (Saleh et al, 2011). Senyawa antioksidan dapat mengurangi penyakit kronis akibat dari senyawa radikal bebas dengan memanfaatkan peran senyawa antioksidan seperti vitamin C, E, A, β-karoten, asam-asam fenol, polifenol, dan flavonoid, karena senyawa-senyawa tersebut memiliki karakter utama untuk menangkap dan menstabilkan radikal bebas (Prakash et al, 2001). Reaksi senyawa antioksidan pada buah kurma dalam menangkap radikal bebas dapat dilihat pada Gambar 2 dan Gambar 3. 6 (Shofia et al, 2013) Gambar 2. Reaksi penangkapan radikal bebas oleh kuersetin beserta muatan proton pada atom OH Gambar 3. Reaksi penangkapan radikal bebas oleh asam ferulat beserta muatan proton pada atom OH 3. Radikal bebas Radikal bebas merupakan suatu molekul yang memiliki elektron-elektron yang tidak berpasangan (unpaired), hal itu dapat menyebabkan radikal bebas menjadi senyawa yang sangat reaktif terhadap sel-sel tubuh dengan cara mengikat elektron molekul pada sel dan dapat menyebabkan oksidasi yang berlebihan (Umayah & Amrun, 2007). Terdapat dua jenis radikal bebas, yaitu reactive oxygen species (ROS) dan reactive nitrogen species (RNS) yang memiliki peran ganda, dapat sebagai perusak dan bermanfaat. ROS dan RNS biasanya dihasilkan oleh enzim yang diatur secara ketat, seperti NO sintesis (NOS) dan NADPH (nicotinamide adenin dinuclotide phosphate hydrogen) oksidase isoform. 7 Kelebihan produk ROS (timbul baik dari rantai transport elektron mitokondria atau stimulasi kelebihan NADPH) menghasilkan stres oksidatif, yaitu suatu proses perusakan yang dapat menjadi mediator penting dari kerusakan struktur sel (membran lipid dan protein) dan DNA (deoxyribose nucleic acid). ROS yang berlebihan tidak hanya menyerang pada DNA, tetapi juga komponen seluler lainnya yang melibatkan residu asam lemak tak jenuh ganda dari fosfolipid yang sangat sensitif terhadap oksidasi. Setelah terbentuk, radikal peroksil (ROO•) disusun kembali melalui reaksi siklikisasi pada endoperoksida (perkursor malondialdehid) dengan produk akhir dari proses peroksidasi menjadi malondialdehid (MDA) (Valko et al, 2007). MDA merupakan suatu radikal bebas hasil dari metabolit peroksidasi lipid yang secara luas digunakan sebagai biomarker biologis peroksidasi lipid untuk menilai stress oksidatif (Gomes et al, 2005). Terdapat banyak faktor-faktor yang dapat menyebabkan pembentukan ROS (Gambar 5). 4. Parasetamol a. Defenisi parasetamol Parasetamol atau asetaminofen (N-asetil-4-aminofenol) mengandung tidak kurang dari 98,0% dan tidak lebih dari 101,0% C8H9NO2, dihitung terhadap zat yang telah dikeringkan. Parasetamol memiliki pemerian serbuk hablur putih, tidak berbau, dan rasanya pahit. Larut dalam 70 bagian air, dalam 7 bagian etanol 96%, dalam 13 bagian aseton, dalam 40 bagian gliserol, dan dalam 9 bagian propilenglikol (Depkes RI, 1979). Parasetamol memiliki khasiat analgetik dan antipiretik, namun bukan antiradang. Obat ini umumnya dianggap sebagai zat antinyeri yang paling aman, termasuk juga untuk swamedikasi (pengobatan mandiri) (Tjay & Rahardja, 2002). (Depkes RI, 1979) Gambar 4. Struktur Parasetamol 8 b. Efek samping Efek samping penggunaan parasetamol pada dosis yang dianjurkan jarang terjadi. Namun dilaporkan adanya keluhan ruam kulit, kelainan darah (trombositopenia, leukopenia, dan neutropenia), hipotensi, kerusakan hati, dan kerusakan ginjal yang disebabkan penggunaan dosis yang berlebihan (BPOM RI, 2008). Menurut Tjay & Rahardja (2002), efek samping yang sering ditimbulkan antara lain reaksi hipersensitifitas dan kelainan darah. Pada penggunaan kronis dosis 3-4 gram sehari dapat terjadi kerusakan hati, pada dosis diatas 6 gram mengakibatkan nekrosis hati yang tidak reversible. c. Hepatotoksisitas Pemberian parasetamol yang berlebihan (overdose) menyebabkan hepatotoksisitas. Karena parasetamol akan dimetabolisme oleh hati dengan enzim sitokrom P450 yang kemudian menjadi produk reaktif yaitu NAPQI (Knight et al, 2003). Pembentukan radikal bebas oleh sitrokrom P450 pada hati, terjadi didalam retikulum endoplasma (Gambar 5). Umumnya NAPQI secara cepat akan didetoksifikasi oleh cadangan glutation (GSH) sel aktif yang mengandung gugus sulfinil yang akan berikatan dengan NAPQI. Reaksi GSH dengan NAPQI akan menghasilkan pembentukan konjugat sistein dan asam merkapturat yang diekskresikan dalam urin, sehingga tidak menimbulkan ketoksikan. Akan tetapi, jika laju reaksi pembentukan NAPQI lebih besar daripada laju detoksifikasi oleh GSH dan jumlah NAPQI berlebihan maka akan terjadi peroksidasi lipid (Murugesh dkk., 2005). Karena kelebihan metabolit NAPQI, maka akan terjadi ikatan dengan makromolekul protein sel hati dan mereduksi O2 manjadi O2•, sehingga menjadi radikal yang reaktif (ROS) yang kemudian akan mengoksidasi fosfolipid dengan proses inisiasi, propagasi, dan terminasi (Gibson & Skett, 1991). 9 Chloroplast: - PSI: electron transport chain Fd, 2Fe-2S, and 4Fe-4s cluster - PSII: electron transport cahain QA dan QB - Chlirophyll pigmen Endoplasmic reticulum: NADPH-dependent electron transport involving Cyt P450 Peroxisome: - Matrix: Xanthine oxidase (XOD) - Membrane: Electron transport chain flavoprotein NADH and Cyt b - Metabolic processes: glycolate oxidase, fatty acid oxidation, flavin oxidases, disproportionation of O2•- radicals ROS Plasma membrane: Electron transporting oxidoreductase NADPH oxidase, quinone oxidase Cell wall: Cell-wall-associated peroxidase diamine oxidase Apoplast: Cell-wall-associated oxalate oxidase dan amine oxidase Mitochondria: - Complex I: NADH dehydrogenase segment - Complex II: reverse electron flow to complex I - Complex III: ubiquinone-cytochrome region Enzyme: Aconitase, 1-galactono-ᵧ lactone,dehydrogenase (GAL) (Sharma et al, 2012) Gambar 5. Faktor-faktor pembentukan ROS E. Landasan Teori Radikal bebas secara sederhana sering disebut produk oksigen yang tereduksi secara parsial, sehingga memiliki potensi untuk menghasilkan reaksi radikal dalam sistem biologis (Sholihah & Widodo, 2008). Jumlah radikal bebas yang berlebihan dalam tubuh dapat membahayakan tubuh karena bisa terjadi oksidasi yang berlebihan terhadap asam nukleat, protein, lemak dan sel DNA, sehingga dapat memicu terjadinya penyakit degeneratif seperti jantung koroner, katarak, gangguan kognisi, kanker, dan kerusakan makromolekul yang mengakibatkan terjadinya kematian sel (Wresdiyati et al, 2007). Antioksidan merupakan senyawa penting bagi tubuh manusia karena berfungsi dalam menangkap radikal bebas yang banyak terbentuk dalam tubuh (Marliana, 2012). Senyawa antioksidan dapat mengurangi penyakit kronis akibat dari senyawa 10 radikal bebas dengan memanfaatkan peran senyawa antioksidan seperti vitamin C, E, A, β-karoten, asam-asam fenol, polifenol, dan flavonid, karena senyawasenyawa tersebut memiliki karakter utama untuk menangkap dan menstabilkan radikal bebas (Prakash et al, 2001). Senyawa-senyawa fenolik dan flavonoid yang terkandung pada buah kurma memiliki aktivitas antioksidan, karena terbukti dapat menghambat kenaikan signifikan lipid peroksida dan protein oksida (Vyawahare et al, 2009). Asam ferulat dan kumarat pada buah kurma juga bertanggungjawab sebagai aktivitas antioksidan (Ismail dan Radzi, 2013). F. Hipotesis Ekstrak etanol buah kurma Ajwah (Phoenix dactylifera) memiliki aktivitas antioksidan dengan menghambat produksi malondialdehid (MDA) tikus putih yang telah diinduksi parasetamol 2,5 g/kgBB.