BAB I - Universitas Sumatera Utara
advertisement
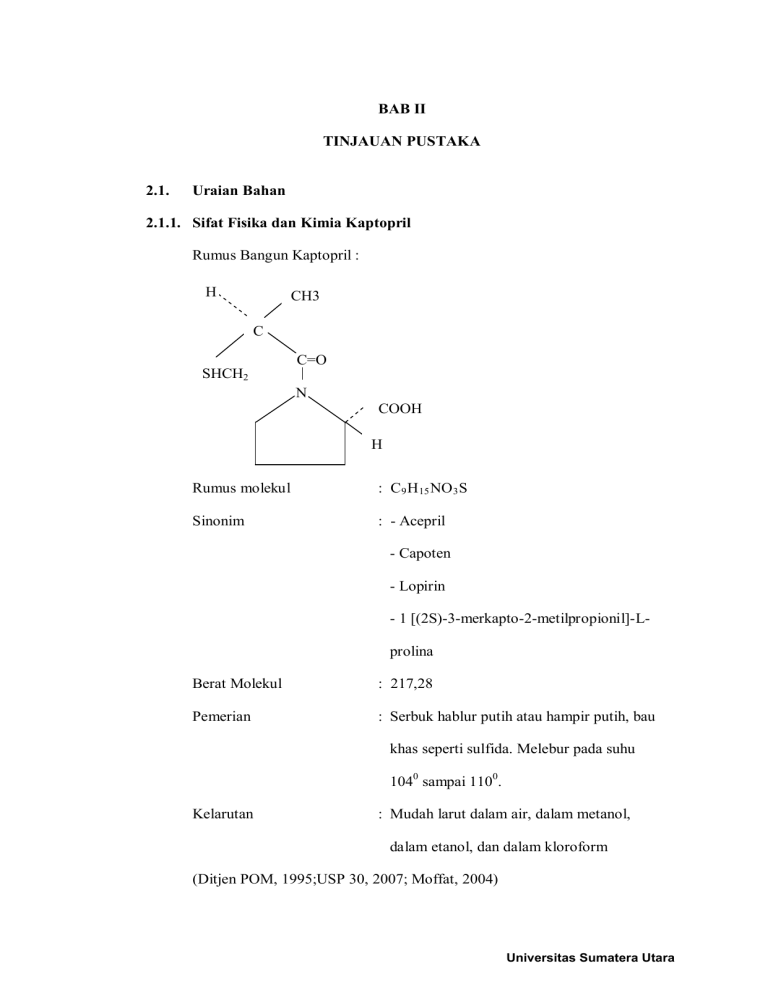
BAB II TINJAUAN PUSTAKA 2.1. Uraian Bahan 2.1.1. Sifat Fisika dan Kimia Kaptopril Rumus Bangun Kaptopril : H CH3 C C=O SHCH2 N COOH H Rumus molekul : C 9 H 15 NO 3 S Sinonim : - Acepril - Capoten - Lopirin - 1 [(2S)-3-merkapto-2-metilpropionil]-Lprolina Berat Molekul : 217,28 Pemerian : Serbuk hablur putih atau hampir putih, bau khas seperti sulfida. Melebur pada suhu 1040 sampai 1100. Kelarutan : Mudah larut dalam air, dalam metanol, dalam etanol, dan dalam kloroform (Ditjen POM, 1995;USP 30, 2007; Moffat, 2004) Universitas Sumatera Utara 2.1.2. Kegunaan Tujuan Penggunaan adalah sebagai terapi pada hipertensi esensial dan hipertensi renovaskuler (Tjay dan Kirana, 2002). 2.1.3. Efek Samping Efek sampingnya yang sering terjadi adalah hilangnya rasa (kadangkadang juga penciuman), batuk kering, dan exanthema (Tjay dan Kirana, 2002). 2.1.4. Dosis Untuk hipertensi: 1-2 kali sehari 25 mg, bila perlu setelah 2-3 minggu 1-2 kali sehari 50 mg. Gagal jantung: 3 kali sehari 12,5-25 mg (Tjay dan Kirana, 2002). 2.1.5. Farmakologi Kaptopril mengandung gugus SH yang dapat berinteraksi membentuk kelat dengan ion Zn dalam tempat aktif ACE, terjadi hambatan secara kompetitif ACE sehingga peredaran angiotensin II dan kadar aldosteron menurun. Akibatnya, tidak terjadi vasokonstriksi dan retensi Na, sehingga tekanan darah menurun Mekanisme yang lain dari senyawa penghambat ACE adalah menghambat pemecahan bradikinin menjadi fragmen tidak aktif, sehingga kadar bradikinin dalam darah meningkat, menyebabkan vasodilatasi dan penurunan tekanan darah. Penghambat ACE memiliki peran khusus yang penting dalam pengobatan pasien dengan nefropati diabetes karena dapat mengurangi proteinuria dan menstabilkan fungsi ginjal (bahkan walaupun tidak terjadi penurunan tekanan darah). Ginjal memegang peranan utama pada pengaturan tingginya tekanan darah, yang berlangsung melalui suatu sistem khusus, yakni Sistem ReninAngiotensin, singkatnya RAS. Bila volume darah yang mengalir melalui ginjal Universitas Sumatera Utara berkurang dan tekanan darah di glomeruli ginjal menurun, misalnya karena penyempitan arteri setempat, maka ginjal dapat membentuk dan melepaskan enzim proteolitis renin. Dalam plasma, renin menghidrolisa protein angiotensinogen (yang terbentuk di dalam hati) menjadi angiotensin I (AT I). Zat ini diubah oleh enzim ACE (Angiotensin Converting Enzyme, yang disintesa di paru-paru) menjadi zat aktif angiotensin II. AT II ini kuat, dan menstimulasi sekresi hormon aldosteron oleh anak-ginjal dengan sifat retensi garam dan air. Akibatnya ialah volume darah dan tekanan darah naik. Faktor-faktor yang dapat meningkatkan tekanan darah antara lain: mengkonsumsi terlalu banyak garam, stress, merokok, kehamilan. Tindakantindakan umum untuk menurunkan tekanan darah; menguruskan badan, mengurangi garam dalam pola makan, berhenti merokok, membatasi minum kopi dan alkohol, cukup istirahat dan tidur. Pengobatan dengan antihipertensi dimulai dengan dosis rendah agar tekanan darah jangan menurun terlalu drastis dengan mendadak. Kemudian, setiap 1-2 minggu dosis berangsur-angsur dinaikkan sampai tercapai efek yang diinginkan. Begitu pula penghentian terapi harus secara berangsur pula (Tjay dan Kirana, 2002). 2.2. Spektrofotometri 2.2.1. Teori Spektrofotometri Spektrofotometer sesuai dengan namanya adalah alat yang terdiri dari spektrometer dan fotometer. Spektrometer menghasilkan sinar dari spektrum dengan panjang gelombang tertentu dan fotometer adalah alat pengukur intensitas cahaya yang ditransmisikan atau yang diabsorpsi. Jadi spektrofotometer Universitas Sumatera Utara digunakan untuk mengukur energi secara relatif jika energi tersebut ditransmisikan, direfleksikan atau diemisikan sebagai fungsi dari panjang gelombang (Khopkar,1990). Sinar ultraviolet mempunyai panjang gelombang antara 200-400 nm, sementara sinar tampak mempunyai panjang gelombang 400-800 nm (Ditjen POM, 1995). Berikut ini adalah uraian bagian-bagian spektrofotometer. 1. Sumber-sumber lampu; lampu deutrium digunakan untuk daerah UV pada panjang gelombang dari 190-350 nm, sementara lampu halogen kuarsa atau lampu tungsten digunakan untuk daerah visibel (pada panjang gelombang antara 350-900 nm). 2. Monokromator: digunakan untuk memperoleh sumber sinar yang monokromatis. Alatnya dapat berupa prisma ataupun grating. Untuk mengarahkan sinar monokromatis yang diinginkan dari hasil penguraian. 3. Sel absorpsi: Pada pengukuran didaerah tampak, kuvet kaca atau kuvet kaca corex dapat digunakan, tetapi untuk pengukuran pada daerah UV kita harus menggunakan sel kuarsa karena gelas tidak tembus cahaya pada daerah ini. Umumnya tebal kuvet adalah 10 mm, tetapi yang lebih kecil ataupun yang lebih besar dapat digunakan. Sel yang biasa digunakan berbentuk persegi, tetapi bentuk silinder dapat juga digunakan. Kita harus menggunakan kuvet yang bertutup untuk pelarut organik. Sel yang baik adalah kuarsa atau gelas hasil leburan serta seragam keseluruhannya. Universitas Sumatera Utara 4. Detektor: Peranan detektor penerima adalah memberikan respon terhadap cahaya pada berbagai panjang gelombang (Khopkar, 1990; Rohman, 2007). 2.2.2. Penyerapan radiasi oleh Molekul Semua molekul mempunyai energi yang dapat digambarkan menjadi beberapa fenomena. (1) molekul secara keseluruhan dapat bergerak yang kejadian ini disebut dengan translasi; energi yang berhubungan dengan translasi disebut dengan energi translasional, E trans ; (2) bagian molekul (atom atau sekelompok atom) dapat bergerak karena berkenaan satu sama lain. Gerakan ini disebut dengan vibrasi dan energinya dinamakan dengan energi vibrasional, E vibr ; (3) molekul dapat berotasi pada sumbunya dan rotasi ini dikarakterisasi dengan energi rotasional, E rot ; (4) disamping bentuk gerakan – gerakan tersebut, suatu molekul memiliki konfigurasi elektronik, dan energinya (energi elektronik, E elek ) tergantung pada keadaan elektronik molekul. Sinar ultraviolet dan sinar tampak memberikan energi yang cukup untuk terjadinya transisi elektronik. Dengan demikian, spektra ultraviolet dan spektra tampak dikatakan sebagai spektra elektronik. Jika suatu molekul sederhana dikenakan radiasi elektromagnetik maka molekul tersebut akan menyerap radiasi elektromagnetik yang energinya sesuai. Interaksi antara molekul dengan radiasi elektromagnetik ini akan meningkatkan energi potensial elektron pada tingkat keadaan tereksitasi. Apabila pada molekul yang sederhana tadi hanya terjadi transisi elektronik pada satu macam gugus yang terdapat pada molekul, maka hanya akan terjadi satu absorpsi yang merupakan garis spektrum. Universitas Sumatera Utara Pada kenyataannya, spektrum UV – Vis yang merupakan korelasi antara absorbansi (sebagai ordinat) dan panjang gelombang (sebagai absis) bukan merupakan garis spektrum akan tetapi merupakan suatu pita spektrum. Terbentuknya pita spektrum UV-Vis tersebut disebabkan oleh terjadinya eksitasi elektronik lebih dari satu macam pada gugus molekul yang sangat kompleks. Terjadinya dua atau lebih pita spektrum UV-Vis diberikan oleh molekul dengan struktur yang lebih kompleks karena terjadi beberapa transisi sehingga mempunyai lebih dari satu panjang gelombang maksimal (Rohman, 2007). Kromofor adalah bagian molekul yang mengabsorpsi dalam daerah ultra violet dan daerah sinar tampak. Dalam satu molekul dapat dikandung beberapa kromofor. Sebagai contoh C=O, dan NO 2 . Dilihat dari struktur kaptopril yang mempunyai kromofor (C=O), maka senyawa ini dapat menyerap radiasi pada daerah ultraviolet. Pada gugus karbonil, disamping mempunyai sepasang elektron sigma dan sepasang elektron pi, juga terdapat dua pasang elektron bebas, sehingga dapat terjadi beberapa transisi (Silverstein, 1986). Menurut hukum Lambert, serapan (A) berbanding lurus dengan ketebalan lapisan (b) yang disinari : A = k.b Dengan bertambahnya ketebalan lapisan, serapan akan bertambah. Menurut Hukum Beer, yang hanya berlaku untuk cahaya monokromatis dan larutan yang sangat encer, serapan (A) dan konsentrasi (c) adalah : A = k.c Jika konsentrasi bertambah, jumlah molekul yang dilalui berkas sinar akan bertambah, sehingga serapan juga bertambah. Kedua persamaan ini digabungkan Universitas Sumatera Utara dalam hukum Lambert-Beer, maka diperoleh bahwa serapan berbanding lurus dengan konsentrasi dan ketebalan lapisan: A = k.c.b Umumnya digunakan dua satuan c (konsentrasi zat yang menyerap) yang berlainan, yaitu gram per liter atau mol per liter. Nilai tetapan (k) dalam hukum Lambert-Beer tergantung pada sistem konsentrasi mana yang digunakan. Bila c dalam gram perliter, tetapan disebut dengan absorptivitas (a) dan bila dalam mol per liter tetapan tersebut adalah absortivitas molar (Є). Jadi dalam sistem dikombinasikan, hukum Lambert-Beer dapat mempunyai dua bentuk: A = a.b.c g/liter atau A = Є . b. C mol/liter Penandaan lain untuk a adalah ekstingsi spesifik, koefisien ekstingsi, dan indeks absorbansi, sedangkan Є adalah koefisien ekstingsi molar (Day and Underwood, 1999; Rohman, 2007)). Beberapa pengertian istilah dalam spektrofotometri a. Kromofor, adalah suatu gugus atom yang menyebabkan terjadinya absorpsi cahaya. b. Auksokrom, adalah suatu gugus atom yang apabila terikat kepada suatu kromofor akan menambah panjang gelombang dan intensitas resapan maksimum (absorbans) ke arah panjang gelombang yang lebih panjang. c. Efek batokrom, adalah pergeseran panjang gelombang resapan maksimum kearah panjang gelombang lebih panjang. Disebut juga Red Shift Effect. d. Efek hipsokrom, adalah pergeseran panjang gelombang yang lebih pendek. Disebut juga Blue Shift Effect. Universitas Sumatera Utara e. Efek hipokrom, adalah pergeseran intensitas resapan kearah intensitas yang lebih kecil. f. Efek hiperkrom, adalah pergeseran intensitas resapan ke arah intensitas yang lebih besar ( Silverstein, 1986). Hal–hal yang harus diperhatikan dalam analisis spektofotometri ultraviolet a. Pemilihan panjang gelombang maksimum Panjang gelombang yang digunakan untuk analisis kuantitatif adalah panjang gelombang dimana terjadi serapan maksimum. Untuk memperoleh panjang gelombang serapan maksimum, dilakukan dengan membuat kurva hubungan antara absorbansi dengan panjang gelombang dari suatu larutan baku pada konsentrasi tertentu. b. Pembuatan Kurva Kalibrasi Dibuat seri larutan baku dari zat yang akan dianalisis dengan berbagai konsentrasi. Masing – masing absorbansi larutan dengan berbagai konsentrasi diukur, kemudian dibuat kurva yang merupakan hubungan antara absorbansi dengan konsentrasi. Bila hukum Lambert-Beer terpenuhi maka kurva kalibrasi berupa garis lurus. c. Pembacaan absorbansi sampel atau cuplikan Absorbansi yang terbaca pada spektrofotometer hendaknya antara 0,2 sampai 0,8 atau 15 % sampai 70% jika dibaca sebagai transmitans. Anjuran ini berdasarkan anggapan bahwa pada kisaran nilai absorbansi tersebut kesalahan fotometrik yang terjadi adalah paling minimal (Rohman, 2007). Universitas Sumatera Utara 2.3. Titrasi dengan Kalium Iodat Metode titrimetri masih digunakan secara luas karena merupakan metode yang murah dan mampu memberikan ketepatan (presisi) yang tinggi. Titrasi redoks merupakan salah satu dari metode-metode titrimetri yang digunakan dalam bidang farmasi. Beberapa cara titrasi redoks, salah satunya adalah dengan menggunakan Kalium Iodat (Rohman, 2007). Dilihat dari struktur kaptopril yang memiliki gugus merkaptan, maka penetapan kadar senyawa obat ini dapat dilakukan secara Iodatometri. Dimana gugus merkaptannya dioksidasi oleh iodium, yang diperoleh dari kalium iodat dan kalium iodida. Titik akhir titrasi ditandai dengan terbentuknya warna biru yang dihasilkan komplek iodium dengan amilum (Siggia, 1963). 2.4. Validasi Validasi adalah suatu tindakan penilaian terhadap parameter tertentu pada prosedur penetapan yang dipakai untuk membuktikan bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya (Harmita, 2004). Parameter analisis yang ditentukan pada validasi adalah akurasi, presisi, kespesifikan, limit deteksi, kelinieran, dan rentang. Akurasi dari suatu metode analisis adalah kedekatan nilai hasil uji yang diperoleh dengan prosedur tersebut dari harga sebenarnya, sering kali dinyatakan dalam persen perolehan kembali analit pada penentuan kadar sampel yang mengandung analit dalam jumlah diketahui. Akurasi merupakan ukuran ketepatan prosedur analisis. Universitas Sumatera Utara Akurasi prosedur analisis ditentukan dengan menerapkan prosedur tersebut pada sampel atau campuran komponen matriks yang telah dibubuhi analit dalam jumlah diketahui. Presisi dari suatu metode analisis adalah derajat kesesuaian diantara masing-masing hasil uji, jika prosedur analisis diterapkan berulang kali pada sejumlah cuplikan yang diambil dari satu sampel homogen. Presisi dinyatakan sebagai deviasi standar atau deviasi standar relatif ( koefisien variasi). Presisi dapat diartikan pula sebagai derajat reprodusibilitas atau keterulangan dari prosedur analisis. Kespesifikan dari suatu metode analisis adalah kemampuannya untuk mengukur kadar analit secara khusus dengan akurat, disamping komponen lain yang terdapat dalam matriks sampel. Limit deteksi adalah nilai parameter uji batas, yaitu konsentrasi analit terendah yang dapat dideteksi. Kelinieran suatu metode analisis adalah kemampuan untuk menunjukkan bahwa nilai hasil uji langsung atau setelah diolah secara matematika, proporsional dengan konsentrasi analit dalam sampel dalam batas rentang konsentrasi tertentu. Rentang suatu metode analisis adalah interval antara batas konsentrasi tertiggi dan konsentrasi terendah analit yang dapat ditentukan dengan presisi, akurasi, dan kelinieran (Satiadarma, 2004). Universitas Sumatera Utara











