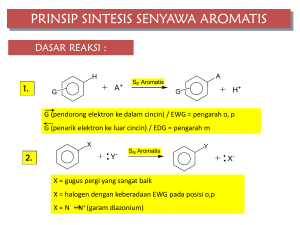
Reaksi alkohol
advertisement

ALKOHOL STRUKTUR TATA NAMA SIFAT - SIFAT REAKSI DAN KEGUNAAN Alkohol Struktur molekul alkohol sama dengan molekul air O O H H H OH Hilang 1 H, tambah 1 gugus R R R H OH Alkohol atau gugus hidroksil (OH) merupakan gugus fungsional alkohol C O H Tempat umumnya reaksi terjadi Karbon alkohol Gugus alkohol Klasifikasi alkohol Alkohol primer (1o) : hanya mempunyai satu karbon yang terikat pada karbon alkohol Alkohol sekunder (2o) : mempunyai dua karbon yang terikat pada karbon alkohol Alkohol tersier (3o) : mempunyai tiga karbon yang terikat pada karbon alkohol H R C OH H 1O I R R C OH I R R C OH II H R 2O 3O Alkohol juga dapat diklasifikasikan menjadi : 1. Monohidrat : hanya mempunyai satu gugus OH per molekul 2. Dihidrat : mempunyai dua gugus OH per molekul 3. Trihidrat : mempunyai tiga gugus OH per molekul Contoh Nama IUPAC Rumus Td (oC) Metanol CH3OH 65.0 Etanol 1 – Propanol 1 - Butanol CH3CH2OH CH3CH2CH2OH CH3CH2CH2CH2OH 78.5 97.0 117.0 Tata nama alkohol 1. Beberapa anggota pertama kelompok alkohol diberi nama umum. Nama umum biasanya dibentuk dari nama alkil yang bergabung dengan gugus OH, diikuti dengan kata alkohol. gugus etil gugus metil Contoh : CH3 – OH CH3CH2 – OH Metil alkohol Etil Alkohol • . 4 3 2 1 • Sistem IUPAC : • Contoh : CH3CH2CH2CH2OH 1-butanol • Pilihlah rantai karbon terpanjang yang mengikat gugus – OH sebagai rantai induk • Akhiran –a dari alkana induk diganti dengan –ol • Lokasi gugus –OH diberi nomor sesuai dengan karbon yang mengikatnya, sebelum nama alkohol. Pisahkan nomor dari nama dengan tanda – 2. Nama alkohol dengan gugus –OH lebih dari satu, ganti akhiran ol dengan diol (untuk dua gugus –OH), triol (tiga gugus –OH) dan seterusnya. 5 4 3 2 1 CH3CH2CH CH2 CH OH OH 1,3 – pentanadiol Dalam alkohol siklik, karbon yang mengikat –OH diberi nomor 1 OH 1 5 2 4 3 CH3 Latihan Beri nama IUPAC senyawa berikut ini : 1. C H H C H O H 2. C H C H C H C H 3C 3 2 2 O H O H O H O H 3. C H 3 Sifat fisik alkohol - 1) O + H CH3 CH3 + Ikatan hidrogen • Adanya perbedaan keelektronegatifan antara karbon dan oksigen alkohol bersifat polar sehingga sifat fisik alkohol berbeda dengan hidrokarbon yang MR nya hampir sama (titik didih, titik leleh) H 2) H + H + R -O O H + O + H + H O +H O - R -O H + + R 2 ikatan hidrogen permolekul alkohol -O H + 3 ikatan hidrogen permolekul air H + H H + O CH4 (Mr 16) titik didih –161 H2O (Mr 18) 100 CH3OH (Mr 32) 65 3) CH3CH2CH2OH n – propil alkohol (titik didih 97o) C H HC H 3C 2 C H HC H 2 C 2 O HO H propilen glikol (titik didih 189o) O HO HO H gliserol (titik didih 290o) • Titik didih alkohol trihidrat > dihidrat > monohidrat, karena pada trihidrat pembentukan ikatan hidrogen lebih banyak O 4) Tidak ada ikatan H R Ujung nonpolar H H Ujung polar H O H O H C C C C O H • Alkohol larut dalam air, makin banyak gugus OH yang terikat, makin banyak cabang maka kelarutan dalam air makin mudah. Reaksi alkohol Hidrasi (penambahan air) dari suatu alkena menghasilkan suatu alkohol. H R C alkena H C H+H OH H+ H H R C C OH H alkohol 2o Reaksi alkohol melibatkan pemutusan ikatan R O H R O H H Dehidrasi alkohol Dehidrasi / hilangnya komponen air ( H dan OH) gugus –OH dari karbon alkohol dan atom H dari karbon yang terikat pada karbon alkohol. Asam sulfat (H2SO4) bertindak sebagai zat penarik air dan sebagai katalis C alkohol + C C HO 180 C C C + HOH H OH Alkohol primer Dehidrasi alkohol sekunder akan menghasilkan dua isomer alkena. Aturan Saytzeff’s : pada dehidrasi alkohol, hidrogen yang lepas dari atom karbon yang terikat karbon alkohol dengan jumlah H paling sedikit. HO + CH3CH2CH CH3 CH3CH CHCH3 + CH3CH2CH 180 C 2 – Butena 1 – Butena OH ( 80% ) ( 20% ) 2 – Butanol CH2 + H2 Latihan : Sempurnakan reaksi dehidrasi dibawah ini + H a) C H C H O H 3 2 1 8 0 C + H b) CH3CH2CH2OH O 180 C CH3 c) CH3 CH CH CH3 OH OH d) CH3CH2CH2CH CH3 Oksidasi alkohol Oksidasi alkohol : bertambahnya oksigen atau hilangnya hidrogen zat pengoksidasi : K2Cr2O7, KMnO4 Oksidasi alkohol terjadi dengan lepasnya satu H dari gugus OH dan satu H dari karbon alkohol, diikuti dengan pembentukan ikatan rangkap C = O. Air terbentuk bila hidrogen yang dibebaskan bersatu dengan oksigen dari zat pengoksidasi Oksidasi alkohol primer C O H (O) R C O + H2O ALDEHID H .. R O H (O) R C OH ASAM KARBOKSILAT .. H Oksidasi alkohol sekunder OH R C O R' (O) R H C R' + H2O KETON Oksidasi alkohol tersier OH (O) R C R'' R' Tidak ada H Oksidasi alkohol di dalam tubuh NAD+ (nikotin amida adenin dinukleotida) adalah zat pengoksidasi di dalam tubuh untuk reaksi yang dikatalis oleh enzim. Konsumsi alkohol • Etanol digunakan sebagai minuman, obat-obatan, dan pelarut dalam sejumlah bahan farmasetikal, padahal etanol adalah racun. Etanol dapat menyebabkan liver mengeras, kematian sel-sel otak, dan kecanduan. • Konsumsi alkohol oleh ibu hamil akan menyebabkan Fetal Alcohol Syndrome (FAS), bayi yang terkena FAS tumbuh tidak normal, mental terbelakang, dan bentuk muka cacat. • Kadar alkohol dalam darah 0,05-0,15%, menghambat koordinasi, di atas 0,01% bersifat racun, 0,3-0,5% menghilangkan kesadaran dengan resiko kematian.