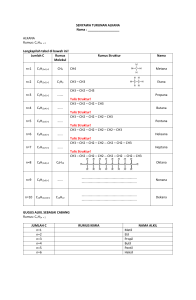
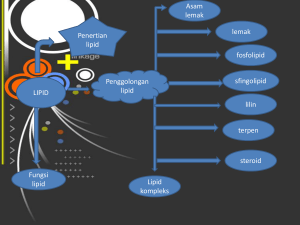
gugus fungsi senyawa karbon
advertisement

Yunita Maimunah ALKOHOL H H H H | | | | H C C H H C C OH H H H H ETANA ETANOL OH sebagai gugus pengganti (gugus fungsi) a Alkohol OH ROH R untuk rantai C , metanol CH3 OH, Etanol C2H5 OH Etanol adalah alkohol yang terdapat dalam spiritus dan dalam minuman keras. Gugus OH dalam alkohol terikat pada gugus karbon alifatik (rantai terbuka) dengan rumus R, ditulis R OH. Sedang OH yang terikat pada gugus C aromatik (Ar) disebut fenol, Ar OH b Eter O atau R O R dietil eter C2H5 O C2H5 digunakan dalam obat bius, eter juga digunakan sebagai pelarut. c Aldehida O — C—H O R — C—H atau CHO atau R CHO Contoh metanal atau formaldehida (Formalin) H CHO yang biasa digunakan sebagai pengawet mayat dan pembuat plastik tidak leleh karena pemanasan (termoset). d Keton O — C— O atau CO RCR atau R CO R’ Contoh Aseton atau propanan CH3 CO CH3, sebagai pembersih cat kuku dan parfum. e Asam Karboksilat O — C—OH atau R—COOH Contoh : asam asetat CH3COOH, Asam semut (Format) f. Ester O R — C—O —R R C O R’ atau COOR atau R COOR’ Contohnya :essence, lilin (wax), lemak (fat) : Lemak dari hewan ; minyak dari tumbuhan ALKOHOL DALAM KEHIDUPAN SEHARI-HARI Metanol Spt alkohol biasa tapi beracun, umum sbg bhn pembuat metanal (formaldehida) sbg bahan pembuat polimer (plastik) Metanol juga sebagai bahan baku ester Campuran bahan bakar mesin 15% krn hsl pembakaran metanol lbh bersih drpd minyak bumi. Etanol Alkohol rumah tangga 70% untuk pembersih luka, mengurangi panas, ada dalam spiritus, minuman dan tape, tidak beracun tetapi memabukkan dan bersifat candu. Diperoleh dari proses peragian 12 – 15% ( jika lebih dari itu bakteri akan mati) disuling sehingga didapat alkohol 95,5%. n C6H12O6 (C6H10O5)n + n H2O amilase amilum glukosa n C6H5OH + 2 CO2 C6H12O6 zimase Etanol Dalam alkohol teknis ditambah zat racun supaya tidak dapat dimakan contoh metanol, piridin atau benzena. Spiritus dibuat dari fermentasi tetes tebu 1. Etilen Glikol (GLIKOL) Sebagai zat anti beku pada radiator mobil mendidih pada suhu 197 oC, membeku pada suhu – 11,5 oC juga sebagai bahan baku pembuatan serat sintetis DACRON H2 C OH H2 C OH 1,2 etana diol (Glikol) 2. Gliserol/Griserin = Tripropana triol H2C OH HC OH C OH H2 Sebagai pelembab pada kosmetik, pada tembakau, obat batuk dan sebagai bahan peledak. o Asam Lemak Jenuh CH3(CH2)10 COOH Asam Laurat C11H23COOH Titik cair 44,2 oC CH3(CH2)14 COOH Asam Palmitat C15H31COOH Titik cair 63,1 oC CH3(CH2)16 COOH Asam stearat C17H35COOH Titik cair 69, 6 oC o Asam lemak tak jenuh CH3(CH2)CH = CH(CH2)7COOH C17H33COOH : Asam oleat, titik cair 13,4oC CH3(CH2)CH = CH(CH2)CH = CH(CH2)7COOH C17H31COOH : Asam Linoleat, titik cair – 5 oC CH3(CH2)CH = CHCH2CH = CHCH2CH = CH(CH2)7COOH C17H29COOH : Asam Linolenat, titik cair – 11oC Senyawa polialkohol Yaitu : senyawa alkohol yang mempunyai gugus lebih dari satu Contohnya: gliserol : untuk pemanis, bahan pelarut obat, bahan baku plastik, kosmetik Cara membuat : Merupakan hasil samping pembuatan sabun Lemak + basa kuat sabun + gliserol Sifat alkohol : Diantara molekul alkohol terdapat ikatan hidrogen dan mempunyai titik didih mendekati titik didih air Bentuk cair Dapat bereaksi dengan logam Na Memabukkan Manfaat eter : a. Pembius, b. Pelarut lemak Halo alkana Substitusi halogen pada alkana dengan pengaruh UV atau suhu tinggi 250 – 400 o C Asam Karboksilat Adalah senyawa asam yang mengandung gugusan karboksil O C OH O Asam metanoat H C OH , CH2O2 O Asam etanoat H3C C OH , C2H4O2 O Asam Pentanoat C4H9 C OH , C5H10O2 Sifat Asam Karboksilat Bereaksi dengan basa membentuk garam O H3C C OH + NaOH H3C C ONa + H2O Asam asetat Na asetat Larut dalam air , merupakan asam lemah Dapat mengalami oksidasi gugus karboksil terikat pada atom H O O H C OH HO C OH Asam fermiamat , CO2 + H2 asam carbonat Dapat bereaksi dengan alkohol membentuk Ester O H3C C OH + C2H5OH H3C C OC2H5 + H2O O Asam asetat Etil asetat (ester) ringkasan Minyak bumi Minyak bumi merupakan senyawa hidrokarbon yang terdiri dari C (83- 87%), H (11-14%), N (0,2-0,5%), Sulfur (0-6%), dan Oksigen (0-3,5%). Proses produksi minyak dari formasi mengandung sekitar 90% air dan komponen lain seperti pasir, garam mineral, aspal, gas CO2, dan H2S. Proses Terjadinya Minyak Mentah Terjadi dari bahan organik yang mengalami proses sedimentasi selama berjuta-juta tahun. Adanya tekanan yang besar di dalam bumi (over burden pressure), suhu, radiasi, disertai oleh proses kimia, lama kelamaan fosil berubah menjadi minyak mentah (crude oil). Minyak bumi yang terbentuk terkumpul dlm pori-pori batuan sedimen laut, kemudian naik ke atas mll batuan sedimen Akhirnya sampai pd bag dasar sedimen tidak dpt ditembus membentuk akumulasi minyak bumi disebut dengan “oil trap”. Gas alam tdpt di atas lapisan minyak, sdg air dibawah lapisan minyak. Komponen minyak bumi dipisahkan melalui proses penyulingan atau destilasi secara bertingkat-tingkat berdasarkan perbedaan titik didih masing2 komponen Komponen hidrokarbon dlm minyak bumi metana ( CH4 ), etana ( C2H6 ), propane ( C3H8 ) dan butana ( C4H10) sampai dengan alkana yang berantai panjang lurus atau bercabang Senyawa alkana yang paling banyak ditemukan dalam minyak bumi adalah normal Oktana dan isooktana ( 2,2,4- trimetil pentana ) CH3 CH3 – (CH2)6 – CH3 CH3 – C – CH2 - C – CH3 CH3 n-oktnan H CH3 ( isooktana) 2,2,4 - trimetil pentana Komponen lain dlm minyak bumi a. Hidrokarbon aromatis Diantaranya adalah etil benzena O - CH2 – CH3 - CH2 – CH3 Atau b. Sikloalkana Sikloalkana yang ditemukan dalam minyak bumi adalah siklopentana dan sikloheksana. Misalnya dalam senyawa metil siklopentana dan etil sikloheksana. dan etil sikloheksana dengan rumus Struktur: CH2 H 2C CH – CH3 H 2C CH – CH2 – CH3 H 2C CH2 H 2C CH2 C C CH2 H2 metil siklopentana etil sikloheksana c. Senyawa anorganik a.l.: - belerang : 0,01-0,7 % - nitrogen : 0,01-0,9 % - oksigen : 0,06-0.4 % sedikit senyawa organologam (vanadium dan nikel). d. Senyawa hidrokarbon tak jenuh Senyawa hidrokarbon tak jenuh, sedikit sekali dlm minyak bumi, Karena senyawa tersebut mudah teradisi membentuk alkana. Pemisahan Fraksi-fraksi Minyak Bumi mll proses penyulingan/destilasi bertingkat berdasarkan pbedaan titik didih komponennya fraksi- fraksi destilasi minyak bumi 1. Gas Tdr dr campuran metana, etana , propane atau isobutana. campuran gas dicairkan tekanan tinggi LPG (Liquid Petroleum Gas ) yi. campuran propane, butana, dan isobutana. 2. Bensin hasil destilasi suhu 70-140 sbg bahan bakar mobil & motor 3. Napta (bensin berat) hasil destilasi suhu 140-180 sbg bhn dasar pembuatan senyawa-senyawa kimia yang lain misal: etilena & senyawa aromatik yg sering digunakan utk zat aditif pd bensin. 4. Kerosin & avtur Titik didih antara 180-250 kerosin = minyak tanah. avtur bhn bakar pesawat 5. Minyak Diesel titik didih 250-350°C minyak diesel 6. Fraksi yang menghasilkan minyak pelumas Paraffin cair dan padat 7. Residu Residu yaitu zat-zat yang masih tertinggal dalam ketel. Menghasilkan petroleumasfalt yang dipakai pada konstruksi jalan Titik didih parafin & aspaltin tidak dapat ditentukan secara pasti, karena sgt bervariasi, tergantung bagaimana komposisi jumlah dari rantai hidrokarbonnya. Jk minyak banyak mengandung hidrokarbon rantai pendek atau jumlah atom karbon lebih sedikit maka titik didihnya lebih rendah, sedang jika memiliki hidrokarbon rantai panjang atau jumlah atom karbon lebih banyak maka titik didihnya lebih tinggi. Mutu bensin Bensin istimewa berisi alkana berantai lurus kurang baik utk bhn bakar motor, karena berkompresi tinggi, sehingga tjd knocking/ketukan pada mesin, ketukan tersebut menyebabkan mesin sangat bergetar dan menjadi sangat panas, sehingga merusak motor. Bahan bensin alkana bercabang, misalnya isooktana, knocking akan berkurang, untuk menyatakan mutu bensin dipergunakan istilah bilangan oktana. contoh bensin standar yang terdiri dari campuran angka oktan 100. bila kerja suatu bensin sama dengan untuk kerja campuran 80% isooktana dan 20% normal heptana, maka angka oktannya bensin itu adalah 80. Bensin mobil di Indonesia adl premium dg bilangan oktana 80, & bensin super dg bilangan oktana 98 meningkatkan mutu bensin dilakukan dengan mencampurkan senyawa-senyawa tertentu pada bensin itu misalnya; tetra etil lead (TEL), ketika terbakar senyawa TEL cenderung bersenyawa dengan radikal karbon bercabang, hal ini memperlambat proses kerja letupan, agar lebih efisien. Industri petrokimia Industri Petrokimia adl industri yg memproduksi bhn2 kimia derivatisasi minyak bumi, gas alam, serta residu minyak bumi scr komersial Beberapa industri lanjutan yang sangat erat hubungannya dengan Petrokimia; Industri plastik Industri serat sintetis Indsutri bahan pelumas Industri pertisida Industri pembuat Pelarut Bahan dasar bagi industri Petrokimia: Jenis paraffin dan olefin, seperti hidrokarbon dengan jumlah atom (1,2,3 dan 4) pembuatan asam asetat, karet dan fiber. Jenis aromat (hidrokarbon aromatik) benzena, pembuatan plastik, penol dan karet