PERBANDINGAN BEBERAPA METODE ISOLASI DNA UNTUK
advertisement

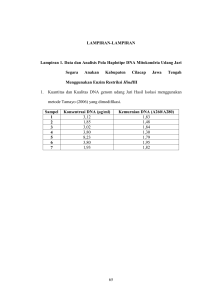
PERBANDINGAN BEBERAPA METODE ISOLASI DNA UNTUK PENENTUAN KUALITAS LARUTAN DNA TANAMAN SINGKONG (Manihot esculentum L.) Molekul DNA dalam suatu sel dapat diekstraksi atau diisolasi untuk berbagai macam keperluan seperti amplifikasi dan analisis DNA melalui elektroforesis. Isolasi DNA dilakukan dengan tujuan untuk memisahkan DNA dari bahan lain seperti protein, lemak, dan karbohidrat. Prinsip utama dalam isolasi DNA ada tiga yakni penghancuran (lisis), ektraksi atau pemisahan DNA dari bahan padat seperti selulosa dan protein, serta pemurnian DNA (Sambrook et al. 1989). Ada beberapa hal yang perlu diperhatikan dalam proses isolasi DNA antara lain harus menghasilkan DNA tanpa adanya kontaminan seperti protein dan RNA; metodenya harus efektif dan bisa dilakukan untuk semua spesies dan metode yang dilakukan tidak boleh mengubah struktur dan fungsi molekul DNA; dengan metode yang sederhana dan cepat. Penggunaan teknik isolasi DNA dengan kit dan manual memiliki kelebihan dan kekurangan. Metode konvensional memiliki kelebihan harga lebih murah dan digunakan secara luas sementara kekurangannya membutuhkan waktu yang relatif lama dan hasil yang diperoleh tergantung jenis sampel. Bahan yang digunakan adalah bibit tanaman singkong varietas Adira 4 dan Jame-Jame (Tabel 1), buffer lysis CTAB, buffer lysis SDS, DNA Isolation Kit, dH2O, ethanol absolute atau isopropanol dingin, CIA (Chloroform Isoamyl Alkohol dengan perbandingan 24:1), agarose, buffer TAE, dan ethidium bromide (EtBr). Lima metode isolasi DNA yang digunakan untuk mengisolasi DNA tanaman singkong yaitu metode isolasi DNA menggunakan CTAB, metode isolasi DNA menggunakan SDS, metode isolasi cepat DNA menggunakan SDS, metode isolasi cepat dengan SDS dan pemanasan, dan metode isolasi cepat DNA menggunakan Isolation Kit (Sigma, dimodifikasi). Alur pengujian dapat dilihat pada Gambar 1. Tabel 1. Berat sampel daun singkong muda untuk isolasi DNA Ulangan Berat Sampel (gram) pada Varietas Adira 4 Jame-jame 1 0,53 0,59 2 0,3 0,2 3 0,02 0,02 4 0,04 0,04 5 0,3 0,3 Ilustrasi rangkaian isolasi DNA tersebut dapat dilihat pada Gambar 1 berikut. a b c d e f Gambar 1.a) pengguntingan daun sampel untuk mempermudah penggerusan jaringan; b) penggerusan daun dengan mortar dan pestle; c) sampel yang telah digerus; d) penambahan chloroform isoamyl alcohol; e) presipitasi DNA; f) pengeringan DNA dengan vaccum. 1 Kuantitas dan kualitas DNA dapat diduga melalui spektrofotometri sinar ultra violet, dengan alatnya yang disebut spektrofotometer. Prinsip kerja spektrofotometer adalah iradiasi sinar ultra violet yang diserap oleh nukleotida dan protein dalam larutan. Penyerapan sinar tersebut oleh nukleotida secara maksimal dicapai pada panjang gelombang 260 nm. Apabila kepadatan optic (optical density) biasa disebut OD260 sama dengan 1, maka konsentrasinya setara dengan 50 µg/mL DNA untai ganda atau 40 µg/mL RNA dan DNA untai tunggal, atau setara dengan 20 µg/mL oligonukleotida untai tunggal (Sulandri et al. 2003). Penentuan kuantitas DNA sampel dua genotype singkong yang diisolasi menggunakan empat metode isolasi DNA pada panjang gelombang 260 nm, dan hasilnya dapat dilihat pada Tabel 2 berikut. Tabel 2. Kuantitas/Konsentrasi DNA Hasil Isolasi DNA menggunakan lima metode isolasi Metode Isolasi Genotype A260 nm Konsentrasi No (µg/mL) 1 CTAB Adira 4 0,125 1250 Jame-jame 0,128 1280 2 SDS Adira 4 0,465 4650 Jame-jame 0,099 990 3 Isolasi Cepat dengan SDS Adira 4 0,029 290 Jame-jame 0,020 200 4 Isolasi Cepat dengan SDS dan pemanasan Adira 4 0,080 800 Jame-jame 0,081 810 5 Kit Isolation Adira 4 0,049 490 Jame-jame 0,029 290 Secara umum seluruh konsentrasi yang dihasilkan dari kelima metode isolasi telah memenuhi syarat minimal konsentrasi DNA yang dibutuhkan untuk pemanfaatan marka molekuler selanjutnya seperti RAPD, SSR, ISSR yang hanya membutuhkan DNA dengan konsentrasi rendah (±50 µg/mL). Perbandingan efisiensi kelima metode isolasi DNA tersebut diatas dapat dikelompokkan berdasarkan efisiensi waktu isolasi DNA dan kebutuhan bahan kimia yang diperlukan selama proses isolasi DNA terutama kebutuhan untuk buffer lisis (lihat Tabel 3). Konsentrasi DNA pada Tabel 3 merupakan hasil konsentrasi DNA pada Tabel 2 dibagi dengan jumlah contoh kerja yang digunakan saat isolasi DNA. Berdasarkan hasil isolasi DNA menggunakan kelima metode isolasi DNA terlihat metode SDS Cepat dengan pemanasan baik pada genotype Adira 4 dan Jamejame memiliki konsentrasi DNA tertinggi. Metode dengan Kit menghasilkan konsentrasi DNA terendah pada kedua genotipe singkong yang digunakan. Berdasarkan Tabel 3 dapat dilihat efisiensi kelima metode isolasi DNA baik waktu dan bahan kimia yang dibutuhkan dalam proses isolasi DNA. Metode isolasi DNA SDS Cepat memiliki waktu penyelesaian yang relatif lebih singkat dan konsentrasi DNA yang dihasilkan relatif lebih tinggi dibandingkan dengan metode lainnya. Metode SDS Cepat dengan pemanasan memiliki efisiensi yang tertinggi yaitu waktu isolasi DNA lebih singkat 45 detik lebih singkat dari metode SDS tanpa pemanasan dan konsentrasi DNA lebih dari 4000 (µg/mL). Sedangkan metode Kit memiliki efisiensi terendah dengan waktu isolasi yang hampir sama dengan metode CTAB dan SDS standar namun membutuhkan bahan kimia yang berupa kit relatif lebih mahal dibandingkan dengan metode lainnya. 2 Tabel 3. Perbandingan Efisiensi Waktu dan Bahan Kimia Empat Metode Isolasi DNA Genotipe Metode Kebutuhan Waktu Kebutuhan Bahan Kimia (menit) Nama Bahan Konsentrasi Stok Kerja Adira 4 CTAB 96 Tris HCl pH 8.0 100 mM NaCl 1400 mM EDTA 20 mM CTAB 2% SDS 96 Tris HCl pH 8.0 200 mM SDS Cepat 63 menit 45 detik NaCl 250 mM SDS Cepat Dengan Pemanasan 64 menit 30 detik EDTA 25 mM SDS 0.5% Kit 93 menit 45 detik JameCTAB 96 Tris HCl pH 8.0 100 mM Jame NaCl 1400 mM EDTA 20 mM CTAB 2% SDS 96 Tris HCl pH 8.0 200 mM SDS Cepat 63 menit 45 detik NaCl 250 mM SDS Cepat Dengan Pemanasan 64 menit 30 detik EDTA 25 mM SDS 0.5% Kit 93 menit 45 detik Konsentrasi DNA 236 1,550 2,900 4,000 82 217 495 2,000 4,050 48 3 Tingginya nilai kuantitas DNA hasil isolasi menggunakan metode isolasi cepat dengan SDS perlakuan pemanasan dibandingkan dengan metode lain dikarenakan SDS merupakan senyawa deterjen anionic yang lebih kuat dibandingkan dengan CTAB (deterjen ionic) dalam merusak membran sel, dan perlakuan pemanasan dapat meningkatkan aktivitas senyawa SDS dalam merusak membrane sel sehingga banyak DNA yang terekstraksi atau terisolasi dari sel. Berdasarkan efisiensi waktu dan bahan kimia yang dibutuhkan untuk mengisolasi DNA daun singkong maka disarankan menggunakan metode SDS cepat dengan pemanasan. Elektroforesis adalah proses migrasi fragmen DNA di dalam gel yang direndam dalam larutan penyangga. Fragmen DNA yang lebih kecil berat molekulnya akan berjalan lebih cepat dari molekul DNA yang lebih besar. Semakin besar tegangan arus listrik, perjalanan molekul DNA akan semakin cepat, demikian pula sebaliknya (Sulandri et al., 2003). Ada bermacam-macam zat kimia yang digunakan sebagai gel di dalam proses elektroforesis. Media penunjang yang biasa dipakai adalah gel agarose, gel pati, gel poliakrilamida dan kertas sellulose poliasetat (Pratiwi, 2001). Terdapat beberapa macam metode elektroforesis termasuk gel yang digunakan antara lain yaitu elektroforesis gel agarose dengan visualisasi menggunakan ethidium bromide, dan elektroforesis gel polyacrylamide dengan visualisasi menggunakan silver staining (Sulandri et al.,2003). Pada praktikum ini yang digunakan adalah elektroforesis horizontal dengan media gel agarose. Konsentrasi gel agarose yang digunakan adalah 1,5% dalam buffer TAE 1x, dan dirunning dengan voltase 100 V selama ±20 menit. Selanjutnya diwarnai dengan ethidium bromide selama 10 menit dan dibilas dengan dH2O selama 20 menit. Setelah itu gel agarose yang telah terwarnai divisualisasikan dengan sinar UV dengan alat UV Transilluminator. Visualisasi gel agarose DNA hasil isolasi DNA dapat dilihat pada Gambar 2. CTAB SDS SDS Cepat SDS Cepat + Pemanasan Kit Isolasi DNA Gambar 2. Visualisasi pengujian kualitas dan kuantitas DNA hasil isolasi DNA sampel daun singkong menggunakan tiga metode isolasi DNA Berdasarkan gambar diatas terlihat bahwa kualitas larutan DNA dengan metode isolasi CTAB dan SDS tidak sebaik dengan metode isolasi cepat dengan SDS baik tanpa perlakuan maupun dengan pemanasan dan metode isolasi menggunakan DNA isolation kit. Pada metode isolasi CTAB dan SDS terlihat masih terdapat banyak kontaminasi baik protein maupun RNA. Berdasarkan hasil diatas kelima metode isolasi yang digunakan metode isolasi cepat dengan SDS tanpa pemanasan dapat dijadikan sebagai metode rujukan dalam mengisolasi DNA tanaman khususnya untuk komoditas singkong dengan 4 menggunakan organ daun sebagai sampel isolasi. Metode ini hanya menggunakan bobot sampel yang relatif sedikit, tidak diperlukan penggerusan menggunakan mortar dan pestle dan tidak membutuhkan nitrogen cair (N2liquid) sebagai sarana membantu proses penggerusan dan memberikan kuantitas serta kualitas DNA yang cukup baik. Metode isolasi CTAB dan SDS dapat diaplikasi untuk isolasi DNA dengan catatan dibutuhkan langkah tambahan atau modifikasi yaitu dengan purifikasi DNA dengan penambahan RNAse serta proteinase. Hal ini bertujuan untuk menghilangkan debris sel (protein dan RNA) yang masih tercampur dengan larutan DNA. Sedangkan isolasi DNA dengan DNA isolation Kit tidak disarankan mengingat harga kit tersebut yang cukup mahal dengan kuantitas dan kualitas DNA hasil isolasi yang cukup rendah. Menurut Jamsari, 2007, beberapa hal penting yang harus diperhatikan dalam kegiatan isolasi DNA adalah 1) keutuhan ukuran molekul DNA karena hal ini berkaitan dengan tindakan-tindakan rekayasa lanjutan yang akan dilakukan seperti pemotongan secara enzimatis dalam pembuatan peta restriksi akan lebih banyak alternative dibandingkan dengan DNA yang sudah terputus; 2) efektifitas isolasi DNA dimana setiap tanaman memiliki spesifikasi struktur fisikokimia yang berbeda-beda sehingga diperlukan metode isolasi yang efektif untuk menghasilkan konsentrasi DNA yang tinggi ; 3) kemurnian isolasi DNA agar tidak terdapat senyawa penghambat proses enzimatis pada tahap selanjutnya; dan 4) praktis dan ekonomis agar laboratorium yang baru dikembangkan dapat mengaplikasikan metode isolasi tersebut. Sumber 1. Jamsari. 2007. Bioteknologi Pemula (Prinsip Dasar dan Aplikasi Analisis Molekuler). Unri Press. Pekan Baru 2. Muladno. 2010. Teknologi Rekayasa Genetika. Edisi Kedua. IPB Press. Bogor 3. Pratiwi Rianta. 2001. Mengenal Metode Elektroforesis. Oseana Volume XXVI Nomor 1 4. Sambrook J, Fritsch EF, Maniatis T. 1989. Molecular Cloning: A Laboratory Manual. 2nd ed. Cold Spring Harbor Laboratory Press. New York. 5. Sulandri Sri, M.Syamsul Arifin Zein. 2003. Panduan Praktis Laboratorium DNA. LIPI -Disusun oleh : Tendy Wijiastuti – PBT Balai Besar PPMB-TPH- 5