Universitas Gadjah Mada 1 PATOGENESIS PENYAKIT
advertisement
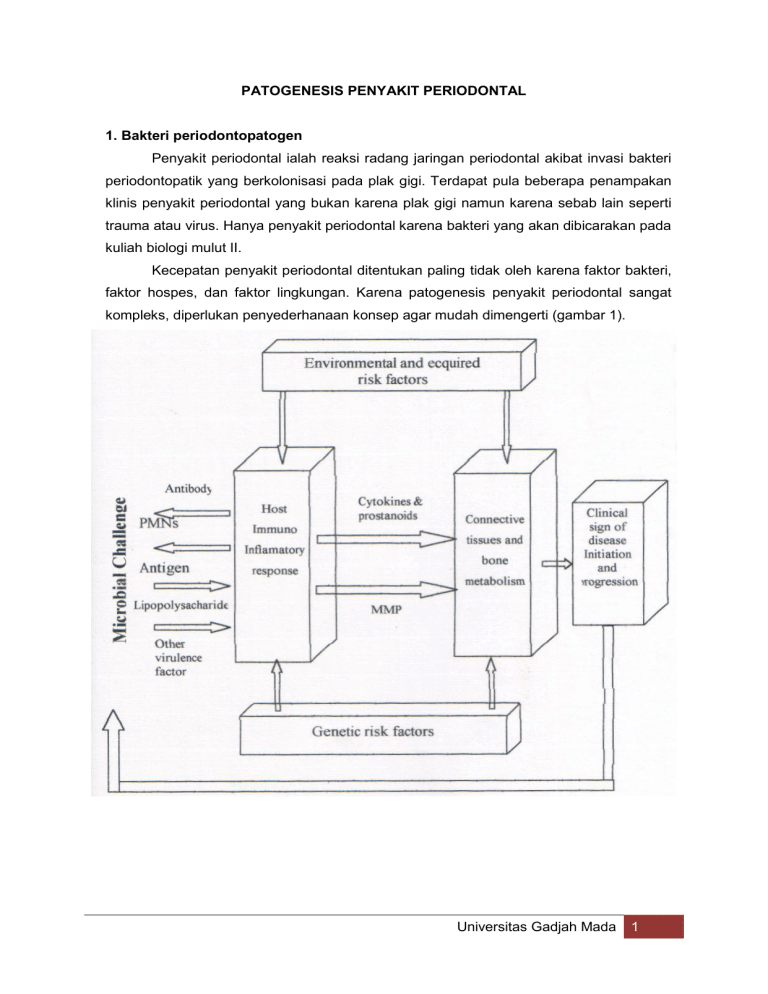
PATOGENESIS PENYAKIT PERIODONTAL 1. Bakteri periodontopatogen Penyakit periodontal ialah reaksi radang jaringan periodontal akibat invasi bakteri periodontopatik yang berkolonisasi pada plak gigi. Terdapat pula beberapa penampakan klinis penyakit periodontal yang bukan karena plak gigi namun karena sebab lain seperti trauma atau virus. Hanya penyakit periodontal karena bakteri yang akan dibicarakan pada kuliah biologi mulut II. Kecepatan penyakit periodontal ditentukan paling tidak oleh karena faktor bakteri, faktor hospes, dan faktor lingkungan. Karena patogenesis penyakit periodontal sangat kompleks, diperlukan penyederhanaan konsep agar mudah dimengerti (gambar 1). Universitas Gadjah Mada 1 a. Peran bakteri plak pada penyakit periodontal Plak bakteri pada daerah subgingiva tidak dipengaruhi oleh Iingkungan mulut namun terbatas oleh ruang yang sangat terbatas dan sistem pertahanan alami (innate) hospes. Ruangan subgingiva sangat terbatas pada individu sehat periodontal. Namun, bila akumulasi plak terjadi terus-menerus, akan terjadi pengurangan perlekatan lapisan epitel gingiva pada permukaan gigi dan berakibat peningkatan kedalaman poket gingiva. Sebaliknya, hospes akan membatasi perkembangan plak dengan memelihara keutuhan lapisan epitel. Cairan krevikular gingivamengandung pula komponen antibakteri seperti lisosim, komplemen dan beberapa faktor pendorong peningkatan permeabilitas pembuluh darah, diantaranya bradikinin, thrombin, dan fibrinogen. Sel polimorfonuklear dan monosit yang keluar dari pembuluh darah dapat pula menghancurkan bakteri. Sel ini memerlukan signal atau faktor yang disebut khemoatraktan (disebut pula khemokin) agar dapat keluar dari pembuluh darah dan berjalan menuju ke plak gigi. Khemokin ini diantaranya interleukin-8 (IL-8) dan MCP-1 (Monocyte Chemotaxis Protein-1). Semakin mendekati lokasi gigi, level protein ini pada gingiva akan semakin meningkat. Bakteri plak gigi diketahui mengeluarkan banyak komponen kedalam ruang mulut dan sulkus gingiva. Bakteri gram negatif mengeluarkan material dinding sel yang berperan sebagai vesikel membran. Material ini diantaranya ialah lipopolisakarida (LPS), lipid dan protein. Material ini berperan pula sebagai signal bagi hospes untuk mengetahui seberapa besar dan macam bakteri plak gigi dan menyebabkan hospes berespon secara langsung maupun tidak langsung. Respon langsung terjadi bila bakteri atau produknya menginduksi sel gingiva untuk mengeluarkan glikoprotein seperti khemokin atau interleukin. Tidak langsung bila bakteri menyebabkan sel terangsang memproduksi glikoprotein yang selanjutnya akan merangsang sel lainnya. Perlu diingat bahwa macam bakteri menentukan pula jenis material yang notabenenya akan menentukan jenis respon hospes. Bakteri gram positif hanya akan menyebabkan produksi khemokin dengan level rendah. Oleh karena bakteri gram positif hanya pada plak gigi dengan jaringan periodontal relatif sehat, maka jarang ditemukan infiltrasi sel pada gingiva. Sebaliknya gram negatif sangat potent merangsang produksi khemokin ini, akibatnya banyak dijumpai infiltrasi sel pada jaringan periodontal yang mengalami inflamasi. Diketahui pula bahwa LPS dari bakteri gram negatif mampu menyebabkan destruksi tulang alveolar dengan cars mengaktifkan set osteoklast. Jadi dapat dimengerti bahwa pada penyakit periodontal tahap lanjut, dijumpai adanya kerusakan tulang alveolar yang parch dan berakibat gigi goyah. Bakteri ini mampu pula merusak integritas lapisan epitel gingiva. Pada individu berusia muda dengan jaringan periodontal sehat, plak gigi didominasi oleh bakteri gram positif, streptokokus dan actinomyces sp (Iihat tabel 1). Universitas Gadjah Mada 2 Semakin tua usia, jenis bakteri plak gigi pada jaringan periodontal sehat akan berubah dengan semakin banyaknya gram negatif seperti Fusobacterium nucleatum, Porphyromonas gingivalis, Prevotella intermedia dan EikeIla corodens.Jadi umur individu sangat menentukan jenis bakteri plak gigi pada jaringan periodontal sehat. Pada penderita gingivitis, jumlah bakteri akan bertambah dan peran sistem pertahanan hospes akan mempengaruhi perubahan jenis bakteri. Plak gigi pada gingivitis didominasi oleh gram negatif (tabel 1). Tabel 1. Komposisi bakteri plak gigi sesuai dengan tingkat penyakit periodontal Sehat Gingivitis Periodontitis 1 Porphyromonas gingivalis Streptococcus oralls Streptococcus °rails Streptococcus sanguis Streptococcus sanguis A, actinomycetemicomitans Streptococcus mitis Streptococcus mitis serotip B Streptococcus gordonii Streptococcus intermedius Bacteroides forsythus PRO Streptococcus mutans Capnocytophaga ochracea spirochete Treponema Streptococcus intermedius Capnpcytophaga gingivalis denticola Prevotella Gemella morbillorum Campylobacter gracilis intermedia Prevotella Rothia denticariosa Prevotella loscheii nigrecens Campylobacter Actinomyces naeslundii Peptostreptococcus micros rectus Peptostreptococcus Actinomyces gerencsenae Eubacterium nodatum micros Fusobacterium Actinomyces odontolycus Actinomyces naeslundii nucleaturn Subsp. Peptostreptococcus Actinomyces israeli Nucleaturn Fusobacterium micros Eubacterium Campylobacter concisus nucleatum Subsp. Vincentii nodatum Capnocytophaga Actinomyces odontolycus Selemonas noxia ochracea : data diambil dari Fusobacterium Selemonas flueggeii Keterangan Darveau RP,nucleatum Tanner A, Page RC. The Microbial Capnpcytophaga Subsp. Nucleatum i Spesies enterik challenge in periodontitis. Periodontology 2000., 1997; 14:12-32 gingivalis Campylobacter Eubacterium brachy Fusobactyerium alocis gracilis Fusobacterium Eikenella corroders A, Lactobacillus uli nucleatum Subsp. periodontitis, actiomycetemicomitans parvula Pada penderita komposisi bakteri plak gigi Veilonella akan semakin kompleks serotipanaerob B danPolymorphum lebih didominasi oleh gram negatif total. Diketahui bahwa bakteri seperti P. gingivalis, Bacteroides forsythus dan Actinobacillus actinomycetemcomitans merupakan bakteri penyebab kerusakan karingan lunak periodontal maupun jaringan tulang alveolar. 2. Respon jaringan periodontal terhadap bakteri periodontopatogen a. Respon hospes terhadap fase akut bakteri Bakteri plak gigi akan mengeluarkan produk/material, seperti asam lemak (contohnya asam butirat dan asam propianat), peptida seperti FMLP (N-formilmethionyl-leucylUniversitas Gadjah Mada 3 phenylalanine) dan LPS, yang akan berdifusi kedalam lapisan epitel gingiva (gambar 2). Material ini akan merangsang sel epitel untuk memproduksi mediator inflamasi seperti interleukin-8 (IL-8), IL-1 beta, prostaglandin E2 (PGE2), matriks metailoproteinase (MMP) dan tumor necrosis factor alpha (TNF-alpha). Mediator ini akan merangsang pembuluh darah menjadi terinflamasi. Akibatnya khemokin seperti IL-8 akan merangsang khemotraksi sel leukosit keluar dari pembuluh darah menuju ke lokasi plak gigi. LPS dapat pula merangsang sel endotel untuk mengeluarkan mediator untuk mengaktifkan sel pada jaringan konektif. Sebagai contoh sel makrofag, fibroblast, dan sel mastus dari jaringan tersebut akan mengeluarkan mediator, seperti histamin, prostaglandin, interleukin dan matriks metalloproteinase, yang berperan sebagai khemokin maupun sebagai mediator penyebab peningkatan permeabilitas vaskular. LPS mengaktifkan pula sistem komplemen jalur tidak langsung dari produksi kinin. b. Fase respon inflamasi akut Peningkatan permeabilitas pembuluh darah menyebabkan ekstravasasi sel leukosit. Protein serum seperti komplemen, protein fase akut dan sistem plasmin akan semakin meningkatkan respon inflamasi dan mengaktifkan sel endotel untuk memproduksi mediator Iebih banyak (Gambar 3) mediator seperti IL-1 akan mengaktifkan sel makrofag untuk memproduksi mediator Iainnya seperti TNFalpha, IL-8, 1L-6, IL-10, IL-12, PGE2, MMP, interferon-gamma (IFN-gamma), dan khemokin seperti RANTES, MCP dan MIP. Meningkatnya level IL-8 jugs menyebabkan aktivasi dan migrasi sel netrofil ke tempat plak gigi. Universitas Gadjah Mada 4 Gambar 2. Repon vaskular dan lapisan epitel pada kolonisasi bakteri awal (akut) C. Fase respon imun oleh aktivasi sel mononuklear Setelah fase awal inflamasi terjadi, sel mononuklear seperti makrofag dan sel limfosit mulai infiltrasi (gambar 4). Sel limfosit T akan mengeluarkan produk mediator seperti IL-2, IL3, IL-4, IL-5, IL-6, IL-10, IL-13, TNF-alpha, TGF-beta (Transforming growth factor beta), dan khemokin seperti RANTES, MCP, dan MIP. LPS mampu pula secara !angsung mengaktifkan sel limfosit B untuk memproduksi antibodi dan merangsang sel makrofag mengeluarkan mediator seperti TGF-beta, IL-1, IL-12, dan IL-10 maupun matriks metalloproteinase. Hasil akhir dari fase ini ialah semakin banyaknya infiltrasi sel makrofag dan limfosit disertai semakin tinggi tingkat kerusakan matriks ekstraselular seperti kolagen. Akibatnya, semakin banyak akumulasi plak gigi, semakin tinggi respon imun dan semakin besar kerusakan jaringan. Hal ini dapat dilihat secara klinis dengan semakin dalamnya poket gingiva dan perdarahan spontan. Universitas Gadjah Mada 5 Gambar 3. Respon lanjut pada jaringan periodontal karena adanya serum protein dan aktivasi sel makrofag. Gambar 4. Hilangnya perlekatan lapisan epitel pada permukaan gigi dan adanya aktivitas sel mononuklear. Universitas Gadjah Mada 6 2. Mekanisme kerusakan jaringan pada penyakit periodontal Mekanisme kerusakan jaringan pada penyakit periodontal tidak terlepas dan peranan enzim matriks metalloproteinase (MMP). Enzim ini juga disebut matriksin atau kolagenase (sebutan yang kurang tepat) adalah enzim proteinase yang mampu merusak matriks ekstraseluler seperti kolagen. MMP ini sebenarnya adalah sekelompok proteinase yang mempunyai fungsi yang hampir sama. Mereka terdiri dari kelompok kolagen interstisial (contohnya ialah MMP-1, MMP8, dan MMP-13), gelatinase (contohnya MMP-2 dan MMP-9), Stromelisin (contohnya MMP-3, MMP-10, MMP-11), kelompok yang berikatan dengan membran (contohnya MMP-14, MMP-15, MMP-16, MMP-17). MMP akan berfungsi melisis target sesuai dengan nama kelompok MMP. Diketahui pula ada substansia yang disebut TIMP (Tissue Inhibitor of Metalloproteinase) dan berfungsi sebagai penghambat kerja TIMP-1, TIMP-2, TIMP-3 dan TIMP-4. MMP dan TIMP diproduksi oleh set makrofag dan fibroblast gingiva dan letaknya sangat berhubungan dengan jaringan yang sedang mengadakan remodeling. Diduga, produk bakteri seperti LPS akan megaktifkan sel fagosit untuk memproduksi mediator seperti IL-1. Mediator ini kemudian akan mengaktifkan sel makrofag dan fibroblast gingiva untuk memproduksi MMP dan regulatornya yaitu TIMP. MMP ini akan mengawali terjadinya destruksi matriks ekstraseluler gingiva seperti kolagen dan merangsang terjadinya resorpsi tulang. a. Mekanisme kerusakan tulang alveolar Pada penderita gingivitis, infiltrasi set mononuklear terus bertambah dan terjadi kerusakan jaringan konektif, tetapi belum nampak adanya resorpsi tulang. Pada penderita periodontitis, infiltrasi sel dan degradasi kolagen bergerak kearah apikal sepanjang akar gigi. Sel osteoblast menghilang tetapi disertai dengan meningkatnya sel osteoklast yang meresorpsi tulang. Permukaan sementum gigi merupakan permukaan terakhir yang diresorpsi osteoklast. LPS bakteri plak gigi akan merangsang sel seperti makrofag dan fibroblast untuk memproduksi mediator seperti IL-1, PGE-2 dan TNF-alpha (Gambar 5). Mediator ini menghambat proses diferensiasi osteoblast, menghambat produksi mediator sel osteoblast dan menghambat produksi matriks ekstraselulera dan proses kalsifikasi. Akibatnya, jumlah maupun fungsi osteoblast semakin menurun.Sebaliknya mediator ini justru meningkatkan diferensiasi osteoklast dan aktivitas osteoklast. Sehingga, penurunan jumlah osteoblast justru diikuti dengan peningkatan jumlah dan fungsi osteoklast. Hal ini berakibat derajat kerusakan tulang tidak dapat diimbangi oleh proses remodeling oleh osteoblast. Universitas Gadjah Mada 7 Gambar 5. Mekanisme resorpsi tulang alveolar pada penyakit periodontal 4. Faktor-faktor yang berpengaruh terhadap patogenesis penyakit periodontal Penyakit periodontal sangat ditentukan oleh faktor-faktor yang amat kompleks. Interaksi faktor-faktor tersebut akan sangat menentukan kecepatan karakteristik pernyakit periodontal. Salah sate faktor tersebut adalah faktor resiko terjadinya penyakit periodontal. Sebutan faktor resiko berarti bagian dari rantai penyebab yang dapat mendorong terjadinya penyakit, jadi dapat bersifat langsung meningkatakan probabilitas terjadinya penyakit. Pada penyakit periodontal paling tidak ada 2 faktor resiko : a. Faktor Predisposisi Faktor predisposisi ini dapat terjadi pada beberapa keadaan seperti : a. Overhanging margin restorasi yang dapat meningkatkan akumulasi plak gigi b. Deposisi material alba, debris dan retensi makanan yang merupakan media yang sangat balk untuk perlekatan dan pertumbuhan bakteri. c. Jenis diet, terutama diet lunak, yang memudahkan lengket pada permukaan gigi. d. Stain gigi yang mengiritasi gingiva dan membuat permukaan gigi lebih kasar, sehinga memudahkan terbentuknya plak gigi. e. Karies gigi yang memudahkan retensi makanan dan pembentukan plak gigi. f. Merokok dan mengunyah tembakau. Universitas Gadjah Mada 8 Individu yang merokok lebih mempunyai resiko terjadinya penyakit periodontal destruktif dibanding individu tidak merokok. Terulang kembalinya penyakit periodontal meskipun telah mendapatkan perawatan periodontal pada perokok jauh lebih tinggi dibanding bukan perokok. Rokok sebagai faktor resiko penyakit ini dapat dibagi 2 yaitu faktor lokal dan sistemik. Faktor lokal lebih disebabkan gangguan lokal karena racun yang terkandung didalam tembakau seperti nikotin. Substansia ini menyebabkan vasokonstriksi lokal, mengurangi aliran darah lokal, edema dan inflamasi. Nikotin dapat pula mengurangi oksigen pada sulkus gingiva sehingga menguntungkan bagi pertumbuhan bakteri anaerob. Faktor sistemik lebih banyak karena gangguan khemotaksis dan fagositosis set netrofil maupun menurunnya kemampuan memproduksi antibodi. Nikotin mampu menurunkan proliferasi sel osteoblast dan mendorong sel monosit lebih banyak produksi IL-1 dan prostaglandin sehingga mempercepat terjadinya kerusakan jaringan periodontal. g. Maloklusi yang menyebabkan peningkatan retensi makanan dan pembentukan plak gigi h. Kekuatan oklusi yang berlebihan menyebabkan degenerasi struktur jaringan periodonsium dan mempercepat kerusakan jaringan tersebut. i. Kebiasaan buruk seperti bruxism, dan menggigit pensil yang berakibat kekuatan terlalu besar yang dapat diterima oleh jaringan periodonsium. Bernafas melalui mulut mengurangi fungsi self cleansing saliva sehingga membuat mulut menjadi kering. Akibatnya pembentukan plak akan jauh Iebih mudah. b. Faktor Sistemik Faktor sistemik merupakan faktor resiko yang dapat bersifat langsung maupun tidak langsung terhadap tingkat keparahan penyakit periodontal. 1. Faktor endokrin Pubertas, kehamilan, menopause merupakan keadaan yang berakibat adanya perunahan hormonal. Pada ibu hamil, sering terlihat adanya pembengkakan gingiva dan perdarahan gingiva spontan. Namun keadaan ini bersifat reversibel dan menghilang setelah ibu melahirkan. 2. Malnutrisi Hubungan sebab-akibat antara malnutrisi dengan penyakit periodontal masih belum diketahui secara pasti. Penelitian tentang hal ini Iebih banyak dilakukan dengan binatang percobaan. Namun, meskipun ada hubungan, diperkirakan hal ini terjadi secara tidak langsung. Sebagai contoh, defisiensi vitamin A dan C dapat menurunkan fungsi fagositosis sel, sehingga mempercepat terjadinya penyakit periodontal, bila ada plak gigi. 3. Obat-obatan Universitas Gadjah Mada 9 Pemakai obat-obatan untuk epilepsi seperti Phenytoin sering terlihat adanya pembengkakan gingiva. Namun demikian, apakah penampakan klinis ini sama seperti penyakit periodontal karena plak gigi masih harus diteliti. 4. Kondisi psikologi Faktor psikososial seperti stress fisik maupun mental dapat mengganggu kestabilan imun respon yaitu adanya gangguan hubungan neuroendokrinrespon imun. Studi epidemiologi memperlihatkan bahwa penderita stress menunjukkan tingkat penyakit periodontal yang lebih parch dibanding kontrol. Diperlihatkan bahwa stress meningkatkan level glukokortikoid yang selanjutnya dapat menurunkan fungsi sel makrofag, netrofil, monosit dan sel mastus. 5. Diabetes Melitus Penderita Diabetes Melitus (DM) yang mempunyai tingkat resiko terjadinya penyakit periodontal destruktif lebih tinggi dibanding individu tanpa tanpa DM. Hal ini disebabkan karena interaksi perubahan patologis akibat DM yaitu (1) Perubahan vaskular Status hiperglikemia yang terlalu lama berakibat adanya perubahan vaskular. Peningkatan gukosa darah yang lama menyebabkan kenaikan pembentukan produk akhir dari proses glikasi lanjut yang berupa protein tanpa proses glikasi enzimatik dan berupa lipid. Produk ini terakumulasi pada dinding pembuluh darah sehingga meningkatkan ketebalan dinding darah. Akibatnya terjadi gangguan diapedesis leukosit, difusi oksigen dan pembuangan hasil metabolisme. (2) Modifikasi respon hospes DM menyebabkan terjadinya gangguan pada khemotaksis, fagositosis dan destruksi bakteri sel netrofil. Gangguan ini mungkin karena peningkatan level PGE2 dan peningkatan level lipid (terutama asam lemak tak jenuh dan trigliserid) akibat turunnya konsentrasi insulin. (3) Gangguan metabolisme jaringan konektivus Gangguan ini lebih banyak karena adanya gangguan metabolisme kolagen (salah satu matriks ekstraseluler). Glikasi non-enzimatik meningkatkan ikatan silang antar kolagen sehingga mengurangi kelarutan dan memperlambat metabolisme kolagen. Hal ini berakibat terjadinya gangguan proses penyembuhan luka. (4) Respon inflamasi yang berlebihan Pada kondisi hiperglikemia pada penderita DM, sensitivitas sel monosit terhadap stimulus seperti LPS meningkat drastis. Jadi setelah stimuli dengan LPS, sei monosit akan memproduksi mediator, seperti IL-1, PGE2 dan TNF-alpha lebih tinggi. Akibatnya lebih cepat terjadi destruksi jaringan periodontal karena aktivitas Universitas Gadjah Mada 10 osteoklast untuk resorpsi tulang dan aktivitas MMP yang merusak matriks ekstraseluler. 6. Infeksi HIV HIV (Human lmmunodefficiency Virus) menyebabkan sindroma imunodefisiensi yang dikenal sebagai AIDS. Pada penderita AIDS, peningkatan keparahan penyakit periodontal mungkin disebabkan karena gangguan khemotaksis, fagositosis dan penghancuran bakteri sel netrofil, penurunan khemotaksis monosit, gangguan penghancuran bakteri via reseptor Fc dan gangguan fungsi sitotoksik sel monosit via antibodi-antigen kompleks. Penurunan jumlah sel CD4 (set T helper) memperjelas gangguan respon imun dan peningkatan penyakit periodontal. c. Faktor Genetik Penentuan bahwa faktor genetik berperan pada penyakit periodontal merupakan perihal yang masih diperdebatkan. Namun penelitian pada pasangan kembar dan pengaruh genetik pada respon imun memperjelas bahwa faktor genetik memang berpengaruh pada kerentanan individu terhadap timbulnya penyakit periodontal. Sampai sekarang paling tidak ada 5 kemungkinan yang termasuk dalam faktor genetik pada penyakit periodontal, yakni: 1. Adanya gangguan genetik pada fungsi netrofil. Ada beberapa gangguan genetik seperti defisiensi adhesif leukosit tipe 1, sindroma Chediak-Higashi, dan Sindroma Papilon-Lefevre yang berakibat gangguan sel netrofil. Pada penderita ini diketahui mempunyai prevalensi penyakit periodontitis yang sangat tinggi. 2. Antibodi Ig2 merupakan antibodi isotip yang sangat dominan pada periodontitis tahap awat maupun pada orang dewasa. Antibodi ini ditentukan secara genetik oleh lokus G2M23. 3. adanya polimorfisme (variasi tinggi) pada gena pengkode reseptor Fcyll yang sangat berhubungan dengan fungsi fagositosis sel netrofil. 4. Adanya polimorfisme gena IL-1. Penggabungan dua polimorfisme gena tersebut akan meningkatkan suseptibilitas individu terhadap timbulnya penyakit periodontal. 5. Adanya gena pengkode enzim prostaglandin endoperoksid sintase yang terletak pada kromosom 9q32-33. Terdapat hubungan yang sangat signifikan antara penderita periodontitis satu famili yang teridentifikasi pada kromosom ini. Universitas Gadjah Mada 11 DAFTAR RUJUKAN Abbas, A.K., Lichtman, A.H , dan Pober, J.. 1997. Cellular and Molecular immuology, Saunders, Philadelphia. Ammann, A.J. 1991. T cell immunodeficiency disorders. Dalam Basic and Clinical Immunology (Stites D.P. dan Terr, A.B. eds.). Ed. Ke-7. Apleton & Lange, Connecticut, h. 335-40. Bellanti, J.A. 1985. Mechnism of immunity to fungal diseases. Dalam Immunology /// (Bellanti J.A. ed.). Sanders, Philadelphia, H 323-9. Bellanti, J.A. dan Kadlec, J.V. 1985. Introduction to immunology. Dalam Immunology III (Bellanti J.A. ed.). Saunders, Philadelphia, h 1-15. Bowden, G.H.W. dan Edwardsson, S. 1994. Oral ecology and dental caries. Dalam Textbook of Clinical Cariology (Thylstrup, A. an Fejerskov, 0. eds.). Ed. Ke-2. Munkegaard. Copenhagen. h. 45-69. Brightman, V.J. 1994. Rend and white lesions of the oral mucosa. Dalam Burket' Oral Medicine Diagnostic and Treatmen (Lynch, M.A., Brightman, V.J., dan Greenberg M.S. eds.) Ed. Ke-9. Lippincott, Philadelphia. h. 51-120. Brightman, V.J., 1984a. Sexually transmitted and blood borne infection. Dalam Burket's Oral Medicine. Diagnostic and Treatmen (Lynch M.A. Brightman V.J. dan Greenberg M.S. eds.). Ed ke-5, Lipincott Philadelphia. h.629-728. Browden, L.R. Dreizen S., dan Bodey G.P. 973. Effect of immunosuppression on the oral flora. Dalam Comparative Immunology of the Oral Cavity (Mergenhagen S.E. dan Scherp. H.W. eds.). U.S. Department of Health Education, and Welfare Bethesda. h. 204-20. Carranza, F.A. dan Bulkacz, J. 996. Defence mechanisms of the gingiva. Daiam Clinical Periodontology. Ed. Ke-8. Lipplincott. Philadelphia. h. 103-11. Cawson, R.A., Binnie, W.H., Eveson, J.W., 1994, Color Atlas of Oral Disease, 2nd ed. Wolfe, London Contos J.G., Corcoran J.F., LaTurno S.A.L., Chiego D.J., dan Regezi J.A. (987) Langerhans cells in apical aperiodontal cysts: an immunohistochemical study. J. Endodon 13: 525. Cymerman J.J.,Cymerman D.H., Walters J., dan Nevins A.J. (1984) Human T lymphocyte subpopulations in chronic periapical lesions J. Endodon 10. 911. Cypess, R.H. 1985. Mechanism immunity to parasitic diseases. Dalam immunology Ill (Bellanti, J.A. ed.). Lippincoti, Philadelphia. h. 306-29. Davis, WL.. 1986, Oral Histology, WB. Saunders Co., Philadelphia Dennison, D.K., Dylee, T.E., 1997, The Acute Inflammatory Response and the Role of Phagocytic cells in Periodontal health and Disease, Periodontology 2000, 14: 54-78 Universitas Gadjah Mada 12 Farber P.A. dan Seltzer, S. 1988. Endodontic micribiology. I. Etiology. J. Endodon. 14:36371. Fawcett, D.W., Bloom, 1994, A Textbook of Histology, 20th ed., Chapman and Hall, New York Fye, K.H. dan Sack, KE. 1991. Rheumatic diseases. Datam Basic and Clinical Immunology (Stites. D. P. dan Terr. A.B. eds.). Ed. Ke-7. Appleton & Lange, Connecticut. HI. 43865. Greenberg, M.S. 1996. Ulcerative vesticular and bullous lesions. Dalam Burket's Oral Medicine. Diagnostic and Treatent (Lynch, M.A., Brigtman, V.J., dan Greenberg, M.S. eds.). Lippincott. Philadelphia. h. 11-50. Greenberg, M.S. 1996a. Immunologic diseases. Dalam Burket's Oral Medicine. Diagnostic and Treatment (Lynch, M.A., Brightman, V.J., dan Greenberg M.S. eds.). Lippincott Philadelphia. h. 563-91. Greenberg, M.S. dan Garfunkel, A. 1996.Hematologic diseases. Dalam Burket's Oral Medicine. Diagnostic and Treatmen Lynch M.A.,Brightman V.J., dan Greenberg M.S. eds.). Philadelphia. Lippincott, h. 510-44. Gunawan, J.A. dan Roeslan, B.Oe. 2000. Kader sigA Liur pada Individu Tahan Karies dan Rentan Karies. Majalah Kedokteran Gigi FKG UNAIR 33. 35-9. Hahn, C., Falker, W.A., dan Siegel, M.A. 1989. A study of T and B cells in ulpal pathosis. J Endodon 15:20-6. Hassell, T.M., 1993, Tissues and Cells of The Periodontium, Periodontology 2000, 3:9-38 Herberman, R.B. dan Bellanti, J.A. 1985. Defence mechanism in tumor immunity. Dalam Immunology Ill (Bellantim J.A. ed.). Saunders, Philadelphia. h. 3239. Jame S.P., Strober, W., dan Greenspan, J.S. 1991. Gastrointestinal, hepatobilliary oral & dental diseases. Dalam Basic and Clinical Immunology (Stites, D.P. dan Terr, A.B. eds.). Ed. Ke-7. Appleton & Lange, Connecticut. h. 506-25. Kettering, J.D. dan Torabinejad M. 1986. Conctrations of Immunoglobulin E in patients with chronic periapical lesions. J Endodon /2 : 306-8. Kettering, J.D. dan Torabinejad, M. 1984. Concentrations of immune complexes IgG, IgM, IgE, and C3 in patient with acute apical abcesses. J Endodon 10:417-21. Killian, M. dan Bratthall, D. 1994. Caries immunolgy. Dalam Textbook of Clinical Cariology (Thylstrup A, dan Fejerskov 0. eds.). Ed. Ke-2. Munksgaard. Copenhagen. Hlm. 35566. Kopp, W. dan Schwarting R. 1989. Differentiation of T lymphocyte subpopulations, macrophag, and HLA-DR-restricted cells of aical granulation tissues. J Endodon 15:72-6. Universitas Gadjah Mada 13 Kornman, K.S., Page, R.C., Tonetti, M.S., 1997, The Host Response to the microbial chalenge in Periodontitis: Assembling the Players, Periodontology 2000, 14: 33-53 Lehner, T. 1975. Immunological aspect of dental caries and periodontal disease. Mr Med Bull 31:125-30. Lehner, T. 1992. Immunological of oral Disease. Blackwell Sci. Publ., Oxford. Lehner, T., 1992, Immunology of Oral Disease, 3 th ed., Blackwell Scientific Pub Melbourne McIntyre, J. 1998. The nature and progression of dental caries. Dalam Preservation and Restoration of Tooth Structure (Mount, G.J. dan Hume, W.R. eds.). Mosby, London. h. 9-17. Moore, W.E.C., Moore L.V.H., 1994, The Bacteria of Periodontal Diseases, Periodontology 2000, 5: 66-77 Morse, D.R. 1977. Immunologic respon of pulpaperiapical. Oral Surg 43: 436-51. Naidorf, I.J. 1985. Endodontic flare-ups: bacteriological and immunological mechanism. J Endodon 11: 462-4. Nevins, A.J. Levine S., Faitlowics-Gayer. Y. dan Svetcov, S. 1985. Sensitization via IgEmediated mechanism in patients with chronic periapical lesions. J Endodon 11: 22830. Newburn, E. 1989. Cariology. Ed. Ke-3. Quintessence, Baltimore. h. 63-72. Newman M.G., Sanz, M., Nisengard, R., dan Haake. S.K. 1996. Host-bacteria interactions in periodontal diseases. Dalam Clinical Periodontology (Caranza F.A. dan Newman M.G. eds.). Ed. Ke-8. Saunders, Philadelphia. h. 121-31 Nisengard, R.C., Newman, M.G., dan Sanz, M. 1996. The host respon: basic consept. Dalam Clinical Periodontology (Carranza, F.A. dan Newman. M.G. eds.). Ed. Ke-8. Saunders,Philadelphia. h. 111-20. Notkins, A.L. 1973. Immunological defence and immunological injury in Herpes simplex virus infection. Dalam Comparative Immunology of the Oral Cavity (Mergenhagen, S.E. dan Scherp, H.W. eds.). U.S. Department of Health, Education, and Welfare, Bethesda.h. 192-203. Okamura, K., Tsubakimoto. K., Uobe. K., Nishida. K., dan Tsusui. M., 1979. Serum proteins and secretory component in human carious dentin, J. Dent Res 58: 1127-33. Oppenheim J.J. dan Horton, J.E. 1973. Role of cellular immunity in oral disease. Dalam Comparative Immunology of the Oral Cavity (Mergenhagen, S.E. dan Scherp, H.W. eds.). U.S. Department of Health, Education, and Welfare, Bethesda. h. 221-36. Orland, F.J., 1982, Microbiology in Clinical Dentistry, John Wright PSG, Boston Reynolds, J.J., Meikle, M.C., 1997, Mechanisms of Connective Tissue Matrix Destruction in Periodontitis, Periodontology 2000, 14: 144-157 Universitas Gadjah Mada 14 Roeslan, B.O. 1990. Efek Protektif sIgA air liur terhadap kuman kariogenik Streptocaccus mutans plak gigi. Ml Kedokt Gigi Edisi Khusus: 11-24. Roitt, I.M., Brostoff. J., dan Nale. D. 1998. Immunology. Ed. Ke-2. Gower Med., New York. Roitt, I.M., dan Lehner, T. 1998. Immunologyof Oral Diseases. Blackwell Sci. Puhl., Oxford. Roth GI and Calmes R., 1981, Oral Biology, The CV Mosby Co., St. Louis Salvi, G.E.. Lawrence, H.P., Offenbacher, S., Beck, J.D., 1997, Influence of Risk Factors on the Patogenesis of Periodontitis, Periodontology 2000, 14: 173201. Sanz, M., Newman, M.G., dan Nisengard . R. 1996. Periodontal microbiology, dalam Clinical Periodontology (Carranza, F.A. dan Newman, M.G. eds.). Ed. Ke-8. Saunders, Philadelphia. h. 342-72. Shulman, L.B. 1973. Immunology of allogeneic tooth transplantation. Dalam Comparative Immunology of the Oral Cavity (Mergenhagen, S.E. dan Scherp. H.W. eds.). U.S. Department of Health Education, dan Welfare, Bethesda. h. 159-181. Steve, M. Torabinejad, M., dan Blanskenship, J. 1991. The concentration of prostaglandin E2 in human penradicular lesions. J Endodon 17:97-9. Sumitami, M., dan Tsutsui, M. 1971. Salivary, serum, and microbial components of human carious dentin. J Dent Res 51: 1067-70. Svetcov S.D., DeAngelo, J.E., McNamara, T., dan Nevins, A.J. 1983. Serum immunoglobulin levels and bacterial flora in subjects with acute oro-facial swellings. J Endodon 9:2335. Tenovuo, J. dan Lagerlof, F. 1994. Saliva. Dalam Textbook of Clinical Cariology (Thylstrup, A. dan Fejerskov, 0. eds.). Ed. Ke-2. Munksgaard, Copenhagen. h. 17-43. Weels. J.V. dan lsbister. J.P. 1991. Hematologic diseases. Dalam Basic and Clinical Immunology (Stites, D.P. dan Terr, A.B. eds.). Ed. Ke-7. Appleton & Lange, Connecticut. h. 576-91. Williams, R.C. dan Gibbons, R.J. 1972. Inhibition of bacterial adherence by secretory immunoglobulin A. Science 177: 697-9. Zvischwartz, Goultschin, J., Dean, D.D., Boyan, B.D., 1997, Mechanisms of Alveolar Bone Destruction in Periodontitis, Periodontology 2000, 14: 158172 Universitas Gadjah Mada 15










