SKRIPSI Diajukan untuk memenuhi sebagian syarat
advertisement

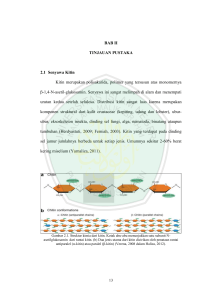
ISOLASI DAN IDENTIFIKASI MIKROORGANISME KITINOLITIK ASAL LIMBAH CAIRAN RUMEN SAPI SERTA OPTIMASI PRODUKSI ENZIM KITINASE SKRIPSI Diajukan untuk memenuhi sebagian syarat memperoleh Derajat Sarjana S-1 pada Program Studi Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam OLEH : WA ODE SURYANI F1C1 11 035 UNIVERSITAS HALUOLEO KENDARI 2016 ii KATA PENGANTAR Puji dan syukur penulis haturkan kehadirat Allah SWT atas limpahan rahmat, taufik serta hidayah-Nya sehingga hasil penelitian yang berjudul “Isolasi Dan Identifikasi Mikroorganisme Kitinolitik Asal Limbah Cairan Rumen Sapi Serta Optimasi Produksi Enzim Kitinase” dapat diselesaikan. Teriring doa, shalawat dan salam atas Nabi Muhammad SAW beserta keluarga. Secara khusus dengan hati yang tulus penghargaan, rasa patuh dan terima kasih yang tak terhingga penulis persembahkan kepada Ayahanda La Ode Masrani dan Ibunda Musrifa tercinta sebagai tanda bakti atas doa restu, semangat bimbingan, arahan kepercayaan, pengorbanan, curahan kasih sayang dan dukungan materil yang diberikan kepada penulis. Penulis menyadari bahwa dalam penyusunan hasil penelitian ini tidak sedikit hambatan yang dihadapi tetapi semuanya itu dapat teratasi berkat petunjuk dari Allah SWT dan disertai ketabahan, kesabaran dan keyakinan dalam berusaha serta berkat bimbingan dan arahan yang sangat berharga dari berbagai pihak. Untuk itu pada kesempatan ini penulis menyampaikan penghargaan dan terima kasih yang setinggi-tingginya kepada Ibu Desy Kurniawati, S,Si., M.Si dan Bapak Drs. H. Muh. Natsir, M.Si., yang selalu memberikan pengarahan dan bimbingan serta meluangkan waktu untuk memberikan arahan dan perbaikanperbaikan sejak awal hingga penyelesaian hasil penelitian ini. Suatu hal yang tidak terlupakan atas dorongan dan bimbingan, serta iii arahan dan bantuan kepada penulis selama melakukan penelitian, maka patutlah kiranya penulis menyampaikan ucapan terima kasih serta penghargaan kepada semua pihak, khususnya : 1. Bapak Prof. Dr. Ir. Usman Rianse, M.Si selaku Rektor Universitas Halu Oleo. 2. Bapak Dr. Muh. Zamrun F., M.Si., M.Sc. selaku Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Halu Oleo. 3. Bapak Dr. La Ode Ahmad Nur Ramadhan, M.Si selaku Ketua Jurusan Kimia FMIPA Universitas Halu Oleo. 4. Ibu Desy Kurniawati, S,Si., M.Si selaku Sekretaris Jurusan Kimia FMIPA Universitas Halu Oleo. 5. Bapak Dr. Imran M.Si., selaku kepala Laboratorium Jurusan Kimia FMIPA Universitas Halu Oleo yang telah memberikan izin kepada penulis untuk melaksanakan penelitian di laboratorium Biokimia. 6. Bapak Dr. Imran M.Si., ibu Dr. Prima Endang Susilowati, M.Si., dan ibu Halimahtussaddiyah Ritonga, S.Si., M.Si selaku Dewan Penguji yang telah banyak memberikan ide dan saran bagi penulis dalam menyelesaikan tugas akhir. 7. Bapak dan ibu dosen Jurusan Kimia, serta seluruh staf di lingkungan FMIPA UHO atas segala fasilitas dan pelayanan yang diberikan kepada penulis dalam menuntut ilmu. 8. Kepada saudaraku La Ode Halim, Wa Ode Agustina, Wa Ode Nur Hanifa, Wa Ode Resky dan La Ode Yusuf serta seluruh keluarga tercinta terima kasih atas doa dan motivasinya sehingga penulis dapat menyelesaikan studi iv dengan baik. 9. Kepada analis laboratorium Ibu Hafni, Ibu Hasma dan Kak Meilani Safitri, S.Si., yang telah membantu memperlancar berlangsungnya penelitian ini. 10. Saudara-saudariku Angkatan 2011 (Sukma S.Si, Ratih, Ain S.Si, Fati, Tia, Osti, Kadek, Melani S.Si, Nur S.Si, Mega S.Si, Herlin S.Si, Tini S.Si, Fetty S.Si, Lia S.Si, Didit S.Si, Sri S.Si, Via S.Si, Hasmi S.Si, Risma S.Si, Ida S.Si, Lusi, Anatia, Suri, Anti, Tuti S.Si, Delvi S.Si, Dedeng, Fina S.Si, Chen Chen S.Si, Andri, Hendra S.Si, Anugrah S.Si, Efraim S.Si, Dion S.Si, Jafar S.Si, Adi, Herdin S.Si, Arham, Andi S.Si, Izar S.Si, Alfan S.Si, Razi S.Si, Ahyar, Wino S.Si, Manan) terima kasih atas kerja samanya selama perkuliahan dan penelitian. 11. Senior-senior yang baik hati Kak Jiran S.Si, Kak Marni S.Si, Kak Yuyun S.Si, Kak Amel S.Si, Kak Dijah S.Si, Kak Piteng S.Si, Kak Asnin S.Si yang senantiasa menyumbangkan pemikiran dan ide maupun tenaga kepada penulis. 12. Anak-anak Biokimia Sukma, Ratih, Andri, Ain, Osti, Kadek, Fina, Fati, Diva, Wulan terima kasih atas kerjasama selama ini sebagai rekan-rekan seperjuangan di Biokimia. 13. Junior-junior yang sering membantu Ismar, Hasrobin, Pipi Andriani, Dahlia, Muli dan yang lainnya dari angkatan 2012, 2013 dan 2014 yang tidak bisa disebut satu persatu. 14. Kepada semua pihak yang tidak dapat disebutkan namanya satu persatu yang turut membantu penulis dalam menyelesaikan penulisan laporan hasil v penelitian. Semoga Allah memberikan balasan yang lebih baik, dan mencatatnya sebagai amal jariyah sehingga akan memperoleh balasan pahala dari Allah subhanahu Wata’Ala, akhir kata penulis berharap semoga khasanah ilmu yang terungkap dalam hasil penelitian ini dapat memberikan banyak manfaat. Aamiin. Kendari, April 2016 Penulis vi ISOLASI DAN IDENTIFIKASI MIKROORGANISME KITINOLITIK ASAL LIMBAH CAIRAN RUMEN SAPI SERTA OPTIMASI PRODUKSI ENZIM KITINASE Oleh : Wa Ode Suryani F1C1 11 035 INTISARI Isolasi dan identifikasi mikroorganisme kitinolitik asal limbah cairan rumen sapi serta optimasi produksi enzim kitinase telah dilakukan. Penelitian ini bertujuan untuk mengisolasi, mengkarakterisasi dan mengoptimasi produksi enzim kitinase yang dihasilkan oleh bakteri kitinolitik yang berasal dari limbah cairan rumen sapi yang diperoleh dari Tempat Pemotongan Hewan (TPH) Anggoeya, Kendari Sulawesi Tenggara. Penelitian ini terdiri atas tiga tahap, yaitu isolasi dan seleksi bakteri kitinolitik, karakterisasi dan identifikasi isolat terpilih dan optimasi produksi enzim kitinase. Mencakup variasi konsentrasi substrat, variasi suhu dan variasi pH. Kondisi optimum produksi enzim kitinase yang diukur aktivitas kitinasenya menggunakan spektrofotometer UV-Vis pada panjang gelombang 584 nm. Enzim kitinase dapat diperoleh dari hasil isolasi bakteri kitinolitik dengan cara menumbuhkan pada media Luria Bertani cair yang mengandung substrat kitin sebagai penginduksi kitinase pada suhu dan pH tertentu yang sesuai. Isolat bakteri kitinolitik yang berhasil ditumbuhkan dan diisolasi, diperoleh indeks kitinolitik sebesar 7,59. Hasil pengamatan morfologi dan uji biokimia menunjukkan isolat bakteri kitinolitik merupakan bakteri Gram negatif berbentuk batang dari spesies bakteri Lactobacillus ruminus. Enzim kitinase diperoleh pada kondisi optimum yaitu konsentrasi substrat sebesar 0,08% (b/v) dengan suhu optimum produksi 40ºC pada pH 6 dengan aktivitas enzim sebesar 125,943 U/mL. Kata Kunci : Kitin, Kitinolitik, N-asetilglukosamin, Rumen Sapi vii ISOLATION AND IDENTIFICATION OF CHITINOLYTIC MICROORGANISM FROM THE COW RUMEN LIQUID WASTE AND OPTIMATION OF ENZYME CHITINASE PRODUCTION By : Wa Ode Suryani F1C1 11 035 ABSTRACT Isolation and identification of microorganisms chitinolytic from cow rumen fluid waste and chitinase enzyme production optimation was carried out. The aims of this study are to isolate, characterize and optimize the production of chitinase enzymes produced by chitinolytic bacteria from cow rumen fluid waste obtained from slaughtering place (TPH) Anggoeya, Kendari, Southeast Sulawesi. The study consisted of three stages, there are the isolation and selection of chitinolytic bacteria, characterization and identification of selected bacteria and optimation of the production of the enzyme chitinase. Includes a variety of substrate concentration, temperature variations and variations in pH. The optimum production conditions of the chitinase enzyme activity was measured by UV-Vis spectrophotometer at a wavelength of 584 nm. Chitinase enzyme can be obtained from the isolation of chitinolytic bacteria by growing in Luria Bertani liquid medium containing chitin as an inducer of chitinase substrate at a certain temperature and pH appropriate. Chitinolytic bacterial isolates were successfully grown and isolated, obtained chitinolytic index of 7.59. The observation of morphological and biochemical tests showed bacteria chitinolytic a rod-shaped Gram-negative bacterium of the species Lactobacillus ruminus. Chitinase enzyme obtained at the optimum condition that is the substrate concentration of 0.08% (w/v) with a temperature of 40ºC production optimum at pH 6 with the enzyme activity of 125.943 U/mL. Keywords : Chitin, Chitinolytic, N-asetilglukosamin, Cow Rumen viii DAFTAR ISI Halaman HALAMAN JUDUL i HALAMAN PENGESAHAN ii KATA PENGANTAR iii INTISARI vii ABSTRACT viii DAFTAR ISI ix DAFTAR TABEL xii DAFTAR GAMBAR xiii DAFTAR LAMPIRAN xiv DAFTAR ARTI LAMBANG DAN SINGKATAN xv I. II. PENDAHULUAN A. Latar Belakang 1 B. Rumusan Masalah 3 C. Tujuan Penelitian 3 D. Manfaat Penelitian 4 TINJAUAN PUSTAKA A. Rumen Sapi 5 B. Kitin 7 C. Mikroorganisme Kitinolitik 8 D. Kitinase 9 E. Identifikasi Mikroorganisme 1. Morfologi koloni Bakteri (Makroskopis) 10 2. Morfologi Sel Bakteri (Mikroskopis) 11 3. Uji Biokimia 12 F. Kondisi Produksi Enzim 14 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian 16 B. Alat dan Bahan 16 ix 1. Alat 16 2. Bahan 16 C. Metode Penelitian 17 1. Pengambilan dan Preparasi Sampel Rumen Sapi 17 2. Proses Pembuatan Kitin 17 a.Deproteinasi 17 b.Demineralisasi 18 c.Dekolorisasi 18 3. Pembuatan koloidal kitin 18 4. Pembuatan Media Kitin 19 5. Isolasi Bakteri Kitinolitik 19 6. Karakterisasi Bakteri Kitinolitik 20 a. Identifikasi Isolat Terpilih 20 1. Morfologi Bakteri 2. Pewarnaan Gram b. Uji Biokimia 21 1. Uji Fermentasi karbohidrat 2. Uji Methyl Red- Voges Proskauer (MR-VP) 3. Uji Sitrat 4. Uji Katalase 5. Uji Hidrogen Sulfida 7. Optimasi Kondisi Produksi Enzim 22 a. Penentuan Substrat Optimum untuk Produksi Enzim 22 Kitinase b. Penentuan Suhu Optimum untuk Produksi Enzim 23 Kitinase c. Penentuan pH Optimum untuk Produksi Enzim Kitinase 23 8. Pengukuran Aktivitas Enzim 23 9. Penentuan Indeks Kitinolitik 24 a. Penentuan Indeks Kitinolitik 24 b. Penentuan Aktivitas Kitinase 24 x IV. HASIL DAN PEMBAHASAN A. Pengambilan Sampel Cairan Rumen Sapi 26 B. Isolasi, dan Seleksi Bakteri 26 C. Karakterisasi dan Identifikasi Isolat 28 D. Optimasi Kondisi Produksi 32 1. Penentuan Substrat Optimum untuk Produksi Enzim 32 Kitinase 2. Penentuan Suhu Optimum untuk Produksi Enzim Kitinase 33 3. Penentuan pH Optimum untuk Produksi Enzim Kitinase 35 Kurva Pertumbuhan Bakteri Kitinolitik 36 PENUTUP 38 DAFTAR PUSTAKA 39 LAMPIRAN 44 E. V. xi DAFTAR TABEL No Teks Halaman 1. Kandungan cairan rumen 6 2. Perbedaan Gram Positif dan Gram Negatif 12 3. Aktivitas Kitinolitik Bakteri 27 4. Uji Biokimia pada Isolat Bakteri Kitinolitik 29 xii DAFTAR GAMBAR No Teks Halaman 1 Rumen Sapi 5 2 Struktur Kitin 8 3 Gambaran morfologi koloni bakteri 11 4 Pengaruh pH terhadap Pertumbuhan Mikroba 14 5 Pengaruh suhu terhadap pertumbuhan Mikroba 15 6 Kondisi Fisik Rumen Sapi 26 7 Morfologi Bakteri Kitinolitik 31 8 Pengaruh Konsentrasi Substrat terhadap Produksi Enzim Kitinase 33 9 Pengaruh Variasi Suhu terhadap Produksi Enzim Kitinase 34 10 Pengaruh Variasi pH terhadap Produksi Enzim Kitinase 36 11 Kurva Pertumbuhan Bakteri kitinolitik 37 xiii DAFTAR LAMPIRAN No Teks Halaman 1 Peta Lokasi Pengambilan Sampel Cairan Rumen Sapi 44 2 Gambaran Umum Alur Penelitian 45 3 Diagram Alir Pengambilan Sampel, Isolasi dan Seleksi Bakteri Kitinolitik, Uji Mikroskopi dan Biokimia 46 4 Pembuatan Koloidal Kitin 49 5 Pembuatan Media 50 6 Optimasi Kondisi Produksi Enzim Kitinase 51 7 Pengukuran Aktivitas Enzim 52 8 Diagram pembuatan kitin dari kulit udang 53 9 Pembuatan Larutan 54 10 Hasil Penelitian 57 11 Dokumentasi 62 xiv DAFTAR ARTI LAMBANG DAN SINGKATAN Lambang / Singkatan Arti Lambang / Singkatan % Persen LB Luria bertani g Gram mL Mili Liter mg/mL Mili gram per mili liter μL Mikro Liter mm Mili Meter cm Senti Meter °C Derajat Celsius ± Kurang lebih BTB Brom Timol Blue MR-VP Methyl Red_Voges Proskauer pH Negatif Logaritma dari Konsentrasi Ion H+ rpm Rotasi per menit λ Panjang gelombang NA Nutrient Agar GlcNAc N-asetilglukosamin TPH Tempat Pemotongan Hewan xv I. PENDAHULUAN A. Latar Belakang Perkembangan dan kemajuan bioteknologi telah mempengaruhi peningkatan pendayagunaan enzim, baik digunakan dalam bentuk hasil ekstraksinya maupun langsung dalam bentuk sel mikroorganisme. Enzim telah banyak digunakan dalam produksi pangan maupun non pangan (Judoamidjojo, dkk. 1989). Salah satu enzim yang banyak digunakan dalam bidang industri baik pangan maupun non pangan ialah enzim kitinase. Peranan kitinase menjadi perhatian besar karena berperan terhadap kehidupan masyarakat dalam bidang pangan maupun non pangan mendorong ilmuwan dan peneliti melakukan eksplorasi mikroorganisme kitinolitik. Mikroorganisme penghasil kitinase ini masih belum banyak diketahui baik tentang jumlah, keragaman maupun fungsi kitinase yang dihasilkan, walaupun kitin merupakan salah satu polimer yang melimpah di alam (Haliza, 2012). Kitin ialah senyawa karbohidrat yang termasuk dalam polisakarida, tersusun atas monomer-monomer asetilglukosamin yang saling berikatan dengan ikatan 1,4 beta membentuk suatu unit polimer linier yaitu β 1,4-N-asetil-Dglukosamin yang merupakan salah satu zat yang banyak digunakan dalam produksi pangan dan non pangan (Pujiastuti, 2001). Kitin adalah polimer yang paling melimpah di laut. Pada kelimpahan di muka bumi, kitin menempati posisi kedua setelah selulosa. Hal ini karena kitin dapat ditemukan di berbagai organisme eukariotik termasuk serangga, 1 moluska dan krustasea. 2 Mikroorganisme pendegradasi kitin umumnya berasal dari kelompok bakteri. Enzim kitinase yang dihasilkan oleh mikroorganisme kitinolitik mempunyai potensi tinggi untuk mendegradasi limbah yang mengandung kitin, karena dengan adanya enzim kitinase memungkinkan konversi kitin yang melimpah menjadi produk yang berguna (Muharni, 2010). Beberapa bakteri kitinolitik yang telah berhasil diisolasi dari air dan tanah diantaranya Streptomyces, Bacillus dan Arthrobacter. Namun, bakteri kitinolitik juga terdapat dalam rumen sapi. Rumen sapi dilaporkan memiliki aktivitas kitinolitik, yakni mampu menguraikan kitin. Mikroorganisme kitinolitik yang terdapat dalam rumen sapi berasal dari pakan yang dikonsumsinya, beberapa jenis pakan yang mengandung kitin ialah bekatul dan rumput raja. Hal ini diungkapkan oleh Wahyu (1992) yang menjelaskan bahwa bekatul mengandung zat anti nutrisi seperti kitin, hemoglutinin dan anti tripsin. Kemampuan ini menyebabkan kelompok bakteri tersebut berpotensi besar untuk dimanfaatkan, misalnya: sebagai penghasil kitinase yang berguna dalam industri pangan, kosmetik, farmasi, dan lain-lain (Pujianto ,dkk. 2008). Rumen merupakan kantong besar dengan berbagai kantong yang menyimpan dan mencampur pakan hasil fermentasi mikroba. Kondisi dalam rumen adalah anaerobik (Padmono. 2005). Mikroorganisme yang terdapat di dalam rumen didominasi oleh bakteri dan protozoa, selain itu juga terdapat mikroorganisme lain seperti fungi dan flagellata yang sering terdapat pada hewanhewan ruminansia muda. Perbandingan mikroorganisme di dalam rumen berkisar 3 dari 1,4x107 per mL cairan rumen sedangkan jumlah protozoa sebesar 106 per mL cairan rumen ( Nuswantara. 2002 ). Berdasarkan pemaparan di atas, maka peneliti berkeinginan untuk melakukan penelitian mengenai isolasi dan identifikasi mikroorganisme kitinolitik asal limbah cairan rumen sapi serta optimasi produksi enzim kitinase. B. Rumusan Masalah Rumusan masalah dalam penelitian ini adalah sebagai berikut : 1. Bagaimana kemampuan bakteri kitinolitik dari limbah cairan rumen sapi dalam mendegradasi kitin? 2. Bagaimana karakteristik isolat bakteri kitinolitik yang berasal dari limbah cairan rumen sapi? 3. Bagaimanakah kondisi pH, konsentrasi substrat dan suhu optimum untuk produksi enzim kitinase? C. Tujuan Penelitian Tujuan yang ingin dicapai dalam penelitian ini, yaitu: 1. Mengetahui kemampuan bakteri kitinolitik dari limbah cairan rumen sapi dalam mendegradasi kitin. 2. Mengetahui karakteristik isolat bakteri kitinolitik yang berasal dari limbah cairan rumen sapi. 3. Menentukan kondisi optimum produksi enzim kitinase baik pH, konsentrasi substrat dan suhu optimum. 4 D. Manfaat Penelitian Manfaat yang diharapkan dari penelitian ini adalah sebagai berikut: 1. Dapat memberikan informasi tentang pemanfaatan limbah cairan rumen sapi sebagai penghasil bakteri kitinolitik dan kemampuan bakteri tersebut dalam mendegradasi kitin. 2. Mengembangkan keterampilan untuk mengisolasi dan identifikasi bakteri kitinolitik. 3. Menambah wawasan keilmuan peneliti, khususnya bidang bioteknologi. II. TINJAUAN PUSTAKA A. Rumen Sapi Rumen ialah bagian lambung sapi yang merupakan organ utama proses pencernaan fermentatif. Di dalam rumen hidup berbagai jenis mikroba seperti bakteri, fungi, yeast dan protozoa. Menurut Dehority dan Orpin (1997) populasi terbesar mikroba rumen terutama adalah bakteri anaerob dan protozoa bersilia yang terutama berperan dalam aktivitas fermentasi (Rahayu, dkk. 2003). Kondisi dalam rumen adalah anaerob dan mikroorganisme yang paling sesuai dan dapat hidup yang ditemukan di dalamnya. Tekanan osmosisnya mirip dengan tekanan aliran darah. Temperatur di dalam adalah 30-42oC, pH dipertahankan dengan adanya absorpsi asam lemak dan amonia. Saliva yang masuk kedalam rumen berfungsi sebagai buffer dan membantu mempertahankan pH pada 6,8. Hal ini disebabkan oleh tingginya kadar ion HCO3- dan PO43- (Arora, 1989). Gambar 1. Rumen sapi Sumber : Commons.wikimedia.org, 2013 Rumen merupakan salah satu limbah rumah pemotongan hewan yang belum dimanfaatkan secara optimal bahkan ada yang dibuang begitu saja sehingga 5 6 menimbulkan pencemaran lingkungan. Limbah ini sangat potensial bila dimanfaatkan sebagai bahan pakan ternak karena rumen merupakan bahan pakan yang belum tercerna sempurna. Selain itu, rumen sapi kaya akan berbagai komposisi sebagaimana ditunjukkan pada Tabel. I berikut. Tabel. 1 Kandungan Cairan Rumen (Suhermiyati. 1984) Kandungan Persentase (%) Air 8,8 Protein kasar 9,63 Lemak 1,81 Serat kasar 24,60 Berat Ekstrak Tanpa Nitrogen 38,40 Abu 16,76 Kalsium 1,22 Posfor 0,29 Cairan rumen sapi, selain mengandung mikroba dan enzim-enzim yang disekresikan oleh mikroba tersebut, juga mengandung zat-zat makanan hasil perombakan mikroba, serta vitamin-vitamin dan mineral-mineral yang larut dalam cairan rumen. Zat-zat makanan tersebut kaya akan protein dan asam amino. Komposisi asam amino, mineral dan vitamin dalam endapan cairan rumen seperti halnya enzim-enzim, juga tergantung dari perlakuan pakan yang diberikan (Budiansyah, dkk. 2011). Dalam rumen terdapat empat jenis mikroorganisme, yaitu bakteri, protozoa, fungi dan flagellata. Dari keempat mikroorganisme tersebut bakteri mempunyai jenis dan populasi yang paling tinggi. Cacahan sel per gram isi rumen dapat mencapai 1010-1011 (McDonald, dkk. 2002). Mikroba rumen menghasilkan produk fermentasi berupa Volatil Fatty Acid (asam asetat, asam propionat, asam butirat), CO2, CH4, dan NH3. Zat makanan yang didegradasi adalah karbohidrat, 7 lemak dan protein. Interaksi yang terjadi antar mikroba rumen adalah simbiosis mutualisme. Bakteri dan protozoa yang hidup dalam rumen menjadikan ruminansia mampu mencerna serat (Hobson dan Stewart, 1992). B. Kitin Kitin adalah suatu polisakarida, polimer linier yang tersusun oleh monomer β-1,4-N-asetil-D-glukosamin (GlcNAc). Kelimpahan kitin di alam menempati urutan terbesar kedua setelah selulosa dan terdistribusi luas di lingkungan biosfer seperti pada kulit crustaceae (kepiting, udang dan lobster), ubur-ubur, komponen struktural eksoskeleton insekta, dinding sel fungi (22-40%), alga dan nematoda. Kitin mempunyai rumus kimia (C8H13NO5)n dengan struktur β-(1,4)-2-asetamida-2-deoksi-D-glukosa didapat dari isolasi kulit dan kepala hewan berkulit keras (Crustacea), serangga dan jamur dengan cara deproteinasi dan demineralisasi (Windholz, 1983). Kitin memiliki ukuran molekul yang relatif besar dan kelarutan rendah, sulit diserap tubuh manusia, sehingga aplikasinya sangat terbatas dan menjadi sumber utama pencemaran senyawa organik (Haliza., W, dkk. 2012). Kitin dan turunannya banyak diaplikasikan pada beberapa industri antara lain industri pangan, farmasi, kosmetik, tekstil dan dapat digunakan sebagai bahan tambahan atau pengawet alami pada makanan. Kitin juga digunakan sebagai antikoagulasi darah, mempercepat penyembuhan luka, dapat menghambat pertumbuhan bakteri dan fungi sehingga banyak dimanfaatkan sebagai antimikroba (Apriani, 2008). 8 Gambar 2. Struktur Kitin Sumber : (Cahyani, 2013) Menurut Muzarelli (1977) proses isolasi kitin secara kimiawi melibatkan proses pemisahan mineral (demineralisasi), pemisahan protein (deproteinisasi) dan penghilangan warna (dekolorisasi). Ikatan antara kitin dengan protein dalam bahan adalah ikatan hidrogen antara gugus karboksil dari protein dengan amino pada glukosamin. Larutan NaOH akan memecahkan ikatan hidrogen tersebut dan menghasilkan Na-proteinat yang larut. Kitin dikelilingi oleh matriks protein (Zikakis, 1984). C. Mikroorganisme kitinolitik Bakteri penghasil enzim kitinolitik banyak berada pada habitat yang memiliki kandungan kitin, seperti kompos yang mengandung kitin (Sakai, dkk.1998), eksoskeleton crustacea (Vogan, dkk. 2002), air laut, sedimen laut dan tanah (Chemin, dkk. 1995). Pada tahun 1992, Liaw dan Mah menyatakan bahwa bakteri kitinolitik umumnya merupakan bakteri halofilik karena banyak dijumpai pada air, sedimen laut dan crustacea yang hidup pada lingkungan berkadar garam tinggi. Mikroorganisme kitinolitik adalah mikroorganisme yang dapat mendegradasi kitin dengan menggunakan enzim kitinase. Mikroorganisme ini 9 dapat diperoleh dari berbagai sumber seperti rizosphere, phyllosphere, tanah atau dari lingkungan air seperti laut, danau, kolam atau limbah udang dan sebagainya. Selain lingkungan mesofil, mikroorganisme kitinolitik juga telah berhasil diisolasi dari lingkungan termofilik seperti sumber air panas, daerah geotermal dan lainlain. Mikroorganisme kitinolitik dapat diseleksi keberadaannya dengan mendegradasi media agar kitin yang dapat dideteksi dengan adanya zona bening disekitar koloni bakteri (Herdyastuti ,dkk. 2009). D. Kitinase Kitinase adalah enzim yang mendegradasi kitin menjadi N- asetilglukosamin, Degradasi kitin dapat dilakukan oleh organisme kitinolitik dengan melibatkan enzim kitinase. Organisme pendegradasi kitin umumnya berasal dari kelompok mikroorganisme diantaranya adalah dari kelompok bakteri. Enzim kitinase yang dihasilkan oleh mikroorganisme kitinolitik mempunyai potensi tinggi untuk mendegradasi limbah yang mengandung kitin, karena dengan adanya enzim kitinase memungkinkan konversi kitin yang melimpah menjadi produk yang berguna (Muharni, 2010). Enzim kitinolitik juga berperan sebagai agen biokontrol terhadap jamur. Hal ini dikarenakan kitin yang merupakan komponen utama dinding sel jamur dapat didegradasi enzim kitinase menghasilkan produk yang ramah lingkungan dibandingkan penggunaan zat kimia juga sebagai agen biokontrol terhadap serangga patogen pada tumbuhan, biopestisida, terlibat dalam pembuatan protein sel tunggal dan berperan sebagai obat terhadap penyakit parasit (Apriani, 2008). 10 Produksi enzim kitinolitik banyak dilakukan dengan memanfaatkan bakteri kitinolitik karena medium pemeliharaan tidak mahal, sehingga dapat mengurangi biaya produksi enzim (Saules, dkk. 2006). Sama seperti enzim pada umumnya, aktivitas enzim kitinolitik juga dipengaruhi oleh faktor lingkungan seperti pH, dan suhu, serta oleh faktor kimiawi tertentu secara khusus dapat mempengaruhi enzim tersebut (Campbell, dkk. 2002). pH optimum enzim kitinolitik berbeda bagi setiap organism. pH optimum enzim kitinolitik pada tumbuhan tingkat tinggi dan alga adalah 4-9, pada hewan 4,8-7,5 dan pada mikroorganisme 3,5-8. Stabilitas enzim kitinolitik terhadap suhu juga bervariasi untuk setiap organisme (Koga, dkk. 1999). E. Identifikasi Mikroorganisme 1. Morfologi koloni Bakteri (Makroskopis) Identifikasi bakteri yang tumbuh pada media kultur dimulai dengan mengamati karakteristik koloni bakteri. Hal ini penting dikarenakan, dari karakteristik koloni tersebut kita bisa menentukan prosedur atau pemeriksaan selanjutnya untuk identifikasi bakteri yang pasti. Identifikasi terhadap karakteristik koloni bakteri dilakukan secara visual langsung terhadap pertumbuhan bakteri pada permukaan agar. Beberapa hal yang biasa dijadikan sebagai acuan untuk menentukan karakteristik sebuah koloni bakteri, yaitu: Ukuran (biasanya dalam milimeter atau ukuran relatif seperti kecil, sedang, besar) Warna/pigmentasi Bentuk (sirkuler, filamentosa, irreguler) 11 Elevasi (datar, meninggi, konveks, umbilikasi) Batas (tegas, irreguler) Densitas (opak, translusen, transparan) Perubahan pada media (misalnya perubahan pH indikator) (Lay,1994) Gambar 3. Gambaran morfologi koloni bakteri Sumber : Microbiology 101 Laboratory Manual, 2012 2. Morfologi Sel Bakteri (Mikroskopis) Pengamatan morfologi sel bakteri secara mikroskopis dilakukan dengan bantuan pewarnaan yaitu pewarnaan Gram. Uji pewarnaan Gram termasuk dalam pewarnaan differensial yang membutuhkan paling sedikit tiga reagen kimia yang digunakan secara berurutan pada ulasan yang difiksasi menggunakan panas. Pewarnaan bertujuan untuk membedakan bakteri ke dalam kelompok Gram negatif dan Gram positif. Berdasarkan bentuk dan efek pewarnaan Gram, bakteri dikelompokkan menjadi kokus Gram-positif, kokus Gram-negatif, batang Grampositif dan batang Gram-negatif. Morfologi sel bakteri secara mikroskopis dapat membantu untuk identifikasi bakteri. Perbedaan bakteri Gram positif dan Gram negatif dapat dilihat pada Tabel 2. 12 Tabel 2. Perbedaan Gram Positif dan Gram Negatif Perbedaan relatif Ciri Gram Positif Gram negatif Struktur dinding sel Tebal (15-80 nm) berlapis Tipis (10-15 nm) tunggal (mono) Berlapis tiga (multi) Komposisi dinding sel Kandungan lipid rendah Kandungan lipid tinggi (1-4%) (11-25%) Peptidoglikan ada sebagai Peptidoglikan ada lapisan tunggal; didalam lapisan kaku komponen utama sebelah dalam; jumlahnya merupakan lebih dari 50% sedikit, sekitar 10% berat berat kering pada sel kering bakteri Asam tekonat Tidak ada asam tekonat Kerentanan terhadap Lebih rentan Kurang rentan penisilin Pertumbuhan dihambat Pertumbuhan dihambat Pertumbuhan tidak begitu oleh zat-zat warna dengan nyata dihambat dasar Persyaratan nutrisi Relatif rumit pada banyak Relatif sederhana spesies Resistensi terhadap Lebih resisten Kurang resisten gangguan fisik Sumber : Pelczar, 1988 3. Uji Biokimia Penentuan karakteristik kultural dari mikroorganisme dilakukan dengan uji biokimia terhadap metabolisme bakteri. Hal ini dilakukan untuk membantu dalam mengidentifikasi dan mengklasifikasikan organisme dalam kelompok taksonominya. Prinsip uji biokimia adalah bila mikroorganisme ditumbuhkan dalam beberapa jenis media, maka mikroorganisme tersebut akan menunjukkan suatu perbedaan secara makroskopik dalam pertumbuhannya. Perbedaan inilah yang dengan karakteristik kultural. Data yang diperoleh digunakan sebagai dasar pengelompokan mikroorganisme dalam taksonominya masing-masing. Karakteristik kultural ditentukan dengan mengkulturasi mikroorganisme pada media diferensial, yaitu media yang digunakan untuk membedakan secara 13 morfologi dan biokimia kelompok organisme. Media ini mengandung senyawa kimia yang jika mikroorganisme diinokulasi atau inkubasi maka akan menghasilkan perubahan pada penampakan pertumbuhannya atau media yang mengelilingi koloni menunjukkan perbedaan (Cappucino, 1983). Uji karakterisasi yang digunakan antara lain : uji fermentasi karbohidrat, uji hidrogen sulfida, uji katalase, uji simmon sitrat dan uji methyl red adalah sebagai berikut : a. Uji fermentasi karbohidrat bertujuan menentukan kemampuan mikroorganisme mendegradasi dan memfermentasikan karbohidrat yang diikuti oleh pembentukan gas atau asam atau keduanya. b. Uji hidrogen sulfida merupakan uji untuk mengetahui kemampuan mikroorganisme dalam menghasilkan hidrogen sulfida dari senyawa seperti asam amino yang mengandung sulfur atau senyawa sulfur anorganik. c. Uji katalase merupakan uji untuk mengetahui kemampuan bakteri dalam mendegradasi hidrogen peroksida dengan menghasilkan enzim katalase. d. Methyl red adalah indikator pH antara 6,0 (berwarna kuning) sampai 4,4 (berwarna merah). Tes ini merupakan tes kuantitatif untuk bakteri yang menghasilkan asam. Bakteri yang mampu menghasilkan asam kuat (laktat, asetat, formik) dari glukosa melalui jalur fermentasi asam dapat dideteksi dengan uji methyl red. Bakteri yang mempertahankan pH asam dalam jangka waktu yang lama (inkubasi 48-72 jam) yang dikatakan tes methyl red-nya positif (Lay, 1994). e. Uji Sitrat digunakan untuk melihat kemampuan mikroorganisme menggunakan sitrat sebagai satu-satunya sumber karbon dan energi. Bila mikroorganisme 14 mampu menggunakan sitrat, maka asam akan dihilangkan dari medium biakan, sehingga menyebabkan peningkatan pH dan mengubah warna medium dari hijau menjadi biru. F. Kondisi Produksi Enzim Produksi enzim memerlukan optimasi kondisi dalam labu erlenmeyer, yaitu pH, suhu dan konsentrasi subsrat. Lloyd dan Nelson (1984) menyatakan bahwa aktivitas optimum enzim berkisar pada pH pertumbuhan mikrooganisme penghasil enzim tersebut, sehingga pH optimum aktivitas enzim ini berbeda-beda tergantung mikroorganisme penghasil enzimnya. Asidofilik 1 2 3 Alkalifilik Neutrofilik 4 5 6 7 8 9 10 11 12 pH Gambar 4. Pengaruh pH terhadap pertumbuhan Mikroba Sumber : Benefield dan Randall (1980) dalam Jujubandung Suhu berpengaruh langsung terhadap kecepatan pertumbuhan mikroorganisme, kecepatan sintesis enzim dan kecepatan inaktivasi enzim. Suhu yang terlalu tinggi dapat mengakibatkan proses pengeringan protein sehingga dapat mengakibatkan kematian sel. Sedangkan suhu yang terlalu rendah dapat mengakibatkan aktivitas enzim berkurang dan pertumbuhan mikroorganisme terganggu (Gambar 5). 15 Tipe Psikrofilik (Flavobacterium) 0 10 20 Tipe Termofilik (Thermos) Tipe Mesofilik (Eschercia) 30 40 50 60 70 80 Termofilik ekstrim (Thermococcus) 90 100 Temperatur (°C) Gambar 5. Pengaruh suhu terhadap pertumbuhan Mikroba Sumber : Benefield dan Randall (1980) dalam Jujubandung Aerasi berfungsi untuk mempertahankan kondisi aerobik untuk desorpsi CO2, mengatur temperatur subsrat dan mengatur kadar air. Aerasi juga membantu menghilangkan sebagian panas yang dihasilkan sehingga temperatur dapat dipertahankan pada temperatur optimal untuk produksi enzim. Tingkat aerasi dipengaruhi oleh sifat mikroorganisme. Tingkat O2 yang dibutuhkan untuk sintesis produk, jumlah panas metabolik yang harus dihilangkan dari bahan yang mudah menguap harus dihilangkan dan tingkat ruang udara yang tersedia didalam subsrat (Richana, 2000). III. METODE PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan Oktober 2015 sampai dengan bulan April 2016 bertempat di Laboratorium Biokimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Halu Oleo Kendari. B. Alat dan Bahan 1. Alat Alat-alat yang digunakan pada penelitian ini adalah neraca analitik (Acis), autoklaf (Wiseclave), Spektrofotometer UV-Vis, waterbath (HWS24), lemari pendingin (SHARP), pipet mikro (DRAGON ONEMED), mistar, spidol, tabung eppendorf, jarum ose, tip, cawan petri (Pyrex), gelas ukur (Pyrex), gelas kimia (Pyrex), labu takar (Pyrex), erlenmeyer (Pyrex), corong (Pyrex), batang L, spatula, dan pipet ukur, batang pengaduk, hot plate, Oven (Memmert), Filler, termometer, termos air panas (Lion Star). 2. Bahan Bahan yang digunakan yaitu: cairan rumen sapi dari Tempat Pemotongan Sapi (TPH), spritus, Alkohol 96%, Medium LB (Luria Bertani) (Pepton 0,4%, Yeast Extract 0,25%, NaCl 0,5%, MgSO40,3%, Akuades, MgSO4.7H2O), Medium NA (Nutrien Agar), Reagen pewarnaan Gram (kristal violet, aquades, yodium, etanol, safranin), kaldu karbohidrat (glukosa, sukrosa, laktosa, maltosa, manitol, BTB (Brom Timol Blue), kaldu methyl red-Voges Proskauer (MR-VP) (Pepton 0,7% (b/v), dekstrosa 0,5% (b/v), dan KH2PO4 0,5% (b/v)), media SIM (pepton 30 16 17 g/L, beef extract 3 g/L, ferro ammonium sulfat 0,2 g/L, natrium tiosulfat 0,025 g/L, dan agar 3 g/L), Kitin (kulit udang, NaOH 3,5 %, aseton teknis 360 mL, akuades, HCl), Medium koloidal kitin (HCl pekat, NaOH 12 N) dan medium kitin (koloidal kitin, K2HPO4, MgSO4.7H2O, NaCl , (NH4)2SO4, yeast extract dan agar), kasa, kapas steril, alumunium foil, kertas saring, kertas pH dan tisu. C. Metode Penelitian 1. Pengambilan dan Preparasi Sampel Rumen Sapi Sampel diambil dari Tempat Pemotongan Hewan (TPH) Anggoeya Kota Kendari dengan menggunakan botol steril. Semua sampel disegarkan dalam media cair LB (Luria Broth), kemudian diinkubasi selama 48 jam pada suhu 30°C. (Rahayu, S. 2003). 2. Proses Isolasi Kitin Proses isolasi kitin dilakukan sesuai metoda Hang (Fahmi, 1997). Isolasi kitin dari kulit udang meliputi tahap deproteinisasi, demineralisasi dan dekolorisasi. a. Deproteinasi Kulit udang yang telah dibersihkan dan dikeringkan, diperkecil ukurannya kemudian ditimbang sebanyak 42 gram. Setelah itu, kulit udang dipanaskan hingga suhu diatas 100ºC menggunakan pelarut NaOH 3,5% dengan perbandingan 1:10 (b/v) yaitu sebanyak 420 mL yang dilengkapi dengan pengaduk, termometer dan diletakkan diatas penangas air. Pemanasan ini bertujuan untuk proses penghilangan kalsium karbonat yang berlangsung selama 3 17 18 jam dengan pengadukan terus-menerus. Kemudian dicuci beberapa kali dengan air bersih sampai pH netral dan dikeringkan pada suhu 50ºC selama 12 jam. b. Demineralisasi Kitin kasar hasil deproteinasi sebanyak 24 gram dimasukkan dalam gelas kimia 1000 mL. Kemudian sempel ditambahkan HCl sebanyak 360 mL dengan perbandingan 1:15 (b/v) kemudian dilakukan pengadukan tanpa proses pemanasan selama 1 jam. Setelah itu, dilakukan penyaringan sehingga diperoleh residu dan filtrat. Terjadinya pemisahan mineral ditunjukkan dengan terbentuknya gas CO2 yang berupa gelembung-gelembung udara pada saat larutan HCl ditambah ke dalam sampel. Residunya dicuci dengan akuades sampai pH netral yang diukur dengan indikator universal. Kemudian residu dikeringkan dalam oven pada suhu 60oC selama 24 jam, sehingga diperoleh kitin kering. c. Dekolorisasi Kitin yang telah didemineralisasi kemudian didekolorisasi dengan cara merendamnya dengan larutan aseton teknis sebanyak 360 mL atau sampai seluruh kitin telah terendam. Proses perendaman berlangsung selama 7 jam. Setelah proses perendaman, kitin tersebut terlebih dahulu dicuci dengan air mengalir sampai sisa asetonnya hilang lalu dicuci dengan akuades hingga pH netral. Kemudian dikeringkan diudara terbuka. 3. Pembuatan Koloidal Kitin Koloidal kitin dibuat dengan melarutkan 10 gram bubuk kitin dalam 150 mL HCl pekat, lalu diaduk selama 1 jam. Kemudian ditambahkan akuades sebanyak 800 mL, larutan kemudian disaring untuk diambil residunya. Kemudian 19 residu dicuci dengan akuades sampai pH koloid kitin menjadi 3 (Hsu dan Lockwood,1975). 4. Pembuatan Medium Kitin Medium kitin yang dimodifikasi yaitu dengan mencampurkan koloidal kitin 2 gram, K2HPO4 0,1 g, MgSO4.7H2O 0,01 g, NaCl 3 g, (NH4)2SO4 0,7 g, yeast extract 0,05 g dan agar 2 g dalam 100 mL akuades, larutan kemudian dihomogenkan dengan magnetic stirrer dan dipanaskan hingga larut kemudian disterilkan dalam autoklaf pada suhu 121°C selama 15 menit. Medium yang telah steril tersebut kemudian dituang ke dalam cawan petri dan dibiarkan hingga mengeras (Park, dkk. 2000). 5. Isolasi Bakteri Kitinolitik Sebanyak 30 mL medium Luria Bertani yang telah disiapkan kemudian disebar pada media pada medium kitin. Isolasi bakteri dilakukan dengan menggunakan media yang mengandung koloidal kitin yaitu 1%; yeast extract 0,2% (b/v); bacto pepton 0,5% (b/v); MgSO4.7H2O 0,05% (b/v); NaCl 0,5% (b/v); CaCl 0,015% (b/v); H3BO3 0,015% (b/v); Na2MoO4.2H2O 0,015% (b/v) dan bubuk agar-agar sebanyak 3% (b/v) (Yuneta dan Putra, 2010). Sampel diambil sebanyak 0,2 mL dan disebarkan diatas padatan agar untuk menumbuhkan bakteri. Isolat diinkubasi selama 24 jam pada suhu 30ºC. 20 6. Karakterisasi Bakteri Kitinolitik a. Identifikasi Isolat Terpilih 1. Morfologi bakteri Pengamatan morfologi bakteri dilakukan dengan metode seri pengenceran (Platting method) yang dilakukan dengan mengambil sebanyak 1 mL sampel dimasukkan kedalam Erlenmeyer yang berisi 9 mL larutan fisiologis sehingga didapat pengenceran 10-1, untuk mendapatkan pengenceran 10-2 dilakukan dengan mengambil 1 mL dari pengenceran 10-1 dimasukkan kedalam tabung reaksi yang berisi 9 mL larutan fisiologis, demikian seterusnya sampai dibuat pengenceran 106 . Masing-masing seri pengenceran diambil 0,1 mL disebar kedalam cawan petri yang telah berisi media padat. Selanjutnya diinkubasi selama 24-48 jam pada suhu optimum. Koloni yang tumbuh diamati secara makroskopis meliputi bentuk, ukuran, tekstur dan warna. Berdasarkan koloni lalu dilakukan tahap pemurnian sehingga akan diperoleh sejumlah isolat (Darmayasa, 2008). 2. Pewarnaan Gram Kaca penutup dan kaca obyek dibersihkan dengan alkohol 96% hingga bebas lemak, kemudian dilewatkan di atas nyala lampu spritus. Diambil secara aseptik sebanyak satu ose isolat bakteri dan diletakkan pada kaca obyek seluas ± 1 cm2 kemudian dilakukan fiksasi di atas nyala lampu spritus. Diteteskan zat warna dasar (kristal violet) sebanyak 2 tetes dan didiamkan selama 1 menit. Setelah itu dicuci dengan air mengalir lalu dikeringkan. Apusan kemudian ditetesi dengan larutan lugol iodine dan didiamkan selama 1 menit. Setelah kering, dicuci dengan larutan peluntur (alkohol 96%) selama ± 30 detik. Selanjutnya dicuci dengan air 21 mengalir lalu dikeringkan. Setelah kering diberi larutan zat warna pembanding/penutup (safranin) selama 2 menit dan dicuci dengan air mengalir lalu dikeringkan. Setelah itu diamati dengan mikroskop, bakteri Gram positif tampak berwarna biru keunguan sedangkan Gram negatif berwarna merah (Lay, 1994). b. Uji Biokimia 1. Uji Fermentasi Karbohidrat Uji fermentasi karbohidrat dapat dilakukan dengan menyiapkan kaldu karbohidrat 1% yaitu glukosa, sukrosa, laktosa, maltosa, dan manitol. Kaldu karbohidrat yang mengandung BTB (Brom Timol Blue) dimasukkan dalam tabung reaksi. Biakan bakteri dinokulasi pada media salanjutnya diinkubasi pada suhu 30ºC selama 24 jam. Uji positif, bila terjadi pembentukan asam (kaldu berubah menjadi warna kuning) (Lay, 1994). 2. Uji Methyl Red- Voges Proskauer (MR-VP) Uji metil red dapat dilakukan dengan menyiapkan kaldu methyl red-Voges Proskauer (MR-VP) (Pepton 0,7% (b/v), dekstrosa 0,5% (b/v), dan KH2PO4 0,5% (b/v)). Biakan bakteri kemudian diinokulasikan kedalam kaldu MR-VP dan diinkubasi pada suhu 30ºC selama 48 jam atau pada suhu optimum selama 72 jam. Hari berikutnya ditambahkan reagen methyl red. Hasil uji positif bila berwarna merah, dan jika warna kaldu berwarna kuning maka hasil uji negatif (Lay, 1994). 3. Uji Sitrat Biakan diinokulasi pada media Simmon sitrat agar ((NH4)2PO4 0,1% (b/v), KH2PO4 0,1% (b/v), NaCl 0,5% (b/v), Na-Sitrat 0,2% (b/v), MgSO4 0,02% (b/v), 22 BTB 0,08% (b/v), Agar 3% (b/v)) dengan inokulum yang tipis, kemudian diinkubasi pada suhu 30ºC selama 48 jam. Jika terjadi perubahan warna hijau menjadi biru menunjukan hasil uji positif (Lay,1994). 4. Uji Katalase Biakan ditumbuhkan pada media Nutrien Agar (NA) dengan cara ditotolkan dan diinkubasi selama 24 jam pada suhu 30ºC kemudian ditambahkan reagen H2O2 3%. Uji positif ditandai dengan pembentukan gelembung udara pada biakan dan disekitarnya (Lay, 1994). 5. Uji Hidrogen Sulfida (H2S) Uji produksi H2S dilakukan dengan menginokulasi biakan bakteri ke media SIM (Sulfide Indole Motil) (pepton 30 g/L, beef extract 3 g/l, ferro ammonium sulfat 0,2 g/L, natrium tiosulfat 0,025 g/L, dan agar 3 g/L) selama 2448 jam pada suhu 30ºC. Uji positif dengan terbentuknya endapan hitam (Lay,1994). 7. Optimasi Kondisi Produksi Enzim a. Penentuan Substrat Optimum untuk Produksi Enzim Kitinase Penentuan substrat optimum untuk produksi enzim kitinase dilakukan dengan menumbuhkan bakteri sebanyak 0,5 mL pada mdia LB mengandung kitin dari limbah cairan rumen sapi 0,02-0,14% dengan interval konsentrasi 2%, kemudian biakan diinkubasi pada suhu 30ºC selama 24 jam. Aktivitas enzim kitinase diukur dengan menggunakan panjang gelombang 584 nm. 23 b. Penentuan Suhu Optimum untuk Produksi Enzim Kitinase Suhu optimum untuk produksi enzim kitinase, dilakukan dengan menumbuhkan isolat bakteri pada media cair LB yang mengandung substrat optimum yang telah didapatkan untuk produksi enzim kitinase dengan variasi suhu 30ºC, 40ºC, 50ºC dan 60ºC selama 24 jam. Aktivitas enzim kitinase diukur menggunakan spektrofotometer dengan panjang gelombang 584 nm dengan menggunakan larutan standar N-asetilglukosamin. c. Penentuan pH Optimum untuk Produksi Enzim Kitinase pH optimum untuk produksi enzim kitinase dilakukan dengan menumbuhkan isolate bakteri sebanyak 0,5 mL pada media cair LB yang mengandung substrat optimum yang didapatkan dari hasil optimasi produksi enzim, dengan variasi pH 3, 4, 5, 6 dan 7, selanjutnya diinkubasi pada suhu optimum yang didapatkan dari hasil optimasi produksi enzim selama 24 jam. Aktivitas enzim kitinase diukur menggunakan spektrofotometer pada panjang gelombang 584 nm dengan menggunakan larutan standar N-asetilglukosamin. 8. Pengukuran Aktivitas Enzim Aktivitas enzim kitinase ditentukan berdasarkan jumlah N-asetil-Dglukosamin yang dibebaskan hidrolisa substrat koloidal kitin. Senyawa N-asetilD-glukosamin diukur dengan metode Schales (Imoto dan Yagashita,1971)yang dimodifikasi. Satu unit aktivitas dinyatakan sebagai jumlah N-asetil-Dglukosamin (Mmol) yang terbentuk permenit. Aktivitas enzim kitinase menggunakan 200 µL substrat kitin 0,3 %, 200 µL buffer pH 7 dan 200 µL ekstrak kasar enzim yang diinkubasi selama 30 menit 24 pada suhu 40ºC. Campuran tersebut kemudian diinkubasi dengan kecepatan 9000 rpm selama 4 menit. Selanjutnya 500 µL filtrat yang dihasilkan ditambahkan 500 µL akuades dan di tambahkan 1 mL pereaksi Schales, dipanaskan selama 10 menit untuk menghentikan aktivitas enzim dan setelah dingin diukur absorbansinya pada panjang gelombang 584 nm. N-asetilglukosamin sebagai kurva standar. 9. Analisis Data a. Penentuan Indeks Kitinolitik Penentuan indeks kitinolitik (IK) dilakukan dengan cara mengukur diameter zona bening yang terbentuk disekitar koloni bakteri, kemudian dibagi dengan diameter koloni yang tumbuh (Tresnawati, dkk., 2006). Indeks Kitinolitik = Diameter Zona Bening - Diameter Koloni Diameter Koloni b. Penentuan Aktivitas Kitinase Aktivitas enzim Kitinase dihitung berdasarkan data kadar N-asetil glukosamin relatif sebagai mg N-asetil glukosamin yang dihasilkan per mL filtrat enzim dengan menggunakan rumus : A = [ N - Asetilglukosamin] BM.N - Asetilglukosamin dimana, A [N-asetilglukosamin] = Aktivitas enzim kitinase (Unit/mL) = Kadar N-asetil glukosamin hasil hidrolisis (mg/L) BM N-asetilglukosamin = Berat molekul N-asetil glukosamin (g/mol) t = Waktu inkubasi (menit) 25 Satu unit aktivitas kitinase didefinisikan sebagai jumlah enzim yang diperlukan untuk melepas 1 µmol N-asetil glukosamin/menit. Penentuan kadar Nasetil glukosamin hasil hidrolisis oleh enzim kitinase didasarkan pada kurva larutan standar N-asetil glukosamin. Larutan standar N-asetil glukosamin dibuat pada kisaran konsentrasi N-asetil glukosamin 2,5; 5; 7,5; 10; 12,5 dan 15 dan diukur serapannya setelah penambahan pereaksi Schales secara spektrofotometer pada panjang gelombang 584 nm (Richana, 2002). IV. HASIL DAN PEMBAHASAN A. Pengambilan Sampel Cairan Rumen Sapi Pengambilan sampel limbah cair rumen sapi dilakukan di Tempat Pemotongan Hewan (TPH) Anggoeya, Kendari Sulawesi Tenggara. Kondisi rumen sapi pada tempat pengambilan sampel mempunyai pH 7 dan suhu 30˚C. Kondisi fisik sampel dapat dilihat pada Gambar. 6. Gambar 6. Kondisi Fisik Rumen Sapi (Koleksi Pribadi, 2015) B. Isolasi dan Seleksi Bakteri Kitinolitik Tahap isolasi dan seleksi bakteri dilakukan untuk memperoleh spesies bakteri dalam bentuk yang terpisah. Koloni terpisah yang dihasilkan kemudian ditumbuhkan pada media pertumbuhan yang mengandung koloidal kitin sehingga diperoleh bakteri yang dapat tumbuh pada konsentrasi tertentu. Komposisi media pertumbuhan bakteri yaitu pepton dan yeast extract yang berfungsi sebagai sumber asam amino, nukleotida, vitamin dan juga sumber karbon. Mineral yang harus ada dalam media pertumbuhan yaitu NaCl yang berfungsi sebagai sumber natrium, MgSO4.7H2O sebagai kofaktor enzim, CaCl2 26 27 sebagai sumber kalsium, agar sebagai agen pemadat, penambahan koloidal kitin dalam media berfungsi sebagai substrat untuk enzim kitinase. Hasil isolasi dan seleksi bakteri pada media kitin diketahui adanya bakteri yang tumbuh dengan tingkat pertumbuhan bakteri yang ditunjukkan dengan indeks kitinolitik yang berbeda-beda jumlahnya (Tabel 3). Hal ini disebabkan karena perbedaan tingkat adaptasi bakteri dengan medium atau lingkungan hidupnya. Pada media padat selektif diketahui bahwa bakteri berpotensi sebagai penghasil kitinase dengan terbentuknya zona bening di sekitar koloni. Semakin banyak enzim yang dihasilkan maka zona bening juga akan semakin luas karena kitin yang terdegradasi semakin banyak (Margareta, 2003). Tabel 3. Indeks Kitinolitik Bakteri Variasi Indeks Kitinolitik A1 5,19 A2 4,39 A3 7,59 Hasil seleksi terhadap kemampuan bakteri pada media yang mengandung substrat koloidal kitin diperoleh bakteri yang memiliki kemampuan mendegradasi kitin dengan baik. Koloidal kitin merupakan penginduksi yang efektif karena koloidal kitin adalah modifikasi kitin yang bersifat amorf dengan kerapatan polimer yang rendah sehingga lebih mudah dihidrolisis oleh enzim. Bakteri yang memiliki aktivitas kitinase ditunjukkan dengan adanya zona bening di sekitar koloni. Isolat bakteri yang dihasilkan dari limbah cair rumen sapi menunjukkan zona bening. Zona bening terbentuk akibat enzim kitinase yang dibebaskan keluar sel bakteri untuk memecah makromolekul kitin menjadi 28 molekul kitin yang lebih kecil, sehingga bakteri dapat mengambil nutrisi dalam bentuk molekul-molekul kecil. Hasil penelitian menunjukkan isolat A3 mempunyai indeks kitinolitik yang besar. Indeks kitinolitik menunjukkan kemampuan degradasi mikroba terhadap kitin. Semakin banyak enzim yang dihasilkan maka zona bening juga akan semakin luas karena kitin yang terdegradasi semakin banyak. Bakteri yang dihasilkan yang memiliki indeks kitinolitik terbesar yang selanjutya dikarakterisasi dan diidentifikasi. C. Karakterisasi dan Identifikasi Isolat Identifikasi isolat bakteri dilakukan untuk mengetahui ciri morfologis dan karakteristik biokimia. Secara morfologis, biakan maupun sel bakteri yang berbeda dapat tampak serupa oleh karena itu ciri fisiologi dan biokimia merupakan kriteria yang penting di dalam identifikasi spesimen yang tidak dikenal. Uji fisiologi biasanya identik dengan uji biokimia. Uji-uji biokimia yang biasanya dipakai dalam kegiatan identifikasi bakteri atau mikroorganisme antara lain uji katalase, uji methyl red, uji hidrogen sulfida, uji sitrat, dan uji fermentasi karbohidrat (Dwidjoseputro,1994). Identifikasi isolat bakteri kitinolitik asal limbah cairan rumen sapi dilakukan untuk mengetahui genus bakteri ini. Teknik pewarnaan Gram bertujuan untuk membedakan permeabilitas dinding sel suatu bakteri. Kandungan peptidoglikan dalam dinding sel bakteri merupakan salah satu indikator dalam pewarnaan Gram. Bakteri Gram positif memiliki kandungan peptidoglikan yang 29 lebih tinggi dibandingkan bakteri Gram negatif. Pewarnaan bakteri Gram positif akan menunjukkan warna biru, sedangkan pada Gram negatif menunjukkan warna merah muda saat bakteri ditambahkan reagen pewarna (safranin, iodium dan kristal ungu) (Beishir, 1991). Identifikasi sifat isolat bakteri kitinolitik secara kualitatif dilakukan dengan memfermentasi bakteri pada berbagai sumber nutrisi sebagai uji biokimia. Tabel. 4 menunjukkan hasil uji biokimia terhadap bakteri kitinolitik yang dihasilkan. Tabel 4. Uji Biokimia pada Bakteri Kitinolitik No. Jenis Uji Hasil Uji 1. Fermentasi Karbohidrat Positif Glukosa Positif Maltosa Positif Sukrosa Positif Manitol Positif Laktosa 2. Uji Metil merah Positif 3. Uji sitrat Positif 4. Uji katalase Negatif 5. Uji hidrogen sulfida Negatif Uji fermentasi pada beberapa jenis karbohidrat (Glukosa, Maltosa, Sukrosa, Manitol, Laktosa), menunjukkan semua hasil fermentasi berupa asam. Hal ini ditandai dengan hasil uji yang positif yaitu warna media karbohidrat yang semula kuning berubah menjadi merah. Indikator yang digunakan untuk mendeteksi penurunan pH pada media adalah larutan methyl red. Hasil ini sejalan dengan hasil uji metil merah yang menunjukkan adanya perubahan pH menjadi asam, yaitu warna hasil fermentasi menjadi merah (Lay, 1994). Pada penelitian ini hasil uji fermentasi pada beberapa jenis karbohidrat menunjukkan hasil positif dengan berubahnya warna media yang semula kuning menjadi merah. 30 Uji sitrat dilakukan untuk mengetahui kemampuan isolat bakteri kitinolitik menggunakan sitrat sebagai satu-satunya sumber karbon dan energi. Pada pengujian ini digunakan media agar yang mengandung Na sitrat (sumber karbon), NH4+ (sumber N) dan brom thymol blue (indikator pH). Bila mikroorganisme mampu menggunakan sitrat, maka terjadi peningkatan pH dan mengubah warna media menjadi biru (Lay, 1994). Bakteri kitinolitik yang diisolasi dari rumen sapi memiliki kemampuan dalam menggunakan sitrat sebagai satu-satunya sumber karbon, hal ini menunjukkan bahwa bakteri kitinolitik yang diperoleh positif uji sitrat. H2S diproduksi oleh beberapa jenis mikroorganisme melalui pemecahan asam amino yang mengandung unsur belerang (S). Adanya H2S dapat diamati dengan menambahkan garam logam berat ke dalam media. Hasil positif apabila H2S menghidrolisis logam berat yang ditandai dengan terbentuknya logam sulfit yang berwarna hitam. Hasil negatif apabila mikroorganisme tidak memiliki kemampuan untuk menghidrolisis logam berat yang terkandung dalam media. Hasil yang diperoleh menunjukkan uji H2S bakteri kitinolitik ialah negatif. Pada penelitian ini, bakteri kitinolitik yang dihasilkan menunjukkan hasil yang negatif. Katalase merupakan salah satu enzim yang digunakan oleh mikroorganisme untuk menguraikan hidrogen peroksida. Pada uji katalase yang dilakukan tidak terbentuk gelembung gas disekitar koloni ketika ditambahkan H2O2. Penentuan adanya katalase diuji dengan larutan H2O2 3%, dimana terbentuk gelembung udara yang merupakan gas O2 di sekitar koloni jika uji yang dilakukan 31 memberikan hasil positif (Lay, 1994). Penelitian ini menunjukkan bahwa bakteri kitinolitik yang dihasilkan negatif uji katalase. H2O2 H2O Katalase + ½ O2 Gelembung udara Berdasarkan Bergey’s Manual of Determinative Bacteriology, karakteristik morfologi dan hasil uji biokimia isolat bakteri kitinolitik menunjukkan ciri-ciri dari genus Lactobacillus murinus yang merupakan kelompok bacteria. Genus Lactobacillus murinus umumnya memiliki bentuk sel batang (basil) dalam bentuk tunggal maupun berpasangan, hal ini sesuai dengan morfologi koloni bakteri yang diperlihatkan pada Gambar 7. Taksonomi genus Lactobacillus murinus berdasarkan Bergey’s Manual Trust (2002) yaitu : Gambar 7. Morfologi Bakteri Kitinolitik (Perbesaran 100 x 10) Kingdom Domain Filum Kelas Order Family Genus : Bacteria : Firmicutes : Bacilli : Lactobacillales : Lactobacillaceae : Lactobacillus : Lactobacillus murinus 32 Berdasarkan hasil identifikasi makroskopis menunjukkan bahwa bakteri kitinolitik berbentuk bulat, berwarna putih, tepi koloni utuh dengan permukaan koloni halus sedangkan hasil identifikasi secara mikroskopis dengan pewarnaan Gram menunjukkan bahwa bakteri kitinolitik merupakan bakteri Gram negatif berbentuk bacilli (batang). D. Optimasi Kondisi Produksi 1. Penentuan Substrat Optimum untuk Produksi Enzim Kitinase Substrat koloidal kitin merupakan penginduksi aktivitas kitinolitik yang paling efektif karena koloidal kitin merupakan turunan kitin yang bersifat amorf dengan kerapatan polimer lebih rendah sehingga lebih mudah dihidrolisis enzim (Fawzya, dkk. 2004) dan lebih mudah tersebar merata dalam medium cair (Muzzarelli, 1977). Konsentrasi substrat adalah faktor penentu untuk produksi enzim. Pada penelitian ini telah dilakukan variasi konsentrasi substrat 0,02-0,14% (b/v) untuk mengetahui konsentrasi yang tepat untuk produksi enzim kitinase. Aktivitas kitinase meningkat pada media yang mengandung substrat dengan konsentrasi 0,02% (b/v) sampai 0,08% (b/v) (Gambar 8). Aktivitas tertinggi tercapai oleh adanya substrat kitin 0,08% (b/v) pada media, dengan aktivitas enzim sebesar 0,277 U/mL. Pada konsentrasi substrat diatas 0,08% (b/v) menyebabkan produksi enzim semakin menurun. Hal ini dikarenakan dalam suatu reaksi enzimatik, enzim akan mengikat substrat membentuk kompleks enzimsubstrat, kemudian kompleks ini akan terurai menjadi enzim dan produk. Makin banyak kompleks enzim substrat yang terbentuk, makin cepat reaksi berlangsung sampai batas kejenuhan. Pada konsentrasi substrat melampaui batas kejenuhan 33 kecepatan reaksi akan konstan. Berdasarkan hasil tersebut maka kondisi produksi enzim kitinase akan optimum dengan penambahan substrat koloidal kitin 0,08%. Gambar 8. Pengaruh Konsentrasi Substrat terhadap Produksi Enzim Kitinase Konsentrasi substrat optimum dalam produksi enzim kitinase juga berbeda untuk setiap jenis bakteri yang berbeda, seperti yang dilakukan oleh Wulandari dan Herdyastuti (2013) yang menyatakan bahwa isolat kitinolitik LA 21 asal tambak udang Lamongan memiliki aktivitas enzim maksimal 0,06%, sedangkan Brzezinska dan Donderski pada tahun 2001 yang menunjukkan aktivitas kitinase Aeromonas hydrophila tertinggi pada konsentrasi koloidal kitin 2%. 2. Penentuan Suhu Optimum untuk Produksi Enzim Kitinase Suhu juga berpengaruh terhadap pertumbuhan mikroorganisme, sintesis enzim dan kecepatan inaktivasi enzim. Suhu yang terlalu tinggi dapat mengakibatkan proses denaturasi protein sehingga dapat mengakibatkan kematian sel. Pada suhu yang terlalu rendah berakibat aktivitas enzim berkurang dan selanjutnya akan mengganggu pertumbuhan mikroorganisme. 34 Uji pengaruh temperatur terhadap aktivitas enzim dilakukan untuk mengetahui kondisi optimum enzim dalam mendegradasi substrat. Setiap enzim memiliki aktivitas maksimum pada temperatur tertentu, aktivitas enzim akan semakin meningkat dengan bertambahnya temperatur hingga temperatur optimum tercapai. Kenaikan temperatur di atas temperatur optimum akan menyebabkan aktivitas enzim menurun (Baehaki, 2011). Penentuan suhu optimum untuk produksi enzim kitinase dilakukan dengan variasi suhu 30ºC, 40ºC, 50ºC dan 60ºC. Dari hasil penelitian, diperoleh bahwa suhu optimum untuk produksi enzim kitinase ialah pada suhu 40ºC dengan aktivitas enzim sebesar 0,886 U/mL (Gambar. 9). Penelitian untuk jenis bakteri kitinolitik menunjukkan kondisi optimum yang sama dalam produksi enzim kitinolitik seperti yang dilaporkan oleh Donderski dan Trzebiatowska (2000) bahwa Anthrobacter sp. menunjukkan bahwa aktivitas kitinolitik tertinggi pada suhu 40ºC. Di samping itu, bakteri kitinolitik jenis Streptomyces sp. PTK19 yang dikaji oleh Pratiwi, dkk. 2015 suhu optimum enzim kitinase sebesar 40°C dan stabil pada kisaran suhu 30-45°C. Gambar 9. Pengaruh Variasi Suhu terhadap Produksi Enzim Kitinase 35 3. Penentuan pH Optimum untuk Produksi Enzim Kitinase Organisme memiliki rentang pH kultivasi yang cukup sempit untuk pertumbuhannya. Penentuan pH kultivasi merupakan faktor yang penting untuk pertumbuhan mikroorganisme dan pembentukan produk metabolitnya. Llyod dan Nelson (1984) menyatakan bahwa aktivitas optimum enzim berkisar pada pH pertumbuhan mikroorganisme penghasil enzim tersebut, sehingga pH optimum aktivitas enzim ini berbeda-beda tergantung mikroorganisme penghasil enzimnya. Enzim memiliki pH optimum yang khas, yaitu pH yang menyebabkan aktivitas maksimum (Lehninger, 1995). Semua reaksi enzim dipengaruhi oleh pH medium tempat reaksi terjadi (Suhartono, 1989), dan pada umumnya enzim aktif pada pH netral atau dengan kisaran pH 5–9 (Rahayu, 2000). Penentuan pH optimum untuk produksi enzim kitinase dilakukan pada rentang pH 3, 4, 5, 6 dan 7. pH optimum untuk produksi enzim kitinase ialah pH 6 dengan aktivitas enzim sebesar 0,194 U/mL. Hal ini sejalan dengan penelitian yang dilakukan oleh Herdyastuti, dkk. pada tahun 2009 yang berhasil mengisolasi genus Trichoderma yang mempunyai stabilitas pH pada kisaran 3,5 - 6,0. Nilai pH optimum 6 juga ditemukan pada kitinase Trichoderma harzianum (Katatny et al., 2000). Namun, berbeda dengan penelitian yang dilakukan oleh Bhattacharya S, dkk. (2012) yang melaporkan pH optimum untuk pertumbuhan Serratia marcescens penghasil enzim kitinase adalah pH 7. 36 Gambar 10. Pengaruh Variasi pH terhadap Produksi Enzim Kitinase E. Produksi Enzim Kitinase Optimasi waktu produksi dilakukan untuk mengetahui waktu panen yang tepat selama proses produksi enzim kitinase, dimana bakteri kitinolitik menghasilkan kitinase dengan aktivitas tertinggi. Untuk menentukan waktu optimum, maka dilakukan produksi enzim pada 0 jam sampai 24 jam dengan selang waktu 2 jam dilakukan sampling untuk penentuan aktivitas kitinase yang dihasilkan. Aktivitas kitinase yang diperoleh dari supernatan kultur meningkat pada jam ke 0 sampai 6 jam, aktivitas enzim tertinggi berada pada 6 jam yang dinyatakan dengan nilai aktivitas enzim sebesar 125,943 U/mL dan kemudian menurun pada 20 jam sampai 24 jam. Peningkatan aktivitas enzim menunjukkan bahwa semakin banyak substrat yang terhidrolisis. Aktivitas enzim kitinase terus meningkat dari 0 jam inkubasi hingga mencapai waktu inkubasi optimum, hal ini dapat terjadi karena pada 0 jam masih sedikit enzim yang bereaksi dengan substrat dan akan meningkat seiring dengan peningkatan waktu inkubasi hingga mencapai waktu inkubasi optimum. 37 Setelah mencapai waktu optimum, aktivitas enzim menurun dikarenakan telah terjadi akumulasi produk hidrolisis yang selanjutnya dapat menghambat aktivitas enzim (Gambar. 11). Gambar 11. Kurva Produksi Enzim Kitinase Aktivitas enzim kitinase yang ditunjukkan oleh bakteri merupakan parameter yang digunakan dalam seleksi bakteri kitinolitik (Park, dkk. 2000). Seleksi sebenarnya membantu untuk mengetahui apakah suatu mikroorganisme menghasilkan senyawa kimia tertentu seperti enzim, antibiotik atau metabolit sekunder lainnya (Huang, dkk. 1999). Aktivitas enzim yang dihasilkan oleh mikroorganisme dapat diketahui dengan seleksi pada media selektif. Media selektif merupakan media dengan komposisi tertentu, sehingga hanya jenis-jenis tertentu saja yang dapat hidup (Gandjar, 1992). Enzim kitinase yang diproduksi dapat diketahui dengan melihat aktivitas enzim kitinolitik. Aktivitas enzim merupakan ukuran perubahan molekul substrat yang menjadi produk dalam satuan waktu pada kondisi tertentu (Green, dkk. 2005). Penentuan aktivitas enzim kitinolitik dapat dilakukan dengan metode Schales menggunakan spektrofotometer UV-Vis. V. PENUTUP A. Kesimpulan Berdasarkan hasil penelitian yang telah dilakukan, maka disimpulkan: 1. Bakteri kitinolitik asal limbah cairan rumen sapi memiliki kemampuan yang baik dalam mendegradasi kitin. Hal ini dibuktikan dengan adanya zona bening dengan indeks kitinolitik sebesar 7,59. 2. Karakteristik bakteri kitinolitik asal limbah cairan rumen sapi menunjukkan isolat bakteri kitinolitik merupakan bakteri Gram negatif berbentuk batang dari spesies bakteri Lactobacillus ruminus. 3. Kondisi optimum produksi enzim kitinase ialah pada konsentrasi substrat 0,08% (b/v) dengan suhu 40ºC pada pH 6 dengan aktivitas enzim sebesar 125,943 U/mL B. Saran Penelitian lebih lanjut perlu dilakukan untuk: 1. Perlu dilakukan pemurnian enzim kitinolitik asal limbah cairan rumen sapi. 2. Perlu dilakukan karakterisasi enzim kitinase. 38 DAFTAR PUSTAKA Apriani, L. 2008. Seleksi Bakteri Penghasil Enzim Kitinolitik Serta Pengujian Beberapa Variasi Suhu dan pH untuk Produksi Enzim. Fakultas Mamatematika dan Ilmu Pengatahuan Alam. Departemen Biologi. Universitas Indonesia: Depok. Arora, S. P. 1989. Pencernaan Mikrobia pada Ruminansia. Gadjah Mada University Press: Yogyakarta. Baehaki, A., Rinto dan B. Arif. 2011. Isolasi dan Karekterisasi Protease dari Bakteri Tanah Rawa Indralaya, Sumatera Selatan. J. Teknologi dan Industri Pangan, Vol. XXII No. 1. Bhattacharya S, Chakrabortty S, and Das A. 2012. Optimization of Process Parameters for Chitinase Production by a Marine Isolate of Serratia marcescens. J. Pharm. Biol. Sci. 2:2, 8-20. Budiansyah, A., Resmi, Nahrowi, Wiryawan, K. G, Suhartono, M. T dan Widyastuti, Y. 2011. Karakteristik Endapan Cairan Rumen Sapi asal Rumah Potong Hewan sebagai Feed Supplement. Jurnal Ilmiah IlmuIlmu Peternakan,Vol. XIV. No.1. Brzezinska, M.S. and Donderski, W. 2001. Occurence of Chitinolytic Bacteria in Water and Bottom Sediment of Eutrophic Lakes in Hawski Lake District. Polish Journal of Environmental Studies Vol. 10 No.5. Cahyani, L. 2013. Pemanfaatan Tepung Cangkang Udang Sebagai Media Produksi Kitinase oleh Bakteri Kitinolitik Isolat 26. Jurusan Biologi FMIPA. Universitas Jember. Cappucino, J.G., and Sherman, N. 1983. Microbiology: A laboratory Manual. Addison-Wesley Publishing Company, Inc. Menlo Park, California. Chemin, L., Z. Ismailov, S. Haran and I. Chet. 1995. Chitinolytic Enterobacter Agglomerans Antagonistic to Fungal Plant Pathogens. Appl. Environ Microbiol. Vol. 61 No. 5. Commons.wikimedia.org, 2013. Pengertian Rumen dan Fungsinya. Darmayasa, I. B. G. 2008. Isolasi dan Identifikasi Bakteri Pendegradasi Lipid (Lipid) pada Beberapa Tempat Pembuangan Limbah dan Estuari DAM Denpasar. Jurnal Bumi Lestari. Vol. 8 No. 2. 39 40 Dehority, B.A and C.G Orphin.1997. Development of Natural Fluctuation in Rumen Microbial Population. In: The Rumen Microbial Ecosystem. PN. Hobson, P. N and C. S Stewart (Editors). Blackie Academic & Professional. London. Donderski, W. and M. Trzebiatowska. 2000. Influence of Physical and Chemical Factors on The Activity of Chitinases Produced by Planktonic Bacteria Isolated from Jeziorak Lake. Polish Journal of Environmental Studies. Vol. 9 No.2. Dwidjoseputro. 1994. Dasar-Dasar Mikrobiologi. Jakarta: Djambaran. Erni Mawar Indah S, Nies Suci Mulyani dan Purbowatiningrum Ria S., 2002. Pengaruh Variasi Temperatur Terhadap Aktivitas Xilanase Hasil isolasi dari Aspergillus niger pada media pertumbuhan CBD (Chapek’s Dox Broth) Hasil Modifikasi dengan sekam Padi. Jurusan Kimia: Universitas Diponegoro Semarang. Fahmi, R. 1997. Isolasi dan Transformasi Kitin menjadi Kitosan. Jurnal Kimia Andalas. Vol. 3. No.1. Fawzya, Y.N., N. Indriati dan T.D. Suryaningrum. 2004. Pengaruh Penambahan Kitin pada Medium Produksi Terhadap Kitin Deasetilase dari Bacillus K29-14. Jurnal Penelitian Perikanan Indonesia. Vol. 10 No.3 Gandjar, I., I.R. Koentjoro., W. Mangunwardoyo. & L. Soebagya. 1992. Pedoman Praktikum Mikrobiologi Dasar. Jurusan Biologi FMIPA-UI, Depok. Green, A.T., M.G. Healy and A. Healy. 2005. Production of Chitinolytic by Serratia Marcescens Qmb1466 using Various Chitinous Substrates. Journal of Chemical Technology and Biotechnology. Vol. 80. Haliza, Winda dan Suhartono, M., T. 2012. Karakteristik Kitinase dari Mikrobia. Buletin Teknologi Pascapanen Pertanian. Vol. 8 No. 1. Herdyastuti, N., Raharjo, T. J., Mudasir dan Matsjeh, S. 2009. Kitinase dan Mikroorganisme Kitinolitik:Isolasi, Karakterisasi dan Manfaatnya. Indo.J. Chem. Vol. 9 No. 1. Hobson, P. N and C. S Stewart.1992. The Rumen Microbial Ecosystem. Blackie Academic & Professional. New York. Hsu, SC and Lockwood. 1975. Powdered Chitin Agar As a Selective Enumerationof Actinomycetes in Water and Soil. Applied Microbiology. Vol. 29 No. 1. 41 Huang, L., S.S. Miles and R.B. Lingham. 1999. Screening for activities. Dalam: Demain, A.L. & J.E. Davies. 1999. Manual of industrial microbiology, Washington. Imoto, I. And K. Yagashita. 1971. A Simple Activity Measurement of Lisoenzyme. Agric. Biol. Chem. 35: 1154-1156. Judoamidjojo. M., E. G. Said., L. Hartono. 1989. Biokonversi Biotek. PAU. IPB. Bogor. Katatny, M. H. E., Somitsch, W. Robra, K. H. Katatny, M. S. E., and Gubitz, G. M. 2000. Production of Chitinase and 1,3-glucanase by Trichoderma harzianum for Control of the Phytopathogenic Fungus Sclerotium rolfsii. J. Food. Technol. Biotechnol. Vol. 38. No.3. Koga, D., M. Mitsutomi, M., M. Kono and M. Matsumiya. 1999. Biochemistry of Chitinases. Dalam: Jolles, P. dan R.A.A Muzzarelli. 1999. Chitin and Chitinases. Birkhauser Verlag, Basel. Lay, B.W. 1994. Analisis Mikroba dilaboratorium. PT. Raja Grafindo Persada. Jakarta. Lehninger, A.L. 1995. Dasar-dasar Biokimia. Jilid 1. Erlangga, Jakarta. Lestari, R., E.I.N. Aidil dan N. Anita. 2002. Biologi. Terjemahan dari Biology. Edisi Kelima oleh Campbell, N.A., J.B. Reece dan L.G. Mitchell.. Penerbit Erlangga. Liaw, H. J. and R. A. Mah. 1992. Isolation and Characterization of Haloanaerobacter Chitinovorans Gen. Appl. Environ Microbiol. Vol. 58 No. 1. Lloyd, N.E. and W.J. Nelson. 1984. Glucose and Fructose Containing Sweeteners from Starch. In Whesler et al. (Eds.). Starch. Chemistry and Technology. Academic Press. p. 611-659. Margareta, M., 2003. Penapisan dan karakterisasi Sejumlah Isolat Bakteri Termofilik Amilolitik. Skripsi. Fakultas Matematika dan Ilmu Pengetahuan Alam. Institut Pertanian Bogor. Bogor. McDonald, P., R. A. Edwards, J. F. D. Greenhalgh and C. A. Morgan. 2002. Animal Nutrition. Prentice Hall. London. Microbiology 101 Laboratory Manual. www.slic2.wsu.edu. Diakses pada 25 Maret 2015. 42 Muharni, 2010.Isolasi dan Identifikasi Bakteri Penghasil Kitinase dari Sumber Air Panas Danau Ranau Sumatera Selatan. Jurnal Penelitian Sains. 10:0609. Mulyono, HAM. 2006. Membuat Reagen Kimia di Laboratorium. PT. Bumi Aksara: Jakarta. Muzarelli RAA. 1977. Chitin. Pergamon Press: New York. Nasran, S., F. Ariyani dan N. Indriati. 2003. Produksi Kitinase dan Kitin Deasetilase dari Vibrio harveyl. Jurnal Penelitian Perikanan Indonesia. Vol. 9 No. 5. Nuswantara, Limbang Kustiawan. 2002. Ilmu Makanan Ternak Ruminansia (Sapi Perah). Jurusan Nutrisi dan Makanan Ternak. Fakultas Peternakan Unversitas Diponegoro: Semarang Padmono, Djoko. 2005. Alternatif Pengolahan Limbah Rumah Potong Hewan Cakung (Suatu Studi Kasus). Jurnal Teknologi Lingkungan P3TL.BPPT. Vol. 6 No. 1. Park, S.H., J. Lee and H.K. Lee. 2000. Purification and Characterization from a Marine Bacterium, Vibrio sp. 98CJ11027. The Journal of Microbiology. Vol. 38 No. 4. Pelczar, M.J. dan Chan E.C.S. 1988. Dasar-Dasar Mikrobiologi. Jilid 2. Jakarta. Pujianto, S., Kusdiyantini, E., dan Hadi, M. 2008. Isolasi dan Seleksi Bakteri Isolat Lokal yang Berpotensi untuk Mengendalikan Larva Nyamuk Aedes Aegypti L. Biodiversitas. Vol. 9 No. 1. Pujiastuti, P. 2001. Kajian Transformasi Khitin Menjadi Khitosan Secara Kimiawi dan Enzimatik, Seminar Nasional Jurusan Kimia, Jurusan Kimia F MIPA: UNS. Rahayu, S. 2000. Pemurnian dan Karakterisasi Kitinase dan Kitin Deasetilase Termostabil dari Isolat Bacillus K-29-14 Asal Kawah Lamojang, Jawa Barat. Thesis Program Pascasarjana, IPB. Rahayu, Sri, Suhartati F., M. Rimbawanto E.,A. Dan Iriyanti, N. 2003. Isolasi dan Identifikasi Bakteri Kitinolitik asal Rumen. Animal Production Journal. Vol. 5 No. 2. Richana,N., P Lestari, A. Thontowi dan Rosmimik., 2000. Seleksi Isolat Bakteri Lokal Penghasil Xilanase. Jurnal Mikrobiologi Indonesia. Vol. 5 No.2. 43 Sakai, K., A. Yokota, H. Kurokawa, M. Wakayama dan M. Moriguchi. 1998. Purification and Characterization of Three Thermostable Endochitinases of A Noble Bacillus Strain MH-1, Isolated from ChitinContaining Compost. Appl. Environ Microbiol. Vol. 64 No. 9. Saules. Meija, J.E., K.N. Waliszewski, M.A. Garcia and R. Cruz-camarillo. 2006. The Use of Crude Shrimp Shell for Chitinase Production by Serratia marcescens. WF. Food Technol. Biotechnol. Vol. 44 No. 1. Suhartono, M.T. 1989. Enzim dan Bioteknologi. Depdikbud. Ditjen Dikti–PAU. IPB, Bogor. p. 53–102. Suhermiyati, S. 1984. Pengujian Cobaan Bahan Limbah RPH dan Ragi Makanan Ternak serta Kombinasinya dalam Ransum Ayam Pedaging. Thesis Fakultas Peternakan IPB, Bogor. Sutardi, T., 1977. Ikhtisari Ruminologi. Bahan Kursus Peternakan Sapi Perah Kayu Ambon, Lembang. Direktorat jendral Peternakan. Jakarta. Vogan, C.L., C. Costa-Ramos and A.F Rowley. 2002. Shell Disease Syndrom in The Edible Crab, Cancer Pangurus-Isolation, Characterization and Pathogenicity of Chitinolytic Bacteria. Microbiology. Wahyu, J., 1985. Ilmu Nutrisi Ternak. Gadjah Mada University Press. Yogyakarta. Windholz. 1983. Chitin and Chitosan. N.Y University : New Castle. Wulandari, H. A. dan Herdyastuti, N. 2013. Optimasi Pertumbuhan Isolat Kitinolitik La 21 yang Diisolasi dari Tambak Udang di Lamongan. UNESA Journal of Chemistry. Vol. 2, No. 2. Yuneta. R dan Putra R.S. 2010. Pengaruh Suhu pada Lipase dari Bakteri Bacillus subtilis. Prosiding Kimia. MIPA. Institut Teknologi Sepuluh November. Surabaya. Zikakis, JP. 1984. Chitin, Chitosan, and Related Enzymes. Introduction. Academic Press: San Diego. LAMPIRAN Lampiran 1. Peta Lokasi Pengambilan Sampel Cairan Rumen Sapi Keterangan : Tanda Merah : TPH Anggoeya, Tempat Pengambilan Sampel Cairan Rumen sapi 44 45 Lampiran 2. Gambaran Umum Alur Penelitian Sampel cairan rumen sapi dari Tempat Pemotongan Hewan (TPH) Kendari Sulawesi Tenggara Isolasi dan Seleksi bakteri Kitinolitik Identifikasi Isolat Terpilih Karakterisasi Isolat Karakteristik mikroskopi Karakteristik sifat biokimia Uji bakteri Gram +/ Bentuk sel Uji katalase Uji fermentasi karbohidrat Uji sitrat Uji Methyl Red Uji H2S Optimasi Produksi Enzim Substrat Optimum Suhu Optimum pH Optimum Kurva Pertumbuhan Aktivitas Enzim Analisis Data 46 Lampiran 3. Diagram Alir Pengambilan Sampel, Isolasi dan Seleksi Bakteri Kitinolitik, Uji Mikroskopi dan Biokimia 1. Pengambilan Sampel Sampel dari TPH - disegarkan dalam media cair LB (Luria Bertani) - diinkubasi selama 48 jam pada suhu 37ºC starter 2. Isolasi dan Seleksi bakteri dari sampel cairan rumen sapi Kultur bakteri dalam media cair LB - diambil 0,2 mL - disebar pada cawan petri berisi media agar selektif kitinase - diinkubasi selama 48 jam Kultur bakteri kitinolitik - diuji pada media koloidal kitin 1% - diinkubasi selama 48 jam pada suhu optimum - diamati zona bening yang terbentuk Bakteri kitinolitik 47 3. Analisis Isolat Bakteri Kitinolitik a. Karakteristik makroskopi (Metode Pengenceran) Isolat bakteri - diencerkan Isolat Bakteri pengenceran 10-1 sampai 10-6 - disebarkan pada media padat LB - diinkubasi pada suhu 37°C selama 48 jam - diamati bentuk, tekstur dan warna koloni Hasil b. Karakteristik Mikroskopi (Uji Pewarnaan Gram) Isolat Bakteri yang telah diremajakan - diambil sebanyak 1 osse - dioles diatas permukaan kaca objek - diteteskan larutan ungu Kristal pada bagian olesan bakteri dan didiamkan selama 1 menit - dicuci dengan air dan dibiarkan sampai kering - diteteskan larutan iodium dan didiamkan selama 2 menit - dicuci dengan air dan dibiarkan sampai kering - diteteskan alkohol dan didiamkan selama 30 detik - diteteskan larutan safranin dan didiamkan selama 30 detik - dicuci dengan air dan dibiarkan sampai kering - diamati di bawah mikroskop Penampakan 48 c. Uji biokimia Isolat Terpilih Uji Biokimia Uji karbohidrat Uji katalase Uji H2S Bergey’s Mannual of Determinative Uji Sitrat Uji Methyl Red 49 Lampiran 4. Pembuatan Koloidal Kitin Bubuk Kitin - dimasukkan ke dalam gelas kimia 1000 mL sebanyak 5 gram - ditambahkan 75 mL HCl pekat - diaduk selama 1 jam - ditambahkan akuades sebanyak 500 mL - disaring Residu - dicuci dengan akuades sampai pH 3 Endapan: Koloidal kitin Filtrat 50 Lampiran 5. Pembuatan Media 1. Media Luria Bertani (LB) Cair 30 ml akuades - dimasukan dalam erlenmeyer - ditambahkan pepton 0,15 gr - ditambahkan yeast extract 0,075 gr - ditambahkan NaCl 0,15 gr - ditambahkan MgSO4.7H2O 0,09 gr - ditambahkan CaCl2, 0,003 gr - disterilisasi dalam autoklaf pada suhu 121°C selama 15 menit. Medium LB Hasil Sterilisasi - didinginkan - dimasukkan isolat sebanyak 200 µL - diinkubasi selama 48 jam Medium LB 2. Media Kitin Modifikasi Koloidal Kitin 2% - dimasukkan kedalam erlenmeyer - dimasukkan akuades sebanyak 100 mL - ditambahkan KH2PO4 0,1 g - ditambahkan MgSO4.7H2O 0,01 g - ditambahkan NaCl 3 g - ditambahkan (NH4)2SO4 0,7 g - ditambahkan yeast extract 0,05 g - ditambahkan agar 2 g - dipanaskan sambil di homogenkan dengan magnetic stirer hingga larut - disterilkan dengan autoklaf pada suhu 121°C selama 15 menit - dituang kedalam cawan petri - dibiarkan memadat Medium Kitin 51 Lampiran 6. Optimasi Kondisi Produksi Enzim Kitinase a. Penentuan Konsentrasi Substrat Optimum 0,5 mL Isolat Bakteri - ditumbuhkan pada media LB cair modifikasi dengan konsentrasi (0,02-0,14 %) - diinkubasi selama 48 jam pada suhu 30ºC - dilihat absorbansnya pada spektrofotometer UV-Vis dengan panjang gelombang 584 nm menggunakan larutan standar N-asetil glukosamin Substrat Optimum Enzim b. Penentuan Suhu Optimum 0,5 mL Isolat Bakteri - ditumbuhkan pada media cair LB yang mengandung substrat optimum - di variasikan suhu pertumbuhannya yaitu 30ºC, 40ºC, 50ºC dan 60ºC selama 24 jam - diukur aktivitasnya dengan spektrofotometer pada λ 584 nm menggunakan larutan standar N-asetil glukosamin Suhu Optimum Enzim c. Penentuan pH Optimum 0,5 mL isolat bakteri - ditumbuhkan pada media cair LB yang mengandung substrat optimum dengan variasi pH 3, 4, 5, 6 dan 7 - diinkubasi pada suhu optimum yang didapatkan dari hasil optimasi produksi enzim selama 24 jam - diukur aktivitasnya menggunakan spektrofotometer pada λ 584 nm dengan larutan standar N-asetil glukosamin pH Optimum Enzim 52 Lampiran 7. Pengukuran Aktivitas Enzim 200 µL ekstrak kasar enzim - dimasukkan kedalam tabung reaksi - ditambahkan 200 µL substrat kitin 0,3 % - di tambahkan 200 µL buffer pH 7 - diinkubasi selama 30 menit dengan suhu optimum - disentrifugasi dengan kecepatan 9000 rpm selama 4 menit - dipisahkan filtrat dengan residunya Residu Filtrat - diambil 500 µL - ditambahkan 500 µL akuades - ditambahkan 1 mL pereaksi Schales - dipanaskan selama 10 menit - diukur absorbansinya pada panjang gelombang 584 nm. N-asetilglukoamin sebagai standar. Aktivitas Enzim 53 Lampiran 8. Diagram pembuatan kitin dari kulit udang a. Deproteinasi Kulit udang - dibersihkan dan dikeringkan - ditimbang sebanyak 45 gram - dipanaskan hingga suhu diatas 100ºC dengan pelarut NaOH 3,5% dengan perbandingan 1:10 (b/v) selama 3 jam - dicuci beberapa kali dengan air mengalir sampai pH netral - dikeringkan pada suhu 50ºC selama 12 jam Kulit udang deproteinasi b. Demineralisasi Kulit udang deproteinasi - diambil sebanyak 25 gram - dimasukkan ke dalam gelas kimia 1000 mL - ditambahkan HCl sebanyak 375 mL dengan perbandingan 1:15 (b/v) - diaduk tanpa proses pemanasan selama 1 jam - disaring Filtrat Residu - dicuci dengan akuades hingga pH netral - dikeringkan pada suhu 60°C selama 24 jam Kulit udang demineralisasi c. Dekolorisasi Kulit udang demineralisasi - direndam dengan aseton teknis sebanyak 360 mL selama 7 jam - dicuci dengan air mengalir hingga pH netral - dikeringkan diudara terbuka Kitin 54 Lampiran 9. Pembuatan Larutan 1. Pembuatan Media LB (Luria Bertani)Cair 30 mL Bahan : Pepton Yeast Extract : 0,075 g NaCl MgSO4.7H2O : 0,09 g CaCl2 : 0,003 g Pelarut : akuades : 0,15 g : 0,15 g 2. Pembuatan Media LB Padat Modifikasi 120 mL Bahan : Koloidal Kitin : 2,4 g KH2PO4 : 1,2 g MgSO4.7H2O : 0,012 g NaCl : 3,6 g Yeast extract : 0,06 g Amonium Sulfat : 0,84 g Agar : 3,36 g Pelarut : akuades 3. Pembuatan Larutan Standar N-asetilglukosamin Bahan : N-asetilglukosamin : 10 mg Akuades : 10 ml 55 10 mg = 10.000 µg = 1000 µg/mL 10 mL 10 mL = 1000 ppm Untuk konsentrasi 2,5 µg/mL 5 µg/mL. V1 = 2,5 µg/mL . 10 mL V1 = 25/5 = 5 mL 4. Pembuatan buffer pH Larutan buffer KHP-HCl (Mulyono, 2006) Larutan A : Kalium Hidrogen Ptalat (KHP): Timbang 5,11 gram KHP dimasukkan ke dalam labu takar 250 mL ¼ labu, dan homogenkan; tambah lagi akuades sampai tanda batas. Larutan X (HCl 0,1 M) : Dipipet 0,82 mL HCl 0,1 M dimasukkan ke dalam labu takar 100 mL ¼ labu, dan homogenkan; tambah lagi akuades sampai tanda batas. A (50 mL) + Keterangan: pH x (mL) y (mL) 3,00 22,3 27,7 3,50 8,2 41,8 4,00 1,0 49,0 A = larutan KHP X = larutan HCl 0,1 M Y = akuades Larutan buffer KHP-NaOH (Mulyono, 2006) Larutan x (NaOH 0,1 M) Dipipet 7,51 mL NaOH 0,1 M dimasukkan ke dalam labu takar 100 mL ¼ labu, dan homogenkan; tambah lagi akuades sampai tanda batas. 56 A (50 mL) + Keterangan : pH x (mL) y (mL) 5,00 22,6 27,4 A = Larutan KHP X = Larutan NaOH 0,1 M Y = Akuades Larutan buffer KH2PO4-NaOH (Mulyono, 2006) Larutan A (KH2PO4) Ditimbang 1,361 gram KH2PO4 dimasukkan ke dalam labu takar 100 mL ¼ labu, dan homogenkan; tambah lagi akuades sampai tanda batas. A (50 mL) + pH x (mL) y (mL) 6,00 5,6 44,4 7,00 29,1 20,9 8,00 46,1 3,9 5. Pembuatan Larutan Schales (Imoto and Yagishita, 1971) Ditimbang 13,25 g Na2CO3 dimasukkan ke dalam dimasukkan labu takar 250 mL ¼ labu, dan homogenkan kemudian ditambahkan 0,125 g K3[Fe(CN)6]; tambah lagi akuades sampai tanda batas. 57 Lampiran 10. Hasil Penelitian 1. Hasil Uji Aktivitas Bakteri Kitinolitik dengan Metode Campur Variasi A1 A2 A3 Indeks Kitinolitik Zona Bening (cm) 2,6 2,2 3,8 Diameter Koloni (cm) 0,5 0,5 0,5 Indeks Kitinolitik = Diameter zona bening – Diameter Koloni Diameter Koloni = 280 – 0,5 0,5 = 759 = 7,59 2. Kurva Standar N-Asetilglukosamin Konsentrasi (µg/mL) 2,5 Absorbansi (A) 0,011 5 0,018 7,5 0,023 10 0,027 12,5 0,032 15 0,036 Diukur pada panjang gelombang 584 nm 5,19 4,39 7,59 58 3. Optimasi Substrat Enzim Kitinase Konsentrasi Substrat (%) 0,02 0,04 0,06 0,08 0,10 0,12 0,14 Diukur pada panjang gelombang 584 nm Absorbans (A) 0,282 0,273 0,253 0,359 0,316 0,210 0,249 Aktivitas Enzim (U/mL) 0,216 0,209 0,193 0,277 0,243 0,159 0,190 Contoh Perhitungan: (0,02 % (b/v) Y = 0,002 X + 0,007 0,282 = 0,002 X + 0,007 X = 0,275 0,002 X = 137,5 mg/mL A = [ N - Asetilglukosamin] BM.N – Asetilglukosamin x t = 137,5 mg/mL x 1000 µmol/mmol 221 mg/mmol x 2880 menit = 0,216 µmol/menit.mL = 0,216 U/mL 59 4. Optimasi Suhu Enzim Kitinase Suhu (ºC) Absorbans (A) 30 0,199 1,135 40 50 0,052 60 0,023 Diukur pada panjang gelombang 584 nm (40ºC) Y = 0,002 X + 0,007 1,135 = 0,002 X + 0,007 X = 1,128 0,002 X = 56 mg/mL A= [ N - Asetilglukosamin] BM.N – Asetilglukosamin x t = 564 mg/mL x 1000 µmol/mmol 221 mg/mmol x 2880 menit = 0,886 µmol/menit.mL = 0,886 U/mL. Aktivitas Enzim (U/mL) 0,151 0,886 0,035 0,013 60 5. Optimasi pH Enzim Kitinase pH 3 Absorbans (A) 0,041 Aktivitas Enzim (U/mL) 0,027 4 0,049 0,033 5 0,038 0,024 6 0,254 0,194 7 0,151 0,113 Diukur pada panjang gelombang 584 nm (pH 6) Y = 0,002 X + 0,007 0,254 = 0,002 X + 0,007 X = 0,247 0,002 = 123,5 A = [ N - Asetilglukosamin] BM.N – Asetilglukosamin x t X = 123,5 mg/mL = 123,5 mg/mL x 1000 µmol/mmol 221 mg/mmol x 2880 menit = 0,194 µmol/menit.mL = 0,194 U/mL. 61 6. Penentuan Produksi Enzim Kitinase Waktu Inkubasi (Jam) Absorbans (A) 2 0,769 4 1,235 6 1,677 8 1,701 10 1,738 12 1,693 14 1,761 16 1,813 18 1,726 20 1,906 22 1,743 24 1,653 Diukur pada panjang gelombang 584 n Contoh Perhitungan : (6 jam) Y = 0,002 X + 0,007 1,677 = 0,002 X + 0,007 X = 1,67 0,002 X = 835 mg/mL A = [ N - Asetilglukosamin] BM.N – Asetilglukosamin x t = 835 mg/mL x 1000 µmol/mmol 221 mg/mmol x 30 menit = 125,942 µmol/menit.mL = 125,942 U/mL. Aktivitas Enzim (U/mL) 57,466 92,609 125,943 127,753 130,543 127,149 132,278 136,199 129,638 143,213 130,920 124,133 62 Lampiran 11. Dokumentasi 1. Kegiatan Pengambilan Sampel Cairan Rumen Sapi di Tempat Pemotongan Hewan (TPH) Anggoeya, Sulawesi Tenggara 63 2. Kegiatan Skrining Bakteri Air Sungai Pohara Preparasi sampel rumen A2 A3 A1 Metode Pengenceran 64 3. Kegiatan Identifikasi Bakteri Uji methyl red Uji Katalase Uji fermentasi karbohidrat Uji sitrat Uji H2S 65 4. Kegiatan Pembuatan Koloidal Kitin Cangkang udang Ditambahkan akuades Dicampur larutan asam pekat Disaring