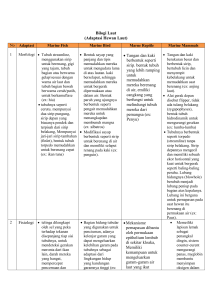
Berdasarkan Analisis RAPD (Random Amplified
advertisement

II. BAHAN DAN METODE 2.1 Materi Ikan Uji Ikan yang digunakan pada penelitian ini terdiri atas 3 populasi yang dikoleksi dari Sumatra (Jambi), Jawa Barat (Tasikmalaya) yang berasal dari lingkungan budidaya, dan Kalimantan Selatan yang berasal dari alam, masingmasing sebanyak 10 ekor. 2.2 Ekstraksi DNA Setiap sampel ikan diambil sirip ekor dan ditimbang sebanyak 5-10 mg dibilas 2 kali dengan menggunakan akuades, lalu dikeringkan dengan tissue dan dimasukan ke dalam tabung eppendorf 1,5 ml, kemudian dilisis dengan menambahkan urea sebanyak 500 µl dan protein kinase (K) 10 µl. Setelah itu dikocok menggunakan alat vortex dan diinkubasi pada suhu 37°C selama 24 jam atau sampai sirip hancur. Selanjutnya ditambahkan larutan phenol:chloroform: isoamilalkohol (PCL) dengan perbandingan 25:24:1 sebanyak 1000 µl dan disentrifuse dengan menggunakan kecepatan 10.000 rpm selama 10 menit. Supernatan lalu dipindahkan ke tabung baru dan ditambahkan etanol 90% sebanyak 1000 µl dan Na asetat sebanyak 10 µl lalu di sentrifugasi pada kecepatan 10.000 rpm selama 10 menit. Supernatan dibuang dan pellet dikering anginkan sampai etanol menguap. DNA dilarutkan dengan menambahkan rehydration solution sebanyak 100 µl. DNA yang belum akan digunakan dalam jangka waktu lama disimpan pada suhu 2-8°C. 2. 3 Amplifikasi DNA dengan teknik PCR Tiga jenis primer yang digunakan adalah OPA2, OPC2, OPC5 (Tabel 1) Tabel 1. Deskripsi sekuen primer RAPD pada amplifikasi DNA ikan sepat Primer OPA 2 OPC 2 OPC 5 Sekuen Nukleotida (5’Æ3’) TGCCGAGCTG GTGAGGCGTC GATGACCGCC 5 Amplifikasi DNA dilakukan menggunakan metode PCR. Komposisi bahan yang digunakan adalah 1 unit dry taq produk Promega, 2 µl DNA genom hasil ekstraksi, 2 µl primer, 21 µl air akuades sehingga total sebanyak 2 µl. Selanjutnya disenrtifugasi terlebih dahulu sampai tidak terdapat gelembung. Setelah itu dimasukkan ke dalam mesin PCR dengan 35 siklus. Secara umum proses PCR terdiri dari 3 tahap yaitu denaturasi (penguraian utas ganda DNA), penempelan primer (annealing) dan pemanjangan utas DNA (elongasi). Predenaturasi dilakukan pada suhu 94°C selama 2 menit untuk memastikan kesempurnaan denaturasi, sedangkan denaturasi dilakukan pada suhu 94°C selama 1 menit, annealing pada suhu 36°C selama 1 menit dan elongasi pada suhu 72°C selama 2 menit. Elongasi akhir dilakukan pada suhu 72°C selama 7 menit untuk meyakinkan proses elongasi berjalan sempurna, dan proses penstabilan pada suhu 4ºC selama 3 menit. Proses PCR ini berlangsung selama 30 siklus. 2.4 Elektroforesis Agar yang digunakan adalah gel agarose 2% ditimbang sebanyak 0.8 mg dan ditambahkan TBE buffer sebanyak 40 ml, kemudian dipanaskan dan sekaligus diaduk di atas hot plate pada suhu 150°C sampai larutan tersebut bewarna bening, kemudian ditambahkan ethidium bromide 10 µl. Setelah mendidih, kemudian dituang ke dalam cetakan agar dan dibentuk sumur gel dengan menggunakan sisir gel. Gel dibiarkan membeku dan sisir diambil dengan hati-hati. Gel kemudian ditempatkan pada alat/ tangki elektroforesis dengan posisi lubang berada pada kutub negatif. Untuk mengetahui keberhasilan amplifikasi primer yang dicobakan, campuran 9 µl hasil PCR dengan 2 µl loading die dielektroforesis pada gel agarose 2% (w/v) dalam larutan TBE dan tegangan 100 volt selama 30 menit untuk mengukur laju migrasi DNA. Gel direndam agar pita DNAnya dapat terlihat pada cahaya ultraviolet untuk keperluan dokumentasi menggunakan kamera. Gene Ruler 100bp DNA Loader digunakan sebagai standar untuk menentukan ukuran fragmen hasil amplifikasi. Untuk keperluan dokumentasi gambar difoto dengan menggunakan kamera pollaroid. Gene Ruler 100bp DNA Loader digunakan sebagai standar untuk menentukan ukuran fragmen hasil amplifikasi. 6 2.5 Karakterisasi Morfometrik Ikan sepat diambil secara acak sebanyak 10 ekor per masing- masing populasi dan dipilih berdasarkan kelengkapan anggota tubuhnya. Metode pengukuran morfometrik dengan menghubungkan jarak titik-titik tanda yang dibuat pada kerangka tubuh (Gambar 1). Pemilihan titik tersebut berdasarkan modifikasi teori Blezinsky and Doyle (1987). Pembuatan titik dilakukan dengan cara ikan diletakkan di atas kertas folio yang berlapis plastik kemudian mulai ditusuk tepat disisi titik-titik yang telah ditentukan. Karakterisasi morfometrik dilakukan dengan membagi tubuh ikan menjadi 3 bagian besar yaitu kepala, ekor dan badan. Sepuluh titik tersebut yaitu: mulut, punuk, awal sirip dorsal, akhir sirip dorsal, awal sirip caudal, akhir sirip caudal, awal sirip anal, awal ventral, awal pektoral, bawah mulut. Selanjutnya masing-masing jarak titik di seluruh badan ikan tadi dihubungkan dan diukur dengan penggaris sehingga dari 10 titik diperoleh 21 karakter yang dapat dilihat pada Gambar 1. B1 B2 D5 A1 A2 A3 A6 A4 A5 C3 C2 B7 B4 B3 B6 B5 D4 D1 D2 D3 C1 Gambar 1. Titik-titik morfometrik pada ikan sepat Keterangan gambar: A1 : Jarak antara titik awal mulut dengan punuk A2 : Jarak antara titik awal mulut dengan bawah mulut A3 : Jarak antara punuk dengan bawah mulut A4 : Jarak antara punuk dengan sirip ventral A5 : Jarak antara punuk dengan sirip pektoral A6 : Jarak antara punuk dengan awal sirip anal B1 : Jarak antara punuk dengan awal sirip dorsal B2 : Jarak antara awal sirip dorsal dengan akhir sirip dorsal B3 : Jarak antara awal sirip dorsal dengan sirip pektoral 7 B4 B5 B6 B7 C1 C2 C3 D1 D2 D3 D4 D5 : Jarak antara sirip dorsal dengan awal sirip ventral : Jarak antara akhir sirip dorsal dengan sirip ventral : Jarak antara akhir sirip dorsal dengan sirip pektoral : Jarak antara awal sirip dorsal dengan awal sirip anal : Jarak antara awal sirip anal dengan sirip pektoral : Jarak antara sirip pektoral dengan sirip ventral : Jarak antara sirip ventral dengan bawah mulut : Jarak antara akhir sirip dorsal dengan akhir sirip caudal : Jarak antara awal sirip caudal dengan akhir sirip caudal : Jarak antara akhir sirip caudal dengan awal sirip anal : Jarak antara awal sirip anal dengan awal sirip caudal : Jarak antara akhir sirip dorsal dengan awal sirip caudal 2.6 Analisis Data Keragaman genetik dianalisis menggunakan program TFPGA (Tools for Population Genetic Analysis) (Nei dan Tajima, 1981). Hubungan kekerabatan interpopulasi dianalisis berdasarkan jarak genetik dengan program UPGMA (Unweight Pair Methods Arithmetic) menurut Wright (1978) yang dimodifikasi oleh Rogers (1972) dalam Arifin et al., (2007) dan disajikan dalam bentuk dendrogram. Data seluruh karakter morfometrik dikonversi ke dalam rasio karakter dibagi dengan panjang standar. Data rasio ukuran karakter dianalisis menggunakan program SPSS 16,0. Analisis keragaman morfologis antar lokasi dilakukan secara deskriptif dengan membandingkan koefisien keragaman (CV). Untuk melihat penyebaran karakter dilakukan dengan analisis canonical dan untuk melihat keeratan korelasi dan kemiripan dilakukan analisis sharing component. 8