II. TINJAUAN PUSTAKA 2.1. Pemanasan Global
advertisement

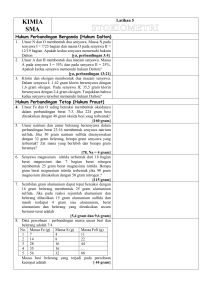
3 II. TINJAUAN PUSTAKA 2.1. Pemanasan Global Pemanasan global merupakan sebuah proses meningkatnya suhu muka bumi. Menurut Abdullah dan Khoiruddin (2009) pemanasan global diakibatkan oleh efek rumah kaca, yakni sebuah proses yang menyebabkan energi panas matahari yang diterima atmosfer dekat permukaan bumi lebih banyak dibandingkan dengan energi panas yang dilepaskan kembali keangkasa. Efeknya suhu muka bumi akan meningkat. Efek rumah kaca ini diakibatkan oleh gas rumah kaca (GRK). Gas rumah kaca merupakan gas-gas yang tertimbun di atmosfer yang sifatnya “menyerap” radiasi gelombang panjang (sinar infra merah) dan menyebabkan naiknya suhu muka bumi. Energi panas yang masuk ke bumi 25% dipantulkan oleh awan dan partikel lain di atmosfer, 25% diserap awan, 45% diapsorpsi permukaan bumi, 5% dipantulkan kembali oleh permukaan bumi. Energi yang diapsorpsi, dipantulkan kembali dalam bentuk radiasi infra merah oleh awan dan permukaan bumi. Namun sebagian besar infra merah yang dipantulkan bumi tertahan oleh awan dan gas-gas rumah kaca, sehingga infra merah tersebut dikembalikan kepermukaan bumi. Dalam keadaan normal, efek rumah kaca diperlukan. Dengan adanya efek rumah kaca perbedaan suhu antara siang dan malam tidak jauh berbeda (Abdullah dan Khoirudin, 2009). Naharia (2004) mengatakan pula bahwa, gas rumah kaca yang tersimpan di permukaan bumi secara langsung maupun tidak langsung akan menyebabkan perubahan iklim secara global. Pemanasan global yang disebabkan oleh adanya efek rumah kaca merupakan suatu fenomena, sehingga gelombang pendek radiasi matahari menembus atmosfer dan berubah menjadi gelombang panjang mencapai permukaan bumi. Setelah mencapai permukaan bumi, sebagian gelombang tersebut dipantulkan kembali ke atmosfer. Namun tidak seluruh gelombang panjang yang dipantulkan itu dilepaskan ke angkasa luar. Sebagian gelombang panjang dipantulkan kembali oleh lapisan gas rumah kaca di atmosfer ke permukaan bumi. Proses ini dapat berlangsung berulang kali, sementara gelombang yang masuk juga terus bertambah. Akibatnya terjadi akumulasi panas 4 di atmosfer. Kondisi ini persis seperti yang terjadi di rumah kaca yang digunakan dalam kegiatan pertanian dan perkebunan. Gas-gas yang dapat bertindak seperti rumah kaca diatmosfer sehingga menyebabkan pemanasan global adalah; karbon dioksida (CO2), karbon monoksida (CO), metana (CH4), dinitrogen oksida (N2O), khloroflouro karbon (CFC) buatan manusia, dan uap air (H2O) (Abdullah dan Khoiruddin, 2009). Pemanasan global dapat menyebabkan berbagai dampak lingkungan, dampak-dampak tersebut dapat berupa kekeringan berkepanjangan, banjir, angin topan, meningkatnya permukaan air laut, mengganggu kehidupan hewan liar bahkan terhadap kesehatan manusia (Abdullah dan khoiruddin, 2009). 2.2. Gas Metana (CH4) Gas CH4 merupakan gas yang mudah terbakar dan menghasilkan CO2 sebagai hasil sampingan. Gas CH4 relatif mudah diuraikan dan diperkirakan memiliki masa hidup di atmosfer sekitar 10 tahun. Laju peningkatan CH4 di atmosfer sekitar 0,9% pertahun (Abdullah dan Khoiruddin, 2009). Metana merupakan salah satu gas rumah kaca utama, yang dapat menyerap radiasi infra merah sehingga berkontribusi terhadap fenomena pemanasan global. Gas CH4 bersama-sama dengan CO2, N2O, dan CFC dapat mengabsorbsi radiasi bumi pada panjang gelombang 7-14 μm yang bersifat panas sehingga mengakibatkan suhu permukaan bumi meningkat. Disamping itu gas CH4 juga memiliki waktu tinggal 8-10 tahun dan dapat juga mempengaruhi proses reaksi kimia di atmosfer yang melibatkan metan oksidasi sebagai pengendali reaksi. Metana meningkat secara cepat dalam dua abad ini dan menduduki peringkat kedua setelah CO2 sebagai GRK yang menyebabkan pemanasan global (Khalil et. al., 1991). Konsentrasi gas CH4 yang terjadi di belahan bumi utara lebih tinggi dibandingkan dengan belahan bumi selatan. Hal ini disebabkan, sebagian besar kegiatan manusia lebih banyak berlangsung di belahan bumi utara, seperti yang terjadi pada tahun 1989 konsentrasi gas CH4 di belahan bumi utara sekitar 1700 ppbv (part per billion volume) dan di belahan bumi selatan sekitar 1670 ppbv (Husin, 1994). Konsentrasinya meningkat dari tahun ke tahun dan telah berlipat 5 ganda selama 200 tahun terakhir (Bouwman, 1990). Konsentrasi gas CH4 sebelum permukaan bumi didominasi oleh kegiatan manusia (200 tahun yang lalu) konsentrasi gas CH4 hanya berkisar 650-750 ppbv. Meningkatnya CH4 dalam kurun waktu 200 tahun terakhir ini disebabkan oleh meningkatnya fluks (70%) (Khalil dan Rasmussen, 1985). Pawitan et. al (2008) mengungkapkan pula bahwa pada skala global konsentrasi CH4 di atmosfer meningkat sekitar 1% setiap tahun. Konsentrasi CH4 saat ini sebesar 1,72 ppm atau lebih dari dua kali lipat konsentrasi pada era pra industri yang besarnya 0,8 ppm. Lahan basah, termasuk lahan sawah menyumbang sekitar 15-45% terhadap konsentarsi CH4 di atmosfer, sedangkan sumbangan lahan kering sekitar 3-10%. Fluks gas CH4 bertumpu pada kegiatan antropogenik, hampir 70% CH4 berasal dari sumber-sumber antropogenik dan sekitar 30% berasal dari sumbersumber alami. Padi sawah, ternak ruminan, pembakaran biomas, aplikasi kotoran hewan dan pemrosesan sampah organik menghasilkan CH4. Aktivitas pertanian menyumbang dua per tiga dari CH4 asal sumber antropogenik. Gas CH4 dihasilkan secara biologis oleh aktivitas mikrob yaitu aktivitas bakteri metanogen melalui penguraian atau pembusukan bahan-bahan organik yang terjadi pada lahan sawah dan fermentasi anterik pada ruminan. Gas CH4 yang berasal dari tambang batubara dan kebocoran dalam sistem distribusi gas alam serta sumur minyak dan gas merupakan sumber antropogenik lainnya. Kemudian 30% fluks CH4 yang berasal dari sumber-sumber alami, sebagian besar merupakan lahanlahan yang tergenang secara alami (Suprihati, 2007). Metana yang dihasilkan sebagian besar akan dibebaskan ke atmosfer baik secara difusi melalui tanah maupun diflukskan oleh tanaman. Variasi pelepasan CH4 dari suatu ekosistem sangat dipengaruhi oleh macam budidaya tanaman, komunitas mikrob, sifat tanah serta interaksinya. Mengetahui hubungan antara sifat tanah, sifat mikrob, dan CH4 pada berbagai macam budidaya sangatlah penting sebagai dasar untuk memahami mekanisme yang terlibat dalam produksi CH4 (Suprihati, 2007). Gas metana biasa terbentuk oleh aktivitas bakteri metanogen pada lingkungan anaerob dengan redoks potensial -220 volt. Menurut Conrad (1987) Selain lingkungan anaerob pembentukan CH4 dipengaruhi pula oleh suhu, baik 6 suhu udara maupun suhu tanah. Keterkaitan pembentukan CH4 dengan suhu lebih detail diungkapkan oleh Vogels et. al. (1988), ia mengungkapkan pada tanah sawah mayoritas bakteri metanogen yang telah diisolasi bersifat mesofilik, dimana aktivitas optimalnya terjadi pada suhu 30-40 oC. Selain bakteri metanogen (bakteri pembentuk gas metana) terdapat pula bakteri pengoksidasi CH4 atau bakteri methanotroph. Bakteri methanotroph adalah mikroorganisme aerobik yang dapat tumbuh dan berkembang dengan CH4 sebagai satu-satunya sumber energi. Oleh karena itu, oksidasi CH4 dapat terjadi pada lingkungan mikro yang bersifat aerobik pada zona perakaran dan pada bagian yang bersifat oksik pada lapisan permukaan tanah. Proses oksidasi CH4 tersebut diinisiasi oleh enzim metan mono-oksigenase yang berperan dalam konversi CH4 menjadi metanol (Oremland dan Capone, 1988). Pada budidaya lahan kering, produksi CH4 terbatas pada site-site anaerob, dengan kondisi yang sangat menunjang pertumbuhan metanotroph, sehingga meningkatkan kapasitas serapan CH4. Serapan CH4 sebesar 0,051-0,055 mg/m2/jam pada pertanaman padi gogo dilaporkan oleh Zaenal (1997). Serapan CH4 oleh hutan di Swedia mencapai 0,6-1,6 kg CH4/ha/tahun atau 6,9-18,5 103 mg CH4/m2/jam (Klemedtsson dan Klemedtsson, 1997). Ernawanto et. al. (2003) melaporkan bahwa fluks CH4 sistem penanaman padi walik jerami adalah 7,18 mg CH4/m2/jam dan sistim penanaman padi gogo rancah adalah 1,73 mg/m2/jam, sebaliknya rosot CH4 sebesar 0,05 mg CH4/m2/jam terjadi pada sistem pertanaman kedelai. Pada penelitian tersebut, fluks CH4 bersih dari sistem penanaman walik jerami - kedelai - gogo rancah diperkirakan sebesar 199,2 kg CH4/ha/tahun dengan rataan 2,3 mg CH4/m2/jam. Sedangkan kisaran fluks CH4 dari pertanaman tebu di Australia adalah 297 hingga 1005 g C-CH4/ha atau 29,7 – 100,5 mg C-CH4/m2, sementara kisaran konsumsinya 442 hingga 467 g C-CH4/ ha atau 44,2 – 46,7 mg C-CH4/m2 (Weier, 1999). Fluks CH4 dari empat macam tipe penggunaan tanah (hutan tua, hutan habis tebang, dibakar setelah tebang dan perkebunan karet) di Jambi, Sumatera berkisar antara -21,2 hingga 4,2 10-3 mg C-CH4/m2/jam (Ishizuka et. al., 2002). Nilai fluks negatif menunjukkan rosot dan berkorelasi nyata dengan kandungan 7 liat pada kedalaman tanah 0-10 cm. Nilai tersebut mengalami peningkatan pada evaluasi berikutnya yaitu menjadi -0,053 hingga 0,049 mg C-CH4 m2/jam pada macam penggunaan lahan yang lebih bervariasi yaitu hutan, kayu manis, karet, kelapa sawit dan alang-alang (Ishizuka et. al., 2005). Pembentukan CH4 juga dapat terhambat oleh pemberian pupuk nitrat seperti yang diutarakan oleh Bouwman (1996), Ia mengungkapkan bahwa aplikasi NO3- akan menunda pembentukan CH4 hingga reduksi NO3- berakhir dan Eh tanah telah cukup menurun bagi berlangsungnya proses reduksi lebih lanjut. Selain itu, NO3- juga memberikan efek toksik terhadap bakteri methanogen. Tanah yang kaya kandungan substrat organik mudah terdekomposisi (asetat, formiat, methanol, amin termetilasi) dan kandungan senyawa akseptor elektron (NO3-, Mn4+, Fe3+) rendah memiliki potensi pembentukan CH4 tinggi (Suprihati, 2007). Pada budidaya lahan kering, produksi CH4 hanya terbatas pada site-site anaerob dan kondisinya sangat menunjang pertumbuhan metanotroph sehingga meningkatkan serapan CH4 (Suprihati, 2007). Furukawa et. al. (2005) mengungkapkan pula bahwa rata-rata nilai fluks CH4 bernilai positif, akan tetapi terdapat nilai yang negatif pada musim kering. 2.3. Gas Dinitrogen Oksida (N2O) Tanah merupakan sumber terpenting dalam pembentukan CO2 dan N2O di atmosfer (Toma et. al., 2010). Abdullah dan Khoiruddin (2009) mengungkapkan N2O merupakan GRK yang memiliki umur sangat panjang sekitar 150 tahun. Selain itu N2O berpotensi menimbulkan pemanasan global sebesar 298 kali dibandingkan CO2. Oleh karena itu sekecil apapun konsentrasi N2O, dapat meningkatkan konsentrasi GRK di atmosfer dengan laju peningkatan sebesar 0,2% per tahun. Selain itu gas N2O juga dapat merusak lapisan ozon di stratosfer (Crutzen, 1981), Sehingga dapat meningkatkan radiasi yang sampai ke permukaan bumi (Ginting dan Eighbal, 2005). Sumber N2O utama adalah kegiatan manusia (antropogenik) yang berkaitan erat dengan pembakaran fosil, pembakaran biomas, dan pertanian. Berdasarkan penelitian Khalil dan Rasmussen (1992), diketahui bahwa fluks N2O dari sumber-sumber alami diperkirakan sebesar 15 Tg/tahun dan dari sumber 8 antropogenik diperkirakan sebesar 8 Tg/tahun. Kecepatan kenaikan konsentrasi rata-ratanya di atmosfer dari tahun 1960 sampai tahun 1976 sekitar 0,4 ± 0,5 ppbv/tahun, sedangkan kenaikannya dari tahun 1976 sampai tahun 1988 adalah sekitar 0,8 ± 0,02 ppbv/tahun. Hal ini menunjukan bahwa N2O meningkat dua kali lebih cepat pada tahun 1980-an dibandingkan pada tahun 1970-an. Menurut Batjes (1992), konsentrasi N2O sebelum masa industri sekitar 285 ppbv (part per billion volume) sementara pada awal 90-an sekitar 310 ppbv. Pathak (1999) mengungkapkan bahwa karbon organik, oksigen, dan senyawa NO3- didalam tanah merupakan tiga komponen penting dalam peningkatan fluks N2O. Faktor yang paling dominan dari ketiga komponen diatas adalah faktor oksigen. Kandungan air tanah membatasi oksigen berada di poripori tanah. Air tanah juga mempengaruhi terjadinya pelepasan karbon organik melalui siklus pembasahan dan pengeringan. Karbon organik menyebabkan ion NO3- tersedia melalui proses mineralisasi/imobilisasi. Ketersediaan ion NO3dipengaruhi proses difusional oleh kadar air tanah. Tekstur dan struktur tanah dapat mempengaruhi fluks N2O di dalam tanah, akhirnya respirasi mikroba dengan tersedianya karbon organik secara dramatis mempengaruhi kadar oksigen ditingkat mikro. Hasil penelitian arcara et. al (1999) mendapatkan bahwa penggunaan slury (bahan organik) dari limbah ternak meningkatkan kehilangan N sebagai N2O, melalui fluks langsung dan denitrifikasi. Fluks N2O dari tanah dibedakan menjadi fluks dari denitrifikasi dan fluks langsung yang merupakan hasil samping nitrifikasi yang berlangsung pada kondisi oksidasi kurang optimal. Kombinasi slury dengan pupuk urea pada takaran N yang sama yaitu sebesar 225 kg N/ha membebaskan gas N2O paling tinggi dari tanah dibanding dengan perlakuan tunggal pupuk urea maupun perlakuan slury. Menurut Suprihati (2007) pemberian pupuk organik yang memiliki kandungan karbon tinggi serta mudah termineralisasi, seperti pupuk kandang diduga mampu meningkatkan biomasa mikroba sehingga meningkatkan fluks N2O dari tanah pertanian. Kombinasi pupuk kandang yang mengandung asam-asam organik diantaranya asam lemak yang mudah menguap dengan pemberian pupuk N mudah tersedia seperti urea, menciptakan kondisi yang memicu pembebasan N2O. Kehilangan N2O terbesar terjadi pada bulan pertama pertanaman jagung. 9 Kehilangan N dalam bentuk N2O meningkat pada tanah yang dipupuk dengan pupuk organik. Dampak aplikasi slury sapi dalam jangka panjang mampu menurunkan pH tanah dibanding perlakuan pupuk kandang. Penurunan pH tanah tersebut akan mempengaruhi sejumlah reaksi biokimia yang berdampak pada biomas mikroba dan kandungan karbon organik tanah. Hal ini ditandai dengan lebih tingginya kandungan karbon organik tanah serta biomas mikroba pada tanah yang dipupuk dengan pupuk kandang dibanding perlakuan slury. Tingginya biomas mikroba dan karbon organik tanah memicu fluks N2O, fluks pada perlakuan pupuk kandang meningkat 2 kali dibanding perlakuan yang lain yaitu sebesar 4,9 kg N-N2O ha/thn melalui denitrifikasi dan fluks langsung sebesar 5,3 kg N-N2O ha/thn (Mogge et. al., 1999). Aplikasi slury dengan cara disemprotkan yang banyak dipraktekan di Amerika Serikat bagian Timur memberikan dampak peningkatan kehilangan N melalui fluks N2O. Pemberian slury mampu meningkatkan ketersediaan N dan kelembaban tanah, kombinasi faktor tersebut memacu reaksi reduksi nitrat. Kehilangan N dalam bentuk N2O selama 8 hari sebesar 8,5 mg N-N2O/m2, nilai tersebut lebih rendah dibanding perlakuan urea yang dikombinasikan dengan glukose sebagai sumber karbon cepat tersedia yang mencapai 20,8 mg N-N2O/m2, diduga pada slury tersebut mengandung senyawa yang mempengaruhi komunitas mikroba yang bekerja pada siklus N. Fluks N2O berkaitan erat dengan dosis N yang diberikan, pada penelitian tersebut digunakan 150 kg N/ha. Hal yang perlu diwaspadai adalah terjadinya fluks N2O yang hebat oleh residu nitrat yang terakumulasi pada tanah tersebut, potensial terdenitrifikasi dengan meningkatnya kelembaban tanah (Whalen, 2000). Selain itu Wrage et. al. (2001), mengungkapkan gas dinitrogen oksida dapat terbentuk oleh proses nitrifikasi maupun denitrifikasi, NH4+ dapat teroksidasi dalam keadaan aerob melalui proses nitrifikasi menjadi senyawa NO3-. Pada proses perubahan ini, N2O dapat terbentuk dalam jumlah yang kecil sebagai hasil sampingan. Sedangkan, senyawa NO3- dapat tereduksi melalui proses denitrifikasi dalam keadaan sedikit aerob menjadi N2O, pada proses ini N2O banyak terbentuk. 10 S Sumber: Wrrage et. al., 2001 2 G Gambar 1. Prroses pembeentukan gas dinitrogen d okksida (N2O) Gas dinitrogen n oksida tterbentuk selama s okssidasi NH4+ melalui d dekomposisi i kimia interrmediet antaara NH4+ dan NO2- (Wrrage et. al., 2001). Hal y yang sama diungkapkan d n oleh Yanaai et. al. (20007), N2O diihasilkan seb bagai hasil s sampingan dari d proses nitrifikasi ddan dihasilkaan pula sebaagai produk menengah p pada prosess denitrifikaasi, pada prooses ini NO O3- dihasilkaan pada saaat keadaan r rendah oksigen. Hasil penelitian p G Ginting dan Eighbal (20005) juga menyatakan m b bahwa NH4+ dan NO3- meningkatka m an fluks N2O. O Mosier (11998) juga menyatakan m p pembentuka an N2O di dalam d tanahh melalui prroses nitrifikasi dan deenitrifikasi. K Kedua prosees ini sangatt dipengaruhhi oleh faktoor lingkungann tanah sepeerti kondisi k kelembaban , status oksig gen tanah, suuhu udara, ketersediaan k N, bahan orrganik, dan p Lind daan Doran (19984) mengunngkapkan baahwa kelembbaban tanahh dalam hal pH. i water filled ini f pore space (WF FPS) meninngkatkan fluuks N2O. Fluks F N2O m maksimum terbentuk ketika WF FPS mencappai 60%, kkarena dalaam proses d denitrifikasi bila WFPS melebihi 600% yang terbbentuk bukann gas dinitroogen oksida ( 2O) melaiinkan gas nittrogen (N2). (N Menuurut Pathakk (1999) kellembapan taanah dapat mempengarruhi proses d denitrifikasi baik secaara langsungg maupun tidak langssung diantaaranya: (1) M Membuat lingkungan yang sesuaai untuk mikroorganis m sme berkem mbang dan b beraktivitas; ; (2) Membaatasi tersediaanya oksigenn (O2) pada pori-pori mikro m tanah; ( Mempermudah peleppasan substrrat karbon (C (3) C) dan Nitroogen (N) melalui siklus 11 pembasahan dan pengeringan. Bagaimanapun yang terpenting dari tingginya kelembaban tanah adalah membatasi adanya O2 pada pori tanah sehingga N2O mudah terbentuk dalam keadaan sedikit anaerobik. Produksi N2O meningkat baik melalui proses nitrifikasi maupun melalui proses denitrifikasi ketika tanah diberi aplikasi pupuk-N. Namun peningkatan unsur N baik dalam bentuk NH4+ maupun NO3- di dalam tanah dapat berasal dari: (1) mineralisasi N dari bahan organik dan immobilisasinya, (2) fiksasi N dari udara oleh mikroorganisme (penambatan N dari udara oleh bakteri simbiotik maupun bakteri non simbiotik), (3) pemupukan (Soepardi, 1983; Leiwakabessy, 1988). Temperatur juga memiliki pengaruh yang penting terhadap pembentukan N2O. Didapatkan N2O meningkat dari suhu 50C sampai 400C. Akan tetapi suhu optimum untuk terjadinya proses denitrifikasi yaitu antara 600C sampai 700C. Saat suhu mencapai keadaan optimum, terjadi kombinasi antara proses biologi dan proses kimia sehingga N2O yang terbentuk dapat optimum (Pathak, 1999). Akan tetapi memperhitungkan fluks N2O secara rinci di tingkat global dari dalam tanah tidak dapat di pastikan keakuratannya (Katayangi et. al., 2008). 2.4. Komoditas Tanaman Di Indonesia, berbagai komoditas tanaman pangan dapat dibudidayakan. Berdasarkan data dari Biro Pusat Statistika, Biro pusat statistika mencatat tanaman pangan utama yang ditanam di Indonesia secara berturut-turut adalah padi, jagung, singkong, kacang tanah dan ubi jalar. Berikut rincian luas panen, produktivitas serta produksi dari tanaman-tanaman pangan utama yang ada di Indonesia. Tabel 1. Luas panen, produktivitas dan produksi tanaman pangan utama Indonesia. No Jenis Tanaman 1 Padi 2 Jagung 3 Singkong 4 Kedelai 5 Kacang Tanah 6 Ubi Jalar Sumber: BPS 2012 Luas Panen (Ha) 13.201.316 3.861.433 1.182.637 620.928 539.230 177.857 Produktivitas (Ku/ha) 49,80 45,65 203,02 13,59 12,81 123,26 Produksi (ton) 65.740.946 17.629.033 24.009.624 843.838 690.949 2.192.242 12 Berdasarkan Tabel 1 diatas, dapat kita ketahui bahwa, dengan cukup luasnya lahan yang ditanami jagung, kacang tanah dan singkong di Indonesia, maka penting untuk melakukan penelitian tentang fluks gas CH4 dan N2O pada ketiga penggunaan lahan tersebut.