Laporan 2 Aktivitas Amilase Kacng Hijau
advertisement

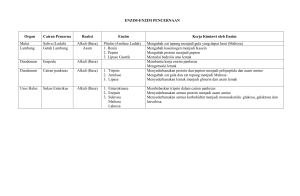
EKSTRAKSI ENZIM AMILASE DARI KECAMBAH KACANG HIJAU EXTRACTION OF AMYLASE ENZYMES FROM MUNG BEAN SPROUT Juliana M. Nur dan Sari Nurmayani Pendidikan Teknologi Agroindustri, Fakultas Pendidikan Teknologi dan Kejuruan, Universitas Pendidikan Indonesia, 2015 ABSTRAK Enzim merupakan katalisator yang berasal dari makhluk hidup seperti hewan, tumbuhan, dan mikroorganisme. Enzim sering digunakan untuk kebutuhan industri seperti industri pangan dan farmasi. Salah satu enzim yang sering digunakan dalam dunia industri pangan adalah enzim amilase yakni enzim yang berfungsi untuk memecah atau menghidrolisis pati menjadi maltosa. Enzim amilase ini dapat diperoleh dari mikroorganisme maupun tanaman, salah satunya kecambah kacang hijau yang diduga memiliki jumlah amilase yang banyak karena sedang dalam proses pertumbuhan yang memecah pati biji endosperma biji. Pada praktikum kali ini enzim amilase diekstrak dari kecambah kacang hijau dengan metode ekstraksi penghancuran dan penyaringan. Jenis pelarut yang digunakan yaitu etanol 70% dan larutan buffer pH 5 dengan variasi rasio berat kecambah dan pelarut 1:6, 1:8, 1:10, 1:12, dan 1:14 dan waktu inkubasi selama 10 menit. Tujuan dari praktikum ini adalah untuk mengetahui efektivitas pelarut serta pengaruh rasio berat sampel dan jumlah pelarut pada aktivitas enzim amilase yang dihasilkan. Dari hasil praktikum diperoleh aktivitas enzim terbesar yaitu 5.644 ml/menit yakni pada perlakuan pelarut buffer pH 5 dengan rasio berat sampel dan jumlah pelarut 1:8. Kata kunci : kecambah kacang hijau, enzim amilase, etanol 70%, buffer pH 5, aktivitas enzim. ABSTRACT Enzymes is a catalysts derived from living organisms such as animals, plants and microorganism. Enzymes are often used for industrial needs such as food and pharmaceutical industries. One of enzyme which often used in food industry is amylase, it’s an enzyme that could break down starch into maltose. this enzyme can obtained from microorganism or plant, One of the source is mung bean sprout, which have many amylase for breaking down the starch in seed to loaded growth needs. In this practice, amylase have been extracted from mung beansprout with dissolved and filtration method. The kind of solvent which used in this extraction are etanol 70% and solute of buffer pH 5 with ratio variation of mass of mung bean sprout and solvent are 1:6, 1:8, 1:10, 1:12, and 1:14 while incubation at 10 minutes. The purpose of this practice is to determine the effectiveness of the solvent and the effect of the weight ratio of the sample and the amount of solvent on the activity of the enzyme amylase produced. From the results practicum the largest enzyme activity is 5.644 ml / min which used buffer pH 5 as solvent and weight ratio of the sample with the amount of solvent 1: 8. Keywords: mung bean sprouts, amylase, ethanol 70%, buffer pH 5, the activity of the enzyme I. PENDAHULUAN 1.1 Tinjauan Pustaka Enzim adalah sekelompok protein yang berperan sebagai pengkatalis dalam reaksi-reaksi biologis. Enzim dapat juga didefenisikan sebagai biokatalisator yang dihasilkan oleh jaringan yang berfungsi meningkatkan laju reaksi dalam jaringan itu sendiri. Semua enzim yang diketahui hingga kini hampir seluruhnya adalah protein.Berat molekul enzim pun sangat beraneka ragam, meliputi rentang yang sangat luas (Suhtanry & Rubianty, 1985). Enzim berperan untuk mempercepat reaksi kimia yang terjadi di dalam tubuh makhluk hidup, tetapi enzim itu sendiri tidak ikut bereaksi. Enzim berperan secara lebih spesifik dalam hal menentukan reaksi mana yang akan dipacu dibandingkan dengan katalisator anorganik sehingga ribuan reaksi dapat berlangsung dengan tidak menghasilkan produk sampingan yang beracun (Juryatin, 1997). Amilase adalah enzim pemecah karbohidrat dari bentuk mejemuk menjadi bentuk yang lebih sederhana. Misalnya, pati dan glikogen dipecah menjadi maltosa, maltotriosa atau oligosakarida. Enzim ini terdapat dalam air liur (ptialin) dan getah pankreas yang membantu pencernaan karbohidrat dalam makanan. Darah normal juga mengandung sedikit amilase dari hasil pemecahan sel yang berlangsung secara normal. Pada penyakit radang pankreas, gondongan, kencing manis, kadarnya dalam darah meningkat. Sebaliknya pada penyakit hati, kadarnya menurun (Anonim, 1990). Amilase dapat diartikan sebagai segolongan enzim yang merombak pati, glikogen, dan polisakarida yang lain. Tumbuhan mengandung α dan ß amylase; hewan memiliki hanya α amylase, dijumpai dalam cairan pankreas dan juga (pada manusia dan beberapa spesies lain) dalam ludah. Amilase memotong rantai polisakarida yang panjang, menghasilkan campuran glukosa dan maltosa. Amilosa merupakan polisakarida yang terdiri dari 100-1000 molekul glukosa yang saling berikatan membentuk rantai lurus. Dalam air, amilosa bereaksi dengan iodine memberikan warna biru yang khas (Fox, 1991). Enzim amilase bisa didapat dari berbagai sumber seperti tanaman, binatang dan mikroorganisme. Ubi merupakan salah satu tanaman yang dapat menghasilkan enzim amilase karena komposisi ubi yang kaya akan karbohidrat. Sumber enzim dapat diperoleh dari tanaman, hewan dan mikroorganisme. Salah satu enzim pemecah pati adalah enzim αamilase (α-1,4-glukan-glukanodidrolase; EC.3.2.1.1.), enzim ini sangat berperan dalam industri pembuatan roti dan sirup. Enzim -amilase banyak terdapat pada kecambah kacang-kacangan. Enzim αamilase dalam biji dibentuk pada waktu awal perkecambahan oleh asam giberilik. Asam giberilik adalah suatu senyawa organik yang sangat penting dalam proses perkecambahan suatu biji karena bersifat sebagai pengontrol perkecambahan tersebut. (Suarni, 2007) Pemilihan kacang hijau sebagai sumber enzim α-amilase karena dalam bentuk kecambah mengandung tokoferol (pro vitamin E) 936,4 ppm, fenolik 11,3 ppm. Senyawa tersebut merupakan antioksidan yang sangat penting terhadap kesehatan terutama balita. Senyawa fenolik dengan antioksidan lainnya pada konsentrasi rendah dapat melindungi bahan pangan tersebut dari kerusakan oksidatif. Selain itu, kacang hijau memiliki kelebihan dari segi ekonomis dan agronomis dibandingkan dengan tanaman kacang-kacangan lainnya. (Suarni, 2007) Keberhasilan isolasi dan pengujian aktivitas enzim sangat tergantung pada macam serta kondisi sumber enzim, letak enzim, kecermatan kerja, bahan dan cara ekstraksi yang dipergunakan serta pengertian sifat-sifat enzim tersebut Enzim α-amilase termasuk ekstraselular, sehingga mengekstraknya relatif mudah. (Suarni, 2007) Larutan buffer ialah suatu larutan encer yang mengandung asam lemah dan basa konjugatnya atau basa lemah dan asam konjugatnya. Perubahan pH-nya sangat kecil ketika sedikit asam atau basa kuat ditambahkan kepadanya dan dengan demikian digunakan untuk mencegah perubahan pH dalam larutan. Larutan buffer digunakan untuk mempertahankan pH pada nilai yang hampir konstan dalam berbagai aplikasi kimia. Banyak bentuk kehidupan berkembang hanya dalam rentang pH yang relatif kecil sehingga mereka memanfaatkan larutan buffer untuk mempertahankan pH konstan. Salah satu contoh larutan buffer ditemukan di alam adalah darah. Larutan buffer mencapai ketahanannya terhadap perubahan pH karena adanya kesetimbangan antara asam HA dan basa konjugasinya A-. HA ═ H+ + A− Bila sejumlah asam kuat ditambahkan ke kesetimbangan campuaran asam lemah dan basa konjugatnya, kesetimbangannya bergeser ke kiiri, sesuai dengan azas Le Chatelier. Karena itu, konsentrasi ion hidrogen meningkat sebesar kurang dari jumlah yang diharapkan untuk jumlah asam kuat yang ditambahkan. Demikian pula, jika kuat alkali ditambahkan ke campuran konsentrasi ion hidrogen berkurang dengan kurang dari jumlah yang diharapkan untuk jumlah alkali yang ditambahkan. Efek ini diilustrasikan oleh titrasi simulasi dari asam lemah dengan pKa = 4,7. Etanol, disebut juga etil alkohol, alkohol murni, atau alkohol, adalah sejenis cairan yang mudah menguap, mudah terbakar, tak berwarna, dan merupakan alkohol yang paling sering digunakan dalam kehidupan sehari-hari. Etanol termasuk ke dalam alkohol rantai tunggal, dengan rumus kimia C2H5OH dan rumus empiris C2H6O. Etanol sering disingkat menjadi EtOH, dengan "Et“ merupakan singkatan dari gugus etil (C2H5). Etanol banyak digunakan sebagai pelarut berbagai bahan-bahan kimia yang ditujukan untuk konsumsi dan kegunaan manusia. Contohnya adalah pada parfum, perasa, pewarna makanan, dan obat-obatan. Dalam kimia, etanol adalah pelarut yang penting sekaligus sebagai bahan untuk sintesis senyawa kimia lainnya. Dalam sejarahnya etanol telah lama digunakan sebagai bahan bakar. Ethanol merupakan senyawa yang tidak terdapat secara bebas di alam. Zat ini adalah golongan alkohol biasa atau alkohol primer yang dibuat dari glukosa atau jenis gula yang lain dengan jalan peragian. 1.2 Tujuan Praktikum Tujuan dari praktikum ekstraksi amilase dari kecambah kacang hijau adalah untuk mengetahui pengaruh pelarut yang digunakan dalam ekstraksi enzim amilase dari kecambah kacang hijau dan untuk mengetahui pengaruh perbandingan berat kecambah dan pelarut yang digunakan dalam ekstraksi enzim amilase. 1.3 Manfaat Praktikum Manfaat dari praktikum ekstraksi amilase dari kecambah kacang hijau adalah agar mahasiswa dapat mengetahui pengaruh pelarut yang digunakan dalam ekstraksi enzim amilase dari kecambah kacang hijau dan agar mahasiswa dapat mengetahui pengaruh perbandingan berat kecambah dan pelarut yang digunakan dalam ekstraksi enzim amilase. II. METODOLOGI a. Waktu dan Tempat Praktikum kali ini dilakukan pada hari Kamis tanggal 26 Maret 2015 di Laboratorium Program Studi Pendidikan Teknologi Agroindustri Gedung Baru FPTK UPI Lantai 4. b. Alat dan Bahan Alat yang digunakan yaitu tabung reaksi, propipet, waterbath, vortex, rak tabung reaksi, pipet 1 dan 10 ml, gelas beker, kompor listrik, rak tabung reaksi, petunjuk waktu. Sedangkan bahan yang digunakan yaitu kecambah kacang hijau, larutan buffer pH 5, aquadest, Dinitrosalicylic Acid (DNSA), NaOH, Ka-Na-tartrate, amilum, es batu dan etanol 70%. c. Prosedur Kerja Mula-mula 2,5 gram kecambah kacang hijau ditimbang lalu dihancurkan dengan mortar. Pelarut untuk ekstraksi ditambahkan sedikit demi sedikit sampai volume yang sesuai dengan perbandingan yang dipakai. Etanol 70% dan buffer yang dipakai dalam keadaan dingin. Lalu ekstrak enzim disaring dengan kain saring. Ulangi penyaringan menggunakan kertas saring. Lalu sentrifugasi 4000 rpm selama 15 menit. Ekstrak enzim amilase disimpan di dalam almari pedingin sebelum dipakai. Lalu gula reduksi diukur pada menit ke-0 dan menit ke – 10. Untuk menit ke-0, 200 μl substrat amilum 1%, 500 μl larutan buffer pH 5 (50 mM) dan 200 μl aquades dimasukkan ke dalam tabung reaksi. Lalu diinkubasi selama 10 menit pada suhu 60oC. Setelah itu larutan DNS sebanyak 1 ml dan 100 μl ekstrak enzim kasar ditambahkan ke dalam tabung reaksi setelah pre-inkubasi. Lalu dihomogenkan dengan vortex. Setelah itu larutan dipanaskan kembali pada air mendidih selama 5 menit. Lalu didinginkan menggunakan air es selama 5 menit. Dan lakukan penghomogenan kembali dengan vortex. Terakhir diabsorbansi pada panjang gelombang λ540 nm. Untuk menit ke-10, 200 μl substrat amilum 1%, 500 μl larutan buffer pH 5 (50 mM) dan 200 μl aquades ditambahkan ke dalam tabung reaksi. Lakukan preinkubasi selama 10 menit pada suhu 60oC. Setelah itu 100 μl ekstrak enzim kasar ditambahkan ke dalam tabung reaksi setelah pre-inkubasi. Lalu diinkubasian selama 10 menit pada suhu 60oC. Setelah itu 1 ml larutan DNS ditambahkan ke dalam tabung reaksi. Lalu dihomogenkan dengan menggunakan vortex. Setelah itu larutan dipanaskan pada air mendidih selama 5 menit. Lalu didinginkan menggunakan air es selama 5 menit. Setelah itu larutan dihomogenkan dengan vortex. Terakhir lakukan peneraan absorbansi pada panjang gelombang λ540 nm. Setelah mengetahui jumlah gula reduksi yang dihasilkan, maka aktivitas enzim amilase pada kecambah kacang hijau dihitung dengan cara di bawah ini: Dari persamaan kurva standar maltosa, y=bx+a Ak = absorbansi kontrol (menit ke-0) As = absorbansi sampel (menit ke-10) Kadar gula reduksi awal/menit ke-0 (mg/ml), Gk = Kadar (Ak−a) b gula reduksi (mg/ml), Gs = akhir/menit ke-10 (As−a) b Jadi, kadar gula reduksi akhir Gh = Gs-Gk III. HASIL DAN PEMBAHASAN 1.1 HASIL PRAKTIKUM Berdasarkan data yang diperoleh saat praktikum, kemudian dilakukan perhitungan dengan metode Bernfeld. Atmaja (2013) menyebutkan Aktivitas amilase diukur dengan menggunakan metode Bernfeld, dimana total gula pereduksi ditentukan menggunakan reagen DNS (3,5dinitrosalicylic acid). Aktivitas enzim didasarkan perhitungan pada kurva standar maltosa (untuk penentuan unit aktivitas enzim) dan kurva standar protein (untuk penetuan kandungan protein). Berdasarkan hasil praktikum, diperoleh kadar maltosa untuk setiap variasi perlakuan yakni sebagai berikut : Tabel 1. Kadar Maltosa (mg/ml) Rasio Buffer pH 5 Etanol 70% 1:06 0.040 0.049 1:08 0.097 0.031 1:10 0.038 0.052 1:12 0.058 0.037 1:14 0.048 0.045 Aktivitas enzim amilase, 𝜇𝑚𝑜𝑙 𝑥𝑉 𝑙𝑎𝑟𝑢𝑡𝑎𝑛 (𝑚𝑙) 𝑚𝑚𝑜𝑙 = 𝑚𝑔 𝑡 (𝑚𝑒𝑛𝑖𝑡)𝑥𝑉 𝑒𝑛𝑧𝑖𝑚 (𝑚𝑙)𝑥𝐵𝑀 𝑀𝑎𝑙𝑡𝑜𝑠𝑎 𝑚𝑚𝑜𝑙 𝐺ℎ𝑥𝑓𝑝𝑥1000 Gh :kadar gula reduksi V larutan: Volume larutan sampel ( ml) Venzim : Volume enzim (ml) t = waktu inkubasi (menit) fp = faktor pengenceran ekstrak enzim kasar BM Maltosa 342 mg/mmol Dari kadar maltosa yang diperoleh maka aktivitas enzim amilase yang diekstrak dari kecambah kacang hijau dapat dihitung dengan rumus sebagai berikut : Gh : Kadar maltosa (dari tabel 1) Fp : faktor pengenceran ekstrak enzim kasar yaitu 20 V larutan : 1 ml t (menit) : 10 V enzim : 0.2 ml BM maltosa : 342 mg/mmol Setalah dilakukan perhitungan maka Aktivitas enzim amilase yang diekstrak dari kacang hijau disajikan dalam tabel 2 sebagai berikut : Tabel 2. Aktivitas Enzim Amilase dari Ekstrak Kecambah Kacang Hijau (ml/menit) Rasio Buffer pH 5 Etanol 70% 1:06 2.363 2.884 1:08 5.644 1.816 1:10 2.197 3.024 1:12 3.380 2.172 1:14 2.782 2.604 Dari tabel di atas, dinamika aktivitas enzim amilase yang diekstrak ari kecambah kacang hijau dapat dilihat dari grafik di bawah ini : Gambar 1. Grafik Aktivitas Enzim Amilase dari Ekstrak Kecambah Kacang Hijau (ml/menit) 3.2 PEMBAHASAN Berdasarkan literatur di atas, Amilase adalah enzim pemecah karbohidrat dari bentuk mejemuk menjadi bentuk yang lebih sederhana. Misalnya, pati dan glikogen dipecah menjadi maltosa, maltotriosa atau oligosakarida. Enzim amilase dapat diisolasi dari berbagai sumber baik dari hewan, tumbuhan, dan mikroorganisme. Pada saat praktikum, enzim amilase diperoleh dari kecambah kacang hijau. Karena menurut Suarni (2007) Enzim amilase banyak terdapat pada kecambah kacang-kacangan. Enzim α-amilase dalam biji dibentuk pada waktu awal perkecambahan oleh asam giberilik. Asam giberilik adalah suatu senyawa organik yang sangat penting dalam proses perkecambahan suatu biji karena bersifat sebagai pengontrol perkecambahan tersebut. Oleh karena itu enzim amilase akan sangat mudah diperoleh dari kacang hijau. Pada saat praktikum, enzim amilase dari kacang hijau diekstraksi dengan metode penghancuran dan penyaringan dan kemudian dilarutkan pada larutan organik yaitu etanol dan larutan buffer 70% dengan variasi rasio berat sampel dan pelarut yang berbeda-beda. Yakni pada rasio 1:6, 1:8, 1:10, 1:12 dan 1:14 hal tersebut bertujuan untuk mengetahui jumlah larutan yang paling baik unuk mendapatkan aktivitas ekstrak enzim kasar yang tinggi. Pelarut yang digunakan saat praktikum adalah etanol dan buffer pH 5, dimana keduaya merupakan jenis pelarut organik yang bersifat non polar sehingga dapat melarutkan enzim dan enzim dari sampel dapat terekstrak secara optimal. Untuk mengukur efisiensi pelarut untuk mengekstrak enzim amilase dari kacang hijau, ekstrak yang diperoleh kemudian diuji aktivitasnya dengan metode DNS (Dinitro salisilic acid). Prinsip pengujian aktivitas enzim dengan penambahan DNS didasarkan pada prinsip reaksi reduksi-oksidasi. Hidrolisis pati menghasilkan molekul oligosakarida dan monosakarida yang mempunyai ujung gugus pereduksi. Ujung gugus pereduksi tersebut mampu mereduksi asam dinitro salisilat yang berwarna kuning menjadi spesi tereduksinya yang berwarna jingga yaitu sewanya 3-amino-5-nitro salicilyc acid, sehingga perubahan warna tersebut dapat ditentukan dengan analisis spektrofotometri. Adanya aktivitas amilase menghasilkan maltosa yang mempunya gugus pereduksi, dengan demikian jumlah ujung gugus pereduksi dalam larutan bertambah. Semakin banyaknya jumlah gula pereduksi maka perubahan warna akan semakin jingga sehingga untuk memperoleh nilai absorbansi maltosa, nilai absoransi yang diperoleh saat inkubasi selama 10 menit dibandingkan dengan absorbansi larutan kontrol pada inkubasi 0 menit. Berikut ini merupakan reaksi gula pereduksi yang terurai akibat aktivitas amilase dengan DNS : Gambar 1. Reaksi DNS dan gula reduksi Sumber : Kongruang (2004) Reagen DNS (3,5 dinitro salicilic acid) yang merupakan senyawa aromatis yang akan bereaksi dengan gula reduksi maupun komponen pereduksi lainnya untuk membentuk 3-amino-5-nitrosalicylic acid, suatu senyawa yang mampu menyerap dengan kuat radiasi gelombang elektromagnetik pada 540 nm. Semakin banyak komponen pereduksi yang terdapat dalam sampel, maka akan semakin banyak pula molekul 3-amino-5-nitrosalicylic acid yang terbentuk dan mengakibatkan serapan semakin tinggi. (Mappiratu, 2009) Berikut ini merupakan pembahasan aktivitas enzim dengan menggunakan pelarut buffer pH 5 dan etanol 70% dengan variasi rasio berdasarkan pengkajian literatur dan hasil praktikum. 1. Ekstraksi Enzim Amilase menggunakan pelarut etanol 70% Pada saat praktikum salah satu pelarut yang digunakan adalah etanol 70% dengan rasio antara berat sampel dan pelarut 1:6, 1:8, 1:10, 1:12, 1:14. Berdasarkan hasil praktikum aktivitas enzim yang dihasilkan dengan pelarut ini berada pada kisaran 1,8 – 3,02 ml/menit. Dengan aktivitas enzim tertinggi yakni 3,024 ml/menit dengan perlakuan pelarutan dengan etanol 70% dengan rasio 1:10. Artinya enzim dengan aktivitas sampai 3,024 ml/menit akan dihasilkan dari 1 gram kecambah kacang hijau yang dilarutkan dengan etanol dingin sebanyak 10 ml. Perlakuan variasi rasio tesebut bertujuan unuk mengetahui kondisi ekstraksi optimum yakni dengan menghasilkan ekstrak enzim kasar dengan aktivitas enzim yang tinggi. Dimana semakin tinggi aktivitas enzim, maka mutu ekstrak enzim semakin baik dan kinerjanya akan semakin optimal. Adapun menurut (Atmaja : 2013) Unit aktivitas enzim didefinisikan sebagai kemampuan amilase untuk menghidrolisis amilosa menjadi maltosa sebanyak 1 mg/mL. Dari pernyataan tersebut dapat diambil kesimpulan bahwa semakin besar aktivitas enzim amilase maka kemampuannya dalam menghidrolisis amilum menjadi maltosa semakin besar dan produk yang dihasilkan akan semakin banyak. Adapun kaitan aktivitas enzim dengan pelarut serta rasio yang digunakan adalah nilai aktivitas enzim berfungsi sebagai indikator penentuan efektivitas larutan dan rasio penggunaan sampel dan pelarut. Dari hasil praktikum tersebut dapat disimpulkan bahwa pelarut etanol dengan rasio penggunaannya sebanyak 10 kali berat sampel sudah cukup untuk melarutkan enzim dari sampel. Artinya, dengan jumlah 10 kali dari sampel, dinding sel kecambah kacang hijau akan mengalami lisis dan metabolit sekundernya, salah satunya amilse akan keluar dan terlarut dalam etanol 70%. Pada saat praktikum, pelarut yang digunakan didinginkan terlebih dahulu, hal ini bertujuan untuk menghindari gesekan mortar dan lumpang yang akan menghasilkan kalor dan menyebabkan enzim terdenaturasi, karena penyusun utama enzim adalah protein dan protein akan mengalami denaturasi saat kontak dengan panas. 2. Ekstraksi Enzim Amilase menggunakan pelarut buffet pH 5 Berdasarkan praktikum yang telah dilakukan, ekstraksi enzim amilase dari kecambah kacang hijau dengan pelarut buffer pH 5 dengan masing-masing variasi perbandingan 1:6, 1:8; 1:10, 1:12 dan 1: 14 (berat kecambah kacang hijau : volume pelarut). Secara umum aktivitas yang dihasilkan dengan pelarut ini berada pada kisaran 2,2 – 5.65 ml/menit. Dengan aktivitas enzim tertinggi yakni 5.644 ml/menit dengan perlakuan pelarutan dengan buffer pH 5 dengan rasio 1:8. Artinya enzim dengan aktivitas sampai 3,024 ml/menit akan dihasilkan dari 1 gram kecambah kacang hijau yang dilarutkan dengan etanol dingin sebanyak 8 ml. Berdasarkan hasil praktikum aktivitas enzim yang paling tinggi yaitu yang menggunakan pelarut buffer pH 5 dengan perbandingan berat sampel kecambah kacang hijau dan pelarut buffer pH 5 sebanyak 1:8, hal ini menunjukan bahwa jumlah pelarut buffer pH 5 sebanyak 8 kali berat sampel sangat efektif untuk mengekstrak enzim amilase dari kecambah kacang hijau. Penambahan larutan buffer asetat (0,1-0,5 M) pH 5 bertujuan untuk menstabilkan pH agar netral karena enzim tidak dapat bertahan pada pH yang terlalu tinggi ataupun terlalu rendah (Winarno, 1986) selain itu, dengan pelarut buffer pH 5 sel akan lebih mudah lisis, sehingga jumlah enzim yang terlarut akan semakin banyak dan aktivitas enzim yang dihasilkan pun menjadi lebih tinggi. Adapun penurunan aktivitas enzim pada pelarut dengan rasio penambahan sebanyak 10, 12, dan 14 kali dari berat kecambah kacang hijau dapat disebabkan oleh inaktifnya enzim amilase karena kondisi yang terlalu asam, karena penyusun utama dari enzim adalah protein, maka sifat fungsional, fisik dan kimiawinya pun akan hampir sama, salah satunya yakni akan mengalami inaktivasi dan denaturasi (kerusakan) pada kondisi pH asam. Perubahan pH mempengaruhi muatan total protein enzim yang dapat mempengaruhi aktivitasnya, baik dengan perubahan struktur maupun dengan perubahan muatan pada residu asam amino yang berfungsi mengikat substrat (Jayanti, 2013). Ekstraksi enzim amilase dengan pelarut buffer 5 lebih efektif daripada menggunakan pelarut etanol, hal ini salah satunya disebabkan oleh pH larutan, dimana pH larutan buffer pH 5 cenderung lebih asam dari pelarut etanol 70% yang cenderung basa. Sehingga sel kecambah kacang hijau akan lebih mudah mengalami lisis karena protein transfer pada membran akan terdenaturasi oleh asam dan enzim amilasenya keluar kemudian terlarut. Berdasarkan sebuah literatur, Pada pengujian aktivitas enzim amilase, ada beberapa faktor yang memengaruhi, yaitu sebagai berikut: Suhu: karena enzim adalah suatu protein maka kenaikan suhu dapat menyebabkan denaturasi dan bagian aktif enzim terganggu sehingga konsentrasi dan kecepatan enzim menurun pH: umumnya efektivitas maksimal enzim pada pH 4,5-8. Pada pH terlau tinggi atau rendah umumnya enzim menjadi non aktif secara irreversible karena denaturasi protein. Konsentrasi enzim: pda konsentrasi substrat tertentu kecepatan reaksi bertambah dengan bertambahnya konsentrasi enzim. Konsentrasi subtrat: umumnya konsentrasi substrat akan menaikkan kecepatan reaksi, akan tetapi pada batas tertentu tidak terjadi peningkatan kecepatan reaksi walau konsentrasi substrat diperbesar. Adanya zat penghambat: hambatan/ inhibitor suatu reaksi berpengaruh terhadap penggabungan substrat pada bagian aktif yang mengalami hambatan. Dengan proses ekstraksi tersebut diatas, enzim amilase yang dihasilkan dapat digunakan untuk berbagai keperluan industri atau laboratorium khususnya untuk konversi pati, pembuatan tepung termodifikasi, pembuatan maltodekstrin, dan pembuatan gula cair. IV. KESIMPULAN DAN SARAN 4.1 Kesimpulan 4.2 Saran DAFTAR PUSTAKA Fox, P.F. 1991. Food Enzymology Vol 2. Elsevier Applied Science. London. Juryatin. 1997. Peran Enzim Amilase pada Tubuh Manusia. http://www.docstoc.com. Diakses 20 Maret 2015 Suarni. 2007. Potensi Kecambah Kacang Hijau sebagai Sumber Enzim Α-Amilase. Department of Chemistry Faculty of Mathematics and Natural Science Hasanuddin University. Suhtanry, Rubianty, 1985. Kimia Pangan. Badan Kerja Sama Perguruan Negeri Indonesia Bagian Timur, Makassar. Jayanti, Dwi. Dkk. 2013. Isolasi, Karakterisasi, Dan Amobilisasi Α-Amilase Dari Aspergillus Oryzae Fncc 6004. Chem Info Vol 1, No 1, Hal 76 – 84. Jurusan Kimia, Fakultas Sains dan, Universitas Diponegoro. Semarang. Winarno, F.G. 1986. Enzim Pangan. Jakarta: Gramedia. S. Kongruang, M. J. Han, C. I. Breton, M. H. Penner, “Quantitative Analysis of Cellulose-Reducing Ends.” Appl Biochem Biotechnol. Vol. 113, no. 116 pp. 213-31, Spring 2004 Atmaja Dwi, dkk. (2013) isolasi, purifikasi dan karakterisasi amilase dari trichoderma viride fncc 6013. Chem Info Vol 1, No 1, Hal 85 - 93, 2013 85 Jurusan Kimia, Fakultas Sains dan, Universitas Diponegoro Suarni, Rauf (2007) Potency Of Mung Bean Sprout As Enzyme Source (Α-Amilase) Indo. J. Chem., 2007, 7 (3), 332-336 1 suarni & rauf patong 332 : department of chemistry faculty of mathematics and natural science LAMPIRAN Pembuatan larutan EKSTRAKSI ENZIM AMILASE DARI KECAMBAH KACANG HIJAU Pengolahan Data Pra-Laporan Praktikum TeknologiEnzimIndusri Disusun untuk memenuhi salah satu tugas mata kuliah Teknologi Enzim Industri yang diampu oleh Siti Mujdalipah, STP., M.Si Disusunoleh : 1. Juliana M. Nur 1306948 2. Sari Nurmayani 1305544 Kelompok : 10 PROGRAM STUDI PENDIDIKAN TEKNOLOGI AGROINDUSTRI FAKULTAS PENDIDIKAN TEKNOLOGI DAN KEJURUAN UNIVERSITAS PENDIDIKAN INDONESIA 2015 DATA HASIL PRAKTIKUM Berikut ini merupakan data absorbansi awal yang diperoleh dari peneraan dengan spektrofotometer pada panjang gelombang 540 nm. Tabel 1. Data Absorbansi awal Rasio Ulangan 1:06 1:08 1:10 1:12 1:14 Buffer pH 5 Ethanol 70% Menit ke-0 Menit ke-10 Menit ke-0 Menit ke-10 1 0.150 0.172 0.116 0.132 2 0.134 0.156 0.108 0.177 1 0.093 0.249 0.142 0.126 2 0.128 0.274 0.145 0.162 1 0.091 0.116 0.142 0.167 2 0.097 0.103 0.137 0.208 1 0.110 0.141 0.113 0.121 2 0.087 0.180 0.116 0.137 1 0.116 0.132 0.141 0.165 2 0.106 0.167 0.159 0.198 Setelah data tersebut diperoleh kemudian dirata-ratakan dalam tabel 2: Tabel 2. Data Absorbansi rata-rata Rasio Buffer pH 5 Ethanol 70% Menit ke-0 Menit ke-10 Menit ke-0 Menit ke-10 1:06 0.142 0.164 0.112 0.155 1:08 0.111 0.262 0.144 0.144 1:10 0.094 0.110 0.140 0.188 1:12 0.099 0.161 0.115 0.129 1:14 0.111 0.150 0.15 0.182 Setelah dirata-ratakan, data absorbansi pada menit ke-10 dikurangi dengan data absorbansi pada menit ke-0 (kontrol) sehingga data absorbansi yang diperoleh lebih akurat dan valid. Data tersebut disajikan dalam tabel 3 Tabel 3. Data absorbansi akhir (selisih menit ke-10 dan ke-0) Rasio Buffer pH 5 Etanol 70% 1:06 0.022 0.043 1:08 0.151 0.001 1:10 0.016 0.048 1:12 0.062 0.015 1:14 0.039 0.032 Setelah data diperoleh Data absorbansi akhir maka kadar maltose yang dihasilkan dapat dihitung dengan menggunakan persamaan garis dari kurva standar maltosa yaitu 𝑦 = 2.2993𝑥 − 0.0709 dengan y sebagai absorbansi larutan dan x sebagai kadar maltosa (mg/ml), sehingga diperoleh persamaan : 𝑦 + 0.0709 𝑥= 2.2993 Kadar maltosa untuk setiap perlakuan disajikan dalam tabel 4 berikut : Tabel 4. Kadar Maltosa (mg/ml) Rasio Buffer pH 5 Etanol 70% 1:06 0.040 0.049 1:08 0.097 0.031 1:10 0.038 0.052 1:12 0.058 0.037 1:14 0.048 0.045 Dari kadar maltosa yang diperoleh maka aktivitas enzim amilase yang diekstrak dari kecambah kacang hijau dapat dihitung dengan rumus sebagai berikut : Gh Fp V larutan t (menit) V enzim BM maltosa : Kadar maltosa (dari tabel 4) : faktor pengenceran ekstrak enzim kasar yaitu 20 : 1 ml : 10 : 0.2 ml : 342 mg/mmol Setalah dilakukan perhitungan maka Aktivitas enzim amilase yang diekstrak dari kacang hijau disajikan dalam tabel 5 sebagai berikut : Tabel 5. Aktivitas Enzim Amilase dari Ekstrak Kecambah Kacang Hijau (ml/menit) Rasio Buffer pH 5 Etanol 70% 1:06 2.363 2.884 1:08 5.644 1.816 1:10 2.197 3.024 1:12 3.380 2.172 1:14 2.782 2.604 Dari tabel di atas, dinamika aktivitas enzim amilase yang diekstrak ari kecambah kacang hijau dapat dilihat dari grafik di bawah ini : Gambar 1. Grafik Aktivitas Enzim Amilase dari Ekstrak Kecambah Kacang Hijau (ml/menit) Aktivitas Enzim Amilase Kacang Hijau Akivitas enzim (ml/menit) 6.000 5.000 4.000 3.000 Buffer pH 5 2.000 Etanol 70% 1.000 0.000 1:06 1:08 1:10 1:12 Rasio enzim : pelarut 1:14