Enzimrffik*fiii
Peter J. Kennelly, PhD & Viclor
'
W. Rodwell,
PhD
PERAN BIOMEDIS
asam D-amino. Karena berikatan dengan substrat melalui
titik perlekatan", enzim bahkan dapat
mengubah sub xrat nonc h iral menjadi prod tk c h iral. Gambar
7-1 melukiskan mengapa redulai substrat piruvat nonchiral
yang dikatalisis oleh enzim menghasilkan L-laktat dan bukan
campuran rasemik Dlaktat dan L-laktat. Spesifisitas enzim
yang sangat tinggi memberi sel hidup kemampuan untuk
sedikitnya "tiga
Enzim adalah polimer biologis yang mengatalisis reaksi
kimia yang memungkinkan berlangsungnya kehidupan
seperti yang kita kenal. Keberadaan dan pemeliharaan
rangkaian enzim yang lengkap dan seimbang merupakan
hal yang esensial untuk menguraikan nutrien menjadi
energi dan chemical building block (bahan dasar kimiawi);
menyusun bahan-bahan dasar tersebut menjadi protein.
DNA, membran, sel, dan jaringan; serra memanfaatkan
secara bersamaan melaksanakan dan secara independen
mengontrol beragam proses kimiawi.
energi untuk melakukan motilitas sel, fungsi saraf, dan
kontraksi otot. Dengan pengecualian molekul RNA katalitik
atau ribozim, enzim adalah protein. Kekurangan jumlah atau
aktivitas katalidk enzim-enzim kunci dapat terjadi akibat
kelainan genetik, kekurangan gizi, atau toksin. Defek enzim
ENZIM DIKLASIFIKASIKAN
BERDASARKAN TIPE REAKSI
Nama-nama yang paling sering digunakan untuk kebanyakan
enzim menjelaskan tipe reaksi yang dikatalisis, diikuti oleh
dapat disebabkan oleh mutasi genetik atau infeksi oleh
akhiran -ase. Contohnya, dehidrogenase mengeluarkan
atom-atom hidrogen, protease menghidrolisis protein,
virus atau bakteri patogen (misalnya Vibrio cholerae). Para
ilmuwan kedokteran mengatasi ketidakseimbangan aktivitas
enzim dengan menggunakan bahan farmakologis untuk
menghambat enzim-enzim tertentu dan sedang meneliti
terapi gen sebagai cara untuk mengobati defisiensi jumlah
dan isomerasr mengatalisis tata-ulang dalam konfigurasi.
Pemodifikasi dapat teletak di depan atau di belakang nama
enzim untuk menjelaskan substrat enzim (xantin olaidase),
sumber enzim (ribonuklease panhreas), pengaturannya
atau Fungsi enzim.
(lipase peka-hormon), atau suatu gambaran dari mekanisme
kerjanya (protease sistein). Jika diperlukan, ditambahkan
penanda alfanumerik untuk menunjukkan berbagai bentuk
suatu enzim (misalnya RNA polimerase III; protein kinase
ENZIM ADATAH KATATIS
YANG EFEKTIF & SANGAT SPESIFIK
cp).
Untuk menghilangkan ambiguitas, International Union
of Biochemists (IUB) menciptakan suatu sistem terpadu
tatanama enzim yaitu setiap enzim memiliki nama dan
Enzim yang mengatalisis perubahan satu atau lebih senyawa
(substrat) menjadi satu atau lebih senyawa lain (produk)
meningkatkan laju reaksi setidaknya 106 kali dibandingkan
jika tidak dikatalisis. Seperti semua katalis lain, enzim
kode khusus yang menunjukkan tipe reaksi yang dikatalisis
dan .substrat yang terlibat. Enzim dikelompokkan ke dalam
tidak berubah
secara permanen atau dikonsumsi sebagai
konsekuensi dari keikutsertaannya dalam reaksi yang
bersangkutan.
enam kelas:
1.
Oksidoreduktase (mengatalisis oksidasi dan
2.
duksi)
Transferase (mengatalisis pemindahan gugus seperti
gugus glikosil, metil, atau fosforil)
Selain sangat efisien, enzim juga merupakan katalis
yang sangat selektifl Tidak seperti kebanyakan katalis yang
digunakan dalam bidang kimia sintetik, enzim bersifat
re-
3. Hidrolase (mengatalisis pemutusan hidrolitilz
C-C, C-O, C-N, dan ikatan lain)
4. Liase, mengatalisis pemutusan C-C, C-O,
C-N, dan ikatan lain dengan eliminasi atom yang
spesifik baik bagi tipe reaksi yang dikatalisis maupun substrat
atau substrat-substrat yang berhubungan erat. Enzim juga
merupakan katalis stereospesifik dan biasanya mengatalisis
reaksi dari hanya satu stereoisomer suatu senyawa, misalnya,
D-gula, tetapi bukan L-gula, asam L-amino, tetapi bukan
menghasilkan ikatan rangkap
53
/
54
BAGIAN l: STRUKTUR & FUNGSI PROTEIN & ENZIM
kovalen atau,nonkovalen. Contoh-contohnya antara lain
adalah piridoksal fosfat, flavin mononukleotida (FMN)'
flavin adenin dinukleotida (FAD), tiamin pirofosfat,
biotin, dan ion logam Co, Cu, Mg, Mn, dan Zn. Logam
v
/-\
g(
V
adalah gugus prostetik yang paling sering di.fumpai. Sekitar
sepertiga dari semua enzim mengandung ion-ion logam yang
terikat erat dan disebut metaloenzim. Ion-ion logam yang
)
,:
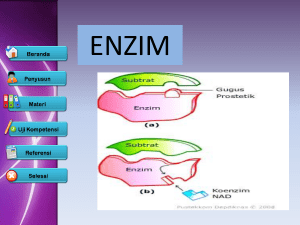
Bagian
enzim
Substral
Gambar 7-1. Representasi planar dari "perlekatan tiga-titik" suatu
substrat ke bagian (tempat) aktif sebuah enzim. Meskipun atom
dan 4 identik, namun jika atom 2 dan 3 telah melekat ke bagian
-l
komplementernya di enzim, hanya atom yang dapat terikat. Karena
itu, jika telah berikatan dengan enzim, atom-atom yang tampak
serupa dapat dibedakan, dan hal ini memungkinkan perubahan
1
kimiawi stereospesifik.
5. Isomerase
6.
(mengatalisis perubahan geometrik atau
struktural di dalam satu molekul)
Ligase (mengatalisis penyatuan dua molekul yang
dikaitkan dengan hidrolisis AIP).
Meskipun sistem
IUB ini jelas, namun nama-nama
enzim menjadi panjang dan relatif tidak praktis sehingga
kita biasanya tetap menamai enzim berdasarkan nama
tradisionalnya meskipun kadang-kadang nama itu
'menyesatkan. Nama IUB untuk heksokinase melukiskan
kejelasan sekaligus kompleksitas sistem IUB. Nama IUB
untuk heksokinase adalah AIP:D-heksosa 6-fosfotransferase
E.C.2.7.1.1. Nama ini menunjukkan heksokinase sebagai
anggota dari kelas 2 (transferase), subkelas 7 (pemindahan
satu gugus fosforil), sub-subkelas I (alkohol adalah alaeptor
fosforil), dan "heksosa-6" menunjukkan bahwa alkohol yang
terfosforilasi berada di karbon enam heksosa. Namun, kita
terus menyebutnya sebagai heksokinase.
ikut serta dalam reaksi redoks umumnya berikatan dengan
gugus prostetik, misalnya heme (Bab 6) atau kelompok besisulfur (Bab 12).Logamjuga mempermudah pengikatan dan
orientasi substrat, pembentukan ikatan kovalen dengan zatzat antara reaksi (Co2- pada koenzim B,r), atau berinteraksi
dengan substrat untuk menyebabkannya lebih elektrofilik
(kekurangan elektron) atau nukleofilik (kaya elektron).
Kofoktor Berikqlon Secoro Reversibel
dengon Enzim ofou Substrot
Kofaktor memiliki fungsi serupa dengan gugus Prostetik
tetapi berikatan secara transien dan mudah terlepas dengan
enzim atau subsuat, misalnya ATP. Tidak seperti gugus
prostetik yang terikat secaia stabil, kofaktor harus terdapat
dalam medium di sekitar enzim agar katalisis dapat terjadi.
Kofaktor yang paling umum adalah ion logam. Enzim
yang memerlukan kofaktor ion logam disebut enzim yang
diaktifkan oleh logam (meul-actiaated enzjrmes) :untuk
membedakannya dafi metaloenzim dengan ion logam
berfungsi sebagai gugus prostetik.
Koenzim Berfungsi Sebogoi Pengongkut
Substrqt
Koenzim berfungsi sebagai pengangkut-atau bahan pemindah gugus-yang dapat didaur-ulang dan memindahkan banyak substrat dari tempat pembentukannya ke tempat
GUGUS PROSTETIK, KOFAKTOR.
& KOENZIM BERPERAN PENTING
DATAM KATATISIS
Banyak enzim mengandung berbagai molekul nonprotein
kecil dan ion logam yang ikut serta secara langsung
dalam katalisis atau pengikatan substrat. Molekul/ion ini,
yang disebut gugus prostetik, kofaktor, dan koenzim,
memperluas ragam kemampuan katalisis melebihi yang
dimungkinkan oleh gugus fungsional (yang jumlahnya
terbatas) di rantai samping aminoasil peptida.
Gugus Prostetik Terintegrosi Erot ke dolom
Struktur Enzim
Gugus prostetik dibedakan berdasarkan integrasinya yang
kuat dan stabil ke dalam struktur protein melalui Saya-gaya
pemakaiannya. Ikatan dengan koenzim juga menstabilkan
substrat, seperti atom hidrogen atau ion hidrida yang ddak
stabil dalam lingkungan cair sel. Gugus kimia lain yang diangkut oleh koenzim antara lain adalah gugus metil (folat),
gugus asil (koenzim A), dan oligosakarida (dolikol).
Bonyok Koenzim, Kofoktor, & Gugus
Prcstetik odqlqh Turunon Vitomin B
Vitamin B larut-air merupakan komponen penting berbagai
koenzim. Selain vitamin B, beberapa koenzim mengandung
gugus adenin, ribosa, dan fosforil AMP atau ADP (Gbr'
7-2). Nikotinamid adalah komponen koenzim redoks
NAD dan NADB sementara riboflavin adalah komponen
koenzim redoks FMN dan FAD. Asam pantotenat adalah
komponen dari koenzim A pengangkut gugus asil. Sebagai
pirofosfatnya, tiamin ikut serta dalam dekarboksilasi asam
BAB Z; ENZIM:MEKANISME
KEUA /
55
ENZIM MENGGUNAKAN BANYAK
MEKANISME UNTUK MEMPERMUDAH
KATALISIS
Enzim menggunakan berbagai kombinasi dari empat
---cH-
tl
k"j
HHH
O:P*O*
mekanisme umum unruk mempercepar laju reaksi kimia.
|
HO
Kotqlisis kqrenq Kedekoton
Agar dapat bereaksi, molekul-molekul harus berada dalam
jarakyang cukup dekat untuk membentuk ikatan saru sama
lain. Semakin tinggi konsentrasinya, akan semakin sering
molekul-molekul itu bertemu saru sama lain dan semakin
besar laju reaksinya. Ketika mengikat molekul substrat di
bagian aktifnya, enzim rnenciptakan suaru regio dengan
konsentrasi substrat lokal yang tinggi. Lingkungan ini juga
secara spasial mengatur arah molekui-molekul substrat
sehingga diperoleh posisi ideal untuk berinteraksi. Hal
tersebut menyebabkan laju reaksi meningkat sedikitnya
seribu kali lipat.
OH
j#i
o:l-o-?*,
o-
l..l
I
r")
H_H
HO
Kotolisis Asom-Bosq
'ffi.
UntukNAD.,R=H.
Gugus-gugus fungsional yang dapat terionisasi pada rantai
samping aminoasil dan (jika ada) pada gugus prosrerik
o-keto dan koenzim asam folat dan kobamid berfungsi
berperan dalam katalisis dengan berfungsi sebagai asam atau
basa. Katalisis asam-basa dapat bersifat spesifik arau umum.
"Spesifik' dalam hal ini diartikan hanya proton (HrO-) atau
ion OH-. Pada katalisis asarn spesifik atau basa spesifik"
Gambar 7-2. Struktur NAD. dan NADP*.
UntukNADP-,R=PO,,.
dalam metabolisme satu-karbon.
laju reaksi peka terhadap perubahan dalam konsentrasi
proton, tetapi tidak bergantung pada konsentrasi asam lain
KATATISIS TERJADI DI BAGIAN AKTIF
Spesifisitas substrat yang ekstrem dan efisiensi katalitik
enzimyang tinggi mencerminkan adanya lingkungan yang
dirancang sedemikian cermar hanya untuk satu reaksi
tertentu. Lingkungan ini yang disebut bagian/tempat aktif
(actiue s//), umumnya berbentuk celah atau kantung.
Bagian aktif pada enzim multimerik sering terletak pada
pertemuan anura subunit-subunit dan merekrut residuresidu dari lebih satu monomer. Bagian aktif tiga-dimensi
ini melindungi substrat dari pelarut dan mempermudah
katalisis. Substrat mengikat bagian aktifdi regio yang bersifat
komplementer dengan bagian substra t yang ti d/1 k mengalami
perubahan kimiawi sewakru reaksi berlangsung. Pengikaran
ini secara simultan menyatukan bagian-bagian substrat yang
ahan mengalami perubahan dengan gugus-gugus fungsional
residu peptidil aminoasil. Bagian aktif juga mengikat dan
mengarahkan kofaktor atau gugus prosrerik. Banyak residu
amino asil yang diperoleh dari berbagai bagian rantai
polipeptida (Gambar 7-3) lkut serra menentul<an karakter
tiga dimensi dan ukuran yang besar pada bagian aktif.
Arg 145
*'*
oH NH:/-.4.*-NH'
I
./"\
l- ll oe| ..H- /;\.,2
i
H
t /.v=o'" )p
I H-9-C,.
/N
'N-H''
ll[\l\.r) i
"
tl'-^i'
His 196 '"'......
4\:
Tyr248
I
-or-G\CH
'-'znr''"
I'
o\
C'.o:
llr\\
ctu72
His
...,.
69
\vrq
[ /
I
H
Gambar 7-3. Cambaran dua-dimensi sebuah substrat dipeptida,
glisil{irosin yang terikat'di dalam bagian aktif karboksipeptidase A.
56
/
BAGIAN l: STRUKTUR & FUNGSI PROTEIN & ENZIM
Ala
/c{o +E
E*cHo..LE \\
/cH
NH. olt
f rE-Cl-l,NH-
KG
CH.NH.
'+E
/
Glu
, , E-cHo
Glu
KG
Pyr
CHO
kompleks
masing-masinS
Gambar 7-4.Mekanisme "ping-pong" untuk transaminasi. E-CHO dan E-CHTNH'
Tewakll]
Clu,
)
KC,
cx,-ketoglutarat;
(Ala,
piruvat;
Pyr,
alanin;
Slutamat
enzim-piridoksal fosfat dan
"nii.-piridoksamin.
(donor proton) atau basa (akseptor proton) yang terdapat
di dalam larutan atau di bagian aktif. Reaksi yang lajunya
responsifterh adap semua asam atau basa yang ada dikatakan
dapat mengalami katalisis basa umum atau asam umum'
Kqtqlisis dengon "Poksoqn"
Enzim yang mengatalisis reaksi lisis yang menyebabkan
putusnya ikatan kovalen biasanya mengikat substratnya
d"l"- suatu konformasi yang agak sedikit
kurang
dengan perubahan-Perubahan dinamik yang menyertai
k"t"'iirir. Kekurangan ini diatasi oleh Daniel Koshland
yang mengajukan model induced rtt' y^ng menyatakan
bahwa ketika mendekati dan berikatan dengan enzim,
substrat menginduksi perubahan konformasi pada enzim'
yaitu perubahan yang analog dengan memasukkan tangan
irr'rbrti"t) ke dalam sarung tangan (enzim) (Gambar 7-5)'
Akibat wajarnya adalah bahwa enzim memicu perubahan
timbal-balik pada substrat dengan memanfaatkan energi
ikatan untuk memfasilitasi transformasi substrat menjadi
oleh
mengikat
studi-studi biofisik pergerakan enzim sewaktu
menguntungkan bagi ikatan yang akan putus tersebut'
produk. Model induced
Konformasi yang terjadi akan meregangkan atau mendistorsi
ikatan sasaran, melemahkannya, dan menyebabkannya lebih
rentan terputus.
substrat.
ft ini rclah banyak dibuktikan
Kcrrqlisis Kovqlen
PROTEASE HIV MENGGAMBARKAN
KATALISIS ASAM.BASA
Proses katalisis kovalen melibatkan pembentukan suatu
ikatan kovalen antara enzim dan satu atau lebih substrat'
Enzim pada famili aspartat Protease yang mencakup
Enzim yang telah mengalami modifikasi tersebut kemudian
menjadi suatu reaktan. Katalisis kovalen memasukkan
suatu jalur reaksi baru dengan energi aktivasi yang lebih
rendah-dan karena itu lebih cepat-daripada jalur realai
dalam larutan homogen. Namun, modifikasi kimiawi pada
enzim bersifat transien. Setelah reaksi selesai, enzim kembali
ke keadaannya sebelurn termodifikasi. Jadi, peran enzim
tersebut tetap katalitik. Katalisis kovalen sering terjadi
pada enzim-enzim yang mengatalisis reaksi pemindahan
enzim pencernaan pepsin, katepsin lisosom, dan protease
fN'7
\/
M
I
gugus. Residu di enzim yang ikut serta dalam katalisis
Lo,od..r umumnya adalah sistein atau serin dan kadangkadang histidin. Katalisis kovalen sering mengikuti suatu
"ping-pong", yaitu mekanisme dengan substrat
^.k"rrir*.
pertama yang terikat dan produknya dibebaskan sebelum
substrat keduanya terikat (Gamb ar 7 -4) '
SUBSTRAT MENGINDUKSI PERUBAHAN
KONFORMASI PADA ENZIM
Pada akhir abad ke-19, Emil Fischer mengibaratkan ikatan
yang sangat spesifik antara enzim dan substratnya sebagai
kunci dan anak kuncinya. Meskipun perumPamaan
"kunci dan anak kuncinya' dapat menjelaskan spesifisitas
yang sangat tinggi pada interaksi enzim-substrat' namun
kesan bahwa bagian aktif enzim bersifat kaku tidak sesuai
Gambar 7-5. Cambaran dua-dimensi model induced tt Koshland
untuk bagian aktif sebuah iase. Pengi katan substrat.A-B menginduksi
perubahin konformasi di enzim yang menyeja.iarkan residu-residu
latalitik yang ikut serta dalam katalisis serta meregangkan ikatan
antara A dan B sehingga ikatan tersebut mudah putus'
I
BAB Z: ENZIM:MEKANISME
o<-
K
ini dengan mendonasikan sebuah proton ke gugus amino
yang terbentuk setelah putusnya ikatan peptida. Kedua
tH
6t'-ro
/o-H
9Y
li
CH,
CH
e=fv I
o"l*
*
At
*'t.fl
?)
NTC_R
H,/': \ciH
,l
\
ti
l'rl
R'\
//N-H
HHO
o.@
\\/
I
cH.
I
AspX
*o
melibatkan
zat antata asil enzim kovalen. Sebuah residu seril yang sangat
reaktif, serin 195, ikut serta dalam "charge-relay netu,,ork"
dengan histidin 57 dan asparrar 102. Di bagian aktif, residuresidu yang terpisah jauh dalam struktur primer ini, berada
dalam jarak yang cukup dekat untuk membentuk ikatan
satu sama lain. Dalam rangkaian Asp 102-His 57-Ser 195,
residu-residu ini membentuk "charge-relay network" yang
berfungsi sebagai'pemindah proton."
ll
+ C-R
H
oo
'il
I
cH_
cH,
Asp Y
Asp X
t'
oleh aspartar prorease
hidrolitik langsung air pada ikaran pepdda, katalisis
oleh serin protease kimotripsin melibatkan pembentukan
serangan
\ ll
cH.
AspY
KIMOTRIPSIN & FRUKTOS A.2,6.
BISFOSFATASE ADATAH CONTOH
KATALISIS KOVATEN
Sementara katalisis
H.
o.poo
\\_,/
cc
aspartat yang berbeda bagian aktifnya dapat bekerja secara
bersamaan sebagai basa umum atau sebagai asam umum
karena lingkungan sekitarnya mempermudah ionisasi salah
satunya, tetapi bukan keduanya.
Kimolripsin
I
1,H
\7
SZ
transisi tetrahedral. Aspartat kedua (Asp Y, Gambar 7-6)
kemudian memfasilitasi dekomposisi zat antara tetrahedral
,, /
t*-31*
H/" LH
..ot
o,..
KEUA /
l-
Gambar 7-6. Mekanisme katalisis oleh suatu aspartat protease
misalnya protease HlV. Tanda panah melengkung menun.jukkan
arah gerakan elektron. O Aspartat X bekerja sebagai basa untuk
mengaktifkan molekul air dengan mengambil sebuah proton.@
Molekul air yang telah aktif menyerang ikatan peptida, membentuk
zat antara tetrahedral yang bersifat sementara. @ Aspartat y
bekerja sebagai asam untuk mempermudah pemutusan zat antara
tetrahedral dan membebaskan produk-produk pecahan dengan
memberikan sebuah proton ke gugus amino yang baru terbentuk.
Pemindahan proton selan.iutnya dari Asp X ke Asp y memulihkan
protease ke keadaan awalnya.
yang diprodulai oleh virus imunodefisiensi manusia (HI\t,
memiliki kesamaan mekanisme katalisis. Katalisis melibatkan
dua residu aspartil yang bekerja sebagai katalis asam-basa.
Pada tahap perrama reaksi, sebuah asparrat yang berfungsi
sebagai basa umum (a.p X, Gambar 7-6) mengekstraksi
Terikatnya substrat memicu pergeseran proton yang
selanjutnya memindahkan proron hidroksil Ser 195 ke Asp
102 (Gambar 7-7). Peningkatan nukleofilisitas oksigen seril
mempermudah serangannya
ke karbon karbonil
ikatan
peptida substrat yang membentuk suatu zat antara asilenzim kovalen. Proton di Asp 102 kemudian berpindah
melalui His 57 ke gugus amino yang dibebaskan ketika
ikatan peptida rerpurus. Bagian pepdda asli dengan satu
gugus amino bebas kemudian meninggalkan bagian aktif
enzim dan digantikan oleh molekul air. Charge-relay network
kini
mengaktifkan molekul air dengan menarik sebuah
proton melalui His 57 ke Asp 102. Ion hidroksida yang
terbentuk menyerang zat antara asil-enzim dan pergeseran
balik proton mengembalikan proron ke Ser 195 yang
memulihkan keadaannya semula. Kimotripsin, meskipun
menga.lami modifikasi sewakru proses katalisis, muncul
tanpa perubahan ketika reaksi selesai. Tiipsin dan elastase
menggunakan mekanisme katalitik serupa, tetapi jumlah
residu di pemindah proron Ser-His-Asp berbeda.
Fru ktosq
-2,6-Bisfosfqtqse
yakni suatu enzim regulatorik
sebuah proton dari molekul air dan menyebabkannya lebih
Fruktosa-2,6-bisfosfatase,
bersifat nukleofilik. Nukleofil yang terbentuk ini kemudian
menyerang karbon karbonil elektrofilik pada ikatan peprida
yang menjadi sasaran hidrolisis yang membentukzatantafa
pada glukoneogenesis (Bab 20), mengatalisis pembebasan
hidrolitik fosfat di [arbon 2 fruktosa 2,6-bisfosfat. Gambar
7-8 melukiskan peran ketujuh residu bagian aktif enzim.
58
/
BAGIAN l: STRUKTUR & FUNGSI PROTEIN & ENZIM
HO
lil
Rr-N-rC-Rr
O
n
/-{^
-'\
o-\ -&-t H , N.\N.Y-H1-O_
ct{.
}rrss
{
I
Asp 102
His 57
oq
H
I
* -*T
o
r*z'i\J
\,/ n-"
14
R?
I
I
I
E-P. Fru-6-P
E-P.
E.P
Ser 195
I
I
Asp 102
E . Fru-2,6-P"
O-
His 57
R,-NH.
\\c-R.
I
@
o\
oro@*n- ruAnt
I
Ser 195
Asp 102
His
". \-*
@ o*S*l7<*_-\F>,,*
Asp
l=
102
His 57
HzO
Gamhar 7-8. Katalisis oleh fruktosa-2,6-bisfosfatase. (1) Lys 356
dan Arg 257, 3O7, dan 352 menstabilkan muatan negatif quadruple
Clu 327 menstabilkan
substrat melalui interaksi antarmuatan
muatan positif di His 392. (2) Nukleofil His 392 menyerang gugus
fosforil C-2 dan memindahkannya ke His 258 yang membentuk
suatu zat antara fosforil-enzim. Fruktosa-6-fosfat meninggalkan
enzim tersebut. (3) Serangan nukleofilik oleh molekul air, mungkin
.
dibantu oleh Clu 327 yang bekerja sebagai sebuah basa dan
membentuk fosfat anorganik. (4) Ortofosfat anorganik dibebaskan
dari Arg 257 dan Arg 307 (Diproduksi ulang dengan izin dari Pilkis Sl et
o
Asp 102
His 57
al: 6-Phosphofructo-2-kinase/fructose-2,6-bisfosfatase: A metabolic signaling
enzyme. Annu Rev Biochem 1995;64:799. O by Annual Reviews, www'
annualreviews.orS. Dicetak ulang dengan izin)'
HOOC-R-
n-o-'-r
@ oo o9---n-ruAr+'q,
Ser 1e5
T
His 57
AsP"102
Gambar 7-7. Katalisis oleh kimotripsin. O Sistem charge-relay
mengeluarkan satu proton dari Ser 195, menyebabkannya menjadi
.195
yang telah aktif menyerang
nukteofil yang lebih kuat. @ Ser
ikatan peptida membentuk suatu zat antara tetrahedral transien.
@ Pembebasan peptida terminal amino dipermudah oleh donasi
sebuah proton ke gugus amino yang baru terbentuk oleh His 57 dari
'l
sistem charge-relay ini menghasilkan zat antara asil-Ser 95. @ His
57 dan Asp 102 berkolaborasi untuk mengaktifkan satu molekul air
yang menyerang asil-Ser 195 dan membentuk zat antara te-trahedral
kedua. O Sistem charge-relay mendonasikan satu proton ke Ser
195 yang mempermudah penguraian zat antara tetrahedral untuk
membebaskan peptida terminal karboksil @.
Katalisis melibatkan "trias katalitik' residu satu Glu dan dua
His serta satu zat antara fosfohistidil kovalen.
RESIDU KATALITIK BERSIFAT
CONSERVED'
'H'GHLY
Anggota-anggota dari suatu famili enzim, misalnya Protease
aspartat atau serin menggunakan mekanisme serupa untuk
mengatalisis suanr tipe reaksi tetapi bekerja pada substrat
yang berbeda. Famili-famili enzim tampaknya btrasal dari
proses duplikasi gen yang menciptakan salinan kedua dari
enzim tefientu. Protein yang disandi oleh
g..r y".rg
-.ttyandi
Ledua gen kemudian dapat mengalami evolusi secara mandiri
untuk mengenal substrat yang berbeda-dan membentuk,
contohnya, kimotripsin, yang memecah ikatan peptida di
BAB Z: ENZIM:MEKANISME
KEUA /
59
Tabel T-1. Sekuens asam amino di sekitar tempat katalitik beberapa protease sapi. Regio yang diperlihatkan
adalah regio di kedua sisitempat katalitik residu seril (S)dan histidil (H)
sisi terminal karboksil asam-asam amino hidrofob besar;
dan tripsin yang memuruskan ikatan peptida di sisi terminal
karboksil asam-asam amino basa. Kesamaan nenek-moyang
(asal-mula) enzim dapat diperkirakan dari adanya asam-asam
amino spesifik di posisi yang sama di setiap anggota famiii
enzim. Residu-residu ini disebut sebagai conseraed residues
(residu yang tidak mengalami perubahan evolusi). Protein-
protein yang memiliki banyak residu jenis ini dianggap
bersifat homolog saru sama lain. Tabel 7-1 menggambarkan
konservasi struktur primer dua komponen dari charge-relay
network untuk beberapa prorease serin. Residu-residu yang
l\
*
u
t
ikut serta secara langsung dalam katalisis termasuk dalam
rT
residu dengan derajat konservasi yang tinggi.
ISOZIM ADATAH BENTUK ENZIM
BERBEDA YANG MENGATATISIS REAKSI
YANG SAMA
Organisme tingkat-tinggi sering mengeluarkan beberapa
versi yang secara fisik berbeda dari suatu enzim, dan masingmasing mengatalisis reaksi yang sama. Seperti anggota famili
protein lainnya, katalis-katalis protein atau isozim ini berasal
dari duplikasi gen. Isozim dapat memperlihatkan perbedaan
ringan dalam sifat seperti sensitivitas terhadap faktor
regulatorik terrenru (Bab 9) atau afinitas substrat (misalnya
heksokinase dan glukokinase) yang mengadaptasikan isozim
ke jaringan atau lingkungan tertentu. Sebagian isozim
juga dapat meningkatkan kelangsungan hidup dengan
1
ffi
4
Gambar 7-9. Pengamatan langsung proses pemutusan DNA
tunggal yang dikatalisis oleh suatu endonuklease restriksi. Molekul
DNA yang telah diimobilisasi menjadi manik-manik
(abu-abu)
diletakkan dalam suatu aliran arus dapar (tanda panah tebal), yang
menyebabkan konformasinya memanjang. Pemutusan di satu
tempat restriksi (ditandai oleh warna) oleh suatu endonuklease
menyebabkan molekul DNA memendek yang dapat diamati secara
langsung dengan mikroskop karena basa-basa nukleotida pada DNA
memperlihatkan fluoresensi. Meskipun endonuklease (lingkaran
terbuka) tidak memperlihatkan fluoresensi, dan karenanya tidak
terlihat, namun cara molekul DNA memendek secara progresif
(1 + 4) mengungkapkan bahwa endonuklease berikatan dengan
ujung bebas molekul DNA dan bergerak
tersebut dari satu tempat ke tempat lain.
di
sepanjang molekul
menyediakan salinan "cadangan" suatu enzim esensial.
AKTIVITAS KATATITIK ENZIM
MEMPERMUDAH DETEKSINYA
yang sesuai (iihat Bab 8), laju reaksi katalitik yang dipantau
setara dengan jumlah enzim yang ada, yang memungkinkan
kita mengukur konsentrasi enzim.
Jumlah enzim yang relatif sedikit di dalam sel mempersulit
penentuan keberadaan dan konsentrasi enzim tersebut.
Enzimologi Molekul Tunggol
Namun, kemampuan untuk secara cepar mengubah
Terbatasnya sensitivitas pengukuran konsentrasi enzim
ribuan molekul suatu substrat rerrentu menjadi produk
tradisional mengharuskan digunakannya sekelompok besar,
memudahkan masing-masing enzim untuk mengungkapkan
keberadaanya. Pengukuran aktivitas katalitik enzim sering
digunakan dalam laboratorium klinis dan riset. Pada kondisi
atau ansambel, molekul enzim untuk menghasilkan produk
dalam jumlah yang dapat diukur. Oleh sebab itu, data yang
diperoleh mencerminkan kemampuan katalitik rata-rara
60 /
BAGIAN l: STRUKTUR & FUNGSI PROTEIN & ENZIM
masing-masing molekul. Kemajuan-kemajuan terkini dalam
bidang nanoteknologi memungkinkan kita mengamati'
biasanya dengan mikroskop fuoresen, katalisis oleh masingmasing enzim dan molekul substrat. Oleh karena itu, para
ilmuwan kini dapat mengukur laju proses katalisis tunggal
dan kadang-kadang masing-masing tahap dalam katalisis
oleh suatu proses yang disebut enzimologi molekul tunggal
(single molecule en4rnologli (Gambar 7-9).
Penemuon Obqr Memerlukqn Pemeriksoqn
Enzim yong Sesuoi untuk Penopison 'High'
Throughput''
Enzim adalah satu dari beberapa kelas utama biomolekul
yang menjadi sasaran untuk pembuatan obat dan agen
terapeutik lain. Contohnya, banyak antibiotik menghambat
enzim yang khas untuk mikroba patogen. Penemuan obat
baru sangat dipermudah jika kita dapat memeriksa secara
cepat dan otomatis sejumlah besar farmakofor potensial-
suatu proses yang disebut sebagai bigh'throughput
screening. Pemeriksaan penyaring high-throughput ini
ideal untuk menyurvei berbagai produk combinatorial
chernistry, sintesis secara bersamaan berbagai senyawa kimia
yang mengandung semua kemungkinan kombinasi dari
satu set zat kimia prekursor. Pemeriksaan kadar enzim yang
menghasilkan produk kromagenik atau fluoresen merupakan
hal ideal dalam bigh-tbrougbput screening karena detektor
optik dapat dirancang
secara mudah untuk menganaiisis
jumlah banyak.
secara cepat sampel dalam
Enzyme-Li nked lm m u noa s sdrl
Sensitivitas pengukuran enzim dapat digunakan untuk mende-
teksi protein yang tidak memiliki aktivitas katalitik. Enzyme'
linhed immt"moassay (ELISA) menggunakan antibodi yang
secara kovalen terhubung ke suatu "enzim reportel'misalnya
alkali fosfatase atau peroksidxe horseradish (sejenis tanaman
lobak) yang produk-produknya mudah didetetsi, umumnya
melalui penyerapan sinar atau dengan fluoresensi' Serum atau
sampel biologis lain yang akan diperiksa diletakkan dalam lempeng mikrotiter plastik, tempat protein melekat pada permukaan plastik dan tidak dapat bergerak. Semua permukaan penyerap dinding sumur yang tersisa kemudian "diblok' dengan
menambahkan protein nonantigenik, misalnya albumin serum
sapi. Kemudian ditambahkan suatu larutan antibodi lang diikat
secara kovalen ke suatu enzim reponer.
Antibodi melekat pada
antigen yang telah diimobilisasi sehingga ikut terimobilisasi.
Kelebihan molekul antibodi bebas kemudian dihilangkan dengan pembilasan. Keberadaan dan jumlah antibodi yang terikat
kemudian ditentukan dengan menambahkan substrat untuk
enzim reporter tersebut.
Dehidrogenqse Dependen-NAD(P).
Diperikso Secqro Spektrofotometris
Sifat fisikokimia reaktan dalam suatu reaksi yang dikatalisis oleh
enzim menentukan jenis pemeriksaan yang dapat digunakan
untuk menilai aktivitas enzim. Pemeriksaan spektrofotometri
memanfaatkan kemampuan suatu subsffat atau produk unruk
menyerap sinar. Koenzim tereduksi NADH dan NADPH yang
ditulis sebagai NAD(P)H, menyerap cahaya pada panjang
NAD(P)teredulai,
(Gambar
NAD(P)7-10). Jika
tidak demikian
penyerapan pada340 nm meningkat sebanding dengan--dan
gelombang 340 nm, sedangkan bentuk teroksidasinya
dengan kecepatan yang ditentukan oleh-jumlah NAD(P)H
yang dihasilkan. Sebaliknya, untuk suatu dehidrogenase yang
mengatalisis oksidasi NAD(P)H, akan dijumpai penurunan
penyerapan pada 340 nm. Pada masing-masing kasus tersebut,
laju perubahan dalam densitas optik pada 340 nm
akan
sebanding dengan jumlah enzim yang ada.
Bonyok Enzim Diukur dengon
Menggobungkqnnyq ke Dehidrogenose
Pengukuran enzim dengan reaksi yang tidak disertai oleh
perubahan penyerapan atau fluoresensi umumnya lebih sulit'
200
250
300
350
400
Panjang gelombang (nm)
Gambar 7-10. Spektrum absorpsi NAD- dan NADH. Densitas
adalah untuk larutan 44 mg/L dalam sebuah sel dengan jalur sinar
1 cm. NADP. dan NADPH masing-masing memiliki spektrum yang
analog dengan NAD. dan NADH.
produk atau substrat yang tersisa dapat
yang lebih mudah dideteksi. Pada
menjadi
senyawa
diubah
reaksi mungkin perlu dipkahkan
iain,
produk
yang
kasus
sebelum diukur. Strategi
bereaksi
tidak
yang
substrat
dari
suatu substrat sintetik
merancang
dengan
adalah
alternatif
atau berfuoresensi'
sinar
menyerap
yang
produk
dengan
Pada beberapa kasus,
BAB Z: ENZIM: MEKANISME
Contohnya, p-nitrofenil fosfat adaiah substrat artifisial
untuk fosfatase rertentu dan untuk kimotripsin yang tidak
KEUA /
OI
Tabel 7-2. Enzim serum utama yang digunakan dalam
diagnosis klinis.
menyerap sinar tampak. Namun, setelah hidrolisis, anionp-
nitrofenilat yang terbentuk akan menyerap sinar pada 419
Pendekatan yang sangat umum lainnya adalah
menerapkan pengukuran "gabungan" (Gambar 7-11).
Biasanya, suatu dehidrogenase dengan substrat berupa
produk enzim yang akan diteliti ditambahkan ke dalam
kelebihan kataiitik. Laju kemuncuian arau menghilangnya
NAD(P)H akan bergantung pada laju reaksi enzim rempar
dehidrogenase digabungkan.
ANATISIS ENZIM TERTENTU MEMBANTU
DIAGNOSIS
Dari ribuan enzim berbeda yang ada di tubuh
manusia,
enzim-enzim yang fungsinya tidak-tergantikan bagi vitalitas
sel akan terdapat di seluruh jaringan tubuh. Enzim iain atau
isozim diekspresikan hanya di sel tertentu pada periode
tertentu perkembangan, atau sebagai respons terhadap
perubahan fisiologis atau patofisiologis tertentu. Analisis
tentang keberadaan dan distribusi enzim d2n i567lm-dsng2n
ekspresi yang biasanya spesifik untuk jaringan, waktu, arau
lingkungan-sering membantu penegakan diagnosis.
Enzim Plqsmo Nonfungsionol Membqntu
Menentukon Diignosis & Prognosis
Enzim dan proenzim tertenru serta substratnya terdapat
setiap saat dalam darah orang normal dan menjalankan fungsi
Glukosa
-- nre,rvrg'.
V
I
IHEKS'K'NASEI
oo''tn'.
It
Glukosa,6-foslat
f ,uqo,ryuqr-l
|'-rtaoP'
IDEH|DROGENASEII _
\
+
INADPHI+ H.
6-Fosfoglukonolakton
Gambar 7-1'l . Pemeriksaan enzim gabungan untuk aktivitas
heksokinase. Pembentukan glukosa 6Josfat oleh heksokinase
dikaitkan dengan oksidasi produk ini oleh glukosa-6-fosfat
dehidrogenase dengan keberadaan enzim tambahan dan NADP..
Jika terdapat kelebihan glukosa-6-fosfat dehidrogenase, laju
pembentukan NADPH, yang dapat diukur pada 340 nm, ditentukan
oleh laju pembentukan glukosa 6Josfat oleh heksokinase.
Catatan: Banyak enzim di atas tidak spesifik untuk pen),akit ),ang tercantum.
fisiologis dalam darah. Contoh enzim plasma fungsional
ini antara lain adalah lipoprotein lipase, pseudokolinesterase,
dan proenzim koagulasi darah dan pelarutan bekuan darah
(Bab 50). Sebagian besar enzim ini disintesis dan disekresi
oleh hati.
Plasma juga mengandung banyak enzim lain yang fungsi
fisiologisnya dalam darah tidak diketahui. Enzim plasma
yang tampaknya nonfungsional ini berasal dari kerusakan
normal rutin eritrosit, leukosit, dan sel lain. Kerusakan ataLr
nekrosis jaringan akibat cedera atau penyakit umumnya
disertai peningkatan kadar beberapa enzim plasma
nonfungsional. Tabel 7-2 mencantrtmkan beberapa enzim
yang digunakan dalam enzimologi diagnostik.
lsozim loktot Dehidrogenose Digunqkqn
untuk Mendeteksi lnfork Miokqrdium
L-Laktat dehidrogenase adalah enzim tetramerik yang
keempat subunitnya terdapat dalam dua bentuk iso
(isoform) yang dinamai H (untuk jantung) dan M (untuk
otot). Subunit-subunit ini dapat berkombinasi seperti
diperlihatkan di bawah untuk menghasilkan isozim L-laktat
dehidrogenase yang secara katalitik aktif:
62
/
BAGIAN l: STRUKTUR & FUNGSI PROTEIN & ENZIM
lsozim Loktot
Dehidrogenose
l1
l2
dalam sampel bioiogis dan forensik. Pada teknik PCR, suatu
HHHH
HHHM
l4
HHMM
HMMM
l5
MMMM
l3
DNA polimerase yang termostabil yang diarahkan oleh
primer oligonukleotida yang sesuai menghasilkan ribuan
salinan dari suatu sampei DNA yang pada awalnya terdapat
dalam kadar yang terlalu rendah untuk dideteksi secara
Subunit
iangsung.
Deteksi res*ietion fragment lengtb pofumorpbisms
(RFLP) memungkinkan kita meiakukan deteksi pranatal
berbagai penyakit herediter, sePerti sifat sel sabit, talasemia
Subunit H dan M disandi oleh gen-gen tersendiri yang
ekspresinya diatur secara diferensial di berbagai jaringan'
Karena jantung mengekspresikan subunit H hampir secara
eksklusif, isozim I, mendominasi di jaringan ini. Sebaliknya'
isozim I, mendominasi di hati. Dalam plasma secara normal
beta, fenilketonuria bayi, dan penyakit Huntington. Deteksi
RFLP melibatkan p€mutusan DNA untai ganda oleh
dehidrogenase. Setelah suatu
endonuklease restriksi, yang dapat mendeteksi perubahan
ringan pada DNA yang memengaruhi temPat-tempat
pengenalannya (recognized sites). Bab 39 menyajikan rincian
infark miokardium atau pada penyakit hati, jaringan yang
lebih ianjut mengenai pemakaian PCR dan enz'im-enzim
rusak membebaskan berbagai bentuk iso laktat dehidrogenase
restriksi untuk diagnosis.
yang khas ke dalam darah. Peningkatan kadar isozim I' atau
I, yan1terjadi dapat dideteksi dengan memisahkan berbagai
iigo-.. laktat dehidrogenase dengan eiektroforesis dan
DNA REKOMBINAN MERUPAKAN ALAT
PENTING UNTUK MEMPETAIARI ENZIM
t.rdap"i sejumlah kecil laktat
mengukur aktivitas katalitiknya (Gambar 7 -12).
Teknologi DNA rekombinan telah muncul sebagai aset
penting dalam penelitian rentang enzim. lJntuk meneliti
itrrlktur dan fungsi enzim diperlukan sampel enzim
dengan tingkat kemurnian yang sangat tinggi' Ir4engisolasi
suatu enzim, terutama yang terdapat daiam konsentrasi
rendah, dari ribuan protein yang ada daiam sebuah sel
mungkin sangat sulit dilakukan. Jika gen untuk enzim
yang bersangkutan telah dapat diklon, biasanya kita dapat
ENZIIYI MEMPERMUDAH DIAGNOSIS
PENYAKIT GENETIK
Meskipun banyak penyakit telah lama diketahui disebabkan
oleh perubahan pada DNA seseorang, namun teknik atau
alat untuk mendeteksi mutasi genetik hanya baru-baru ini
iersedia secara luas. Teknik-teknik ini mengandalkan efisiensi
katalitik dan spesifisitas katalis enzim. Contohnya, reaksi
berantai polimerase Qtolymerase chain reactioz, PCR)
mengandalkan kemampuan enzim untuk berfungsi sebagai
penguat katalitik untuk menganalisis DNA yang terdapat
{Laktat)
SH
S
menghasilkan sejumlah besar protein yang disandi oleh gen
,..r.Lrr, melalui Escherichia coli atau sei ragi. Namun, tidak
semua protein hewani dapat diekspresikan dalam bentuk
aktif di sel mikroba. Demikian iuga dengan mikroba' tid:rk
(Piruvat)
Jantung
NAD.
NADH + H
PMS teroksidasi
(tidak berwarna)
formazan biru)
(LDH) dalam serum manusia' lsozinr
Cambar 7-,t2.pola normal dan patologis berbagai isozim laktat dehidrogenase
penggunakan
skema reaksi penggabungan yang
dengan
LDH pada serum dipisahkun oleh elekiroforesis dan c{ilihat
kunun tampak elektroferogram yang telah
Di
metilsulfat).
fenazin
PMS,
(NBT,
tetrazolium;
nitroblue
kir,i.
di
diperlihatkan
serum normal; dan C adalah
diwarnai. pola A adalah serum dari seorang pasien dengan infark miokardium; B adalah
isozim LDH spesifik'
serum dari seorang pasien dengan penyakit hati. Angka-angka menandai
BAB Z: ENZIM: MEKANISME
dapat melaksanakan proses-proses pengolahan pascatranslasi
tertentu. Oleh sebab itu, suatu gen dapat diekspresikan
dalam biakan sistem sel hewan yang menggunakan vektor
ekspresi baculovirus untuk mentransformasikan biakan sel
serangga. Untuk rincian lebih lanjut mengenai teknik DNA
rekombinan, lihat Bab 39.
sering menyandi suatu tempat pemutusan untuk suatu
protease yang sangat spesifik misalnya trombin di regio yang
menghubungkan dua bagian protein. Hal ini memungkinkan
kita mengeiuarkan domain fusi yang ditambahkan tersebut
seteiah tindakan pemurnian afi nitas.
Jika kemampuan untuk mengekspresikan suatu protein
Teknologi DNA rekombinan juga dapat digunakan untuk
menciptakan protein modifikasi yang mudah dimurnikan
dengan kromatografi afinitas. Gen dari protein yang
bersangkutan dikaitkan ke suatu sekuens oligonukleotida
yang menyandi suatu perpanjangan terminal karboksil atau
amino ke protein yang disandi tersebut. Protein modifikasi
yang terbentuk, disebut protein fusi, mengandung suatu
domain yang dirancang untuk berinteraksi dengan matriks
afinitas spesifik. Salah satu pendekatan yang populer adalah
melekatkan suatu oligonukleotida yang menyandi enam
ta!'
("berlabel
histidin') yang diekspresikan ini kemudian mengikat
matriks kromatografik yang mengandung ion iogam
divalen, misalnya Ni2-. Cara lain, domain pengikat-substrat
pada glutation S-transferase (GST) dapat berfungsi sebagai
"GST tad'. Gambar 7-13 melukiskan pemurnian suatu
protein fusi-GST dengan menggunakan matriks afinitas
dari gen klon-nya telah diperoleh, residu-residu aminoasil
spesifik dari protein tersebut dapat diubah dengan mengubah
kodon-kodonnya menggun akan site-directed mutagenesis.
Pendekatan ini, jika digunakan bersama dengan analisis
kinetik dan kristalografi sinar-X, mempermudah kita
mengidentifikasi peran-peran spesifik residu aminoasil
tertentu pada pengikatan dan katalisis substrat. Contohnya,
kesimpuian bahwa suatu residu aminoasil tertentu berfungsi
sebagai asam umum dapat diuji dengan me nggaatinya dengan
suatu residu aminoasil yang tidak mampu mendonasikan
sebuah proton.
RINGKASAN
.
.
yang mengandung glutation yang terikat. Protein fusi juga
m
GST
Plasmid yang menyandi GST
dengan tempat trombin (T)
63
Mutogene sis Site - Di recfed Mem beri ko n
Pemqhomon Mekonistik
Profein Fusi Rekombinqn Dimurnikon
dengon Kromotogrofi Afiniros
residu hisitidin berurutan. Protein " His
KEUA /
Klon DNAyang
menyandi enzim
Enzim adalah katalis yang sangat efektifdan spesifik.
Gugus prostetik organik dan anorganik, kofaktor, dan
koenzim berperan penting dalam katalisis. Koenzim
yang banyak di antaranya berupa turunan dari vitamin
B, berfungsi sebagai "pengangkut".
.
Mekanisme katalitik yang digunakan oleh enzim
.
mencakup introduksi sra in (vntai), aproksimasi reaktan,
katalisis asam-basa, dan katalisis kovalen.
Pada semua kelas dari suatu enzim tertentu, residu
aminoasil yang
Disatukan
GST
ikut serta dalam
katalisis
sangat
terkonservasi (tidak berubah selama evolusi)
Substrat dan enzim saling memicu perubahan konformasi
yang mempermudah pengenalan dan katalisis substrat
Aktivitas katalitik enzim mengungkapkan keberadaannya, mempermudah deteksinya, da4 menjadi dasar bagi
berbagai pemeriksaan enzyme- linked immunoassay.
Banyak enzim dapat diukur secara spektrofotometrik
dengan menggabungkannya ke dehidro genase dependen-
NAD(P)..
Ilmu kimia kombinatorial
menghasilkan beragam
aktivator dan inhibitor enzim potensial yang dapat diuji
dengan h igh- t hro ughp u! screen i ng.
Pengukuran enzim plasma membantu diagnosis dan
prognosis. Contohnya, infark miokardium meningkatkan kadar isozim I, laktat dehidrogenase dalam serum.
Gambar 7-13. Pemakaian protein fusi glutation S-transf-erase (CST)
untuk memurnikan protein rekombinan- (CSH, Blutation.)
Endonukiease restriksi mempermudah diagnosis
penyakit genetik dengan mengungkapkan restiction
fagment length
po $morphism.
64 /
.
BAGIAN l: STRUKTUR & FUNGSIPROTEIN & ENZIM
Site-directed mutagenesis
yang digunakan untuk
mengubah residu yang dicurigai penting dalam katalisis
atau pengikatan substrat, memberikan
.
pemahaman
tentang mekanisme kerja enzim.
Protein fusi rekombinan, misalnya enzim fusi GST
atau enzim berlabel-His mudah dimurnikan dengan
kromatografi afinitas.
HM,
Brik A, Vong C-H. HIV-1 protease: Mechanism and drug
discovery. Org Biomol Chem 2003;1:5.
GB et al: Metal requirements of a
diadenosine
pyrophosphatase from Bartonella bacilliformis. Magnetic
resonance and kinetic studies of the role of Mn2.. Biochemistry
Schoenen F,'Wagner
D, lVagner R: Combinatorial
compound libraries for drug discovery: An ongoing challenge.
Nature Rev Drug Disc 2003;2:222.
Goddard J-B Reymond J-L: Enzyme assays for high-throughput
screening. Curr Opin Biotech 2004;15:314.
Hedstrom L. Serine protease mechanism and specificiry. Chem Rev
2002;102:4501.
Ishijima A, Yanagida T: Single molecule nanobioscience. Tiends
Biochem
REFERENSI
Conyers
Geysen
S
ci 200 1 ;26:438.
Schafer B, Gemeinhardt H, Greulich KO' Direct microscopic
observation of the time course of single-molecule DNA
restriction reacdons. Agnew Chem Int Ed 2001 ;40:4663
Silverman RB: The Organic Chemistry of Enzyme-Catalyzed
Reactions. Academic Press, 2002.
Guide to
Suckling CJ: Enzyme Chemistry. Chapman & Hall, 1990.
Sundaresan Y Abrol R: Towards a general model for proteinsubstrate stereoselectiviry. Protein Sci 2002;11 :1330.
Frank RA'S7, et al: A molecular switch and proton wire synchronize
Todd AE, Orengo CA, Thornton JM: Plasticiry of enzyme active
sites. tends Biochem Sci 2002;27 :419.
2000;39:2347.
Fersht
A.
Strucnrre and Mechanism
in Protein
Science:
A
Enzyme CataQsis and Protein Folding. Freeman, 1999
the active sites in thiamine enzymes. Science2004;306:872
\falsh CT: Enzymatic Reaction Mechanisms. Freeman, 1979.