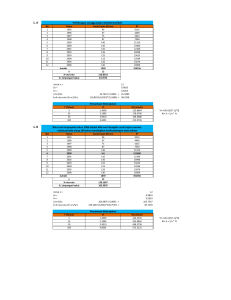
KELOMPOK 5 Ani Julita Sari Ina Triana Tika widia wati Irma Yanti Ginting Nidia Rizka Ninda Bela fantona Rizkani Indah Permata Sari ORDE REAKSI DARI SUATU KINETIKA OBAT ORDE REAKSI • Orde reaksi ialah jumlah semua komponen (dari konsentrasi dalam persamaan laju. orde reaksi suatu substansi (seperti reaktan, katalis atau produk) adalah banyaknya faktor konsentrasi yang mempengaruhi kecepatan reaksi. Orde reaksi juga menyatakan besarnya pengaruh konsentrasi reaktan (pereaksi) terhadap laju reaksi. • Laju reaksi didefenisikan sebagai perubahan konsentrasi persatuan waktu . Laju reaksi kimia terlihat dari perubahan molekul produk terhadap waktu. Laju reaksi tidak tetap melainkan berubah terus menerus seiring dengan perubahan konsentrasi . Faktor yang mempengaruhi laju reaksi • Konsentrasi Suatu zat yang bereaksi mempunyai konsentrasi yang berbeda–beda. Konsentrasi menyatakan pengaruh kepakatan atau zat yang berperan dalam proses reaksi. Semakin bernilai konsentrasi, maka laju reaksi akan semakin cepat . • Temperature Pada umumnya reaksi akan berlansung lebih cepat bila suhu dinaikkan . Dengan menaikkan suhu maka energi kinetik molekul–molekul zat yang bereaksi akan bertambah sehingga akan lebih banyak molekul memilih energi yang sama. • Luas permukaan Semakin luas permukaan zat semakin kecil ukuran parrtikel zat , maka reaksi pun akan semakin cepat • Katalis Katalis adalah suatu senyawa yang dapat menaikkan laju reaksi, tetapi tidakk ikut menjadi reaktan / produk dalam sistem itu sendiri. Setelah reaksi selesai, katalis dapat diperoleh kembali tanpa mengalami perubahan kimia . Orde reaksi dapat ditentukan dengan beberapa metode • Metode substansi Data yang terkumpul dari hasil pengamatan jalannya suatu reaksi disubstitusikan kedalam bentuk integral dari persamaan berbagai orde reaksi. Jika persamaan itu menghasilkan harga K yang tetap konstan dalam batasbatas variasi percobaan , maka reaksi dianggap berjalan sesuai dengan orde tersebut. • Metode grafik Plot data dalam bentuk grafik dapat digunakan untuk mengetahui orde reaksi tersebut . Jika konsentrasi di plot terhadap t dan didapatkan garis lurus , reaksi tersebut adalah orde nol. Reaksi dikatakan orde pertama bila log ( a-x ) terhadap t menghasilkan garis lurus. • Metode waktu – paruh Waktu paruh merupakan waktu yang dibutuhkan oleh suatu obat untuk terurai setengahnya dari konsentrasi mula–mula. Obat yang sama dapat menunjukkan orde penguraian yang berbeda pada kondisi yang berbeda. Parameter farmakokinetik merupakan besaran yang diturunkan secara matematis dari hasil pengukuran obat atau metabolit aktif dalam darah atau urin. Parameter–parameter farmakokinetik mencakup sebagai berikut : • Tetapan Kecepatan Absorbsi → ( Ka ) • Kadar puncak obat dalam darah / plasma / serum → ( Cmax ) • Waktu untuk mencapai kadar puncak → ( Tmax ) • Tetapan kecepatan eliminasi → ( kel ) • Waktu paro eliminasi → ( T ½ ) • Luar area / daerah dibawah kurva → ( AUC ) Parameter – parameter farmakokinetika suatu obat akan berbeda–beda tergantung orde reaksi masing–masing obat. Orde reaksi suatu obat menunjukkan cara bagaimana konsentrasi obat atau pereaksi mempengaruhi laju reaksi suatu kimia. Laju reaksi kimia atau proses kimia diartikan sebagai kecpatan terjadinya suatu reaksi kimia . REAKSI ORDE NOL Dalam reaksi orde nol, laju reaksinya independen dari konsentrasi reaktan, sehingga perubahan konsentrasi tidak mengubah laju reaksi. Reaksi dikatakan berorde nol terhadap salah satu pereaksinya apabila perubahan konsentrasi pereaksi tersebut tidak mempengaruhi laju reaksi. • Reaksi orde nol terjadi bila jumlah ( obat A ) berkurang dalam suatu jarak yang tetap ( t ) , maka laju hilangnya obat A dinyatakan sebagai berikut : 𝑑𝐴 𝑑𝑡 = -K0 K0 adalah tetapan laju reaksi orde nol dan dinyatakan dalam satuan massa / waktu ( missal : mg/menit ). Integrasi persamaan diatas menghasilkan persaman berikut : A = K0 t + A0 A0 adalah jumlah obat A pada t = 0 T½= 0,5 𝐴0 𝐾0 Contoh perhitungan parameter farmakokinetika obat menggunakan orde nol : • Seorang farmasi menimbang tepat 10 g obat dan larutkan dalam 100 mL air . Larutan disimpan pada suhu kamar dan diambil cuplikan larutan itu secara berkala untuk ditentukan kadarnya. Data yang diperoleh sebagai berikut: Konsentrasi obat ( mg / mL) Waktu ( jam ) 100 0 95 2 90 4 85 6 80 8 75 10 70 12 Berapa laju penurunan konsentrasi obat ( K0 ) tersebut? • Jawab : A0 = 100 mg / mL pada t = 0 A = 90 mg / mL pada t = 4 Jam • Maka : A = -K0 . t + A0 90 = -K0 ( 4 ) + 100 K0 = 2,5 mg / mL. jam REAKSI ORDE SATU Reaksi Orde Satu • Jika laju reaksi bergantung pada satu reaktan dan jumlah eksponennya satu, maka reaksi itu adalah reaksi orde pertama. Suatu reaksi dikatakan berorde satu terhadap salah satu pereaksinya jika laju reaksi berbanding lurus dengan konsentrasi itu. • Reaksi orde satu terjadi bila jumlah obat A berkurang dengan laju yang sebanding dengan jumlah obat A tersisa , maka laju hilangnya obat A dinyatakan sebagai berikut : 𝑑𝐴 𝑑𝑡 = -KA K adalah tetapan laju reaksi orde kesatu dan dinyatakan dalam satuan waktu-1 ( missal : jam-1) . Slop −𝐾 Log A = . t + log 2,3 −𝐾 log 𝑌2−𝐿𝑂𝐺 𝑌1 = = 2,3 𝑥2−𝑥1 A0 Contoh perhitungan parameter farmakokinetika obat menggunakan orde satu: • Seorang farmasi menimbang tepat 10 g obat dan larutkan dalam 100 mL air . Larutan disimpan pada suhu kamar dan diambil cuplikan larutan itu secaraberkala untuk ditentukan kadarnya . Konsentrasi obat (mg/mL) Waktu ( jam ) Log konsentrasi 100 0 2 50 4 1,7 25 8 1,4 12,5 12 1,1 6,25 16 0,8 3,13 20 0,5 1, 56 24 0,2 K dalam contoh ini , t ½ adalah 4 jam , maka ketetapan laju reaksi orde satu dapat diperoleh dengan cara : • Slop = • -K= −𝐾 2,3 = log 𝑌2−𝐿𝑂𝐺 𝑌1 𝑥2−𝑥1 2,3 (log 50−log 100 4−0 • K = 0,173 Jam-1