Soal As.karboks
advertisement
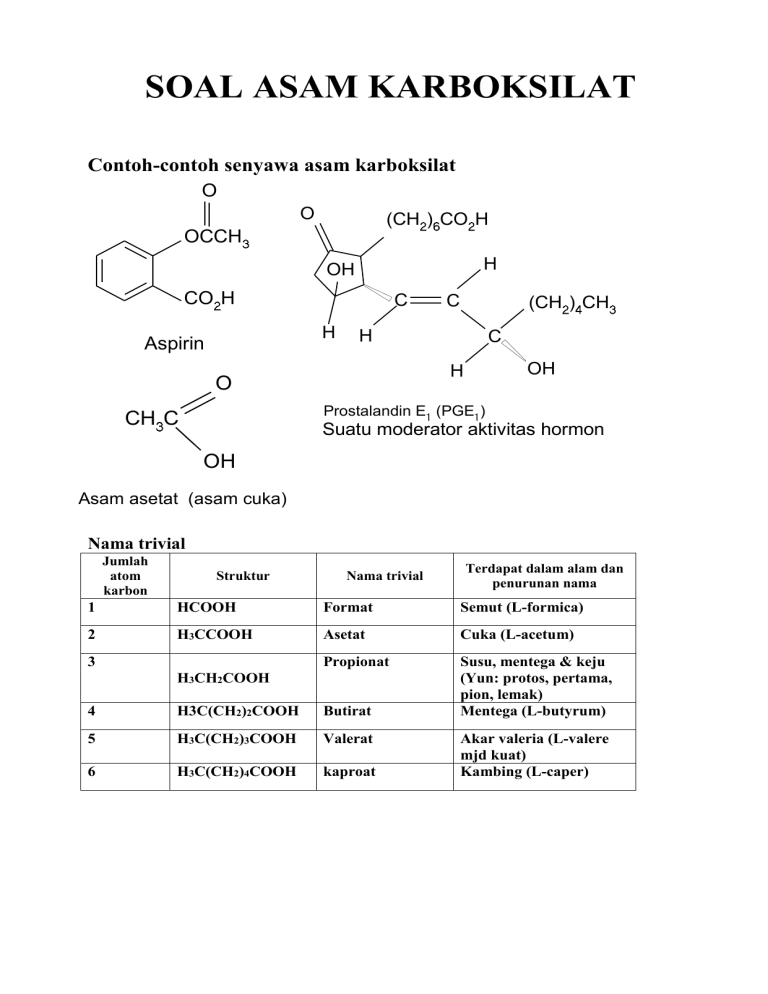
SOAL ASAM KARBOKSILAT Contoh-contoh senyawa asam karboksilat O O (CH ) CO H OCCH H OH CO H C H Aspirin C (CH ) CH H C OH H O Prostalandin E (PGE ) CH C Suatu moderator aktivitas hormon OH Asam asetat (asam cuka) Nama trivial Jumlah atom karbon Struktur Nama trivial Terdapat dalam alam dan penurunan nama 1 HCOOH Format Semut (L-formica) 2 H3CCOOH Asetat Cuka (L-acetum) Propionat Susu, mentega & keju (Yun: protos, pertama, pion, lemak) Mentega (L-butyrum) 3 H3CH2COOH 4 H3C(CH2)2COOH Butirat 5 H3C(CH2)3COOH Valerat 6 H3C(CH2)4COOH kaproat Akar valeria (L-valere mjd kuat) Kambing (L-caper) Berilah nama senyawa senyawa a) b) CH CH CH-CHCO H CH CH CHCO H CH CH CH C) CH CH CH CO H d) CH CH CHCO H Cl e) CH CHCO H CO H f) OH CH Br COOH g) h) NO CH CH CO H NO CH i) Cl k) j) COONa CCH CO H l). (CH COO) Ca m) HCOONH CH -CH-COOK Br Br 120 o O O O R 120 C 120 o O o R C C H O datar R O H polar elektron bebas Sifat polar dan datar (tak terintangi) reaksi tidak terlalu dipengaruhi oleh sisa molekul SIFAT FISIS ASAM KARBOKSILAT - adanya atom O membentuk ikatan hidrogen antar molekul dimer dengan molekul air akibatnya: td BM H O H 3C larut dalam air C C O H H O O O Antar molekul CH 3 H3C C O O H Dengan molekul air H H Contoh soal : Tunjukkan ikatan hidrogen yang mungkin terjadi dari senyawa-senyawa berikut : COOH a. b. COOH OH COOH c. dan CH3OH SIFAT FAALI YANG KHAS DARI ASAM KARBOKSILAT bau yang khas untuk BM BM Contoh : (C>10) sukar menguap bau berkurang as. format/asetat, berbau merangsang as. propionat, bau lemak tengik as. butirat, bau mentega tengik as. kaproat, bau kambing dsb. Bagaimana kerja anjing pelacak? TURUNAN ASAM KARBOKSILAT Definisi : Senyawa yang menghasilkan asam karboksilat bila direaksikan dengan air. O R C OR O Ester R C Cl halida asam O TURUNAN ASAM KARBOKSILAT R C NH 2 amida O R C O O C R anhidrida R C N nitril TATA NAMA TURUNAN ASAM KARBOKSILAT ESTER Terdiri dari dua kata a. Kata pertama adalah nama gugus alkil yang terikat pada oksigen ester. b. Kata kedua berasal dari nama asam karboksilatnya, dengan menghilangkan kata asam. c. Terdapat kemiripan antara nama ester dan garam karboksilat. Contoh : O O H3CH2C C O H H3CH2C C O Na Suatu asam Suatu garam O H3CH2C C O CH3 Suatu ester IUPAC As. propanoat Natrium propanoat Metil propanoat TRIVIAL As. propionat Natrium propionat Metil propionat Turuna asam karboksilat yang lain dan turunannya CH3COOH Asam etanoat Asam asetat CH3COCl Etanoil klorida Asetil klorida (CH3CO)2O anhidrida etanoat anhidrida asetat C O H Asam …. –at/oat Asam benzoat C O Cl Asam …. –at/oat …..il klorida Benzoil klorida C O Asam Anhidrida Asam....–at/oat ….amida O C O Anhidrida benzoat CH3CONH2 Etanamida Asetamida C O NH 2 benzamida NITRIL Nama senyawa yang mengandung gugus C N Disebut senyawa siano atau sianida Nama IUPAC banyaknya atom karbon, termasuk karbon dalam gugus CN, menentukan alkana induknya, nama alkana tsb diberi akhiran nitril. Nama trivial Nama asam karboksilat ( asam-at, diganti nitril atau o-nitril jika induknya tidak punya huruf o). IUPAC TRIVIAL H3C C N etananitril asetonitril C N Benzenakarbonitril benzonitril SOAL LATIHAN: Berilah nama IUPAC dan trivial untuk senyawa-senyawa berikut 1. CH3CH2CHBrCHBrCOOH 2. CH3CH2CH(CH2CH3)CONHC6H5 3. (CH3)2CHCN 4. (CH3)2CH(CH2)3COOC2H5 SIFAT FISIK TURUNAN KARBOKSILAT Adanya gugus –C=O senyawa polar Klorida asam, anhidrida dan ester mempunyai titik didih yang hampir sama dibanding aldehid/keton dengan BM sebanding. Sedangkan amida bp lebih tinggi. Pada amida terdapat ikatan hidrogen antar molekul yang kuat. R N O C C H O H N R Ester yang volatil pembuatan parfum mempunyai bau karakteristik bahan REAKSI SUBSTITUSI PADA SENYAWA TURUNAN AS. KARBOKSILAT Turunan as. karboksilat dibuat langsung/tidak langsung dari asam karboksilat Dengan hidrolisis kembali ke asam karboksilat Masing-masing derivat dapat diubah satu dengan yang lain. ASAM KARBOKSILAT HALIDA ASAM ATAU ANHIDRIDA KETON AMIDA ESTER PEMBUATAN ASAM KARBOKSILAT A. HIDROLISIS TURUNAN ASAM KARBOKSILAT H+ atau OH- : RCOOR’ + H2O ESTER : RCONR’2 + H2O AMIDA ANHIDRIDA : RCO-O-OCR’ + H2O H+ atau OH- H+ atau OH- RCO2H + HOR’ RCO2H + HNR’2 RCO2H + R’CO2H - H+ atau OH RCO2H + X- HALIDA ASAM : RCOX + H2O : RC≡N + H2O NITRIL H+ atau OH- RCO2H + NH3 B. OKSIDASI Ag+ / OH ( p. Tohlens ) O O R C R C H OH Cr2O72- / H+ C. REAKSI GRIGNARD 1. MgBr CO2 COOH 2. H2O , H+ REAKSI ASAM KARBOKSILAT 1. Reaksi dengan basa RCO2H + Na+OH- RCO2- Na+ + H2O Dalam NaHCO3 HCO3RCO2- + [H2CO3] RCO2H H2O + CO2 HCO3ArOH dan ROH tidak ada reaksi Dalam NaOH OHRCO2H RCO2- + H2O ArO- + H2O OHArOH OHROH tidak ada reaksi Campuran asam karboksilat dan senyawa organik lain NaHCO3 RCO2- Na+ + H2O + CO2 (larut air) Catatan : Jika R sangat panjang tidak larut dalam NaHCO3 dan bahkan NaOH ASAM BENZOAT TERSUBSTITUSI Substituen pada cincin berpengaruh karena “ efek induktifnya” Penarik elektron………meningkatkan keasaman Pendorong elektron…...(m,p) menurunkan keasaman Hampir semua posisi (baik pelepas maupun pendorong elektron) menaikkan kuat asam, karena faktor sterik dan elektronik. Bagaimana dengan p-hidroksi dan p-metoksi benzoat? Tabel harga pKa untuk beberapa asam benzoat Asam Posisi substitusi dan pKa orto meta para 4,2 4,2 4,2 3,9 4,3 4,4 COOH COOH H3C 3,0 4,1 4,5 4,1 4,1 4,5 2,9 3,8 4,0 2,9 3,8 4,0 2,2 3,5 3,4 COOH HO COOH H3CO COOH Br COOH Cl COOH O2N 3. CARBOXYLIC ACID DERIVATIVES