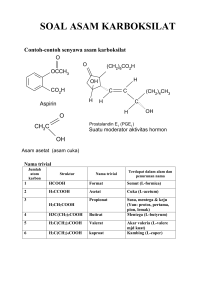
Kelompok 5 1. 2. 3. 4. 5. Vini Aprianti DG Baji Adwitiya Widyatna Ermunadi Afnitasari Rusniati Meutia Nurul Ainunnisa Defenisi Asam karboksilat Asam karboksilat merupakan senyawa organik yang mempunyai gugus karboksil (COOH) di ujung rantai karbonnya Rumus Umum : O R C OH Tata Nama Asam Karboksilat Berdasarkan aturan IUPAC (International Union for Pure and Applied Chemistry) pemberian nama pada asam karboksilat didasarkan atas alkana penyusunnya dengan memberi awalan asam dan mengganti akhiran-ana pada alkana dengan akhiran-anoat. Sedangkan penamaan secara trivial (nama umum/nama lazim) di dasarkan atas sumber asam karboksilat tersebut. Tata Nama IUPAC • Dimulai dengan asam + rantai karbon terpanjang yang mengandung gugus karboksilat (CO2H) + akhiran oat. Contoh : Jika mengandung rantai cabang, maka atom C dari gugus karboksilat dengan rantai terpanjang diberi nomor 1 Contoh : • CH3 5 CH2 4 CH 3 CH3 CH2 2 asam 3 - metil pentanoat COOH 1 5 CH3 4 CH OH 3 CH2 2 CH 1 COOH CH3 asam 4 - hidroksil - 2 - metil pentanoat • Jika terdapat lebih dari satu cabang atau gugus cabang maka penulisan rantai atau gugus cabang menurut abjad. • Jika senyawa mempunyai lebih dari satu gugus karboksilat, maka penamaan rantai utama diberi akhiran tambahan di, tri dan seterusnya. Contoh : Tata Nama Trivial (Lazim) • Ini didasarkan pada sumber alami asam yang bersangkutan. berikut adalah beberapa nama trivial asam karboksilat : Formula/struktur IUPAC Trivial sumber HCO2H As. metanoat Asam formiat Semut ( formica) CH3CO2H As. Etanoat Asam asetat Cuka (Asetum) C2H5COOH As. Propanoat Asam propionat Susu (Protospion) CH3(CH2)2CO2H As. butanoat Asam butirat Mentega (Butyrum) CH3(CH2)2CO2H As. Pentanoat Asam valerat Akar Valerian (Valera) • Jika menggunakan nama trivial, maka posisi gugus-gugus penggantian atau cabang-cabang dinyatakan dengan huruf latin. • Atom karbon yang terikat langsung pada gugus –COOH yaitu atom C nomor 2 ditandai dengan , atom C nomor 3 ditandai dengan , atom C nomor 4 ditandai dengan , atom C nomor 5 ditandai dengan dan seterusnya. CH3 5 CH2 4 CH2 3 CH2 2 O C 1 OH Cl CH3 CH COOH asam - kloroproponoat Formula/struktur IUPAC Trivial HCO2H As. metanoat Asam formiat CH3CO2H Asam etanoat Asam asetat CH3(CH2)2CO2H Asam butanoat Asam butirat CH3(CH2)2CO2H As. pentanoat Asam valerat CH3(CH2)4CO2H As. heksanoat Asam kaproat CH3(CH2)5CO2H As. heptanoat Asam enantat HO2CCO2H As. etandioat Asam oksalat HO2CCH2CO2H As.propandioat As. malonat HO2(CH2)2CO2H As. butandioat As. suksinat Sifat-sifat Asam Karboksilat • asam karboksilat dengan jumlah atom C sedikit (suku rendah) cenderung mudah menguap dan berbau tajam dan sebaliknya jika jumlah atom C-nya banyak senyawa semakin sukar menguap. • Asam karboksilat Mempunyai titik didih & titik lebur yang relatif tinggi • Kelarutan Asam karboksilat suku rendah dapat larut dalam air, tetapi asam karboksilat suku yang lebih tinggi sukar larut air. • Asam karboksilat mempunyai gugus hidroksil yang bersifat polar sehingga asam karboksilat bersifat polar (mudah larut dalam air). • Kereaktifan asam karboksilat merupakan asam lemah dan makin lemah untuk suku yang lebih tinggi. Sintesis Asam Karboksilat 1. Alkohol Primer Pada umunya zat pengoksidasi [KMnO4/H2CrO4] mengoksidasi alkohol primer menjadi asam karboksilat. Alkohol primer mula-mula dioksidasi dulu menjadi aldehida. Aldehida lebih mudah dioksidasi daripada alkohol. 2. Aldehida Aldehida sangat mudah teroksidasi menjadi asam karboksilat. Hampir setiap reagensia yang mengoksidasi suatu alkohol juga mengoksidasi suatu aldehida. Aldehida dioksidasi menjadi asam dengan [KMnO4/H2CrO4]. 3. Alkena (Olefin) Alkena (Olefin) dioksidasi menjadi asam dengan K2Cr2O7/H2SO4 4. Nitrit Hidrolisis nitrit menghasilkan asam karboksilat pada suasana asam atau basa 5. Raksi grignardt Suatu reaksi Grinard antara senyawa reagensia Grinard (pimer, sekunder, tersier, vinilik, atau aril) dan karbon dioksida (berbentuk gas atau es kering) DISKUSI 1. Kelompok 6 Apa yang dimaksud suku tinggi dan suku rendah? => yang dimaksud dengan suku tinggi yaitu asam karboksilat dengan jumlah atom C banyak sedangkan suku rendah yaitu asam karboksilat dengan jumlah atom C sedikit 2. Kelompok 2 Bagaimana reaksi nitrit ? => Hidrolisis nitrit menghasilkan asam karboksilat pada suasana asam atau basa 3. Kelompok 4 Perbedaan alkohol primer dan aldehida, mengapa aldehid dioksidasi terlebih dahulu dibanding asam karboksilat ? => alkohol primer adalah alkohol yang gugus –OH terikat pada atom C primer (atom C yang mengikat 1 atom C yang lain). sedangkan aldehida adalah suatu senyawa yang mengandung sebuah gugus karbonil yang terikat pada sebuah atau dua buah atom hidrogen. Karena aldehid lebih mudah dioksidasi menjadi asam karboksilat daripada Alkohol primer yang dioksidasi menjadi asam karboksilat. 4. Kelompok 3 Bagaimana perlakuan reaksi grignard ? => reaksi grinard adalah reaksi kimia dimana alkil atau aril mangnesium halides menambah gugus karbonil aldehida atau keton. Reagen grinard berfungsi sebagai nukleofil, menyerang atom karbon elektrofilik yang hadir dalam ikatan polar gugus karbonil. Penambahan pereaksi grinard untuk karbonil biasanya hasilnya melalui keadaan transisi enam beranggota cincin. Namun tanpa pereaksi grignard ,reaksi dapat berlangsung dengan transfer elektron tungal. Jalur serupa diasumsikan untuk reaksi lain pereaksi grignard.contohnya dalam pembentukan ikatan karbon-fosforus, karbon-timah, karbon-silikon, karbon-boron, dan karbon-heteroatom lainnya. 5. Kelompok 1 apakah Asam karboksilat bisa direaksikan dengan ester ? => suatu ester dapat dibentuk dengan reaksi langsung antara suatu asam karboksilat dan suatu alkohol melalui reaksi esterifikasi. Ester asam karboksilat adalah suaru seyaa yang mengandung gugus –CO2R dengan R dapat berbentuk alkilmaupun aril. TERIMA KASIH