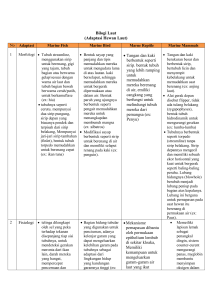
ketentuan-ketentuan pada kegiatan inventarisasi ikan air tawar
advertisement

KETENTUAN-KETENTUAN PADA KEGIATAN INVENTARISASI IKAN AIR TAWAR Oleh: Dewa Gede Raka Wiadnya, Aprilian Kusuma Wijaya & Ahmad Fauzi Rizal [Taksonomi: Leiognathidae] Fakultas Perikanan & Ilmu Kelautan, UB Malang Kontak: [email protected] [Makalah dipresentasikan pada Penyegaran Pejabat Fungsional PEH Balai Taman Nasional Meru Betiri, Tertanggal 21 – 23 Februari 2012 di Petung Sewu – Dau, Malang] Saran sitasi: Wiadnya, D.G.R., & A.K. Wijaya, 2012. Ketentuan-ketentuan pada kegiatan inventarisasi ikan air tawar. Lokakarya Penyegaran Pejabat Fungsional PEH Balai Taman Nasional Meru Betiri, 21 – 23 Februari 2012., Petung Sewu – Dau, Malang: 16pp Ringkasan Atribut ikan yang sering disebut sebagai pembeda dengan kelompok vertebrata (binatang bertulang belakang) lainnya ialah SIRIP, INSANG dan habitat AKUATIK. Ikan mempunyai anggota kelompok (spesies) yang paling banyak dan beragam dibanding kelompok vertebrata lainnya. Kegiatan inventarisasi ikan hampir selalu memerlukan koleksi specimen1, dalam kerangka penamaan kode nomenklatur yang tepat (correct naming). Sebagai bagian dari konfirmasi nomenklatur, petugas sering harus mengirimkan specimen yang didapat kepada taksonomist. Pengiriman dan/atau saling mempertukarkan specimen harus diikuti dengan dokumen pendukung tentang metode koleksi dan pengawetan specimen. Tulisan ini dipersiapkan melalui studi perbandingan (pustaka) dari beberapa museum zoology, termasuk Raffles Zoological Museum, Singapura, Museum Zoologi Brunae Darussalam, Museum Zoologicum Bogoriense dan konsultasi dengan “fish-taxonomist” senior dari LIPI – Dr. Teguh Peristiwady 1. Rasional Kegiatan inventarisasi ikan air tawar (termasuk hewan air lainnya) terdiri dari tahapan: (i) survei cepat (reconnaissance survey), (ii) koleksi specimen, (iii) preservasi specimen, (iv) identifikasi specimen, dan (v) kurasi atau penyimpanan specimen untuk penelitian lanjutan dalam periode waktu yang belum bisa ditentukan. Inventarisasi yang dilakukan secara berulang (dengan metode yang sama) menjadi kegiatan monitoring. Perubahan yang terjadi pada hasil inventarisasi per perubahan waktu ialah indikator kondisi bio-geografi suatu wilayah. Jika inventarisasi dilakukan di dalam suatu kawasan konservasi dan berulang, dia akan menjadi alat ukur kinerja manajemen (monitoring). 1 Sebuah specimen ikan ialah satu individu ikan atau lebih, atau bagian dari individu ikan (seperti jaringan) yang digunakan sebagai perwakilan untuk mepelajari populasi spesies secara keseluruhan. Dalam mempelajari suatu taksa (taxon) ikan, ahli atau taksonomist biasanya mengacu pada individu specimen yang disebut sebagai holotype. Taksa ialah kelompok organisme (satu individu atau lebih) dalam satu struktur ranking taksonomi. Setiap taksa biasanya mendapat nama ilmiah sesuai dengan kode nomenklatur. Sebagai contoh, ikan mas berada dalam satu kelompok Cyprinidae, yang terdiri dari beberapa spesies. 1 Inventarisasi ikan air tawar – Refresher PEH TN-Meru Betiri, 21 – 23 Februari 2012 Masing-masing tahapan pada kegiatan inventarisasi ikan mengikuti prosedur yang umum digunakan pada tingkat global. Namun tidak semua prosedur (baku) tersebut memungkinkan untuk diterapkan pada kondisi lokal di Indonesia. Teks menyajikan ketentuan minimal yang bisa dilakukan tanpa harus membatalkan kegiatan inventarisasi lapang. 2. Survei cepat 2.1. Petugas Kegiatan inventarisasi ialah pekerjaan seorang NATURALIST2. Naturalist ialah orang yang tertarik untuk mempelajari (studi) alam, termasuk tumbuhan atau hewan, dengan pendekatan observasi dibandingkan dengan pendekatan eksperimen. Karakteristik dasar dari seorang naturalist ialah: (i) senang berada di alam bebas dibandingkan di dalam ruangan atau kantor yang sempit (tertutup) dan tersekat-sekat, (ii) selalu tertarik pada objek atau pengalaman baru, (iii) suka bercerita (narrator), (iv) pergaulan luas / multi-segmen dan fleksibel, dan (v) periang. Karakter unik lainnya dari seorang naturalist (vi) ialah mempunyai pengetahuan yang luas (komprehensif) tentang berbagai objek di alam, walaupun tidak mendalam. Sifat ini mungkin sedikit agak aneh pada dunia modern saat ini, dengan sumber daya manusia yang sangat terspesialisasi pada bidang ilmu sempit, kompetitif dan kurang tertarik untuk memperhatikan lingkungan di sekitarnya. Survei lapang untuk kegiatan inventarisasi sebaiknya dilakukan oleh petugas yang mempunyai karakter seperti di atas, walaupun tenaga tersebut mungkin sulit didapat. Survei cepat ialah penelusuran wilayah survei secara cepat, menentukan satsiun dan melakukan kegiatan sampling. Petugas dengan karakter dasar naturalist umumnya sangat sensitive dan mempunyai pengetahuan yang luas tentang wilayah sampling. Sifat-sifat ini memudahkan dalam memilih strategi sampling, menentukan lokasi dan objek sampling yang memungkinkan untuk dilakukan secara cepat. 2.2. Perlengkapan petugas Inventarisasi ikan air tawar umumnya dilakukan pada dua tipe habitat yang berbeda, ialah: perairan mengalir (lotic, riverine) seperti sungai, dan perairan tenang (limnetic) seperti danau atau waduk. Kedua tipe lingkungan survei ini terbuka dengan sinar matahari langsung, sengatan atau gigitan binatang berbisa. Kondisi alam yang relatif asli (pristine), belum banyak diketahui orang, bisa membuat petugas kehilangan arah. Petugas survei lapang harus dilengkapi dengan peralatan pribadi minimal sebagai berikut: (i) polarized sun glasses dan sun block, (ii) booties (cattle-pak), (iii) hat (topi pelindung matahari), (iv) first-aid kit (kotak P3K), (v) handheld GPS, dan (vi) HP atau radio komunikasi. Sengatan sinar matahari bisa menimbulkan iritasi pada kulit, jika terjadi secara berlebihan dan terus menerus, diduga bisa menimbulkan “skin cancer”. Sinar matahari yang terlalu berlebihan tidak sehat bagi mata. Petugas survei sebaiknya melindungi diri dari sengatan matahari secara berlebih – cream sun-block, topi dan kaca mata (polarized) diduga menjadi pelindung yang efektif dari sengatan matahari langsung. Pada saat koleksi specimen ikan, petugas sering kali harus menginjak dasar sungai atau pinggir danau / waduk yang dasarnya tidak terlihat. Telapak kaki bisa menginjak pecahan botol, 2 Naturalist ialah seseorang yang tertarik untuk mempelajari objek (alam) dan kehidupan melalui pendekatan eksploratif. Hasil studi ialah deskripsi tentang objek secara kualitatif – jenis kegiatan yang dilakukan seorang naturalist sering disebut dengan exploratory research, sebagai kebalikan dari explanatory research dengan pendekatan eksperimen. 2 Inventarisasi ikan air tawar – Refresher PEH TN-Meru Betiri, 21 – 23 Februari 2012 kaca ataupun besi paku, terutama pada kondisi lingkungan di Indonesia yang masih belum tertata dengan baik. Booties atau cattle-pak ialah alat bantu yang bisa mengurangi (minimasi) peluang resiko negatif tersebut. Menjelajah alam liar (menyatu dengan alam) tidak harus membiarkan diri untuk misalnya menjadi korban dari alam (victim of the nature). Setiap petugas lapang harus sensitive dan mampu melakukan respon cepat (rapid response) terhadap segala bentuk atau kemungkinan alam. Gigitan ular, lebah, laba-laba atau binatang buas lainnya ialah beberapa bentuk resiko alam liar yang sebaiknya dihindari, walaupun peluang tersebut selalu ada. Sebagai antisipasi, petugas harus dilengkapi dengan first-aid kit (kotak P3K) untuk bertahan selama proses evakuasi. Disoritentasi atau tersesat ialah resiko lainnya yang bisa dihadapi petugas. Sebaiknya, tim lapang juga dilengkapi dengan peta, pemandu arah dan alat komunikasi yang menghubungkan petugas dengan pos jaga terdekat. Pisau dan parang, pada beberapa kasus bisa membantu jika ada hambatan selama perjalanan. Namun keputusan ini harus dibicarakan dengan ketua tim survei (membawa pisau atau parang bisa berdampak buruk pada beberapa kasus). Semua ketentuan di bawah bisa dijadikan prosedur tetap dari petugas lapang yang melakukan aktifitas inventarisasi ikan air tawar. Hal-hal yang dilakukan petugas inventarisasi sebelum mulai survei: 1. Mengolesi permukaan kulit (yang mengalami kontak langsung dengan matahari) dengan sun block, untuk mengurangi peluang skin-cancer akibat sengatan matahari; 2. Refresh – mengganti pakaian lapang dengan booties atau cattle pak (mengurangi resiko langsung sengatan atau gigitan binatang berbisa, maupun dasar perairan yang tidak terlihat); 3. Mengenakan polarized sun glasses dan topi untuk melindungi mata dari sengatan langsung sinar matahari; 4. Camera, HP dan / atau radio komunikasi dimasukkan ke dalam dry-bag (menghindari kerusakan peralatan jika jatuh ke dalam air) 5. Salah seorang petugas membawa kotak P3K (first aid kit), pertolongan pertama dari sengatan dan atau gigitan binatang liar. 6. Pada saat mulai survei, petugas melapor ke stasiun kontrol radio (bisa juga dilakukan melalui SMS) 7. Selama survei, petugas selalu berhubungan dengan petugas radio kontrol pada pos terdekat. Petugas radio kontrol selalu mencatat posisi petugas survei pada peta. 3. Koleksi specimen ikan Koleksi specimen ikan air tawar sangat umum dilakukan dengan menggunakan metode “electro-fishing”. Namun metode ini tidak lazim diaplikasikan di Indonesia karena termasuk kegiatan illegal. Petugas atau kolektor yang membawa peralatan electro-fishing di sungai, jika dilihat oleh orang kebanyakan, bisa berakibat kurang baik, walaupun sudah mendapat ijin khusus dari pengelola kawasan atau pemerintah. Oleh karena itu, metode elektro-fishing tidak akan dibahas pada teks ini. 3 Inventarisasi ikan air tawar – Refresher PEH TN-Meru Betiri, 21 – 23 Februari 2012 Alat tangkap yang disarankan untuk koleksi ikan ialah jala pencar (stow net). Pencar ialah alat tangkap jaring berbentuk lingkaran yang dioperasikan dengan tangan. Alat ini sudah sering digunakan pada koleksi specimen ikan untuk kebutuhan Museum Zoologi di Brunae Darussalam, dan bisa diterima oleh masyarakat zoology global. Luasan wilayah sampling ditentukan oleh diameter lingkaran pada jaring pencar. Sedangkan ukuran ikan hasil tangkap tergantung dari ukuran mata jaring (mesh size #). Jika sampling dilakukan pada kubangan air yang agak tertutup dan terisolasi, petugas bisa menggunakan bahan anaestetik untuk menangkap ikan. Bahan anaestetik yang disarankan ialah campuran minyak cengkeh dengan alcohol 50%, dengan perbandingan 1:3. Sebagai catatan – bahan anaestetik ini relatif tidak berbahaya bagi lingkungan, namun kurang baik jika diketahui oleh masyarakat umum. Petugas harus membuat pertimbangan yang matang sebelum menerapkan metode ini. Alat gill net atau jaring insang dan perangkap seperti bubu juga digunakan untuk koleksi sample. Kelemahannya ialah bahwa kedua alat ini sangat selektif, hanya menangkap ikan dengan jenis dan ukuran tertentu. Sebelum mulai sampling, petugas mencatat tanggal, kode lokasi, nama lokasi dan posisi sampling pada alat GPS. Posisi koordinat dicatat dengan menggunakan kertas khusus (wet paper) yang tidak hancur jika terkena air. Keterangan yang harus diisi ialah deskripsi singkat lokasi sampling. Selain keterangan narasi, petugas juga membuat visualisasi (foto-foto) dari lokasi sampling. Hal-hal yang dipersiapkan petugas inventarisasi ketika sampling: 1. Mengambil foto-foto visualisasi lokasi sampling; 2. Mengisi form survei (dengan pensil) tentang: (i) tanggal, (ii) kode lokasi; (iii) nama lokasi, (iv) posisi lokasi (GPS), (v) deskripsi naratif lokasi sampling dan (vi) nama petugas survei; 3. Mempersiapkan dan mengoperasikan alat dan bahan sampling (pencar, gill net, perangkap dan/atau anaestetik, hanya jika diperlukan); 4. Memilah specimen hasil sampling berdasarkan kategori kekerabatan ikan; 5. Catatan: jika kebetulan bertemu masyarakat awam, petugas harus bisa menunjukkan surat tugas dan ijin sampling dengan menggunakan alat dan bahan seperti yang tertera pada ijin sampling; 6. Jika bekerja dengan mitra, tim survei juga harus bisa menunjukkan surat SIMAKSI atau surat ijin kegiatan khusus untuk tenaga asing (surat ijin dari Kementrian Riset dan Teknologi); 7. Tim survei harus dipimpin oleh seorang ketua regu yang paling mengetahui kondisi lokal. Jika kegiatan sampling tidak memungkinkan untuk dilanjutkan (karena alasan cuaca, keamanan atau alasan lain), keputusan diambil oleh ketua regu yang bertanggung jawab di lapang. Semua anggota regu (pada kondisi khusus), harus tunduk dengan keputusan ketua regu; 8. Semua anggota tim harus mengetahui, memahami dan mengikuti aturan sampling/survei yang telah ditetapkan dalam protokol 4. Pengawetan awal Inventarisasi satwa (ikan) selalu dimulai dengan pemberian nama yang benar (correct naming). Correct naming hanya bisa dilakukan melalui konfirmasi oleh taksonomist yang autoritatif – 4 Inventarisasi ikan air tawar – Refresher PEH TN-Meru Betiri, 21 – 23 Februari 2012 di Indonesia, scientific authority untuk taxonomi ialah peneliti dari LIPI (Lembaga Ilmu Pengetahuan Indonesia). Kolektor ikan pada tingkat lapang harus bisa menunjukkan setiap specimen yang didapat untuk konfirmasi ilmiah oleh peneliti LIPI atau taksonomi senior. Oleh karena itu, kolektor harus bisa menunjukkan bahwa setiap specimen didapat melalui etika dan metode koleksi yang tepat. Sebelum kegiatan identifikasi, specimen juga harus diawetkan dengan metode yang juga memerlukan persyaratan standar atau yang umum dipakai oleh curator maupun museum zoology. Metode yang dijelaskan pada teks ini ialah salah satu prosedur yang umum digunakan oleh beberapa museum. Ikan hasil sampling yang telah dipisahkan berdasarkan kategori kekerabatan harus segera diawetkan. Bahan pengawet awal ialah formalin 10%. Keterangan: formalin 100% ialah bahan yang mengandung bahan formaldehyde jenuh 40%. Artinya, formalin 10% akan mengandung formaldehyde dengan kejenuhan 4%. Larutan pengawet yang dimaksud ialah formalin 10% (atau setara dengan formaldehyde 4%). Ikan dengan ukuran > 15 cm disuntik dengan larutan formalin untuk mencegah pembusukan pada organ dalam. Jika tidak, ikan sering mengambang pada larutan pengawet di dalam botol koleksi. Perbandingan antara larutan formalin dan ikan pada wadah pengawet ialah 3:1. Tempat penyimpan sample sementara ialah kantong atau botol plastik yang tidak mudah bocor. Ikan yang ukurannya relatif besar harus disiapkan tempat khusus, karena harus disimpan pada posisi lurus (tidak bengkok). Ikan juga tidak boleh disimpan berdesakan pada kantong (botol) plastik, terutama jenis ikan yang mempunyai duri keras sirip yang memanjang (Gambar 1). Setiap kantong plastik diberi label kode sampling dan nomor kantong (botol). Awetan awal ini bisa disimpan dalam periode waktu antara 3 – 7 hari. Catatan: selama proses pengawetan awal, petugas harus memakai masker (penutup hidung) dan handschoen (slop tangan plastik). Formalin ialah bahan kimia yang diduga kuat bersifat karsinogenik. Petugas harus menghindari kontak langsung dengan bahan ini. Persiapan dan kegiatan petugas pada saat pengawetan awal di lapang: 1. Mempersiapkan: (i) masker dan slop tangan; (ii) bahan pengawet, formalin 10%, (iii) jarum suntik (syringe), (iv) kantong (botol plastik) untuk menyimpan sample; (v) label dan pensil untuk menulis kode sample; (vi) penggaris kayu (30 cm) dan (vii) kotak stereofoam untuk menyimpan sample; 2. Petugas mengenakan masker dan slop tangan; 3. Ikan hasil sampling harus segera dimatikan (bisa dilakukan dengan menyuntikkan formalin ke dalam organ dalam); 4. Ikan yang sudah dipisahkan segera dimasukkan ke dalam kantong atau botol plastik yang mengandung formalin 10%; 5. Perbandingan antara volume formalin dan ikan pada kantong (botol) ialah 3:1; 6. Kantong atau botol plastik harus segera ditutup rapat dan tidak bocor. Jika kantong ternyata bocor, harus segera diganti dengan kantong yang baru; 7. Setiap kantong koleksi diberi label (dengan pensil): kode sampling dan nomor botol (kode sampling sama dengan lembar sebelumnya) 8. Formalin yang tersisa harus segera ditutup rapat agar tidak mencemari lingkungan dan/atau petugas; 9. Semua kantong koleksi bersama bahan formalin disimpan pada kotak stereofoam penyimpan sample; 10. Petugas membuka slop tangan, mencuci tangan, dan membuka masker. Sisa masker dan slop tangan tidak boleh dipakai lagi, tapi disimpan pada kotak tersendiri yang terpisah dari bahan yang belum dipakai 5 Inventarisasi ikan air tawar – Refresher PEH TN-Meru Betiri, 21 – 23 Februari 2012 Gambar 1 Spesies dari Famili carangidae – pengawetan dan perlakuan specimen pada botol koleksi harus dilakukan secara hati-hati karena sirip dorsal dan anal yang rapuh (Foto oleh Choirun Nisa, Ahmad Rizal & Gede Wiadnya – Lab. IK_FPIK, 23 Oktober 2011) 5. Entry data Seluruh rangkaian kegiatan (2, 3 dan 4) dilakukan di lapang, pada setiap lokasi stasiun survei. Setelah kembali dan sampai di kantor (laboratorium), petugas harus segera mencuci semua peralatan yang digunakan untuk survei. Booties (cattle pak) bersama topi, sun glasses dan alat sampling (pencar, gill net atau perangkap) harus dicuci bersih dan kering angin sebelum disimpan (agar bisa digunakan kembali). Semua sample harus dibuka dari kotak penyimpanan, dilihat jika ada yang bocor dan disimpan pada tempat aman. Semua peralatan dan bahan yang sudah terpakai dipilah untuk dibuang pada tempat yang sesuai untuk mengurangi beban lingkungan. Sisa formalin dan anaestetik harus disimpan pada tempat yang aman (di laboratorium). Catatan: jika ada peralatan lapang yang rusak dan tidak berfungsi, petugas harus segera membuat catatan tertulis. Laporan ini akan memudahkan koordinasi petugas survei berikutnya. Terakhir, semua petugas membersihkan badan (refresh). Jika memungkinkan, setelah beristirahat secukupnya, petugas lapang harus segera memasukkan semua formulir lapang ke dalam format file di dalam computer. Jika menunggu terlalu lama, petugas akan segera lupa tentang semua tahapan yang sudah dilakukan di lapang. Rancangan penyimpanan data pada file pada computer umumnya menggunakan program worksheet Microsoft Excel atau Microsoft Access. Setelah entry data selesai, seluruh formulir lapang disimpan pada file folder (hard copy) tersendiri. Dokumen ini menjadi bukti hard copy kegiatan survei lapang. Pada saat analisis data, bisa jadi, petugas mendapatkan data-data pencilan (outliers) sebagai akibat dari kesalahan dalam proses entry data. Pada kondisi seperti ini bukti formulir (hard copy) akan sangat bermanfaat. Jika data hard copy tidak jelas, petugas analisis data bisa bertanya kepada petugas survei yang tertera pada formulir. Setelah seluruh rangkaian ini selesai, kegiatan inventarisasi ikan pada tingkat lapang bisa dianggap selesai. 6 Inventarisasi ikan air tawar – Refresher PEH TN-Meru Betiri, 21 – 23 Februari 2012 Beberapa kegiatan petugas setelah kembali dari survei sampling di lapang: 1. Membuka (unloading) seluruh bahan dan peralatan yang digunakan selama survei; 2. Mencuci alat tangkap, booties, topi dan sun glasses – semua alat dikering angin dan disimpan pada tempat yang telah ditentukan; 3. Mengisi formulir pengembalian alat dan bahan, dan membuat laporan tertulis jika ada alat yang sudah rusak. Informasi ini sangat dibutuhkan pada saat kegiatan survei selanjutnya; 4. Memeriksa kantong specimen (kebocoran) dan menyimpan di laboratorium; 5. Memeriksa bahan anaestetik dan formalin, dan menyimpan di laboratorium yang telah dipersiapkan; 6. Mengumpulkan dan membuang sisa bahan maupun alat habis pakai agar tidak merusak lingkungan di sekitarnya; 7. Mencuci kertas (wet paper) formulir survei (mengguyur dengan air bersih) dan menyimpan (setelah kering angin) – petugas membersihkan diri dan istirahat secukupnya; 8. Melakukan entry data dari formulir lapang ke dalam format computer yang telah dipersiapkan; 9. Memindahkan foto-foto hasil survei ke dalam file computer, disertai dengan caption (keterangan file foto) 10. Menyimpan formulir lapang (wet paper) ke dalam file forlder untuk dokumen hard copy; 11. Seluruh rangkaian survei lapang selesai 1. Pengawetan alcohol Setelah penyimpanan 3 – 7 hari (tergantung dari ukuran ikan), semua sample ikan harus segera dikeluarkan dari kantong plastik. Ikan-ikan yang berukuran < 15 cm umumnya memerlukan masa fiksasi sekitar tiga hari. Sedangkan ikan-ikan > 15 cm sebaiknya disimpan formalin selama tujuh hari. Penyimpanan dengan bahan formalin bisa mempertahankan warna dan daya awet dari specimen dalam waktu lama. Namun formalin relatif kurang aman dan tidak sehat bagi peneliti yang akan melakukan studi terhadap specimen. Oleh karena itu, specimen harus segera disimpan dengan menggunakan alcohol. Masing-masing specimen dikeluarkan dari kantong plastik dan dicuci dengan air mengalir selama 24 – 48 jam. Selama proses ini, petugas laboratorium harus menggunakan masker dan slop tangan. Setelah 24 jam, bau formalin pada ikan biasanya sudah hilang. Jika bau formalin masih terasa, pencucian dengan air mengalir dilanjutkan sampai 48 jam. Setiap specimen dimasukkan ke dalam larutan alcohol 95%. Setiap individu specimen diberi label dengan membuat lubang pada tutup insang sebelah kanan, ketika ikan dibuat menghadap ke kiri (dari arah petugas). Label kode specimen dituliskan pada kain keras yang dilindungi bahan kimia tekstil (pewarna agar tidak larut pada alcohol). Label kemudian diikat dengan cable TIS pada bagian tutup insang. Ketentuan kode label bisa dilakukan tanpa mengikuti prosedur museum zoology. Suatu contoh label specimen ialah: TN0101A01 – TN = specimen koleksi pertama (holotype, paratype, neotype) dari Taman Nasional Meru Betiri. 01 pada dua digit pertama menunjukkan nomor urut survei lapang. 01 pada dua digit 7 Inventarisasi ikan air tawar – Refresher PEH TN-Meru Betiri, 21 – 23 Februari 2012 kedua ialah nomor stasiun pada survei. A = kode botol specimen, dan 01 pada dua digit terakhir menunjukkan nomor ikan pada botol koleksi A (jika terdapat lebih dari satu ikan dalam satu botol koleksi). Label ini harus bisa diurut secara konsisten dengan formulir survei lapang. Oleh karena itu, formulir survei lapang harus mempunyai label yang sama (TN0101A). Formulir dengan kode ini mengandung seluruh keterangan survei, termasuk foto-foto yang menggambarkan lokasi survei. Tata urutan pada kegiatan pengawetan alcohol ialah sebagai berikut: 1. Mempersiapkan botol koleksi (kaca) specimen, larutan alcohol 95%, bak (plastik) perendaman sample dan kran air mengalir; 2. Mengenakan masker, kaca mata dan slop tangan – ikan diambil dari dalam botol koleksi lapang dan dimasukkan ke dalam bak perendaman. Catatan: ikan dari dalam satu botol sample tidak boleh tertukar dengan ikan dari botol sample lainnya. Kran air dibuka agar terjadi pertukaran air yang cukup ke dalam bak; 3. Setelah 24 jam, semua ikan dikeluarkan dari dalam bak dan diletakkan pada tray atau nampan. Petugas tidak lagi menggunakan masker – jika masih terasa bau formalin, perendaman dilanjutkan sampai 48 jam. Petugas tidak boleh tinggal terlalu lama di dalam laboratorium. Hal ini bisa mengurangi sensitivitas terhadap bau formalin; 4. Petugas membuat label pada kain keras dan melobangi tutup insang bagian kanan ketika specimen menghadap ke kiri dari arah petugas. Label kain keras diikatkan pada lobang tutup insang; 5. Ikan dimasukkan ke dalam botol yang sudah berisi larutan alcohol 95%. Perbandingan antara larutan alcohol dan ikan ialah 3:1., dan semua ikan (specimen) harus terendam pada larutan pengawet. 6. Setiap botol diberi label (bisa dibuat dari kertas) yang ditempel dengan tape (pelindung). Catatan: alcohol ialah bahan kimia yang mudah menguap, walaupun botol sample sudah ditutup rapat. Petugas harus melakukan pemeriksaan secara berkala jika alcohol pada botol sudah berkurang (untuk ditambahkan larutan yang baru); 7. Setiap botol specimen disimpan pada tempat yang aman dan mulai saat itu specimen bisa dipelajari untuk kepentingan taksonomi maupun studi lainnya (bio-geografi) 7. Material Transfer Agreement (MTA) Keberhasilan inventarisasi dimulai dari sistem penamaan yang benar atau correct naming. Penamaan yang benar biasanya dilakukan melalui konfirmasi oleh taksonomist dari LIPI atau ahli yang credible. Sering kali, taksonomist tersebut tidak tersedia pada kondisi lokal. Terkait dengan usaha pemberian nama, specimen sering harus dipindah tangan (dipinjamkan) untuk sementara. Pemindahan specimen harus disertai dengan copy dokumen tentang survei, termasuk foto-foto pada saat kegiatan lapang. Hal ini akan membantu taksonomist dalam melakukan identifikasi. Ketentuan lebih lanjut mengenai MTA diatur oleh instansi pemilik specimen. 8 Inventarisasi ikan air tawar – Refresher PEH TN-Meru Betiri, 21 – 23 Februari 2012 8. Identifikasi specimen 8.1. Jumlah spesies ikan di dunia Hampir semua ahli dan pakar menyatakan bahwa ikan ialah termasuk kelompok vertebrata dengan anggota kelompok paling tinggi (Nelson, 2006; Carpenter & Niem, 1998). Jumlah total spesies ikan di dunia yang sudah tercatat sampai penemuan sebelum tahun 2004 mencapai 28.506 spesies (Froese & Pauly, 2011). Jumlah total spesies ikan yang ditemukan di dalam wilayah perairan Indonesia mencapai 4.161 spesies, terdiri dari 1.125 spesies ikan air tawar dan 3.240 jenis ikan laut. Indonesia diduga kuat mempunyai jumlah spesies ikan terbanyak di dunia. Jumlah total spesies ikan air tawar dari Brazil termasuk 2x lebih banyak dibandingkan spesies yang ada di Indonesia. Namun kenyataan di lapang bisa saja terjadi sebaliknya. Hutan hujan tropis Amazon pernah mendapat predikat sebagai paru-paru dunia. Icon atau label ini telah membuat Lembah Amazon diidentifikasi sebagai wilayah strategis untuk dilindungi. Sebagai akibatnya, dana-dana dari lembaga internasional memberikan dukungan yang kuat dan jumlah studi di sana jauh lebih intensif dibandingkan di Indonesia. Jumlah total spesies ikan yang ditemukan di Indonesia sedikit lebih banyak dibandingkan dengan ikan-ikan yang ditemukan di Australia. Namun, penelitian tentang yang dilakukan di Benua Asutralia mungkin 100x lebih banyak dibandingkan dengan di Indonesia. Tambahan lagi, mereka mempunyai ahli, fasilitas, informasi dan jejaring yang jauh lebih luas dan lebih berkembang – Gerald Allen, ahli ikan karang yang sering melakukan penelitian ikan di Indonesia, berasal dan menetap di Australia. Artinya, spesies ikan-ikan di Indonesia kemungkinan besar akan jauh lebih banyak dibandingkan yang sudah dilaporkan saat ini – ikan dan perairan kita jauh lebih banyak dari yang kita ketahui saat ini. Tabel 1. Jumlah total spesies ikan (laut dan tawar) yang telah berhasil ditemukan pada 10 negara di dunia (Sumber: Forese & Pauly, 2011) NO NEGARA SPESIES LAUT SPESIES TAWAR TOTAL SPESIES 1 Brazil 1.019 2.359 3.318 2 Amerika Serikat (semua bagian) 2.137 924 2.935 3 Australia 3.888 381 4.110 4 Filipina 2.794 361 2.993 5 Papua New Guinea 2.425 397 2.653 6 Afrika Selatan 1.894 214 2.019 7 Thailand 816 726 1.439 8 Malaysia 1.080 599 1.568 9 Belanda 166 70 210 3.240 1.125 4.161 10 Indonesia Sumber: Froese & Pauly, 2011 9 Inventarisasi ikan air tawar – Refresher PEH TN-Meru Betiri, 21 – 23 Februari 2012 8.2. Metode dalam Identifikasi Ikan Identifikasi ikan sudah dipastikan ialah pekerjaan yang sangat sulit dan hanya bisa dilakukan oleh ahli yang sangat berpengalaman pada bidangnya (fish taxonomist). Proses dan pendekatan dalam identifikasi bisa dilakukan melalui dua metode – A PRIORI ialah metode identifikasi yang dilakukan tanpa melalui pengukuran atau eksperimen terhadap specimen. Hal ini biasa dilakukan oleh ahli atau berpengalaman terhadap ikan-ikan lokal. Metode apriori juga dilakukan pada kondisi tidak memungkinkan untuk melakukan metode lainnya. Melakukan sensus ikan laut/karang pada habitat terumbu karang umumnya dilakukan dengan metode apriori. Setiap penyelam (peneliti) harus mempunyai pengalaman dan waktu selam yang cukup tinggi untuk bisa melakukan identifikasi ikan secara cepat dan tepat – ikan yang terlihat oleh penyelam sering kali tidak lebih dari 10 – 15 detik, sebelum ikan tersebut berpindah atau pergi menghindar dari penyelam. Kedua, marker atau tanda khusus pada ikan bisa berbeda di dalam air dibandingkan kalau dilihat di atas permukaan. Penyelam berpengalaman sering menggunakan kebiasaan tingkah laku ikan untuk mengidentifikasi spesies. Pendekatan kedua dalam proses identifikasi disebut A POSTERIORI. A posteriori ialah proses identifikasi dan klasifikasi ikan yang dilakukan melalui proses eksperimen secara kuantitatif. Metode ini lebih pasti dalam menentukan suatu spesies, walaupun metodenya tidak lebih mudah dari pendekatan sebelumnya. Metode identifikasi a posteriori umumnya menggunakan dua sistem, ialah sistem morfometri dan meristik dan yang kedua ialah sequencing DNA. Morfometri ialah sistem identifikasi dengan mengetahui bentuk-bentuk luar dari ikan, seperti: posisi mulut, bentuk badan, bentuk sirip ekor, jenis sisik, posisi sirip dada dan tanda-tanda lain seperti warna (marker). Meristik ialah mempelajari ikan dengan menghitung jumlah bagian-bagian tubuh, seperti: jumlah duri keras pada sirip punggung, jumlah sisik pada gurat sisi, jumlah duri lunak pada sirip anus, jumlah baris pada gidi, jumlah gill racker dan jumlah organ tubuh yang penting lainnya. Proses ini memerlukan pengetahuan tentang definisi organ tubuh ikan yang sering menggunakan bahasa latin (pada daftar referensi, terdapat fish dictionary yang bisa dipelajari lebih lanjut). Setiap organisme (spesies) mempunyai susunan basa-basa tertentu pada anak inti sel maupun sitoplasma. Sususnan basa-basa ini di-sequencing untuk mengetahui jenis atau spesies dari ikan uji. Namun pendekatan ini tidak dibahas lebih lanjut dalam teks. 8.3. Karakteristik Morfometri Bentuk-bentuk badan ikan secara normative sangat sulit untuk dijadikan pembeda antara spesies ikan yang satu dengan lainnya – bentuk badan antara lain termasuk: oval, segi-empat, lonjong, kompres (pipih vertical), depress (pipih lateral), elongate (memanjang), fusiform (seperti cerutu) dan lain-lain. Pengetahuan tentang istilah-istilah tersebut tentu saja belum cukup untuk menentukan atau membuat klasifikasi ikan berdasarkan spesies. Bentuk badan oval antara spesies satu dengan spesies berdekatan akan sangat sulit dibedakan. Para taksonomist kemudian mengembangkan suatu metode yang disebut dengan TRUSS MORFOMETRI. Truss morfometri ialah metode pembandingan antara ukuran-ukuran tubuh bagian penting dari ikan dengan satu ukuran yang dianggap standar. Panjang kepala dan panjang standar ialah dua variable yang sering digunakan untuk menentukan spesies ikan. Sebagai contoh, perbandingan antara panjang standar dengan tinggi badan akan menentukan bentuk badan dari ikan. Keterangan berikut ialah beberapa contoh definisi yang sering digunakan untuk menentukan spesies ikan. 10 Inventarisasi ikan air tawar – Refresher PEH TN-Meru Betiri, 21 – 23 Februari 2012 Gambar 2. Penentuan posisi landmark untuk menentukan korfometri dan bantuk tubuh ikan sebagai penanda dalam proses identifikasi yang biasa dilakukan oleh taksonomist (Abraham et al., 2011; Chakarbarty & Sparks, 2007; Chakrabarty et al., 2010) Fork Length (FL) – panjang fork, ialah jarak dari ujung mulut paling depan (point-1) sampai titik fork (cagak paling dalam) dari sirip ekor (point-16) Standard Length (SL) – panjang baku, ialah jarak antara ujung mulut paling depan atau anterior (point-1) sampai akhir vertebral column atau hypural plate (point-6; akhir plate didapat dengan membengkokkan sirip ekor secara lateral) (Coad & McAllister, 2007; Carpenter & Niem, 1999) Body depth (BD) – tinggi maksimum (garis lurus) dari badan secara vertical. BD dicari dengan menggeser vernier caliper untuk mendapatkan jarak lurus (vertical) yang maksimum (tidak termasuk sirip, sisik atau bagian daging dari sirip dorsal atau anal) Dorsal Body Depth (DBD) – tinggi badan dorsal, ialah garis lurus vertical yang diukur dari bagian anterior sirip dorsal atau punggung (point-3) ke arah perut (ventral) Anal Body Depth (ABD) – tinggi badan anal, ialah garis lurus vertical yang diukur dari bagian anterior sirip anal atau dubur (point-9) ke arah punggung (dorsal) Head Length (HL) – panjang kepala, ialah jarak dari ujung mulut paling depan atau anterior (point-1) sampai tepi paling akhir tulang tutup insang atau opercle, tidak termasuk opercular membrane (point-17) Snout Length (SNL) – panjang moncong (hidung), ialah jarak dari ujung depan mulut (point-1) sampai tepi depan (bagian tengah) tulang pelindung mata atau orbit (point13) 11 Inventarisasi ikan air tawar – Refresher PEH TN-Meru Betiri, 21 – 23 Februari 2012 Orbit Diameter (OD) – Diameter Orbit, ialah diameter maksimum diantara tulang pelindung mata, jarak ini tidak selalu horizontal (point-13 dengan point-14) Postorbital Length (POL) – Panjang Postorbital, ialah jarak terpanjang antara tulang tutup mata bagian belakang (point-14) dengan tepi tulang tutup insang atau opercle (point-17) Predorsal Length (PDL) – panjang predorsal, ialah jarak dari ujung depan dasar sirip dorsal (point-3) sampai ujung mulut bagian paling depan atau anterior (point-1) Prepelvic Length (PVL) – panjang prepelvic, ialah jarak dari ujung anterior dasar sirip perut atau pelvic (point-10) sampai ujung mulut bagian paling depan atau anterior (point-1) PrePectoral Length (PPL) – panjang prepectoral, ialah jarak dari dasar sirip dada atau pectoral (point 15) sampai ujung mulut bagian paling depan atau anterior (point-1) Preanal Length (PAL) – panjang preanal, ialah jarak dari ujung anterior dasar sirip anal (point-9) sampai ujung mulut bagian paling depan atau anterior (point-1) Caudal Peduncle Length (CPL) – jarak dari akhir sirip anal (point-8) sampai akhir dari hypural plate (point-6) Caudal Peduncle Depth (CPD) – tinggi caudal peduncle, ialah jarak terpendek di wilayah caudal peduncle (diukur sebagai garis lurus vertical) Dorsal Fin Base (DFB) – dasar sirip dorsal, ialah panjang lurus dari dasar duri keras paling depan (point-3) sampai bagian akhir duri lunak yang menopang sirip dorsal (point-4) Anal Fin Base (AFB) – dasar sirip anal, ialah panjang lurus dari dasar duri keras paling depan (point-9) sampai akhir duri lunak yang menopang sirip anal (point-8) Dorsal Fin Length (DFL) – panjang sirip dorsal, ialah jarak terpanjang dari dasar duri sirip sampai bagian ujung, diukur pada duri sirip terpanjang Anal Fin Length (AFL) – panjang sirip anal, ialah jarak terpanjang dari dasar duri sirip sampai bagian ujung, diukur pada duri sirip terpanjang Pectoral Fin Length (PFL) – panjang sirip dada atau pectoral, ialah jarak terpanjang dari dasar duri sirip sampai bagian ujung, diukur pada duri sirip terpanjang Ventral Fin Length (VFL) – panjang sirip perut atau ventral, ialah jarak terpanjang dari dasar duri sirip sampai bagian ujung, diukur pada duri sirip terpanjang 8.4. Beberapa Kunci dalam Strategi Identifikasi Specimen Tabel 2 menyajikan urutan jumlah spesies dari 20 Famili yang berbeda serta habitat utama dari berbagai ikan yang tersebar di dunia. Cyprinidae ialah Famili yang paling penting untuk diketahui atau dipelajari untuk identifikasi spesies ikan air tawar. Famili Cyprinidae termasuk Famili dengan jumlah spesies paling banyak dan semuanya hidup di perairan tawar, sebagian bisa menempati wilayah air payau. Namun tidak ada anggota Famili Cyprinidae yang hidup di laut. Masalahnya, ikanikan dari Famili ini sangat sulit untuk diidentifikasi satu sama lain. Dia mempunyai ukuran dari panjang 300 cm (Catlocarpio siamensis), namun banyak yang mempunyai ukuran < 5 cm. Famili kedua yang terpenting ialah Chiclidae (kelompok ikan mujaer dan nila). Ikan ini biasa hidup pada wilayah perairan rawa, dataran rendah dan airnya relatif tenang. Kelompok selanjutnya ialah Gobiidae. Ikan-ikan dari kelompok ini relatif sulit dikenali karena ukurannya yang relatif kecil. 12 Inventarisasi ikan air tawar – Refresher PEH TN-Meru Betiri, 21 – 23 Februari 2012 Tabel 2 Jumlah spesies dari 20 Famili (tersusun dari urutan spesies terbanyak) yang tersebar pada seluruh perairan di dunia (Froese & Pauly, 2011) No 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 Famili Cyprinidae Cichlidae Gobiidae Characidae Loricariidae Balitoridae Serranidae Labridae Macrouridae Blenniidae Pomacentridae Apogonidae Liparidae Ophichthidae Poeciliidae Jml Spesies 2.408 1.451 1.410 1.002 688 601 500 479 383 370 360 333 324 296 294 Habitat utama: Air tawar & payau Air tawar & payau Sebagian besar laut & payau, namun banyak yang tawar Air tawar, lebih umum Benua Amerika Air tawar Air tawar Laut & payau - jarang air tawar Laut Laut Terutama laut, jarang payau atau tawar Laut dan payau Terutama laut, beberapa payau, jarang tawar Laut Terutama laut, beberapa sampai ke sungai Air tawar dan payau Tabel 3 Jumlah jenis ikan berdasarkan Famili yang ditemukan pada beberapa wilayah perairan di Indonesia NO 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 13 FAMILY Cyprinidae Gobiidae Bagridae Eleotridae Ambassidae Chanidae Clariidae Mugilidae Osphronemidae Poeciliidae Sisoridae Anguillidae Balitoridae Carangidae Cichlidae Gerreidae Leiognathidae Lutjanidae Siganidae Tetraodontidae Anabantidae Aplocheilidae Apogonidae Aceh 26 10 6 6 5 4 4 4 4 3 3 2 2 2 2 2 2 2 2 2 1 1 1 B. Solo D. Toba Muara Enim 15 2 1 4 1 1 1 1 1 1 2 14 1 1 1 2 2 2 2 1 1 Inventarisasi ikan air tawar – Refresher PEH TN-Meru Betiri, 21 – 23 Februari 2012 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 Ariidae Engraulidae Haemulidae Hemiramphidae Kuhliidae Loricariidae Megalopidae Microdesmidae Monodactylidae Mullidae Muraenidae Paralichthyidae Scatophagidae Serranidae Siluridae Synbranchidae Syngnathidae Terapontidae 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 114 1 1 Penelitian terhadap ikan-ikan yang ditemukan pada wilayah perairan tawar di Aceh mendapatkan paling tidak 41 Famili. Famili terbanyak ialah Cyprinidae, diikuti oleh Gobiidae, Bagridae, Eleotridae dan Ambassidae. Famili Bagridae secama umum relatif dekat atau mirip dengan ikan-ikan dari Famili Ariidae. Nama umum dari ikan-ikan Famili ini ialah Bagrid Catfish. Famili Eleotridae disebut juga ikan-ikan mud-sleeper. Ikan-ikan kelompok ini umumnya berukuran kecil (5 cm) dan sering tinggal pada tempat-tempat yang berlumpur. Indonesia memiliki 438 spesies ikan air tawar yang endemic, dari total 1.125 spesies yang sudah ditemukan. Dari total spesies endemic, 82 spesies (19%) berasal dari ikan-ikan Famili Cyprinidae. Famili dengan spesies endemic cukup tinggi setelah Cyprinidae ialah Osphronemidae (48 spesies), Melanotaeniidae (32 spesies) dan Bagridae (28 spesies). Dalam kegiatan identifikasi ikan, sangat sulit untuk melakukannya secara cepat dan praktis. Berikut ialah urutan petunjuk yang mungkin akan bermanfaat atau bisa membantu: Perhatikan cirri khas dari beberapa Famili penting untuk air tawar, seperti: Cyprinidae, Bagridae, Gobiidae, Eleotridae, Adrianichthyidae, Balitoridae dan Ambassidae. Ikan-ikan dari Famili Clariidae (lele), Osphronemidae (gurami & sepat & tambakan), Chiclidae (mujaer & nila) termasuk relatif mudah dikenali. Gunakan petunjuk dari Nelson (2006) – buku ini tersedia melalui pdf file secara terpisah dari teks; Ketika melakukan sampling, tanyakan nama lokal dari setiap ikan dalam sample. Karena ketua regu mempunyai koneksi yang luas dengan masyarakat di sekitar lokasi, hal ini relatif bisa dilakukan. Coba cari nama lokal tersebut dalam daftar FishBase – Program FishBase2004 (software) tersedia dalam 5 DCROM (terpisah dari teks). Anda bisa install program tersebut dengan license dari FPIK-UB. Catatan: instalasi program FishBase2004 memerlukan kapasitas tambahan pada hard disk setara sekitar 6 GB. Laptop atau Desk Top harus dipersiapkan untuk kebutuhan ruang ini; Schuster & Djajadiredja (1952) ialah satu-satunya (mungkin) buku yang membuat nama lokal (dihubungkan dengan nama ilmiah) dari ikan-ikan yang ditemukan di Indonesia. Buku tersebut tersedia dalam bentuk hard copy di Fakultas Perikanan. Anda bisa mendapatkan 14 Inventarisasi ikan air tawar – Refresher PEH TN-Meru Betiri, 21 – 23 Februari 2012 copy dari buku tersebut jika diperlukan (usaha untuk memindahkan kedalam bentuk file pdf belum dilakukan). Weber & de Beaufort (1931) ialah buku 11 seri yang mencatat ikan-ikan yang ditemukan di wilayah Indo-Australia. Buku tersebut tersedia di ruang baca FPIK-UB (bentuk hard copy). Buku ini bisa membantu untuk menelusuri kemungkinan ikan sampai tingkat genus. Menelusuri daftar ikan-ikan yang sudah ditemukan di Indonesia, mencari foto dari ikan tersebut dalam FishBase2004 dan melakukan penelusuran melalui foto-foto yang tersedia. Internet juga akan sangat membantu. Tabel 4 jumlah spesies ikan air tawar endemic (per Famili) yang ditemukan di Indonesia NO FAMILY 1 Cyprinidae 2 Osphronemidae 3 Melanotaeniidae 4 5 6 7 8 Bagridae Hemiramphidae Balitoridae Telmatherinidae Eleotridae 9 10 11 12 13 14 15 16 17 18 19 20 Adrianichthyidae Akysidae Siluridae Clariidae Cobitidae Gobiidae Pangasiidae Sisoridae Ambassidae Sundasalangidae Ariidae Channidae Jml Spesies 82 48 32 28 24 22 17 15 14 14 13 12 8 8 7 7 5 5 4 3 Beberapa petunjuk di atas belum tentu bisa membantu secara tuntas untuk identifikasi ikan – ingat: ikan ialah kelompok vertebrata dengan jumlah spesies yang paling besar dan tinggal pada habitat di luar kelompok vertebrata lainnya. Mudah-mudahan beberapa petunjuk tersebut bisa membantu. Seandainya tidak bisa, mari kita melakukan diskusi, saling menukar specimen dan saling berbagi. TERIMAKASIH Daftar Pustaka Abraham, K. J., K.K. Joshi, & V.S.R. Murty (2011). "Taxonomy of the fishes of the family Leiognathidae (Pisces, Teleostei) from the West coast of India." Zootaxa 2886: 1-18. Hoese, D.F. and M. Kottelat 2005. Bostrychus microphthalmus, a new microphthalmic cavefish from Sulawesi (Teleostei: Gobiidae). Ichthyol. Explor. Freshwat. 16(2):183-191. Kottelat, M., 1995. Four new species of fishes from the middle Kapuas basin, Indonesian Borneo (Osteichthyes: Cyprinidae and Belontiidae). Raffles Bull. Zool. 43(1): 51-64. 15 Inventarisasi ikan air tawar – Refresher PEH TN-Meru Betiri, 21 – 23 Februari 2012 Kottelat, M. and A.J. Whitten., 1996. Freshwater fishes of Western Indonesia and Sulawesi: additions and corrections. Periplus Editions, Hong Kong. 8 p. Kottelat, M. and E. Widjanarti 2005 The fishes of Danau Sentarum National Park and the Kapuas Lakes area, Kalimantan Barat, Indonesia. Raffles Bull. Zool. Supplement (13):139-173. Kottelat, M. and P.K.L. Ng. 1994. Diagnoses of five new species of fighting fishes from Banka and Borneo (Teleostei: Belontiidae). Ichthyol. Explor. Freshwat. 5(1):65-78. Kottelat, M., A.J. Whitten, S.N. Kartikasari and S. Wirjoatmodjo. 1993. Freshwater fishes of Western Indonesia and Sulawesi. Periplus Editions, Hong Kong. 221 p.; Nelson, J. S. (2006). Fishes of the world. New Jersey, USA., John Wiley & Sons. Ng, H.H. 2001. <i>Clarias microstomus</i>, a new species of clariid catfish from Eastern Borneo (Teleostei: Siluriformes). Zool. Stud. 40(2):158-162. Ng, H.H. 2003 Clarias insolitus, a new species of clariid catfish (Teleostei: Siluriformes) from southern Borneo. Zootaxa 284:1-8. Page, L.M., R.K. Hadiaty, J.A. López, I. Rachmatika and R.H. Robins 2007 Two new species of the Akysis variegatus species group (Siluriformes: Akysidae) from Southern Sumatra and a redescription of Akysis variegatus Bleeker, 1846. Copeia 2:292-303. Parenti, L.R. and B. Soeroto 2004 Adrianichthys roseni and Oryzias nebulosus, two new ricefishes (Atherinomorpha: Beloniformes: Adrianichthyidae) from Lake Poso, Sulawesi, Indonesia. Ichthyol. Res. 51:10-19. Roberts, T.R. 1989. The freshwater fishes of Western Borneo (Kalimantan Barat, Indonesia). Mem. Calif. Acad. Sci. 14:210 p. Schuster, W. H., & R.R. Djajadiredja (1952). Local common names of Indonesia fishes. Bandung, W. van Hoeve. Sudarto, G.G. Teugels and L. Pouyaud. 2003. Description of two new <i>Clarias</i> species from Borneo (Siluriformes, Clariidae). Cybium 27(2):153-161. Tan, H.H. and H.H. Ng. 2000. The catfishes (Teleostei: Siluriformes) of central Sumatra. J. Nat. Hist. 34:267-303. Tan, H.H. and M. Kottelat., 1998. Redescription of <i>Betta picta</i> (Teleostei: Osphronemidae) and description of <i>B. falx</i> sp. n. from central Sumatra. Rev. Suisse Zool. 105(3):557568. Tan, H.H. and M. Kottelat. 1998. Two new species of <i>Betta</i> (Teleostei: Osphronemidae) from the Kapuas Basin, Kalimantan Barat, Borneo. Raffles Bull. Zool. 46(1):41-51. Tan, H.H. and P.K.L. Ng 2005 The labyrinth fishes (Teleostei: Anabantoidei, Channoidei) of Sumatra, Indonesia. Raffles Bull. Zool. Supplement (13):115-138. Tan, H.H. and P.K.L. Ng 2006 Six new species of fighting fish (Teleostei: Osphronemidae: Betta) from Borneo. Ichthyol. Explor. Freshwat. 17(2):97-114. Tan, H.H. and S.H. Tan. 1994. <i>Betta miniopinna</i>, a new species of fighting fish from Pulau Bintan, Riau Archipelago, Indonesia (Teleostei: Belontiidae). Ichthyol. Explor. Freshwat. 5(1):41-44. 16 Inventarisasi ikan air tawar – Refresher PEH TN-Meru Betiri, 21 – 23 Februari 2012