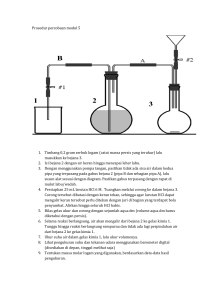
preparasi sampel
advertisement

4 SKS ( 2 /0/2) PUSTAKA : Fundamentals of anlytical chemistry , Skoog, west and Holler. A text book of Macro and Semimicro Qualitative Inorganic Analysis. Vogel. Quantitative Analysis, Day and Underwood TAHAPAN ANALISA 1. Difinisi masalah Merencanakan analisa, mempertimbangkan proses dimana informasi analitik itu diperlukan. Pemilihan metodeSesuai dengan informasi yang diperlukan. 2. SamplingPenseleksian dan mengambil sejumlah kecil sampel yang representatif. 3. Perlakuan awal sampel dan Pemisahan yaitu mengubah ke dalam bentuk yang sesuai untuk di analisa. Tahapan ini mungkin memerlukan/tidak proses pemisahan. 4. Pengukuranmendapatkan data analisa yang mentah (asli) dari pengukuran pada perlakuan sampel. 5. Kalibrasi mendapatkan data analisa asli dari standar yang disediakan. 6. Evaluasi mengevaluasi data yang diperoleh dari pengukuran dan kalibrasi. 7. Aktionmenganalisa hasil untuk memutuskan apakah pekerjaan ini sesuai dengan masalah yang diberikan. EFISIENSI ANALISA Metode analisa dipilih sesuai dengan tujuan analisa serta pretreatment (perlakuan awal ) sampel singkat dan sederhana. Membandingkan 2 metode dengan memilih salah satu yang lebih baik. Tahapan perlakuan awal yg harus dipertimbangkan: Hasil analisa harus akurasi dan reliability. Jumlah total waktu analisa yg diperlukan. Jumlah minimum perlakuan awal sampel. PERSIAPAN PERLAKUAN SAMPEL Grinding sampel padat 1. Buat ukuran butiran yg sesuai (di ayak dengan ayakan yang berukuran (sieve). Angka mesh dalam ayakan berarti diameter dari lubang dalam ayakan, angka mesh tinggi berarti diameter partikelnya kecil. Alat yang digunakan: -Diamond mortar, terbuat dari baja ( sampel yg sangat keras, dan rapuh) -Ball Mill , terbuat dari porselin (sampel yang brittle/ lunak). Untuk sampel yg tidak brittle (pada temperatur ruang) seperti plastik & karet, maka sampel didinginkan & dialiri udara nitrogen cair. Preparasi sampel untuk analisa keadaan padat. analisa dengan mikroskop, X-ray fluoresens spectroskopi, spektroskopi emisi,spektroskopi IR. 2. Preparasinya: Cutting /Memotong dengan pisau yg sesuai (microtome). Polishing /Menghaluskan / memoles permukaan sampel (x-Ray fluoresens). Compression dalam bentuk disc (IR) Casting of thin film. Untuk plastik dan polimer (termoplastik) untuk IR dan x_ray. Chill-casting, sampel dilebur dalam furnace lalu dcetak dalam bentuk yg sesuai, didinginkan (spektroskopi emisi) 3. Pengeringan sampel • Sampel biologi : oven pada suhu ~100° , catat berat sampel yg hilang. • Vakum desikator dan freeze drying: untuk sampel yg sensitiv panas dibekukan lalu dikeringkan dalam keadaan beku (kondisi vakum) • Simpan sampel dalam desikator, sebelum analisa cek kembali berat sampel. Leaching (melepaskan) dan ekstraksi (mengambil) komponen dari sampel padat. 4. • Leaching: mengambil satu atau lebih komponen sampel dalam bentuk larutan melalui reaksi kimia dari sampel padat. Larutan tsb kemudian dipisahkan dari fase padat melalui penyaringan. • Leaching senyawa logam yg larut dari tanah => dilarutkan dengan : air , asam encer, larutan buffer larutan berair dari zat pengomplek logam organik. • Ekstraksi senyawa organik yg larut dari matrik yg tak larut (plastik atau karet) mengocok sampel dg pelarut dan menyaring, atau refluks sampel dg pelarut panas, atau ekstraksi dg soxhlet. 5. Penyaringan - Untuk memisahkan partikel padat tersuspensi (suspended solid), karena: - Dapat mengganggu analisa ( memecahkan sinar dalam larutan pada spektrometry, atau menyumbat nebulizer pada AAS) - Untuk menghitung total suspended solid pada analisa air. Dekomposisi dan pelarutan padatan anorganik 1. Sampel dalam bentuk larutan digunakan untuk analisa: Gravimetri, Titrimetri, Spektrofotometri, Spektrofluorometri, Flame emisi, AAS, Fluoresensi atom, Emisi plasma, Elektroda ion selektif Polarografi, Elektrogravimetri, Coulometri, Kromatografi ion, Kromatografi kertas, KLT, Elektroforesa, Analisa isotop 2. Sampel dalam bentuk padat atau larutan digunakan untuk: Analisa aktivasi dan Analisa x-ray 3. Sampel dalam bentuk padat digunakan untuk: Spektroskopi emisi DC arc, Spektroskopi emisi AC spark, Teknik microprobe, Teknik pembakaran Dissolution/ pelarutan sampel langsung diubah dalam bentuk larutan tanpa perubahan kimia. Opening out mengubah sampel kedalam bentuk kimia yg berbeda tetapi masih dalam bentuk padatan, lalu dilakukan proses pelarutan. Contoh : - Sampel kawat kuningan dipanaskan dengan larutan HNO3 1 : 1 sampai larutan jernihDissolution - Sampel silikat yg tak larut dipanaskan dengan Na2CO3 berlebih sampai meleleh jernih, lalu didinginkan (jadi keras), dilarutkan dengan HCl encerOpening-out - Sampel ferrosilikon diperlakukan dengan campuran larutan HNO3 + HF, dipanaskan /dikeringkan , lalu ditambah larutan HNO3 + H2O2 hingga larutan jernihDissolution TEKNIK PELARUTAN I. Pelarutan sederhana tanpa reaksi kimia Digunakan air/pelarut berair / buffer tetapi tidak terjadi reaksi kimia. Pelarut tidak boleh menginterferensi analisis kemurnian tinggi, hilangnya analat dapat diminimalisir, tidak bereaksi dengan wadah (adsorpsi/ absorpsi), larut sempurna dan prosedurnya cukup aman. II. Dekomposisi dan pelarutan sampel dengan asam A. Penggunaan asam encer. Jika sampel tak larut dalam air, maka dilarutkan dalam asam encer : logam yg lebih elektropositif dari pada H (potensial reduksi positif berarti logam tsb lebih elektronegatif dibanding H, sebagai reduksi dan reaksi berjalan spontan) , serta yang berbentuk oksida logam, karbonat, sulfida, misalnya logam Zn, MgO, CaCO3 dan FeS larut dalam HCl. Pada proses pelarutan, biasanya anion diubah menjadi bentuk volatil dan hilang sebagai gas (CO2 dan H2S). Logam Al dan Cr menjadi passive dengan adanya asam, karena terbentuk lapisan film tipis pada permukaan logam , sehingga mencegah reaksi dengan asam Asam encer bereaksi dengan sampel dalam cara lainnya dari pada sebagai asam sederhana. Misal logam Cu dan Ag lebih larut dalam HNO3 (1:1) dari pada dalam HCl. Sebagai zat pengoksidasi, HNO3, akan mengoksidasi CuCu2+, dan HNO3 mengalami reduksi : HNO3H2O, NO,NO2. B. Penggunaan asam pekat panas. Jika pemakaian asam encer tidak dapat melarutkan semua sampel, maka dapat diganti dengan asam pekat panas’ Sampel dididihkan dengan asam dalam beker yang ditutupi kaca arloji sampel dididihkan dengan asam secara refluks. Sampel dididihkan dengan asam dan diikuti dengan penguapan sampai hampir kering (dryness). Penambahan lebih dari jenis asam dapat dilakukan. Penggunaan teknik bomb. Asam pekat panas dapat melarutkan logam yang kurang elektropositif, alloy (stainless steel), oksida logam, sulfida, fosfat dan silikat. Jenis asam pekat yang dipakai untuk pelarutan: HCl (12 M) Jika dididihkan, gas HCl akan lepas dan TD akan naik sampai campuran azeotrop terbentuk (HCl 6M, TD=109oC). Beberapa logam klorida larut dalam air, kecuali Hg2Cl2, AgCl dan TiCl, sedang PbCl2 sedikit larut dalam air dingin tetapi larut dalam air panas. HCl melarutkan logam yang lebih elektropositif, bentuk oksida serta hidroksidanya. HCl melarutkan beberapa fosfat, borat, karbonat dan sulfida. campuran azeotrop : campuran cairan ketika titik didihnya menghasilkan komposisi uap = cairannya. Titik didih campuran azeotrop pada tekanan tetap adalah konstan. Komponen campuran azeotrop tidak dapat dipisahkan oleh destilasi. HNO3.65-69%. HNO3 dalam campuran azeotrop dengan air terbentuk pada HNO3 67% dengan TD 1210C, walaupun ini memungkinkan untuk mendapatkan asam pekat lebih sampai 100%, Td 830C. HNO3 adalah asam kuat dan zat pengoksidasi paling kuat, dapat mengoksidasi semua logam kecuali logam mulia, dan melarutkan sedikit logam Al, Cr, Ti, Nb dan Ta. Logam-logam tsb menjadi pasif dengan adanya asam. Semua logam nitrat larut dalam air, ion nitrat adalah ion pengompleks yang sangat lemah. Beberapa ion logam dihidrolisa dalam larutan asam nitrat, menghasilkan endapan oksida hidrat, contohnya Sn, W dan Sb. H2SO4 98% TD 3300C (TD nya paling tinggi), dapat digunakan pada suhu tinggi untuk proses pelarutan, termasuk asam kuat dan zat pengoksidasi kuat ketika dipanaskan. Dapat menghancurkan bahan organik. Logam sulfat larut dalam air kecuali CaSO4 (sedikit), SrSO4, BaSO4 dan PbSO4. Keuntungan logam sulfat adalah volatilitasnya rendah. H2SO4 dapat menghilangkan HF dari matriks oleh penguapan hingga mendekati kering logam fluorida membentuk logam sulfat dan melepaskan HF. Melarutkan semua logam kecuali logam mulia dan alloy seperti beberapa oksida, hidroksida, karbonat, sulfida dan biji arsen serta beberapa senyawa lainnya. Pemakaian pada TD>3300C dapat dilakukan dengan teknik bomb, atau dengan menambah Na2SO4, K2SO4 atu (NH4)2SO4. HClO4 60 -72% Bentuk azeotrop dengan air (72% dan TD 2030C), jika panas, sangat ekstrem sebagai zat pengoksidasi dan dapat melarutkan semua logam kecuali logam mulia dan alloy serta mengubah bentuk ionnya dengan bilok paling tinggi. Semua logam perklorat larut dalam air kecuali KClO4, RbClO4 dan CsClO4. Hati-hati pada pemakaian dalam kondisi panas dan pekat, karena bersifat explision hazard. Cara penanganan yang baik: • jangan menggunakan pada konsentrasi di atas 72%. • jangan gunakan pemanasan asam pekat dengan zat yang mudah dioksidasi. • jika menguapkan asam perklorat, kerjakan pada wadah khusus yg tidak dibuat dari bahan organik. • terkadang pemakaiannya dilakukan setelah destruksi bahan dengan HNO3. HF 36% Campuran azeotrop dengan air dan TD 1110C. Termasuk asam lemah dan bukan pengoksidasi. Namun ion Fadalah anion pengomplek yg paling kuat dan membentuk fluorida yg stabil dan kompleks fluoro dengan beberapa unsur tetapi khususnya unsur refraktory yaitu sukar dilarutkan karena membentuk oksida tak larut yg stabil. Melarutkan bahan yang mengandung silikat. Silikon hilang dalam matriks sebagai SiF4 yang volatil tetapi membiarkan matrik dalam larutan. Masalah pemakaian HF: jangan gunakan wadah dari gelas, karena mengandung silkat, gunakan dari platinum, PTFE atau yg terbuat dari plastik. HF dapat membakar kulit, hati-hati gunakan sarung tangan dari plastik Ion fluorida dapat dihilangkan dari matriks setelah pelarutan dengan cara uapkan hingga mendekati kering dg asam sulfat, ulangi beberapa kali atau dapt juga dengan asam perklorat. H3PO4 85% TD 1580C, bukan zat pengoksidasi, melarutkan sampel anorganik, beberapa fosfat tidak larut dalam air. Jika dipanaskan , maka kondensatnya mengandung H3PO4 100%, tetapi merupakan campuran asam dipoli-, tripolidan tetrapoli-, campuran ini dapat digunakan pada suhu 250-3000C. Asam ortofosfat mendidih pada 2130C. Asam ini dapat digunakan untuk melarutkan bentuk sulfida dg melepaskan H2S, juga untuk ferrit, kromit (bilok tetap rendah), dan silikat. C. 1. 2. Campuran asam. Asam pengompleks dan asam pengoksidasi: HF + HNO3 , HF + HClO4, HF + H2SO4 HF = zat pengompleks, asam lainnya = zat pengoksidasi. digunakan untuk baja dan alloy yang mengandung logam refraktory. asam pengoksidasi ditambahkan dahulu hingga larut lalu HF untuk menyempurnakan pelarutan. Membentuk produk yang reaktif: Akua regia (HCl + HNO3 = 3 + 1). Saat HNO3 + HCl maka terbentuk warna kuning dan bau klorin. HNO3 mengoksidasi HCl → klorin dan nitrosil klorida. 3. Satu asam bersifat moderat terhadap lainnya: HNO3 + HClO4 . Daya pengoksidasi HClO4 moderat dibanding HNO3. Tambahkan HNO3 dulu baru HClO4 4. Penggantian satu asam dengan asam lain: HF + H2SO4 (1+10) Sampel dilarutkan dalam HF kemudian diuapkan hingga dryness beberapa kali dengan H2SO4. 1. 2. 3. 4. Ada 4 proses pelarutan dengan menggunakan asam campuran yaitu : Sampel dilarutkan dengan dipanaskan dalam campuran HCl:HNO3 ( 3:1). Sampel dipanaskan dengan HNO3 pekat, lalu dididihkan untuk melepaskan uap HNO3, kemudian HClO4 ditambahkan dan pemanasan dilanjutkan sampai pelarutan sempurna, Sampel dipanaskan dengan HF dan H2SO4 (1:10), lalu uap SO3 dikeluarkan, kemudian ditambah sedikit H2SO4 ‘ Sampel dipanaskan dengan HCl pekat dan kemudian HF pekat ditambahkan tetes demi tetes sampai pelarutan sempurna. D. Campuran asam dengan reagen lain 1. campuran zat pengoksidasi asam dengan: H2O2 (untuk melarutkan baja) Br2 (untuk biji yang mengandung Te) KClO3 ( dengan HCl untuk melarutkan As dan yang mengandung –S). Dengan elektrolit inert: 2. Na2SO4, K2SO4, (NH4)2SO4 untuk menaikkan titik didih H2SO4 Dengan zat pengompleks: 3. Ion logam dalam larutan sebagai kompleks, dengan ditambah anion asam organik yaitu sitrat dan tatrat. Dengan katalis: 4. Agar reaksi logam dengan asam cepat dapat ditambah katalis misalnya Cu2+ dan Hg2+. Beberapa silikat dapat larut dalam HF, akan tetapi HF cukup tidak sesuai untuk pelarutan silikat. HF tidak sesuai untuk melarutkan silikat jika Si yang ditentukan , sedang bila dipakai HF, maka Si akan hilang dari matriks sebagai SiF4 yang volatil, juga untuk Boron yang hilang sebagai BF3. Alternatinya dipakai metode opening-out, dasarnya adalah teknik fusion. Caranya : sampel halus + asam/basa elektrolit / asam pengoksidasi dalam krus nikel atau platina dan dipanaskan sampai meleleh, lalu didinginkan. Kemudian dilarutkan dalam air atau asam encer. III.Teknik Fusion Digunakan jika proses pelarutan dengan asam mungkin kurang sesuai atau kurang stabil ( seperti silikat yang cenderung mengendap). Ada beberapa bahan yang sering bermasalah jika pelarutannya dengan asam: Semen Aluminat Silikat Biji Ti dan Zr Slags Campuran biji Be, Si , Al. Residu yang tak larut dari biji besi Oksida Cr, Si dan Fe Campuran oksida w, Si dan Al. Keunggulan teknik fusion: 1. Elektrolit anorganik yang meleleh (flux) diketahui sangat mudah larut. 2. Suhu dari fusion ini dapat mencapai 12000C, dan reaktiv, kelarutannya bertambah dengan tingginya suhu. 3. Lelehan elektrolit bertindak sebagai asam lewis atau basa lewis tergantung reaksi dengan sampel. Contoh elektrolit Na2CO3 (flux) dipilih untuk fusion pada bahan yang mengandung silika. Pada pemanasan, Na2CO3 terdekomposisi dan menghasilkan O2- yang akan bereaksi dengan silika (SiO2 +O2- SiO32-. Garam ini mudah larut dalam air. Pada proses ini SiO2 asam lewis dan O2- basa lewis. Contoh material flux (elektrolit anorganik) yang digunakan untuk teknik fusion: a. Na2CO3 (TL: 8510C) basa flux untuk silikat dan senyawa refraktory lainnya. Flux ini dapat ditingkatkan fungsinya dengan menambah zat pengoksidasi seperti KNO3, KClO3 atau Na2O2 untuk sampel yang mengandung S, As, Sb atau Cr. Selain itu K2CO3 (TL=891oC) dapat digunakan sebaik NaKCO3 (campuran Na2CO3 dan K2CO3 50:50, TL=712oC) NaOH (TL : 318oC)dan KOH (TL:360oC) untuk silikat, aluminosilikat, sikon karbida atau senyawa lain. Na2O2terdekomposisi pada pemanasan, basa flux untuk sulfida danalloy yang tak larut asam seperti Fe, Ni, Cr, Mo, W dan La. KHSO4, K2S2O7 pada pemanasan dihasilkan SO3 dan digunakan untuk Al2O3, Beo,Fe2O3, Cr2O3,MoO3,TeO2, TiO2, ZrO2. semua oksida diubah dalam bentuk logam sulfida yang mudah larut . Borak oksida (TL:450oC) untuk silikat yang dapat digunakan sebagai alternatif basa flux, jika akan menentukan logam alkali. Keuntungan flux ini adalah kelebihan B2O3 dapat dihilangkan dari matriks dengan distilasi dengan metanol. CaCO3 + NH4Cl campuran ini dipanaskan menghasilkan CaO + CaCl2. flux ini khusus untuk ekstraksi logam alkali dari silikat. KF dan KHF flux pada suhu rendah (beberapa logam fluorida volatil) digunakan untuk menahan silikat dan oksida dari unsur yang membentuk kompleks fluoro yang stabil seperti Be, Nb, Ta dan Zr. Lelehannya dapat diuapkan (fume) dengan H2SO4 untuk menghilangkan F-. Logam fluorida sangat tidak larut, dan Si serta B dapat hilang sempurna dari matriks dalam fusion sebagai SiF4 dan BF3 yang volatil Disodium tetraborat decahydrat (Boraks, N2B4O7.10H2O) untuk Al2O3, ZrO2 biji Zr, mineral yang mengandung Ti, Nb atau Ta, atau mengandung Al, Fe dan slags. Suhu fusion :1000oC – 1200oC. IV. Teknik pelarutan lainnya. Dengan menggunakan larutan NaOH pekat dalam air yang digunakan untuk melarutkan Al atau Be dan alloy tertentu seperti Al/Mg dan Al/Si). Hidrogen akan dilepaskan dan Al membentuk sodium aluminat yang mudah larut. Peralatan yang digunakan: 1. Wadah dari gelas dapat dipakai asal tidak digunakan HF. 2. Teflon dapat digunakan dengan HF tetapi suhu tidak lebih dari 250oC, jika suhunya lebih tinggi dapat dipakai krus platinum. 3. Untuk fusion, krus jenis gelas, silka dan porselin tidak digunakan, sebab flux akan bereaksi dengan bahan tsb. Sebaiknya dipakai krus platinum ( fusion untuk karbonat, sufat, fluorida, borat) sedangkan krus Nikel dipakai untuk fusion oksida, hidroksida dan peroksida. 4. Hal lain yang perlu diperhatikan yaitu agar bahan dari wadah/krus tidak bereaksi dengan analat. Misalnya fusion alkalin dalam krus platinum, dimana bisa mungkin terjadi ion logam direduksi menjadi logam bebas, kemudian logam bebas mungkin bercampur dengan platinum dan sampel akan berkurang. Komponen yang mungkin hilang seluruhnya atau sebagian selama pelarutan atau opening-out. Bentuk perlakuan Komponen yang hilang 1. 5. Asam (encer, dingin)....... Basa............................... Oksidasi........................... Reduksi............................ HF.................................... 6. HCl panas........................ 6. 7. H2SO4 atau HClO4 panas dengan 7. adanya Cl-............... 1. 2. 3. 4. 2. 3. 4. 5. CO2,SO2, H2S,H2Se,H2Te, HCN,HSCN. NH3 Cl2, Br2, I2 PH3,AsH3, SbH3. SiF4, BF3 (hilang total), logam fluorida (As, Ti,nb, Ta) hilang sebagian. Beberapa logam klorida : As, Sb, Sn,Ge, Hg,Se, Te dan Re Bi, Mn, Mo, Tl, V, Cr 8. H2SO4 atau HClO4 panas... 8. H3PO4 9. Larutan berair asam panas.... 9. H3BO3, HNO3, HCl, HBr, HI, 10. HF/HClO4 atau HF/H2SO4...... 10. 11. Fusion KF atau KHF2.......... 11. 12. Fusion K2S2O7......................... 12. 13. Fusion Na2B4O7 dan Na2CO3... 13. OsO4, RuO4, Re2O7. Si, B,As, Se, Sb, Hg, Ge, Cr, Re, Os dan Ru. Si, B, Nb, Ta, Ti Hg, anion dari asam volatil, PO43-. Tl, Hg, Se, As, halogen