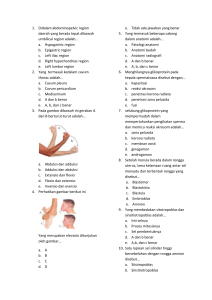
BAB II TINJAUAN PUSTAKA 2.1 Definisi Fragile X Syndome Fragile X Syndrome (FXS) adalah penyakit genetik yang diwarisi melalui kromosom X, disebabkan oleh ekspansi abnormal pada jumlah pengulangan CGG trinukleotida yang terletak di UTR 5 'pada gen X retardasi mental X rapuh (FMR1) pada Xq27.3. Ini adalah mutasi dinamis dengan perluasan pengulangan CGG di setiap generasi yang bergerak dari kisaran premedikasi 55 sampai 200 mengulangi dan berkembang menjadi mutasi penuh (Hagerman, 2014). Gambar 2.1 letak Gen FMR1 pada lengan panjang (q) dari kromosom X pada posisi 27.3. Sumber : Warren (2014) 2.2 Sejarah Pada tahun 1943, Martin dan Bell 'menggambarkan seks terkait keterbelakangan mental tanpa fitur dismorfik dalam sebuah keluarga di mana keduanya menyerang lakilaki dan betina diamati. Tiga puluh enam tahun Kemudian, Lubs2 melaporkan kromosom X marker (kemudian dikenal sebagai kromosom X rapuh) sebagai temuan yang tidak konsisten dalam sitogenetika studi pada leukosit beberapa keterbelakangan mental lakilaki Asam folat dan timidin habis media kultur sel diidentifikasi sebagai faktor penting untuk induksi ini situs rapuh yang dapat diwariskan di Xq27.3 Selama tahun tujuh puluhan, kombinasi X terkait mental retardasi dan anggrek makro recognised. Kemudian, karakteristik klinis lainnya didirikan, misalnya, wajah panjang dengan telinga besar dan menonjol, dan tingkah laku fitur, termasuk menghindari kontak mata, hiperaktif, mengepakkan tangan, dan tekun pidato (Oostra, et al., 1998). Sindrom X rapuh didiagnosis pada Waktu itu dengan deteksi sitogenetik yang rapuh situs di Xq27.3. Itu memiliki beberapa fitur khusus untuk sebuah gangguan terkait X. Sekitar 30% dari betina pembawa wajib sedikit atau cukup terbelakang dan sebagian 3 4 besar (± 50%) tidak memiliki ekspresi X rapuh sitogenetik. Juga, secara fisik nenek moyang menghubungkan dua cabang keluarga dengan sindrom X rapuh diamati. Ini "normal mentransmisikan laki-laki "tanpa klinis atau Fitur sitogenetik tampaknya bisa menular sindrom X rapuh. Gen yang terlibat dalam sindrom X rapuh, Retardasi Mental Fragile X (FMRl) gen, diidentifikasi pada tahun 1991.9-l 'gen Cacat adalah ekspansi trinukleotida pertama ulangi untuk ditemukan dan seluruh kelas Gangguan sekarang diketahui terkait dengan jenis mutasi ini (Oostra, et al., 1998). 2.3 Epidemiologi Prevalensi aktual di seluruh dunia, ditentukan oleh molekul tes, diperkirakan satu per 5.000 pria dan satu per 4.000 untuk 6.000 perempuan. Ricaurte adalah distrik kotamadya Bolívar, terletak di utara Valle del Cauca, di mana telah ada mengidentifikasi prevalensi cacat mental yang tinggi, 39 secara intelektual nonaktifkan individu dalam 1124 habitants. Selama akhir 1990an, Studi menemukan bahwa penyebab kecacatan di kawasan ini adalah FXS. Dalam penelitian ini 19 pasien didiagnosis dengan sindrom ini kariotipe dengan band G pada medium kekurangan folat; selanjutnya Diagnosis klinis dilakukan pada 16 pasien lainnya di antaranya kariotipe tidak dilakukan Kasus ditemukan di 3 keluarga nama dan kemungkinan leluhur bersama telah dipostulasikan mengingat pola migrasi dan karakteristik bangunan kota. Oleh tahun 1999 prevalensi FXS di Ricaurte ditentukan sebagai 1:38 pria dan 1: 100 waita, yang melebihi 100 kali lipat prevalensi dilaporkan dalam literature (Sherman SL et al, 2009). Sejumlah kondisi medis dan sindrom, terkait dengan pembawa premutation termasuk depresi, kecemasan, migraine sakit kepala, hipertensi, sleep apnea, penyakit mediated immune termasuk hipotiroidisme dan fibromyalgia, dan FXTAS dan FXPOI telah dijelaskan dalam 10 tahun terakhir. Prevalensi dari premedikasi pada populasi umum adalah 1: 130-200 wanita dan 1: 250 sampai 450 orang. Tremor / Ataxia Syndrome terjadi di sekitar 40% pria dengan premedikasi dan 16% wanita, sedangkan FXPOI terjadi pada sekitar 16 sampai 20% wanita dengan permutation (Hagerman P, 2013). 2.4 Etiologi Menurut The Fragile X Association of Australia (2017) etiologi dari Fragile X Sindrom adalah : 1. Fragile X Syndrome (FXS) disebabkan oleh perluasan atau pemanjangan gen FMR1 pada kromosom X, yang dikenal sebagai mutasi gen. Kromosom X adalah satu dari 5 dua jenis kelamin yang menentukan kromosom. Bila gen memanjang maka matikan produksi protein yang terlibat dalam pengembangan otak dan fungsi lainnya. 2. Betina memiliki dua kromosom X dan jantan memiliki satu X dan satu Y. Biasanya, kromosom X mengandung antara 6 dan 50 ulangan gen (gen FMR1) yang bertanggung jawab untuk memproduksi protein yang penting untuk perkembangan otak normal. 3. Pada beberapa orang, gen ini mungkin mengandung antara 50 dan 200 ulangan. Ini disebut premosis Fragile X. Seseorang dengan premedikasi ini disebut 'pembawa'. FXS disebabkan ketika gen ini membentang hingga lebih dari 200 ulangan yang mengganggu produksi normal protein ini dan oleh karena itu perkembangan otak normal. 4. Gen Fragile X dapat diturunkan melalui setiap generasi. Anak perempuan yang lahir dari pembawa laki-laki akan mewarisi ayah mereka yang terkena kromosom X dan mereka juga akan menjadi pembawa. Anak laki-laki yang lahir dari pembawa laki-laki tidak akan mewarisi kromosom X ayah mereka dan karenanya tidak akan terpengaruh oleh Fragile X. 5. Karena betina memiliki dua kromosom X, anak-anak dari kedua jenis kelamin yang lahir dari pembawa wanita memiliki kemungkinan 50% untuk mewarisi gen yang terkena. Jika mereka mewarisi gen yang terkena, mereka akan menjadi pembawa atau memiliki mutasi penuh Fragile X. 6. Mutasi Fragile X sering meningkat saat diwariskan dari ibu ke anak dan turun dari generasi ke generasi keluarga. Ini berarti bahwa anak-anak yang lahir dengan Fragile X sering muncul dalam keluarga tanpa riwayat kecacatan intelektual sebelumnya. Gambar 2.2 Tipe pedigree Fragile X Sindrom ( X-Linked Pedigree), Perhatikan adanya transmisi pria dan antisipasi dengan individu yang lebih terpengaruh pada generasi selanjutnya. Sumber : Hagerman R,( 2016) 6 2.5 Patofisiologi Genetics of fragile X Fragile X syndrome (FXS), kondisi X-linked yang pertama kali dijelaskan oleh Martin and Bell, adalah penyebab utama cacat intelektual bawaan (inheritance intellectual disability / ID). Perkiraan dilaporkan bahwa FXS mempengaruhi sekitar 1 dari 2.500 sampai 5.000 pria dan 1 dari 4.000 sampai 6.000 wanita. FXS disebabkan oleh mutasi pada gen FMR1, yang terletak pada kromosom X dan lokusnya di Xq27.3 bertepatan dengan situs rapuh folat. Metode sitogenetika yang digunakan di masa lalu untuk mendiagnosis FXS telah digantikan oleh diagnostik molekuler DNA FMR1 dengan menggunakan analisis Southern blot dan, yang lebih baru lagi, PCR. Laki-laki yang terkena dampak menunjukkan berbagai tingkat gejala mulai dari yang ringan sampai yang parah. Karena kompensasi oleh kromosom X yang tidak terpengaruh, hanya sepertiga pembawa wanita dengan mutasi penuh (FM) memiliki ID; mayoritas memiliki IQ normal, meski kesulitan belajar dan masalah emosional biasa terjadi. (Bagni et al., 2012) Diidentifikasi pada tahun 1991 oleh kloning posisional, gen FMR1 ditandai dengan adanya urutan triplet CGK polimorfik di UTR 5 '. Ekspansi dalam urutan triplet ini memunculkan FXS, yang merupakan prototipe gangguan ekspansi triplet yang tidak stabil. Variabilitas triplet mendefinisikan empat jenis alel (Figure 1). Alel normal memiliki sejumlah pengulangan CGG, berkisar antara 5 sampai 54, dengan mode 30. Alel mayor (PM) memiliki sejumlah pengulangan CGG, berkisar antara 55 hingga 200. Alel PM tidak stabil dan memiliki kecenderungan kuat untuk berkembang. untuk alel FM pada transmisi ibu. Ekspansi dari PM ke FM dapat terjadi dengan alel sekecil 56 CGG. Alel yang memiliki antara 45 dan 54 pengulangan CGG, disebut alel zona abu-abu atau perantara, diusulkan untuk menjadi prekursor alel PM, yang berpotensi karena ketidakstabilan meiotik pada ayah dan ibu. Resiko transisi PM ke FM bergantung pada ukuran ulang CGG, sehingga risiko ekspansi hampir 100% untuk alel> 99 CGG berulang. Sebuah studi barubaru ini menunjukkan bahwa jumlah gangguan AGG yang ada dalam pengulangan CGG berkorelasi terbalik dengan risiko ekspansi ke FM di generasi berikutnya. Kehadiran gangguan AGG, selain panjang CGG, dengan demikian dapat menentukan risiko penularan dari PM ibu ke FM pada keturunannya. (Bagni et al., 2012) Gambar 2.3 Keempat alel gen FMR1 manusia. Menurut tingkat ekspansi triplet CGG dan tingkat transkripsi FMR1 mRNA dan Perubahan terjemahan, empat alel dihasilkan: normal, PM, UFM, dan FM. Sumber : Hagerman R. (2012). 7 FMR1 silencing adalah konsekuensi modifikasi epigenetik yang agak kompleks. Di FXS, sitosin yang terletak kira-kira sampai 1 kb hulu dari urutan ulangan CGG, termasuk promotor FMR1, dimetilasi. Alel normal juga dimetilasi di daerah promotor FMR1 namun tidak dekat dengan pengulangan CGG, yang tampaknya merupakan "batas" alel normal yang mencegah metilasi menyebar. Batas ini hilang dalam alel FM, dan sitosin di bagian hulu dari pengulangan CGG dimetilasi sekitar minggu ketigabelas perkembangan embrio. Sebagai konsekuensinya, transkripsi gen dihambat, menyebabkan tidak adanya produk protein FMRP-nya. Dari catatan, beberapa alel tetap sebagian atau bahkan tidak terionisasi penuh (UFM), meskipun mengandung> 200 CGG berulang, namun perbedaan dalam status metilasi kurang dipahami. (Bagni et al., 2012) Selain mengubah status metilasi, alel FXS menunjukkan deasetilasi histone H3 dan H4, mengurangi metilasi lisin 4 (K4), dan meningkatkan metilasi lisin 9 (K9) pada histone H3. Perubahan epigenetik ini mempromosikan konfigurasi heterokromatik yang mengecualikan pengikatan faktor transkripsi tertentu, sehingga mengubah ekspresi gen. Alel UFM yang langka terutama mempertahankan aktivitas transkripsi FMR1 normal atau lebih tinggi, dengan tingkat FMRP yang berkurang; asetilasi histone H3 dan H4 dan metilasi lysine 9 pada H3 alel UFM lebih mirip dengan alel FM, sedangkan tingkat metilasi lisin 4 dan 27 pada H3 lebih mirip dengan alel normal. (Bagni et al., 2012) Heritability Heritabilitas FXS tidak memiliki pola pewarisan klasik Mendelian. Hal ini tergantung pada jumlah CGG trinucleotide yang berulang dalam promoter gen FMR1. Transisi dari alel PM ke FM terjadi karena fenomena ekspansi selama transmisi kromosom X yang membawa PM ke anak-anaknya. Ekspansi ini tidak terjadi selama transmisi kromosom X ayah, dengan PM, untuk anak perempuan mereka. Soall anak perempuan laki-laki dengan premedikasi akan menjadi pembawa premedikasi wajib tetapi anak perempuan ini memiliki risiko 50% untuk memiliki anak dengan FXS. (Saldarriaga et al., 2014) a. Dynamic of the mutation Resiko transisi dari PM ke FM pada keturunan bergantung pada jumlah pengulangan trinucleotide pada alel PM, mencapai ~ 100% untuk alel PM dengan lebih dari 99 kali pengulangan. Ekspansi dari PM ke FM pada meiosis dapat terjadi pada alel dengan sedikit seperti 56 CGG mengulangi; kemungkinan bahwa ini terjadi bergantung pada rentang pengulangan dimana pasien diklasifikasikan, jumlah gangguan AGG dan usia ibu (Tabel 1). Biasanya ada jangkar AGG dengan setiap 9 atau 10 pengulangan CGG di FMR1. Jangkar dapat memodifikasi risiko perluasan pengulangan CGG saat diteruskan oleh ibu. Wanita dengan premedikasi dan 2 jangkar AGG memiliki risiko ekspansi yang lebih rendah terhadap mutasi penuh dibandingkan wanita tanpa jangkar AGG. (Saldarriaga et al., 2014) 8 tabel 2.1 Perbandingan risiko ekspansi dari premutation ke mutasi penuh (FM) antara persentase yang dilaporkan tergantung hanya pada jumlah pengulangan CGG2 dan persentase yang dilaporkan baru-baru ini tergantung pada gangguan AGG dan ibu Sumber : Saldarriaga et al., (2014) b. Inheritance and recurrence risk Pria. Sebagian besar pria dengan FM biasanya tidak bereproduksi dengan hanya 1% dari mereka yang dilaporkan memiliki keturunan. Pasien laki-laki dengan FM dan FXS memiliki kesempatan 100% untuk meneruskan premis tersebut kepada anak perempuan mereka sehingga anak perempuan mereka hanya akan menjadi pembawa dan biasanya mereka tidak hadir dengan cacat intelektual. Inilah hilangnya FM dalam pembentukan sperma dan hanya premutation yang diteruskan. Semua anak laki-laki mereka akan menerima kromosom Y sehingga mereka tidak akan terpengaruh dengan mutasi FMR1. Sementara itu, pria dengan PM hanya akan mentransmisikan PM ke anak perempuan mereka dan jumlah pengulangannya relatif stabil (Saldarriaga et al., 2014). Wanita. Perlu dicatat bahwa pembawa PM dapat memperluas alel mereka ke FM dengan kemungkinan tergantung pada jumlah pengulangan, jumlah gangguan dan usia AGG (Tabel 1). Dampak dari gangguan AGG disebabkan oleh penurunan selip DNA polimerase dalam replikasi. Oleh karena itu, gangguan ini memberi stabilitas dalam transmisi gen namun tidak mengganggu transkripsi gen atau terjemahannya (Saldarriaga et al., 2014). Selain itu, menurut jenis kelamin bayi baru lahir, karakteristik klinisnya akan diferensikan. Pasien laki-laki dengan FM akan mengalami gangguan mental. Sebaliknya, anak perempuan yang mewarisi FM memiliki kesempatan 30% untuk memiliki kecerdasan intelektual normal, 25% memiliki kecacatan intelektual dengan IQ kurang dari 70, namun mereka dapat mempresentasikan pembelajaran sebesar 60% dan kesulitan emosional (70%). (Saldarriaga et al., 2014) 9 2.6 Manifestasi Klinis Tabel 2.2. Karakteristik klinis pasien dengan mutasi penuh dan Fragile X Syndrome Jenis kelamin Karakteristik Wajah Pria Wanita Besar dan menonjol telinga (75- Besar dan menonjol telinga (7578%) 78%) Wajah panjang Wajah panjang Prognatisme mandibula (80% pria Prognatisme mandibular dewasa) Celah langit-langit Dahi yang menonjol Macrocephaly Ophthalmologic Bagian Strabismus (8%) Strabismus (8%) Kesalahan bias Kesalahan bias dalam Ketulian karena kambuhnya infeksi telinga telinga yang tinggi Neurologis Kejang (23%) Kejang (23%) Hipotonia (anak-anak) Hipotonia (anak-anak) Clonus (dewasa) Clonus (dewasa) Refleks palmomental positif Refleks palmomental positif Kontak mata yang buruk Kontak mata yang buruk Psikiatrik Attention deficit hyperactivity disorder Kegelisahan Perilaku motorik berulang Karakteristik autistik Agresi dan distress crisis Perkembangan Keterbelakangan mental Keterbelakangan mental Defisit kognitif dan bahasa (yang Defisit kognitif dan bahasa (yang terakhir berulang) Ortopedi terakhir berulang) Kaki rata Hyper extensibility metacarpophalangeal joint Skoliosis in the 10 jempol ganda Thorax Pectus excavatum Genitourinaria Macro orchidism (95% of adult men) Kardiovaskular Kelainan jantung (prolaps katup mitral) Lain- Lain Obesitas, gigi yang sempit, tinggi atau pendek * Mayoritas karakteristik fenotipik telah dijelaskan pada pria dengan FXS, wanita biasanya memiliki fitur serupa meski seringkali kurang parah. Sumber : Saldarriaga W/et al/Colombia Médica - Vol. 45 Nº4 2014 (Oct-Dec) Gambar 2.4 Deskripsi karakteristik fenotipik khas Fragile X Syndrome. Sumber : Saldarriaga W/et al/Colombia Médica - Vol. 45 Nº4 2014 (Oct-Dec) 11 Table 2.3 Temuan Fisik dan Perilaku Mayor pada Fragile X Sindrom (FXS) Fisik Perilaku - Wajah memanjang - Kecemasan - telinga besar - Hiperaktif - Makroorchidisme - Defisit perhatian - Prolaps katup mitral - Ketidakmampuan emosional - Hiperlabilitas sendi - Gerakan stereotip - Displasia jaringan ikat - Echolalia - Hipotensi otot - ASD (Autism spectrum disorder) Sumber : Neri G. (2017) Gambar 2.5 Dua pria muda berusia awal 20-an, dengan ciri wajah yang lebih menonjol, dan pria yang lebih tua dengan manifestasi wajah penuh: dahi tinggi, wajah memanjang, hipoplasia midface, philtrum panjang dan dagu, telinga besar. Sumber : Neri G. (2017) Gambar 2.6 (A) Pandangan tangan menunjukkan spatulated fingers dengan kulit berlebihan dan (B) hyperextensibility sendi. Sumber : Neri G. (2017) 12 2.7 Diagnosis Fragile X Sindrom Awalnya, diagnosis FXS dilakukan melalui kariotipe, yang memungkinkan pengamatan penyempitan distal lengan panjang kromosom X pada pita 27.3 (Xq27.323.8) dengan menggunakan mikroskop cahaya. Temuan penyempitan distal dapat dilakukan pada kromosom yang berbeda, dan dikenal sebagai situs rapuh, dari tempat FXS yang diberi nama (Hagerman, 2014). Saat ini ada beberapa tes molekuler yang tersedia untuk diagnosis FXS yang jauh lebih sensitif dan spesifik daripada kariotipe. Selain memungkinkan diagnosis pasien dengan FM dan FXS, tes tesis ini memungkinkan identifikasi pembawa PM, yang merupakan individu biasanya dengan IQ normal, namun pembawa wanita memiliki risiko tinggi memiliki anak dengan FXS. Selain itu ada tes molekuler yang memungkinkan kuantifikasi RNA pembawa pesan (mRNA) dan protein FMRP, yang memungkinkan pemahaman fisiopatologi penyakit lebih baik dengan menghubungkan hasilnya dengan fenotipe pasien FM dan PM2. Polymerase chain reaction (PCR) dan Southern blot adalah tes rutin untuk diagnosis DNA FXS yang memungkinkan penentuan jumlah pengulangan CGG dan status metilasi gen FMR1 (Hagerman, 2014). PCR melalui penggunaan primer spesifik untuk gen FMR1 memungkinkan amplifikasi daerah yang mengandung pengulangan CGG dan, dapat mengidentifikasi pasien dengan alel FMR1 yang diperluas terutama pada premedikasi tetapi juga pada rentang mutasi penuh.Biasanya analisis Southern blot adalah digunakan untuk mencirikan alel yang lebih baik dalam kisaran mutasi penuh dan untuk menentukan status metilasi. Namun, dengan teknik PCR baru yang menggunakan primer ganda untuk PCR nested, kuantifikasi pengulangan triplet CGG dan identifikasi pasien FM dan PM dimungkinkan (Hagerman, 2014). 13 Gambar 2.7 Penggunaan teknik molekuler untuk diagnosis Fragile X Syndrome (SXF) Sumber : Saldarriaga W/et al/Colombia Médica - Vol. 45 Nº4 2014 (Oct-Dec) Tes untuk diagnosis FXS harus dipesan untuk pasien dengan cacat intelektual dan / atau autisme dan tambahan fitur berikut ini: fitur wajah yang berbeda seperti telinga besar yang menonjol, wajah panjang, antara lain; riwayat keluarga cacat intelektual, autisme, makroorchidisme (Hagerman, 2014). Setelah ditentukan bahwa pasien memiliki FM atau PM untuk FXS, pengujian molekuler DNA harus dilakukan pada semua anggota keluarga yang dicurigai melalui analisis silsilah sebagai pembawa. Demikian juga anggota keluarga dengan tremor, ataksia, gejala neurologis atau insufisiensi ovarium dini juga akan menjadi kandidat untuk tes molekular (Hagerman, 2014). 14 Diagnosis FXS dapat dilakukan bahkan pada janin pembawa hamil atau pasien dengan FXS menggunakan tes molekuler yang sama seperti di atas (Southern blot and PCR) pada pengambilan sampel villi chorionic (Hagerman, 2014). Gambar 2.8 Diagnosis gold standart untuk sindrom X rapuh (FXS) menggunakan kombinasi Southern blot dan analisis polymerase chain reaction (PCR). Angka ini menunjukkan hasil dari molekul berbasis PCR yang berbeda pendekatan (A-G) dan dari Southern blot (H) diarahkan pada diagnosis FXS. Tabel menunjukkan kategori alel jelas terdeteksi oleh pendekatan molekuler yang berbeda. Sumber : Mila M. (2017) Diagnosis molekuler FXS didasarkan pada ukuran pengulangan CGG, dan juga metilasi status CpG island yang berada di daerah promotor gen tersebut. Analisis Southern blot menjadi teknik diagnostik DNA standar emas. Southern blot dilakukan dengan pencernaan DNA menggunakan dua enzim restriksi: satu bertujuanmenentukan ukuran ekspansi dan yang lainnya pada status metilasi. Pendekatan ini memberikan karakteristik pola mutasi untuk masing-masing status individu sebagaimana yang ditunjukkan. Sampai saat ini, kombinasi dari polymerase chain reaction (PCR) (sangat berguna untuk CGG ukuran dalam kisaran PM) dan analisis Southern blot (untuk mengukur alel yang lebih besar dan untuk menentukannya status metilasi mereka) masih merupakan metodologi DNA standar emas untuk diagnosis FXS. (Mila M., 2017). 15 PCR konvensional, . Dalam pendekatan PCR, primer berlabel fluoresen yang mengelilingi daerah CGG digunakan (Fu et al., 1991) dan produk dianalisis dalam penganalisis gambar untuk menentukan jumlah pasti pengulangan CGG menggunakan sejumlah kecil DNA. Jumlah CGGs yang tepat sangat penting untuk melakukan diskriminasi antara alel normal, intermediate, dan PM (Mila M., 2017). dalam dekade terakhir sejumlah strategi diagnosis berbasis PCR telah diajukanuntuk identifikasi perluasan ulang gen FMR1. Metode tripel repeat-primed PCR (TP-PCR) dikembangkan oleh Warner et al. (1996) untuk menyaring untuk kehadiran alel yang diperluas pada distrofi myotonic. Ini kemudian digunakan untuk memperkuat alel diperluas gen FMR1 ke dalam kisaran FM. Pada saat bersamaan, pendekatan ini memberikan informasi tentang adanya dan distribusi gangguan AGG (Mila M., 2017). PCR metilasi spesifik alel-spesifik dan elektroforesis kapiler. Status metilasi adalah ditentukan dengan menggunakan enzim restriksi yang sensitif terhadap metilasi dan PCR dengan dua set didaur ulang primer, dan alel diukur dengan elektroforesis kapiler. Metilasi PCR memungkinkan penilaian metilasi tingkat tinggi, resolusi tinggi, dan semiquantitatif FMR1 alel, serta penentuan ulang ulang CGG. Telah diusulkan untuk menjadi lebih pendekatan sensitif daripada analisis Southern blot (Mila M., 2017). kombinasi dua metode PCR sederhana-TP-PCR dan TP-MS-PCR-bisa memberikan informasi tentang keseluruhan rentang ekspansi, gangguan AGG, dan status metilasi. Hal ini dapat mengkarakterisasi betina homozigot dari betina FM, dengan demikian mencapai diagnosis FXS prenatal dan postnatal yang cepat dan dapat diandalkan (Mila M., 2017). (MS-QMA), pengukuran metilasi di Situs FREE2 diusulkan menjadi metodologi yang sesuai untuk skrining bayi baru lahir untuk keduanya FXS dan kromosom seks aneuploidi. MSQMA digunakan untuk memperkirakan adanya alel FM samar pada individu yang juga membawa alel zona normal atau abu-abu. Penulis menyatakan bahwa sensitivitas diagnostik dan analitis Teknik ini lebih tinggi dari analisis TP-PCR atau Southern blot dan bisa digunakan sebagai metode penyaringan lini pertama (Mila M., 2017). DNA diperoleh dari berbagai jaringan termasuk air liur, darah, jaringan otak, amniotik cairan, atau chorionic villi dapat digunakan untuk diagnosis DNA. Untuk diagnosis pralahir, lebih baik untuk melakukan penelitian di villi chorionic, dan dengan demikian, harus diperhitungkan itu sampel ini tidak sepenuhnya dimetilasi sampai setelah minggu ke 14 kehamilan. Dalam kasus Kontaminasi ibu, perempuan harus dikesampingkan (Mila M., 2017) 16 2.8 . Diagnosa Banding Diagnosis bandingnya meliputi sindrom Sotos, Prader-Willi dan Klinefelter karena mereka memiliki karakteristik tertentu. Untuk masing-masing sindrom ini ada tes molekuler spesifik yang membantu mengkonfirmasi diagnosis. Tes ini akan dipesan sesuai dengan temuan fenotipik dan analisis klinis pasien. Temuan klinis yang paling sering terjadi di antara sindrom ini yang dapat dikontraskan dengan FXS adalah: Sotos syndrome: cacat intelektual, tinggi badan, macrocephaly, dan epilepsi. Sindrom Prader-Willi: cacat intelektual, obesitas, perawakan pendek, dan hipogenitalisme. Sebuah subkelompok pasien dengan FXS akan memiliki fenotipe Prader-Willi namun tidak akan mengalami delesi pada daerah 15 q11-13, walaupun tingkat protein CYFIP dari daerah ini rendah. Sindrom Klinefelter: perawakan tinggi, hipogenitalisme, cacat intelektual (20%) FRAXE: cacat intelektual, gangguan bahasa, hiperaktif, perilaku autistik (karena pengulangan abnormal triplet CCG pada gen FMR2) Ketidakmampuan intelektual dan kerapuhan kromosom di situs rapuh lainnya telah dijelaskan (gen FRAXD dan FRAXF). (Hagerman, 2014) Tabel 2.4 Diagnosa Banding Fragile X Sindrom Sindrom Keterbelakangan Stature Perimeter Ukuran mental Cephalic testis * * Berat* Tes diagnostik * Fragile X Ringan sampai syndrome sedang +++ ++ +++ ++/+++ PCR, Southern Blot Sotos Masalah belajar +++ syndrome ringan +++ ++ ++ Sequencing dan / atau gen FISH NSD1 Prader- Ringan Willi sedang syndrome sampai + ++ + +++ FISH 15q11.2q13 17 Klinefelter Tidak ada atau +++ syndrome ringan ++ + ++/+++ Karyotype * digunakan Konvensi berikut : + Ukuran lebih kecil dari populasi umum; ++ Mirip dengan populasi umum; +++ Ukuran lebih besar dari populasi umum Sumber : Saldarriaga W/et al/Colombia Médica - Vol. 45 Nº4 2014 (Oct-Dec) Sindrom lainnya yang kurang sering, dengan prevalensi yang lebih rendah dari satu di antara 50.000, memiliki mekanisme genetik dan fisiopatogen serupa serta fenotipe ke FXS. Di antara sindrom ini ada sindrom Fragile X E dan sindrom Fragile X F, karena adanya perubahan gen FMR2, FAM11A dan FRAXD. Jika fenotip pasien sangat menyarankan FXS dan hasil south blot keluar negatif, pengujian molekuler untuk gen yang disebutkan di atas harus dipertimbangkan (Hagerman, 2014). 2.9 Permasalahan dengan Fragile X Sindrom a. After birth problems Anak laki-laki dengan FXS sedikit lebih besar dari rata-rata di berat saat lahir Berat lahir rata-rata dari sebelumnya studi berkisar dari 3.490 gram. sampai 4.046 gram. Berat lahir rata-rata anak laki-laki dengan FXS berada di persentil ke-70, mereka juga memiliki berat lahir lebih tinggi dari pada saudara mereka, saat ini dikoreksi untuk usia gestasi dan jenis kelamin. Berat lahir rata - rata di FXS meningkat dan Pertumbuhan linier rata-rata juga di atas rata-rata, untuk Anak laki-laki biasanya berkembang dengan peningkatan terbesar setelah tahun kedua kehidupan. Sebaliknya, beratnya pengukuran rata-rata di bawah rata-rata sampai dua tahun. Setelah kelahiran, lingkar kepala cenderung naik di atas Persentil ke-50 dan terus menjadi lebih besar dari itutanpa FXS. Jacobs dkk. Mencatat bahwa dalam enam dari Sembilan Orang yang terkena dampak, lingkar kepala lebih besar dari persentil ke-90, namun penelitian lain menunjukkan bahwa rata - rata lingkar kepala (19-21) (Hagerman R, 2016). Seperti yang terlihat di FXS bisa mengakibatkan peningkatan proliferasi progenitor sel glial dan pertumbuhan kortikal serebral selanjutnya. Adanya perbedaan otak awal di kalangan anak-anak muda dengan FXS menunjukkan otak dini yang menyimpangperkembangannya (Hagerman R, 2016). Disfungsi hipotalamus disfungsi ini dapat menyebabkan Peningkatan sekresi prematur estrogen dosis tinggi, sehingga menyebabkan epifisis mengalami pematangan dini. Hipotesis aktivasi dini sumbu hipotalamus-hipofisis-gonad dapat menjelaskan 18 penyebab penurunan pertumbuhan di FXS dan sesekali ditemui pubertas prekoks pada wanita dengan FXS (Hagerman R, 2016). b. Otitis media (OM) 85% anak-anak dengan FXS memiliki setidaknya satu episode terdiagnosis OM. Telinga Pemeriksaan dijamin untuk setiap perubahan perilaku dan Pola tidur juga gejala lainnya termasuk demam, muntah, dan sakit kepala. Anak-anak dengan FXS umumnya mengembangkan komplikasi OM termasuk penurunan pendengaran akut dan setidaknya seperempat mengalami sinusitis akut. Otitis Media dapat menyebabkan defisit pendengaran konduktif dan memperburuk kognitif, bahasa, dan perilaku masalah yang ada pada sindrom ini (Hagerman R, 2016). c. Seizures Fmr1 knockout (KO) mouse menunjukkan koneksi dendritik yang belum matang, Peningkatan jumlah duri panjang dan tipis yang menunjukkan kekurangan pada seleksi normal atau pemangkasan kontak sinaptik yang terjadi di neuronal pembangunan. Patofisiologi kejang pada orang dengan FXS bisa terjadi terkait dengan ketidakseimbangan rangsang dan penghambatan sistem neurotransmiter (Hagerman R, 2016). Pada mereka dengan Kejang terbuka, semua jenis kejang bisa terjadi. Dominasi generalisasi kejang, kejang umum sekunder dan status kejang epileptikus. Kejang di FXS mungkin juga terjadi menyerupai epilepsi fokal jinak di masa kanak-kanak di centrotemporal spikes. Secara umum, kompleks kejang parsial adalah jenis perampasan utama di FXS. Kejang pada usia dini nampaknya terkait dengan morbiditas perkembangan dan perilaku yang bisa berdampak fungsi otak. Hebatnya, pasien-pasien dengan FXS dan kejang lebih cenderung memiliki ASD. Pada saat kejang: perilaku yang tidak dapat dijelaskan, atipikal wajah gerak tubuh, muntah di malam hari, regresi perkembangan, perubahan bahasa atau perilaku, dan juga signifikan gangguan tidur (Hagerman R, 2016). d. Mitral valve prolapse Prolaps Katup Mitral (MVP, katup mitral floppy) adalah kondisi jantung katup yang ditandai dengan Perpindahan katup mitral yang kental selebaran ke atrium kiri selama sistol. Studi tentang individu dengan FXS telah menunjukkan bahwa MVP terjadi kira-kira 50% laki-laki dan 20% perempuan dengan ekokardiogram. MVP lebih sering terjadi pada orang dewasa dari pada anak-anak dan seringkali tidak dapat didiagnosis hanya dengan auskultasi. jika murmur sistolik atau murmur MVP klasik terdeteksi (klik pertengahan sistolik, diikuti oleh Murmur sistolik yang terlambat terdengar paling baik di 19 puncak), maka dianjurkan untuk meminta evaluasi kardiologi yang mana harus melakukan ekokardiogram. Kasus MVP yang langka itu dan gejala aritmia atau dysautonomia mungkin akibat dari beta-blocker. Individu dengan MVP adalah pada risiko lebih tinggi dari endokarditis infektif (Hagerman R, 2016). MVP dikaitkan dengan regurgitasi mitral parah. Pada populasi umum, MVP diamati di individu yang cenderung memiliki indeks massa tubuh rendah (BMI). Serat elastin abnormal telah terdeteksi di katup jantung dan di kulit individu dengan FXS jadi MVP dianggap terkait dengan jaringan ikat masalah yang terlihat di FXS dan terkait dengan kelainan pada serat elastin. Dilatasi akar aorta juga terlihat pada banyak individu dengan FXS di masa kecil dan dewasa dan ini juga terkait dengan abnormal serat elastin; Biasanya, ini tidak progresif. MVP membawa risiko komplikasi yang sangat rendah, Tetapi pada kasus yang jarang terjadi, komplikasi mungkin termasuk regurgitasi mitral, endokarditis infektif dan kegagalan jantung kongestif (Hagerman R, 2016). e. Gastrointestinal problems Masalah gastro intestinal (GI) pada FXS tetap harus ditentukan, menderita diare dan gastroesofagus refluks disease (GERD). anak-anak Masalah GI telah digambarkan terjadi kelainan jaringan ikat, seperti Ehlers-Danlos sindrom (EDS) dan sindrom Marfan, masalah seperti itu termasuk GERD, irritable bowel syndrome, dan diare. Yang lebih menarik lagi adalah asosiasi dari premutation dan irritable bowel syndrome dan adanya gangguan perkembangan dan autisme, konstipasi , diare yang diamati di FXS. Individu dengan FXS memiliki rasa sakit yang lebih tinggi seiring dengan defisit komunikasi dan lainnya gejala gastrointestinal, pemantauan tinggi dan berat badan yang tepat untuk menentukan adanya kegagalan dalam berkembang, berat badan yang buruk kemungkinan dusebabkan karena diare pada FXS, ini terkait dengan disregulasi otonom termasuk Simpatis hiperaktif dan kecemasan kronis (Hagerman R, 2016). f. Sleep Masalah tidur sangat umum terjadi pada anak kecil dengan FXS. Ada banyak masalah yang mengganggu pola tidur normal seperti sering terbangun di malam hari, terbangun terlalu dini, dan parasomnia. Pada anak-anak dengan FXS prevalensi masalah tidur dilaporkan 26-47%. Paling sering permasalahan yang dilaporkan adalah sulitnya tertidur dan seringnya malam hari terbangun. Selain itu, pola tidur dan profil melatonin yang tidak teratur telah diamati pada remaja dengan FXS, variabilitas yang lebih besar pada total waktu tidur, kesulitan dalam pemeliharaan tidur, dan secara signifikan produksi 20 melatonin pada anak laki-laki dengan FXS lebih besar pada malam hari. Anak-anak dengan FXS berada pada risiko yang lebih tinggi untuk masalah tidur saat usia muda (~ 3 tahun) dan masalah tidur mungkin terjadi (Hagerman R, 2016). g. Obstructive sleep apnea Obstructive sleep apnea (OSA) ditandai oleh penyempitan aliran udara di oralnasal jalan nafas yang terjadi saat tidur. Penghentian aliran udara lengkap (apnea) atau parsialobstruksi aliran udara (hypopnea) dan pengurangan sementara kadar oksigen otak. Tidur terjadi lebih sering selama rapid eye movement (REM) dan jarang ada gerakan tubuh. Prevalensi OSA di antara anak normal adalah sekitar 0,8% sampai 2,8%; Namun, bisa lebih tinggi lagi anak-anak dengan masalah pengembangan saraf pada FXS. Gejala terkait OSA termasuk mendengkur, apnea, terbangun dengan napas terengah-engah, enuresis dan kantuk di siang hari. OSA pada anak-anak adalah terkait dengan konsentrasi yang rendah, kemampuan mengurangi pembelajaran, fungsi kognitif yang rendah, dan kesulitan sekolah. Kelemahan kewaspadaan dan defisit neuropsikologis adalah salah satu gejala utama yang terlihat di OSA. Beberapa studi menunjukkan bahwa gangguan kewaspadaan disebabkan kebanyakan hipoksemia nokturnal. Sebagai tambahannya masalah kognitif, sejumlah besar penelitian menemukan OSA dikaitkan dengan masalah medis seperti perubahan jaringan jantung serta tekanan darah sistolik dan diastolik. Anakanak dengan OSA dan tonsil hipertrofi cenderung mensekresi aspirasi orofaringeal yang bisa menyebabkannya pneumoenia. Asosiasi GERD dengan OSA telah didokumentasikan sebelumnya, mungkin karena lebih tinggi Tekanan negatif esofagus yang ditimbulkan oleh pernafasan yang meningkat (Hagerman R, 2016). h. Strabismus Strabismus adalah salah satu karakteristik fenotipik di FXS dan itu adalah kelainan motilitas ocular dan penyimpangan mata dari penglihatan binokular. Strabismus lebih baik didefinisikan sebagai eksotropia, esotropia, hipotropia, dan hipertropi yang menggambarkan orientasi mata. Exotropia adalah yang paling umum jenis strabismus yang ditemukan di FXS dan diperkirakan disebabkan oleh nada asimetris ekstraokular otot. sebuah studi FXCRC baru-baru ini melaporkan prevalensi 17,5%. Tingkat awal yang lebih tinggi dianggap terkait dengan bias seleksi sebelumnya studi. Meski begitu, prevalensinya pun signifikan lebih tinggi dari prevalensi pada anak-anak biasa (2,6% vs 4%) (Hagerman R, 2016). 21 i. Tic disorder Kelainan tics umumnya diklasifikasikan menurut usia , durasi, dan tingkat keparahan gejala dan adanya vokal dan / atau motorik. Edisi kelima dari Manual Diagnostik dan Statistik Gangguan Mental (DSM-5) mencantumkan tiga jenis Kelainan tic : Sindrom Tourette (TS), motor kronis atau gangguan vokal tic, dan transient tic disorder. Prevalensi gangguan tic transient di Indonesia Anak usia 13-14 tahun adalah dari 3-15% dan kronis motorik berkisar antara 2-5% (134-136); Namun, Kelainan tic mungkin lebih sering terjadi dari prevalensi yang dilaporkan karena banyak pasien dengan tics tidak menjadi perhatian medis (Hagerman R, 2016). Kelainan tic adalah ditandai dengan tidak disengaja, mendadak, singkat dan cepat, berulang, tidak berirama, motor tak terduga, tidak berarti dan gerakan stereotip, seperti, mata berkedip, bahu mengangkat bahu dan pembersihan atau bunyi tenggorokan yang dihasilkan dengan menggerakkan udara melalui hidung, mulut atau tenggorokan (phonic atau vokal tics). Tics tidak konstan dan muncul di Aktivitas motorik normal, kecuali kasus sangat parah. Kelainan tics muncul sebelum usia 18 tahun dan terjadi sebelum mengkonsumsi obat perangsang pada FXS (Hagerman R, 2016). 22 2.10 Management Fragile X Sindrom Tabel 2.5 Ringkasan masalah dan manajemen medis Masalah Prevalensi medis Pertumbuhan Umur presentasi Berat lahir rendah - 2-5 tahun - FXCRC: 9% - Penelitian lain: Severity Moderat Komplikasi - Kegemukan Rekomendasi Follow up - Perubahan gaya - Pantau pasien Pertumbuhan otak hidup termasuk berat, tinggi dan yg terlalu cepat diet sehat dan lingkar kepala olahraga di setiap kunjungan 8% Preterm - perlambatan tinggi: untuk meminimalkan - FXCRC: 16% setelah pubertas masalah - Penelitian lain: terkait dengan 12% peningkatan berat Otitis media - FXCRC: 55% Masa kecil Ringan - Sinusitis akut - Pneumococcal dan - Pengawasan - Penelitian lain: - Otitis rekuren vaksin influenza terhadap 45-85% media - Menyusui untuk di berpotensi - memperburuk minimal 4-6 bulan merugikan kognitif dan - Hilangkan paparan efek antibiotik defisit bahasa pasif profilaksis - konduktif untuk asap tembakau termasuk gangguan - Mengurangi dot dan hipersensitivitas 23 pendengaran botol reaksi dan pemakaian gastrointestinal - Terapi antibiotik masala - Penempatan tabung telinga Kejang - FXCRC: 10% Anak usia dini - Penelitian lain: Ringan sampai - perkembangan - Mendidik orang tua - EEG parah dan perilaku dan - Obat darah morbiditas tindak lanjuti pasien spesifik dengan uji sejarah kejang - Hentikan - Carbamazepine pengobatan - asam valproik Setelah pasien 12-18% seizurefree selama 2 tahun kecuali EEG tidak normal Katup mitral - FXCRC: 0,8% Masa kanak – kanak Kebanyakan - jarang mitral - Perbaikan katup - prolaps - Penelitian lain: ke regurgitasi, mitral atau jantung 50% laki-laki masa remaja jantung kongestif pengganti jarang evaluasi dan 20% dari kegagalan dan wajib perempuan endokarditis asimtomatik Surveillance 24 Masalah - FXCRC: 2% -8% Gastrointestinal - Penelitian lain: 11% Masalah tidur Masa kanak – kanak Ringan - Gagal untuk - Agen pengental - Pengawasan di ke berkembang - Antasida tinggi dan berat masa remaja - mudah tersinggung - Histamin-2 blocker - Perilaku - Proton pump masalah inhibitor - FXCRC: 26,9% Bayi dan Ringan sampai - Gangguan - Intervensi perilaku - Pantau sisi - Penelitian lain: masa kecil moderat di siang hari - Melatonin efek tidur kinerja - Clonidine obat-obatan 32% -47% - Perilaku - Sejarah yang masalah cermat kebiasaan tidur Obstructive - FXCRC: 7% sleep apnea - Penelitian lain: 21-32% Masa kecil Sedang sampai - kewaspadaan - Steroid untuk - Monitoring dan parah penurunan nilai dan mengurangi tonsil mengelola neuropsikologis hipertrofi obstruktif defisit - Jalan nafas positif apnea tidur di setiap - Penurunan di hari terus-menerus kunjungan anak kinerja waktu tekanan - Rujuk untuk tidur - kenaikan - Bedah intervensi spesialis perilaku termasuk masalah tonsilektomi 25 - Terapi perilaku Strabismus - FXCRC: 17% - Penelitian lain: 8% Anak usia dini Ringan sampai moderat - Amblyopia - Kacamata korektif - Latihan latihan visual - Operasi - FXCRC: 6% - Penelitian lain: 15% Sebelum 18 tahun Ringan - Biasanya tidak rumit - Pendidikan dan suportif pendekatan - Obat jarang perlu Toileting issues 49% Tertunda beberapa tahun Ringan sampai moderat - Enuresis - Encopresis Sensory integration problem Anak usia dini Sedang sampai parah Tic disorder 20% -50% Sumber : (Hagerman R, 2016 - Terapi perilaku - Desmopressin - Serat suplemen dalam kasus sembelit - Kurangnya - Pengobatan yang ikut serta dalam terkait dengan kegiatan yang kurang perhatian, diperlukan untuk otak cemas, pengembangan agresi dan otonom gejala - Terapi OT - Komprehensif oftalmologi pemeriksaan setiap anak dengan FXS by usia 4 atau lebih cepat jika strabismus terdeteksi - Jangka panjang hubungan dengan memperbaiki pasien selfesteem dan coping dengan tics mereka - Konseling toilet dengan usia 1 tahun - alat penilaian seperti sensorik kuesioner profil, dll. 26