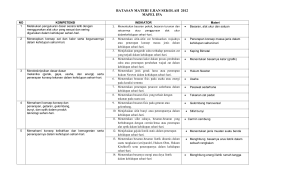
5. Hukum hukum pada Termodinamika
advertisement

Hukum hukum pada Termodinamika Oleh: 1. Muhammad Iqbal 2. Muhammad Syah Dau H. 3. Nury Akbar 4. Mutia Salfa 5. Patricia Sulia 6. Raden Bima Termodinamika Termodinamika adalah ilmu pengetahuan yang mempelajari transformasi dari berbagai bentuk energo,pembatasan-pembatasan dalam transformasi ini serta penggunannya. Termodinamika didasarkan atas dua postulat pokok yang dikenal sebagai hukum pertama dan hukum kedua. Hukum pertama menyangkut masalah pertukaran energy, sedangkan hukum kedua membahas arah dari pertukaran tersebut. 1. Entalpi (H) Entalpi (H) adalah jumlah energi yang dimiliki sistem pada tekanan tetap. Entalpi (H) dirumuskan sebagai jumlah energi yang terkandung dalam energi sistem (E) dan kerja (W). Dimana : H=E+W H = entalpi E = energi sistem W = kerja dengan W = P V P = Tekanan V = Volume 2. Perubahan Entalpi (ΔH) Perubahan isi kalor/entalpi yang terjadi selama proses penambahan atau pelepasan kalor disebut perubahan entalpi : ΔH = Hakhir – Hawal Pada reaksi ; Maka, A → B ΔH = HB - HA a. Bila H produk/B > H reaktan/A, maka ΔH bertanda positif, berarti terjadi penyerapan kalor dari lingkungan ke sistem. b. Bila H reaktan/A > H produk/B, maka ΔH bertanda negatif, berarti terjadi pelepasan kalor dari sistem ke lingkungan. Sistem dapat dikelompokkan menjadi: a. Sistem terbuka: sistem di mana dapat terjadi pertukaran materi dan energi antara sistem dan lingkungan. b. Sistem tertutup: sistem di mana dapat terjadi pertukaran energi, tetapi tidak dapat terjadi pertukaran materi antara sistem dan lingkungan. c. Sistem terisolasi: sistem di mana tidak dapat terjadi pertukaran materi maupun energi antara sistem dan lingkungan. Berdasarkan perubahan entalpinya, reaksi kimia dibedakan menjadi dua, yaitu: a. Reaksi eksoterm: 1) 2) 3) 4) Reaksi yang melepaskan panas. Panas berpindah dari sistem ke lingkungan. ΔH = negatif (–) H akhir < H awal Contoh : H2 + O2 → H2O ΔH = - 270 kJ b. Reaksi endoterm: 1) 2) 3) 4) Reaksi yang menyerap panas. Panas berpindah dari lingkungan ke sistem. ΔH = positif (+) H akhir > H awal Contoh : H2O →H2 + O2 ΔH = + 270 kJ Harga perubahan entalpi reaksi eksoterm dan endoterm dalam reaksi yang sama adalah kebalikannya : ΔH eksoterm = - ΔH endoterm Berbagai macam perubahan entalpi diukur pada kondisi standar, yaitu pada suhu 25oC (298 K) dan tekanan 1 atm dinyatakan dalam satuan kJ dan perubahan entalpi molar dalam satuan kJ/mol. a. Perubahan Entalpi Pembentukan Standar (ΔHf0) Adalah perubahan entalpi yang terjadi pada pembentukan 1 mol senyawa dari unsur-unsurnya pada kondisi standar. Contoh : 1. Reaksi pembentukan air (H2O) H2 + O2 → H2O ΔHf0 = - 270 kJ 2. Reaksi pembentukan HN3 N2 + H2 → NH3 ΔHf0 = + 300 kJ Contoh soal : Diketahui reaksi termokimia : 1. H2 + I2 → 2 HI ΔH = - 650 kJ 2. N2 + 2 O2 → 2 NO2 ΔH = + 245 kJ Tentukan reaksi pembentukkan standar dari reaksi di atas ! Jawab : 1. H2 + I2 → 2 HI ΔH = - 650 kJ H2 + I2 → 2 x HI H2 + I2 → HI 2. N2 + 2 O2 → 2 NO2 N2 + 2 x O2 → 2 x ΔHf0 = - kJ = - 325 kJ ΔHf0 = - 325 kJ ΔH = + 245 kJ NO2 N2 + O2 → NO2 ΔHf0 = + 245 x kJ = + 122,5 kJ ΔHf0 = + 122,5 kJ b. Perubahan Entalpi Penguraian Standar (ΔHd0) Adalah perubahan entalpi yang terjadi pada penguraian 1 mol senyawa menjadi unsur-unsurnya pada kondisi standar. Contoh : 1. Reaksi penguraian air (H2O) H2O →H2 + O2 ΔHd0 = + 270 kJ 2. Reaksi pembentukan HN3 NH3 → N2 + H2 ΔHd0 = - 300 kJ Contoh soal : Diketahui reaksi termokimia : 1. 2 HI → H2 + I2 ΔH = + 650 kJ 2. 2 NO2 →N2 + 2 O2 ΔH = - 245 kJ Tentukan reaksi penguraian standar dari reaksi di atas ! Jawab : 1. 2 HI → H2 + I2 2 x HI → H2 + I2 HI → H2 + I2 2. 2 NO2 → N2 + 2 O2 2x NO2 → N2 + 2 x NO2 → N2 + O2 ΔH = + 650 kJ ΔHd0 = + kJ = + 325 kJ ΔHd0 = + 325 kJ ΔH = - 245 kJ O2 ΔHd0 = - 245 x kJ = - 122,5 kJ ΔHd0 = - 122,5 kJ c. Perubahan Entalpi Pembakaran Standar (ΔHc0) Adalah perubahan entalpi yang terjadi pada pembakaran 1 mol zat pada kondisi standar. Contoh : Tentukan reaksi termokimia pembakaran alkohol standar jika ΔHc0 C2H5OH = - 560 kJ ! Jawab : C2H5OH + 2 O2 → 2 CO2 + 3 H2O ΔHc0= - 560 kJ d. Perubahan Entalpi Penguapan Standar Adalah perubahan entalpi yang terjadi pada penguapan 1 mol zat dari fase cair menjadi fase gas pada kondisi standar. Contoh : H2O (l) → H2O (g) ΔH = + 250 kJ e. Perubahan Entalpi Netralisasi Adalah perubahan entalpi yang terjadi pada penetralan 1 mol asam oleh basa atau 1 mol basa oleh asam pada kondisi standar. Contoh : NaOH + HCl → NaCl + H2O ΔH = - 199 kJ Selain kalor reaksi di atas masih terdapat berbagai kalor reaksi yang lain, yaitu: a. Kalor pelarutan, adalah kalor reaksi yang menyertai pelarutan 1 mol zat menjadi larutan encer. Contoh : NaOH (s) → Na+ (aq) + OH- (aq) ΔH = + 89 kJ b. Kalor peleburan, adalah kalor reaksi yang menyertai perubahan 1 mol zat dari padat menjadi bentuk cair pada titik leburnya. Contoh : C12H22O11 (s) → C12H22O11 (l) ΔH = + 1700 kJ Penerepan Hukum Laplace Hukum Laplace Hukum ini diajukan oleh Marquis de Laplace dan dia menyatakan bahwa jumlah kalor yang dilepaskan dalam pembentukan sebuah senyawa dari unsur-unsurnya sama dengan jumlah kalor yang dibutuhkan untuk menguraikan senyawa tersebut menjadi unsurunsurnya. Panjabaran dari hukum ini untuk entalphi reaksi ΔH dan kalor reaksi; C + O2 → CO2 ΔH = -94 Kkal CO2 → C + O2 ΔH = +94 Kkal Sedangkan untuk kalor reaksi, C + O2 → CO2 -94 Kkal CO2 → C + O2 +94 Kkal Untuk reaksi pertama, unsur C bereaksi dengan gas oksigen menghasilkan karbondioksida dan kalor sebesar 94 Kkal. Sedangkan reaksi kedua karbondioksida terurai menjadi unsur C dan gas oksigen dengan membutuhkan kalor sebesar 94 Kkal. Dari sisi tanda, tampak jelas perbedaan antara entalphi reaksi dengan kalor reaksi, jika entalphi bernilai positif maka kalor reaksi bernilai negatif, demikian pula sebaliknya jika entalphi negatif maka kalor reaksi positif. Hukum Hess Hukum ini diajukan oleh Germain Hess, dia menyatakan bahwa entalphi reaksi (ΔH) hanya tergantung pada keadaan awal reaksi dan hasil reaksi dan tidak bergantung pada jalannya reaksi. Jika suatu reaksi merupakan penjumlahan aljabar dari dua atau lebih reaksi, maka perubahan entalphi (ΔH) atau kalor reaksinya juga merupakan penjumlahan aljabar dari (ΔH) yang menyertai reaksi. Untuk lebih mudah memahaminya kita perhatikan Bagan 10.17. Bagan 10.17. Penjumlahan aljabar reaksi dan entalphi menurut Germain Hess Berdasarkan persamaan reaksi gas karbon dioksida dapat terbentuk melalui dua tahap, yang pertama pembentukan karbonmonoksida dari unsur-unsurnya dan dilanjutkan dengan oksidasi dari karbonmonoksida menjadi karbondioksida. Penjumlahan aljabar ΔHreaksi dari setiap tahap reaksi juga dilakukan sesuai dengan tahap reaksi, maka ΔHreaksi dari pembentukan gas Karbon dioksida juga dapat dilakukan. Berdasarkan berbagai jenis reaksi, maka kita juga dapat mengembangkan jenis kalor reaksi atau ΔH yang disesuaikan dengan jenis reaksinya, ada empat jenis kalor reaksi yaitu kalor reaksi pembentukan, penguraian, pembakaran dan pelarutan. Keempat klasifikasi tersebut disederhanakan dalam bagan pada Bagan 10.18.