Chapter 20 Carboxylic Acids
advertisement

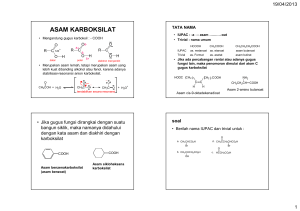
Chapter 20 ASAM KARBOKSILAT Pengantar • Gugus fungsi dari asam karboksilat terdiri atas ikatan C=O dengan –OH pada karbon yang sama. • Gugus karboksil biasanya ditulis -COOH. • Asam alifatik memiliki gugus alkil terikat pada -COOH. • Asam aromatik memiliki gugus aril. • Asam lemak merupakan rantai panjang asam alifatik. Robby Noor Cahyono, S.Si., M.Sc. 2 TATA NAMA UMUM • Asam alifatik banyak memiliki nama sejarah. • Posisi substituen pada rantai diberi label dengan huruf Yunani. α-asam klorobutirat β-asam fenilkaprat Robby Noor Cahyono, S.Si., M.Sc. 3 TATA NAMA IUPAC • Hapus –a dari nama alkana (atau alkena), tambahkan –oat dan diberi awalan asam. • Karbon dari gugus karboksil diberi nomor 1. asam 2-klorobutanoat trans-3-fenil-2-propenoat asam (asam sinamat) Robby Noor Cahyono, S.Si., M.Sc. 4 Penamaan Asam Siklik • Sikloalkana terikat pada-COOH yang dinamakan sebagai asam karboksilat sikloalkana. • Asam aromatik disebut sebagai asam benzoat. Asam 2-isopropilsiklopentanakarboksilat asam o-hidroksibenzoat (asam salisilat) Robby Noor Cahyono, S.Si., M.Sc. 5 Asam Dikarboksilat • Asam dikarboksilat alifatik biasanya disebut dengan nama-nama umumnya (untuk diingat) • Untuk tata nama IUPAC, penomoran rantai dari ujung paling dekat dengan suatu substituen. • Dua gugus karboksil pada cincin benzena menunjukkan asam ftalat. Asam 3-bromoheksadioat Asam β-bromoadipat Robby Noor Cahyono, S.Si., M.Sc. 6 Struktur karboksil • Hibridisasi karbon adalah sp2. • sudut ikat dekat dengan 120°. • O-H tumpang tindih dengan C=O, untuk mendapatkan orbital π tumpang tindih dengan orbital pasangan elektron bebas pada oksigen. Robby Noor Cahyono, S.Si., M.Sc. 7 Titik Didih Titik didihnya lebih tinggi dari alkohol yang setara, terjadi karena pembentukan dimer. Asam asetat, t.d. 118°C Robby Noor Cahyono, S.Si., M.Sc. 8 Titik Lebur • Asam alifatik dengan karbon lebih dari 8 berbentuk padat pada suhu kamar. • Ikatan rangkap (terutama cis) menurunkan titik leleh. Catatan asam 18-C: ¾Asam stearat (jenuh): 72° C ¾Asam oleat (satu ikatan rangkap cis): 16 °C ¾Asam linoleat (dua cis ikatan ganda): -5 °C Robby Noor Cahyono, S.Si., M.Sc. 9 Kelarutan • Kelarutan air menurun dengan bertambah panjang rantai karbon. • Sampai dengan 4 karbon, asam larut dalam air. • Lebih larut dalam alkohol. • Juga larut dalam pelarut yang relatif nonpolar seperti kloroform karena larut sebagai dimer. Robby Noor Cahyono, S.Si., M.Sc. 10 Keasaman Robby Noor Cahyono, S.Si., M.Sc. 11 Stabilisasi Resonansi Robby Noor Cahyono, S.Si., M.Sc. 12 Efek Substituen Pada Asam pKa = 4.46 pKa = 4.19 pKa = 3.47 pKa = 3.41 Robby Noor Cahyono, S.Si., M.Sc. pKa = 2.16 => 13 Garam dari Asam Karboksilat • Sodium hidroksida menghilangkan sebuah proton untuk membentuk garam. • Menambahkan asam kuat, seperti HCl, akan menghasilkan asam karboksilat kembali. => Robby Noor Cahyono, S.Si., M.Sc. 14 Penamaan Garam Asam • Nama kation. • Kemudian nama anion. potassium β-klorovalerat potassium 3-kloropentanoat Robby Noor Cahyono, S.Si., M.Sc. 15 Sifat Asam Garam • Biasanya bentuk padat dengan bau tak sedap • Garam karboksilat Na+, K+, Li+, dan NH4+ yang larut dalam air. • Sabun adalah garam natrium yang larut dari asam lemak rantai panjang • Garam dapat dibentuk oleh reaksi asam dengan NaHCO3,melepaskan CO2. Robby Noor Cahyono, S.Si., M.Sc. 16 Pemurnian Asam Robby Noor Cahyono, S.Si., M.Sc. 17 Beberapa Asam Penting • Asam asetat dalam cuka dan makanan lain, digunakan industri sebagai pelarut, katalis, dan reagen untuk sintesis. • Asam lemak dari lemak dan minyak. • Asam benzoat dalam obat-obatan, pengawet. • Asam adipat digunakan untuk membuat nilon 66. • Asam Ftalat digunakan untuk membuat poliester Robby Noor Cahyono, S.Si., M.Sc. 18 Review Sintesis • Oksidasi dari alkohol primer dan aldehida dengan asam kromat. • Pemutusan dari suatu alkena dengan KMnO4 panas menghasilkan asam karboksilat jika ada hidrogen pada karbon ikatan rangkap. • Alkil benzena dioksidasi menjadi asam benzoat oleh KMnO4 panas atau asam kromat panas. Robby Noor Cahyono, S.Si., M.Sc. 19 Sintesis Grignard Reagen Grignard menghasilkan CO2+ garam karboksilat. => Robby Noor Cahyono, S.Si., M.Sc. 20 Hidrolisis Nitril Hidrolisis asam atau basa dari nitril menghasilkan asam karboksilat. => Robby Noor Cahyono, S.Si., M.Sc. 21 Turunan Asam • Gugus fungsi terikat pada karbon asil menentukan kelompok senyawa: ¾-OH, asam karboksilat ¾-Cl, klorida asam ¾-OR’, ester ¾-NH2, amida • Perubahan ini melalui substitusi asil nukleofilik. Robby Noor Cahyono, S.Si., M.Sc. 22 Esterifikasi Fischer • • • • Asam + alkohol menghasilkan ester + air. Asam mengkatalisis nukleofil lemah. Semua tahap berjalan reversibel. Reaksi mencapai ketimbangan. => Robby Noor Cahyono, S.Si., M.Sc. 23 Mekanisme Fischer (1) Protonasi karbonil dan serangan alkohol, (sebuah) nukleofil lemah. Robby Noor Cahyono, S.Si., M.Sc. 24 Mekanisme Fischer (2) Protonasi –OH dan pelepasan air. Robby Noor Cahyono, S.Si., M.Sc. 25 Klorida Asam • Bentuk aktif dari asam karboksilat . • Klorida adalah gugus pergi yang baik, sehingga mudah mengalami substitusi asil. • Untuk mensintesis klorida asam digunakan tionil klorida atau oksalil klorida dengan asam. Robby Noor Cahyono, S.Si., M.Sc. 26 Ester dari Klorida Asam • Klorida asam bereaksi dengan alkohol untuk menghasilkan ester dengan hasil yang baik. • Mekanismenya adalah adisi nukleofilik oleh alkohol pada gugus karbonil, ion klorida lepas,kemudian deprotonasi. Robby Noor Cahyono, S.Si., M.Sc. 27 Amida dari Klorida Asam • Klorida asam bereaksi dengan amonia dan amina untuk menghasilkan amida. • Basa (NaOH atau piridin) ditambahkan untuk menetralkan HCl yang dihasilkan. Robby Noor Cahyono, S.Si., M.Sc. 28 Diazomethana • CH2N2 bereaksi dengan asam karboksilat untuk menghasilkan ester metil kuantitatif. • Sangat beracun, eksplosif. Larut dalam eter. Robby Noor Cahyono, S.Si., M.Sc. 29 Mekanisme Diazomethana Robby Noor Cahyono, S.Si., M.Sc. 30 Amida dari Asam • Amina (basa) mengambil sebuah proton dari asam karboksilat membentuk suatu garam. • Memanaskan garam di atas 100°C menghasilkan uap dan bentuk amida. Robby Noor Cahyono, S.Si., M.Sc. 31 Reduksi Menjadi Alkohol Primer • Menggunakan reduktor kuat, LiAlH4. • Borana, BH3 dalam THF, mereduksi asam karboksilat menjadi alkohol, namun tidak mereduksi keton. Robby Noor Cahyono, S.Si., M.Sc. 32 Reduksi Menjadi Aldehid • Sulit menghentikan reduksi pada aldehid. • Menggunakan bentuk yang lebih reaktif dari asam (klorida asam) dan reduktor lemah, litium alumunium tri(t-butoksi)hidrida. Robby Noor Cahyono, S.Si., M.Sc. 33 Alkilasi Membentuk Keton Satu mol asam karboksilat bereaksi dengan 2 mol organolitium. Robby Noor Cahyono, S.Si., M.Sc. 34