Penggunaan Katalis Asam Fosfat Pada Reaksi Esterifikasi Asam p
advertisement

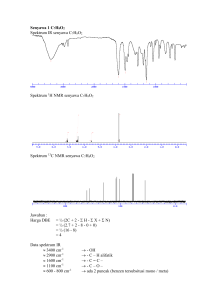
Penggunaan Katalis Asam Fosfat Pada Reaksi Esterifikasi Asam p-Kumarat Ihsan Charismawan, Firdaus, Nunuk Soekamto Program Studi Kimia FMIPA Unhas Abstrak Penelitian tentang penggunaan katalis asam fosfat di dalam reaksi sintesis metil p-kumarat dari asam p-kumarat dengan metanol telah dilakukan. Reaksi berlangsung di dalam alat Dean Strark trap pada suhu 59 ̊C selama 36 jam menghasilkan kristal metil p-kumarat dengan titik leleh 138-139 ̊C dan rendamen sebanyak 66,21%. Karakterisasi senyawa menggunakan analisis TLC, pengukuran titik leleh, dan data spektroskopi FT IR, 1H dan 13C-NMR. Kata Kunci: p-kumarat, metil p-kumarat, metanol, asam fosfat, esterifikasi Abstract Research about phosphoric acid as catalyst in synthesis reaction of methil p-coumaric from p-coumaric acid and methanol have been done. The reaction was conducted using dean strark trap apparatus, temperature was 59 ̊C for 36 hours gave methil p-coumaric as white cristall with melting point 138-139 ̊C and 66,21% yield. The product compound was characterized using TLC analysis, melting point, and spectroscopic data of FT-IR, 1H and 13C-NMR. Keywords: p-coumaric acid, methyl p-coumaric, methanol, phosphoric acid, esterification PENDAHULUAN Senyawa sinamamida adalah salah satu kelompok senyawa fenolik yang sangat penting dan banyak diteliti karena sifat bioaktivitasnya yang sangat tinggi. Studi tentang epidemik telah menunjukkan bahwa konsumsi makanan yang kaya akan senyawa fenolik dapat memberikan korelasi penurunan timbulnya penyakit kardiovaskular (Criqui dan Rinngel, 1994). Hal ini terjadi karena senyawa fenolik dapat memperlambat proses penyempitan pembuluh nadi dengan berfungsi sebagai antioksidan terhadap lipoprotein-LDL dan menetralkan radikal bebas pada daerah yang mengalami tekanan oksidasi (Frankel dkk., 1993; Meyer dkk., 1998) Firdaus dkk. (2009) mensintesis senyawa p-kumaramida dari asam p-kumarat, kemudian melakukan pengujian terhadap sel tumor leukemia P-388. Hasil pengujian terhadap sel tumor leukemia P-388 menunjukkan senyawa p-kumaramida memiliki aktivitas biologis yang menarik, dengan IC50 = 44 μg/mL. Menurut Anderson (1990), senyawa memiliki aktivitas antikanker yang kuat jika nilai IC50 ˂ 20 μg/mL. Beragam bioaktivitas dari sinamamida mendorong banyaknya penelitian untuk menemukan senyawa-senyawa turunan sinamamida yang mempunyai aktivitas farmakologi yang tinggi dan toksisitas yang rendah (Widyarmoko dan Arie, 2006). Salah satu senyawa turunan sinamamida yang berhasil diisolasi dari ekstrak etil asetat kulit akar K. hospita Linn adalah senyawa p-kumaramida(phidroksisinamamida). Senyawa ini memperlihatkan aktivitas yang cukup tinggi terhadap udang A. salina (180,53 μg/ml) sehingga dapat diduga memiliki potensi sebagai antitumor (Ilyas, 2008). Akan tetapi kandungan senyawa p-kumaramida dalam kulit akar kayu K. hospita Linn relatif sangat kecil (1,6 ppm) (Ilyas, 2008). Metode lain yang dapat dilakukan untuk mendapatkan senyawa turunan p-kumaramida adalah dengan mensintesis senyawa tersebut, salah satu jalur sintesis adalah melalui reaksi esterifikasi turunan p-kumaramida dengan menggunakan asam p-kumarat sebagai kerangka dasar, dilanjutkan dengan reaksi amidasi. Menurut Kadu dkk (2011), reaksi eseterifikasi dapat dilakukan dengan atau tanpa katalis, namun untuk mendapatkan hasil yang optimum harus menggunakan katalis dan dapat berjalan baik jika dalam suasana asam. Katalis yang sangat sering digunakan untuk reaksi esterifikasi adalah seperti asam mineral kuat, garam, dan resin penukar kation. Katalis asam yang juga biasa digunakan pada reaksi esterifikasi adalah seperti, H2SO4, H3BO3, H3PO4, HCl dan H+ (Pinto dkk., 2005). Asam sulfat paling banyak digunakan dalam industri karena memberikan konversi tinggi dan laju reaksi yang relatif cepat. Asam klorida banyak dipakai untuk skala laboratorium, namun jarang dipakai untuk skala industri karena sangat korosif. Asam fosfat jarang digunakan sebagai katalis dalam industri karena memberikan laju reaksi yang relatif lambat, namun penggunaan dan penanganannya di laboratorium lebih mudah serta lebih ramah lingkungan. Akan tetapi, pada reaksi esterifikasi olefinil pkumaramida, ikatan rangkap dikhawatirkan akan terbuka pada penggunaan katalis H2SO4 menghasilkan bentuk karbokation yang dapat diserang lebih lanjut oleh nukleofilik. Gambar 1. Pengaruh H2SO4 terhadap ikatan olefinil p-kumaramida METODOLOGI Bahan. Bahan-bahan yang digunakan pada penelitian ini adalah asam p-kumarat p. a, H3PO4, silika gel 7733, pipa kapiler, plat KLT, akuades, kloroform p. a, metanol p. a, etil asetat p. a, nheksana p. a, aseton p. a, benzena p. a, HCl 2 M, Na2SO4 anhidrat, etanol p. a, Na2CO3, kertas saring whatman 42, kertas pH universal dan kertas saring biasa. Alat. Alat-alat yang digunakan pada penelitian ini adalah labu alas bulat leher tiga, kondensor, o termometer 100 C, neraca analitik, spektrofotometer IR (Shimadzu seri FTIR8201PC), NMR, heating stirrer, dean-stark apparatus, melting point apparatus, lampu KLT, evaporator, corong Buchner, dan alat-alat gelas yang umum digunakan dalam laboratorium. Prosedur. Asam p-kumarat sebanyak 0,5 gram (3 mmol) ditambahkan dengan metanol sampai larut dan 1,4 mL (27 mmol) H3PO4 pekat (97%), perhitungan dapat dilihat pada Lampiran 2. Larutan tersebut dimasukkan ke dalam labu alas bulat leher tiga kemudian direfluks pada suhu 59 ̊C selama 12, 24, dan 36 jam reaksi (analisis dengan KLT tiap 3 jam). Setelah direfluks larutan didinginkan pada suhu kamar kemudian dinetralkan dengan Na2CO3, dicuci dengan aquades kemudian fase airnya diekstraksi dengan kloroform (2x20 mL) fase organik yang diperoleh digabung, dikeringkan dengan Na2SO4 anhidrat, lalu dievaporasi sampai diperoleh kristal putih. Endapan putih tersebut direkristalisasi panas menggunakan kloroform : n-heksana (1:2) sampai diperoleh kristal murni, selanjutnya diukur titik lelehnya, dianalisis dengan KLT dan diukur dengan spektroskopi FTIR, 1H-NMR dan 13 C-NMR. Hasil dan Pembahasan Hasil reaksi esterifikasi asam p-kumarat menggunakan katalis asam fosfat, dilakukan dengan metode Dean stark trap dan melibatkan benzena sebagai pemindah air secara azeotrop antara benzena dan air adalah metil p-kumarat berdasarkan uji KLT, titik leleh, dan elusidasi struktur. Beberapa foto dokumentasi penelitian dapat dilihat pada Lampiran 4. Reaksi katalisis asam fosfat mula-mula dilakukan selama 12 jam dan didapatkan hasil dengan kromatogram seperti pada Gambar 2a yang menunjukkan reaktan masih ada sehingga reaksi dilanjutkan sampai 24 jam. Kromatogram hasil analisis KLT dapat dilihat pada didapatkan seperti Gambar 2b menunjukkan reaktan masih terisisa sedikit. Reaksi dilanjutkan sampai mencapai 36 jam dan dilakukan analisis KLT yang terlihat satu noda pada Gambar 2c yang berarti reaksi telah selesai. Proses kirstalisasi dan rekristalisasi hasil reaksi dan diperoleh kristal putih dengan titik leleh 138-139 ̊C yang menandakan kemurniannya dan rendamen sebesar 66,21% (0,3539 gr). Gambar 2. Kontrol waktu refluks menggunakan KLT (kloroform:etil asetat 7:3) (a) 12 jam pertama, (b) 24 jam kemudian, (c) 36 jam terakhir Pada umumnya, reaksi esterifikasi adalah reaksi kesetimbangan sehingga perlu dilakukan usaha untuk memindahkan produknya sesaat setelah terbentuk. Pada reaksi esterifikasi asam p-kumarat yang telah dilakukan, salah satu produknya adalah air. Pemindahan air dari sistem reaksi dilakukan dengan metode distilasi azeotropik dengan benzena menggunakan Dean Stark trap. Campuran azeotrop air-benzenametanol menguap pada suhu 58 oC. Adanya air pada Dean Stark trap menunjukkan bahwa reaksi telah berlangsung. Tidak bertambahnya produk air pada Dean Stark trap mengindikasikan bahwa reaksi telah selesai. Pada penelitian ini, pembentukan air berhenti setelah dilakukan refluks selama 36 jam. Reaksi ini berjalan lambat disebabkan karena adanya ikatan rangkap terkonjugasi yang dapat menstabilkan karbon karbonil setelah terprotonasi. Campuran reaksi dinetralkan dengan K2CO3 untuk menghindari terjadinya ionisasi ester pada pH asam serta untuk menghilangkan garam yang terdapat pada campuran. Produk yang diperoleh berupa kristal berwarna putih dengan titik leleh sebesar 138139 ̊C berpendar hitam di bawah lampu UV λ 254 nm. Uji kemurnian dilakukan menggunakan analisis KLT dengan tiga macam perbandingan eluen. Kromatogram hasil analisis KLT sebagai uji kemurnian kristal ditunjukkan pada Gambar 4. Analisis KLT hasil rekristalisasi menggunakan pelarut n-heksana:etil asetat (7:3), n-heksana : aseton (5:5), kloroform : etil asetat (7:3), masing-masing memperlihatkan satu noda pada kromatogramnya (Gambar 3). Spektrum FTIR yang didapatkan menunjukkan adanya gugus karbonil (C=O) ester yang khas memberikan pita serapan berintensitas kuat pada bilangan gelombang 1687,71 cm-1 dan didukung oleh serapan pada 1199,72 cm-1 dan 1172,72 cm-1 yang menandakan adanya gugus C-O ester. Gugus hidroksil (-OH) pada cincin fenil ditunjukkan oleh spektrum pada 3379,29 cm-1. bilangan gelombang Gambar 3. Uji kemurnian padatan menggunakan eluen berbeda (a) n-heksana:etil asetat (7:3); (b) n-heksana:aseton (5:5); (c) kloroform:etil asetat (7:3) Rentangan C-H aromatik ditunjukkan oleh pita serapan pada bilangan gelombang 3045,60 cm-1 dan 3008,95 cm-1 yang didukung adanya serapan C=C aromatik pada 1600,92 cm-1 dan 1514,12 cm-1. Serapan pada 1633,71 cm-1 menunjukkan serapan C=C olefin. Gugus C-H alifatik ditunjukkan oleh pita serapan pada 2951,09 cm1 yang didukung serapan pada 1357,39 cm-1 menunjukkan gugus metil (-CH3). Gambar 4. Spektrum IR senyawa yang diuji Analisis spektrum 1H-NMR senyawa 1 (Gambar 5) menunjukkan pada δ 5,9 ppm terdapat gugus hidroksil (-OH). Pada δ 2,9 ppm (3H, s, H-1) mengindikasikan adanya gugus metil (-CH3) yang berasal dari gugus oksikarbon (-OCH3), hal ini ditunjukkan dari nilai geseran kimia yang lebih besar jika dibandingkan gugus metil yang berikatan dengan karbon. Adanya gugus metil membuktikan bahwa asam p-kumarat telah mengalami esterifikasi. Pada δ 6,8 ppm (2H, d, J = 9 Hz, H-6 dan H-10) dan δ 7,4 ppm (2H, d, J = 9 Hz, H-7 dan H-9) terdapat dua jenis proton ekuivalen yang menunjukkan adanya sistem fenil di-substitusi. Selain itu, pada δ 6,3 ppm (1H, d, J = 16 Hz, H-3) dan δ 7,6 ppm (1H, d, J = 16, H-4) menunjukkan bahwa posisi kedua proton berada dalam geometri trans. H-1 H-7 & H-9 H-6 & H-10 H-3 H-4 -OH Gambar 5. Spektrum 1H-NMR senyawa yang diuji Spektrum 13C-NMR memperlihatkan adanya 8 sinyal yang mewakili 10 karbon. Sinyal ini terdiri atas satu oksikarbon (-OCH3) pada δ 51,87 ppm, satu gugus karbonil (-CO) pada δ 168,27 ppm, dan terdapat 8 karbon sp2 pada geseran di atas 100 ppm yang berasal dari 2 karbon alkena (115,21 ppm C-3 dan 144,94 ppm C-4) dan 6 karbon aromatik C-6 C-10 C-4 C-2 C-8 (127,23; 130,15; 116,05 dan 158,05 ppm). Sinyal pada geseran 116,05 ppm (C-7 dan C-9) dan 130,15 ppm (C-6 dan C-10) menunjukkan intensitas sinyal yang lebih tinggi dibandingkan sinyal lainnya, hal ini mengindikasikan terdapat dua jenis karbon ekuivalen dalam satu sistem cincin fenil di-substitusi. C-7 C-9 C-3 C-5 C-1 Gambar 6. Spektrum 13C-NMR senyawa yang diuji Berdasarkan analisis data spektoskopi FT IR, 1H-NMR, dan 13C-NMR, struktur senyawa yang diuji telah sesuai dengan senyawa target yang diharapkan yaitu metil p-kumarat dengan struktur seperti ditunjukkan pada Gambar 7. Mekanisme reaksi yang dapat terjadi pada pembentukan senyawa metil p-kumarat dapat dilihat pada Gambar 8. Gambar 7. truktur senyawa metil p-kumarat Gambar 8. Reaksi pembentukan metil p-kumarat dari asam p-kumarat dengan metanol KESIMPULAN Senyawa metil p-kumarat (t.l 138-139 o C) dapat disintesis melalui reaksi esterifikasi asam p-kumarat dengan metode Dean Strak trap dengan perbandingan 3 mmol asam p-kumarat dengan 3 mmol metanol menggunakan 27 mmol katalis asam fosfat pada suhu refluks 59 oC selama 36 jam dengan rendamen sebanyak 66,21% (0,3539 gr). DAFTAR PUSTAKA Anderson, J. E., Goetz, C. M., and McLaughlin, J. L., 1990, A Blind Comparison of Simple Bench-top Bioassays and Human Tumour Cell Cytotoxicities as Antitumor Prescreen, J. Phytochemical analysis, 6:107 - 111. Crique, M.H., Ringel, B.L., 1994, Does Diet or Alcohol Explain The French Paradox?, Lancet, 344:1719-1723. Firdaus, Soekamto, N. H., dan Karim, A., 2009, Sintesis Senyawa pHidroksinamamida dari Asam p-Kumarat Melalui Reaski Esterifikasi dan Amonolisi, J. Chemica Acta,:Vol. 2:2, 37-43. Frankel, E. N., Kanner, J., German, J. B., Park, E., Kinsella, J. E., 1993, Inhibition of Oxidation of Human Low-Density Lipoprotein by Phenolic Sustances in Red Wine, Lancet., 341:454-457. Ilyas, A., 2008, Isolasi dan Idenfikasi Metabolit Sekunder dari Ekstrat Etilasetat Kulit Akar Tumbuhan Kleinhovia hospita Linn. (Paliasa) dan Uji Toksitasnya Terhadap Artemia salina Leach, Tesis tidak dipulikasikan, Program Pascasarjana Universitas Hasanuddin, Makassar. Kadu, S. S., Kulkarni, S. J. and Tapre, R. W., 2011, Kinetics of Esterificaion of p-tert. butyl Cyclohexanol with Acetic Acid Over Ion Exchange Resin Catalyst, Institute of Technology, Nirma University, Ahmedabad 382-481. Pinto, A. C., Guarieiro, L. L. N., Rezende, M. J. C., Ribeiro, ed N. M., Torres, E. A., Lopes, W. A., de P Pereira, P. A & de Andrade, J. B. 2005. Biodiesel: An overview. Braz Chem Soc 16(6B): 1313-1330. Widyarmoko dan Arie, 2006, Sintesis n-(pBromofenil)-p Metoksisinamamida dari Materi Awal Asam-p-Metoksisinamat: Metode Pereaksi Kopling Disikloheksilkarbodiimida, Universitas Airlangga, Surabaya.