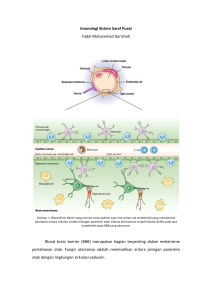
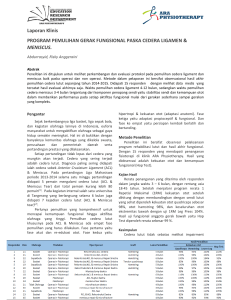
inflammation process and glukoneogenesis process at severe head
advertisement

REVIEW The Indonesian Journal of Medical Science Volume 1 No.6 October 2009 p. 368-379 INFLAMMATION PROCESS AND GLUKONEOGENESIS PROCESS AT SEVERE HEAD INJURY Willy Adhimarta, Asadul Islam Department of Neurosurgery, Medical Faculty, Hasanuddin University Corresponding author: W illy Adhimarta, Department of Neurosurgery, Wahidin Sudirohusodo Hosptal, Jl. Perintis Kemerdekaan 10 Tamalanrea, Makassar 90245, Indonesia. Email: [email protected] ABSTRACT Inflammation proces sincluding cytokine release, adhesion molecule expression and cellular infiltration take a place soon after severe head injury. Moreover, as a response to the head injury, there will be an increase of energy mobilization in the blood (gluconeogenesis). How far the influence of inflammation and the gluconeogenesis on head injury are still not clear. Better understanding about both process will be discussed Keywords: TNF-, glukoneogenesis, head injury. INFLAMASI DAN PROSES GLUKONEOGENESIS PADA CEDERA KEPALA BERAT Proses inflamasi termasuk pelepasan sitokin, ekspresi molekul adhesi dan infiltrasi seluler terjadi segera setelah cedera kepala berat. Selain itu, sebagai respon terhadap cedera, terjadi kenaikan metabolisme dimana bahan bakar mengalami mobilisasi sehingga kadarnya dalam darah meningkat (proses glukoneogenesis). Sejauh mana pengaruh proses inflamasi (TNF-) dan proses glukoneogenesis (katekolamine) pada cedera kepala masih dipertanyakan. Tulisan ini bertujuan untuk membahas lebih mendalam mengenai kedua proses tersebut. Kata Kunci: TNF-, glukoneogenesis, head injury, GFAP PENDAHULUAN Cedera otak akibat kecelakaan lalu lintas pada umumnya berupa multiple system disorders sehingga penanganannya harus secara holistik. Terdapat kecenderungan peningkatan angka kematian dan angka kesakitan akibat cedera otak dan hal ini 368 akan membawa dampak yang besar pada program kesehatan masyarakat secara keseluruhan. Pemahaman menyangkut variabilitas luaran cedera otak membutuhkan kajian yang cermat dan mendalam untuk mengungkapkan Willy Adhimarta, et al. Glukoneogenesis process at severe head injury hubungan antara beratnya cedera awal dan luaran, serta pemahaman bahwa cedera otak merupakan awal dari suatu proses yang bersifat dinamis.1 Kasus cedera kepala berat sering sekali disertai dengan edema otak.2 Edema otak dapat terlokalisasi atau menyeluruh dan dapat terjadi secara primer maupun sekunder yang menyebabkan terjadinya peningkatan volume intrakranial oleh karena meningkatnya jumlah cairan pada jaringan otak dan menyebabkan kematian oleh karena kerusakan sekunder pada batang otak.3,4 Pada kasus trauma lebih sering terjadi edema vasogenik oleh karena peningkatan permeabilitas kapiler. 5 Sedangkan edema sitotoksik lebih sering terjadi pada pasien dengan keadaan hipoksia j aringan saraf oleh karena gagalnya pompa natrium adenosine triphosphate (ATP) pada membran sel, sehingga terjadi penumpukan natrium intraselular.5,6 Penderita cedera otak, terutama cedera otak berat, nampaknya mengalami dua masalah utama yakni kerusakan otak sendiri dan gangguan sistemik yang bersifat tidak langsung, hipermetabolisme yang terjadi berkaitan erat dengan berat ringannya cedera otak.6 Kenaikan tekanan intra kranial atau peradangan otak mempunyai hubungan erat dengan kenaikan metabolisme.6 Demikian pula dengan kenaikan kadar sitokin seperti tumor necrosis factor (TNF-) dan interleukin 1 (IL-1) akan meningkatkan metabolisme dan mempunyai pengaruh terhadap cedera otak sekunder.7,8 Pada cedera otak perlu terj adi keseimbangan antara sitokin yang menimbulkan reaksi inflamasi, dengan tujuan untuk membatasi dan memulihkan kerusakan yang terjadi, serta sitokin anti inflamasi (IL-10) yang membatasi agar kerja dari sitokin inflamasi ini tidak berlebihan, yang bila terjadi justru akan menimbulkan efek yang merugikan. 9 Respon proliferatif dari sel B dan T sangat erat hubungannya dengan besarnya morbiditas dan mortalitas penderita cedera otak.9 Glial Fibrillary Acid Protein(GFAP) didapatkan hanya pada sel glial dan juga astrosit. Peningkatan GFAP pada cedera otak berhubungan dengan beratnya kejadian neurodegeneratif (kerusakan sel otak).10,11 Oleh karena itu, GFAP serum merupakan biomarker yang spesifik untuk kerusakan sel-sel otak, karena pada penderita dengan multitrauma tanpa cedera otak, GFAP tidak ditemukan dalam darah.10,11 Hiperglikemia merupakan kondisi yang umum pada setiap trauma ekstensif, dimana tubuh memberi respon dalam mengatasi cedera, bahan bakar dimobilisasi sehingga kadarnya dalam darah meningkat (proses glukoneogenesis).9,12,13 Berdasarkan fakta tersebut diatas, tulisan ini akan mendiskusikan proses inflamasi (TNF-) dan proses glukoneogenesis (katekolamine) pada pasien cedera kepala berat, dan sejauh mana perannya dalam cedera otak sekunder dan kerusakan jaringan otak yang progresif. PEMBAHASAN Peningkatan angka insidensi cedera kepala di negara berkembang antara lain adalah karena meningkatnya kuantitas sarana transportasi tanpa disertai peningkatan kualitas dan kurangnya disiplin pengguna jalan itu sendiri. Cedera kepala lebih sering terjadi pada laki-laki usia produktif, karena aktivitas dan mobilitas yang lebih tinggi 369 The Indonesian Journal of Medical Science Volume 1 No.6 October 2009 p. 368-379 dibandingkan dengan perempuan. Selain menyebabkan kematian, cedera kepala juga dapat menurunkan produktivitas dan menyebabkan kecacatan yang permanen.2 Cedera otak sekunder dan akibatnya Cedera otak sekunder (COS) mempunyai jalur kaskade yang rumit dan belum semuanya dapat terungkap. Penelitian secara klinis maupun eksperimental terus mencoba untuk menjawab mekanisme sesungguhnya yang terjadi di otak setelah trauma kepala. Pemahaman terhadap cedera kepala sekunder yang lebih lengkap diharapkan dapat mengurangi tingkat kematian dan kecatatan akibat trauma kepala. Tugas penelitian saat ini adalah menemukan terapi invasif maupun noninvasif untuk mengurangi efek cedera otak sekunder.3 Faktor penting yang harus diperhatikan untuk meningkatkan luasan pasien oleh karena cedera kepala adalah kerusakan lebih lanjut pada otak setelah kejadian. Tidak semua kerusakan otak terjadi pada saat cedera. Hal inilah yang menjadi dasar pemikiran mekanisme dari trauma untuk mengklasifikasikan kerusakan otak setelah cedera kepala antara fokal atau difus.2 Pada pasien cedera kepala berat lebih dari 72% mengalami peningkatan tekanan intrakranial. 10 Telah dilaporkan bahwa pasien cedera kepala disertai dengan peningkatan tekanan intrakranial mempunyai hasil yang buruk. Walaupun mekanisme peningkatan tekanan intrakranial dapat menyebabkan defisit neurologis masih belum jelas tetapi telah dibuktikan bahwa peningkatan ini berhubungan dengan penurunan aliran darah ke otak.10 Cedera otak sekunder (COS) adalah cedera otak yang terjadi segera setelah cedera kepala. Hal ini bisa terjadi karena 370 adanya reaksi inflamasi, biokimia, gangguan neurotransmiter, dan gangguan autoregulasi. Bila COP adalah fenomena mekanik, maka COS adalah fenomena metabolik. Penyebab COS ada dua yaitu ekstrakranial (sistemik ) dan intrakranial. 5 Penyebab COS sistemik adalah: hipotensi, hipoksemia, anemia, koagulopati, hipoglikemia, hiperglikemia, hipertermia, dan hiponatremia. Penyebab COS intrakranial adalah: tekanan tinggi intrakranial, kej ang, infeksi, dan vasospasme. Setelah terjadi COP seperti diatas maka akan terjadi COS melalui tiga mekanisme:5 (1) Kerusakan pada neuron otak yang akan menimbulkan efek hipoksia dan iskemia dapat berlanjut menjadi edema sitotoksik, (2) Kerusakan pada vaskular otak yang akan menimbulkan efek massa dan edema vasogenik dan sitotoksik, (3) Kerusakan pada hipotalamus yang akan menimbulkan efek sistemik berupa hiperglikemia, asidosis yang akan memperberat efek hipoksia neuron yang telah ada. Kegagalan pompa ion mengarahkan akumulasi natrium intraselular dan kalium ekstraselular sehingga cairan bergerak kedalam intraselular.7 Rongga intraselular membesar dan rongga ekstraselular mengkerut, pada awalnya tidak mempengaruhi volume otak. Lebih lanjut lagi natrium dari darah masuk kedalam otak dan kalium keluar dari otak masuk kedalam darah yang mengarahkan adanya penumpukan cairan dalam otak. 7 Pada umumnya edema otak terjadi oleh karena respons dari injuri saraf pusat yang dapat diperberat oleh adanya kerusakan pembuluh darah.7 Respon inflamasi Inflamasi merupakan bagian terpenting dari patofisiologi cedera otak traumatika. Willy Adhimarta, et al. Glukoneogenesis process at severe head injury Sitokin yang dilepaskan segera setelah cedera otak akan menimbulkan balans nitrogen negatif dan terjadinya hiperglikemi. 9 Pada suatu kejadian, cedera otak perlu terjadi keseimbangan antara sitokin yang menimbulkan reaksi inflamasi, dengan tuj uan untuk membatasi dan memulihkan kerusakan yang terjadi, serta sitokin anti inflamasi (IL-10) yang membatasi agar kerja dari sitokin inflamasi ini tidak berlebihan, yang bila terjadi justru akan menimbulkan efek yang merugikan.9 Respon proliferatif dari sel B dan T sangat erat hubungannya dengan besarnya morbiditas dan mortalitas penderita cedera otak.9 Jika regulasi yang dilakukan oleh IL-10 kurang maka akan terjadi produksi berlebihan TNF- sehingga terj adi kerusakan jaringan, bersihan jaringan debris yang tidak sempurna serta perjalanan penyakit ke arah kronis.14 Hasil penelitian dari Islam AA (2006) menemukan bahwa IL-10 mempunyai peran yang lebih besar daripada TNF- dalam menentukan luaran penderita cedera otak, karena meskipun kadar TNF meningkat tetapi kadar IL-10 lebih tinggi maka luaran cedera otak akan lebih baik.15 Stimulasi aktivitas adrenergik menyebabkan dilepasnya hormon stres seperti katekolamin sehingga akan meningkatkan laju metabolik, keseimbangan nitrogen negatif, intoleransi glukosa dan resistensi insulin.16 Hiperglikemia merupakan kondisi yang umum pada setiap trauma ekstensif. Akibat aktivasi siklus glukosa-laktatterjadi peningkatan proses glukoneogenesis (alanin dan laktat). Untuk mengatasi cedera tubuh memberi respon dengan cara memobilisasi bahan bakar sehingga kadarnya dalam darah meningkat.9,15 Terjadinya hiperglikemia pada trauma berhubungan dengan hipermetabolisme, sedangkan hipermetabolisme sendiri berkaitan erat dengan berat ringannya cedera otak. Jeremitsky dkk. (2003), mengemukakan bahwa hiperglikemia mempunyai hubungan dengan peningkatan angka mortalitas dan lamanya perawatan dirumah sakit. 17 Dalam penelitian lain, disebutkan tingginya kadar glukosa darah berhubungan dengan hasil luaran yang semakin buruk karena glukosa darah mempunyai hubungan dengan asidosis jaringan otak.18 Biomarker cedera otak Penelitian terhadap biomarker cedera otak terus berlanjut dan laporan terakhir menunjukkan bahwa penelitian banyak terfokus pada pemeriksaan kadar GFAP dalam darah. GFAP yang merupakan protein rantai intermediet dengan berat molekul 45 kD didapatkan hanya pada sel glial dan juga astrosit. Pada cedera otak terjadi pelepasan GFAP dimana kadarnya berhubungan dengan beratnya kejadian neurodegeneratif (kerusakan sel otak). Oleh karena itu, GFAP serum merupakan biomarker yang spesifik untuk kerusakan sel-sel otak.11,18 Respon imun Meskipun otak berbeda dari organ lainnya karena hampir terisolasi sempurna dari aliran darah akibat adanya sawar darah otak, namun tahapan dalam aktivasi sistem imun tidak berbeda jauh dengan organ lainnya. Sejumlah mediator imun dilepaskan dalam beberapa menit setelah trauma otak. Mediator ini akan menuntun terjadinya inflamasi termasuk ekspresi molekul adhesi, infiltrasi seluler dan molekul-molekul inflamasi serta faktor- 371 The Indonesian Journal of Medical Science Volume 1 No.6 October 2009 p. 368-379 faktor pertumbuhan sehingga akan terjadi kematian atau regenerasi sel-sel otak. Masih belum jelas mana inflamasi menguntungkan atau merugikan bagi jaringan otak, dan sejauh mana perannya dalam cedera otak sekunder dan kerusakan otak yang progresif.19-22 Proses inflamasi terjadi segera setelah trauma yang ditandai dengan aktifasi substansi mediator yang menyebabkan dilatasi pembuluh darah, penurunan aliran darah, dan permeabilitas kapiler yang meningkat. Hal ini menyebabkan akumulasi cairan (edema) dan leukosit pada daerah trauma. Sel terbanyak yang berperan dalam respon inflamasi adalah sel fagosit, terutama sel leukosit Polymorphonuclear (PMN), yang terakumulasi dalam 30 - 60 menit yang memfagosit jaringan mati. Bila penyebab respon inflamasi berlangsung melebihi waktu ini, antara waktu 5-6 jam akan terjadi infiltrasi sel leukosit mononuklear, makrofag, dan limfosit. Makrofag ini membantu aktivitas sel PMN dalam proses fagositosis.18, 23-27 Inflamasi, yang merupakan respon dasar terhadap trauma sangat berperan dalam terjadinya cedera sekunder. Pada tahap awal proses inflamasi, akan terj adi perlekatan netrofil pada endotelium dengan beberapa molekul perekat IntraCellular Adhesion Molecules-1 (ICAM-1). Proses perlekatan ini mempunyai kecenderungan merusak/merugikan karena mengurangi aliran dalam mikrosirkulasi. Selain itu, netrofil juga melepaskan senyawa toksik (radikal bebas), atau mediator lainnya (prostaglandin, leukotrin) di mana senyawa-senyawa ini akan memacu terjadinya cedera lebih lanjut. Makrofag juga mempunyai peranan penting sebagai sel radang predominan pada cedera otak.16,28-30 Gambar 1. Patofisiologi Cedera Otak CEDERA OTAK PRIMER Proses Berlanjut Tidak dapat dicegah Neurotransmiter Proses inflamasi Asidosis Opioid Endogen Radikal bebas Hormonal EDEMA SITOTOKSIK Cedera Otak Sekunder Nekrosis / Apoptosis 372 Resusitasi Dapat dicegah Hipoksia (PaO2 ) Iskemia (CBF) Anaerobik Metabolisme Willy Adhimarta, et al. Glukoneogenesis process at severe head injury Gambar 2. Bagan respon tubuh pada trauma (modifikasi dari Evans & ParkBlackwell, 1997) Tipe, lama dan beratnya cedera Makroendokrin Cedera Pain Nekrisis dan inflamasi jaringan Persepsi sensory Pituitary Hypothalamus Catecholamin Cortisol Glucagon INSULIN Hiperglikemi Adrenal Iskemia/hipotensi Hipoksi Infeksi Microendocrine Neutrophil Citokine Macrophage IL1 TNF Respon stress cedera GFAP IL-10 Endothelium Beberapa penelitian memberikan bukti bahwa respon inflamasi pada otak terhadap trauma sangat menonjol dan berperan dalam terjadinya cedera sekunder, sehingga penghambatan reaksi radang akan menghambat pula terjadinya cedera sekunder dan akhirnya memperbaiki luaran penderita.7,20,26 Bila trauma atau infeksi berlangsung terus, maka respon inflamasi akan ditambah dan diperkuat dengan sistem imun selluler dan humoral. Sistem imun ini menghasilkan sitokin yang merupakan polipeptida yang terdiri dari mediator, misalnya interferon, interleukin (IL), tumor nekrosis faktor (TNF), dengan perannya masing-masing.24,32 Peningkatan hormon pada cedera kepala Pada trauma beberapa hormon diaktifkan dan akan mengalami peningkatan seperti adrenalin, noradrenalin, kortisol dan glukagon. Aksis simpatiko-adrenal merupakan sistem utama tubuh untuk bereaksi terhadap cedera. Perubahan ini disebabkan oleh dampak adrenergik dan katekolamin, dimana katekolamin meningkat setelah terjadinya cedera. Terj adinya systemic inflammatory respons setelah trauma ditandai oleh peningkatan aktivitas sistem kardiovaskuler, metabolisme, konsumsi oksigen, katabolisme protein dan hiperglikemia.9, 28, 31, 32 Glukoneogenesis terj adi di hati dan distimulasi oleh hormon glukagon, kortisol dan growth hormone. 25 Glikogenolisis distimulasi oleh katekolamin, sedangkan mediator sitokin menstimulasi kedua proses tersebut. Resistensi insulin terjadi melalui proses penghambatan kerj a oleh hormon 373 The Indonesian Journal of Medical Science Volume 1 No.6 October 2009 p. 368-379 glukagon melalui pengikatan reseptor glukosa pada sel.22 Proses glukoneogenesis sebenarnya merupakan upaya kompensasi tubuh untuk menyediakan sumber energi bagi kelangsungan sel, karena glukosa yang terbentuk sangat dibutuhkan sebagai bahan bakar utama bagi jaringan yang mengalami cedera. Rendahnya kadar insulin di samping resistensi insulin yang terjadi menyebabkan terjadinya lipolisis dan mobilisasi cadangan lemak tubuh sebagai upaya penyediaan energi. Pelepasan hormon stress dan mediator sitokin menyebakan terjadinya proteolisis protein otot yang bertujuan membentuk protein fase akut, penyembuhan, peningkatan imunitas, dan proses glukoneogenesis.21 Glukosa dimobilisasi dari persediaan glikogen dihati oleh katekolamin, glukokortikoid dan glukagon. 9 Glukosa dapat diperoleh dari glikogen hanya untuk 12-18 j am, karena cadangan glikogen terbatas. 9 Pada fase dini kadar insulin dalam darah rendah karena aktivitas adrenergik pada degranulasi sel â pankreas. Setelah itu, glukoneogenesis dirangsang oleh kortikosteroid dan glukagon. Kadar insulin yang rendah menyebabkan dilepasnya asam amino dari otot yang dimanfaatkan untuk glukoneogenesis. Fase penghancuran protein otot untuk glukoneogenesis dan hiperglikemia yang diakibatkannya merupakan karakteristik fase katabolik dari respon metabolik pada trauma. Kadar glukosa darah setelah trauma harus dipantau dengan baik, disamping hiperglikemia dapat meningkatkan insufisiensi ventilasi, dapat pula merangsang diuresis osmotik dan hiperosmolaritas.9,35 Pada umumnya fase hipermetabolik tersebut akan mencapai puncaknya 374 dalam waktu 48-72 jam dan kembali normal setelah 7-10 hari, tetapi apabila dalam masa itu terjadi komplikasi infeksi, iskemia atau masih terdapat sisa fokus inflamasi, maka fase hipermetabolik akan terus berlangsung sedangkan menurut Moore FD fase flow dapat berlangsung selama 4 hari.9 Perubahan ion Segera setelah cedera otak, akan terjadi kerusakan membran neuronal, axon menjadi tegang dan terbukanya saluran voltage-dependent K+ channel yang menyebabkan peningkatan K+ ekstraseluler. Depolarisasi non spesifik merupakan awal dari pelepasan asamamino eksitatori terutama glutamatexcitatory amino acid (EAA) akan menyebabkan peningkatan flux K dengan mangaktifkan kainat, N-Methyl-D-Aspartat (NMDA ) dan reseptor D-Amino-3-Hydroxy5-Methyl-4-Isozaxole-Propionic Acid (AMPA). Secara normal peningkatan K ekstraseluler diserap oleh sel Glial disekitarnya. Dengan mekanisme ini, otak dapat mempertahankan kadar fisiologis dari K+ setelah adanya trauma ringan, tetapi pada trauma yang lebih berat kompensasi ini akan menghilang. Dalam usaha mempertahankan homeostasis ionik, maka dibutuhkan energi membrane pump yang lebih aktif, Na-K pump membutuhkan lebih banyak ATP dan memicu peningkatan penggunaan glukosa (hipermetabolisme). 36 Peningkatan metabolisme glukosa dikatakan bertahan selama 4 jam pada daerah yang jauh dari pusat kontusio, sedangkan pada daerah yang cedera bertahan lebih dari 30 menit. 36 Oleh karena metabolisme oksidatif otak berlangsung hampir mendekati nilai maksimum, sedikit saja peningkatan kebutuhan energi akan Willy Adhimarta, et al. Glukoneogenesis process at severe head injury Gambar 3. Mekanisme Perubahan ionik pada cedera otak. (Alzheimer C, 2003) terj adi peningkatan glikolisis. 36 Kecepatan glikolisis akan meningkatkan produksi asam laktat.36 Pada keadaan hiperglikolisis setelah cedera otak, metabolisme oksidatif juga mengalami gangguan. Hal ini akan mengganggu fungsi mitokondria dan produksi ATP menjadi berkurang, yang akan menjadi stimulus lanj utan untuk terj adinya peningkatan glikolisis lagi. Peningkatan asam laktat dapat menyebabkan disfungsi neuronal dengan menginduksi asidosis, kerusakan membran, gangguan permeabilitas sawar darah otak dan edema otak. 36 Namun disisi lain hipotesis sementara beranggapan bahwa produksi laktat dari sel glia yang meningkat setelah cedera otak, akan diangkut ke dalam neuron untuk digunakan sebagai bahan bakar cadangan. Depolarisasi setelah cedera dan K+ efflux memicu pelepasan EAA yang diikuti oleh aktifasi reseptor N-methyl-D-aspartat (NMDA). Aktifasi ini akan membentuk saluran sehingga Ca2+ dapat masuk ke dalam sel. Peningkatan Ca2+ dalam sel akan tertumpuk di dalam mitokondria yang akan mengganggu metabolisme oksidatif dan menyebabkan kegagalan pembentukan energi (ATP).36 Penelitian pada tikus menunj ukkan sitokrom oksidase yang dipakai untuk mengukur metabolisme oksidatif mengalami pengura-ngan pada hari 1 dan akan diikuti dengan pemulihan pada hari ke 2, kemudian akan mencapai tingkat dasar pada hari ke 5, dan akan pulih kembali pada hari ke 10.36 Kematian sel otak yang mengalami cedera dapat berlangsung melalui proses apoptosis dan nekrosis. Kerr dkk (1972) pertama kali membedakan proses apoptosis dan nekrosis yang merupakan bentuk manifestasi kematian sel. Nekrosis adalah proses pasif disintegrasi sel, sedangkan apoptosis adalah mekanisme proses aktif yang membutuhkan energi. 26 Iskemia yang sedang sampai berat menginduksi terjadinya kematian sel secara nekrosis, sedangkan proses apoptosis secara predominan terjadi justru pada daerah 375 The Indonesian Journal of Medical Science Volume 1 No.6 October 2009 p. 368-379 yang mengalami iskemia ringan. Data lain juga menunjukkan bahwa kadar kalsium intraseluler yang rendah pada sel cedera cenderung menyebabkan apoptosis, sebaliknya kadar kalsium intraseluler tinggi akan menyebabkan kematian sel secara nekrosis.26 Pengaruh peningkatan katekolamin, kortikosteroid, glukagon, hormon pertumbuhan (growth hormone) dan interleukin (IL-1, IL-6, IL-8) dapat menyebabkan terj adinya hipermetabolisme, hiperglikemia dan hiperkata-bolisme.9 Terjadinya hiperglikemia pada trauma karena berhubungan dengan terjadinya hipermeta-bolisme, sedangkan hipermeta-bolisme sendiri berkaitan erat dengan berat ringannya cedera otak. Menurut penelitian Jeremitsky dkk., hiperglikemia mempunyai hubungan dengan peningkatan angka mortalitas dan lamanya perawatan dirumah sakit.17 Zygun (2004) j uga mengemukakan bahwa kadar glukosa darah mempunyai hubungan dengan asidosis jaringan otak. Pada penderita cedera otak disebutkan tingginya kadar glukosa darah berhubungan dengan hasil luaran yang semakin buruk.7,8,21 Glial Fibrillary Acid Protein (GFAP) GFAP adalah protein berfilamen intermediate tipe III yang ditemukan pada sel-sel glia seperti astrosit, berperan dalam mempertahankan kekuatan mekanik sel astrosit untuk mempertahankan bentuknya.10 Pertama kali ditemukan pada tahun 1971, GFAP merupakan protein intermediate berfilamen tipe III yang pada manusia terletak pada kromosom 17q21, berhubungan erat dengan vimentin, desmin dan peripherin yang terlibat pada fungsi dan struktur dari sel sitoskeleton.10 376 Filamen intermediate tipe III terdiri dari tiga domain yang paling dilindungi dari semuanya adalah rod domain. DNA spesifik dari regio protein ini dapat berbeda pada gen filamen intermediate tipe III yang berbeda tetapi struktur dari protein yang paling dilindungi. Rantai rod domain disekitar filamen membentuk dimer dengan N-terminal dan C-terminal pada rantai lurus.11 Filamen tipe III seperti GFAP mampu untuk membentuk baik homodimer maupun heterodimer, GFAP dapat berpolimerasi dengan protein tipe III yang lain atau dengan protein neurofilamen. Menarik bahwa GFAP dan protein intermediate filamen tipe III yang lain tidak dapat bersatu dengan keratin, intermediate filamen tipe I dan II.11 Pada sel, dua filamen intermediate yang berbeda bekerj a sama yang memungkinkan terjadinya spesialisasi dan meningkatkan variasi. Bentuk kerj asama dimana dimer awal bergabung akan membentuk tetramer yang merupakan subunit dasar dari filamen intermediate. 11 Rod sendiri secara invitro tidak dapat membentuk filamen, domain non heliks dibutuhkan untuk membentuk filamen. Dua regio yang lain, kepala dan ekor, memiliki rangkaian dan struktur yang bervariasi. Kepala dari GFAP terdiri dari dua arginin dan satu aromatik residu. Ukuran dari kepala dan ekor memiliki perbedaan antara GFAP dan vimentin yang bila bersatu dapat membentuk head to head daripada head to tail, struktur ini memungkinkan filamen bekerja secara fleksibel.11 Peningkatan ekspresi dari GFAP terjadi pada situasi yang berbeda, umumnya akibat dari aktivasi astrosit. Selama perkembangan, vimentin, filamen intermediate tipe III yang lain Willy Adhimarta, et al. Glukoneogenesis process at severe head injury ditempatkan dengan GFAP pada sel yang imatur, seperti sel glioma tetapi tidak pada sel imatur astrosit. Hal ini dapat mengindikasikan, sebagaimana tujuan dari struktur “head to head”, GFAP dan filamen vimentin bekerja untuk tujuan yang berbeda.11 GFAP diekspresikan pada SSP dalam sel astrosit. GFAP terlibat pada banyak proses fungsi seluler seperti struktur dan pergerakan sel, komunikasi sel dan fungsi dari blood brain barrier. GFAP diketahui bekerja pada mitosis dengan mengatur kerja dari filamen yang ada dalam sel. Selama mitosis, terdapat peningkatan fosforilasi. GFAP juga berperan pada interaksi astrosit dan neuron. In vitro, dengan menggunakan RNA antisense, astrosit yang kekurangan GFAP yang tidak memanjang ditemukan bersama neuron-neuron. 10,11 SIMPULAN Kekenaikan kadar TNF- akan meningkatkan metabolisme dan mempunyai pengaruh terhadap peningkatan kadar GFAP. Mediator ini akan menuntun pada tahapan terjadinya inflamasi termasuk ekspresi molekul adhesi, infiltrasi seluler dan molekulmolekul inflamasi serta faktor-faktor pertumbuhan sehingga akan terj adi kematian atau regenerasi sel-sel otak oleh karena peningkatan tekanan tinggi intrakranial yang disebabkan bertambahnya volume otak (edema) sehingga akan mempengaruhi mikrosirkulasi ke otak. Pada suatu kejadian cedera otak perlu terjadi keseimbangan antara sitokin yang menimbulkan reaksi inflamasi, dengan tujuan untuk membatasi dan memulihkan kerusakan yang terjadi, serta sitokin anti inflamasi yang membatasi agar kerja dari sitokin inflamasi ini tidak berlebihan, yang bila terj adi j ustru akan menimbulkan efek yang merugikan.Untuk mengatasi efek yang merugikan dengan pemberian sitokin anti inflamasi (IL-10) untuk menjaga agar produksi TNF- tidak berlebihan. Proses glukoneogenesis sebenarnya merupakan upaya kompensasi tubuh untuk menyediakan sumber energi bagi kelangsungan sel, karena glukosa yang terbentuk sangat dibutuhkan sebagai bahan bakar utama bagi jaringan yang mengalami cedera. Rendahnya kadar insulin di samping resistensi insulin yang terjadi menyebabkan terjadinya lipolisis dan mobilisasi cadangan lemak tubuh sebagai upaya penyediaan energi. Stres hiperglikemia adalah suatu terminologi kedokteran adanya peningkatan sementara dari glukosa darah disebabkan karena stres dari j aringan. Stres hiperglikemia dapat menyebabkan penyembuhan luka yang buruk, resiko infeksi yang tinggi, prognosis yang buruk, lama perawatan yang panj ang dan meningkatkan mortalitas oleh karena itu perlu dilakukan perhatian lebih pada pasien-pasien dengan stres hiperglikemia. Pelepasan hormon-hormon stres seperti katekolamin, kortisol, growth hormone dan glukagon sebagai faktor glukogenesis dimana akan menstimulasi perubahan cascade metabolic yang akan mengaktifkan subtrat (hiperglikemi) dengan pemecahan sumber protein dan lemak. Peningkatan sekresi katekolamin oleh medulla adrenal terj adi oleh karena adanya luka, sehingga menyebabkan penekanan terhadap produksi hormone insulin dan menyebabkan terj adinya peningkatan kadar gula darah. oleh karena itu perlu diberikan sediaan insulin 377 The Indonesian Journal of Medical Science Volume 1 No.6 October 2009 p. 368-379 pada pasien cedera kepala berat sebagai upaya penyediaan energi yang dapat mengurangi atau mencegah terjadinya edema otak (peningkatan tekanan tinggi intrakranial) sebagai efek dari cedera sekunder otak. DAFTAR RUJUKAN 1. 2. Shohami E, Stahel PF, Younis FM, Kariya K. Experimental closed head injury : analysis of neurological outcome, blood brain barrier death in mice deficient in gene for proinflamatory cytokines, J Cereb Blood Flow Metab 2000; 20 (2): 369-80. Beaumont A, Marmau A. Response of the brain to physical injury: neurosurgery the scientific basis of clinical practice. London: Blackwell Science Ltd 2000; 3 (1) 3. Iskandar J. Cedera kepala. Jakarta: PT Bhuana Ilmu Populer; 2004. 4. Narayan RK, Wilberger JE, Povlishock JT. Neurotrauma; neurophatology of head injury, emergency room management of the head injured patient. USA: Mc Graw Hill; 1996. 5. Setti RS, Richard EG. Principle of neuros urgery: inc rease intrac ranial pressure, cerebral edema, and brain herniation. Edisi ke-2. Philadelphia USA: Elsevier Mosby; 2005. 6. J ulian YR. Neurologic al surgery: intracranial pressure. Edisi ke-4. Volume 1. California USA: W.B. Sounders Company; 1996. 7. Shohami E, Ginis I, Hallenbac, JM. Dual role of tumor necrosis factor alpha in brain injury.Cytokine Growth Factor Rev 1999; 10(2): 119-30. 8. Knoblach SM, Faden AI. Interleukin-10 improves outcome and alter proinflamatory cytokine expression after experimental traumatic brain injury. Exp Neurol1998; 153(1):143-51. 9. DSTC, 2008. Patofisiologi Trauma. 2-18 10. Hergenroeder GW, Redell JB, Moore AN, Dash PK. Biomarkers in the clinic al 378 diagnosis and management of traumatic brain injury. Molec uler diagnosis and therapy 2008; 12 (6): 345-58. 11. Pelinka LE. Serum markers of severe traumatic brain injury: Are they useful?, Review article Indian Journal of Critical Care Medicine 2004; Vol. 8. 12. Magistretti PJ, Pellerin L, Martin JL.Brain Energy Metabolism an Integrated Cellular Perspective 2003. 13. Signorini DF, Andrews P. JD, Jone PA. Predicting survival using simple clinical variables: a case study in traumatic brain injury. Neurol neurosurgery psychiatry 1999; 66: 20-5. 14. Islam AA. Peran sitokin inflamasi dan anti inflamasi dalam meramal luaran penderita c edera otak tertutup yang dilakukan tindakan operasi. Disertasi doktor. Program Pascasarjana, Universitas Hasanuddin, Makassar 2006: 80-99. 15. Mendelow DA, Crawford PJ. Primary and secondary brain injury in pathopisiology and management of severe closed head injury. Eds. Reilly P, Bullock R,6th ed, Chapman and Hall Medical, London, 1987, 1-21. 16. Hergenroeder GW, Redell JB, Moore AN, Dash PK. Biomarkers in the clinic al diagnosis and management of traumatic brain injury. Molec uler diagnosis and therapy 2008; 12 (6): 345-58. 17. Istiajid MES. Respon metabolik cedera otak berat, Basic science of neurosurgery, Pertemuan ilmiah berkala, Proyek Trigonum Plus III, April 2002. 18. Riahi D. Apoptosis pada cedera otak traumatika. Simposium: Apoptosis charming to death. Hotel Borobudur Jakarta 2006. Willy Adhimarta, et al. Glukoneogenesis process at severe head injury 19. Mesotten D, Vanhorebeek, Van den Berghe G. Glucose and insulin management in critical care. Trauma critical care 2003; 2.: 1075 – 80. 20. Magistretti PJ, Pellerin L. Astrocyte couple synaptic activity to glucose utilization in the brain. News in Physiological Sciences 1999; 14: 177-82. 21. Benjamini E. Elements of innate and acquired immunity. In Immunology a short course. Second Edition, New York. W ileyLiss,1991:17-36. 22. Young B, Ott L, Dempsey R. Relationship between admission hyperglycemia and neurologic outcome of severely braininjured patient. Division of Neurosurgery, University of Kentuc ky Medical Center.1989: 466-72. 23. Tisdall MM, Smith M. Multimodal monitoring in traumatic brain injury: current status and f uture direc tions . Britis h Journal of Anaesthesia 2007; 99 (1): 61-7. 24. Royo NC, Shimizu S, Sc houten J W. Pharmacology of traumatic brain injury. Current Opinion in Pharmacology 2003; 2732. 25. Schmidt OI, Infanger M, Heyde, CE. The role of neuroinflammation in traumatic brain injury, Eur J Trauma 2004; 30:135-49. 26. Harrison MJG. Head injury in contemporary neurology. Butterwoths, London, 1984: 453462. 27. Hertz L, McFArlin DE, W aksman BH. Astrocytes: auxilliary cells for immune res pons es in the central nervous system.Immunology Today 1990; 11(8): 265-8. 28. Inao S, Marmarou A, Clarke GD. Production and clearence of lactate from brain tissue, cerebrospinal fluid, and serum following experimental brain injury. J. Neurosurgery 1988; 69: 736-44. 29. Kamada H, Yu F, Nito C, Chan PH. Influence of hyperglycemia on oxidative stress and Matrix Metalloproteinase-9 activation after focal cerebral ischemia/ reperfus ion in rat. Americ an heart association 2007; 38: 1044-9. 30. Strong AJ. The management of plasma glucose in acute cerebral ischemia and traumatic brain injury: more research needed. Intensive Care Medicine 2008: 1169-72. 31. Kawamata T, Katayama, Hovda DA. Lactate accumulation following concussive brain injury: the role of ionic fluxes induced by excitatory amino acids. Brain Research 1995; 647: 196-204. 32. Walz W, Mukerji S. Lactat production and release in cultured astrocyte. Neuroscience Letters 1988; 86: 296-30. 33. Darmadipura MS. Cedera otak dan dasardasar penanganannya. Basic science of neurosurgery, Pertemuan Ilmiah Berkala, Proyek Trigonum Plus III, April 2002. 34. Moppett IK. Traumatic brain injury: as sessment, res usc itation and early management. Britis h Journal of Anaesthesia 2007; 99 (1): 18-31. 379