teori atom - WordPress.com
advertisement

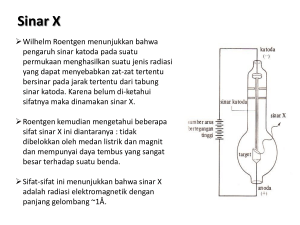
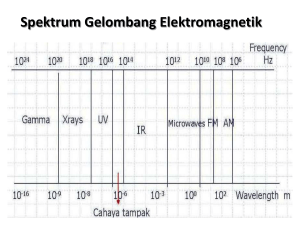
Salah satu konsep ilmiah tertua adalah bahwa semua materi dapat dipecah menjadi zarah (partikel) terkecil, dimana partikel-partikel itu tidak bisa dibagi lebih lanjut. A : Tidak, Tomos : memotong. Dinamakan atom karena dianggap tidak dapat dipecah lagi Pencetus teori atom modern. Teorinya dilandasi oleh kejadian kimiawi dan data kuantitatif. Teori Dalton ditunjang juga oleh 2 percobaan (oleh Lavoisier dan Prost) dan 2 hukum alam (Kekekalan massa dan Perbandingan tetap) Mula-mula tinggi cairan merkuri dalam wadah yang berisi udara adalah A, tetapi setelah beberapa hari merkuri naik ke B dan ketinggian ini tetap. Beda tinggi A dan B menyatakan volume udara yang digunakan oleh merkuri dalam pembentukan bubuk merah (merkuri oksida). Untuk menguji fakta ini, Lavoisier mengumpulkan merkuri oksida, kemudian dipanaskan lagi. Bubuk merah ini akan terurai menjadi cairan merkuri dan sejumlah volume gas (oksigen) yang jumlahnya sama dengan udara yang dibutuhkan dalam percobaan pertama. Massa bahan keseluruhan setelah reaksi kimia sama dengan sebelum reaksi Pada tahun 1799 Proust menemukan bahwa senyawa tembaga karbonat baik yang dihasilkan melalui sintesis di laboratorium maupun yang diperoleh di alam memiliki susunan yang tetap. Percobaan ke- Sebelum pemanasan (g Mg) Setelah pemanasan (g MgO) Perbandingan Mg/MgO 1 0,62 1,02 0,62/1,02 = 0,61 2 0,48 0,79 0,48/0,79 = 0,60 3 0,36 0,60 0,36/0,60 = 0,60 Tiap unsur kimia tersusun oleh partikel-partikel kecil yang tidak bisa dihancurkan dan dibagi, yang disebut atom. Selama perubahan kimia, atom tidak bisa diciptakan dan juga tidak bisa dimusnahkan Semua atom dari suatu unsur mempunyai massa (berat) dan sifat yang sama, tetapi atom-atom dari suatu unsur berbeda dengan atom dari unsur yang lain, baik massa (berat) maupun sifat-sifatnya berlainan. Dalam senyawa kimiawi, atom-atom dari unsur yang berlainan melakukan ikatan dengan perbandingan numerik yang sederhana : Misalnya satu atom A dan satu atom B (AB) satu atom A dan dua atom B (AB2). Bila dua unsur membentuk lebih dari satu senyawa, perbandingan massa dari unsur pertama dengan unsur kedua merupakan bilangan yang sederhana. Metana H C H Etilena C H BA =5 BA =1 BA =1 BA =5 BA =1 Per gram hidrogen dalam gas etilena terdapat 5 gram karbon, jadi 5 gram karbon 1 gram hidrogen Per gram hidrogen dalam gas metana terdapat 2,5 gram karbon, jadi 5 g karbon 2,5 g karbon 2 g hidrogen 1 g hidrogen 5 g karbon/1 g hidrogen 2 Perbandingan 2,5 g karbon/1 g hidrogen 1 Dalton meneliti bahwa hidrogen pada gas metana adalah dua kali dari hidrogen yang terdapat pada gas etilena. Ia menyatakan bahwa rumus gas metana adalah H2 dan etilena CH (Rumus yang benar berdasarkan pengetahuan sekarang adalah CH4 dan C2H4). Sifat-sifat sinar katoda : 1. Sinar katoda dipancarkan oleh katoda dalam sebuah tabung hampa bila dilewati arus listrik (aliran listrik adalah penting) 2. Sinar katoda berjalan dalam garis lurus 3. Sinar tersebut bila membentur gelas atau benda tertentu lainnya akan menyebabkan terjadinya fluoresensi (mengeluarkan cahaya). Dari fluoresensi inilah kita bisa melihat sinar, sinar katoda sendiri tidak tampak. 4. Sinar katoda dibelokkan oleh medan listrik dan magnit; sehubungan dengan hal itu diperkirakan partikelnya bermuatan negatif 5. Sifat-sifat dari sinar katoda tidak tergantung dari bahan elektrodanya (besi, platina dsb.) Sinar katoda tidak tampak, hanya melalui pengaruh fluoresensi dari bahan sinar ini dapat dilacak. Berkas sinar katoda dibelokkan oleh medan magnit. Pembelokkan ini menunjukkan bahwa sinar katoda bermuatan negatif. Kode C = Katoda; A = Anoda; E = lempeng kondensor bermuatan listrik; M = magnet; F = layar berfluoresens. Berkas 1 : Hanya dengan adanya medan listrik, berkas sinar katoda dibelokkan keatas menyentuh layar pada titik 1. Berkas 2 : Hanya dengan adanya medan magnit, berkas sinar katoda dibelokkan kebawah menyentuh layar pada titik 2. Berkas 3 : Berkas sinar katoda akan lurus dan menyentuh layar dititik 3, bila medan listrik dan medan magnit sama besarnya Berdasarkan eksperimennya Thomson mengukur bahwa kecepatan sinar katoda jauh lebih kecil dibandingkan kecepatan cahaya, jadi sinar katoda ini bukan merupakan REM. Selain itu Ia juga menetapkan perbandingan muatan listrik (e) dengan massa (m). Hasil rata-rata e/m sinar katoda kira-kira 2 x 108 Coulomb per gram. Nilai ini sekitar 2000 kali lebih besar dari e/m yang dihitung dari hidrogen yang dilepas dari elektrolisis air (Thomson menganggap sinar katoda mempunyai muatan listrik yang sama seperti atom hidrogen dalam elektrolisis air. Kesimpulan : Partikel sinar katoda bermuatan negatif dan merupakan partikel dasar suatu benda yang harus ada pada setiap atom. Pada tahun 1874 Stoney mengusulkan istilah elektron. Percikan tetes minyak dihasilkan oleh penyemprot (A). Tetes ini masuk kedalam alat melalui lubang kecil pada lempeng atas sebuah kondensor listrik. Pergerakan tetes diamati dengan teleskop yang dilengkapi alat micrometer eyepiece (D). Ion-ion dihasilkan oleh radiasi pengionan seperti sinar x dari sebuah sumber (E). Sebagian dari tetes minyak memperoleh muatan listrik dengan menyerap (mengadsorbsi) ion-ion. Tetes diantara B dan C hanya melayang-layang, tergantung dari tanda (+ atau -) dean besarnya muatan listrik pada tetes. Dengan menganalisis data dari jumlah tetes, Milikan dapat menghitung besarnya muatan q. Milikan menemukan bahwa tetes selalu merupakan integral berganda dari muatan listrik elektron e yaitu : q = n.e (dimana n = 1, 2, 3 ...) Nilai yang bisa diterima dari muatan listrik e adalah –1,60219 x 10-19C. Dengan menggabungkan hasil Milikan dan Thomson didapat massa sebuah elektron = 9,110 x 10-28 gram. Dalam tahun 1886 Eugen Goldstein melakukan serangkaian percobaan dan ia menemukan partikel jenis baru yang disebut sinar kanal (canal rays) atau sinar positif. Sinar katoda mengalir kearah anoda. Tumbukannya dengan sisa atom gas melepaskan elektron dari atom gas, menghasilkan ion yang bermuatan listrik positif. Ion-ion ini menuju ke katoda (-) tetapi sebagian dari ion ini lolos melewati lubang pada katoda danmerupakan arus partikel mengarah kesisi lain. Berkas sinar positif ini disebut sinar positif atau sinar kanal. 1. 2. 3. 4. Partikel-partikelnya dibelokkan oleh medan listrik dan magnit dan arahnya menunjukkan bahwa muatannya positif. Perbandingan muatan dan massa (e/m) sinar positif lebih kecil daripada elektron. Perbandingan e/m sinar positif tergantung pada sifat gas dalam tabung. Perbandingan terbesar dimiliki oleh gas hidrogen. Untuk gas lain e/m merupakan pecahan integral (mis. ¼, 1/20 dari hidrogen). Perbandingan e/m dari sinar positif yang dihasilkan bila gas hidrogen ada dalam tabung adalah identik dengan e/m untuk gas hidrogen yang dihasilkan melalui air. Pengamatan ini dapat diterangkan dengan model atom yang dibuat J.J. Thomson yaitu model plum pudding. Kesimpulan dari sifat sinar kanal ini ialah semua atom terdiri dari satuan dasar yang bermuatan positif, pada atom H terdapat satu dan atom-atom lainnya mengandung jumlah lebih banyak. Satuan dasar ini sekarang disebut dengan proton. Beberapa peneliti melihat bahwa kadangkadang benda diluar tabung sinar katoda bersinar selama percobaan, Wilhelm Roentgen menunjukkan bahwa pengaruh sinar katoda pada suatu permukaan menghasilkan suatu jenis radiasi yang dapat menyebabkan zat-zat tertentu bersinar pada jarak tertentu dari tabung sinar katoda. Karena belum diketahui sifatnya maka dinamakan sinar X. Roentgen kemudian mengetahui beberapa sifat sinar X ini diantaranya : tidak dibelokkan oleh medan listrik dan magnit dan mempunyai daya tembus yang sangat besar terhadap suatu benda. Sifat-sifat ini menunjukkan bahwa sinar X adalah radiasi elektromagnetik dengan panjang gelombang ~1Å. Sinar matahari Uranium & kalium disulfat Lempeng fotografi Dibungkus kertas hitam tebal Mendung Ernest Rutherford membuktikan adanya dua jenis radiasi, sinar alfa dan sinar beta. Sinar mempunyai kekuatan ionisasi besar tetapi daya tembusnya terhadap materi rendah. Sinar ini dapat ditahan oleh kertas biasa. Sinar ini adalah partikel yang membawa 2 satuan dasar muatan + dan mempunyai massa identik dengan He (Sinar = ion He2+). Sinar sebaliknya memiliki kekuatan ionisasi rendah dan daya tembus besar. Sinar ini dapat melewati lempeng alumunium setebal 3 mm. Sinar ini memiliki partikel bermuatan negatif dengan e/m sama seperti elektron. Bentuk radiasi ketiga mempunyai daya tembus sangat besar dan tidak dibelokkan oleh medan listrik dan magnit. REM ini dikenal dengan sinar gamma (). Tahun 1909 Hans Geiger dan Ernest Marsden membuat serangkaian percobaan yang menggunakan lempeng emas yang sangat tipis dan logam lain (tebal 10-4 s.d. 10-5 cm) sebagai sasaran partikel yang berasal dari radioaktif. Geiger dan Marsden mengamati bahwa” 1. Sebagian besar dari partikel menembus lempeng logam tanpa pembelokkan. 2. Sebagian (~1 dari tiap 20.000) mengalami pembelokkan setelah menembus lempeng logam. 3. Dalam jumlah yang sama (poin 2) tidak menembus lempeng logam sama sekali tetapi berbalik sesuai arah datangnya sinar. Sebagian dari massa dan muatan (+) sebuah atom berpusat pada daerah yang sempit yang disebut inti atom, sebagian besar atom merupakan ruang kosong. Besarnya muatan pada inti berbeda untuk atom yang berbeda dan kira-kira setengah dari nilai numerik bobot atom suatu unsur. Diluar inti suatu atom harus terdapat elektron yang jumlahnya sama dengan satuan muatan inti (agar atom netral). Pada tahun 1913 Moseley menemukan bahwa panjang gelombang sinar x bervariasi tergantung dari bahan sasarannya. Dengan menghubungkan hal ini ke persamaan matematis disimpulkan bahwa setiap unsur dapat ditetapkan dengan suatu bilangan bulat yang disebut nomor atom. Tahun 1919 Rutherford mengembangkan satuan dasar muatan positif yang disebut proton hasil risetnya dari jalur lintasan partikel diudara. Konsep yang dipopulerkan oleh Rutherford adalah inti mengandung sejumlah proton yang sama dengan nomor atomnya dan sejumlah partikel netral yang disebut neutron agar sesuai dengan massa atom. Pada tahun 1930-an Chadwick membuktikan keberadaan neutron melalui percobaan pemboman berilium dan boron dengan partikel , sehingga model atom yang terdiri dari elektron, proton dan neutron lengkap ditemukan.