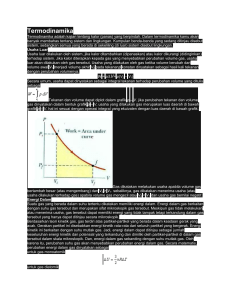
Termodinamika
advertisement

D.TERMODINAMIKA 1. Kalor Jenis Gas Suhu suatu gas dapat dinaikkan dalam kondisi yang bermacam-macam. Volumenya dikonstankan, tekanannya dikonstankan atau kedua-duanya dapat dirubah-rubah sesuai dengan kehendak kita. Pada tiap-tiap kondisi ini panas yang diperlukan untuk menaikkan suhu sebesar satu satuan suhu untuk tiap satuan massa adalah berlainan. Dengan kata lain suatu gas mempunyai bermacam-macam kapasitas panas. Tetapi hanya dua macam yang mempunyai arti praktis yaitu : - Kapasitas panas pada volume konstan (Cv) - Kapasitas panas pada tekanan konstan (Cp) Kapasitas panas gas ideal pada tekanan konstan selalu lebih besar dari pada kapasitas panas gas ideal pada volume konstan (Cp>Cv), dan selisihnya sebesar konstanta gas umum (universal) yaitu : R = 8,317 J/mol 0K. dipanaskan (pada tekanan tetap) ; maka volume akan bertambah dengan V. Usaha yang dilakukan oleh gas terhadap udara luar : W = p. ∆ V 2. Usaha dalam (U) adalah : Usaha yang dilakukan oleh bagian dari suatu sistem pada bagian lain dari sitem itu pula. Pada pemanasan gas seperti di atas, usaha dalam adalah berupa gerakan-gerakan antara molekul-molekul gas yang dipanaskan menjadi lebih cepat. Energi dalam suatu gas Ideal adalah : U= 3 n RT 2 Cp – Cv = R Cp = kapasitas panas jenis ( kalor jenis ) gas ideal pada tekanan konstan. Cv = kapasitas panas jenis ( kalor jenis ) gas ideal pada volume konstan. Berdasarkan teori kinetik gas kita dapat menghitung panas jenis gas ideal, sebagai berikut: a. Untuk gas beratom tunggal ( monoatomik ) diperoleh bahwa : 5 3 γ = cP = 1,67 cP = 2 R cV = 2 R cV b. Untuk gas beratom dua ( diatomik ) diperoleh bahwa : 7 5 γ = cP = 1,4 cP = 2 R cV = 2 R cV γ = konstanta Laplace. 2. Usaha Yang Dilakukan Gas. Temodinamika merupakan cabang ilmu fisika yang mempelajari mengenai pengaliran panas, perubahan-perubahan energi yang diakibatkan dan usaha yang dilakukan oleh panas. 1. Usaha luar (W) yaitu : Usaha yang dilakukan oleh sistem terhadap sekelilingnya terhadap sistem. Misalkan gas dalam ruangan yang berpenghisap bebas tanpa gesekan 3. Kalor (Energi Panas) Kalor dikenal sebagai bentuk energi yaitu energi panas dengan notasi Q. Untuk kalor pada tekanan konstan : Qp = Cp ∆ T Untuk kalor pada volume konstan : Qv = Cv ∆ T 4. Hukum I Termodinamika. Dalam suatu sistem yang mendapat panas sebanyak ∆ Q akan terdapat perubahan energi dalam ( ∆ U) dan melakukan usaha luar ( ∆ W ) Q (+) Lingkungan W (+) sistem ∆U Lingkungan Q(-) W (-) ∆Q= ∆U+ ∆W ∆ Q (+) = Kalor yang masuk sistem ∆Q ∆ Q (-) = Kalor yang keluar dari sistem ∆ U = perubahan energi dalam ∆W ∆ W (+) = Sistem melakukan usaha pada lingkungan ∆ W (-) = Sistem dikenai usaha Pada proses ini gas dipanaskan dengan tekanan tetap (lihat gambar). 5. Proses - Proses Thermodinamika Pada Hukum I 1. Hukum I Thermodinamika untuk Proses Isokhorik / Isovolumik (volume konstan ) sebelum dipanaskan Pada proses ini volume sistem konstan. ( lihat gambar ) Sebelum dipanaskan. sesudah dipanaskan Persamaan : Dari ∆ Q = ∆ U + ∆ W, maka : 3 Cp ∆ T = n R ∆T + p. ∆ V 2 3 Cp ∆ T = n R ∆T + n R ∆T 2 Sesudah dipanaskan. Cp = Persamaan : Dari ∆ Q = ∆ U + ∆ W, maka : 3 Cv ∆ T = n R ∆T + p. ∆ V, karena 2 isokhoris (V = konstan) ∆ V = 0 → W= 0 3 Cv ∆ T = n R ∆T 2 Cv = Atau dengan mengingat Cv = Sebagaimana telah dijelaskan sebelumnya Grafik : Dalam proses ini berlaku persamaan BoyleGayLussac 3 nR 2 V1 V2 = T1 T2 Jika grafik ini digambarkan dalam hubungan P dan V maka dapat grafik sebagai berikut : P1 P2 = T1 T2 Jika digambarkan dalam grafik hubungan P dan V maka grafiknya sebagai berikut : W = luasan Pemanasan Pendinginan Interpretasi : Karena ∆ V = 0 maka dari W = p . ∆ V, W = 0 (tidak ada usaha luar selama proses) ∆ Q = U2 - U1 Kalor yang diserap oleh sistem hanya dipakai untuk menambah energi dalam ( ∆ U ) ∆Q= ∆U dengan ∆ U = m . cv ( T2 - T1 ) 2. 3 n R , didapat : 2 Cp – Cv = R Grafik : Dalam proses ini berlaku Hukum Boyle-Gay Lussac dalam bentuk : Pemanasan 5 nR 2 Hukum I termodinamika untuk Proses Isobarik (tekanan konstan) W = luasan Pendinginan Interpretasi : Usaha luar yang dilakukan adalah : W = p (V2 - V1). karena itu hukum I termodinamika dapat dinyatakan : ∆ Q = ∆ U + p ( V2 - V1 ) dw Dari persamaan p = → dw = p dv dv w = ∫ p dv → w = luasan dibawah kurva p Vs v Panas yang diperlukan untuk meningkatkan suhu gas pada tekanan tetap dapat dinyatakan dengan persamaan : ∆ Q = m cp ( T2 - T1 ) Pertambahan energi dalam gas dapat pula dinyatakan dengan persamaan : ∆ U = m . cp ( T2 - T1 ) Karena itu pula maka usaha yang dilakukan pada proses isobarik dapat pula dinyatakan dengan persamaan : ∆ W = ∆ Q - ∆ U = m ( cp - cv ) ( T2 - T1 ) dengan : m = massa gas cp = kalor jenis gas pada tekanan tetap cv = kalor jenis pada volume tetap. V2 V ) = n R T2 ( ln 2 ) V1 V1 P P W = n R T1 ( ln 1 ) = n R T2 ( ln 1 ) P2 P2 ln x =2,303 log x V V W = P1V1 (ln 2 ) = P2V2 (ln 2 ) V1 V1 P P W = P1V1 (ln 1 ) = P2V2 (ln 1 ) P2 P2 W = n R T1 ( ln 4. Hukum I Termodinamika untuk proses Adiabatik Selama proses tak ada panas yang masuk / keluar sistem jadi Q = 0 ( lihat gambar ) 3. Hukum I termodinamika untuk proses Isothermik (suhu konstan) Selama proses suhunya konstan (lihat gambar) Sebelum proses Sebelum dipanaskan. Sesudah dipanaskan. Persamaan : Dari ∆ Q = ∆ U + ∆ W, karena suhunya konstan, maka ∆ T = 0 → ∆ U = 0. Jadi berlaku ∆ Q = ∆ W Selama/akhir proses Persamaan : Dari ∆ Q = ∆ U + ∆ W, Q = 0, maka berlaku ∆ U = - ∆ W atau ∆ W = - ∆ U Grafik : Oleh karena tidak ada panas yang masuk / keluar sistem maka berlaku Hukum Boyle-Gay Lussac PV PV 1 1 = 2 2 T1 T2 Grafik : Oleh karena suhunya tetap, maka berlaku Hukum Boyle Jika digambarkan dalam grafik hubungan P dan V maka berupa : P1 V2 = P2 V2 Jika digambarkan grafik hubungan P dan V maka grafiknya berupa : Pengembangan Pemampatan # Catatan : Grafik Adiabatis lebih curam dibanding grafik isothermis Pemanasan Pendinginan Interpretasi : Karena suhunya konstan T2 = T1 maka : ∆ U = U2 - U1 = 23 n R T2 - 23 n R T1 = 0 (Usaha dalamnya nol ) Kalor yang diserap sistem hanya dipakai untuk usaha luar saja. Dari persamaan : V nRT W = ∫ p dv → W = ∫ dv → W = nRT ln 2 v V1 Interpretasi : Karena ∆ Q = 0 maka O = ∆ U + ∆ W U2 -U1 = - ∆ W. Bila ∆ W negatif (-W = sistem ditekan) usaha dalam sistem ( ∆ U ) bertambah. Sedangkan hubungan antara suhu mutlak dan volume gas pada proses adibatik, dapat dinyatakan dengan persamaan PVγ = c P1.V1γ = P2.V2γ Dengan γ = Cp CV semula. Jadi untuk melakukan usaha secara terus menerus, suatu siklus harus melakukan usaha secara terus menerus. Suatu siklus harus bekerja dalam suatu siklus. → Konstanta Laplace Juga berlaku persamaan :T.Vγ-1 = c 2. Efisiensi Mesin T1.V1γ-1 = T2.V2γ-1 Usaha yang dilakukan pada proses adiabatik adalah : W = m . cv ( T1 - T2 ) atau W= Mengubah tenaga panas menjadi tenaga mekanik pertama-tama selalu memerlukan sebuah mesin, misalnya : mesin uap, mesin bakar atau mesin diesel. Pengalamanpengalaman dengan mesin-mesin yang terdapat dalam praktek membawa kita kepada hukum Termodinamika II yang ringkasnya sebagai berikut : “ Adalah Tidak Mungkin Membuat Suatu Mesin Yang Bekerja Dalam Lingkaran Yang Tidak Menimbulkan Efek Lain Selain Daripada Mengambil Panas Dari Suatu Sumber Dan Merubah Panas Ini Seluruhnya Menjadi Usaha “. P1.V1 ( V2γ-1 - V1γ-1) 1−γ =====O0O===== 3. Siklus Carnot 6. Penerapan Hukum I Siklus carnot yang disebut siklus ideal ditunjukkan pada gambar di bawah ini. Termodinamika . 1. Pengertian Siklus Suatu pesawat yang dapat mengubah seluruh kalor yang diserapnya menjadi usaha secara terus menerus belum pernah kita jumpai. yang ada hanya pengubahan kalor menjadi usaha melalui satu tahap saja. Misalnya : proses isothermis. Agar sistem ini dapat bekerja terus-menerus dan hasilnya ada kalor yang diubah menjadi usaha, maka harus ditempuh cara-cara tertentu. Perhatikan gambar di bawah ini. - Mulai dari (P1,V1) gas mengalami proses isothermis sampai (P2,V2 ). - Kemudian proses isobarik mengubah sistem dari (P2,V2) sampai (P2 , V1). - Akhirnya proses isokhorik membuat sistem kembali ke (P1 ,V1). Usaha yang dilakukan sama dengan luas bagian gambar yang diarsir proses seperti yang ditunjukkan pada gambar diatas disebut : SIKLUS. Pada akhir proses sistem kembali ke keadaan semula. Ini berarti pada akhir siklus energi dalam sistem sama dengan energi dalam Siklus Carnot dibatasi oleh garis lengkung isothermik dan dua garis lengkung adiabatik. Hal ini memungkinkan seluruh panas yang diserap (input panas) diberikan pada satu suhu panas yang tinggi dan seluruh panas yang dibuang (panas output) dikeluarkan pada satu suhu rendah. − Kurva ab dan cd masing-masing adalah kurva pengembangan dan pemampatan isotermis. − Kurva bc dan da masing-masing adalah kurva pengembangan dan pemampatan adiabatik. Untuk bahan perbandingan, ditunjukkan beberapa siklus untuk berbagai jenis mesin. 4. Siklus Mesin Bakar Siklus mesin bakar atau lebih umum disebut siklus Otto di tunjukkan pada gambar di bawah ini. Siklus Otto dibatasi oleh dua garis lengkung adiabatik dan dua garis lurus isokhorik. Dimulai dari titik a, maka : − Kurva ab dan cd masing-masing adalah kurva pemampatan dan pengembangan adiabatik. − Garis lurus bc dan da masing-masing adalah garis lurus untuk pemanasan dan pendinginan isokhorik. 5.Siklus Mesin Diesel Siklus untuk mesin diesel ditunjukkan pada gambar di bawah ini. Siklus pada mesin diesel dibatasi oleh dua garis lengkung adiabatik dan satu garis lurus isobarik serta satu garis lurus isokhorik. - Garis fa adalah proses pengembunan sehingga kembali ke keadaan awalnya. =====O0O===== 7. Hukum II Termodinamika 1. Effisiensi (daya guna mesin) Dalam hukum II Termodinamika akan dibahas perubahan kalor menjadi energi mekanik melalui sebuah mesin, dan ternyata belum ada sebuah mesin pun yang dapat mengubah sejumlah kalor menjadi energi mekanik seluruhnya. Reservoir panas Suhu mutlak T1 Q1 Dimulai dari titik a, maka : − Kurva ab dan cd masing-masing adalah kurva pemampatan dan pengembangan adiabatik. − Garis lurus bc adalah garis lurus pemanasan isobarik. − Garis lurus cd adalah garis lurus pendinginan isokhorik.. 6. Siklus Mesin Uap Siklus mesin uap yang juga disebut siklus Rankine ditunjukkan pada gambar di bawah ini. Siklus ini dibatasi oleh dua garis lengkung adiabatik dan dua garis lurus isokhorik, hanya saja pada mesin uap ini terdapat proses penguapan dan pengembunan. W proses Q2 Reservoir dingin Suhu mutlak T2 Sebuah mesin diberi energi berupa kalor Q1 pada suhu tinggi T1, sehingga mesin melakukan usaha mekanik W. Energi yang dibuang berupa kalor Q2 pada suhu T2. Menurut hukum Thermodinamika I (hukum kekekalan energi) : Q1 = W + Q2 → W = Q1 – Q2 Effisiensi mesin adalah : Energi yang bermanfaat W η= = Energi yang dim asukkan Q1 η= Mula-mula air dalam keadaan cair dengan suhu dan tekanan rendah di titik a. - Kurva ab adalah kurva pemampatan secara adiabatik dengan tekanan yang sama dengan tekanan di dalam periuk pendingin. - Garis cd adalah proses pengubahan air menjadi uap. - Garis de adalah prosers pemanasan sehingga suhu uap sangat tinggi. - Kurva ef adalah proses pengembangan secara adiabatik. W Q1 − Q2 = Q1 Q1 atau Q 1 η = 1 − 2 x 100% Q Menurut Carnot : Q ∼ T, di dapat : Q1 T1 = Q2 T2 sehingga effisiensi mesin carnot dapat ditulis : T 1 η = 1 − 2 x 100% T Rumus Praktis Mesin Carnot : 1. Suhu Tinggi T1' (1 - η’) = T1(1 - η) 2. Suhu Rendah T2' (1 - η) = T2 (1 – η’) Sebenarnya tidak ada mesin yang mempunyai effisiensi 100 % dan dalam praktek effisiensi mesin kurang dari 50 %. 2. Mesin Pendingin / Refrigerator Kalor dapat dipaksa mengalir dari benda dingin ke benda panas dengan melakukan usaha pada sistem. Peralatan yang bekerja dengan cara seperti ini disebut mesin pendingin (refrigerator), contohnya adalah lemari es (kulkas) dan pendingin ruangan (AC). Perhatikan gambar dibawah ini. Reservoir panas Suhu mutlak T1 Q1 W pendingin Q2 Reservoir dingin Suhu mutlak T2 • T1 > T2 • Q 2 = kalor yang diserap dari suhu rendah • Q 1 = kalor yang diserap dari suhu rendah • W = Q 1 – Q 2 = kerja / usaha yang diperlukan Ukuran penampilan sebuah mesin pendingin din yatakan sebagai koefisien daya guna (koefisien performansi), yang diberi lambang Kp. Q Q2 T2 Kp = 2 = = W Q1 − Q2 T1 − T2 Kulkas dan pendingin ruangan memiliki koefisien performansi dalam jangkauan 2-6. Semakin tinggi nilai Kp, semakin baik mesin pendingin tersebut. 3. Perumusan Kelvin-Plank Tentang Hukum II Termodinamika Pada dasarnya perumusan antara Kelvin dan Plank mengenai suatu hal yang sama, sehingga perumusan keduanya dapat digabungkan dan sering disebut : Perumusan Kelvin-Plank Tentang Hukum II Termodinamika. Perumusan Kelvin-Plank secara sederhana dapat dinyatakan sebagai berikut : “Tidak Mungkin Membuat Pesawat Yang Kerjanya Semata-Mata Menyerap Kalor Dari Sebuah Reservoir Dan Mengubahnya Menjadi Usaha” Sebagai contoh marilah kita perhatikan proses yang sebenarnya terjadi pada motor bakar dan motor bensin. − Mula-mula campuran uap bensin dan udara dimasukkan ke dalam silinder dengan cara menarik penghisap. − Kemudian penghisap ditekan, dengan demikian campuran tadi dimampatkan sehingga temperatur dan tekanannya naik. − Campuran tadi kemudian dibakar dengan loncatan bunga api listrik. Proses pembakaran ini menghasilkan campuran dengan temperatur dan tekanan yang sangat tingi, sehinga volume campuran tetap (proses isokhorik) − Hasil pembakaran tadi mengembang, mendorong penghisap, sedangkan tekanan dan temperaturnya turun, tetapi masih lebih tinggi dari tekanan dan temperatur di luar. − Katub terbuka, sehingga sebagian campuran itu ada yang keluar sedangkan penghisap masih tetap ditempatnya. − Akhirnya penghisap mendorong hampir seluruhnya campuran hasil pembakaran itu keluar. 4. Perumusan Clausius Tentang Hukum II Termodinamika Perumusan Clausius tentang hukum II Termodinamika secara sederhana dapat diungkapkan sebagai berikut : “Tidak Mungkin Membuat Pesawat Yang Kerjanya Hanya Menyerap Dari Reservoir Bertemperatur Rendah Dan Memindahkan Kalor Itu Ke Reservoir Yang Bersuhu Tinggi, Tanpa Disertai Perubahan Lain Sebagai contoh marilah kita lihat proses pada lemari pendingin (lemari es) yang bagannya pada gambar di bawah ini. Contoh Soal dan Pembahasan : 1. Jika volume gas ideal diperbesar dua kali volume semula dan ternyata energi dalamnya menjadi empat kali semula, tekanan gas tersebut menjadi .... (A) 4 kali (D) ¼ kali (B) 2 kali (E) 6,4 x 105 Pa (C) ½ kali Jawaban : B V2 = 2 V1, U2 = 4 U1, maka P2 = ? 3 Dari U = n R T , padahal PV = n R T , 2 sehingga U ∼ PV. Jadi dari U2 = 4 U1 diperoleh P2V2 = 4 P1V1. Dengan memasukkan V2 = 2 V1, maka P2 = 2 P1 − − − − Zat cair di dalam wadahnya pada tekanan tinggi harus melalui saluran yang sempit, menuju ke ruang yang lapang (Avoporator). Proses ini disebut : Proses Joule-Kelvin. Tiba di ruang yang lapang, temperatur dan tekanan zat cair tadi berkurang, dan zat cair juga menguap. Untuk menguap maka zat cair ini memerlukan kalor yang diserap dari reservoir T2 (suhu reservoir dingin = suhu benda yang akan didinginkan). Kemudian uap pada tekanan rendah ini masuk ke dalam kompresor, dimampatkan, sehingga tekanannya dan temperaturnya naik. Temperatur uap ini lebih tingi dari temperatur reservoir T1 (temperatur suhu tingi) dan T1 > T2 Di dalam kondensor uap ini memberikan kalor pada reservoir T1. Sebagai reservoir T1 dapat digunakan udara dalam kamar atau air. Zat yang sering dipakai pada pesawat pendingin adalah : Amoniak. Pada proses ini selain pemindahan kalor dari reservoir dingin T2 ke reservoir T1, terjadi pula perubahan usaha menjadi kalor yang ikut dibuang di T1 . =====O0O===== 2. Sebanyak 1,5 m3 gas helium yang bersuhu 27oC dipanaskan secara isobarik sampai 87oC. Jika tekanan gas helium 2 x 105 N/m2, gas helium melakukan usaha luar sebesar .... (A) 60 kJ (D) 480 kJ (B) 120 kJ (E) 660 kJ (C) 280 kJ Jawaban : A V1 = 1,5 m3, T1 = 300 K, T2 = 360 K, dan P = 2 x 105 N/m2, maka W = ? Ingat ! W = p ∆V → W = p (V2 – V1) T V V Proses Isobarik 1 = 2 →V2 = 2 V1 T1 T2 T1 360 V2 = (1,5) m 3 = 1,8 m 3 . Jadi : 300 W = 2 x 105 (0,3) J = 60 kJ 3. Sejumlah gas ideal dengan massa tertentu mengalami pemampatan secara adiabatik. Jika W adalah kerja yang dilakukan oleh sistem (gas) dan ∆T adalah perubahan suhu dari sistem, maka berlaku keadaan .... (A) W = 0; ∆T > 0 (D) W < 0; ∆T > 0 (B) W = 0; ∆T < 0 (E) W < 0; ∆T < 0 (C) W > 0; ∆T = 0 Jawaban : D Karena pemampatan, maka volume diperkecil yang mengakibatkan W < 0. Dari Q = W + ∆ U. Proses adiabatis Q = 0, sehingga 0 = W + ∆ U → ∆ U = - W. Karena W < 0, maka ∆ U > 0, sehingga : ∆T>0 4. Suatu gas yang volumenya 0,5 m3 perlahanlahan dipanaskan pada tekanan tetap sehingga volumenya menjadi 2 m3. Jika usaha luar gas tersebut 3 x 105 joule, tekanan gas adalah .... (A) 6 x 105 N m-2 (D) 2 x 105 N m-2 (B) 4 x 105 N m-2 (E) 1,5 x 105 N m-2 (C) 3 X 105 N m-2 (A) 1, 2 dan 3 (B) 1 dan 3 (C) 2 dan 4 Jawaban : D Jawaban : B (1) Pernyataan benar. Proses isochorik (2) Pernyataan salah. Usaha dari A ke B Isokhorik → W = 0 (3) Pernyataan benar. Karena Q < 0 (4) Pernyataan salah. Grafik isotermik mestinya melengkung Ingat ! W = p ∆V → p = W (V2 − V1 ) 3 x 10 5 N m-2 = 2 x 105 N m-2 p= 3 2 5. P(N m-2)2 3 PB PA 1 V (m3) 0 VA VB Sebuah mesin kalor kecil menjalani siklus seperti pada gambar dengan PA = 1,2 x 105 Pa PB = 7,2 x 105 Pa VA = 2,5 x 10-4 m3 VB = 2 x 10-3 m3 Jika mesin bekerja 6 siklus per sekon, berapa daya keluaran mesin itu? (A) 6300 W (D) 525 W (E) 87,5 W (B) 3150 W (C) 1050 W Jawaban : B 6 siklus = 1 detik → 1 siklus = 1 det ik 6 W = luasan segitiga kurva p-V W = ½ (PB − PA ) (VB − V A ) W = ½ (6 x 105) (2 – 0,25) 10-3J = 525 J W 525 p= → p= watt → p = 3150 W 1 t 6 2 6. P (N/m ) C B 5 2 A V (m3) 0 1 3 Dari proses sebuah mesin dengan gas ideal yang digambarkan dalam diagram di samping, maka pernyataan yang benar ialah .... (1). proses dari A ke B adalah proses isokhorik (2). usaha yang dilakukan dalam proses dari A ke B adalah 6 joule (3). pada proses dari B ke C kalor keluar (4). proses dari C ke A adalah proses isotermal Pernyataan diatas yang sesuai adalah : (D) 4 (E) semua salah 7. Sejumlah gas pada suhu 7oC dan tekanan 1,0 x 105 N/m2 dimampatkan secara isotermal sehingga volumenya menjadi sepertiga volume semula. Gas itu kemudian mengembang secara adiabatik ke volumenya semula. Jika γ = 1,40, hitung tekanan akhir gas. (A) 3,2 x 104 Pa (D) 3,1 x 105 Pa 4 (B) 6,4 x 10 Pa (E) 6,4 x 105 Pa (C) 8 x 104 Pa Jawaban : B TA = (7 + 273) K = 280 K PA = 1,0 x 105 N/m2 VB = ⅓ VA. dan γ = 1,40 PC = ? Soal diatas dapat diilustrasikan sebagai berikut : P PB B PA A PC C V VB VA = VC Proses A-B (Proses Isotermik): V PA V A = PB VB → PB = A PA VB 5 2 PB = 3 (1,0 x 10 N/m ) = 3 x 105 N/m2 Proses B-C (Proses Adiabatik): γ V PB.VBγ = PC.VCγ → PC = B PB VC 1, 4 1 VA PC = 3 (3 x 105 N/m2) VA Pc = 6,4 x 104 Pa 8. Siklus Carnot dibatasi oleh dua proses yaitu…. (A) Isobarik dan isotermik (B) Isobarik dan isokhorik (C) Isotermik dan adiabatik (D) Isotermik dan isokhorik (E) Isokhorik dan isentropik 2. P A B 5 2 Jawaban : C Cukup jelas ! Lihat kembali teori dasarnya 10. Sebuah mesin Carnot yang menggunakan reservoir suhu tinggi 800 K mempunyai efisiensi 20%. Untuk menaikkan efisiensi menjadi 36%, maka suhu reservoir suhu tinggi dinaikkan menjadi….. (A) 928 K (D) 1200 K (B) 1000 K (E) 1380 K (C) 1160 K Jawaban : B Gunakan rumus praktis : T1' (1 - η’) = T1(1 - η) T1' (1 – 0,36) = 800(1 – 0,2) → T1' = 1000 K C V 0 9. Suatu mesin menerima 200 kalori dari sebuah reservoir bersuhu 400 K dan melepaskan 175 kalor ke sebuah reservoir lain yang suhunya 320 K. Efisiensi mesin itu adalah .... (A) 12,5% (D) 25,0% (B) 14,3% (E) 87,5% (C) 20,0% Jawaban : A Q η = 1 − 2 x 100 % Q1 175 η = 1 − x100% = 12,5 % 200 D 2 4 Sejumlah gas ideal menjalani siklus ABCDA (lihat gambar). Suhu di titik C = 400 K, maka .... 1. kalor yang diserap gas per siklus 20 J 2. usaha gas 6 J 3. perubahan energi dalam gas 2 J 4. suhu di titik A 500 K Pernyataan diatas yang sesuai adalah : (A) 1, 2 dan 3 (D) 4 (B) 1 dan 3 (E) semua benar (C) 2 dan 4 3. Perhatikan pernyataan-pernyataan berikut .. (1). Pada proses isokhorik, gas tidak melakukan usaha (2). Pada proses isobarik, gas selalu mengembang (3). Pada proses adiabatik, gas selalu mengembang (4). Pada proses isotermik, energi dalam gas tetap Pernyataan yang sesuai dengan konsep termodinamika adalah .... (A) (1) dan (2) (B) (1), (2), dan (3) (C) (1) dan (4) (D) (2), (3), dan (4) (E) (3) dan (4) 4. P (N/m2) B =====O0O===== 1 Soal-soal : 1. P (N/m2) 25 20 15 A B V (m3) 0 8 16 A 1 C VB Jika perubahan energi dalam gas pada proses C sama dengan perubahan energi dalam pada proses AB, besar usaha yang dilakukan gas pada proses AB = .... (A) 420 joule (D) 240 joule (B) 300 joule (E) 210 joule (C) 280 joule C 3 2 V (m3) Gas menjalani proses ABC. Kalor yang dibutuhkan untuk proses tersebut adalah .... (A) 3 joule (D) 10,5 joule (B) 4,5 joule (E) 12 joule (C) 7,5 joule 5. Suatu sistem mengalami proses adiabatik. Pada sistem dilakukan usaha 100 J. Jika perubahan energi dalam sistem adalah ∆U dan kalor yang diserap sistem adalah Q, maka .... (A) ∆U = - 1000 J (D) Q = 10 J (B) ∆U = 100 J (E) ∆U +Q = -100 J (C) ∆U = 0 6. P (C) 2 dan 4 B PB 10. PA A C a Q1 b T1 = 900 K V 0 VA VB Sebanyak 10 mol gas ideal monoatomik menjalani siklus BCA (AB lurus) seperti pada gambar. PA = 2/3P B = 8,3 X 105 n m-2 VA = 1/2 VB TA = 103 K R = 8,3 J mol -1 K-1 Jumlah kalor yang diserap gas selama proses AB adalah .... (A) 5,2 x 105 J (D) 2,1 x 105 J 5 (B) 4,7 x 10 J (E) 1,2 x 105 J (C) 3,6 x 105J 7. Sejumlah gas ideal bermassa m menjalani proses pada tekanan tetap P. Jika volumenya berubah dari V1 menjadi V2 dan suhunya berubah dari T1 dan T2 sedangkan cp adalah kalor jenis pada P tetap, dan cv adalah kalor jenis pada V tetap, naka perubahan energi dalamnya adalah .... (A) mcp (T2- T1) (B) mcp (V2- V1) (C) mcv(T2- T1) (D) mcv(V2- V1) (E) mcp (V2T2- V1T1) 8. Sebuah silinder mesin diesel berisi udara dengan volume 90 cm3 pada suhu 27oC dan tekanan 1 atm. Udara itu dimampatkan secara adiabatik sehingga volumenya menjadi 15 cm3. dengan menganggap udara mengikuti sifat gas ideal dengan γ = 1,4 dan 1 atm = 1 x 105 N/m2, tentukan besar suhu udara jika 61,4=12. (A) 150 K (D) 450 K (B) 750 K (E) 600 K (C) 300 K 9. Sejumlah gas ideal bermassa m menjalani proses pada tekanan P yang tetap. Jika volumenya berubah dari T1 menjadi T2 sedangkan cp = kalor jenis pada P konstan dan cv = kalor jenis pada volume konstan, maka usaha (kerja) yang dilakukan oleh gas dinyatakan sebagai .... (1) P(V2 – V1) (2) m(cp – cv )(T2- T1) (3) mcp(T2- T1) (4) mcv (T2- T1) Pernyataan diatas yang sesuai adalah : (A) 1, 2 dan 3 (D) 4 (B) 1 dan 3 (E) semua benar c d T2 = 600 K Q2 Pada grafik P-V mesin Carnot di samping, W = 2 x 105 J. Banyaknya kalor yang dilepas oleh mesin tiap siklus adalah .... A. 3 x 105 J D. 6 x 105 J B. 4 x 105 J E. 6 x 106 J 5 C. 5 x 10 J 11. Sebuah mesin Carnot yang reservoir suhu rendahnya 27oC memiliki daya guna 405. jika daya gunanya akan diperbesar menjadi 50%, reservoir suhu tingginya haurs dinaikkan sebesar .... (A) 25 K (D) 100 K (B) 50 K (E) 150 K (C) 75 K 12. Suatu mesin Carnot bekerja di antara suhu 600 K dan 300 K dan menerima masukan kalor 1000 J. Usaha yang dilakukan mesin adalah .... (A) 300 J (D) 600 J (B) 400 J (E) 700 J (C) 500 J 13. Suhu dalam suatu ruangan bermesin pendingin T2 = -23oC sedangkan suhu di luar T1 = 27OC. Setiap 30 menit dapat dikeluarkan kalor Q1= 3 X 106 J. Daya listrik yang terpakai dalam menjalankan mesin pendingin Carnot itu besarnya .... 1 5 (A) x10 4 watt (D) x10 4 watt 36 18 1 (B) 10 4 watt (E) x10 4 watt 18 1 (C) x10 4 watt 6 14. Suatu pesawat pendingin memiliki koefisien daya guna = 6,5. Jika temperatur ruang (reservoir) yang bersuhu tinggi ialah 27oC, suhu ruang temperatur rendah ialah .... (A) – 10oC (D) – 13oC o (B) – 11 C (E) – 14oC (C) – 12oC 15. Suhu di dalam ruangan suatumesin pendingin (kulkas) 0oC dan suhu di luar 27o C. Setiap jam panas yang dikeluarkan dari ruangan ialah 6,7 x 106 joule. Berapa watt besar daya listrik yang dipakai untuk kulkas tersebut? (A) 92 W (B) 6,0 x 105 W (C) 184 W (D) 200 W (E) 132,48 W 16. Suatu sistem mengalami perubahan dari keadaan 1 ke keadaan 2 melalui berbagai lintasan proses. Besaran berikut ini yang perubahannya tidak bergantung pada lintasan yang ditempuh adalah .... (1) usaha (3) kalor (2) entropi (4) energi dalam Pernyataan diatas yang sesuai adalah : (A) 1, 2 dan 3 (D) 4 (B) 1 dan 3 (E) semua benar (C) 2 dan 4 17. Mesin kalor Carnot mengambil 1000 kkal dari reservoir 627oC dan mengeluarkannya pada reservoir 27oC. Kalor yang dikeluarkan ke reservoir 27oC adalah .... (A) 43,1 kkal (D) 666,7 kal (B) 333,3 kkal (E) 956,9 kal (C) 600 kkal 18. Sebuah pesawat pendingin Carnot mempunyai koefisien kinerja 6,5. Jika reservoir yang tinggi bersuhu 27˚C, maka reservoir suhu rendahnya bersuhu…. (A) – 5˚C (D) – 12˚C (B) – 8˚C (E) – 13˚C (C) – 10˚C 19. Koefisien performansi sebuah kulkas adalah 5,0. Besar energi listrik untuk memindahkan 3000 J. Kalor dari makanan di dalam kulkas adalah…. (A) 600 J (D) 12000 J (B) 1500 J (E) 15000 J (C) 5000 J 20. Sebuah mesin Carnot memiliki efisiensi 40% menghasilkan daya keluaran 100 MW dan membuang kalor pada reservoir bersuhu 27˚C. Kalor tiap sekon yang dibuang ke suhu rendah sebesar…. (A) 50 MJ (D) 250 MJ (B) 100 MJ (E) 350 MJ (C) 150 MJ =====O0O=====