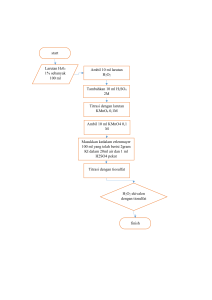
BAB IV HASIL DAN PEMBAHASAN 4.1. Data Pengamatan a. Pembakuan Larutan Kalium Permanganat Prosedur 1. Kristal KMnO4 Hasil Pengamatan diencerkan, Massa KMnO4 = 3,25 gram dipanaskan dan didiamkan 1 malam 2. Kristal Na2C2O4 dipanaskan 2 jam Massa Na2C2O4 = 0,3 gram (105-110oC), dilarutkan dalam H2SO4, Volume H2SO4 = 12,5 mL diencerkan, dipanaskan hingga Volume H2C2O4 = 250 mL = 0,25 L mendidih (70-80oC) 3. Na2C2O4 dititrasi dengan KMnO4 Terjadi perubahan warna dari bening secara duplo menjadi ungu gelap V Na2C2O4 = 10 mL V1 KMnO4 = 2,7 mL V2 KMnO4 = 3,1 mL Vrata-rata = 2,9 mL b. Penentuan Kalsium (Ca2+) dalam CaCO3 Prosedur Hasil Pengamatan 1. Kristal CaCO3 diencerkan dengan massa CaCO3 = 0,2 gram akuades, VCaCO3 = 250 mL 2. CaC2O4 ditambah 3 tetes indikator Volume(NH4 oksalat) = 25mL MM, didihkan. didihkan kembali massaNa2C2O4 = 0,3 gram ditambahkan NH4 oksalat, VolumeH2SO4 = 12,5 mL ditambahkan ammonia 1:1 akuades, VolumeH2C2O4 = 250 mL = 0,25 L dipanaskan 15 menit (70-80oC) Volumeammonia = 2 mL Volumeakuades = 2 mL 3. Penyaringan dengan kertas whatman 4. 10 mL Filtrat dititrasi dengan KMnO4 Vfiltrat = 10 mL secara duplo V1 KMnO4 = 0,2 mL V2 KMnO4 = 0,1 mL Vrata-rata = 0,15 mL 5. Pencucian endapan dengan larutan panas asam asetat (1:8) disuhu 60oC, dilarutkan dan diaduk 6. Larutan endapan ditirasi (duplo) Terjadi perubahan warna dari bening dengan KMnO4 menjadi ungu gelap Vlarutan endapan = 10 mL V1 KMnO4 = 0,6 mL V2 KMnO4 = 0,8 mL Vrata-rata = 0,7 mL 4.2. Perhitungan a. Pembakuan Larutan Kalium Permanganat Diketahui: m Na2CO3 Ditanya: = 0,3 gram V Na2C2O4 = 10 mL BM Na2C2O4 = 134 g/mol V pengenceran = 250 mL V KMnO4 = 2,9 mL V KMnO4…? Dijawab: m Na2C2O4 n Na2C2O4 = M Na2C2O4 = N Na2C2O4 = M Na2C2O4 x 2 BM Na2C2O4 n Na2C2O4 Vpengenceran = = 0,3 𝑔 = 2,2 x 10-3 134 𝑔/𝑚𝑜𝑙 2,2 𝑥 10^−3 0,25 = 8,9 x 10-3 M = 8,9 x 10-3 x 2 = 0,0178 N N KMnO4 = V Na2C2O4 𝑥 N Na2C2O4 V KMnO4 = 10 𝑚𝐿 𝑥 0,0178 𝑁 2,9 𝑚𝐿 = 0,061 N b. Penentuan Kadar Kalsium (Ca2+) dalam CaCO3 Diketahui: Ditanya: N KMnO4 = 0,006 N V1 KMnO4 = 0,6 mL V2 KMnO4 = 0,8 mL V rata-rata KMnO4 = 0,7 mL BA Ca = 40 g/mol Kadar Ca2+…? Dijawab: n H2C2O4 = 2/5 (N KMnO4 x V rata-rata KMnO4) = 2/5 (0,006 N x 0,7 mL) = 0,0168 mmol CaC2O4 + H2SO4 → CaSO4 + H2SO4 CaC2O4 → Ca2+ + C2O42N Ca2+ = n H2C2O4 = 0,0168 mmol Massa Ca2+ = mol Ca2+ x BA Ca = 0,0168 mmol x 40 g/mol = 0,0672 mg atau 6,72 x 10-4 gram Kadar Ca2+ = 6,72 𝑥 10^−4 0,2 𝑔 x 100% = 0,336% Jadi, kadar Ca2+ dalam CaCO adalah 0,336%