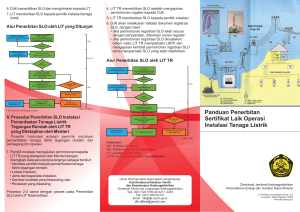
SN1 Substitution and Elimination • If an sp3 C is bonded to electronegative atom Substitution reactions and Elimination reactions are possible This chapter is all about substitution SN2 and SN1 Reactions SN2 - Reaction – bonds break and form at the same time SN2 SN1 - CX bond breaks, forming a C+ then reacts with a nucleophile + C X C+ + X SN1 C+ + Nu: C Nu Nucleophilic Substitution Reactions Either mechanism depends on the: • structure of the alkyl halide • reactivity of the nucleophile • concentration of the nucleophile • The solvent in which the Rx is carried out • The leaving group SN1 Reactions • Reaction of t-butyl bromide with water should be slow – water is a poor nucleophile – t-butyl bromide is sterically hindered However – Reaction is a million times faster than with CH3Br CH3 CH3 CH3 C Br CH3 t-butyl bromide + H 2O CH3 C OH CH3 t-butyl alcohol (Maybe not an SN2 reaction!) + HBr SN1 Reactions • SN1 Mechanism • Rate determining step does not involve nucleophile Step 1 Step 2 SN1 Mechanism SN1 Reactivity • Relative Reactivities in an SN1 Reaction 1o RX < 2o RX < 3o RX Increasing Reactivity SN1 Stereochemistry • Because a planer carbocation is formed, nucleophilic attack is possible on both sides, so both isomers are possible SN1 Stereochemistry SN1 should yield racemic mixture but it doesn’t This is due to the steric hindrance of the leaving group Stereochemistry • As the leaving group goes (Marvin K) it blocks the path of any incoming nucleophiles SN1 vs SN2 Inversion of configuration racemization with partial inversion What Makes SN1 Reactions work the best • Good Leaving Group – The weaker the base, the less tightly it is held (I- and Br- are weak bases) • Carbocation – How stable is the resulting carbocation? • 3o > 2o > 1o > methyl Increasing Stability What Doesn’t Matter In an SN1 Reactions • The Nucleophile • It has NO EFFECT on rate of Rx!!! • Solvolysis Reactions • (the nucleophile is also the solvent) Carbocation Rearrangements Since a carbocation is the intermediate, you may see rearrangements in an SN1 Rx No rearrangements in an SN2 Rx Carbocation Rearrangement • Methyl Shift Reaksi Substitusi Halida Alilik dan Benzilik Terdapat dua macarn halida yang berbeda dari alkil halida dalam sifat pada reaksi SN 1 dan SN 2, yakni halida alilik dan halida benzilik. A. Reaksi SN1 Kebanyakan alkil halida primer bereaksi substitusi dengan jalan SN 2 secara eksklusif dan tidak dengan reaksi SN I. Tetapi suatu halida alilik atau benzilik primer sangat reaktif , baik dalam reaksi SN 1 maupun SN 2. Meningkatnya reaktivitas kedua tipe halida dalam suatu reaksi SN 1 karena adanya stabilisasi-resonansi (dari) karbokation dari keadaan transisi ,Karbokation distabilkan oleh menyebarnya muatan positif. Stabilisasi-resonansi menyangkut penyebaran muatan positif oleh ikatan ikatan pi. Struktur-struktur yang berbeda hanya dalam hal posisi elektron π adalah struktur resonansi. Karena kation alil itu terstabilkan oleh resonansi, energi keadaan transisi yang dihasilkannya relatif rendah. Akibatnya, laju reaksinya cukup cepat. Stabilisasi induktif menyangkut penyebaran muatan positif lewat ikatan-ikatan sigma. Kedua karbon terminal (ujung) dalarn kation alil mempunyai jumlah muatan positif sama. Lalu atom mana yang akan diserang oleh nukleofil? Jawabnya ialah kedua-duanya. Benzil haIida juga menunjukkan peningkatan laju SN I, karena stabilisasiresonansi dalam keadaan transisi yang menghasilkan karbokation itu. Dalarn hal ini elektron-pi dalam dari cincin benzena membantu menyebarkan muatan. Kedua struktur resonansi pertama yang ditunjukkan di atas adalah penyumbang utama karena struktur ini memiliki stabilisasi aromatik. Oleh karena itu karbon yang paling positif dalam zat-antara itu ialah karbon benzil. Karbon inilah yang diserang oleh nukleofil.