Uploaded by
rhesma_uli85
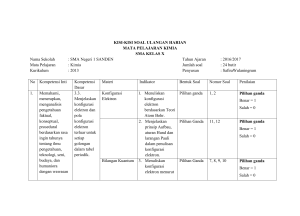
Analisis Soal Ujian Harian: Teori Atom Mekanika Kuantum, Bentuk Molekul, Gaya Antar Molekul - Kelas 11
advertisement

ANALISIS SOAL UJIAN HARIAN KELAS XI BAB: TEORI ATOM MEKANIKA KUANTUM, BENTUK MOLEKUL, DAN GAYA ANTARMOLEKUL Petunjuk Umum : Telitilah soal terlebih dahulu, perangkat soal terdiri dari 20 soal pilihan ganda dan 5 soal uraian. Tidak diperkenankan membuka buku atau catatan apapun atau bekerja sama dengan siswa lain. Waktu untuk mengerjakan adalah 60 menit. A. SOAL OBJEKTIF 1. Indikator : peserta didik dapat mengingat tokoh kimia yang mengemukakan tentang teorinya. Butir Soal : Pernyataan di bawah ini yang merupakan teori atom Niels Bohr adalah..... a. Elektron-elektron mengitari inti atom pada tingkat energi tertentu. b. Elekktron dapat berpindah dari tingkat energi satu ke tingkat energi yang lain. c. Lintasan berbentuk lingkaran. d. Elektron bersifat gelombang dan partikel. e. Ruang di disekitar inti ditemukan elektron yang disebut orbital. A. a, b, c B. a, c, e C. a, b, d D. b, c, e E. c, d, e Analisis : Soal ini termasuk dalam C1, K1 (mengingat, pengetahuan fakta kimia) karena dalam soal ini, peserta didik dituntut untuk mengingat fakta mengenai Teori Atom Bohr. 2. Indikator : peserta didik dapat mengingat tokoh kimia beserta teori yang dikemukakannya. Butir soal : Gerakan partikel yang bergerak dengan kecepatan mendekati kecepatan cahaya seperti gerakan elektron mengitari inti atom, mempunyai sifat gelombang. Pernyataan diatas merupakan hipotesis dari ... A. Max Planck D. Niels Bohr B. Louis de Broglie E. Erwin Schrodinger C. Ernest Rutherford Analisis : Soal ini termasuk dalam C1, K1 (mengingat, pengetahuan fakta kimia) karena dalam soal ini, peserta didik dituntut untuk mengingat fakta mengenai Hipotesis Louis de Broglie. 3. Indikator : peserta didik mampu mengingat fungsi dari bilangan-bilangan kuantum. Butir Soal : Fungsi dari bilangan kuantum azimuth (l) adalah ... A. Menunjukkan orbital khusus mana yang ditempati elektron pada suatu sub-kulit. B. Menunjukkan posisi elektron dalam kulit elektron. C. Menunjukkan sub-kulit yang nilainya tergantung dari bilangan kuantum sebelumnya. D. Menyatakan orientasi khusus dari orbital dalam ruang relatif terhadap inti. E. Menunjukkan arah rotasi elektron. Analisis : Soal tersebut termasuk C1, K2 (mengingat, pengetahuan konsep kimia) karena dalam soal tersebut peserta didik dituntut untuk dapat mengingat fungsi dari bilangan kuantum. 4. Indikator : peserta didik dapat menentukan jumlah elektron maksimum yang dapat menempati sub-kulit tertentu. Butir soal : Atom dengan bilangan kuantum utama = 2, maka jumlah elektron maksimum yang dapat menempati sub-kulit tersebut adalah ... A. 14 D. 4 B. 10 E. 2 C. 6 Analisis : : Soal ini termasuk C3, K2 (mengaplikasikan, pengetahuan konsep kimia), karena pada soal ini, peserta didik dituntut untuk mengaplikasikan konsep kimia dalam menentukan jumlah elektron maksimum yang dapat menempati suatu subkulit berdasarkan bilangan kuantum utama. 5. Indikator : peserta didik dapat menentukan 4 bilangan kuantum berdasarkan nomor atom yang telah diketahui. Butir soal :Dalam atom X dengan nomor atom 35, keempat bilangan kuantum untuk elektron terakhirnya adalah ... A. n= 4, l= 0, m=0, s= +1/2 B. n=4, l=0, m=0, s= -1/2 C. n=4, l=1, m=0, s= -1/2 D. n=4, l=1, m=0, s= -1/2 E. n=4, l=1, m=1, s= -1/2 Analisis : : Soal ini termasuk C3, K3 (mengaplikasikan, pengetahuan metodologi), karena pada soal ini, peserta didik dituntut untuk mengaplikasikan konsep kimia dan metodologi dalam menentukan keempat bilangan kuantum berdasarkan nomor atom yang telah diketahui. 6. Indikator : peserta didik dapat mengingat tokoh kimia dan pendapat yang dikemukakannya. Butir soal : Satu orbital hanya terdapat maksimum 2 elektron. Sehingga jumlah maksimum elektron setiap subkulit adalah dua kali jumlah orbitalnya. Pernyataan ini dikemukakan oleh ... A. Aufbau D. Heisenberg B. Pauli C. Hund E. Planck Analisis : Soal tersebut termasuk C1, K2 (mengingat, pengetahuan fakta kimia) karena dalam soal tersebut peserta didik dituntut untuk dapat mengingat pendapat dari tokoh kimia dengan aturan yang dikemukakannya tentang konfigurasi elektron. 7. Indikator : peserta didik mampu menentukan konfigurasi elektron berdasarkan tingkat energi. Butir soal : Cara pengisisan elektron yang tepat pada tingkat energi sesuai urutan adalah ... A. 1s, 2s, 2p, 3s, 3p, 4s, 4p, 3d, 3f B. 1s, 2s, 2p, 3s, 3p, 3d, 4s, 4p, 4d C. 1s, 2s, 2p, 2d, 3s, 3p, 4s, 3d, 4p D. 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s E. 1s, 2s, 2p, 3s, 3p, 3d, 3f, 4s, 4p Analisis : soal tersebut termasuk C3 K2 (mengaplikasikan, pengetahuan konsep kimia) karena dalam soal tersebut peserta didik dituntut untuk dapat mengaplikasikan konsep kimia dalam menentukan konfigurasi elektron berdasarkan tingkat energi. 8. Indikator : peserta didik dapat menentukan konfigurasi elektron berdasarkan aturan Aufbau. Butir soal : Konfigurasi elektron atom Mn (Z=25) berdasarkan aturan Aufbau adalah ... A. 1s2 , 2s2 , 2p6 , 3s2 , 3p6 , 4s2 , 3d5 B. 1s2 , 2s2 , 2p6 , 3s2 , 3p6 , 4s1 , 3d6 C. 1s2 , 2s2 , 2p6 , 3s2 , 3p6 D. 1s2 , 2s2 , 2p6 , 3s2 E. 1s2 , 2s2 , 2p6 , 3s2 , 3p6 , 4s1 Analisis : soal tersebut termasuk C3 K3 (mengaplikasikan, pengetahuan metodologi) karena dalam soal tersebut peserta didik dituntut untuk dapat mengaplikasikan konsep kimia dan metodologi dalam menentukan konfigurasi elektron berdasarkan unsur yang telah diketahui nomor atomnya. 9. Indikator : peserta didik dapat menetukan konfigurasi elektron dengan menyingkat menggunakan nomor atom dari unsur gas mulia. Butir soal : Penulisan konfigurasi elektron dengan cara menyingkat pada atom 42Mo adalah ... A. [Ar] 3d10 , 4s2 D. [Kr] 4d4, 5s2 B. [Ar] 3d10 ,4s2 , 4p6 E. [Kr] 4d10 C. [Kr] 4d10, 5s2 Analisis : soal tersebut termasuk C3 K3 (mengaplikasikan, pengetahuan metodologi) karena dalam soal tersebut peserta didik dituntut untuk dapat mengaplikasikan konsep kimia dan metodologi dalam menentukan konfigurasi elektron dengan menyingkat menggunakan unsur dari gas mulia. 10. Indikator : peserta didik dapat menentukan konfigurasi elektron dengan mengetahui golongan dan perioda. Butir soal : Unsur yang terdapat pada golongan VI A dan perioda 3 dalam sistem periodik unsur memiliki konfigurasi elektron ... A. 1s2 , 2s2 , 2p6 , 3s2 , 3p6 , 4s2 , 3d4 B. 1s2 , 2s2 , 2p6 , 3s2 , 3p6 C. 1s2 , 2s2 , 2p6 , 3s2 , 3p4 D. 1s2 , 2s2 , 2p6 , 3s2 , 3p5 , 4s1 E. 1s2 , 2s2 , 2p6 , 3s1 , 3p5 Analisis : soal tersebut termasuk C3 K3 (mengaplikasikan, metodologi) karena dalam soal tersebut peserta didik dituntut untuk dapat mengaplikasikan konsep kimia dan metodologi dalam menentukan konfigurasi elektron berdasrkan golongan dan perioda yang telah diketahui. 11. Indikator : peserta didik dapat menentukan golongan dan perioda dari konfigurasi elektron suatu unsur. Butir soal : Konfigurasi elektron dari suatu atom unsur X adalah 1s2 , 2s2 , 2p6 , 3s2 , 3p6 , 4s2 , 3d5 unsur tersebut terletak pada golongan dan perioda ... A. VII A dan 4 D. III A dan 5 B. VII B dan 4 E. V A dan 3 C. VIIA dan 3 Analisis : soal tersebut termasuk C3 K3 (mengaplikasikan, pengetahuan metodologi) karena dalam soal tersebut peserta didik dituntut untuk dapat mengaplikasikan konsep kimian metodologi dalam menentukan golongan dan perioda dari konfigurasi elektron yang telah diketahui. 12. Indikator : peserta didik dapat menentukan unsur segolongan dalam tabel periodik unsur. Butir soal : Diketahui unsur : A (Z= 3) D (Z= 15) B (Z= 11) E (Z= 19) C (Z= 20) Unsur yang terletak pada golongan yang sama adalah ... A. A, B, C B. B, C, D C. C, D, E D. A, B, E E. A, C, E Analisis : soal tersebut termasuk C2 K2 (memahami, pengetahuan konsep kimia) karena dalam soal tersebut peserta didik dituntut untuk dapat memahamitabel periodik unsur dan konsep kimia dalam menentukan unsur yang segolongan. 13. Indikator : pesrta didik dapat menentukan PEB dan PEI dari suatu senyawa. Butir soal : PEI dan PEB dari senyawa BeCl2 (Z Be= 4 dan Z Cl= 17) adalah... A. 2 dan 0 D. 0 dan 1 B. 2 dan 1 E. 2 dan 2 C. 1 dan 2 Analisis : soal tersebut termasuk C3 K2 (mengaplikasikan, pengetahuan konsep kimia) karena dalam soal tersebut peserta didik dituntut untuk dapat mengaplikasikan konsep kimia dalam menentukan PEB dan PEI dari suatu senyawa yang telah diketahui nomor atomnya. 14. Indikator : peserta didik dapat mengingat bentuk molekul dari deskripsi yang telah dijabarkan. Butir soal : Jika terdapat 3 pasang elektron, maka tolak menolak minimum terjadi jika ketiga pasang elektron membentuk sudut 120 0, maka bentuk molekulnya ... A. Linear D. Bipiramida Trigonal B. Trigonal planar E. Bengkok C. Tetrahedral Analisis : soal tersebut termasuk C2 K2 (memahami, pengetahuan konsep kimia) karena dalam soal tersebut peserta didik dituntut untuk dapat memahami konsep kimia dalam menentukan menentukan bentuk molekul dari sebuah deskripsi. 15. Indikator : peserta didik dapat memahami konsep kimia untuk menentukan kekuatan daya tolak menolak antar domain. Butir soal : Urutan kekuatan daya tolak menolak antar domain adalah ... A. DEB-DEB > DEB- DEI > DEI-DEI B. DEB-DEI >DEI-DEI > DEB- DEI C. DEI-DEI > DEB-DEB >DEB-DEI D. DEB-DEI >DEB-DEB > DEI-DEI E. DEI-DEI > DEB-DEI > DEB-DEB Analisis : soal tersebut termasuk C3 K2 (mengaplikasikan, pengetahuan konsep kimia) karena dalam soal tersebut peserta didik dituntut untuk dapat mengaplikasikan konsep kimia dalam menentukan urutan energi tolak menolak antar domain. 16. Indikator : peserta didik dapat menentukan tipe molekul yang dimiliki oleh senyawa. Butir soal : Tipe molekul yang dimiliki oleh senyawa SO3 adalah ... A. AX4 D. AX2E2 B. AX3 E. AX3E2 C. AX2 Analisis : soal tersebut termasuk C3 K3 (mengaplikasikan, pengetahuan metodologi) karena dalam soal tersebut peserta didik dituntut untuk dapat mengaplikasikan konsep kimia dan metodologi dalam menentukan tipe molekul. 17. Indikator : peserta didik mampu menentukan orbital hibrida dari senyawa. Butir soal : Orbital hibrida dari BeH2 adalah ... A. Sp D. Sp2d B. Sp2 E. Sp3d C. Sp3 Analisis : soal tersebut termasuk C3 K3 (mengaplikasikan, pengetahuan metodologi) karena dalam soal tersebut peserta didik dituntut untuk dapat mengaplikasikan konsep kimia dan metodologi dalam menentukan orbital hibrida. 18. Indikator : peserta didik dapat mengingat bentuk molekul dari orbital hibrida yang telah diketahui. Butir soal : Bentuk molekul dari orbital hibrida sp 3d adalah ... A. Linear D. Bipiramida trigonal B. Trigonal planar E. Oktahedral C. Tetrahedral Analisis : soal tersebut termasuk C1 K2 (mengingat, pengetahuan konsep kimia) karena dalam soal tersebut peserta didik dituntut untuk dapat mengingat konsep kimia dalam menentukan bentuk molekul dari orbital hibrida yang telah diketahui. 19. Indikator : peserta didik dapat menentukan urutan kekuatan gaya london dari molekul-molekul. Butir soal : Untuk molekul H2 , N2 ,O2 , Br2. Urutan kekuatan Gaya London dari yang terlemah ke yang paling kuat adalah ... A. Br2 - O2 – N2 – H2 D. N2- H2 –O2 –Br2 B. H2 - N2 - O2 - Br2 E. O2 – H2 – Br2 –N2 C. O2 – N2 – H2 – Br2 Analisis : soal tersebut termasuk C2 K2 (memahami, pengetahuan konsep kimia) karena dalam soal tersebut peserta didik dituntut untuk dapat memahami konsep kimia dalam menentukan urutan kekuatan Gaya London. 20. Indikator : peserta didik dapat mengetahui senyawa yang memiliki ikatan hidrogen. Butir soal : Contoh senyawa yang mempunyai Gaya London kecuali ... A. CO2 D. CH4 B. PCl5 E. HF C. SF6 Analisis : soal tersebut termasuk C3 K2 (memahami, pengetahuan konsep kimia) karena dalam soal tersebut peserta didik dituntut untuk dapat memahami konsep kimia dalam menentukan senyawa yang memiliki ikatan hidrogen. B. SOAL URAIAN Kerjakan soal dibawah ini dengan benar dan singkat! 1. Indikator : peserta didik dapat menentukan harga keempat bilangan kuantum dari elektron terakhir dari unsur. Butir soal : tentukan keempat bilangan kuantum dari elektron terakhir dari unsur-unsur berikut. a. 22Ti b. 20Ca c. 28N d. 30Zn Analisis : Soal ini termasuk C3, K3 (mengaplikasikan, pengetahuan metodologi), karena pada soal ini, peserta didik dituntut untuk mengaplikasikan tentang pengetahuan metodologi, yaitu cara menentukan bilangan kuantum elektron terakhir dari suatu unsur. 2. Indikator : peserta didik dapat menentukan konfigurasi elektron dan diagram orbital dari unsur kimia. Butir soal : Suatu unsur Sc memiliki nomor atom 21, unsur K memiliki nomor atom 19. Tentukan: a. Konfigurasi elektron berdasarkan tingkat energi. b. Konfigurasi elektron berdasarkan kulitnya. c. Konfigurasi elektron dari Sc3+ dan K+ d. Gambarkan diagram orbital elektron valensi masing-masing unsur Analisis : Soal ini termasuk C3, K3 (mengaplikasikan, pengetahuan metodologi), karena pada soal ini, peserta didik dituntut untuk mengaplikasikan tentang pengetahuan metodologi, yaitu cara menentukan konfigurasi elektron dan diagram orbital dari suatu unsur. 3. Indikator : Peserta didik dapat mencari letak suatu unsur pada tabel periodik melalui konfigurasi elektron dan mengelompokkan unsur dalam satu golongan berdasarkan konfigurasi elektronnya. Butir soal : unsur K, Rb, dan Sr yang masing-masing unsur memlili nomor atom secara berurutan 19, 37, dan 38. a. Tentukan letak masing-masing unsur dalam tabel periodik unsur b. Tentukan unsur yang segolongan dan seperioda Analisis : Soal ini termasuk C3, K2 (mengaplikasikan, pengetahuan konsep kimia), karena pada soal ini, peserta didik dituntut selain untuk mencari letak unsur juga mengelompokkan unsur yang terdapat dalam satu periode. 4. Indikator : Peserta didik dapat menentukan bentuk molekul dari suatu senyawa dengan mengaplikasikan teori hibridisasi. Butir soal : Tentukan konfigurasi elektron, diagram orbital sebelum dan sesudah hibridisasi, orbital hibrida, dan bentuk molekul SiCl 4. Analisis : Soal ini termasuk C3, K2 (mengaplikasikan, pengetahuan konsep kimia) karena peserta didik dituntut untuk memahami konsep hibridisasi. 5. Indikator : Peserta didik dapat menentukan gaya antarmolekul yang bekerja pada suatu senyawa. Butir soal : Sebutkan gaya apa yang bekerja pada senyawa berikut! a. HF b. HCl c. I2 d. HBr e. NH3 Analisis : Soal ini termasuk dalam C3,K2 (mengaplikasikan, pengetahuan konsep kimia) karena dalam soal ini, peserta didik dituntut untuk mengingat konsep tentang gaya antarmolekul dan menentukan jenis gaya yang bekerja pada senyawa tersebut. KUNCI JAWABAN A. Soal Objektif 1. A 8. A 15. A 2. B 9. D 16. B 3. C 10. C 17. A 4. C 11. B 18. D 5. D 12. D 19. B 6. B 13. A 20.E 7. D 14. B B. Soal Uraian 1. 22Ti : 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d2 n=3, l=2, m= -1, s= +1/2 20Ca : 1s2, 2s2, 2p6, 3s2, 3p6, 4s2 n=4, l=0, m=0, s= -1/2 28N : 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d8 n=3 , l=2, m=1, s= -1/2 30Zn : 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10 n=3, l=2, m=2, s= -1/2 2. * 21Sc : 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d1 19K : 1s2, 2s2, 2p6, 3s2, 3p6, 4s1 *21Sc : 1s2, 2s2, 2p6, 3s2, 3p6, 3d1 , 4s2 19K : 1s2, 2s2, 2p6, 3s2, 3p6, 4s1 *Sc3+ : 1s2, 2s2, 2p6, 3s2, 3p6 K+ : 1s2, 2s2, 2p6, 3s2, 3p6 *21Sc : 3d1 , 4s2 19K 3. : 4s1 *19K : 1s2, 2s2, 2p6, 3s2, 3p6, 4s1 ( golongan IA dan perioda 4) 37Rb dan 38Sr : 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10 ,4p6, 5s1 (golongan IA perioda 5) : 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10 ,4p6, 5s2 (golongan IIA dan perioda 5) Unsur yang segolongan yaitu : K dan Rb Unsur yang seperioda yaitu : Rb dan Sr 4. Konfigurasi elektron atom pusat : 14Si : 1s2 2s2 2p6 3s2 3p2 Diagram Orbital sebelum hibridisasi : Diagram Orbital setelah hibridisasi: Orbital hibrida : sp3 Bentuk molekul : Tetrahedral 5. Gaya apa yang bekerja pada senyawa berikut a. HF : gaya hidrogen b. HCl : gaya antar dipol c. I2 : gaya london d. HBr : gaya antar dipol e. NH3 : gaya antar dipol PEDOMAN PENSKORAN 1. SOAL OBJEKTIF Untuk soal pilihan ganda, benar mendapatkan skor 1 x 2 ; salah 0; dan kosong 0. 2. SOAL URAIAN Butir soal no 1 No Konsep yang diskor 1 Menuliskan harga ke empat bilangan kuantum Skor 12 dari masing masing unsur: 22Ti : 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d2 n=3, l=2, m= -1, s= +1/2 20Ca : 1s2, 2s2, 2p6, 3s2, 3p6, 4s2 n=4, l=0, m=0, s= -1/2 28N : 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d8 n=3 , l=2, m=1, s= -1/2 30Zn : 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10 n=3, l=2, m=2, s= -1/2 Jumlah skor 12 Butir soal no 2 No Konsep yang diskor 1 Menuliskan konfigurasi elektron dari masing- Skor 3 masing unsur sesuai tingkat energi * 21Sc : 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d1 19K 2 : 1s2, 2s2, 2p6, 3s2, 3p6, 4s1 Menuliskan konfigurasi elektron berdasarkan 3 kenaikan kulit 21Sc 19K 3 : 1s2, 2s2, 2p6, 3s2, 3p6, 3d1 , 4s2 : 1s2, 2s2, 2p6, 3s2, 3p6, 4s1 Menuliskan konfigurasi elektron dari ion-ion 3 Sc3+ : 1s2, 2s2, 2p6, 3s2, 3p6 K+ : 1s2, 2s2, 2p6, 3s2, 3p6 4 Menggambarkan diagram orbital elektron valensi 3 dari Sc dan K : 3d1 , 4s2 21Sc 19K : 4s1 Jumlah skor 12 Butir soal no 3 No Konsep yang diskor 1 Skor Menuliskan konfigurasi elektron kemudian 8 menjelaskan atom tersebut dalam golongan dan periode berapa 19K : 1s2, 2s2, 2p6, 3s2, 3p6, 4s1 ( golongan IA dan perioda 4) 37Rb : 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10 ,4p6, 5s1 (golongan IA dan 38Sr perioda 5) : 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10 ,4p6, 5s2 (golongan IIA dan perioda 5) 2 Menggolongkan unsur dalam satu golongan dan 4 perioda Unsur yang segolongan yaitu : K dan Rb Unsur yang seperioda yaitu : Rb dan Sr Jumlah skor 12 Butir soal no 4 No Konsep yang diskor 1 Dapat menuliskan konfigurasi elektron dari Skor 2 atom pusat 14Si 2 : 1s2 2s2 2p6 3s2 3p2 Dapat menggambar diagram orbital sebelum 2 hibridisasi 3 Dapat menggambar orbital hibrida setelah hibridisasi 4 4 Dapat menentukan orbital hibridanya Orbital hibrida 5 : sp3 Dapat menentukan bentuk molekulnya Bentuk molekul 2 2 : tetrahedral Jumlah skor 12 Butir soal no 5 No Konsep yang diskor 1 Gaya antarmolekul dari masing-masing unsur Skor 12 adalah sebagai berikut: HF : gaya hidrogen HCl: gaya antar dipol I2: gaya london HBr : gaya antar dipol NH3 : gaya antar dipol Skor Butir Skor Total = (Skor Objektif x 2) + Skor uraian = (20 x2) x 60 = 100 12