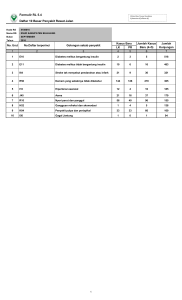
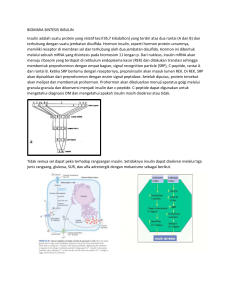
BAB II PEMBAHASAN 2.1 Anatomi Pankreas Pankreas merupakan organ pipih retroperitoneal yang terletak di bagian posterior dari dinding lambung. Letaknya diantara duodenum dan limfa, di depan aorta abdominalis dan arteri serta vena mesenterica superior. Organ ini konsistensinya padat, panjangnya kira-kira 20-25 cm, tebal ± 2,5 cm dan beratnya sekitar 80 gram. Struktur organ ini lunak dan berlobus, terdiri dari bagian kepala/caput yang terletak di sebelah kanan, diikuti corpus ditengah, dan cauda di sebelah kiri berdekatan dengan limfa. Ada sebagian kecil dari pancreas yang berada di bagian belakang arteri mesenterika superior yang disebut dengan processus uncinatus.[7] Gambar 2.1.1. Anatomi Pankreas [9] 2 Pankreas juga merupakan suatu organ yang terdiri dari jaringan eksokrin dan endokrin. Bagian eksokrin berbentuk seperti anggur yang disebut sebagai asinus/Pancreatic acini, mengeluarkan larutan encer alkalis serta enzim pencernaan melalui duktus pankreatikus ke dalam lumen saluran cerna. Bagian endokrin terletak diantara sel-sel eksokrin di seluruh pankreas yang tersebar berkelompok atau membentuk “pulau” sel endokrin yang dikenal sebagai pulau (islets) Langerhans. Sel endokrin pankreas menghasilkan hormon insulin dan glukagon.[7] Gambar 2.1.2. Asinus dan Pulau Langerhans Pulau-pulau Langerhans tersebut terdiri dari beberapa sel yaitu:[8] 1. Sel α (sekitar 10%), menghasilkan hormon glucagon, proglucagon, glucagon like peptide (GLP-1 dan GLP-2) 2. Sel β (dengan jumlah paling banyak 70-80%), menghasilkan hormon insulin, C-peptide, proinsulin, amylin, aminobutyric acid (GABA) 3. Sel δ (sekitar 3-5%), menghasilkan hormon somatostatin atau growh hormon-inhibiting hormone (GH-IH) 4. Sel F atau PP (paling jarang < 2%), menghasilkan polipeptida pankreas. 2.1.1 Fisiologi Pankreas Fungsi eksokrin pankreas adalah menghasilkan cairan jernih tidak berwarna, mengandung air, beberapa garam, sodium bikarbonat dan enzim-enzim. pH cairan 3 pankreas alkali (Ph: 7.1–8.2) karena mengandung sodium bikarbonat. Keadaan pH ini akan menghambat gerak pepsin dari lambung dan menciptakan lingkungan yang sesuai dengan enzim-enzim dalam usus halus.[10,11] Enzim-enzim pada pankreas yang dihasilkan oleh sel-sel asinar, fungsinya membantu pemecahan protein, karbohidrat dan lemak. Enzim-enzim yang berperan ini di produksi di dalam sel-sel pankreas dalam bentuk tidak aktif yaitu tripsinogen, kimotripsinogen dan prokarboksipeptidae. Setelah di sekresi kedalam saluran pencernaan, zat tersebut diaktifkan, tripsinogen di aktifkan oleh enzim untuk pencernaan enterokinase yang oleh tripsin diubah menjadi kemotripsin, demikian juga terjadi pada prokarboksipeptidase.[10,11] Pengaturan produksi dari cairan pankreas dilakukan oleh pengaturan saraf dan pengaturan hormonal. Pengaturan saraf terjadi bila adanya stimulus dari fase sefalik dan sekresi lambung sehingga impuls parasimpatis secara serentak dihantarkan sepanjang nervus vagus ke pankreas dan mengakibatkan produksi cairan pankreas. Sedangkan pengaturan hormonal terjadi akibat stimulasi hormon sekretin dan kolesistokinin yang menyebabkan peningkatan sekresi enzim.[10] Sedangkan untuk fungsi endokrin pankreas, berhubungan erat dengan sel-sel yang ada pada pulau Langerhans dalam pengaturan secara langsung sekresi hormon sesuai dengan fungsi sel masing- masing. Adanya umpan balik negatif langsung antara konsentrasi gula darah dan kecepatan sekresi sel alfa, tetapi hubungan tersebut berlawanan arah dengan efek gula darah pada sel beta. Kadar gula darah akan dipertahankan pada nilai normal oleh peran antagonis hormon insulin dan glukagon, akan tetapi hormon somatostatin menghambat sekresi keduanya.[9] 4 Gambar 2.1.1. Feedback negative system antara insulin dan glucagon[7] 2.1.2 Fisiologi Insulin Insulin dilepaskan oleh sel beta pankreas setelah terjadi transport glukosa oleh GLUT-2 masuk kedalam sel beta, glukosa yang masuk kedalam sel beta akan mengalami proses glikolisis oleh glikokinase menjadi glukosa- 6 Phospate, yang mengaktifkan pembentukan Asetyl-Co A, masuk kedalam siklus krebs dalam mitokondria untuk diubah menjadi ATP (Adenosine Tri Phospat) sehingga meningkatkan jumlah ATP dalam sel, hal ini akan menginkativasi pompa kalium sensitif ATP, lalu menginduksi depolarisasi dari membran plasma dan voltage dependent calcium channel, menyebabkan influks calcium extrasel yang merangsang pergerakan cadangan kalsium intrasel sehingga menginduksi terjadinya pengikatan granula produsen insulin ke membran sel dan pelepasan insulin kedalam peredaran darah. [7,12,13] 5 Gambar 2.1.2. Mekanisme Sekresi Hormon Insulin[7,13] Secara singkat kerja fisiologis insulin adalah mentransportasi glukosa kedalam sel otot dan hati terkait dengan kadar glukosa didalam darah, efek kerja insulin berlawanan dengan glukagon yang akan memicu proses pembentukan glukosa di dalam hati melalui proses glikolisis dan gluconeogenesis.[12,13,14,15,16] Insulin disekresikan ke dalam sistem pembuluh darah porta hepatik. Pada individu normal kadar insulin setelah puasa 8 jam berkisar antara 5 - 15 umol/L. Kadar insulin pada vena porta sekitar 3 kali lipat dari kadar insulin pada plasma darah arteri. Sehingga kadar insulin plasma darah pada sinusoid hati yang merupakan kombinasi dari 20% campuran darah arteri dan 80% campuran darah dari vena porta berkisar antara 15 - 45 umol/L.[13,14] Adanya peningkatan kadar gula darah (hiperglikemia) (normal kadar gula darah 70-110 mg /dl), asam amino, serum lemak bebas serta stimulus saraf parasimpatik akan memicu peningkatan sekresi insulin. Sedangkan rendahnya kadar gula darah 6 (hipoglikemia) serta adanya aktivasi dari stimulus saraf simpatis dan prostaglandin akan menghambat produksi insulin.[10] 2.1.3 Fisiologi Glukagon Glukagon disekresikan oleh sel alfa pankreas yang memiliki sifat antagonis terhadap insulin, glukagon merupakan hormon polipeptida yang awalnya disintesis sebagai proglukagon yang akan di proses secara proteolitik menjadi prohormon glukagon. Glukagon tidak hanya ada di jaringan pankreas namun juga ada di jaringan lain seperti di bagian enteroendokrin dalam lumen usus dan di jaringan otak. Sasaran utama glukagon adalah hati, yaitu dengan mempercepat konversi glikogen dalam hati dari nutrisi lainnya seperti asam amino, gliserol dan asam laktat menjadi glukosa (glukoneogenesis). [7,10,13] Secara umum fungsi glukagon adalah merombak glikogen menjadi glukosa, mensintesis glukosa dari asam lemak dan asam amino (glukoneogenesis ) serta pembebasan glukosa ke darah oleh sel-sel hati. Sekresi glukagon secara langsung di kontrol oleh kadar gula darah melalui system feed back negative. Ketika gula darah menurun maka akan merangsang sel-sel alfa untuk mensekresi glucagon.[10,13] Hormon somatostatin juga menekan sekresi glukagon, sedangkan epinephrin memacu pengeluaran glukagon dengan aktivasi Beta-2 adrenergik receptor sel. Epinephrin bersifat inhibisi sekresi insulin dengan cara mengaktivasi Alpha-2 adrenergik sehingga menekan produksi sel beta. Aktivasi saraf parasimpatis (vagal) juga memacu sekresi glukagon. [7,10,13] 7 Gambar 2.1.3 Peran binding insulin dalam sintesis glikogen (glukoneogenesis)[7,13] 2.2 Diabetes Melitus 2.2.1 Definisi dan Epidemiologi Diabetes melitus (DM) termasuk dalam kelompok penyakit metabolik yang ditandai dengan hiperglikemia kronik yang disebabkan oleh gangguan dari sekresi insulin, aksi insulin atau keduanya. Secara umum diabetes dibagi dalam dua bentuk utama yaitu kerusakan sel beta pankreas yang menyebabkan defisiensi sebagian atau keseluruhan insulin, dan resistensi insulin pada jaringan dengan sedikit atau tanpa gangguan sintesis atau pelepasan insulin sehingga menyebabkan gangguan metabolisme karbohidrat, lemak dan protein.[2] Data Riskesdas (2013) menunjukkan bahwa proporsi diabetes di Indonesia pada tahun 2013 meningkat hampir dua kali lipat dibandingkan tahun 2007. Proporsi diabetes melitus di Indonesia sebesar 6,9 %, toleransi glukosa terganggu (TGT) sebesar 29,9% dan glukosa darah puasa (GDP) terganggu sebesar 36,6%. Proporsi penduduk di pedesaan yang menderita diabetes melitus hampir sama dengan penduduk di perkotaan. Prevalensi diabetes melitus meningkat dari 1,1 persen (2007) menjadi 2,1 persen (2013).[17] 8 2.2.2 Klasifikasi Menurut American Diabetes Association (ADA) tahun 2016, diabetes melitus dibagi menjadi beberapa klasifikasi berdasarkan etiologinya, yaitu:[1] a. Diabetes Tipe-1, adanya kerusakan sel β pankreas sehingga terjadi defisiensi insulin secara absolut sehingga menyebabkan ketergantungan insulin (apabila penderita tidak mendapat insulin tambahan maka akan koma ketoasidosis). Diabetes tipe-1 ini biasa terjadi pada anak-anak dengan penyebabnya berupa autoimun atau idiopatik. b. Diabetes Tipe-2, terjadi akibat dominasi resistensi insulin (obesitas), hingga menyebabkan terjadinya defisiensi insulin relatif sampai dominasi sekresi insulin disertai resistensi insulin (banyak terjadi pada orang dewasa). c. Diabetes Tipe Lain, terjadi akibat penyakit eksokrin pankreas, endokrinopati, defek genetik fungsi sel beta, defek genetik fungsi insulin, pengaruh obat dan zat kimia (kortikosteroid), infeksi, sindeom genetik lain yang berkaitan dengan diabetes. d. Diabetes Gestasional, diabetes yang didiagnosis pertama kali pada saat kehamilan. Keadaan ini terjadi akibat hormon-hormon pertumbuhan yang berfungsi untuk pertumbuhan janin merupakan hormon kontraregulasi insulin, sehingga menyebabkan kadar glukosa darah meningkat. Kadar glukosa darah setelah melahirkan dapat kembali normal atau menetap dan menjadi diabetes. 9 Tabel 2.2.1 Klasifikasi Diabetes dan Intoleransi Glukosa Abnormal (ADA, 2016) Klasifikasi Diabetes dan Intoleransi Glukosa Abnormal American Diabetes Association (ADA) 1. Diabetes mellitus a. Tipe 1 1) Autoimun 2) Idiopatik b. Tipe 2 2. Diabetes mellitus kehamilan (GDM) 3. Tipe spesifik lain a. Cacat genetik fungsi sel beta: MODY b. Cacat genetik kerja insulin: sindrom resistensi insulin berat c. Endokrinopati: sindrom Cushing, akromegali d. Penyakit eksokrin pankreas e. Obat atau diinduksi secara kimia f. Infeksi 4. Ganggan toleransi glukosa (IGT) 5. Gangguan glukosa puasa (IFG) Kemungkinan diabetes tipe lain perlu dipikirkan pada anak dengan riwayat keluarga autosomal dominan, berhubungan dengan tuli, atrofi optik, atau gambaran sindrom yang lain, resistensi insulin, riwayat terpapar obat-obatan yang toksik terhadap sel β dan yang menyebabkan tejadinya resistensi insulin. (18) Pada tipe Diabetes Monogeniik ‘Maturity onset diabetes of the young’ (MODY) terdapat kelainan genetik dari fungsi sel β atau aksi insulin. Karakteristik kelainannya berupa: timbul sebelum usia 25 tahun, autosomal dominan, diabetes nonketotik. Kelainan genetiknya memperlihatkan gambaran yang berbeda antara subgroup genetik. Oleh sebab itu pada tipe ini terdapat banyak variasi derajat hiperglikemia, kebutuhan terhadap insulin, dan risiko komplikasi yang akan terjadi 10 Tabel 2.2.2 Karakteristik klinik DM tipe-1, tipe-2, dan monogenik yang direkomendasikan oleh International Society of Pediatric and Adolesence Diabetes dan WHO[1,18] Karakteristik Genetik Onset Tipe-1 Poligenik 6 bulan – dewasa muda Tipe-2 Monogenik Poligenik Monogenik Pubertas (sd lebih Sering setelah tua) pubertas kecuali glukokinase dan diabetes neonatal Sering akut, Bervariasi : Bervariasi : Gambaran klinik cepat perlahan, sedang, insidensial pada berat glukokinase Tidak Tidak Berhubungan dengan Ya Autoimun Sering Tidak Sering terjadi pada Ketosis diabetes neonatal tapi jarang pada bentuk lain Banyak Meningkat pada Banyak pada Obesitas populasi populasi Tidak Ya Tidak Akantosis nigrikans Beberapa Negara < 1-3% Angka kejadian (% pada >90% 10% semua kasus diabetes anak) 2-4% 80% 90% Orang tua diabetes 2.2.3 Kriteria Diagnosis DM ditegakkan atas dasar pemeriksaan kadar glukosa darah. Diagnosis tidak dapat ditegakkan atas dasar adanya glukosuria. Pemeriksaan glukosa darah yang dianjurkan adalah pemeriksaan glukosa secara enzimatik dengan bahan darah plasma vena. Pemantauan hasil pengobatan dapat dilakukan dengan menggunakan pemeriksaan glukosa darah kapiler dengan glucometer.Diagnosis DM dapat ditegakkan apabila memenuhi salah satu kriteria sebagai berikut:[17] 1. Kadar glukosa darah puasa ≥ 7,0 mmol/L (≥ 126 mg/dL). Puasa adalah tanpa asupan kalori minimal selama 8 jam. 2. Pemeriksaan glukosa plasma ≥200 mg/dl 2 jam setelah Tes Toleransi Glukosa Oral (TTGO) dengan beban 75 gram 3. Pemeriksaan glukosa plasma sewaktu ≥200 mg/dl dengan keluhan klasik 11 4. Pada penderita yang asimptomatis ditemukan kadar glukosa darah sewaktu >200 mg/dL atau kadar glukosa darah puasa lebih tinggi dari normal dengan tes toleransi glukosa yang terganggu pada lebih dari satu kali pemeriksaan. Keluhan klasik DM: poliuria, polidipsia, polifagia dan penurunan berat badan yang tidak dapat dijelaskan sebabnya. Keluhan lain: lemah badan, kesemutan, gatal, mata kabur, dan disfungsi ereksi pada pria, serta pruritus vulva pada wanita. [17] Hasil pemeriksaan yang tidak memenuhi kriteria normal atau DM, maka dapat digolongkan ke dalam kelompok prediabetes yang meliputi: toleransi glukosa terganggu (TGT), glukosa darah puasa terganggu (GDPT). [17] Glukosa darah puasa terganggu (GDPT): Hasil pemeriksaan glukosa plasma puasa antara 100 - 125 mg/dl dan pemeriksaan TTGO glukosa plasma 2 jam <140 mg/dl Toleransi glukosa terganggu (TGT): Hasil pemeriksaan glukosa plasma 2 jam setelah TTGO antara 140-199 mg/dl Pada anak biasanya tes toleransi glukosa (TTG) tidak perlu dilakukan untuk mendiagnosis DM, karena gambaran klinis yang khas. Indikasi TTG pada anak adalah kasus-kasus yang meragukan yaitu ditemukan gejala klinis yang khas untuk DM, namun pemeriksaan kadar glukosa darah tidak meyakinkan.[2] Pemeriksaan petanda autoantibodi diabetes seperti ICA (Islet Cell Antibodies), GAD (Glutamic Acid Decarboxylase), IA2 (Autoantibodi terhadap tirosin fosfat), IAA (Autoantibodi terhadap insulin) dan/atau HbA1c dapat membantu menegakkan diagnosis diabetes, meskipun HbA1c tidak rutin digunakan untuk mendiagnosis diabetes. Pemeriksaan HbA1c >6,5% dengan menggunakan metode High-Performance Liquid Chromatography (HPLC) yang terstandarisasi oleh National Glycohaemoglobin Standarization Program (NGSP).[2] 12 2.3.Diabetes Melitus Tipe 1 2.3.1 Definisi DM tipe-1 merupakan kelainan sistemik akibat gangguan metabolisme glukosa yang ditandai oleh hiperglikemia kronik. Keadaan ini disebabkan oleh kerusakan sel-β pankreas baik oleh proses autoimun maupun idiopatik sehingga produksi insulin berkurang atau terhenti.[19] 2.3.2 Epidemiologi Insiden DM tipe 1 sangat bervariasi baik antar negara maupun di dalam suatu negara. Di beberapa negara barat kasus DM tipe 1 mencakup 5-10% dari seluruh jumlah penderita diabetes di negara masing-masing. Secara global DM tipe1 ditemukan pada 90% dari seluruh diabetes pada anak dan remaja. Di Indonesia insidens tercatat semakin meningkat dari tahun ke tahun, terutama dalam 5 tahun terakhir. Jumlah penderita baru meningkat dari 23 orang per tahun di tahun 2005 menjadi 48 orang per tahun di tahun 2009 [20]. Insidensi DM Tipe 1 meningkat tiap tahunnya sebesar 3%-5% secara global. Di Indonesia, tidak ada data epidemiologi khusus. Namun, prevalensi diabetes mellitus tipe 1 sekitar 4,8%-5,1% pada tahun 2012, dengan perkiraan 58,8% dari semua kasus diabetes tidak terdiagnosa. Berdasarkan data registri nasional DM tipe-1 pada anak dari Ikatan Dokter Anak Indonesia hingga tahun 2014 tercatat 1021 kasus dengan 2 puncak insidens yaitu pada usia 5-6 tahun dan 11 tahun.[2,4,5,6] Faktor genetik dan lingkungan sangat berperan dalam terjadinya DM tipe 1. Faktor genetik dikaitkan dengan pola HLA pada kromosom 6, meliputi 40% DM1 familial. HLA berperan sebagai suatu susceptibility gene atau faktor kerentanan, lebih dari 90% anak dengan DM1 memiliki HLA DR3, HLA DR4, atau keduanya. Saudara kandung atau anak dari pasien diabetes memiliki risiko 3-6% untuk terkena diabetes, sedangkan kembar identik memiliki risiko 30-50% untuk terkena diabetes.[3] Diperlukan suatu faktor pemicu yang berasal dari lingkungan untuk menimbulkan gejala klinis DM tipe 1 pada seseorang yang rentan. Faktor 13 lingkungan yang dianggap berperan antara lain, pemberian susu sapi sebelum usia 2 bulan, infeksi virus (virus coxsackie B, cytomegalovirus, mumps, dan rubella) dan defisiensi vitamin D. [3,21] Untuk penderita baru DM tipe 1 terdapat 3 pola gambaran klinis saat awitan: klasik, silent diabetes, dan ketoasidosis diabetik (KAD). Di Indonesia 33,3% penderita baru DM tipe 1 didiagnosis dalam bentuk ketoasidosis diabetik (KAD), sedangkan bentuk silent diabetes paling jarang dijumpai; biasanya diketahui karena skrining/penelitian atau pemeriksaan khusus karena salah seorang keluarga penderita telah menderita DM tipe 1 sebelumnya.[20] 2.3.3 Patogenesis Faktor genetik dan lingkungan sangat berperan pada terjadinya DM tipe-1. Walaupun hampir 80% penderita DM tipe-1 baru tidak mempunyai riwayat keluarga dengan penyakit serupa, faktor genetik diakui berperan dalam patogenesis DM tipe-1. Faktor genetik dikaitkan dengan pola HLA tertentu, meskipun bukan faktor dominan pada patogenesis DM tipe-1. HLA berperan hanya sebagai suatu susceptibility gene atau faktor kerentanan sehingga diperlukan suatu faktor pemicu yang berasal dari lingkungan (infeksi virus, toksin dll) untuk menimbulkan gejalagejala klinis DM tipe 1 pada seseorang yang rentan.[3] Proses ini akan berlangsung dalam beberapa bulan sampai tahun sebelum manifestasi klinisnya muncul. Infeksi enterovirus berhubungan dengan timbulnya autoantibodi pada populasi dan enterovirus telah ditemukan di dalam sel islet anak diabetes. Hasil pengamatan menunjukkan kejadian DM tipe-1 lebih rendah pada bayi yang mendapat ASI. Paparan dini dengan susu sapi akan memicu timbulnya DM terutama pada individu yang memiliki kerentanan terhadap penyakit ini. Bila secara klinis menunjukkan gejala DM tipe-1 (sering dihubungkan dengan KAD) tetapi tidak ditemukan antibodi maka diklasifikasikan sebagai DM tipe-1B (idiopatik). Kasus ini banyak ditemukan pada keturunan Afrika dan Asia.[3,21] Anak dengan defisiensi insulin absolut akan berkembang menjadi KAD. Awalnya terjadi kerusakan sel β pankreas yang dipicu melalui mekanisme sel T. Gejala klinis dalam berbagai derajat tingkat kerusakan akan muncul bila kerusakan 14 sel β pankreas sudah mencapai 90%. Delapan puluh lima sampai 90% anak dengan hiperglikemia puasa akan ditemukan petanda autoantibodi terhadap sel β pankreas seperti sel islet, GAD, IA-2, IA-2β, atau autoantibodi insulin.[18] 2.3.4 Patofisiologi Gambar 2.1.4 Patofisiologi Diabetes Melitus Tipe 1 Timbulnya penyakit klinis merupakan tahap akhir dari kerusakan sel beta yang pada DM tipe 1. Berbagai lokus gen telah dipelajari untuk menentukan hubungan mereka dengan DM tipe 1. Antigen yang terlibat dalam tipe 1 DM meliputi antigen 64kD, asam glutamat dekarboksilase (GAD) dan antigen sitoplasma sel islet. Antibodi sel islet (ICA) mengikat komponen sitoplasma sel islet pada bagian pankreas manusia dan endapan antibodi 64kDa merupakan protein 64kDa dari ekstrak sel islet. Antigen target dari Antibodi 64kDa diidentifikasi sebagai GAD enzim. Sel Islet tertentu pada baris sel beta memproduksi antibodi IgG yang terikat ke antigen sitoplasma sel islet yang ditemukan. Dengan demikian, GAD sebagai target antigen utama pada DM tipe 1, maka dari itu antibodi untuk GAD dijadikan penanda sensitif untuk perkembangan diabetes, walaupun antibodi GAD ada dalam individu yang rentan secara genetik tetapi tidak mungkin untuk mengembangkan penyakit.[21] 15 C Gambar 2.1.5. Patomekanisme yang terjadi pada Diabetes Melitus type 1 . Destruksi progresif sel-sel beta mengarah pada defisiensi insulin progresif. Meskipun defisiensi insulin merupakan cacat primer, beberapa perubahan sekunder yang melibatkan hormon stress (epinefrin, kortisol, hormon pertumbuhan dan glukagon) memperbesar kecepatan dan beratnya dekompensasi metabolik. Peningkatan konsentrasi plasma dari hormon kontra-regulasi ini memperberat kekacauan metabolik dengan mengganggu sekresi insulin selanjutnya (epinefrin), mengantagonisme kerja insulin (epinefrin, kortisol, hormon pertumbuhan), serta mempermudah glikogenolisis, glukoneogenesis, lipolisis dan ketogenesis sambil menurunkan penggunaan glukosa serta clearance ginjal. Semua perubahan abnormal ini kembali normal dengan terapi insulin yang adekuat. [21] Pada saat terjadi kekurangan insulin akibat kerusakan dari sel beta di pankreas, maka hiperglikemia berkembang sebagai hasil dari tiga proses: (1) peningkatan glukoneogenesis (pembuatan glukosa dari asam amino dan gliserol), (2) glikogenolisis dipercepat (pemecahan glukosa disimpan) dan (3) pemanfaatan glukosa oleh perifer jaringan. [21] 16 2.3.5 Perjalanan Penyakit DM tipe-1 bisa terjadi pada semua umur, dari bayi baru lahir sampai usia lanjut. Perjalanan penyakit diabetes ditandai melalui beberapa periode :[3] 1. Pre-diabetes 2. Manifestasi klinis diabetes 3. Periode “honeymoon” 4. Ketergantungan insulin yang menetap Pre-diabetes Fase prediabetes diawali dengan kerentanan genetik dan diakhiri dengan kerusakan total sel β pankreas. Kerusakan sel β pankreas ditandai oleh menurunnya sekresi C-peptide. Periode ini ditandai dengan ditemukannya antibody (ICA, GAD, IA, dll) dan merupakan predictor terhadap timbulnya diabetes klinis. Bila ditemukan lebih dari satu autoantibodi akan meningkatkan kemungkinan timbulnya diabetes, misalnya jika terdapat IA2 dan GAD maka risiko untuk menjadi DM tipe-1 adalah sebesar 70% dalam kurun waktu 5 tahun. Parameter yang bisa membantu menentukan stadium ini adalah: Islet cell autoantibodies (ICA) Glutamic acid decarboxylase autoantibodies (65K GAD) IA2 (dikenal sebagai ICA 512 atau tyrosine phosphatase) autoantibodies Insulin autoantibodies (IAA) HLA typing Petanda genetik dengan tipe HLA tertentu, akan meningkatkan atau menurunkan kerentanan terhadap timbulnya DM tipe-1. Faktor lingkungan seperti rubella kongenital, infeksi enterovirus (coxsackie) dan virus ECHO, kasein, protein gluten susu sapi. Manifestasi Klinis Diabetes 17 Pemantauan jangka panjang menunjukkan bahwa gejala klinis bervariasi, bisa mendadak dalam beberapa hari kemudian menjadi KAD atau dalam beberapa minggu menunjukkan gejala klasik DM. Periode “honeymoon” Periode “honeymoon” ini berlangsung beberapa hari sampai beberapa minggu atau bulan setelah terapi insulin, diitandai dengan adanya periode “remisi” (parsial). Periode ini terjadi akibat berfungsinya kembali jaringan residual pankreas sehingga pankreas mensekresikan kembali sisa insulin. Periode ini akan berakhir apabila pankreas sudah menghabiskan seluruh sisa insulin. Kriteria periode “honeymoon” bila kebutuhan insulin kurang dari 0,5 U/kgBB/hari dengan HbA1c <7%. Hal ini perlu dijelaskan kepada keluarga terutama di negara berkembang seperti Indonesia dimana pengobtan tradisional masih banyak digemari oleh masyarakat yang biasanya menganggap fenomena ini sebagai tanda-tanda kesembuhan, padahal keadaan ini hanya bersifat sementara sebelum memasuki periode ketergantungan total terhadap insulin. Periode Ketergantungan Terhadap Insulin Perjalanan penyakit pada periode “honeymoon” ke periode tergantung insulin seumur hidup biasanya lambat, tetapi bisa dipercepat dengan adanya penyakit lain. Terapi sulih insulin merupakan satu-satunya pengobatan untuk DM tipe-1. 2.3.6 Gambaran Klinis Sebagian besar penderita DM tipe-1 mempunyai riwayat perjalanan klinis yang akut. Gejala klinis khasnya berupa poliuria, polidipsia, polifagia, dan berat badan yang cepat menurun (terjadi antara satu sampai dua minggu sebelum diagnosis ditegakkan). Apabila gejala-gejala klinis ini disertai dengan hiperglikemia maka diagnosis DM tidak diragukan lagi.[2,18,19] Insidens DM tipe-1 di Indonesia masih belum diketahui dengan pasti, sehingga masih sering terjadi kesalahan dalam menegakkan diagnosis. Akibatnya pasien sering datang dengan ketoasidosis diabetik pada saat awitan diagnosis. 18 Kesalahan diagnosis yang sering terjadi adalah napas Kussmaul disangka sebagai bronkopneumonia atau dehidrasi dianggap disebabkan oleh gastroenteritis.[2] Strategi utama untuk mengurangi keterlambatan diagnosis adalah meningkatkan kewaspadaan terhadap DM tipe-1. DM tipe-1 harus dipertimbangkan sebagai salah satu diagnosis banding pada anak dengan enuresis nocturnal (pada anak yang sudah besar), anak dengan dehidrasi sedang sampai berat tetapi masih ditemukan diuresis (polyuria) apalagi disertai dengan pernafasan Kussmaul dan bau keton.[2] 2.3.7 Diagnosis Anamnesis Bentuk klasik: - Polidipsi, poliuri, polifagi. Poliuria biasanya tidak diutarakan secara langsung oleh orangtua kepada dokter, yang sering dikeluhkan adalah anak sering mengompol, mengganti popok terlalu sering, disertai infeksi jamur yang berulang di sekitar daerah tertutup popok, dan anak terlihat dehidrasi. - Penurunan berat badan yang nyata dalam waktu 2-6 minggu disertai keluhan lain yang tidak spesifik. - Mudah lelah. Pada kasus KAD: - Awitan gejala klasik yang cepat dalam waktu beberapa hari - Sering disertai nyeri perut, sesak napas, dan letargi Pemeriksaan fisis dan tanda klinis 1. Tanpa disertai tanda gawat darurat - Polidipsi, poliuri, polifagi disertai penurunan berat badan kronik - “Irritable” dan penurunan prestasi sekolah - Infeksi kulit berulang - Kandidiasis vagina terutama pada wanita prepubertas - Gagal tumbuh 19 - Berbeda dengan DMT2 yang biasanya cenderung gemuk, anak-anak DMT1 biasanya kurus 2. Disertai tanda gawat darurat - Penurunan berat badan yang nyata dalam waktu cepat - Nyeri perut dan muntah berulang - Dehidrasi sedang sampai berat namun anak masih poliuria - Sesak napas, napas cepat dan dalam (Kussmaul) disertai bau aseton - Gangguan kesadaran - Renjatan 3. Kondisi yang sulit didiagnosis (sering menyebabkan keterlambatan diagnosis KAD) - Pada bayi atau anak < 2-3 tahun - Hiperventilasi: sering didiagnosis awal sebagai pneumonia atau asma berat - Nyeri perut: sering dikira sebagai akut abdomen - Poliuria dan enuresis: sering didiagnosis awal sebagai infeksi saluran kemih - Polidipsi: sering didiagnosis awal sebagai gangguan psikogenik - Muntah berulang: sering didiagnosis awal sebagai gastroenteritis 4. Harus dicurigai sebagai DMT2 Adanya gejala klinis poliuri, polidipsi, dan polifagi yang diserai dengan adanya hal-hal di bawah ini: - Obesitas - Usia remaja (>10 tahun) - Adanya riwayat keluarga DMT2 - Penanda autoantibodi negative - Kadar C-peptida normal atau tinggi - Ras atau etnik tertentu (Pima-Indian, Arab) 20 2.3.8 Pemeriksaan Penunjang - Kadar gula darah sewaktu: ≥ 200 mg/dL (11,1 mmol/L). Pada penderita asimtomatis ditemukan kadar gula darah puasa lebih tinggi dari normal dan uji toleransi glukosa terganggu pada lebih dari satu kali pemeriksaan. - Kadar gula darah puasa: ≥ 126 mg/dL (puasa tidak ada asupan kalori selama 8 jam). - Kadar gula darah 2 jam pasca toleransi glukosa: ≥ 200 mg/dL (11,1 mmol/L). - Kadar C-peptida: untuk melihat fungsi sel β residu yaitu sel β yang masih memproduksi insulin; digunakan apabila sulit membedakan diabetes tipe 1 dan 2. - Pemeriksaan HbA1c: dilakukan rutin setiap 3 bulan. Pemeriksaan HbA1c bermanfaat untuk mengukur kadar glukosa darah selama 120 hari yang lalu (sesuai usia eritrosit), menilai perubahan terapi 8-12 minggu sebelumnya, dan menilai pengendalian penyakit DM dengan tujuan mencegah terjadinya komplikasi diabetes. - Glukosuria: tidak spesifik untuk DM perlu dikonfirmasi dengan pemeriksaan gula darah. - Penanda autoantibodi: hanya sekitar 70-80% dari penderita DMT1 memberikan hasil pemeriksaan autoantibodi (ICA, IAA) yang positif, sehingga pemeriksaan ini bukan merupakan syarat mutlak diagnosis. [2,3,19,20] Untuk diagnosis diabetes mellitus: diperlukan pemeriksaan glukosa darah sewaktu / puasa atau 2 jam setelah makan/post prandial dan setelah pemberian glukosa per-oral (TTGO). Antibodi untuk petanda (marker) adanya proses autoimun pada sel beta adalah islet cell cytoplasmic antibodies (ICA), insulin autoantibodies (IAA), dan antibodi terhadap glutamic acid decarboxylase (antiGAD). [2,22,23] 21 ICA bereaksi dengan antigen yang ada di sitoplasma sel-sel endokrin pada pulau-pulau pankreas. ICA ini menunjukkan adanya kerusakan sel. Adanya ICA dan IAA menunjukkan risiko tinggi berkembangnya penyakit ke arah diabetes tipe 1. GAD adalah enzim yang dibutuhkan untuk memproduksi neurotransmiter gaminobutyric acid (GABA). Anti GAD ini bisa teridentifikasi 10 tahun sebelum onset klinis terjadi. Jadi, 3 petanda ini bisa digunakan sebagai uji saring sebelum gejala DM muncul. Untuk membedakan tipe 1 dengan tipe 2 digunakan pemeriksaan C-peptide. Konsentrasi C-peptide merupakan indikator yang baik untuk fungsi sel beta, juga bisa digunakan untuk memonitor respons individual setelah operasi pankreas. Konsentrasi C-peptida akan meningkat pada transplantasi pankreas atau transplantasi sel-sel pulau pankreas. [22,23] Sampling untuk Pemeriksaan Kadar Gula Darah Untuk glukosa darah puasa, pasien harus berpuasa 6-12 jam sebelum diambil darahnya. Setelah diambil darahnya, penderita diminta makan makanan seperti yang biasa di makan atau minum glukosa per oral (75 gr) untuk TTGO, dan harus dihabiskan dalam waktu 15-20 menit. Dua jam kemudian diambil darahnya untuk pemeriksaan glukosa 2 jam PP.[17] Pemeriksaan untuk Pemantauan Pengelolaan Diabetes Mellitus Yang digunakan adalah kadar glukosa darah puasa, 2 jam PP, dan pemeriksaan glycated hemoglobin, khususnya HbA1C, serta pemeriksaan fruktosamin. Pemeriksaan fruktosamin saat ini jarang dilakukan karena pemeriksaan ini memerlukan prosedur yang memakan waktu lama. Pemeriksaan lain yang bisa dilakukan ialah urinalisa rutin. Pemeriksaan ini bisa dilakukan sebagai self-assessment untuk memantau terkontrolnya glukosa melalui reduksi urin. [22,24] Pemeriksaan HbA1C HbA1C adalah komponen Hb yang terbentuk dari reaksi non-enzimatik antara glukosa dengan N terminal valin rantai b Hb A dengan ikatan Almidin. 22 Produk yang dihasilkan ini diubah melalui proses Amadori menjadi ketoamin yang stabil dan ireversibel. [2,17] HbA1C akan meningkat secara signifikan bila glukosa darah meningkat. Karena itu, HbA1C bisa digunakan untuk melihat kualitas kontrol glukosa darah pada penderita DM (glukosa darah tak terkontrol, terjadi peningkatan HbA1C-nya) sejak 3 bulan lalu (umur eritrosit). HbA1C meningkat: pemberian tatalaksana lebih intensif untuk menghindari komplikasi. Nilai yang dianjurkan PERKENI untuk HbA1C (terkontrol): 4%-5,9%. Jadi, HbA1C penting untuk melihat apakah penatalaksanaan sudah adekuat atau belum. Sebaiknya, penentuan HbA1C ini dilakukan secara rutin tiap 3 bulan sekali.[2,17] 2.3.9 Tatalaksana Diabetes mellitus tipe 1 memerlukan pengobatan seumur hidup. Kepatuhan dan keteraturan pengobatan merupakan kunci keberhasilan. Penyuluhan pada pasien dan keluarga harus terus menerus dilakukan. Penatalaksanaan dibagi menjadi:[2,18,19] Pemberian insulin Pengaturan makan Olahraga/Latihan fisik Edukasi Home monitoring (pemantauan mandiri) Pemberian Insulin[19] - Tujuan: menjamin kadar insulin yang cukup di dalam tubuh selama 24 jam untuk memenuhi kebutuhan metabolisne sebagai insulin basal maupun insulin koreksi dengan kadar yang lebih tinggi (bolus) akibat efek glikemik makanan. - Regimen insulin sangat bersifat individual regimen apapun yang digunakan bertujuan untuk mengikuti pola fisiologi sekresi insulin orang normal sehingga mampu menormalkan metabolisme gula atau paling tidak mendekati orang normal. 23 - Pemilihan regimen insulin harus memperhatikan: umur, lama menderita DM, gaya hidup penderita (pola makan, jadwal latihan, sekolah, dsb), target kontrol metabolik, dan kebiasaan individu maupun keluarganya. - Regimen apapun yang digunakan, insulin tidak boleh dihentikan pada keadaan sakit. Dosis insulin disesuaikan dengan sakit penderita dan sebaiknya dikonsulkan ke dokter. - Harus diperhatikan: jenis, dosis, kapan pemberian, cara penyuntikan serta penyimpanan. - Jenis insulin berdasar lama kerjanya yang bisa digunakan: ultrapendek, pendek, menengah, panjang, dan mix (campuran menengah-pendek). - Bagi anak-anak sangat dianjurkan paling tidak menggunakan 2 kali injeksi insulin per hari (campuran insulin kerja cepat/pendek dengan insulin basal). - Dosis insulin harian, tergantung pada: Umur, berat badan, status pubertas, lama menderita, fase diabetes, asupan makanan, pola olahraga, aktifitas harian, hasil monitoring glukosa darah dan HbA1c, serta ada tidaknya komorbiditas. - Dosis insulin (empiris): Dosis selama fase remisi parsial, total dosis harian insulin <0,5 IU/kg/hari. Prepubertas (diluar fase remisi parsial) dalam kisaran dosis 0,7-1 IU/kg/hari. Selama pubertas kebutuhan biasanya meningkat menjadi 1,2-2 IU/kg/hari. - Dosis insulin ini berkurang sedikit pada waktu remisi dan kemudian meningkat pada saat pubertas. Pada follow up selanjutnya dosis dapat disesuaikan dengan hasil monitoring glukosa darah harian. - Saat awal pengobatan insulin diberikan 3-4 kali injeksi (kerja pendek). Setelah diperoleh dosis optimal diusahakan untuk memberikan regimen insulin yang sesuai dengan kondisi penderita. - Penyuntikan setiap hari secara subkutan di paha, lengan atas, sekitar umbilicus secara bergantian. 24 - Insulin relatif stabil pada suhu ruangan asal tidak terpapar panas yang berlebihan. Insulin sebaiknya disimpan di dalam lemari es pada suhu 4-8°C bukan dalam freezer. Potensi insulin baik dalam vial atau penfill yang telah dibuka, masih bertahan 3 bulan bila disimpan di lemari es; setelah melewati masa tersebut insulin harus dibuang. Insulin Insulin merupakan elemen utama kelangsungan hidup penderita DM tipe-1. Saat ini telah dikembangkan beberapa jenis insulin yang memungkinkan pemberian insulin dalam berbagai macam regimen. [2,18,19] Kerja Insulin Awitan, puncak kerja, dan lama kerja insulin merupakan faktor yang menentukan dalam pengelolaan penderita DM. Respons klinis terhadap insulin tergantung pada beberapa faktor: [2,18,19] Umur individu Tebal jaringan lemak Status pubertas Dosis insulin Tempat injeksi Latihan (exercise) Kepekatan, jenis, dan campuran insulin Suhu ruangan dan suhu tubuh Jenis Insulin Insulin kerja panjang kurang sesuai untuk anak, kecuali pada regimen basal bolus. Jenis insulin yang digunakan harus disesuaikan dengan usia anak (proses tumbuh kembang anak), aspek sosioekonomi (pendidikan dan kemampuan finansial), sosiokultural (sikap muslim terhadap insulin babi), dan faktor distribusi obat. 25 Dua hal yang penting dikenali pada pemberian insulin adalah efek Somogyi dan efek Subuh (Dawn effect). Kedua efek tersebut mengakibatkan hiperglikemia pada pagi hari, namun memerlukan penanganan yang berbeda. Efek Somogyi terjadi sebagai kompensasi terhadap hipoglikemia yang terjadi sebelumnya (rebound effect). Akibat pemberian insulin yang berlebihan terjadi hipoglikemia pada malam hari (jam 02.00-03.00) yang diikuti peningkatan sekresi hormon kontra-insulin (hormon glikogenik). Sebaliknya efek subuh terjadi akibat kerja hormon-hormon kontra insulin pada malam hari. Efek Somogyi memerlukan penambahan makanan kecil sebelum tidur atau pengurangan dosis insulin malam hari, sedangkan efek Subuh memerlukan penambahan dosis insulin malam hari untuk menghindari hiperglikemia pagi hari. [2,18,19] Tabel 2.1.3. Jenis Sediaan Insulin dan Profil Kerjanya Jenis Insulin Kerja cepat (Aspart, Awitan Puncak Lama (jam) Kerja (jam) Kerja (jam) 0,15 - 0,35 1-3 3-5 Waktu Pemberian Bersamaan dengan makan Glulisin, Lispro) Kerja pendek 0,5 - 1 2-4 5-8 30 menit (Reguler/soluble) makan Kerja menengah 30 Semilente 1-2 4 - 10 8-6 NPH 2-4 4 - 12 12 - 24 Tipe lente IZS 3-4 6 - 15 18 - 24 Kerja panjang 4-8 12 - 24 20 - 30 Tipe ultra lente menit sebelum sebelum makan 30 menit makan 26 sebelum Basal analog Diberikan 1-2 kali per Glargine 2-4 Tidak ada 24* Detemir 1-2 6 - 12 20 - 24 Campuran hari 30 Cepat-menengah 0,5 1 - 12 16 - 24 Pendek-menengah 0,5 1 - 12 16 - 24 menit makan Gambar 2.3.1. Profil farmakokinetik insulin manusia dan insulin analog. Terlihat lama kerja relatif berbagai jenis insulin. Lama kerjanya bervariasi antar dan intra perorangan Insulin Kerja Cepat (Rapid Acting) [2,18,19] Insulin monomer ini berupa larutan yang jernih, mempunyai awitan kerja yang cepat (5-15 menit), puncak kerja 30-90 menit, dan lama kerja berkisar 3-5 jam. Potensi dan efek hipoglikemi sama dengan insulin regular. 27 sebelum Gambar 2.3.2. Profil farmakokinetik insulin kerja cepat (rapid acting). Terlihat lama kerja relatif 3-5 jam, dengan awitan kerja yang cepat 5-15 menit, dan puncak kerja 30-90 menit. Insulin kerja cepat direkomendasikan untuk digunakan pada jam makan, atau penatalaksanaan insulin saat sakit. Dapat diberikan dalam regimen 2 kali sehari, atau regimen basal-bolus. Pada beberapa keadaan berikut, insulin kerja cepat sangat efektif digunakan: Pada saat snack sore Setelah makan Pada penggunaan CSII (continuous subcutaneous insulin influsion) atau pompa insulin Hiperglikemia dan ketosis saat sakit Insulin Kerja Pendek (Short Acting) [2,18,19] Insulin jenis ini dikenal sebagai insulin “reguler”. Biasanya digunakan untuk mengatasi keadaan akut seperti ketoasidosis, penderita baru, dan tindakan bedah. Kadang-kadang juga digunakan sebagai pengobatan bolus (15-20 menit) sebelum makan, atau kombinasi dengan insulin kerja menengah pada regimen 2 kali sehari.Penderita DM tipe 1 yang berusia balita sebaiknya menggunakan jenis ini untuk menghindari efek hipoglikemia akibat pola hidup dan pola makan yang seringkali tidak teratur. Fleksibilitas penatalaksanaan pada usia balita menuntut pemakaian insulin kerja pendek atau digabung dengan insulin kerja menengah. 28 Gambar 2.3.3. Profil farmakokinetik insulin kerja pendek (short acting). Terlihat lama kerja relatif 5-8 jam, dengan awitan kerja 30-60 menit, dan puncak kerja 2-4 jam. Insulin Kerja Menengah (Intermediate Acting) [2,18,19] Insulin jenis ini lebih sesuai bila digunakan dalam regimen 2 kali sehari dan sebelum tidur pada regimen basal-bolus. Insulin ini lebih sering digunakan untuk penderita yang telah memiliki pola hidup yang lebih teratur. DM tipe-1 usia bayi (0-2 tahun) mempunyai pola hidup (makan, minum, dan tidur) yang masih teratur sehingga lebih mudah mencapai kontrol metabolik yang baik. Apabila orang tua segan menggunakan regimen insulin dengan insulin kerja menengah secara multipel (2 kali sehari), penggunaan 1 kali sehari masih dimungkinkan pada golongan usia ini dengan terlebih dahulu memperhatikan efek insulin terhadap kontrol metaboliknya. Dua sediaan insulin kerja menengah yang saat ini tersedia adalah: Isophane atau insulin NPH (Neutral Protamine Hagedorn) Insulin Crystalline zinc-acetate (insulin lente) Insulin Isophane paling sering digunakan pada anak, terutama karena memungkinkan untuk digabung dengan insulin reguler dalam satu syringe tanpa adanya interaksi. 29 Gambar 2.3.4. Profil farmakokinetik insulin kerja menengah (intermediate acting). Terlihat lama kerja relatif 12-24 jam, dengan awitan kerja 2-4 jam, dan puncak kerja 4-12 jam. Insulin Kerja Panjang (Long Acting) [2,18,19] Insulin kerja panjang tradisional (UltralenteTM) mempunyai masa kerja lebih dari 24 jam, sehingga dapat digunakan dalam regimen basal-bolus. Penggunaan analog insulin basal mempunyai keunggulan dibandingkan ultralente. Gambar 2.3.5. Profil farmakokinetik insulin kerja panjang (long acting). Terlihat lama kerja relatif 20-30 jam, dengan awitan kerja 4-8 jam, dan puncak kerja 12-24 jam. 30 Insulin Kerja Campuran[2,18,19] Insulin campuran mempunyai pola kerja bifasik; terdiri dari kombinasi insulin kerja cepat dan menengah, atau kerja pendek dan menengah. Sediaan yang ada adalah kombinasi 30/70 artinya terdiri dari 30% insulin kerja cepat atau pendek, dan 70% insulin kerja menengah. Pemakaian sediaan ini dianjurkan bagi penderita yang telah mempunyai kontrol metabolik yang baik. Penggunaan sediaan ini banyak bermanfaat pada kasus-kasus sebagai berikut: Penderita muda dengan pendidikan orang tua yang rendah. Penderita dengan masalah psikososial individu maupun pada keluarganya. Para remaja yang tidak senang dengan perhitungan dosis insulin campuran yang rumit. Penderita yang menggunakan insulin dengan rasio yang stabil. Gambar 2.3.6. Profil farmakokinetik insulin kerja campuran Insulin Basal Analog[2,18,19] Insulin basal analog merupakan insulin jenis baru yang mempunyai kerja panjang sampai dengan 24 jam. Di Indonesia saat ini sudah tersedia insulin glargine dan determir; keduanya mempunyai profil kerja yang lebih terduga dengan variasi harian yang lebih stabil dibandingkan insulin NPH. Insulin ini tidak 31 direkomendasikan untuk anak-anak di bawah usia 6 tahun. Insulin glargine serta determir tidak dapat dicampur dengan insulin jenis lainnya. Mengingat sifat kerjanya yang tidak mempunyai kadar puncak (peakless) dengan lama kerja hingga 24 jam, maka glargine dan detemir direkomendasikan sebagai insulin basal. Bila dibandingkan dengan NPH, glargine dan detemir dapat menurunkan kadar glukosa darah puasa dengan lebih baik pada kelompok usia 516 tahun, namun secara keseluruhan tidak memperbaiki kadar HbA1c secara bermakna. Insulin glargine dan detemir juga mengurangi risiko terjadinya hipoglikemia nocturnal berat. Gambar 2.3.7. Profil farmakokinetik insulin basal (tidak mempunyai kadar puncak dengan lama kerja 24 jam) Regimen Insulin[2,18,19] 1. Split-Mix Regimen Injeksi 1 kali sehari Sering sekali tidak sesuai digunakan pada penderita DM tipe-1 anak maupun remaja. Namun dapat diberikan untuk sementara pada saat fase remisi. Regimen insulin yang dapat digunakan adalah insulin kerja 32 menengah atau kombinasi kerja cepat/pendek dengan insulin kerja menengah Injeksi 2 kali sehari Digunakan campuran insulin kerja cepat/pendek dan kerja menengah yang diberikan sebelum makan pagi dan sebelum makan malam. Regimen ini biasa digunakan pada anak-anak yang lebih muda. Injeksi 3 kali sehari Insulin campuran kerja cepat/pendek dengan kerja menengah diberikan sebelum makan pagi, insulin kerja cepat/pendek diberikan sebelum makan siang atau snack sore, dan insulin kerja menengah pada menjelang tidur malam hari. Regimen ini biasa digunakan pada anak yang lebih tua dan remaja yang kebutuhan insulinnya tidak terpenuhi dengan regimen 2 kali sehari. 2. Basal-Bolus Regimen Menggunakan insulin kerja cepat/pendek diberikan sebelum makan utama, dengan insulin kerja menengah diberikan pada pagi dan malam hari atau dengan insulin basal (glargine, detemir) yang diberikan sekali sehari (pagi atau malam hari). Regimen ini biasa digunakan pada anak remaja ataupun dewasa. Komponen basal biasanya berkisar 40-60% dari kebutuhan total insulin, yang dapat diberikan menjelang tidur malam atau sebelum makan pagi atau siang, atau diberikan dua kali yakni sebelum makan pagi dan makan malam; sisanya sebagai komponen bolus terbagi yang disuntikkan 20-30 menit sebelum makan bila menggunakan insulin reguler, atau segera sebelum makan atau sesudah makan bila menggunakan analog insulin kerja cepat. 3. Pompa Insulin Hanya boleh menggunakan analog insulin kerja cepat yang deprogram sebagai insulin basal sesuai kebutuhan penderita (biasanya 40- 33 60% dari dosis total insulin harian). Untuk koreksi hiperglikemia saat makan, diberikan dosis insulin bolus yang diaktifkan oleh penderita. 4. Penyesuaian dosis insulin[2,18,19] Penyesuaian dosis insulin bertujuan untuk mencapai kontrol metabolik yang optimal, tanpa meningkatkan risiko terjadinya hipoglikemia dan tanpa mengabaikan kualitas hidup penderita baik jangka pendek maupun jangka panjang. Pengaturan dosis insulin yang kaku atau terlalu fleksibel bukan merupakan jawaban untuk mencapai kontrol metabolik yang baik. Penyesuaian dosis biasanya dibutuhkan pada honeymoon period, masa remaja, masa sakit, dan sedang menjalankan pembedahan. Pada fase honeymoon period, dosis insulin yang dibutuhkan sangat rendah, bahkan pada beberapa kasus kontrol metabolik dapat dicapai tanpa pemberian insulin sama sekali. Dosis insulin pada fase ini perlu disesuaikan untuk menghindari serangan hipoglikemia. Pada kasus remaja, kebutuhan insulin meningkat karena bekerjanya hormone seks steroid, meningkatkan amplitudo dan frekuensi sekresi growth hormon, yang kesemuanya merupakan hormon kontra insulin. Pada saat sakit, dosis insulin perlu disesuaikan dengan asupan makanan tetapi jangan menghentikan pemberian insulin. Penghentian insulin akan meningkatkan lipolisis dan glikogenolisis sehingga kadar glukosa darah meningkat dan penderita rentan untuk menderita ketoasidosis. Pada saat terjadi perubahan pola makan untuk jangka tertentu misalnya pada bulan puasa, dosis insulin juga harus disesuaikan hingga 2/3 atau 3/4 dari insulin total harian, serta distribusinya harus disesuaikan dengan porsi dosis sebelum buka puasa lebih besar dari dosis sebelum makan sahur. (14) 34 Pengaturan Makan[2,18,19] - Tujuan: mencapai kontrol metabolik yang baik, tanpa mengabaikan kalori yang dibutuhkan untuk metabolisme basal, pertumbuhan, pubertas, ataupun untuk aktivitas yang dilakukan. - Jumlah kalori yang dibutuhkan: [1000 + (usia (tahun) x 100)] kalori per hari. Komposisi kalori yang dianjurkan adalah 60-65% berasal dari karbohidrat, 25% berasal dari protein dan sumber energi dari lemak <30%. - Jadwal: 3 kali makan utama dan 3 kali makanan kecil. Tidak ada pengaturan makan khusus yang dianjurkan pada anak, tetapi pemberian makanan yang mengandung banyak serat seperti buah, sayuran, dan sereal akan membantu mencegah lonjakan kadar glukosa darah. - Pemilihan jenis makanan dianjurkan karbohidrat dengan indeks glikemik dan glicemic load yang rendah. Olahraga [2,10,18,19] - Olahraga tidak memperbaiki kontrol metabolik, akan tetapi membantu meningkatkan jatidiri anak, mempertahankan berat badan ideal, meningkatkan kapasitas kerja jantung, mengurangi terjadinya komplikasi jangka panjang, membantu kerja metabolisme tubuh sehingga dapat mengurangi kebutuhan insulin. - Yang perlu diperhatikan dalam berolahraga adalah: Diskusikan jumlah pengurangan dosis insulin sebelum olahraga dengan dokter. Jika olahraga akan dilakukan pada saat puncak kerja insulin maka dosis insulin harus diturunkan secara bermakna. Pompa insulin harus dilepas atau insulin basal terakhir paling tidak diberikan 90 menit sebelum mulai latihan. Jangan suntik insulin pada bagian tubuh yang banyak digunakan untuk latihan. 35 Pemantauan terhadap kemungkinan terjadinya hipoglikemia atau hiperglikemia saat atau pasca olahraga, sehingga mungkin memerlukan penyesuaian dosis insulin. - Jenis olahraga disesuaikan dengan minat anak. Pada umumnya terdiri dari pemanasan selama 10 menit, dilanjutkan 20 menit untuk latihan aerobik seperti berjalan atau bersepeda. Olahraga harus dilakukan paling sedikit 3 kali seminggu dan sebaiknya dilakukan pada waktu yang sama untuk memudahkan pemberian insulin dan pengaturan makan. Lama dan intensitas olahraga disesuaikan dengan toleransi anak. - Asupan cairan perlu ditingkatkan sebelum, setelah, dan saat olahraga. - Jika glukosa darah tinggi, glukosa darah > 250 mg/dL (14 mmol/L) dengan ketonuria/ketonemia (> 0,5 mmol/L) Olahraga atau latihan fisik harus dihindari. Berikan insulin kerja cepat (rapid acting) sekitar 0,05 U/kg atau 5% dari dosis total harian. - Tunda aktivitas fisik sampai keton sudah negatif. Konsumsi 1,0-1,5 gram karbohidrat per kg massa tubuh per jam untuk olahraga yang lebih lama atau lebih berat jika kadar insulin yang bersirkulasi tinggi atau insulin sebelum latihan tidak dikurangi. - Makanan yang mengandung tinggi karbohidrat harus dikonsumsi segera setelah latihan untuk mencegah tejadinya hioglikemia pasca latihan fisik. - Risiko terjadinya hipoglikemia nocturnal pasca olahraga cukup tinggi terutama jika kadar glukosa darah sebelum tidur < 125 mg/dL (<7.0 mmol/L). Dosis insulin basal sebelum tidur sebaiknya dikurangi. - Pasien dengan retinopati proliferative atau nefropati harus menghindari olahraga yang bersifat anaerobic atau yang membutuhkan ketahanan fisik karena dapat menyebabkan tekanan darah tinggi. Edukasi[2,18,19] - Penyuluhan dan tatalaksana merupakan bagian integral terapi. Diabetes mellitus tipe 1 merupakan suatu life long disease. Keberhasilan untuk 36 mencapai normoglikemia sangat bergantung dari cara dan gaya hidup penderita/keluarga atau dinamika keluarga sehingga pengendalian utama metabolik yang ideal tergantung pada penderita sendiri. Kegiatan edukasi harus terus dilakukan oleh semua pihak, meliputi pemahaman dan pengertian mengenai penyakit dan komplikasinya serta memotivasi penderita dan keluarganya agar patuh berobat. - Edukasi pertama dilakukan selama perawatan di rumah sakit yang meliputi: pengetahuan dasar mengenai DM tipe 1 (terutama perbedaan mendasar dengan DM tipe lainnya mengenai kebutuhan insulin), pengaturan makan, insulin (jenis, dosis, cara penyuntikan, penyimpanan, efek samping, dan pertolongan pertama pada kedaruratan medik akibat DM tipe 1 (hipoglikemia, pemberian insulin pada saat sakit)). - Edukasi selanjutnya berlangsung selama konsultasi di poliklinik. Selain itu penderita dan keluarganya diperkenalkan dengan sumber informasi yang banyak terdapat di perpustakaan, media massa maupun internet. Home monitoring (Pemantauan Mandiri) [2,18,19] - Oleh karena DM tipe 1 merupakan penyakit kronik dan memerlukan pengobatan seumur hidup, maka pasien serta keluarganya harus dapat melakukan pemantauan kadar glukosa darah serta penyakitnya di rumah. Hal ini diperlukan karena sangat menunjang upaya pencapaian normoglikemia. Pemantauan dapat dilakukan secara langsung (darah) dan secara tidak langsung (urin). - Pemeriksaan glukosa darah secara langsung lebih tepat menggambarkan kadar glukosa pada saat pemeriksaan. Pemeriksaan sebaiknya dilakukan secara teratur pada saat awal perjalanan penyakit, pada setiap penggantian dosis insulin, atau pada saat sakit. - Frekuensi pemantauan glukosa darah mendiri berbeda-beda untuk masingmasing individu tergantung dari ketersediaan alat dan kemampuan anak untuk mengidentifikasi hipoglikemia. Untuk mengoptimalkan kontrol 37 glikemik maka pemantauan glukosa darah mandiri harus dilakukan 4-6 kali sehari. (13) Pagi hari setelah bangun tidur untuk melihat kadar glukosa darah setelah puasa malam hari. Setiap sebelum makan. Pada malam hari untuk mendeteksi hipoglikemia atau hiperglikemia. 1,5-2 jam setelah makan. 2.3.10 Komplikasi [2,18,19] Komplikasi DM tipe-1 dapat digolongkan sebagai komplikasi akut dan komplikasi kronik baik reversibel maupun ireversibel. Sebagian besar komplikasi akut bersifat reversibel sedangkan yang kronik bersifat ireversibel tetapi perjalanan penyakitnya dapat diperlambat melalui intervensi. Secara umum, komplikasi kronik disebabkan kelainan mikrovaskular (retinopati, neuropati dan nefropati) dan makrovaskular. Komplikasi Jangka Pendek Komplikasi jangka pendek yang sering tejadi adalah hipoglikemia dan ketoasidosis diabetikum. Hipoglikemia dapat mengakibatkan kerusakan otak yang menetap. Insidens hipoglikemia dapat dihindari dengan meningkatkan pemantauan gula darah. Akibat kerja insulin yang berlebihan, dapat terjadi hipoglikemia berat dengan gejala kejang, koma, bahkan kematian. Pada keadaan hipoglikemia ringan, tubuh akan memberikan gejala dan tanda sehingga penderita akan bertindak (misalnya minum air gula). Dengan melakukan tindakan sederhana tersebut penderita akan terhindar dari efek hipoglikemia berat. Walaupun demikian gejala dan tanda hipoglikemia harus dicatat dan selalu ditanyakan kepada penderita. Keterangan tersebut kemudian dicocokan dengan data hasil pemantauan mandiri glukosa darah. Apabila didapatkan hasil glukosa darah yang rendah tetapi penderita tidak merasa apa-apa maka perlu diwaspadai adanya hypoglycemic 38 unawareness. Fenomena ini terjadi akibat menurunnya ambang hipoglikemia seorang penderita DM tipe-1 sehingga penderita tidak akan merasakan gejala awal hipoglikemia, yang akan membahayakan penderita. (14) 1) Gejala Hipoglikemia Gejala klinis hipoglikemia bervariasi dan dibagi menjadi gejala neurogenik dan gejala neuroglikopenia seperti dibawah ini: Tabel 2.3.2. Gejala-gejala hipoglikemia Gejala Neurogenik Gejala Neuroglikopenia Berkeringat, lapar, parestesia di sekitar Pusing, iritabel, lemah, mengantuk, sakit mulut, tremor, takikardi, pucat, palpitasi, kepala, lemas, gelisah, mual. lamban dan pelo, vertigo dan dizziness, gangguan penglihatan, bicara kesulitan berpikir, lelah, perubahan afektif (depresi, marah), bicara ngaco, kejang, penurunan kesadaran, koma. Orangtua dan pengasuh biasanya akan melihat gejala-gejala awal hipoglikemia pada anak berupa perubahan tingkah laku seperti iritabilitas, pucat, dan berkeringat. Umumnya sebelum berlanjut menjadi hipoglikemia berat, tubuh akan memberikan respon yang cepat apabila diberikan dekstrosa oral atau intervena atau injeksi glukagon. Tabel 2.3.3 Gejala hipoglikemia berdasarkan berat ringannya gejala klinis Tingkat Gambaran Klinis Terapi Ringan Lapar, tremor, mudah goyah, Sari buah, limun manis, anggur pucat, ansietas, berkeringat, manis, palpitasi, takikardi, penurunan hipoglikemia sangat ringan dapat konsentrasi, dan kemampuan diatasi dengan memajukan jadwal kognitif. makan, apabila episode terjadi makanan ringan. 39 Jika dalam 15-30 menit dari jadwal yang ditentukan. Sedang Sakit kepala, perubahan sakit perut, 10-20 gram gula yang dapat dicerna tingkah laku, segera, diikuti dengan pemberian agresif, gangguan visus, bingung, ngantuk, lemah, kesulitan bicara, pucat, berkeringat, snack. takikardi, dilatasi pupil. Berat Disorientasi berat, penurunan Bila jauh dari pertolongan medis: kesadaran, koma, kejang. bila tersedia glukagon, berikan injeksi glukagon (SC, IM atau IV) untuk usia <5 tahun berikan 0,5 mg dan usia >5 tahun 1,0 mg. Bila tak ada respon dalam 10 menit ulangi sekali lagi. Kemudian diikuti dengan makan dan monitoring berkala. Bila tidak ada glukagon, oleskan selai atau madu kebagian dalam mulut sambil segera membawa pasien ke rumah sakit. Di rumah sakit: berikan dekstrose 10% intravena dengan dosis 2 mL/kgBB diikuti infus dekstrose untuk menstabilkan kadar glukosa darah antara 90-180 mg/dL (5-10 mmol/L) 40 2) Derajat Hipoglikemia The Diabetes Control and Complications Trial (DCCT) mendefinisikan hipoglikemia berat sebagai hipoglikemia yang memerlukan bantuan orang lain untuk mengatasinya, misalnya penderita dengan penurunan kesadaran. Hipoglikemia dapat simptomatik atau asimptomatik. Hipoglikemia simptomatik dibagi dalam 3 tingkat berdasarkan kriteria dibawah ini: Derajat I Bila anak dapat mendeteksi dan mengobati sendiri hipoglikemianya. Hipoglikemia pada anak dibawah 5 tahun tidak dapat diklasifikasikan sebagai derajat I karena mereka belum dapat mengobati sendiri. Derajat II Bila membutuhkan pertolongan orang lain untuk dapat mengatasi hipoglikemia ini, tetapi pengobatan masih dapat dilakukan secara oral. Derajat III Bila anak pingsan, tak sadar, kejang dan tak dapat diatasi dengan glukosa secara oral. Terapi dilakukan dengan injeksi glukagon atau glukosa intravena. Berdasarkan kadar gula darah derajat hipoglikemia dibagi atas: - Hipoglikemia ringan: GDS kapiler 55-70 mg/dL - Hipoglikemia sedang: GDS kapiler <55 mg/dL tanpa penurunan kesadaran - Hipoglikemia berat: GDS kapiler <70 mg/dL disertai penurunan kesadaran atau kejang Pencegahan Hipoglikemia[2] Hal-hal yang sering menyebabkan hipoglikemia diantaranya asupan makanan yang tidak teratur, olahraga yang berlebihan tanpa ditunjang oleh makanan yang cukup serta pengobatan insulin yang berlebihan. Hipoglikemia dapat dicegah dengan keteraturan pengobatan insulin, pengaturan makan/asupan makanan yang disesuaikan dengan aktivitas atau kegiatan yang dilakukan. 41 Pada DM tipe-1 seringkali terjadi hipoglikemia pada malam hari yang disebabkan oleh faktor-faktor seperti umur yang lebih muda, dosis insulin yang berlebihan, dan regimen insulin yang dipakai. Untuk mencegah hipoglikemia pada malam hari maka kadar gula tengah malam diusahakan sekitar 120-180 mg/dL (710 mmol/L). Makanan yang sebaiknya dikonsumsi pada malam hari adalah karbohidrat yang lambat dicerna seperti susu, roti, pisang, apel dan protein. Semua anak dan remaja penderita diabetes harus membawa permen atau tablet glukosa yang siap dimakan sewaktu-waktu bila terjadi hipoglikemia. Pencegahan hipoglikemia bisa dimulai dari memilih regimen insulin usahakan memilih yang se-fisiologis mungkin sesuai dengan pola kehidupan penderita melalui penyesuaian dosis insulin berdasarkan pola makan, profil glukosa darah (bukan berdasarkan kadar glukosa darah sesaat) dan jenis kegiatan (olahraga). Usahakan kadar gula darah mendekati normal dengan fluktuasi seminimal mungkin untuk memberikan kesempatan supaya hormon kontrainsulin dapat bekerja dengan baik. Berikan edukasi tentang teknik penyuntikan insulin, absorbsi insulin dan tentang masa kerja insulin. Hal ini menentukan interval waktu antara penyuntikan dan makan. Edukasikan pula pada pasien dan orang disekitarnya untuk waspada terhadap gejala dan tanda hipoglikemia. Berikan dukungan psikologis untuk meningkatkan rasa percaya diri pasien. Komplikasi Jangka Panjang[2] Komplikasi jangka panjang diabetes mellitus terjadi akibat perubahan mikrovaskular (retinopati, nefropati, dan neuropati) dan makrovaskular. Pada anak komplikasi akibat perubahan makrovaskular sangat jarang dijumpai sedangkan komplikasi akibat perubahan mikrovaskular dapat ditemukan, berikut merupakan komplikasi jangka panjang DM Tipe 1 : 1. Retinopati Retinopati yang ditemukan pada anak dengan DM tipe1 tidak berbeda dengan orang dewasa yaitu berupa obstruksi pembuluh darah, kelainan progresif mikrovaskular di dalam retina, dan infark serabut saraf 42 retina yang mengakibatkan bercak pada retina. Gambaran khas retinopati proliferative adalah neovaskularisasi. Pembuluh darah ini bisa pecah mengakibatkan perdarahan ke ruang vitreus dan menyebabkan kebutaan. Beberapa teknik yang digunakan untuk mendeteksi adanya diabetes retinopati, adalah oftalmoskopi, angiografi fluoresensi, stereoscopic digital and color film-based fundal photography. Kontrol glikemik yang optimal merupakan upaya pencegahan dini terjadinya retinopati. Perbaikan HbA1c 1% dapat menurunkan risiko komplikasi jangka panjang sebesar 20-50%. Deteksi dini retinopati dapat dilakukan dengan melakukan kontrol teratur ke dokter mata. Sebelum usia 15 tahun kontrol dilakukan setiap 2 tahun sedangkan pada usia lebih dari 15 tahun dilakukan setiap tahun. Pasien yang terdiganosis DM pada usia prapubertas, pemeriksaan mata dilakukan 5 tahun setelah diagnosis. DCCT merekomendasikan untuk melakukan pemeriksaan mata tiap 3 bulan untuk pasien dengan kontrol metabolik buruk yang kronis. 2. Nefropati Tanda awal terjadinya nefropati pada DM tipe-1 adalah ditemukannya mikroalbuminuria. Mikroalbuminuria persisten merupakan terjadinya nefropati diabetik dan meningkatnya risiko mortalitas kardiovaskuler. Nefropati diabetik sering berhubungan dengan adanya hipertensi. Diperkirakan 30-40% nefropati pada DM tipe- 1 dapat berlanjut menjadi gagal ginjal kronik. Mikroalbuminuria lebih banyak terdeteksi pada anak yang lebih tua. Sepertiga pasien DM akan menderita mikroalbuminuria persisten dalam kurun waktu 10-30 tahun awitan diagnosis. Peningkatan tekanan darah ringan yang dideteksi pada ambulatory monitoring selama 24 jam dapat digunakan sebagai parameter tanda awal terjadinya mikroalbuminuria. Pada anak yang lebih tua, albuminuria yang borderline (ekskresi albumin 7,2-20 mg/menit) merupakan faktor prediktor bahwa dalam 15-50 bulan kemudian akan berkembang menjadi mikroalbuminuria persisten. Mikroalbuminuria 43 dengan hipertensi mempunyai prognosis lebih buruk dibandingkan tanpa hipertensi. Deteksi dini nefropati diabetik dengan melakukan pemeriksaan mikroalbuminuria setiap tahun sejak memasuki usia remaja (walaupun tidak ada gejala) disertai pemeriksaan tekanan darah teratur pada setiap kunjungan. Sangatlah penting kontrol glikemik yang dicapai dengan terapi insulin disertai penggunaan ACE inhibitor dapat mencegah atau memperlambat progresivitas mikroalbuminuria menjadi nefropati diabetik. Pengelolaan Ketoasidosis Diabetik[2,3] Ketoasidosis diabetik (KAD) merupakan komplikasi akut DM tipe-1 yang disebabkan oleh kekurangan insulin. Sering ditemukan pada: 1. Penderita DM tipe-1 tidak patuh jadwal dengan suntikan insulin 2. Pemberian insulin dihentikan karena anak tidak makan/sakit 3. Kasus baru DM tipe-1 Kekurangan insulin menyebabkan glukosa dalam darah tidak dapat digunakan oleh sel untuk metabolisme karena glukosa tidak dapat memasuki sel, akibatnya kadar glukosa dalam darah meningkat (hiperglikemia). Pada anak sakit walaupun tidak makan, didalam tubuh tetap terjadi mekanisme glukoneogenesis sehingga tetap terjadi hiperglikemia. Benda keton yang terbentuk karena pemecehan lemak disebabkan oleh ketiadaan insulin. Akumulasi benda keton ini menyebabkan terjadinya asidemia, dan asidemia ini dapat menimbulkan ileus, menurunkan kemampuan kompensasi terhadap poliuria, dan menimbulkan diuresis osmotik menyebabkan terjadinya dehidrasi berat. Makin meningkatnya osmolaritas karena hiperglikemia dan asidosis yang terjadi, menyebabkan penurunan fungsi otak sehingga dapat terjadi penurunan kesadaran. Oleh karena itu pada penderita KAD ditemukan berbagai tingkatan dehidrasi, hiperosmolaritas, dan asidosis. Bila tidak segera ditangani dengan tepat maka angka kematian karena KAD cukup tinggi. 44 Pada KAD, insulin yang diberikan adalah jenis kerja pendek (short actingHumulin R® atau Actrapid®), diberikan secara kontinu intravena dosis kecil 0,1 U/kgBB/jam dalam jalur infus tersendiri (sebaiknya menggunakan syringe pump atau infusion pump agar pemberiannya tepat). Bila pada penilaian pendahuluan terhadap pasien ditemukan tanda-tanda renjatan, segera lakukan penanganan renjatan sesuai standar (pemberian cairan 1020 ml/kgBB/dalam 1-2 jam). Setelah teratasi, jumlah cairan yang diberikan ditambahkan pada cairan rumatan yang diperhitungkan untuk pemberian selama 3648 jam ke depan, sesuai protokol KAD. Pemberian cairan yang tepat baik dalam tonisitas, jumlah, dan kecepatan pemberian juga mampu menurunkan kadar gula darah. Pemantauan harus dilakukan dengan cermat dan gangguan elektrolit harus di atasi dengan baik. Kadar Na yang terukur saat diagnosis KAD ditegakkan bukanlah kadar natrium yang sebenarnya karena keadaan hiperglikemia dan hyperlipidemia yang terjadi pada kondisi KAD akan menarik cairan dari dalam sel sehingga mengencerkan kadar natrium dalam darah. Oleh sebab itu diperlukan penghitungan natrium koreksi dengan rumus sebagai berikut: Na+ darah sesungguhnya : [Na] darah terlihat + 1,6 (kadar glukosa darah – 100) 100 Bila angka koreksi natrium masih dalam kisaran hypernatremia, mengindikasikan bahwa ruang intraseluler sangat hiperosmoler dan ini menunjukkan masih terjadi dehidrasi berat. Angka koreksi natrium juga dapat menunjukkan kecepatan rehidrasi. Penurunan yang drastis kadar natrium sesungguhnya, memperlihatkan cairan yang diberikan terlalu cepat dan perlu di perlambat. Asidosis yang ditemukan pada KAD seringkali sudah amat berat (pH < 7,1), Natrium bikarbonat sebaiknya hanya diberikan bila pH darah mencapai < 7,1 karena pada nilai pH yang serendah itu bisa terjadi gagal organ yang mengancam jiwa. Pemberian koreksi Natrium bikarbonat sebaiknya dilakukan per drip. 45 2.3.11 Prognosis Diabetes Mellitus tipe 1 adalah penyakit kronis yang serius, menurut beberapa literatur mengenai penyakit ini disebutkan bahwa umur dari penderita 10 tahun lebih pendek dibandingkan dengan orang yang bukan penderita. Pada anak yang menderita DM Tipe-1 kemungkinan akan mengalami penghambatan pertumbuhan sehingga akan menjadi lebih pendek dibandingkan dengan orang normal, selain itu perkembang seksual dari anak penderita diabetes mellitus tipe 1 juga akan terhambat sehingga pencapaian umur pubertas akan lebih tua dari anak yang normal. Prognosis akan menjadi buruk bila terjadi kesalahan diagnosis pada awal awitan penyakit atau keterlambatan deteksi. Diagnosis yang terlambat ditegakkan akan mengakibatkan meningkatnya kemungkinan komplikasi akut maupun kronis yang cukup berat sehingga dapat mengancam jiwa penderita. Perubahan pola hidup yang ekstrem seperti kebutuhan insulin absolut setiap hari juga merupakan sebuah masalah bagi orangtua penderita maupun penderita itu sendiri terutama bagi penderita dengan umur dibawah 10 tahun. Prognosis baik akan didapatkan apabila diagnosis dapat cepat ditegakkan, ketepatan pengobatan, pengelolaan status hiperglikemia dan pencegahan komplikasi jangka pendek maupun jangka panjang terlaksana dengan baik, Oleh karena itu, edukasi kepada orangtua, orang sekitar penderita dan penderita DM tipe 1 mengenai penyakit, penkgobatan dan komplikasinya sangatlah penting supaya orangtua maupun orang disekitar penderita dapat membantu mencegah komplikasi yang mengancam jiwa timbul dikemudian hari. 46