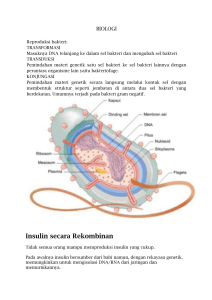
Meskipun lintasan ke arah suksinat merupakan jalur utama
advertisement

GLUKONEOGENESIS DAN PENGONTROLAN KADAR GULA DARAH OLEH DINA MULYANI NIM 07250013 PROGRAM STUDI BIOLOGI FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS PGRI ADIBUANA SURABAYA 0 DAFTAR ISI Kata Pengantar 1 Daftar Isi 2 BAB I BAB II PENDAHULUAN 1.1 Latar belakang 3 1.2 Rumusan Masalah 4 1.3 Tujuan 4 PEMBAHASAN 2.1 Glukoneogenesis melibatkan Glikolisis Siklus Asam Sitrat dan Beberapa Reaksi Khusus 2.2 5 Glikolisis dan Glukoneogenesis mempunyai Lintasan yang sama tetapi arahnya berbeda, maka kedua proses ini arus diatur secara timbal balik 2.3 Fruktosa 2,6-Bisfosfat Mempunyai Peranan yang Unik di dalam Regulasi Glikolisis dan Glukoneogenesis 2.4 11 Glukosa darah berasal dari Makanan Glukoneogenesis dan Glikogenesis BAB III 10 Konsentrasi Glukosa Darah Diatur dalam Batas-batas yang sempit 2.5 7 11 PENUTUP 3.1 Kesimpulan 18 3.2 Saran 20 3.3 Evaluasi 20 Kepustakaan 23 Lampiran Gambar 24 1 BAB I PENDAHULUAN 1.1 Latar Belakang Glukoneogenesis merupakan istilah yang digunakan untuk mencakup semua mekanisme dan lintasan yang bertanggung jawab untuk mengubah senyawa nonkarbohidrat menjadi glukosa atau glikogen. Subtrat utama bagi glukoneogenesis adalah asam amino glukogenik, laktat, gliserol dan propionat. Hati dan ginjal merupakan jaringan utama yang terlibat, Karena kedua organ tersebut mengandung komplemen enzim-enzim yang diperlukan. Glukoneogenesis memenuhi kebutuhan tubuh akan glukosa pada saat karbohidrat tidak tersedia dalam jumlah yang cukup di dalam makanan. Pasokan glukosa yang terus menerus diperlukan sebagai sumber energi, khususnya bagi sistem syaraf dan eritrosit. Kegagalan pada Glukoneogenesis biasanya berakibat fatal. Kadar glukosa darah di bawah nilai yang kritis akan menimbulkan disfungsi otak yang dapat mengakibatkan koma dan kematian. Glukosa juga dibutuhkan di dalam jaringan adiposa sebagai sumber gliserida-gliserol, dan mungkin mempunyai peran di dalam mempertahankan kadar intermediat pada siklus asam sitrat dibanyak jaringan tubuh. Bahkan dalam keadaan lemak memasok sebagian besar kebutuhan kalori bagi organisme tersebut, selalu terdapat kebutuhan basal tertentu aaakan glukosa. Glukosa merupakan satu-satunya bahan bakar yang yang memasok energi bagi otot rangka pada keadaan anaerob. Unsur ini merupakan prekursor gula susu (laktosa) di kelenjar payudara dan secara aktif diambil oleh janin. Selain itu, mekanisme glukoneogenik dipakai untuk membersihkan berbagai produk metabolisme jaringan lainnya dari darah, missal laktat yang dihasilkan oleh otot dan eritrosit, dan gliserol yang secara terus-menerus diproduksi oleh jaringan adipose. Propionat, yaitu asam lemak glukogenik utama yang dihasilkan dalam proses digesti karbohidrat oleh hewan pemamah biak, merupakan substrat penting untuk Glukoneogenesis di dalam tubuh spesies ini. 2 1.2 Tujuan Makalah ini bertujuan sebagai berikut : 1. Mengetahui ganguan ketiadaan enzim-enzim neoglikolisis (Glukoneogenesis) 2. Mengetahui ketiadaan enzim fruktosa bisfofatase dalam hati 3. Mengetahui penggunaan obat Penofarmin oleh penderita Diabestes militus 3 BAB II PEMBAHASAN 2.1 GLUKONEOGENESIS MELIBATKAN GLIKOLISIS SIKLUS ASAM SITRAT DAN BEBERAPA REAKSI KHUSUS Penghalang Termodinamik Mencegah Pembalikan Sederhana Glikolisis Krebs menegaskan bahwa penghalang energi merintangi pembalikan sederhana reaksi glikolisis antara piruvat dan fosfoenolpiruvat, antara fruktosa 1,6-bisfosfat dan fruktosa6-fosfat antara glukosa 6-fosfat dan glukosa, serta antara glukosa 1-fosfat dan glikogen. Semua reaksi ini bersifat non-ekuilibrum dengan melepas banyak energi bebas dalam bentuk panas dan karenanya secara fisiologis tidak reversibel. Reakrireaksi tersebut dielakkan oleh sejumlah reaksi khusus. A. Piruvat dan Fosfoenolpiruvat: Di dalam mitokondria terdapat enzim Piruvat karboksilase, yang dengan adanya ATP, Vitamin B biotin dan CO2 akan mengubah piruvat menjadi oksaloasetat. Biotin berfungsi untuk mengikat CO2 dari bikarbonat pada enzim sebelum penambahan CO2 pada piruvat (Gambar 52-13). Enzim kedua, fosfoenolpiruvat karboksinase, mengatalisis konversi oksaloasetat menjadi fosfoenolpiruvat. Fosfat energi tinggi dalam bentuk GTP atau ITP diperlukan dalam reaksi ini, dan CO2 dibebaskan. Jadi, dengan bantuan dua enzim yang mengatalisis transformasi endergonik ini dan laktat dehidrogenase, maka laktat dapat diubah menjadi fosfoenolpiruvat sehingga mengatasi penghalang energi antara piruvat dan fosfoenolpiruvat. B. fruktosa 1,6-bisfosfat dan fruktosa 6-fosfat: Konversi fruktosa 1,6-bisfosfat menjadi fruktosa 6-fosfat, yang diperlukan untuk mencapai pembalikan glikolisis, dikatalisis oleh suatu enzim spesifik, yaitu fruktosa 1,6bisfosfatase. Enzim ini sangat penting bila dilihat dari sudut pandang lain, karena keberadaanya menentukan dapat-tidaknya suatu jaringan menyintesis glikogen bukan saja dari piruvat tetapi juga dari triosafosfat. Enzim fruktosa 1,6-bisfosfatase terdapat di hati dan ginjal dan juga telah diperlihatkan di dalam otot lurik. Enzim tersebut diperkirakan tidak terdapat dalam otot jantung dan otot polos. 4 C. Glukosa 6-fosfat dan glukosa: Konversi glukosa 6-fosfat menjadi glukosa dikatalisis oleh enzim fosfatase yang spesifik lainnya, yaitu glukosa 6fosfatase. Enzim ini terdapat di hati dan ginjal tetapi tidak ditemukan di jaringa adipose serta otot. Keberadaanya memungkinkan jaringan untuk menambah glukosa ke dalam darah. D. Glukosa 1-Fosfat dan Glukogen : Pemecahan glikogen menjadi glukosa 1fosfat dilaksanakan oleh enzim fosforilase Sintesis glikogen melibatkan lintasan yang sama sekali berbeda melalui pembentukan uridin disfosfat glukosa dan aktivotas enzim glikogen sintase Enzim yang penting ini memungkinkan pembalikan glikolisis memainkan peran utama di dalam glukoneogenesis. Hubungan antara glukoneogenesis dan lintasan glikolisis. setelah transminasi atau deaminasi, asam amino glukogenik membentuk piruvat atau anggota lain siklus asam sitrat. Dengan demikian, reaksi yang diuraikan di atas dapat menjelaskan proses konversi baik asam amino glukogenik maupun laktat menjadi glukosa atau glikogen. Jadi, senyawa laktat membentuk piruvat dan harus memasuki mitokondria sebelum konversi menjadi oksaloasetat serta konversi akhir menjadi glukosa langsung. Propionat merupakan sumber utama glukosa pada hewan pemamah-biak, dan memasuki lintasa glukogenesis utama lewat siklus asam sitrat setelah proses konversi menjadi suksinil KoA. Propionat pertama-tama diaktifkan dengan ATP dan KoA oleh enzim asil-KoA sintetase yang tepat. Propionil –KoA, yaitu produk reaksi ini, menjalani reaksi fiksasi CO2 untuk membentuk D-metilmaloni-KoA, dan reaksi ini dikatalis oleh enzim propionil-KoA karboksilase. Reaksi fiksasi ini analog dengan fiksasi CO2 dalam asetil-KoA oleh enzim asetil KoA karboksilase , yaitu sama-sama membentuk derivat malonil dan memerlukan vitamin biotin sebagai koenzim.DMetilmalonil KoA harus diubah menjadi bentuk stereoisomernya, yakni Lmetilmalonil-KoA, oleh enzim metilmalonil-KoA rasemase, sebelum langsung isomerisasi akhir senyawa tersebut menjadi suksinil KoA oleh enzim metilmalonilKoA isomerase yang memerlukan vitamin B12 sebagai koenzim. Definisi vitami B12 pada manusia dan hewan akan mengakibatkan ekskresi sejumlah besar metil malonat (Basiduria metilmalonat) 5 Meskipun lintasan ke arah suksinat merupakan jalur utama metabolisme, propionat dapat pula digunakan sebagai molekul yang mempersiapkan proses sintesis asam lemak di jaringan adipose dan kelnjar payudara dengan jumlah atom karbon ganjil pada molekul tersebut. Asam lemak C15 dan C17 terutama ditemukan di dalam lemak hewan pemamah-biak. Dalam bentuk seperti itu, lemak tersebut merupakan sumber asam lemak yang penting di dalam makanan manusia dan akhirnya akan dipecah menjadi propionat di jaringan tubuh. Gliserol merupakan produk metabolisme jaringan adipose dan hanya jaringan yang mempunyai enzim pengaktifnya, gliserolkinase, yang dapat menggunakan senyawa gliserol. Enzim ini, yang memerlukan ATP, ditemukan di hati dan ginjal di antara jaringan lainya. Gliserol kinase mengatalis proses konversi gliserol menjadi gliserol 3-fosfat. Lintasan ini berhubungan dengan tahap triosafosfat pada lintasan glikolisis, karena gliserol 3-fosfat dapat dioksidasi menjadi dihidroksiaseton fosfat oleh NAD+ dengan adanya enzim gliserol 3-fosfat dehidrogenase. Hati dan ginjal mampu mengubah gliserol menjadi glukosa darah dengan menggunakan enzim di atas, beberapa enzim glikolisis dan enzim spesifik pada lintasan glukoneogenesis, yaitu fruktosa-1,6-biofosfatase serta glukosa–6-fosfatase. 2.2 GLIKOLISIS DAN GLUKONEOGENESIS MEMPUNYAI LINTASAN YANG SAMA TETAPI ARAHNYA BERBEDA, MAKA KEDUA PROSES INI HARUS DIATUR SECARA TIMBAL BALIK. Perubahan keberadaan substrat bertanggung jawab langsung atau tidak langsung atas sebagian besar perubahan di dalam metabolisme. Fluktuasi pada konsentrasi substrat di dalam darah yang disebabkan oleh perubahan keberadaanya di makanan bisa mengubah laju sekresi hormon yang selanjutnya akan mempengaruhi pola metabolisme pada lintasa metabolik-sering dengan mempengaruhi aktivitas enzimenzim penting, yang mencoba mengompensasi perobahan-awal keberadaan substrat. Ada tiga tipoe mekanisme yang diketahui bertanggung jawab atas pengaturan aktivitas enzim-enzim yang berhubungan dengan metabolisme karbohidrat dan dapat dikenali di dalam tabel 21-1, yaitu : (1) Perubahan laju sintesis enzim, (2) modifikasi kovalen oleh fosforilasi yang reversibel, dan (3) efek alosterik. 6 Tabel 1.1 Enzim – enzim pengatur dan adaptif pada tikus (terutama hati) Aktivitas Pada Pemberian Kelaparan Karbohidrat diabetes dan Penginduksi Represor Aktivator Inhibitor Insulin Glukosa 6- Glukagon fosfat fosforilase, glikogen Enzim-enzim pada glikogenesis, glikolisis & Oksidasi piruvat Sistem glikogen Insulin sintase Glukosa-6 Fosfat1 Heksokinase Glukokinase Insulin Glukagon (cAMP) Fosfofruktokinase- Insulin Glukagon (cAMP) 1 Piruvat kinase (cAMP) Insulin, fruktosa Glukagon (cAMP) AMP, Fruktosa-6- Asam sitrat (lemak fosfat, p fruktosa 2, badan keton)1 ATP1 6-bisfosfat glukagon (cAMP) Fruktosa 1,6- 1 bisfosfat insulin ATP, Alanin, glukagon (cAMP), epinefrin Piruvat KoA, NAD, Insulin2, Asetil-KoA, NADH, dehidrogenase ADP, piruvat ATP (asamlemak, badan keton) Enzim-enzim glukoneogenesis Piruvat Glukortiroid, Karboksilase glukagon, epinefrin (cAMP) 7 Insulin Asetil KoA ADP1 Fosfoenolpiruvat Glukortiroid, karboksikinase glukagon, epinefrin Insulin Glukagon? Insulin Glukagon (cAMP) (cAMP) Fruktosa 1,6- bisfosfat Glukortiroid, Fruktosa glukagon, epinefrin Bisfosfat, (cAMP) Fruktosa bisfosfat Glukosa-6- Glukortiroid, fosfatase glukagon, epinefrin 1-6AMP, 2, 6- 1 Insulin (cAMP) Enzim-enzim pada lintasan pentosa fosfat dan lipogenesis Glukosa-6 fosfat Insulin dehidrogenase 6-Fosfoglukonal Insulin dehidrogenase Enzim Malat Insulin ATP-Sitratliase Insulin Asetil-KoA Insulin? ADP Sitrat1, insulin Karboksilase Asil KoA rantalpanjang, CAMP, Glukagon Asam lemak Insulin? sintase 1 Alosentrik 2 Di Jaringan adipose di hati 8 2.3 Fruktosa 2,6-Bisfosfat Mempunyai Peranan yang Unik di dalam Regulasi Glikolisis dan Glukoneogenesis Efektor alosterik positif paling poten dari fruktokinase-1 dan inhibitor fruktosa1,6-bisfosfatase di hati adalah fruktosa-2,6-bisfosfat. Senyawa ini mengurangi inhibisi fosfofruktokinase-1 oleh ATP dan meningkatkan afinitas terhadap fruktosa6-fosfat. Senyawa ini juga menghambat enzim fruktosa-1,6-bisfosfatase dengan meningkatkan milai Km untuk fruktosa 1,6-bisfosfat. Konsentrasinya berada di bawah kontrol substrat (alosterik) maupun hormonal (modifikasi kovalen). Fruktosa 2,6-bisfosfat dibentuk melalui fosforilasi senyawa fruktosa 6-fosfat oleh enzim fosfofruktokinase-2. protein enzim yang sama juga bertanggung jawab atas proses pemecahannya karena mengandung aktivitas enzim fruktosa-2,6-bisfosfatase. Enzim dwifungsi ini berada di bawah kontrol alosterik senyaw fruktosa6-fosfat, yang kalaui konsentrasinya naik sebagai akibat berlimphnya glukosa, yaitu dalam keadaan makan kenyang, akan merangsang kinase dan menghambat fosfatase. Sebaliknya, dalam keadaan kekurangan glukosa, hormon glukagon akan merangsang produksi cAMP dengan mengaktifkan protein kinase yang bergantung cAMP dan enzim iniselanjutnya menginaktifkan fosfofruktokinase-2 serta mengaktifkan enzim fruktosa 2,6-bisfosfatase melalui fosforilasi. Jadi, dalam keadaan glukosa yang berlimpah, konsentrasi senyawa fruktosa 2,6bisfosfat akan meningkat sehingga merangsang glikolisis dengan mengaktifkan fosfofruktokinase-1 dan menghambat fruktosa-1,6-bisfosfatase. Dalam keadaan kekurangan glukosa, glukoneogenesis dirangsang oleh penurunan konsentrasi fruktosa 2,6-bisfosfat yang kemudian menghilangkan aktivitas fosfofruktokinase-1 dan meniadakan penghambatan kerja fruktosa-1, 6-bisfosfatase. Mekanisme ini juga menjamin bahwa stimulasi glukagon pada glikogenolisis di hati mengakibatkan pelepasan glukosa bukannya glikolisis. Penelitian baru-baru ini menunjukkan bahwa glukosa 1,6 bisfosfat memainkan peranan yang serupa di beberapa jaringan ekstraheptik. 9 2.4 KONSENTRASI GLUKOSA DARAH DIATUR DALAM BATAS-BATAS YANG SEMPIT Pada keadaan setelah penyerapan makanan, kadar glukosa darah pada manusia dan banyak mamalia berkisar antara 4,5 – 5,5 mmol/L. setelah ingesti makanan yang mengandung karbohidrat kadar tersebut naik hingga 6,5 – 7,2 mmol/L. Di saat puasa kadar glukosa darah akan turun menjadi sekitar 3,5 – 3,9 mmol/L. Kadar glukosa darah pada burung sangat tinggi (14,0 mmol/L) dan pada hewan pemamamh biak sangat rendah (sekitar 2,2 mmol/L pada domba dan 3,3 mmol/L pada ternak sapi). Kadar yang lebih rendah ini tampaknya dikaitkan dengan kenyataan bahwa hewan pemamah biak pada hakekatnya akan memfermentasikan semua karbohidrat dalam pakannya menjadi asam lemak yang lebih rendah (mudah menguap), dan unsur ini dengan luas menggantikan glukosa sebagai bahan bakar utama metabolik jaringan dalam keadaan kenyang. Penurunan mendadak kadar glukosa darah akan menimbulkan seranagn konvulsi, seperti terlihat pada keadaan overdosis insulin, karena ketergantungan otak langsung pada pasokan glukosa. Namun, kadar yang jauh lebih rendah dapat ditoleransi asalkan terdapat adaptasi tyang progresif; missal, tikus yang sudah teradaptasi dengan diet tinggi lemak akan tampak normal dengan konsentrasi glukosa darah 1,1 mmol/L. 2.5 GLUKOSA DARAH BERASAL DARI MAKANAN GLUKONEOGENESIS DAN GLIKOGENOLISIS Sebagian besar karbohidrat yang dicerna di dalam makanan akhirnya akan memebentuk glukosa. Karbohidrat di dalam makanan yang dicerna secara aktif mengandung residu secara aktif mengandung residu glukosa. Glaktosa dan fruktosa yang akan dilepas di intestinum. Zat –zat ini lalu diangkut ke hati lewat veha perta hati. Galaktosa dan fruktosa segera dikonversi menjadi glukosa di hati. Glukosa dibentuk dari senyawa-senyawa glukogenik yang mengalami glukoneogenesis. Senyawa ini dapat dogolongkan ke dalam 2 kategori: (1) senyawa yang melibatkan konversi neto langsung menjadi glukosa tanpa daur ulang yang bermakna, seperti beberapa asam amino serta propionat; dan (2) senyawa yang merupakan produk metabolisme parsial glukosa pada jaringan tertentu dan yang diangkut ke hati serta ginjal untuk disintesi kembali menjadi glukosa. Oleh karena itu , 10 laktat yang dibentuk oleh oksidasi glukosa di dalam otot rangka dan oleh eritrosit, ditranspor ke hati dan ginjal untuk dijadikan glukosa kembali, yang membuat unsur ini tersedia lagi lewat sirkulasi untuk oksidasi di jaringan. Proses ini dikenal sebagai siklus Cori dan siklus laktat. Gliserol 3-fosfat untuk sintesis triasilgliserol di jaringan adipose berasal dari glukosa darah. Senyawa asilgliserol pada jaringan adipose terus menerus mengalami hidrolisis untuk membentuk gliserol bebas, yang tidak dapat digunakan oleh jaringan adiposa dan karenanya akan difusi keluar serta masuk ke dalam darah. Gliserol bebas ini dikonversi kembali menjadi glukosa lewat mekanisme glukoneogenesis di hati dan ginjal. Diantara asam-asam amino yang ditranspor dari otot ke dalam hati selama masa kelaparan, alaninlah yang paling dominan. Kenyaraan ini kemudian menghasilkan postulasi siklus glukosalanin, yang berefek pendauran glukosa dari hati ke otot dengan pembentukan piruvat, yang diikuti dengan transminasi menjadi alanin, lalu transpor alanin ke hati, dan kemudian diikuti oleh glukoneogenesis kembali menjadi glukosa. Pemindahan neto nitrogen amino dari otot ke hati dan energi bebas dari hati ke otot dengan demikian bisa terlaksana. Energi yang diperlukan untuk sintesis glukosa di hti dari piruvat berasal dari oksidasi asam-asam lemak. Glukosa juga dibentuk dari glikogen hati melalui glikogenilisis. 2.5.1 Mekanisme Metabolik dan Hormonal Mengatur Konsentrasi Glukosa Darah Proses mempertahankan kadar glukosa yang stabil di dalam darah merupakan salah satu mekanisme homeostasis yang diatur paling halus dan juga menjadi salah satu mekanisme dengan hati jaringan ekstrahepatik serta beberapa hormon turut mengambil bagian. Sel-sel hati tampak dapat dilewati glukosa dengan bebas (melalui transpoter GLUT 2), sedangkan sel-sel pada jaringan ekstrahepatik, dan glukosa mengalami fosforilasi dengan cepat oleh heksokinase pada saat masuk ke dalam sel. Sebaliknya, aktivitas enzim tertentu dan konsentrasi beberapa intermediat yang penting mungkin memberi pengaruh yang jauh lebih langsung terhadap pengambilan atau pengeluaran glukosa dari hati. Walaupun begitu, konsentrasi glukosa di dalam darah merupakan factor penting yang mengendalikan kecepatan ambilan glukosa baik di hati maupun jaringan ekstrahepatik. 11 Peranan berbagai protein pengngkut glukosa, yang ditemukan pada membran sel dengan masing-masing memiliki 12 buah wilayah transmembran, diperlihatkan tabel 12 Tabel 1-2 Pengangkut Glukosa Lokasi Jaringan Pengangkut fasilitatif dua-arah GLUT 1 Otak, ginjal, kolon, plasenta,eritrosit GLUT 2 Hati, sel B pankreas, usus halus, ginjal GLUT 3 Otak, ginjal, plasenta GLUT 4 Otot jantung dan rangka, jaringan adiposa GLUT 5 Usus halus Pengangkut satu-arah yang bergantung-natrium SGLT 1 Usus halus dan ginjal 12 Fungsi Ambilan glukosa Ambilan dan pelepasan glukosa yang cepat Ambilan glukosa Ambilan glukosa yang dirangsang oleh insulin Absorpsi glukosa Ambilan aktif glukosa dari lumen dan reabsorpsi glukosa di tubulus proksimal ginjal melawan gradien konsentrasi 2.5.2 Glukokinase Merupakan Enzim yang Penting dalam Mengatur Glukosa Darah Sesudah Makan Harus dicatat bahwa heksokinase dihambat oleh glukosa 6-fosfat, sehingga beberapa pengkontrolan umpan-balik dapat dilakukan terhadap ambilan glukosa di jaringan ekstahepatik yang bergantung pada heksokinase untuk fosforilasi glukosa. Hati tidak mengalami kendala ini karena glukokinase tidak dipengaruhi oleh glukosa 6fosfat. Glukokinase, yang mempunyai nilai Km yang lebih tinggi (afinitas lebih rendah) untuk glukosa daripada nilai Km heksokinase, meningkat aktivitasnya melabihi kisaran kadar glukosa yang fisiologik dan enzim ini agaknya mempunyai hubungan yang khusus dengan ambilan glukosa ke hati pada konsentrasi lebih tinggi yang ditemukan pada verta porta hati sesudah memakan makanan yang mengandung karbohidrat. Tidak adanya enzim glukokinase pada hewan pemamahbiak, karena hanya sedikit glukosa yang masuk ke dalam sirkulasi darah porta dari intestinum sebanding dengan fungsi ini. Pada konsentrasi glukosa darah sistematik yang normal (4,5 – 5,5 mmol/L), hati tampaknya merupakan penghasil neto glukosa, akan tetapi, dengan naiknya kadar glukosa, proses keluaran glukosa akan terhenti sehingga pada kadar yang tinggi terdapat ambilan neto. Pada tikus diperkirakan bahwa kecepatan ambilan setara dengan kecepatan pengeluaran glukosa pada konsentrasi glukosa dalam darah vena porta sebesar 8,3 mmol/L 2.5.3 Insulin Memainkan Peranan Sentral dalam Mengatur Glukosa Darah Di samping pengaruh langsung hiperglikemia dalam meningkatkan ambilan glukosa baik ke hati maupun jaringan perifer, hormon insulin juga mempunyai peranan sentral dalam mengatur konsentrasi glukosa darah. Hormon ini dihasilkan oleh sel-sel B pada pulau-pulau Langerhans pankreas sebagai reaksi langsung terhadap keadaan hiperglikemia. Sel-sel pada pulau Langerhans dapat dilewati denagn bebas oleh glukosa lewat pengangkut GLUT 2, dan glukosa akan mengalami fosforilasi oleh enzim glukokinase yang memiliki nilai Km yang tinggi. Karena itu, konsentrasi glukosa darah menentukan aliran lewat glikolisis, siklus asam sitrat dan pembentukan ATP. Peningkatan konsentrasi ATP akan menhambat saluran K+ yang sensitive terhadap ATP sehingga menyebabkan depolarisasi membaran sel-B, keadaan depolarisasi membran 13 sel ini akan meningkatkan aliran masuk Ca2+ lewat saluran Ca2+ yang sensitive terhadap voltase dan dengan demikian menstimulasi eksosilosis insulin. Penting untuk diperhatikan bahwa obat-obatan golongan sulfonilurea yang digunakan untuk menstimulasi sekresi insulin pada penyakit diabetes mulitus tipe II (diabetes militus yang tidak bergantung insulin ; NIDDM) memberikan khasiatnya dengan menghambat saluran K+ yang sensitif terhadap ATP. Jadi, konsetrasi glukosa darah sejajar dengan konsentrasi glukosa darah. Pemberian insulin akan mengakibatkan hipoglikemia seketika. Zat-zat lain yang menyebabkan pelepasan insulin adlah asam amino, asam lemak bebas, badan keton, glukagon, sekretin dan obat-obat sulfoniluria tolbutamid serta gliburid. Epinefrin dan neropinefrin menyekat pelepasan insulin. Insulin mempunyai efek segera yang meningkatkan ambilan glukosa di jaringan seperti jaringan adipose dan otot. Kerja insulin ini disebabkan oleh peningkatan transpor glukosa (GLUT 4) dari bagian dalam sel ke membran plasma. Sebaliknya, hormon insulin tidak memiliki efek langsung terhadap penetrasi glukosa pada sel-sel hati; hasil penemuan ini sesuai dengan kenyataan bahwa metabolisme glukosa oleh sel-sel hati tidak dibatasi kecepatannya oleh permeabilitasnya terhadap glukosa. Meskipun demikian, secara tidak langsung insulin akan meningkatkan ambilan jangka panjang glukosa oleh hati sebagai hasil kerjanya pada sintesis enzim yang mengkontrol glikolisis, glikogenesis dan glukoneogenesis. Insulin memiliki efek segera dalam mengaktifkan enzim glikogen sintase. 14 Vmax 100 Aktivasi Heksokinase 50 0 Glukokinase 5 10 15 20 25 Glukosa Darah (mmol/L) Gambar : Variasi aktivitas fosgorilasi glukosa pada enzim heksokinase dan glukokinase dengan meningkatka konsentrasi glukosa darah. Nilai Km heksokinase untuk glukosa adalah 0,005 mmol/L dan nilai Km glukokinase untuk glukosa adalah mmol/L 2.5.4 Glukagon Melawan Kerja Insulin Glukagon merupakan hormon yang dihasilkan oleh sel-sel A pada pulau-pulau Langerhans pankreas. Sekresi hormon ini dirangsang oleh keadaan hipoglikemia. Pada saat mencapai hati (lewat vena porta), hormon glukagon menimbulkan glikogenolisis dengan mengaktifkan enzim fosforilase. Sebagian besar glukagon endogen (dan insulin) dibersihkan dari sirkulasi darah oleh hati. Berbeda dengan epinefrin, glukagon tidak mempunyai pengaruh pada enzim fosforilase otot. Glukagon juga meningkatkan glukoneogenesis dari asam amino dan laktat. Pada semua cara kerja ini, glukagon bekerja dengan menghasilkan cAMP, baik efek hiperglikemia glukagon, yang kerjanya berlawanan dengan kerja insulin. 2.5.5 Hormon Lain Mempengaruhi Glukosa Darah Kelenjar hipofisis anterior menyekresikan hormon yang cenderung meneikkan kadar glukosa darah dengan demikian mengatagonis kerja insulin. Hormon-hormon ini adalah hormon pertumbuhan, ACTH (kortikotropin), dan mungkin pula preparat 15 hormon dengan prinsip “diabetogonik” lainnya. Sekresi hormon pertumbuhan dirangsang oleh keadaan hipoglikemia. Hormon pertumbuhan menutunkan ambilan glukosa di jaringan tertentu, missal otot. Sebagian efek ini mungkin tidak langsung, karena hormon pertumbuhan memobilisasi asam lemak bebas itu sendiri menghambat penggunaan adiposa dan asam lemak lemak bebas itu sendiri menghambat penggunaan glukosa. Pemberian hormon pertumbuhan untuk jangka waktu lama akan menimbulkan keadaan diabetes. Dengan menghasilkan hiperglikemia, hormon tersebut merangsang sekresi insulin yang pada akhirnya menimbulkan kelelahan sel B. Glukokortikoid (11-oksisteroid) disekresikan oleh korteks adrenal dan sangat penting di dalam metabolisme karbohidrat. Pemberian preparat steroid ini akan menyebabkan peningkatan glukoneogenesis. Peristiwa ini terjadi akibat peningkatan katabolisme protein di jaringan, peningkatan ambilan asam amino oleh hati, dan peningkatan aktivitas enzim transaminase serta enzim lainya yang berhubungan dengan glukoneogenesis di hati. Selain itu, glukokortikoid menghambatpenggunaan glukosa di jaringan akstahepatik. Dalam melaksanakan semua kegiatan ini, glukokortikoid bekerja secara antaginistik terhadap insulin. Epinefrin disekresikan oleh mondula adrenal sebagai akibat dari rangsangan yang menimbulkan stress (ketakutan, kegembiraan, perdarahan, hipoksia, hipoglikemia, dll) dan menimbulkan glikogenolisis di hati serta otot karena stimulasi enzim fosforilase dengan menghasilkan cAMP. Di dalam otot, sebagai akibat tidak adanya enzim glukosa-6-fosfatse, glikogenolisis terjadi dengan pembentukan laktat sedangkan di hati, glukosa merupakan produk utama yang menyebabkan peningkatan kadar glukosa darah. Hormon Tiroid harus pula dipandang sebagai hormon yang mempengaruhi glukosa darah. Terdapat bukti-bukti eksperimental bahwa tiroksin mempuntyai kerja diabetogonik dan bahwa tindakan tirokoidektomi menghambat perkembangan diabetes. Juga ditemukan bahwa glikogen sama sekali tidak terdapat di hati hewan yang menderita tirotoksikosis. Pada manusia, kadar glukosa puasa yang normal atau meningkat, sedangkan parien hipertiroid mengalami penurunan kemampuan dalam menggunakan glukosa. Di samping itu, pasien hipotiroid mempunyai sensitivitas terhadap insulin jauh lebih rendah bila dibandingkan dengan orang-orang normal atau penderita hipertiroid. 16 BAB III PENUTUP 3.1 Kesimpulan Dari pembahasan diatas maka dapat disimpulkan 1. Glikosuria Terjadi Jika Ambang Ginjal Untuk Glukosa Dilampui pada laju sekitar 350 mg/menit. Ketika kadar glukosa darah naik Kadar glukosa darah naik hingga kadar yang relatif tinggi, ginjal juga melakukan suatu pengaturan. Glukosa disaring oleh glomerulus secara terus-menerus, tetapi kemudian akan dikembalikan sekuruhnya ke dalam darah melalui sistem reabsorpsi tubulus ginjal. Reabsorbsi glukosa melawan gradien konsentrasinya terkait dengan pengadaan ATP di sel-sel tubulus. Kapasitas sistem tubulus untuk mereabsorpsi glukosa terbatas, fitrat glomerulus dapat mengandung glukosa lebih banyak daripada junmlah yang bisa direabsorpsi; kelebihan ini kan dikeluarkan ke urin sehingga menimbulkan gejala glikosuria. Pada orang-orang normal, glikosuria terjadi ketika konsentrasi glukosa di dalam darah vena melampaui 9,5 – 10,0 mmol/L. keadaan ini dinamakan ambang ginjal (renal thresholl\d) untuk glukosa. Glikosuria dapat ditimbulkan pada hewan-hewan percobaan dengan pemberian florizin yang menghambat sistem reabsorbsi glukosa di tubulus. Keadaan ini dikenal sebagai glukosuria renal. Glikosuria yang penyebabnya pada ginjal ini dapat terjadi akibat kelamin ginjal yang diwariskan atau bisa didapat sebagai akibat proses penyakitnya. Adanya glikosuria sering merupakan indikasiuntuk penyakit diabetes mellitus. 2. Defisiensi Fruktosa –1,6-Bisfosfatase Menyebabkan Asidosis Laktat dan Hipoglikemia Penyekatan glukoneogenesis oleh defisiensi enzim ini akan mencegah laktat dan substrat glukogenik lainnya dikonversi menjadi glukosa di hati. Keadaan tersebut dapat dikontrol dengan memberikan diet tinggi-karbohidrat tetapi rendah fruktosa dan sukrosa dan dengan mengihari puasa. 17 3. Gangguan Oksidasi Asam Lemak Menyebabkan Hipoglikemia Beberapa keadaan dengan terjadinya gangguan oksidasi asam lemak akan ditandai dengan hipoglikemia. Hal ini disebabkan oleh ketergantungan glukoneogenesis pada oksidasi asam lemak yang aktif (lihat di atas). 4. Hipoglikemia Dapat Terjadi Selama Kehamilan dan Pada Neonatus Pada saat kehamilan konsumsi glukosa oleh janin akan meningkat dan terdapat resiko hiperglikemia maternal dan mungkin pula hipoglikemia fetal, khususnya jika terdapat interval yang lama antara saat makan atau pada malam hari. Selanjutnya, bayi premature dan bayi dengan berat kahir rendah lebih rentan terhadap keadaan hipoglikemia karena bayi tersebut memiliki sedikit jaringan adiposa untuk menyediakan bahan bakar alternatif seperti asam lemak bebas atau benda keton selama masa transisi dari ketergantungan janin ke kehidupan yang independen. Mungkin pada saat itu enzim-enzim glukoneogenesis masih belum berfungsi sepenuhnya dan proses tersebut akan bergantung pada pasokan asam lemak bebas untuk mendapatkan energi. Gliserol yang dalam keadaan normal dilepas dari jaringan adiposa tidak begitu tersedia bagi keperluan glukoneogenesis. 5. Kemampuan Tubuh untuk Menggunakan Glukosa Dapat Dipastikan Dengan Mengukur Toleransi Glukosa Toleransi glukosa ditunjukkan oleh sifat kurva glukosa darah sesudah pemberian sejumlah glukosa untuk tes. Penyakit Diabetes melitus (diabetes mellitus tipe I atau diabetes mellitus bergantung insuli, IDDM) ditandai dengan penurunan toleransi glukosa akibat berkurangnya sekresi insulin sebagai respons terhadap pemberian glukosa. Manifestasi klinis penyakit ini berupa kenaikan kadar glukosa darah (Hiperglikemia) dan glukosuria yang dapat disertai perubahan pada metabolisme lemak. Toleransi terhadap glukosa bukan saja menurun pada penyakit diabetes tipe I tetapi juga pada kerusakan hati; pada beberapa infeksi; pada penyakit diabetes melitus tipe II (NIDDM), yang sering disertai obesitas serta peningkatan kadar asam lemak bebas di dalam plasma;pada keadaan di bawah pengaruh beberapa obat tertentu; dan kadang –kadang pada aterosklerosis. Penurunan toleransi glukosa ini diperkirakanakan terjadi pula pada hiperaktivitas kelenjar hipofisi atau kortek adrenal, karena sifat antagonisme hormon-hormon kelenjar endokrin terhadap kerja insulin. 18 Insulin meningkatkan toleransi glukosa. Penyuntikan insulin akan menurunkan kandungan glukosa di dalam darah dan meningkatkan pemakaian serta penyimpanan di hati serta otot sebagai glikogen. Insulin yang berlebihan dapat menyebabkan hipoglikemia berat, yang menimbulkan gejala konvulsi dan bahkan kematian bila tidak segera disuntikkan glukosa. Peningkatan toleransi terhadap glukosa terlihat pada insufisiensi kelenjar hipofisis atau korteks adrenal, yang bisa dikaitkan dengan penurunan sifat antagonis terhadap insulin oleh hormon-hormon ynag secara normal akan dihasilkan oleh kedua kelenjar ini. 15 Glukosa darah (mmol/L) Pasien Diabetes 10 5 Orang Normal 0 1 2 Waktu (jam) Gambar : Tes toleransi glukosa (GTT; Glucose tolerance test). Kurva glukosa darap pada orang normal dan penderita diabetes sesudah pemberian glukosa 50 gr per oral. Perhatikan kenaikan awal konsentrasi glukosa pada pasien diabetes. Kriteria keadaan normal adalah kembalinya kurva tersebut pada nilai awal dalam waktu 2 jam 3.2 Saran Setelah membahas beberapa masalah diatas penulis memberi saran agar sedapat mungkin kita menjalani pola hidup sehat agar kita dapat menjalankan aktivitas sehari hari dengan sehat, tanpa penyakit diantaranya Diabetes Mellitus. 19