optimisasi ekstraksi flavonoid total daun jati belanda
advertisement

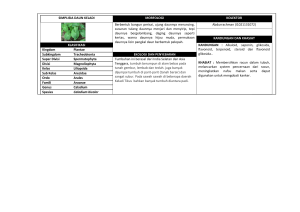
1 OPTIMISASI EKSTRAKSI FLAVONOID TOTAL DAUN JATI BELANDA FARAH UMAR DEPARTEMEN KIMIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR BOGOR 2008 2 ABSTRAK FARAH UMAR. Optimisasi Ekstraksi Flavonoid Total Daun Jati Belanda. Dibimbing oleh LATIFAH KOSIM DARUSMAN dan UTAMI DYAH SYAFITRI. Salah satu tanaman yang biasa digunakan sebagai obat tradisional adalah jati belanda (Guazuma ulmifolia Lamk.). Daun jati belanda ini dapat digunakan sebagai obat pelangsing tubuh. Sebagian besar obat tradisional disajikan dalam bentuk ekstrak karena penyajiannya dinilai lebih efisien dan praktis. Salah satu upaya yang dilakukan untuk mengurangi besarnya biaya produksi ialah dengan mengoptimumkan ekstrak yang diperoleh. Bermacam-macam upaya telah dilakukan untuk mengekstraksi flavonoid dari daun jati belanda. Dalam penelitian ini, daun jati belanda diekstraksi dengan metode refluks, pelarut etanol, dan dengan meragamkan 3 parameter ekstraksi, yaitu konsentrasi pelarut 50, 70, dan 90%; waktu ekstraksi 3, 5, dan 7 jam; dan nisbah bahan baku pelarut 1:5, 1:10, dan 1:15. Dalam hal ini dapat dilihat pengaruh konsentrasi pelarut, waktu ekstraksi, dan nisbah bahan baku pelarut terhadap kadar flavonoid total yang dihasilkan. Penelitian menggunakan rancangan fraksional faktorial. Kadar ditentukan dengan menggunakan metode AlCl3 dan diukur dengan spektrofotometer berkas ganda, kadar optimumnya ditentukan dengan metode permukaan respons menggunakan perangkat lunak SAS 9.1. Persamaan kadar flavonoid total yang diperoleh adalah Kadar = -1.20208 – 0.06167(waktu) + 0.00125(waktu)2 + 0.04208(konsentrasi) – 0.0003 (konsentrasi)2 + 0.04383(nisbah) – 0.0034(nisbah)2 + 0.00650(nisbah*waktu) dengan R2 = 99.67%. Kondisi optimum ekstraksi teramati pada konsentrasi pelarut 70%, nisbah bahan bakupelarut 1:10, dan waktu ekstraksi 3 jam. ABSTRACT FARAH UMAR. Extraction Optimization of Total Flavonoid from Daun Jati Belanda. Supervised by LATIFAH KOSIM DARUSMAN and UTAMI DYAH SYAFITRI. One of many plants used for traditional medicine is jati belanda. It can be used as an antiobesity. Most of traditional medicine are available practically as an extract ion. One of the efforts to reduce the production cost is optimizing the extract. Various treatments were applied to extract flavonoid from jati belanda leaves. In the research, jati belanda was extracted using reflux method with ethanol as a solvent, at concentrations of 50, 70, and 90%, for 3, 5, and 7 hours, with sample to solvent ratio of 1:5, 1:10, and 1:15. All of this conditions were used to study the effect of solvent’s concentrations, time, and sample to solvent ratio to total flavonoid content. The data were analyzed designed using fractional factorial design. Determination of total flavonoid content was conducted with AlCl3 method and measured with double beam spectrophotometer, and the optimum content was determined by response surface method using SAS 9.1 software. The obtained model was Content = -1.20208 – 0.06167(time) + 0.00125(time)2 + 0.04208(concentration) – 0.0003 (concentration)2 + 0.04383(material ratio) – 0.0034(material ratio)2 + 0.00650(material ratio*time) with R2 = 99.67%. The optimum condition of extraction was obtained at 70% for solvent concentration, 3 hours for extraction time, and 1:10 for the ratio of sample to solvent. 3 OPTIMISASI EKSTRAKSI FLAVONOID TOTAL DAUN JATI BELANDA FARAH UMAR Skripsi sebagai salah satu syarat memperoleh gelar Sarjana Sains pada Departemen Kimia DEPARTEMEN KIMIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR BOGOR 2008 4 Judul Skripsi : Optimisasi Ekstraksi Flavonoid Total Daun Jati Belanda Nama : Farah Umar NIM : G44203001 Disetujui: Pembimbing I, Pembimbing II, Prof. Dr. Ir. Latifah K Darusman, MS NIP 13053668 Utami Dyah Syafitri, M.Si NIP 132311922 Diketahui: Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Dr. drh. Hasim, DEA NIP 131578806 Tanggal lulus: 5 PRAKATA Bismillahirrohamanirrohim. Alhamdulillahirabbil ‘alamin, segala puji dan syukur penulis panjatkan ke hadirat Allah SWT atas limpahan rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan karya ilmiah ini. Shalawat dan salam semoga selalu tercurahkan kepada nabi Muhammad SAW, keluarga, sahabat, dan umatnya hingga akhir zaman. Tema yang dipilih dalam karya ilmiah ini adalah optimisasi ekstraksi, dengan judul Optimisasi Ekstraksi Flavonoid Total Daun Jati Belanda. Penulis mengucapkan terima kasih kepada Ibu Tuti Setiawati Sudjana (almh), Ibu Latifah K Darusman, dan Ibu Utami Dyah Syafitri yang telah membimbing penulis dalam menyelesaikan karya ilmiah ini. Ungkapan terima kasih juga disampaikan kepada seluruh keluarga atas segala doa, semangat, dan kasih sayang; segenap staf pengajar di Departemen Kimia FMIPA IPB atas pengajaran yang diberikan; seluruh staf pegawai Departemen Kimia FMIPA IPB khususnya Pak Eman, Pak Dede, Pak Ridwan, Pak Engkos, dan Bu Nunung yang selalu setia mendampingi dan membantu segala keperluan yang menyangkut penyelesaian karya ilmiah ini. Penulis juga berterima kasih kepada rekan-rekan Analitik 40, Kimia 40, B-14, Al-Ghifari atas dukungan dan inspirasinya; MSC atas doa, semangat, dan ukhuwah; Pusat Studi Biofarmaka dan Departemen Statistika IPB. Semoga karya ilmiah ini dapat bermanfaat. Bogor, Juni 2008 Farah Umar 6 RIWAYAT HIDUP Penulis dilahirkan di Tegal pada tanggal 14 Oktober 1984 dari ayah Umar Said Basalamah dan ibu Zubaedah Umar Al-Kathiri. Penulis merupakan putri pertama dari dua bersaudara. Tahun 2003 penulis lulus dari SMU Sekolah Indonesia Jeddah dan pada tahun yang sama lulus seleksi masuk IPB melalui jalur Undangan Seleksi Masuk IPB. Penulis memilih Program Studi Kimia, Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam. Selama mengikuti perkuliahan, penulis menjadi asisten mata kuliah Kimia Dasar pada tahun ajaran 2005/2006, 2006/2007, dan 2007/2008, mata kuliah Kimia Analitik II pada tahun ajaran 2006/2007, serta mata kuliah Kimia Analitik I pada tahun ajaran 2007/2008. Penulis pernah aktif di kegiatan organisasi kemahasiswaan, yaitu sebagai salah satu staf Departemen Kajian dan Jurnalistik Islam DKM Al-Ghifari pada tahun 2006 dan 2007. Pada Juli-Agustus 2006 penulis melaksanakan praktik lapangan di PT Indofarma Cibitung dengan judul Kualifikasi Mesin Dissolution Tester Hanson Research Tipe Sr-8 Plus Menggunakan Metode Spektrofotometri. 7 DAFTAR ISI Halaman DAFTAR TABEL .......................................................................................................... viii DAFTAR GAMBAR ..................................................................................................... viii DAFTAR LAMPIRAN .................................................................................................. viii PENDAHULUAN ......................................................................................................... 1 TINJAUAN PUSTAKA Jati Belanda .......................................................................................................... Flavonoid ............................................................................................................. Ekstraksi .............................................................................................................. Rancangan Fraksional Faktorial .......................................................................... Optimisasi Ekstraksi ........................................................................................... 1 2 3 3 4 BAHAN DAN METODE Bahan dan Alat ..................................................................................................... Metode Penelitian ................................................................................................ 4 4 HASIL DAN PEMBAHASAN Ciri Fitokimia ...................................................................................................... Hasil Rancangan Fraksional Faktorial.................................................................. Kondisi Ekstraksi.................................................................................................. Kurva Standar Flavonoid dan Kadar Contoh........................................................ Model dan Analisis Regresi.................................................................................. Kadar Flavonoid Total Optimum ......................................................................... 6 6 7 7 7 9 SIMPULAN DAN SARAN Simpulan .............................................................................................................. Saran .................................................................................................................... 9 9 DAFTAR PUSTAKA ..................................................................................................... 9 LAMPIRAN ................................................................................................................... 11 8 DAFTAR TABEL Halaman 1 Hasil uji fitokimia daun jati belanda ............................................................................ 6 2 Kombinasi perlakuan yang dicobakan dari hasil fraksionasi....................................... 6 3 Perbandingan kadar flavonoid total hasil percobaan dengan dugaan .......................... 8 4 Hasil pendugaan kadar flavonoid total untuk kombinasi perlakuan yang tidak dicobakan .................................................................................................................. 8 DAFTAR GAMBAR Halaman 1 Daun jati belanda ......................................................................................................... 2 2 Struktur umum senyawa flavonoid .............................................................................. 2 3 Kurva standar flavonoid total....................................................................................... 7 4 Kurva hubungan antara nisbah, konsentrasi, dan waktu terhadap kadar flavonoid total .............................................................................................................. 8 5 Kurva permukaan respons kadar terhadap konsentrasi pelarut dan nisbah bahan baku-pelarut ..................................................................................................... 9 6 Peta kontur kadar terhadap konsentrasi pelarut dan nisbah bahan baku-pelarut ................................................................................................................ 9 DAFTAR LAMPIRAN Halaman 1 Diagram alir penelitian .............................................................................................. 12 2 Diagram alir ekstraksi flavonoid ............................................................................... 13 3 Hasil penentuan kadar air .......................................................................................... 14 4 Kombinasi perlakuan berdasarkan pengacakan dengan SAS 9.1 ............................... 15 5 Rendemen ekstrak daun jati belanda dari perlakuan yang dicobakan......................... 16 6 Absorbans standar flavonoid total............................................................................... 16 7 Kadar flavonoid total dari ekstrak daun jati belanda dari perlakuan yang dicobakan 17 8 Uji keragaman dengan menggunakan chi-square untuk Δ kadar................................ 18 9 Keluaran SAS 9.1 dalam pembuatan model kadar flavonoid total ............................. 19 10 Keluaran SAS 9.1 dalam penentuan titik optimum ekstraksi flavonoid total ............ 20 1 PENDAHULUAN Indonesia kaya akan keanekaragaman hayati yang dapat dimanfaatkan dalam semua segi kehidupan manusia. Obat tradisional adalah salah satu bentuk nyata pemanfaatan sumber daya alam hayati tersebut. Sebagai salah satu negara hutan hujan tropis, Indonesia kaya akan keanekaragaman flora yang dapat digunakan sebagai obat tradisional. Hal ini mendorong para ahli untuk menggali sumbersumber komponen bahan alam dari tumbuhan yang bermanfaat dalam pengobatan berbagai penyakit. Salah satu tanaman yang lazim digunakan sebagai obat tradisional adalah jati belanda (Guazuma ulmifolia Lamk.). Tanaman ini dimanfaatkan antara lain sebagai pelangsing tubuh, obat sakit perut/diare, perut kembung, perut nyeri, batuk, batuk rejan, dan kaki bengkak gatal berair. Bagian tanaman yang digunakan adalah daun, buah, dan biji. Kegunaan jati belanda sebagai obat tidak lepas dari keberadaan senyawa-senyawa kimia yang bertanggung jawab terhadap respons hayati. Senyawa golongan flavonoid merupakan salah satu senyawa yang berperan dalam respons tersebut. Sebagian besar obat tradisional kini disajikan dalam bentuk ekstrak, karena seiring perkembangan zaman, selera konsumen terhadap sediaan obat tradisional telah mengalami pergeseran. Dulu sediaan jamu yang diseduh dengan air panas banyak diminati masyarakat karena aromanya yang kuat dan karena adanya fragmen ampas serbuk yang menurut sebagian konsumen dapat menambah cita rasa jamu. Hal ini merupakan pilihan yang menguntungkan karena biaya produksi lebih murah. Namun, masyarakat dewasa ini menghendaki sediaan jamu dengan kemasan yang lebih praktis karena penyajiannya dinilai lebih efisien. Karena itu, sehingga para pelaku industri obat tradisional kini banyak melirik sediaan ekstrak, untuk dapat mengikuti perkembangan selera konsumen tersebut. Adanya beberapa senyawa aktif dalam tanaman yang tidak larut sempurna dalam air seperti flavonoid nonpolar (golongan flavonon, flavonol, dan isoflavon), juga membuat penggunaan pelarut organik menjadi salah satu pilihan yang dapat dipertimbangkan meskipun biaya produksi menjadi lebih mahal. Salah satu upaya yang dilakukan untuk mengurangi besarnya biaya ekstraksi flavonoid ialah dengan mengoptimumkan proses ekstraksinya. Kondisi ekstraksi yang berbeda dapat menghasilkan senyawa golongan flavonoid dalam jumlah dan jenis yang berbeda pula. Beberapa penelitian telah dilakukan untuk mencari kondisi ekstraksi yang dapat menghasilkan ekstrak yang optimum dalam jumlah dan mutu. Xu et al. (2005) mencari kondisi optimum untuk ekstraksi flavonoid dengan meragamkan 4 faktor, yaitu konsentrasi pelarut, suhu, nisbah bahan bakupelarut, dan waktu ekstraksi. Masing-masing faktor ini memiliki 3 taraf. Pengaruh dari tiap faktor tersebut diteliti secara sendiri-sendiri baru kemudian dihasilkan kondisi yang optimum, yaitu pada konsentrasi pelarut 95%, suhu 80 °C, nisbah bahan baku-pelarut 1:10, dan waktu ekstraksi 3 jam. Pada tahun 2005 Badan Penelitian Tanaman Obat Tawangmangu juga telah melakukan penelitian mengenai pengaruh konsentrasi etanol dan lamanya waktu ekstraksi terhadap kadar flavonoid total herba tapak liman. Kedua faktor yang digunakan memiliki 3 taraf sehingga terdapat 9 kombinasi perlakuan yang dicobakan, karena dalam penelitian tersebut digunakan rancangan faktorial lengkap. Kondisi optimum untuk ekstraksi flavonoid yang dihasilkan adalah pada konsentrasi etanol 90% dan waktu ekstraksi 6 jam. Penelitian ini bertujuan mengetahui pengaruh konsentrasi pelarut, waktu ekstraksi, dan nisbah bahan baku (g)-pelarut (ml) pada ekstraksi daun jati belanda terhadap kadar flavonoid total. Kondisi ekstraksi yang optimum juga ditentukan. TINJAUAN PUSTAKA Jati Belanda Jati belanda (G. ulmifolia Lamk.) yang dikenal juga dengan nama jati londo atau jatos landi telah lama digunakan sebagai obat pelangsing badan. Secara taksonomi, jati belanda diklasifikasikan dalam divisi Spermatophyta, subdivisi Angiospermae, kelas Dicotyledonae, bangsa Malvales, suku Sterculiaceae, marga Guazuma, dan jenis G. ulmifolia Lamk. Jati belanda adalah pohon yang dapat tumbuh dengan cepat mencapai 20 m dan didatangkan dari Amerika bagian tengah. Kini di Jawa pohon ini ditanam sebagai peneduh di pinggir-pinggir jalan. Tanaman ini mempunyai batang yang keras, dan bulat, dengan permukaan yang kasar, dan banyak alur, bercabang, serta berwarna hijau keputihputihan. Daunnya tunggal, bulat telur, 2 memiliki permukaan kasar dengan tepi bergerigi, berujung runcing, dengan pangkal berlekuk, pertulangan menyirip, dan berseling, panjangnya 10–16 cm, lebarnya 3–6 cm, dan berwarna hijau. Bunganya tunggal, bulat, dan terdapat di ketiak daun, berwarna hijau muda. Buahnya berbentuk bulat, kasar, dengan permukaan berduri, dan berwarna hitam. Bijinya kecil, keras, berdiameter sekitar 2 mm, dan berwarna cokelat muda. Akarnya tunggang dan berwarna putih kecoklatan. Bentuk morfologis daun jati belanda dapat dilihat pada Gambar 1. semua bagian tumbuhan termasuk daun, akar, kulit kayu, tepung sari, nektar, bunga, buah, dan biji. Flavonoid juga terkandung pada hewan, misalnya dalam kelenjar bau berangberang, propolis (sekresi lebah), dan di dalam sayap kupu-kupu, dengan anggapan bahwa flavonoid tersebut tidak dibiosintesis di dalam tubuh mereka (Markham 1988). Flavonoid merupakan golongan terbesar dari senyawa fenolik di samping fenol sederhana, fenilpropanoid, dan kuinon fenolik (Harborne 1996). Sebanyak 2% dari seluruh karbon yang difotosintesis oleh tanaman diubah menjadi flavonoid atau senyawa yang berhubungan erat dengannya (Markham 1988). Dalam tumbuhan, aglikon flavonoid terdapat dalam berbagai bentuk struktur. Semuanya mengandung 15 atom C dalam inti dasarnya yang tersusun dalam konfigurasi C6C3-C6, yaitu dua cincin aromatik yang dihubungkan oleh 3 karbon yang dapat atau tidak dapat membentuk cincin ketiga. Struktur umum flavonoid dapat dilihat pada Gambar 2. B Gambar 1 Daun jati belanda. Kandungan senyawa kimia yang telah ditemukan di dalam daun jati belanda adalah flavonoid, asam fenolat, tanin, steroid, triterpenoid, dan saponin. Fungsi senyawasenyawa dalam jati belanda yang telah diketahui antara lain sebagai pelindung kerusakan hati, antibakteri, antijamur, dan sebagai antioksidan. Flavonoid Flavonoid berasal dari kata flavon yang merupakan nama dari salah satu jenis flavonoid yang terbesar jumlahnya dan sering ditemukan di alam. Beberapa golongan flavonoid yang bersifat polar merupakan senyawa yang larut dalam air. Golongan jenis flavonoid dalam jaringan tumbuhan yang didasarkan pada telaah sifat kelarutan dan reaksi warna meliputi antosianin, proantosianin, flavonol, flavon, glikoflavon, biflavonol, kalkon dan auron, flavonon, dan isoflavon. Flavonoid alam ditemukan dalam bentuk glikosida, yaitu suatu bentuk kombinasi antara gula dan alkohol. Flavonoid merupakan kandungan khas tumbuhan hijau. Flavonoid terdapat pada A C Gambar 2 Struktur umum senyawa flavonoid (Markham 1988). Flavonoid mengandung sistem aromatik yang terkonjugasi sehingga menunjukkan pita serapan kuat pada daerah spektrum ultraviolet (UV) dan tampak (Vis). Pengelompokan flavonoid berdasarkan pada cincin heterosiklik-oksigen tambahan dan gugus hidroksil yang tersebar menurut pola yang berlainan (Robinson 1995). Golongan terbesar flavonoid memiliki cincin piran yang menghubungkan rantai tiga-karbon dengan salah satu cincin benzena. Pada umumnya ada 2 bentuk flavonoid, yaitu flavonoid yang terikat pada gula sebagai glikosida dan flavonoid bebas (aglikon). Bentuk-bentuk ini dapat berada pada satu tumbuhan dalam beberapa bentuk kombinasi glikosida (Harborne 1996). Metode yang biasa digunakan untuk analisis kualitatif dan kuantitatif flavonoid adalah kromatografi cair kinerja tinggi. Metode ini cukup baik untuk proses kuantitasi, tetapi sering kali penerapannya terhambat oleh keterbatasan standar autentik 3 yang tersedia. Oleh sebab itu, untuk proses analisis rutin, metode kolorimetri lebih sering digunakan. Penentuan flavonoid total berdasarkan parameter standar umum ekstrak tumbuhan obat Departemen Kesehatan Republik Indonesia (Depkes RI 2000) dilakukan dengan metode kolorimetri aluminium klorida. Metode ini melibatkan pembentukan kompleks antara flavonoid dan AlCl3. AlCl3 membentuk kompleks yang stabil dengan gugus keto C4 dan gugus hidroksil dari C3 atau C5 pada flavon dan flavonol. Banyaknya kompleks yang terbentuk diketahui dari hasil pengukuran spektrofotometer UV-Vis. Hukum Lambert-Beer menyatakan perbandingan lurus antara absorbans dan kadar analit. Ekstraksi Ekstraksi adalah peristiwa pemindahan zat terlarut di antara dua pelarut yang tidak saling campur. Zat terlarut akan tersebar pada kedua fase pelarut sehingga nisbah konsentrasinya pada suhu tertentu merupakan suatu tetapan kesetimbangan (konstanta distribusi/Kd). Secara sederhana ekstraksi merupakan istilah yang digunakan untuk setiap proses yang didalamnya komponen-komponen pembentuk suatu bahan berpindah dari bahan ke cairan (pelarut). Metode sederhana ekstraksi adalah dengan mencampurkan seluruh bahan dengan pelarut, lalu memisahkan larutan dengan padatan tidak terlarut. Faktor penting dalam ekstraksi adalah pemilihan pelarut. Pelarut yang digunakan dalam ekstraksi harus dapat menarik komponen aktif dalam campuran. Hal-hal penting yang harus diperhatikan dalam pemilihan pelarut adalah selektivitas, sifat pelarut, kemampuan untuk mengekstraksi, tidak bersifat racun, kemudahan untuk diuapkan, dan harganya yang relatif murah (Gamse 2002). Perlakuan pendahuluan sebelum ekstraksi bergantung pada sifat senyawa dalam bahan yang akan diekstraksi (Robinson 1995). Perlakuan pendahuluan untuk bahan padat dapat dilakukan dengan beberapa cara di antaranya dengan pengeringan bahan baku sampai kadar air tertentu dan penggilingan untuk mempermudah proses ekstraksi dengan memperbesar kontak antara bahan dan pelarut (Harborne 1996). Perendaman bahan dapat menaikkan permeabilitas dinding sel melalui tiga tahapan: (1) masuknya pelarut ke dalam dinding sel tanaman dan membengkakkan sel; (2) senyawa yang terdapat pada dinding sel tanaman akan lepas dan masuk ke dalam pelarut; (3) difusi senyawa yang terekstraksi oleh pelarut keluar dari dinding sel tanaman. Proses ekstraksi padat-cair dipengaruhi oleh banyak faktor, di antaranya lamanya ekstraksi, suhu yang digunakan, pengadukan, dan banyaknya pelarut yang digunakan (Harborne 1996). Ada beberapa teknik ekstraksi, yaitu maserasi, perkolasi, refluks, dan soxhlet. Pemilihan teknik ekstraksi untuk mengekstraksi suatu bahan tumbuhan bergantung pada tekstur, kandungan air, bahan tumbuhan, dan jenis senyawa yang akan diisolasi. Teknik ekstraksi yang dilakukan pada penelitian ini adalah refluks yang diawali dengan maserasi. Maserasi merupakan proses ekstraksi dengan cara merendam contoh dalam pelarut yang sesuai pada waktu tertentu, tanpa adanya tambahan energi panas. Refluks merupakan proses ekstraksi dengan cara mendidihkan campuran antara contoh dan pelarut yang sesuai pada suhu dan waktu tertentu, dan mengembunkan kembali uap yang terbentuk dalam kondensor agar kembali ke labu reaksi, sehingga volume campuran tetap. Teknik ini dapat digunakan untuk kepentingan preparatif, pemurnian, pemisahan, dan analisis pada semua skala kerja, baik analisis dalam skala industri maupun skala laboratorium. Rancangan Fraksional Faktorial Rancangan faktorial digunakan dalam melakukan suatu percobaan untuk melihat pengaruh dari 2 faktor atau lebih terhadap hasil yang diperoleh. Setiap perlakuan dalam rancangan faktorial merupakan kombinasi perlakuan yang mungkin untuk setiap taraf dalam faktor yang dicoba. Dalam rancangan faktorial lengkap, perlakuannya terdiri atas semua kemungkinan kombinasi taraf dari beberapa faktor yang dicobakan (Montgomery 2001). Pengurangan kombinasi perlakuan dapat dilakukan dengan rancangan fraksional faktorial, yaitu jumlah kombinasi perlakuan yang akan dicobakan diminimumkan dengan tidak menghilangkan informasi tentang pengaruh utama dan interaksi tingkat rendah yang merupakan informasi penting dalam percobaan. Salah satu contohnya adalah rancangan fraksional faktorial tingkat 1/3 4 untuk 3 taraf pada masing-masing faktor. Rancangan ini dapat mereduksi jumlah perlakuan hingga menjadi sepertiga dari jumlah perlakuan pada rancangan faktorial lengkap. Apabila rancangan faktorial lengkap menghasilkan 3k perlakuan, maka dengan rancangan ini, perlakuan dapat direduksi menjadi 3k-1 (Lundstedt et al.1998). Optimisasi Ekstraksi Optimisasi bertujuan menemukan nilai peubah dalam proses yang menghasilkan nilai terbaik pada syarat-syarat kondisi yang digunakan. Penyelesaian optimisasi terfokus pada pemilihan peubah terbaik di antara keseluruhan dan proses metode kuantitatif yang efisien termasuk komputer serta perangkat lunak program komputasi yang tepat dan hemat biaya. Konsep desain optimisasi adalah memperlihatkan semua kemungkinan analisis percobaan. Metamodel Permukaan Respons (RSM) merupakan salah satu metode yang cukup menjanjikan dalam optimisasi ini. RSM merupakan cara yang efektif untuk melihat sistem respons ketika taraf dari faktor-faktor yang terlibat berubah (Harvey 2000). Metode ini telah dikenal dalam kimia dan teknik industri. RSM dapat memberikan hasil yang memuaskan untuk memilih data berdasarkan metode regresi standar berupa model polinomial dengan memberikan masukan untuk mendapatkan luaran yang diinginkan. Model matematis dari suatu permukaan respons dapat berupa model teoretis atau empiris. Model teoretis hanya dapat digunakan jika hubungan fisik dan kimia antara respons dan faktor diketahui dengan pasti. Hubungan ini sering kali tidak diketahui, sehingga yang sering digunakan adalah model empiris. Pembuatan model empiris untuk suatu permukaan respons dapat dilakukan dengan mengumpulkan data dari suatu rancangan percobaan (Harvey 2000). Faktor penting dalam metode permukaan respons adalah pembuatan model regresi yang menghubungkan respons dengan peubahpeubah bebas, sehingga akan diperoleh model sebagai fungsi respons terhadap peubahpeubah yang berpengaruh signifikan terhadap respons tersebut. BAHAN DAN METODE Bahan dan Alat Bahan-bahan yang digunakan adalah daun jati belanda yang berumur 2 bulan dan berasal dari kebun percobaan Cikabayan dan standar kuersetin. Alat-alat yang digunakan adalah perangkat refluks, spektrofotometer UV-Vis Shimadzu 1700, dan perangkat lunak SAS 9.1 serta Minitab 14. Metode Penelitian Penelitian ini dilakukan dalam beberapa tahap, yaitu penyiapan contoh, perlakuan pendahuluan, ekstraksi, penentuan kadar flavonoid total contoh, dan penentuan kondisi optimum. Diagram alir penelitian disajikan dalam Lampiran 1. Penyiapan Bahan Baku Contoh daun jati belanda dikeringkan dalam oven pada suhu 60 °C kemudian digiling dan dihomogenkan ukurannya sehingga diperoleh serbuk daun jati belanda dengan ukuran 300 mesh. Perlakuan Pendahuluan Penentuan kadar air contoh sebelum ekstraksi dilakukan berdasarkan ketentuan Departemen Kesehatan RI 1995. Cawan porselen dikeringkan pada suhu 105 ºC selama 30 menit, kemudian didinginkan dalam eksikator dan ditimbang bobot keringnya. Contoh daun jati belanda sebanyak ± 1 g dimasukkan ke dalamnya lalu dikeringkan lagi dalam oven 105 ºC selama 3 jam, didinginkan dalam eksikator, dan ditimbang. Prosedur ini dilakukan berulang-ulang sampai diperoleh kadar air yang tetap. Kadar air diperoleh dengan persamaan Kadar air = (X − Y) × 100% X X adalah bobot contoh awal dan Y adalah bobot contoh setelah pengeringan. Uji Fitokimia Uji Alkaloid. Sebanyak 1 g contoh dilarutkan dalam 10 ml kloroform dan beberapa tetes NH4OH, kemudian disaring dan filtratnya dimasukkan ke dalam tabung reaksi bertutup. Ekstrak kloroform dalam tabung reaksi dikocok dengan 10 tetes H2SO4 2 M dan lapisan asamnya dipisahkan dalam 5 tabung reaksi yang lain. Lapisan asam ini diteteskan pada lempeng tetes dan ditambahkan pereaksi Mayer, Wagner, dan Dragendorf yang akan menimbulkan endapan warna berturut-turut putih, cokelat, dan merah jingga. Uji Triterpenoid dan Steroid. Sebanyak 1 g contoh dilarutkan dalam 25 ml etanol panas (50 ºC) kemudian larutan disaring ke dalam pinggan porselen dan diuapkan sampai kering. Residu ditambahkan eter, lalu ekstrak eter dipindahkan ke dalam lempeng tetes dan ditambahkan 3 tetes anhidrida asam asetat dan 1 tetes H2SO4 pekat (uji LiebermannBuchard). Warna merah atau ungu menunjukkan adanya triterpenoid dan warna hijau atau biru menunjukkan adanya steroid. Uji Saponin dan Flavonoid. Sebanyak 1 g contoh dimasukkan ke dalam gelas piala kemudian ditambahkan 100 ml air panas dan dididihkan selama 5 menit. Setelah itu, larutan disaring dan filtratnya digunakan untuk pengujian. Uji saponin dilakukan dengan mengocok 10 ml filtrat dalam tabung reaksi tertutup selama 10 detik kemudian dibiarkan selama 10 menit. Adanya saponin ditunjukkan dengan terbentuknya buih yang stabil. Sebanyak 10 ml filtrat yang lain ditambahkan 0,5 gram serbuk Mg, 2 ml alkohol klorhidrat (1 ml HCl 37% dan 1 ml etanol 95%), dan amil alkohol. Terbentuknya warna merah, kuning, dan jingga pada lapisan amil alkohol menunjukkan adanya flavonoid. Ekstraksi Flavonoid (Depkes RI 2000) Sebanyak 25 g serbuk daun jati belanda dimaserasi selama 24 jam dengan etanol teknis dalam labu bulat 1000ml, sambil sesekali dikocok. Maserat dalam labu lalu direfluks. Refluks diulangi 1 kali lagi dan seluruh hasil refluks digabungkan. Ekstraksi dilakukan dengan meragamkan 3 peubah, yaitu konsentrasi etanol (50%, 70%, dan 90%), waktu (3, 5, dan 7 jam), dan nisbah bahan baku (g) per ml pelarut (1:5, 1:10, dan 1:15). Ekstrak dipekatkan dengan penguap putar dan ditimbang untuk menentukan rendemennya. Selanjutnya dianalisis kandungan flavonoid total dengan cara mengukur serapannya menggunakan spektrofotometer UV-Vis pada panjang gelombang 366,4 nm. Analisis Kuantitatif Flavonoid Total (Depkes RI 2000) Standar kuersetin 50 μg/ml diencerkan dengan asam asetat glasial 5% v/v (dalam metanol) hingga diperoleh konsentrasi 3,0; 6,0; 12,0; 15,0; dan 24,0 μg/ml. Setelah itu serapan diukur menggunakan spektrofotometer pada panjang gelombang 366,4 nm, untuk membuat kurva standar. Ekstrak ditimbang setara dengan 200 mg simplisia lalu dimasukkan ke dalam labu alas bulat. Sistem hidrolisis ditambahkan ke dalamnya, yaitu 1 ml larutan 0,5% (b/v) heksametilenatetramina, 20 ml aseton, dan 2 ml larutan 25% HCl dalam air, lalu campuran dipanaskan sampai mendidih selama 30 menit. Campuran hasil hidrolisis lalu disaring menggunakan kapas ke dalam labu ukur 100 ml. Residu kemudian ditambah 20 ml aseton untuk dididihkan kembali sebentar; penambahan aseton dan pendidihan ini dilakukan sebanyak 2 kali. Seluruh filtrat dikumpulkan ke dalam labu takar. Setelah labu takar dingin, volume ditepatkan dengan aseton sampai 100 ml dan dikocok hingga tercampur sempurna. Filtrat hasil hidrolisis dalam labu takar diambil sebanyak 20 ml, dimasukkan ke dalam corong pisah, dan ditambahkan 20 ml akuades. Selanjutnya campuran diekstraksi, pertama dengan 15 ml etil asetat, kemudian 2 kali dengan 10 ml etil asetat. Fraksi etil asetat dikumpulkan ke dalam labu takar 50 ml dan ditambahkan etil asetat sampai tepat 50 ml. Sebanyak 10 ml larutan ini dipindahkan ke dalam labu takar 25 ml, kemudian ditambahkan 1 ml larutan 2 g AlCl3 dalam 100 ml larutan asam asetat glasial 5% (v/v) (dalam metanol). Larutan asam asetat glasial 5% (v/v) ditambahkan secukupnya sampai tepat 25 ml. Selanjutnya larutan dikocok dan diukur serapannya pada panjang gelombang 366,4 nm. Rancangan Penelitian Penelitian ini didesain menggunakan rancangan fraksional faktorial 33-1, sehingga hanya 9 perlakuan yang dilakukan. Kombinasi perlakuan dibentuk dengan bantuan perangkat lunak SAS 9.1. Pengolahan Data Pengolahan data yang dihasilkan dilakukan dengan perangkat lunak SAS 9.1 dan Minitab 14. Pengolahan data dilakukan dengan cara membuat model regresi yang baik kemudian kondisi optimum ekstraksi 6 ditentukan dengan melihat juga kebaikan dari model yang dibuat. HASIL DAN PEMBAHASAN Ciri Fitokimia Contoh yang kadar airnya besar akan mudah rusak sehingga dalam penyimpanannya diperlukan perlakuan khusus. Karena itu, contoh daun jati belanda dalam penelitian ini dikeringkan pada suhu 60 °C. Selanjutnya contoh daun kering digiling dan dihomogenkan ukurannya hingga diperoleh serbuk berukuran 300 mesh. Hal ini bertujuan memperluas permukaan bahan sehingga pada tahap ekstraksi, interaksi antara pelarut pengekstraksi dan bahan yang diekstraksi menjadi lebih efektif. Kadar airnya ditetapkan dengan gravimetri evolusi tidak langsung, yaitu dengan menghitung bobot bahan sebelum dan sesudah dikeringkan pada suhu di atas titik didih air selama periode waktu tertentu (Harjadi 1986). Penentuan kadar air berguna untuk mengetahui ketahanan suatu bahan yang akan disimpan dalam selang waktu yang cukup lama, karena kandungan air di dalam suatu bahan merupakan medium tumbuh bagi bakteri dan mikroorganisme. Hal ini berkaitan dengan kelembapan bahan tersebut. Kadar air contoh diperoleh sebesar 6.89% (Lampiran 3), cukup rendah untuk dapat disimpan dalam jangka waktu yang lama. Hal ini sesuai dengan monografi ekstrak BPOM (2004) yang menyatakan bahwa untuk daun jati belanda nilai kadar air yang baik adalah tidak lebih besar dari 9.3%. Selain itu, menurut Winarno (1997), bila kadar air bahan berkisar antara 3 dan 7%, maka kestabilan optimum bahan akan tercapai dan pertumbuhan mikrob dapat dikurangi. Kadar air juga berguna untuk menentukan kadar zat aktif berdasarkan bobot keringnya, karena jumlah air yang terkandung bergantung pada perlakuan yang telah dialami bahan dan kelembapan udara tempat penyimpanan. Bahan yang sama jika dianalisis pada waktu yang sama dapat menghasilkan kadar zat aktif yang berbeda jika kelembapan bahan tersebut berubah. Tahap selanjutnya dalam penelitian ini adalah uji fitokimia. Uji fitokimia dilakukan untuk menguji keberadaan beberapa komponen aktif seperti alkaloid, flavonoid, steroid, triterpenoid, saponin, dan tanin. Hasilnya ditunjukkan pada Tabel 1, dan memperlihatkan bahwa daun jati belanda mengandung flavonoid yang selanjutnya akan ditentukan kadar totalnya dalam penelitian ini sebagai respons dari beberapa perlakuan kondisi ekstraksi. Tabel 1 Hasil uji fitokimia daun jati belanda Golongan senyawa aktif Hasil Uji Alkaloid Flavonoid Steroid Triterpenoid Saponin Tanin +++ + + + ++ Ket: + – = contoh mengandung senyawa aktif = contoh tidak mengandung senyawa aktif Hasil Rancangan Fraksional Faktorial Dalam penelitian ini terdapat 3 faktor yang diragamkan, yaitu konsentrasi pelarut, waktu ekstraksi, dan nisbah bobot bahan baku terhadap volume pelarut. setiap faktor tersebut memiliki 3 taraf sehingga terdapat 33 (27) kombinasi perlakuan yang seharusnya dicobakan, tetapi karena dalam penelitian ini digunakan rancangan fraksional faktorial 1/3, hanya 33-1 (9) kombinasi perlakuan yang dicobakan. Rancangan fraksional faktorial 1/3 dimaksudkan untuk mereduksi jumlah perlakuan yang akan dicobakan tanpa banyak menghilangkan informasi penting. Pemilihan kombinasi perlakuan dilakukan dengan menggunakan perangkat lunak SAS 9.1 dan dihasilkan luaran berupa kombinasi perlakuan yang dilakukan seperti tercantum pada Lampiran 4. Kombinasi perlakuan yang akan dicobakan selengkapnya dapat dilihat pada Tabel 2. Tabel 2 Kombinasi perlakuan yang dicobakan dari hasil fraksionalisasi No. Waktu Konsentrasi Nisbah Percobaan (jam) Pelarut (%) 1 3 50 1:5 2 3 70 1:15 3 3 90 1:10 4 5 50 1:15 5 5 70 1:10 6 5 90 1:5 7 7 50 1:10 8 7 70 1:5 9 7 90 1:15 7 standar kuersetin dengan berbagai konsentrasi diukur pada panjang gelombang 370,8 nm dengan spektrofotometer. Namun, dalam penelitian ini pengukuran dilakukan pada 366,4 nm, karena setelah dilakukan pemayaran pada panjang gelombang 200–400 nm diperoleh serapan maksimum pada panjang gelombang tersebut. Pergeseran panjang gelombang maksimum ini dapat disebabkan oleh perbedaan kondisi dan alat yang digunakan. Data absorbans untuk pembuatan kurva standar diberikan pada Lampiran 6. Kurva standar yang diperoleh memiliki persamaan garis y = 0.0329x – 0.0121 dengan R2 = 0.9998 (Gambar 3), yang menunjukkan bahwa konsentrasi mampu menerangkan keragaman absorbans sebesar 99.98%, dan hanya sekitar 0.02% yang diterangkan oleh faktor lain. Metode ekstraksi flavonoid daun jati belanda yang digunakan dalam penelitian ini adalah refluks yang didahului dengan proses maserasi. Proses maserasi dilakukan untuk mengekstraksi flavonoid yang berada di luar sel. Karena yang akan dioptimumkan dalam penelitian ini adalah kadar flavonoid total, ekstraksi daun jati belanda dilanjutkan dengan proses refluks. Bantuan energi berupa panas akan membantu proses pemecahan dinding sel sehingga flavonoid intra sel dapat terekstraksi. Ekstraksi flavonoid total dari daun jati belanda dilakukan dengan pelarut etanol, karena sifatnya yang semipolar memungkinkan seluruh jenis flavonoid ikut terekstraksi. Selain itu, Departemen Kesehatan RI hanya mengizinkan etanol dan air sebagai pelarut obat. Etanol juga memiliki daya absorpsi yang lebih baik jika dibandingkan dengan air. HCl juga ditambahkan dalam proses analisis kunatitatifnya untuk menghidrolisis ikatan glikosida yang terdapat pada flavonoid sehingga diharapkan flavonoid bebas yang terekstraksi. Ekstraksi dilakukan dengan meragamkan 3 faktor dan pada masing-masing faktor terdapat 3 taraf, yaitu waktu ekstraksi (3, 5, dan 7 jam), konsentrasi pelarut (50, 70, dan 90%), dan nisbah bahan baku(g)-pelarut (ml) (1:5, 1:10, dan 1:15). Pemilihan waktu 3, 5, dan 7 jam didasarkan pada penelitian Xu et al. (2005) yang menunjukkan bahwa kadar flavonoid akan terus meningkat pada waktu ekstraksi 2– 3 jam, dan mencapai optimum pada selang waktu ekstraksi 3–7 jam. Pemilihan konsentrasi pelarut 50, 70, dan 90% juga didasarkan pada penelitian tersebut yang menunjukkan bahwa kadar flavonoid yang diperoleh cukup tinggi saat diekstraksi dengan etanol yang selang konsentrasinya 50–90%. Demikian pula halnya dengan nisbah bahan baku-pelarut. Rendemen yang diperoleh berkisar antara 7,88 dan 16,09%. Data rendemen selengkapnya dapat dilihat pada Lampiran 5. Kurva Standar Flavonoid dan Kadar Contoh Pembuatan kurva standar flavonoid didasarkan pada metode AlCl3 (Depkes RI 2000). Sebagai standar digunakan kuersetin, suatu senyawa penciri flavonoid yang telah umum digunakan. Menurut metode ini, larutan absorbans Kondisi Ekstraksi 0,9 0,8 0,7 0,6 0,5 0,4 0,3 0,2 0,1 0 y = 0,0329x - 0,0121 R2 = 0,9998 0 5 10 15 20 25 30 konsentrasi (ppm) Gambar 3 Kurva standar flavonoid total. Berdasarkan kurva standar, dapat ditentukan kadar flavonoid total dari contoh sesuai perlakuan yang dicobakan. Hasil selengkapnya disajikan dalam Lampiran 7. Model dan Analisis Regresi Penelitian ini dilakukan dengan 2 kali ulangan, dan data yang diolah adalah data ulangan pertama, karena berdasarkan uji keragaman (Lampiran 8) didapatkan keragaman Δ kadar kedua ulangan sama dengan 1. Hal ini menunjukkan bahwa selisih antara ulangan 1 dan 2 relatif kecil. Analisis yang digunakan adalah analisis respons yang menggunakan pendekatan regresi. Pembuatan model regresi dilakukan sampai diperoleh model dengan R2 yang tinggi dan parameter yang terlibat berpengaruh signifikan terhadap kadar. Dari hasil pemodelan regresi diperoleh model regresi dengan R2 = 99.67%, yaitu 8 Kadar = -1.20208 – 0.06167 (waktu) + 0.00125 (waktu)2 + 0.04208 (konsentrasi) – 0.0003 (konsentrasi)2 + 0.04383 (nisbah) – 0.0034 (nisbah)2 + 0.00650 (nisbah*waktu) Berdasarkan model tersebut dan pengujian parameter (Lampiran 9) pada α = 7% dapat diketahui bahwa faktor yang berpengaruh signifikan terhadap kadar flavonoid adalah konsentrasi pelarut dan nisbah bahan bakupelarut. Kedua faktor tersebut berpengaruh secara kuadratik. Hal ini terlihat dari nilai-p yang lebih kecil daripada α = 0.07. Secara statistik faktor waktu tidak berpengaruh signifikan terhadap kadar pada α = 7%. Hal ini dapat terjadi karena waktu yang diragamkan adalah waktu yang digunakan dalam proses refluks, sedangkan pada metode yang digunakan dalam penelitian ini ekstraksi flavonoid didahului oleh maserasi selama 24 jam. Diduga selama proses maserasi tersebut telah banyak flavonoid yang terekstraksi, karena flavonoid lebih banyak terdapat di luar sel tanaman. Akibatnya, meskipun ada perbedaan kadar (semakin lama waktu ekstraksi kadar flavonoid semakin meningkat) seperti terlihat pada Gambar 4, setelah dibandingkan nilai tengah dari masing-masing kadar, selisih yang terjadi relatif kecil, atau hasilnya tidak berbeda nyata secara statistika. Nisbah 0,36 Tabel 3 Perbandingan kadar flavonoid total hasil percobaan dengan dugaan No. Kadar Kadar Kadar dugaan perc percobaan dugaan pada selang (%) (%) kepercayaan 93% 1 0.21 0.21 0.0991–0.3209 2 0.29 0.28 0.1837–0.3863 3 0.27 0.27 0.1737–0.3763 4 0.25 0.25 0.1537–0.3563 5 0.42 0.42 0.3091–0.5309 6 0.18 0.17 0.0737–0.2763 7 0.34 0.33 0.2337–0.4363 8 0.26 0.26 0.1637–0.3663 9 0.36 0.36 0.2491–0.4709 Berdasarkan Tabel 3 dapat dilihat bahwa secara umum nilai kadar dugaan sama dengan nilai kadar percobaan. Hal ini menunjukkan bahwa model yang digunakan mempunyai keakuratan yang baik. Galatnya hanya 0.33%. Tabel 4 [etanol] 0,32 Waktu (jam) 0,28 0,24 kadar Manfaat lain dari model persamaan kadar yang dihasilkan adalah dapat dilakukan pendugaan kadar flavonoid total untuk kombinasi perlakuan yang dicobakan. Perbandingan kadar hasil percobaan dengan dugaan disajikan dalam Tabel 3. 0,20 5 10 15 50 70 90 Waktu 0,36 0,32 0,28 0,24 0,20 3 Gambar 4 5 7 Kurva hubungan antara nisbah, konsentrasi, dan waktu terhadap kadar flavonoid total. Berdasarkan Gambar 4 dapat dilihat bahwa kadar flavonoid total tertinggi dihasilkan pada nisbah bahan baku-pelarut 1:10, karena pada nisbah bahan baku-pelarut 1:5 jumlah bahan yang digunakan lebih banyak sedang pengekstraknya sedikit sehingga tidak mencukupi untuk mengekstrak seluruh flavonoid yang ada, dan untuk nisbah bahan baku-pelarut 1:15 jumlah pengekstraknya terlalu banyak. Selain itu juga dapat dilihat bahwa kadar tertinggi dihasilkan saat digunakan pelarut etanol teknis dengan konsentrasi 70%. 3 3 3 3 3 3 5 5 5 5 5 5 7 7 7 7 7 7 Hasil pendugaan kadar flavonoid total untuk kombinasi perlakuan yang tidak dicobakan Konsentrasi Nisbah Kadar pelarut (%) dugaan (%) 50 10 0.27 50 15 0.16 70 5 0.33 70 10 0.39 90 5 0.21 90 15 0.17 50 5 0.17 50 10 0.30 70 5 0.29 70 15 0.38 90 10 0.30 90 15 0.26 50 5 0.14 50 15 0.36 70 10 0.46 70 15 0.49 90 5 0.15 90 10 0.34 Model ini juga dapat digunakan untuk menduga kadar pada kombinasi perlakuan yang tidak dicobakan. Tabel 4 menunjukkan 9 90 hasil dugaan kadar untuk kombinasi perlakuan yang tidak dicobakan. kadar < > 0,20 0,25 0,30 0,35 [etanol] 80 Kadar Flavonoid Total Optimum Analisis kadar flavonoid total daun jati belanda dilakukan dengan metode kolorimetri yang didasarkan pada reaksi pembentukan kompleks antara flavonoid dan aluminium klorida yang diukur dengan spektrofotometer UV-Vis berkas ganda. Kadar flavonoid total ekstrak daun jati belanda dapat diketahui dengan memasukkan data absorbans yang diperoleh ke persamaan kurva standar yang telah dihasilkan. Parameter kondisi ekstraksi yang dioptimisasi dalam percobaan ini adalah waktu ekstraksi, konsentrasi pelarut, dan nisbah bahan baku-pelarut. Optimisasi tersebut menggunakan perangkat lunak SAS 9.1 dan Minitab 14. Dalam hal ini akan terlihat pengaruh faktor-faktor tersebut terhadap kadar flavonoid total, tetapi karena faktor waktu tidak berpengaruh signifikan secara statistik maka yang terlihat pada kurva permukaan respons kadar adalah pengaruh faktor konsentrasi pelarut dan nisbah bahan baku-pelarut. Hal ini dapat dilihat pada Gambar 5 berikut. Titik optimum 0,4 kadar 1 0,20 0,25 0,30 0,35 0,40 0,40 70 60 50 5,0 7,5 10,0 Nisbah 12,5 15,0 Gambar 6 Peta kontur kadar terhadap konsentrasi pelarut dan nisbah bahan baku-pelarut. Gambar 6 menunjukkan peta kontur yang dapat mempertegas daerah optimum yang dihasilkan. Gambar 5 dan 6 menunjukkan bahwa kondisi optimum ekstraksi teramati pada konsentrasi pelarut 70%, nisbah bahan baku-pelarut 1:10, dan waktu ekstraksi 3 jam dengan kadarnya adalah 0.42%. Kondisi tersebut ada pada kisaran yang dicobakan. SIMPULAN DAN SARAN Simpulan Konsentrasi pelarut dan nisbah bahan baku pelarut berpengaruh nyata terhadap kadar flavonoid total yang dihasilkan, sedangkan waktu ekstraksi tidak. Kondisi optimum untuk ekstraksi flavonoid total dari daun jati belanda yang diperoleh pada penelitian ini adalah konsentrasi pelarut 70%, nisbah bahan bakupelarut 1:10, dan waktu ekstraksi 3 jam. 0,3 90 0,2 75 5 10 Nisbah 60 Saran [etanol] 15 Gambar 5 Kurva permukaan respons kadar terhadap konsentrasi pelarut dan nisbah bahan baku-pelarut. Gambar 5 menunjukkan permukaan respons dari masing-masing faktor terhadap kadar total flavonoid yang dihasilkan. Dari gambar tersebut dapat dilihat bahwa model penentuan kadar yang diperoleh dalam penelitian ini dapat digunakan untuk ragam taraf dari tiap faktor yang masih tercakup dalam permukaan yang dihasilkan. Perlu dilakukan validasi terhadap model yang telah diperoleh pada penelitian ini. Selain itu perlu dicobakan penelitian lanjutan dengan memperluas kisaran taraf yang lebih luas untuk parameter yang digunakan. DAFTAR PUSTAKA [BPOM RI] Badan Pengawas Obat dan Makanan Republik Indonesia. 2004. Monografi Ekstrak Tumbuhan Obat Indonesia Volume 1. Jakarta: BPOM RI. 10 Day RA, Underwood AL. 1998. Analisis Kimia Kuantitatif. Sopyan I, penerjemah; Jakarta: Penerbit Erlangga. Terjemahan dari: Quantitative Analysis. [Depkes RI] Departemen Kesehatan Republik Indonesia. 2000. Petunjuk Operasional Penerapan CPOB. Ed ke-2. Jakarta: Depkes. [Depkes RI] Departemen Kesehatan Republik Indonesia. 1995. Farmakope Indonesia. Ed ke-5. Jakarta: Depkes. Gamse T. 2002. Liquid-Liquid Extraction and Solid-Liquid Extraction. Graz University of Technology. Harborne JB. 1996. Metode Fitokimia. Ed ke-2. Padmawinata K, Soediro I, penerjemah. Bandung: Penerbit ITB. Terjemahan dari: Phytochemical Methods. Harjadi W. 1886. Ilmu Kimia Analitik Dasar. Jakarta: PT Gramedia Pustaka Umum. Harvey D. 2000. Modern Analytical Chemistry. New York: McGraw Hill. Markham KR. 1988. Techniques of Flavonoid Identification. London: Academic Pr. Montgomery DC. 2001. Design and Analysis of Experimental Ed ke-5. New York: J Wiley. Robinson T. 1995. Kandungan Organik Tumbuhan Tinggi. Bandung: Institut Teknologi Bandung. Walpole RE. 1995. Pengantar Statistika Ed ke-3. Sumantri B, penerjemah; Sidhi IP, editor. Jakarta: PT Gramedia Pustaka Utama. Winarno FG. 1997. Kimia Pangan dan Gizi. Jakarta: PT Gramedia Pustaka Utama. Xu Y, Zhang R, Fu H. 2005. Studies on the optimal process to extract flavonoids from red-raspberry fruits. J Nat Sci 3:43-46 11 LAMPIRAN 12 Lampiran 1 Diagram alir penelitian Simplisia daun Jati Belanda Uji Pendahuluan Uji Fitokimia Kadar Air Ekstraksi Ragam Ragam Waktu Konsentrasi pelarut Refluks Penentuan Kadar Flavonoid Total Optimisasi Kondisi Optimum Rancangan Percobaan Ragam Nisbah bahan bakupelarut Fraksionalisasi 13 Lampiran 2 Ekstraksi flavonoid Serbuk daun jati belanda + etanol maserasi 24 jam maserat Filtrat direfluks dengan berbagai ragam waktu Filtrat residu Filtrat direfluks dengan berbagai ragam waktu residu digabung dipekatkan dengan penguap putar ekstrak pekat analisis flavonoid secara kuantitatif dibuang 14 Lampiran 3 Hasil penentuan kadar air Ulangan Bobot Contoh Awal (a) (g) Bobot Contoh Kering (b) (g) Kadar Air (%) 1 1,0023 0,9334 6,87 2 1,0033 0,9346 6,85 3 1,0046 0,9347 6,96 Rerata 6,89 Contoh perhitungan • Penentuan kadar air ulangan 1 Kadar air = a -b × 100% a Kadar air = 1,0023 - 0,9334 × 100% 1,0023 Kadar air = 6,87% • Penentuan kadar air rerata ulangan 1 + ulangan 2 + ulangan 3 Kadar air rerata = 3 Kadar air rerata = 6,87% + 6,85% + 6,96% = 6,89% 3 15 Lampiran 4 Kombinasi perlakuan berdasarkan pengacakan dengan SAS 9.1 The FACTEX Procedure Design Points Experiment Number konsentrasi waktu nisbah ƒƒƒƒƒƒƒƒƒƒƒƒƒƒƒƒƒƒƒƒƒƒƒƒƒƒƒƒƒƒƒƒƒƒƒƒƒƒƒƒ 1 -1 -1 -1 2 -1 0 1 3 -1 1 0 4 0 -1 1 5 0 0 0 6 0 1 -1 7 1 -1 0 8 1 0 -1 9 1 1 1 The FACTEX Procedure Factor Confounding Rules nisbah = (2*konsentrasi)+(2*waktu) The FACTEX Procedure Aliasing Structure konsentrasi = (2*waktu)+(2*nisbah) (2*konsentrasi) = waktu+nisbah waktu = (2*konsentrasi)+(2*nisbah) (2*waktu) = konsentrasi+nisbah nisbah = (2*konsentrasi)+(2*waktu) (2*nisbah) = konsentrasi+waktu (2*konsentrasi)+ waktu = konsentrasi+(2*nisbah) = (2*waktu)+nisbah konsentrasi +(2*waktu) = (2*konsentrasi)+nisbah = waktu+(2*nisbah) 16 Lampiran 5 Rendemen ekstrak daun jati belanda dari perlakuan yang dicobakan Waktu Konsentrasi Nisbah Rendemen (jam) Pelarut (%) c (g) b (g) (%) a (g) 3 50 1:5 25,0024 37,3914 41,1075 14,86 3 70 1:15 25,0033 37,1590 40,0386 11,52 3 90 1:10 25,0060 37,6764 40,0421 9,46 5 50 1:15 25,0048 36,9019 40,7805 15,51 5 70 1:10 25,0086 38,2348 41,0736 11,35 5 90 1:5 25,0073 37,2697 39,2396 7,88 7 50 1:10 25,0007 36,6797 40,7035 16,09 7 70 1:5 25,0048 36,1694 38,6245 9,82 7 90 1:15 25,0053 38,7203 41,4780 11,03 Contoh perhitungan: Rendemen = = a -b x 100% c 41,1075 - 37,3914 x 100% 25,0024 = 14,86% Keterangan: a = bobot labu+ekstrak (g) b = bobot labu kosong (g) c = bobot contoh (g) Lampiran 6 Absorbans standar flavonoid total Konsentrasi standar (μg/ml) 3 6 12 15 24 Absorbans 0,091 0,184 0,378 0,478 0,780 17 Lampiran 7 Kadar flavonoid total dari ekstrak daun jati belanda untuk perlakuan yang dicobakan Waktu Konsentrasi Nisbah Ulangan A a (g) b (g) c (g) Kadar (jam) Pelarut (%) (%) 3 50 1:5 1 0,413 3,7161 0,2312 25,0024 0,21 3 50 1:5 2 0,603 5,5330 0,2531 25,0008 0,23 3 70 1:15 1 0,734 2,8796 0,1838 25,0033 0,29 3 70 1:15 2 0,640 6,6088 0,2724 25,0081 0,35 3 90 1:10 1 0,773 2,3657 0,1980 25,0060 0,27 3 90 1:10 2 0,349 4,1590 0,1844 25,0017 0,32 5 50 1:15 1 0,347 3,8786 0,3093 25,0048 0,25 5 50 1:15 2 0,339 7,6076 0,3160 25,0126 0,26 5 70 1:10 1 0,542 2,8388 0,1627 25,0086 0,42 5 70 1:10 2 0,362 5,7702 0,1999 25,0084 0,39 5 90 1:5 1 0,510 1,9699 0,1190 25,0073 0,18 5 90 1:5 2 0,511 3,6035 0,1440 25,0181 0,30 7 50 1:10 1 0,374 4,0238 0,1688 25,0007 0,34 7 50 1:10 2 0,470 6,3546 0,2127 25,0113 0,34 7 70 1:5 1 0,412 2,4551 0,1008 25,0048 0,26 7 70 1:5 2 0,399 2,4152 0,1182 25,0038 0,24 7 90 1:15 1 0,216 2,7577 0,1280 25,0053 0,36 7 90 1:15 2 0,418 4,0424 0,1682 25,0060 0,33 Contoh perhitungan: Kadar flavonoid total untuk waktu 3 jam, konsentrasi pelarut 50%, dan nisbah bahan baku-pelarut 1:5 y = 0.0329x – 0.0121, dengan y = absorbans x = konsentrasi flavonoid total (μg/ml) x = y + 0.0121 0.0329 x = 0,413 + 0,0121 0,0329 x = 12,92 ppm kadar Kadar flavonoid flavonoid total flavonoid total a x fp ppm x 0,01 l x 3,7161 = 0,2312 25,0024 Kadar contoh x b c total = 12,92 Kadar ( μ g/ml) x volume = 2,08 mg/g g g = 0,21 % Keterangan: a = bobot ekstrak yang diperoleh (g) b = bobot ekstrak yang diuji (g) c = bobot contoh awal (g) g x 25 18 Lampiran 8 Uji keragaman dengan menggunakan chi-square untuk Δ kadar Peubah Δ kadar N 9 Mean 0,02 StDev 0,0495 Variance 0,0024 Minimum -0,03 Q1 Median 0,01 Hipotesis: H0 : Keragaman sama dengan 1 H1 : Keragaman lebih besar dari 1 χ2hitung = (N - 1) S σ ( 9 − 1 )( 0 , 0024 ) = 1 = 0,0192 χ20.05 (8) = 15.5073, karena χ2hitung < χ20.05 (8) maka kesimpulannya terima H0 Q3 Maximum 0,12 19 Lampiran 9 Luaran SAS 9.1 dalam pembuatan model kadar flavonoid total The SAS System The REG Procedure Model: MODEL1 Dependent Variable: kadar_1 kadar 1 Number of Observations Read Number of Observations Used 9 9 Analysis of Variance Source Sum of Squares DF Model Error Corrected Total 7 1 8 0.04545 0.00015000 0.04560 Root MSE Dependent Mean Coeff Var Square Mean F Value Pr > F 43.29 0.1165 0.00649 0.00015000 0.01225 0.28667 4.27237 R-Square Adj R-Sq 0.9967 0.9737 Parameter Estimates Variable Label Intercept Waktu waktu2 etanol etanol2 Nisbah nisbah2 wak_nis Intercept Waktu etanol Nisbah DF 1 1 1 1 1 1 1 1 Parameter Estimate -1.20208 -0.06167 0.00125 0.04208 -0.00030000 0.04383 -0.00340 0.00650 Standard Error t Value 0.13063 0.02345 0.00217 0.00429 0.00003062 0.00823 0.00034641 0.00086603 -9.20 -2.63 0.58 9.80 -9.80 5.33 -9.81 7.51 Pr > |t| 0.0689 0.2314 0.6667 0.0647 0.0648 0.1182 0.0646 0.0843 20 Lampiran 10 Luaran SAS 9.1 dalam penentuan titik optimum ekstraksi flavonoid total The SAS System The RSREG Procedure Response Surface for Variable kadar_1: kadar 1 Response Mean Root MSE R-Square Coefficient of Variation Regression Type I Sum of Squares R-Square DF Linear Quadratic Crossproduct Total Model 3 2 2 7 0.016450 0.020500 0.008500 0.045450 Residual Total Error Parameter Intercept Nisbah etanol Waktu Nisbah*Nisbah etanol*Nisbah etanol*etanol Waktu*Nisbah Waktu*etanol Waktu*Waktu 0.286667 0.012247 0.9967 4.2724 DF Estimate 1 1 1 1 1 1 1 1 0 0 -1.162083 0.042833 0.039833 -0.044167 -0.003400 0.000050000 -0.000287 0.006000 0 0 F Value Pr > F 36.56 68.33 28.33 43.29 0.1208 0.0852 0.1317 0.1165 0.3607 0.4496 0.1864 0.9967 DF Sum of Squares Mean Square 1 0.000150 0.000150 Standard Error t Value 0.169009 0.008411 0.005799 0.012500 0.000346 0.000086603 0.000037500 0.001225 . . Pr > |t| -6.88 5.09 6.87 -3.53 -9.81 0.58 -7.67 4.90 . . 0.0919 0.1234 0.0920 0.1756 0.0646 0.6667 0.0826 0.1282 . . actor DF Squares Sum of Mean Square F Value Pr > F Label Nisbah etanol Waktu 4 3 2 0.033367 0.014467 0.009617 0.008342 0.004822 0.004808 55.61 32.15 32.06 0.1002 0.1288 0.1239 Nisbah etanol Waktu 21 The SAS System 20:18 Tuesday, April 10, 2007 The RSREG Procedure Canonical Analysis of Response Surface Factor Critical Value Nisbah etanol Waktu 7.361111 69.915459 0.621075 Label Nisbah etanol Waktu Predicted value at stationary point: 0.374335 Eigenvalues Nisbah Eigenvectors etanol Waktu 0.001748 -0.000287 -0.005148 0.503489 0.000726 0.864002 0.006183 0.999971 -0.004444 0.863980 -0.007580 -0.503470 Stationary point is a saddle point. 99