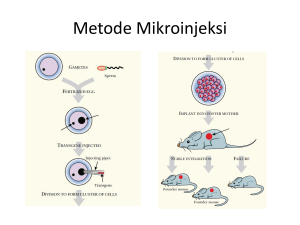
PERKEMBANGAN DAN PENGGUNAAN HEWAN TRANSGENIK
advertisement

PERKEMBANGAN DAN PENGGUNAAN HEWAN TRANSGENIK Perbaikan genetik ternak dan hewan domestik Æ perkawinan + seleksi Æ waktu lama & mahal Perkembangan perbaikan genetik dengan transgenesis Æ lambat Strategi introduksi gen ke kromosom hewan tk tinggi: -Gen diinjeksikan ke inti sel telur yang telah dibuahi -Telur diletakkan di dalam betina reseptif -Beberapa keturunan membawa gen sasaran -Hewan yang membawa gen sasaran di dalam sel nutfah disilangkan untuk mendapat galur baru Transgenesis pada hewan Æ alat: -mempelajari ekspresi gen dan perkembangan -hewan model untuk penyakit manusia -protein farmasetik bagi manusia (susu dari kelenjar susu) Produksi protein melalui kelenjar susu: Æ Melalui air susu, karena: 1. dapat diperbaharui 2. dapat diambil terus tanpa membahayakan hewannya Protein farmasetik yang dihasilkan dalam air susu harus: 1. tidak mempunyai efek sampingan thd proses fisiologi dari hewan transgenik 2. melalui proses pascatranslasi Æ mirip protein manusia 3. mudah melakukan purifikasi Tikus Transgenik -awal perkembangan transgenesis pada hewan -sejak 1980an: 100an gen Æ galur baru Kontribusi: -mengetahui regulasi ekspresi gen, perkembangan sel -mengetahui perkembangan tumor, spesifisitas imunologi -mengetahui proses biologi fundamental -pengujian kelayakan produksi obat terapetik manusia -model penyakit manusia Introduksi DNA sasaran ke dalam sel inang melalui: 1. Vektor retrovirus Æ sel embrio tahap awal Æ betina reseptif 2. Mikroinjeksi ke inti sel sperma yang membesar (pronukleus jantan) dari sel telur yang telah dibuahi 3. Sel batang embrionik Æ embrio stadia awal Æ betina reseptif Metode vektor retrovirus -keuntungan: integrasi transgen ke dalam genom efektif -kerugian: -transgen ukuran kecil (< 8 kb) shg transgen kekurangan regulator ekspresi gen -genom retrovirus dapat melakukan replikasi walaupun menggunakan vektor defektif replikasi Æ secara komersial jarang (tidak) digunakan Metode mikroinjeksi DNA Tahapan: 1. Meningkatkan jumlah telur terbuahi Æ stimulasi superovulasi pada betina donor Cara: serum kuda hamil Æ injeksi Æ 48 jam: chorionic gonad-otropin manusia Æ 35 sel telur (normal: 5-10 sel) 2. Betina tsb x jantan Æ telur diambil dari oviduct 3. Telur diinjeksi (segera) Transgen Æ linier (bebas DNA prokaryot) 4. Telur ditanam di induk betina angkat 5. Identifikasi tikus transgenik Tikus transgenik x WT Æ integrasi transgen? Tikus transgenik (lanjutan) Injeksi sel telur Mamalia: Sperma masuk ke sel telur Æ inti sel sperma (pronukleus jantan) terpisah dari inti sel telur. Setelah inti sel telur selesai meiosis Æ pronukleus betina Æ fusi dengan pronukleus jantan (karyogami). Pronukleus jantan > pronukleus betina Æ injeksi dilakukan pada pronukleus jantan (sel telur dapat difiksasi dan diorientasikan) Penanaman sel telur ke induk betina palsu 25-40 sel telur ditanam di betina angkat (bedah mikro) yang telah dibuat hamil palsu. Hamil palsu: perkawinan dengan jantan mandul (vasektomi) Æ persiapan uterus untuk implantasi 3 minggu Æ lahir anak tikus Identifikasi tikus transgenik DNA (ekor/darah) Æ hibridisasi southern atau PCR Tikus transgenik x WT Æ integrasi transgen? Keturunan x sesamanya Æ homozigot transgenik Efisiensi 66% telur hidup setelah diinjeksi 25% telur yang ditanam berkembang menjadi anak 25% anak yang lahir adalah transgenik Î 1000 telur diinjeksi Æ 30-50 anak transgenik Metode sel batang embrionik yang telah direkayasa Sel dari embrio stadia blastosis Æ proliferasi Æ sel batang embrionik (ESC) ES Æ pluripotent Æ direkayasa tetap pluripotent Transgen diintegrasikan ke genom ES Æ blastosis Æ ditanam Æ transgenik Transfeksi ESC dengan transgen: -sel dengan integrasi transgen pada situs bukan sasaran -sel dengan integrasi transgen pada situs sasaran -sel tidak mengandung transgen Peningkatan jumlah sel dengan situs sesuai sasaran: seleksi positif – negatif Seleksi positif: memilih sel dengan integrasi di sembarang situs Seleksi negatif: membuang sel yang mengandung transgen terintegrasi di sembarang situs Situs sasaran: di daerah yang bukan penyandi (tidak penting) sehingga perkembangan dan fungsi sel tidak terganggu Vektor untuk seleksi positif-negatif 1. 2 blok sekuen DNA (HB1 dan HB2) yang homolog dengan situs sasaran 2. Transgen (TG) Æ fungsi baru untuk resipien 3. Sekuen DNA penyandi resistensi terhadap G418 (NeoR) 4. 2 gen berbeda untuk thymidine kinase (tk1 dan tk2) dari virus simplex herpes tipe I dan II (HSV-tk1 dan HSV-tk2) Di antara HB: transgen dan gen neoR Di luar HB: gen HSV-tk1 dan HSV-tk2 Jika integrasi terjadi pada situs bukan sasaran Æ salah satu atau kedua HSV-tk terintegrasi kedalam genom sel resipien Jika integrasi terjadi pada situs sasaran Æ HSV-tk tidak terintegrasi Sel + G418 Æ sel tanpa neoR Æ mati (sel hidup punya neoR). + gancyclovir Æ sel yang mengekspresikan tk Æ mati (gancyclovir diubah oleh tk menjadi toxinÆ sel mati) Sel + G418 + gancyclovir Æ sel yang mengandung transgen yang terintegrasi pada situs sasaran Seleksi dengan PCR Uji ESC yang mengandung transgen pada situs sasaran Æ PCR ESC transgenik Æ kultur Æ disisipkan kedalam embrio stadia blastosis Æ ditanam pada betina pembawa (hamil palsu) Æ galur transgenik. Homozigot: kawin sesama transgenik Fungsi gen di suatu organisme dapat diganggu melalui penyisipan potongan DNA (biasanya penanda seleksi) ke dalam gen tsb Æ untuk: •mengetahui pengaruh suatu gen terhadap fisiologi dan pertumbuhan organisme ybs •sistem model untuk mempelajari penyakit manusia secara molekuler Inaktivasi gen = gene disruption = gene knockout Inaktivasi fungsi gen Contoh pemanfaatan gene disruption: Gangguan terhadap gen rhodopsin mencit Æ kerusakan rod cells dari retina ~ retinitis pigmentosa pada manusia Æ digunakan mengetahui degenerasi retina & pengaruh agen terapetik 250 mencit yang mengalami gene knockout Æ model untuk kajian berbagai kelainan pada manusia Modifikasi genetik dengan sistem rekombinasi Cre-loxP Sistem rekombinasi cre-loxP Æ gene knockout Cre-loxP dari fage P1 (100 kb) Æ linier-sirkuler genom P1: genom sirkuler Æ replikasi genom viral (siklus lisis), linier (terintegrasi) Æ jarang Rekombinase Cre (circularization recombination): memotong & merekombinasi DNA dari situs loxP (locus of crossing over in P1) Situs loxP: 2 DNA berulang 13 bp yang dipisahkan oleh 8 bp Hasil rekombinasi tergantung orientasi loxP: -berbeda arah: daerah pemisah mengalami inversi -searah: daerah pemisah kedua loxP Æ eksisi (hilang) Cre-loxP Æ berfungsi bila kedua situs loxP berjauhan contoh: mencit yang mempunyai gen yang termodifikasi secara spesifik 1. Tikus transgenik Cre: promoter spesifik sel + gen cre Æ MT1 2. Klon DNA (termasuk smg) (floxed) diapit 2 loxP searah Æ MT2 3. MT1 x MT2 Æ MT3: rekombinasi antara 2 loxP karena ada rekombinase Cre Rekombinasi Cre-loxP Ekson2 diapit loxP searah Æ hilang Æ gen tidak berfungsi Aktivasi gen dengan rekombinasi Cre-loxP Konstruksi floxed mengandung DNA yang mencegah transkripsi Floxed ditempatkan di antara promoter dan gen penyandi Cre Æ rekombinasi di loxP Æ DNA yang mencegah transkripsi Æ eksisi (hilang) Æ gen diekspresikan Transgenesis dengan vektor berkapasitas besar Gen utuh, multigen Æ vektor kapasitas besar Kelompok gen b-globin= 250 kb Antibodi: tetramer: rantai berat (H) dan ringan (L) H: variable (VH), diversity (DH), joining (JH), constant (CH) di sel B L: tipe λ dan κ Æ Vλ & Vκ, Jλ & Jκ, Cλ & Cκ Antibodi H manusia: 95 VH, 30 DH, 6 JH dan 5 C (Cα, Cγ, Cδ, Cε, Cμ) Lokus k: 76 Vκ, 5 Jκ, 1 Cκ H & κ @ 1-1.5 Mb Aplikasi tikus transgenik -model penyakit manusia Æ uji senyawa terapetik misal: Alzheimer, muscular dysthrophy, tumorigenesis, hypertension, neurodegenerative disorder, endocrinological dysfunction, -Uji produksi 1. Model penyakit Alzheimer Penyakit alzheimer: kelainan otak, kehilangan ingatan secara progresif, gangguan bicara, lamban Di dalam neocortex dan hippocampus dari otak pasien alzheimer, serabut neofibril mengakumulasikan di dalam badan neuron senile plaque yang mengandung badan amyloid dan sel-sel otak (neuron) hilang. Protein utama badan amyloid Alzheimer: prot 4 kDa Æ Aβ (β-amyloid, protein β, β−amyloid protein atau β/A4): 39-42 aa (terbanyak: Aβ40 & Aβ42) hasil pemotongan proteolitik β-amyloid precursor protein (APP) Æ disebabkan oleh mutasi pada gen APP (beberapa famili) Model penyakit Alzheimer Promoter dari virus spesifik otak + gen APP penyandi 100 aa terakhir dari ujung C yang mengandung βA4 Æ histokimia: Alzheimer Konstruksi model penyakit Alzheimer di tikus transgenik Alzheimer: APP-177: ValÆPhe; APP-670/671: Lys+Met ÆAsn+Leu promoter platelet-derived growth factor β + APP-cDNA intron Æ tikus mengandung plaque amyloid, kematian sel neuron, kehilangan ingatan APP-670/671 Æ tikus dg penampakan Alzheimer (kelebihan Aβ42) APP-177 Val GUU GUC Phe UUU UUC GUA GUG CUU CUC APP-670/671 Lys AAA AAG Asn AAU AAC Met Leu AUG UUA UUG CUA CUG 2. Model sistem ekspresi/produksi Produksi susu yang mengandung protein dari transgen Studi fungsi CFTR (Cystic Fibrosis Trans-membrane Regulator) dan potensi terapi untuk CF (Cystic Fibrosis): CFTR perlu jumlah banyak CF rusak Æ fungsi CFTR rusak (sebagai kanal klorida) Æ aliran Cl rusak Æ akumulasi lendir di pankreas & paru Lendir: situs infeksi bakteri Æ sulit dikendalikan dengan antibiotik Bakteri mati Æ lendir tebal Æ fungsi organ terganggu: menyumbat saluran Æ memperburuk efek CF (harapan hidup penderita CF: 25 th) Produksi CFTR In vitro, produksi CFTR rendah (akumulasi di membran). Penanggulangan: membran diambil (produksi tinggi, purifikasi mudah) Sel kelenjar susu Æ sekresi lemak yang dibungkus oleh membran plasma (globule dalam susu) cDNA CFTR Æ di tengah gen β-casein yang tidak lengkap dari kambing (delesi dari E2 akhir s/d E7 awal) di bawah kontrol promoter dan terminator β-casein. β-casein diekspresikan di kelenjar susu selama laktasi dan dalam jumlah yang tinggi Tikus transgenik: susu mengandung protein CFTR yang terikat di membran dari globule lemak (tidak ada efek negarif bagi induk & anak). CFTR mengalami glikosilasi dan mudah diekstraksi dari fraksi kaya lemak dari susu. Peningkatan produksi CFTR Æ mamalia besar (sapi, kambing, domba) Pengklonan ternak melalui transfer inti Domba Dolly: inti dari sel mammary Sapi Transgenik Kelenjar susu: bioreaktor Æ sapi sangat berpotensi (10.000 l/th, dengan 35 g protein/l susu) Modifikasi mikroinjeksi pada tikus Penggunaan prosedur tanpa pembedahan dalam implantasi embrio: 2 sapi transgenik dari 2470 oocyte Æ tidak efisien Perbaikan: uji sel embrio Æ embrio transgenik Æ implantasi Salah satu tujuan: mengubah kandungan susu Keju Æ κ-casein Æ over ekpresi transgen κ-casein Ekspresi lactase di kelenjar susu Æ susu bebas laktosa Transgenesis pada sapi Æ lambat (2 th dari telur terbuahi s/d anak sapi) Untuk ternak Æ resistensi terhadap bakteri, virus, parasit Imunisasi in vivo: introduksi transgen penyandi antibodi untuk antigen spesifik Kambing, Domba, dan Babi Transgenik -penekanan pada kelenjar susu sebagai bioreaktor Æ protein farmasetik -metode: seperti tikus dengan promoter spesifik kelenjar susu -kambing, domba Æ protein (manusia) yang disekresikan ke dalam susu mengalami glikosilasi, dan punya aktivitas -Ekspresi GH dengan promoter metallothionein di babi Æ besar, tapi timbul penyakit bernanah di saluran pencernaan, terganggunya fungsi ginjal, hati. -potensi: produksi hemoglobin (darah) manusia dari babi? Daerah regulator β-globin manusia + 2 gen α1-globin manusia + 1 gen βA-globin manusia Æ hemoglobin man Unggas Transgenik Mikroinjeksi ke telur yang sudah terbuahi sulit: -Fertilisasi: beberapa sperma masuk ke dalam sel telur Æ sulit mengidentifikasi pronukleus jantan yang akan berfusi dengan pronukleus betina -Injeksi DNA ke sitoplasma Æ DNA tidak terintegrasi ke genom sel telur -Setelah fertilisasi Æ telur cepat berkembang, diselimuti membran yang kuat, diliputi oleh albumin yang tebal, dan dilapisi membran cangkang dalam dan luar Inokulasi embrio pada stadia blastoderma dengan vektor retrovirus yang defektif replikasi dan gen penanda Æ ayam, puyuh transgenik Æ retrovirus? Cara lain: rekayasa sel ESC unggas Æ belum diidentifikasi? Sel blastoderma Æ liposom (lipid kation) + transgen Æ introduksi ke subgerminal embrio dari telur Keturunan: campuran sel (donor+resipien) Æ kimera Seleksi kimera Æ sel nutfah transgenik Æ persilangan Radiasi (540-660 rad) terhadap embrio resipien Æ meningkatkan rasio donor Ayam transgenik: -resistensi penyakit -efisiensi pakan -penurunan kadar lemak dan kolesterol dalam telur -kualitas daging Ikan Transgenik Mikroinjeksi DNA kedalam sel telur terbuahi: salem Pronukleur tidak terlihat dengan mikroskop Æ DNA linier diinjeksikan kedalam sitoplasma sel telur yang sudah dibuahi atau ke embrio stadia awal (4 sel). Telur ikan berkembang di luar induk Æ suhu lingkungan diatur Setelah injeksi, 35-80% embrio hidup Æ transgenik 10-70% Identifikasi transgen Æ PCR dengan cetakan DNA dari sel darah merah Transgenesis : GH Promoter gen penyandi protein antibeku dari ocean pout + cDNA GH salem + terminator gen antibeku dari ocean pout Æ salem atlantik Salem transgenik: tumbuh cepat dan lebih besar (pada kondisi air dingin Æ ekspresi GH sangat tinggi)