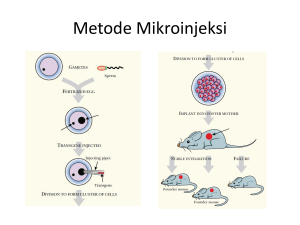
introduksi dan ekspresi gen
advertisement

37 V. EXPRESSION OF GROWTH HORMONE GENE OF TILAPIA (tiGH) IN CATFISH (Clarias sp.) TRANSGENIC FIRST GENERATION ABSTRACT The research intends to analyse expression of growth hormone gene of tilapia (tiGH) at the first generation of transgenic catfish (Clarias sp). Founder transgenic catfish which produced from the previous research was maintained until they get ready for spawning. The male founder transgenic catfish was crossed to nontransgenic female catfish; on the contrary the female founder transgenic catfish was crossed to non-transgenic male catfish. Spawning process is meant to be semi artificial spawning (induced spawning). Hatchery and larva nursery was undertaken in line with SNI (Indonesia National Standard) procedures (2004). The observed parameter was gene expressions by means of phenotype and genotype method. Phenotype method was the observation of catfish growth, while genotype was done by RT-PCR. Identification of fish carrying tiGH gene was performed by PCR method with specific primary for tiGH gene. The research shows that first generation of transgenic catfish which carried tiGH gene was as much 8,33% (15 from 180) and 4,0% (6 from 150). The catfish growth from first generation is significantly different between transgenic and non-transgenic where transgenic grew up to 7 faster than non-transgenic. It comes to the conclusion that the transferred gene of tiGH might be integrated into catfish genome so that transgene can be transmitted to the first generation and enhanced the growth. Keywords : gene expressions, growth hormone encoding gene, gene transmissions PENDAHULUAN Ikan lele dalam proses pembenihannya dapat dilakukan dengan cara pemijahan alami, semi buatan dan buatan. Telur ikan lele yang dihasilkan dari satu pasang induk dapat mencapai puluhan ribu yang akan dibuahi secara eksternal. Embrio relatif mudah diperoleh, dimanipulasi, diinkubasi dan menetas secara cepat pada beberapa jenis ikan. Menurut Dunham (2004), karena ikan mengalami pembuahan di luar merupakan potensi yang sangat besar untuk embrio berkembang karena tidak membutuhkan manipulasi yang komplek, seperti mengkultur embrio secara in vitro dan mentransfer ke dalam tubuh induknya. Hal ini membuat ikan merupakan organisma yang baik untuk mengaplikasikan transfer gen. Teknologi transgenesis salah satu solusi yang ditawarkan pada abad ini untuk meningkatkan produktivitas akuakultur sangat mungkin untuk diaplikasikan. Aplikasi teknologi transgenesis di Indonesia saat ini belum dilakukan untuk menghasilkan ikan transgenik. Ikan transgenik hasil rekayasa genetika akan bermanfaat sebagai plasma nutfah jika transgen di dalam genomnya stabil 38 dari generasi ke generasi. Stabilitas yang dimaksud adalah dalam hal integrasinya dalam genom, ekspresi dan pewarisaannya/transmisinya dari generasi ke generasi sehingga tingkah laku transgen dapat diperkirakan. Salah satu keuntungan dari teknologi transgenesis antara lain adalah gen yang telah diintroduksi dapat terintegrasi dalam genom resipien dan selanjutnya dapat ditransmisikan ke keturunannya (Khoo 2000). Ekspresi gen adalah proses dimana kode-kode informasi yang ada pada gen diubah menjadi protein-protein yang beroperasi di dalam sel. Ekspresi gen melibatkan tahap transkripsi, pascatranskripsi dan translasi (Meyer 1995). Gen adalah sepotong DNA yang menyandikan rantai polipeptida dan RNA. Tidak semua gen diekspresikan secara tepat dalam bentuk rantai polipeptida. Beberapa gen menyandikan beberapa jenis RNA transfer dan gen lain menyandi berbagai jenis RNA ribosomal. Gen yang menyandi polipeptida dan RNA dikenal sebagai gen struktural. Gen ini menentukan struktur beberapa produk akhir gen, seperti suatu enzim atau RNA yang stabil. DNA juga mengandung segmen atau urutan lain yang hanya menjalankan fungsi pengaturan (regulasi). Beberapa diantara segmen pengatur menyusun isyarat yang menunjukkan awal dan akhir gen struktural, yang lain berpartisipasi dalam memulai atau mengakhiri proses transkripsi gen struktural. Jadi kromosom mengandung gen struktural dan urutan pengatur (Lehninger 1994). Teknologi transgenik sudah dilakukan sejak tahun 1984 dengan model sistem tentang integrasi dan ekspresi dari rekombinan human growth hormone (hGH) pada ikan maskoki. Akhir-akhir ini posisi integrasi telah di karakterisasi dan dibandingkan antara ikan transgenik dan ikan nontransgenik dalam penggunaan pakan dan performa pertumbuhan. Biosafety dan bioethics ikan transgenik dengan menggunakan konstruksi gen „all fish” CagcGH yaitu promoter beta-aktin ikan mas berfusi dengan gen pengkode hormon pertumbuhan dari ikan grass carp yang diinduksi pada ikan mas (Cyprinus carpio) yang berasal dari sungai Yellow di China telah aman dimakan oleh manusia setiap hari. Hal ini telah dilakukan pengujian dengan prinsip uji pathologis dari Departemen Kesehatan China (Gang et al. 2003). Hal ini juga didukung dari hasil penelitian Guillen et al. (1999), dilakukan penelitian terhadap sukarelawan sebanyak 22 orang dan dibagi menjadi 2 kelompok yaitu kelompok A sebanyak 11 orang mengkonsumsi ikan nila transgenik selama 5 hari dari hari Senin sampai Jumat. Kelompok B mengkonsumsi ikan transgenik dan 39 nontransgenik selama 2 hari. Parameter yang diamati adalah sampel darah seluruh individu secara klinik dan biokimia. Hasilnya tidak ada perbedaan secara klinis dan biokimia antara kelompok A, B dan kontrol. Di negara Kanada ada dua cara yang dilakukan untuk meningkatkan produksi ikan salmon yaitu memproduksi ikan salmon dengan cara menyisipkan gen anti beku dan meningkatkan laju pertumbuhan dengan melakukan transfer gen pengkode hormon pertumbuhan (Fletcher et al. 2003). Hasil yang didapatkan dengan melakukan transfer gen pengkode hormon pertumbuhan pada ikan salmon adalah pertumbuhan ikan menjadi 10 kali lipat dibandingkan dengan nontransgenik (Devlin et al. 1994). Gen hormon pertumbuhan secara normal diekspresikan pada kelenjar pituitari yang dikontrol oleh sistem saraf pusat. Selanjutnya dengan kontrol sistem saraf pusat ini akan memodifikasi elemen spesifik jaringan dari gen yang akan diekspresikan dan dapat bekerja dimana saja. Integrasi genom transgen frekuensinya yang telah diamati hampir sama dengan gen anti beku berkisar 2 – 3%. Hal ini dapat diakibatkan karena penggunaan konstruksi gen yang berbeda dengan jenis ikan yang mendapat transfer gen. Transgen dapat terintegrasi ke dalam satu atau lebih kromosom dan lebih dari satu kopi gen. Seluruh founder transgenik GH adalah mosaik mengindikasikan bahwa transgen tidak terintegrasi ke dalam kromosom pada saat proses organogenesis dan separuh dari mereka gagal diteruskan pada keturunannya. Kira-kira 40% ikan founder transgenik meningkat laju pertumbuhannya di atas rata-rata sampai 3 – 6 kali dibandingkan dengan kontrol. Berdasarkan hukum Mendel transgen GH dan kecepatan tumbuh secara fenotipe akan stabil setelah generasi ketiga (Fletcher 2003). Pada penelitian ini dilakukan transfer gen pengkode hormon pertumbuhan yang berasal dari ikan nila dan promoter beta-aktin yang berasal dari ikan medaka, hal ini memperlihatkan bahwa penelitian ini termasuk ke dalam allotransgenik dimana transgenik tersebut mengandung bahan-bahan transgenik dari spesies yang berbeda. Pada transgenik, penggunaan elemen yang homolog antara gen struktural dan promoter biasanya lebih efektif dibandingkan dengan heterolog. Generasi dari ikan autotransgenik yang membawa konstruksi GH (dimana elemen tersebut berasal dari ikan yang sama) secara signifikan meningkatkan fenotipe pertumbuhan (Nam et al. 2008). Oleh karena itu pada penelitian ini dilakukan analisis ekspresi gen mBP-tiGH pada ikan lele transgenik generasi pertama. 40 BAHAN DAN METODE Pembesaran Ikan Lele Transgenik F0 Benih ikan lele yang positif membawa gen tiGH hasil mikroinjeksi pada bulan April 2009 sebanyak 22 ekor dilakukan pemeliharaan di Balai Besar Pengembangan Budidaya Air Tawar (BBPBAT) Sukabumi sampai mencapai ukuran siap matang gonad dengan prosedur SNI (2004). Benih dipelihara dalam wadah pemeliharaan dengan pemberian pakan sebanyak 3 kali sehari dengan feeding rate berkisar antara 3-5% perhari. Jenis pakan yang diberikan disesuaikan dengan ukuran larva dan benih yaitu pakan alami dan pakan buatan. Pakan alami antara lain Artemia sp, Daphnia sp dan cacing rambut sedangkan pakan buatan dalam bentuk pelet. Waktu yang dibutuhkan untuk mencapai matang gonad berkisar antara 8 - 12 bulan. Produksi Ikan Lele Transgenik F1 Induk ikan lele dumbo transgenik founder yang telah matang kelamin diseleksi secara individu. Berdasarkan seleksi secara individu diperoleh 3 ekor induk jantan dan 1 ekor induk betina yang matang gonad. Ikan lele betina transgenik disilangkan dengan ikan lele jantan normal untuk menghasilkan progeni F1 atau ikan lele jantan transgenik disilangkan dengan ikan lele betina normal. Induk betina yang telah matang gonad disuntik ovaprim dengan dosis 0,3 ml/kg bobot ikan, sedangkan induk jantannya menggunakan dosis 0,1 ml/kg bobot ikan. Induk jantan dan betina yang telah disuntik dimasukkan ke dalam wadah pemijahan dan dilakukan pengamatan sampai terjadi proses pemijahan. Setelah induk selesai memijah, pada pagi harinya telur ikan lele diangkat untuk ditetaskan di wadah penetasan. Telur ikan lele menetas menjadi larva setelah 20 jam dari saat pemijahan. Perawatan Larva dan Benih F1 Setelah telur menetas, kakaban diangkat untuk menghindari penurunan kualitas air akibat adanya pembusukan dari telur – telur yang tidak menetas. Disamping itu juga dilakukan pergantian air bak penetasan dengan membuang air sampai ¾ bagian volume air dan kemudian diisi kembali dengan air yang 41 baru. Larva ikan lele yang baru menetas akan berwarna hijau dan berkumpul di dasar bak penetasan di bagian yang gelap. Setelah berumur 2 hari, larva mulai bergerak dan menyebar ke seluruh bak penetasan. Sampai umur 2 hari larva tidak perlu diberi pakan tambahan, karena masih memanfaatkan cadangan makanan yang dibawa di dalam tubuhnya. Larva ikan lele baru diberikan pakan tambahan setelah berumur 2 hari dengan memberikan emulsi kuning telur ayam atau naupli Artemia sp. Pemberian pakan tersebut sampai umur 7 hari. Setelah menginjak umur 6 hari, larva diberi pakan alami antara lain kutu air (Daphnia sp) atau cacing sutera (Tubifex sp). Selama pemeliharaan benih atau larva dilakukan pengelolaan kualitas air dengan melakukan penyifonan dan pergantian air. Pergantian air dilakukan setiap 2 – 3 hari sekali. Jumlah air yang diganti sebanyak 50 – 70 % dengan cara menyifon. Pemeliharaan benih ikan lele transgenik generasi pertama dilakukan di Balai Besar Pengembangan Budidaya Air Tawar Sukabumi sampai benih benih berumur 3 bulan. Identifikasi Individu Ikan Membawa Transgen Individu ikan transgenik keturunan pertama (F1) yang membawa gen tiGH diidentifikasi menggunakan metode PCR dengan cetakan DNA genomik yang telah diekstraksi dari sirip ekor pada umur 4 minggu. Isolasi DNA genomik dilakukan menggunakan DNA Purification Kit (Puregene, Minneapolis, USA) dengan prosedur sesuai manual. PCR dilakukan menggunakan 2 set primer spesifik yang bisa membedakan tiGH dengan gen GH endogenous ikan lele, yaitu tiGH-1F Forward primer (5’-AGA CAG CCA GCG TTT GTT CT-3’) dan tiGH-1R Reverse primer (5’CCA GGA CTC AAC CAG TCC AT-3’) (Kobayashi et al. 2007). Program PCR yang digunakan adalah 95°C selama 5 menit, 35 siklus (95°C selama 20 detik, 62°C selama 15 detik, 72°C selama 20 detik), dan 72°C selama 3 menit. Setelah mesin menunjukkan suhu 4°C, maka mesin dapat dimatikan. Selanjutnya hasil PCR dapat langsung dianalisa dengan elektroforesis atau disimpan di dalam refrigerator dengan suhu 4°C. Analisis Ekspresi Transgen Ekspresi transgen pada benih ikan yang telah berumur 3 bulan dianalisis menggunakan metode RT-PCR. RNA diekstraksi dari sirip ekor ikan transgenik F1. Ekstraksi RNA diperoleh dari sampel jaringan sirip ekor sebanyak 7 sampel 42 yang dimasukkan ke dalam mikrotube 1,5 ml. Prosedur isolasi RNA dengan menggunakan RNeasy Mini Kit (Qiagen) sesuai manual. Jaringan dari sirip ekor ditimbang 30 mg dan dimasukkan ke dalam mikrotube 1,5 ml secara on ice. Selanjutnya ditambahkan larutan buffer RLT sebanyak 600 µL untuk melisiskan jaringan, kemudian digerus sampai semua jaringan hancur. Larutan disentrifugasi dengan kecepatan 12.000 rpm pada suhu ruang selama 3 menit, supernatan dibuang dengan cara pipetting dan di pindahkan ke mikrotube yang baru. Penambahan 600 µL Etanol 70% ke dalam mikrotube dan dicampur dengan cara pipetting, tidak boleh disentrifugasi. Sebanyak > 700 µL sampel termasuk precipitate lainnya yang terbentuk dipindahkan ke dalam RNeasy spin column 2 ml collection tube. Kemudian tabung ditutup rapat dan larutan disentrifugasi dengan kecepatan 10.000 rpm pada suhu ruang selama 15 detik. Larutan yang berada dibagian bawah dibuang. Selanjutnya dilakukan penambahan 700 µL buffer RW1 ke dalam RNeasy spin column dan ditutup rapat. Larutan disentrifugasi dengan kecepatan 10.000 rpm pada suhu ruang selama 15 detik. Larutan yang berada dibagian bawah dibuang dan ditambahkan 500 µL buffer RPE ke dalam RNeasy spin column dan ditutup rapat. Larutan disentrifugasi dengan kecepatan 10.000 rpm pada suhu ruang selama 15 detik. Larutan yang berada dibagian bawah dibuang. Penambahan 500 µL buffer RPE ke dalam RNeasy spin column dan ditutup rapat. Larutan disentrifugasi dengan kecepatan 10.000 rpm pada suhu ruang selama 2 menit. RNeasy spin column dipindahkan ke collection tube yang baru. Kemudian ditambahkan 30 – 50 µL RNase free water langsung ke dalam spin column membran dan ditutup rapat, kemudian dilakukan sentrifugasi pada suhu ruang dengan kecepatan 10.000 rpm selama 1 menit untuk elute DNA. Konsentrasi larutan RNA diukur dengan alat Gene Quant. Hasil dari ekstraksi RNA dan diperoleh konsentrasi larutan RNAnya dilakukan analisis ekspresi gen dengan menggunakan Qiagen One Step RT-PCR Kit sesuai prosedur. RT-PCR dilakukan dengan volume reaksi 20 µL yang mengandung 5X Qiagen Buffer 4 µL, 1 µL dNTPs mix, 1 µL Qiagen enzyme mix, 9 µL Rnase free water, 2 µl RNA template dan 1,5 µL dari masing-masing primer forward dan reverse yang spesifik untuk transgen yaitu tiGH-1F Forward primer (5’-AGA CAG CCA GCG TTT GTT CT-3’) dan tiGH-1R Reverse primer (5’CCA GGA CTC AAC CAG TCC AT-3’). Program PCR yang digunakan adalah 50oC selama 30 menit untuk melakukan proses Reverse Transcription : 95°C selama 15 menit, 35 siklus (95°C selama 20 detik, 62°C selama 15 detik, 72°C selama 43 15 detik), dan 72°C selama 10 menit . Setelah mesin menunjukkan suhu 4°C, maka mesin dapat dimatikan. Selanjutnya hasil PCR dapat langsung dianalisa dengan elektroforesis atau disimpan di dalam refrigerator dengan suhu 4°C. Dua µl hasil PCR dielektroforesis menggunakan 1% gel agarose, distaining dengan red gel, dan difoto dengan kamera digital dalam kondisi disinari dengan cahaya ultraviolet. Tahap Pengumpulan Data Pengumpulan data dilakukan dengan menguji keberadaan gen tiGH pada generasi pertama dan mengukur pertumbuhan benih ikan lele. Untuk mengetahui pertumbuhan ikan yang dipelihara antara ikan transgenik dan nontransgenik, dilakukan pengukuran pertambahan panjang dan bobot tubuh setiap bulan sekali selama tiga bulan pemeliharaan. Selanjutnya dapat dihitung laju pertumbuhan harian spesifik (Specifik Growth Rate/SGR) menggunakan rumus : ln W2 – ln W1 SGR = t2 – t1 dimana : W1 : berat ikan pada periode waktu 1 (t1) W2 : berat ikan pada periode waktu 2 (t2) Analisis Data Data yang diperoleh dianalisis secara statistik untuk mengetahui perbedaan antara transgenik dan nontransgenik mempunyai pengaruh nyata. Sedangkan data analisa DNA dianalisis secara deskriptif dan ditampilkan dalam bentuk tabel dan gambar. 44 HASIL DAN PEMBAHASAN Ikan lele transgenik founder yang diperoleh dari hasil mikroinjeksi pada bulan April tahun 2009 dilakukan pemeliharaan di BBPBAT Sukabumi. Setelah 12 bulan pemeliharaan dilakukan pengecekan kematangan gonad ikan. Ikan lele yang sudah matang gonad dilakukan pemijahan antara transgenik jantan dan nontransgenik betina atau transgenik betina dan nontransgenik jantan. Induk ikan lele generasi founder yang siap untuk dipijahkan diperoleh empat ekor induk siap memijah yang terdiri dari tiga ekor jantan dan satu ekor betina. Proses pemijahan dilakukan secara semi buatan dan diperoleh hasil dua induk jantan transgenik founder berhasil memijah. Larva ikan lele yang diperoleh dilakukan pemeliharaan sesuai standar operasional. Setelah berumur satu bulan dilakukan pengujian analisa DNA untuk melihat transmisi gen tiGH pada generasi pertama. Benih ikan lele generasi pertama dari hasil mikroinjeksi pada penelitian sebelumnya dilakukan pengujian analisa DNA dengan mengambil sampel jaringan pada sirip ekor sebanyak 180 ekor benih lele secara pooling. Diperoleh hasil sebanyak 30 ekor positif membawa gen tiGH dan dilakukan pengujian analisa DNA secara individu diperoleh hasil sebanyak 15 ekor. Pada benih ikan lele generasi pertama lainnya dilakukan pengujian analisa DNA sebanyak 150 ekor secara pooling dan diperoleh hasil sebanyak 30 ekor positif membawa gen tiGH dan dilakukan pengujian analisa DNA secara individu diperoleh hasil sebanyak 6 ekor (Tabel 4). Tabel 4. Transmisi gen tiGH pada generasi pertama dari induk ikan lele jantan yang berbeda. Jantan Transgenik Jumlah sampel (ekor) Nomor 1 Nomor 2 180 150 Jumlah individu Transgenik (ekor) 15 6 Persentase Transmisi transge (%) 8,33 4,00 Pada generasi pertama ekspresi gen tiGH ikan lele transgenik dianalisis dengan teknik RT-PCR. Dari tujuh sampel yang positif membawa gen tiGH pada generasi pertama diperoleh 5 individu yang mempunyai ekspresi gen tiGH (Gambar 9). Hal ini memperlihatkan bahwa gen yang telah disisipkan tersebut terekspresi, walaupun tidak semua mengekspresikan transgen. Menurut Iyengar et al. (1996), bahwa pada awal perkembangan embrio, gen yang ditransfer akan direplikasi tanpa mengalami integrasi ke dalam genom resipien. Lebih lanjut 45 dijelaskan bahwa setelah mengalami beberapa pembelahan sel, sebagian gen asing tersebut terintegrasi secara acak ke dalam genom resipien di salah satu blastomer sehingga akan terdapat dua macam sel, yaitu sel yang membawa transgen dan sel yang tidak membawa transgen. Hal ini mengakibatkan tidak semua sel membawa transgen atau dikenal dengan istilah kejadian mosaik. ◄ 200 bp Gambar 9. Deteksi ekspresi dari transgen pada ikan transgenik generasi pertama (F 1 ) menggunakan metode One Step RT-PCR. M merupakan Marker DNA 1 log ladder, 1 – 7 adalah hasil amplifikasi RT-PCR RNA ikan lele generasi pertama dan K+ adalah kontrol positif. Menurut Chou et al. (2001) ketika fragmen DNA yang terdiri dari suatu gen target atau gen penanda homolog maupun heterolog ditransfer, maka akan sangat umum menemukan kejadian mosaik. Selain itu, menurut Alimuddin et al. (2003) selain terintegrasi ke dalam genom, ada sebagian dari gen asing berada dalam suatu posisi ekstrakromosomal. Lebih lanjut dijelaskan bahwa gen asing yang terintegrasi akan stabil di dalam genom, sementara dalam bentuk ekstrakromosomal akan terdegradasi oleh endogeneus nuclease. Berdasarkan hasil penelitian ini memperlihatkan bahwa gen yang telah disisipkan tersebut terekspresi, walaupun tidak semua mengekspresikan transgen. Selain itu dapat juga memperlihatkan bahwa gen tiGH yang disisipkan dapat ditransmisikan pada keturunannya. Gen asing yang dapat ditransmisikan pada generasi pertama ini menunjukkan bahwa gen asing tersebut telah terintegrasi ke dalam gonad ikan lele transgenik founder. Rahman & Maclean (1999) melakukan penyisipan gen GH ikan salmon-gen antibeku ocean pout (OPAFPcsGH), laju germline transmision dari F0 ke F1 hanya kurang dari 10%. Namun laju transmisi transgen dari F1-F2 adalah sekitar ± 50% (sesuai dengan hukum Mendel). Sedangkan berdasarkan hasil penelitian Kobayashi et al. (2007) yang juga menggunakan 46 gen mBP-tiGH pada generasi pertama ditransmisikan pada generasi pertama sebesar 5,71% dan 14,3%. Setiap individu yang terintegrasi gen asing ke dalam genom akan ditransmisikan kepada keturunannya. Untuk mengaplikasikan teknik ini pada akuakultur maka produksi massal ikan transgenik diperlukan (Yoshizaki et al. 1991). Pada penelitian ini diperoleh hasil bahwa individu ikan lele transgenik founder membawa gen yang telah disisipkan kepada keturunannya sebesar 4,0% dan 8,33% pada generasi pertama. Hal ini sesuai dengan hasil penelitian sebelumnya pada ikan nila transgenik dengan konstruksi gen yang sama memberikan hasil transmisi pada generasi pertama sebesar 5,7% – 14,3%. Pada ikan mud loach laju transmisi transgen pada generasi pertama bervariasi berkisar antara 2% – 33% (Nam et al. 2001). Menurut Alimuddin et al. (2005) laju transmisi transgen pada generasi pertama bervariasi antara 4,2% – 44,1%. Untuk mengetahui pengaruh introduksi gen tiGH terhadap pertumbuhan benih ikan lele dilakukan pengamatan terhadap pertumbuhan panjang dan berat sampai benih berumur 3 bulan. Pertumbuhan antara ikan lele transgenik F 1 dan ikan lele nontransgenik yang berasal dari populasi yang sama dilakukan pengukuran dan diperoleh data bobot ikan transgenik generasi pertama (F 1) pada umur satu bulan tidak berbeda antara transgenik dan nontransgenik. Pada umur 2 bulan bobot ikan transgenik berkisar antara 15 gram – 30 gram, sedangkan bobot ikan nontransgenik berkisar antara 5 gram – 20 gram. Hal ini memperlihatkan pada umur 2 bulan perbandingan bobot antara transgenik dan nontransgenik berkisar 1 – 3 kali lipat. Pada umur tiga bulan dilakukan pengukuran bobot benih ikan transgenik berkisar antara 25 gram – 150 gram, sedangkan benih ikan nontransgenik berkisar antara 6 gram – 22 gram. Hal ini memperlihatkan pada umur 3 bulan perbandingan bobot antara transgenik dan nontransgenik berkisar antara 1 – 7 kali lipat (Gambar 10 dan11). 47 12 Jumlah (ekor) 10 8 Transgenik 6 Nontransgenik 4 2 0 5 10 15 20 25 30 Bobot (g) Gambar 10. Sebaran distribusi bobot benih ikan lele transgenik dan nontransgenik generasi pertama (F1) umur 2 bulan. 12 Jumlah (ekor) 10 8 Transgenik 6 Nontransgenik 4 2 0 5 10 15 20 25 30 35 40 45 70 150 Bobot (g) Gambar 11. Sebaran distribusi bobot benih ikan lele transgenik dan nontransgenik generasi pertama (F1) umur 3 bulan. Pertumbuhan adalah perubahan ukuran baik panjang, berat atau volume dalam jangka waktu tertentu. Pertumbuhan ini secara fisik diekspresikan dengan adanya perubahan jumlah atau ukuran sel penyusun jaringan tubuh pada periode waktu tertentu. Pada penelitian ini dilakukan pengukuran laju pertumbuhan harian setiap bulan selama tiga bulan pemeliharaan dan diperoleh hasil antara transgenik dan nontransgenik pada bulan pertama pemeliharaan tidak terdapat perbedaan, perbedaan laju pertumbuhan harian terjadi pada bulan kedua dan ketiga setelah pemeliharaan (Gambar 12). Performa pertumbuhan bobot ratarata antara benih ikan lele transgenik dan nontransgenik pada umur tiga bulan secara fenotipe dan genotipe berbeda (P< 0,05) (Gambar 13 dan 14). Laju Pertumbuhan Harian (%) 48 18 16 14 12 Transgenik 10 Non Transgenik 8 6 4 2 0 1 2 3 Bulan ke- Gambar 12. Laju pertumbuhan harian antara ikan transgenik generasi pertama dan nontransgenik. 60 Bobot (gram) 50 40 Nontransgenik 30 Transgenik 20 10 0 1 2 3 Umur (bulan) Gambar 13. Pertumbuhan rata-rata ikan lele trangenik dan nontransgenik generasi pertama A. Transgenik B. Nontransgenik Gambar 14. Ikan transgenik generasi pertama (A) dan nontransgenik (B) umur 3 bulan. 49 Pertumbuhan ikan lele transgenik generasi pertama lebih baik dari kontrol walaupun pertumbuhannya tidak luar biasa dan hasil pertumbuhan ikan lele transgenik generasi pertama memberikan pertumbuhan 1-7 kali lipat daripada nontransgenik, hal ini memperlihatkan bahwa hasil penelitian dengan menggunakan konstruksi gen yang sama pada ikan nila memberikan hasil yang sama karena bisa mencapai 7 kali lipat (Kobayashi et al. 2007). Pertumbuhan yang terjadi dapat disebabkan oleh berbagai macam faktor. Pertumbuhan adalah pertambahan ukuran panjang atau berat dalam suatu waktu, sedangkan pertumbuhan bagi populasi sebagai pertambahan jumlah. Pertumbuhan itu merupakan proses biologis yang komplek dimana banyak faktor mempengaruhinya. Pertumbuhan dalam individu ialah pertambahan jaringan akibat dari pembelahan sel secara mitosis. Urat daging dan tulang pada ikan merupakan bagian terbesar dari tubuhnya. Pertambahan sel-sel pada jaringan tersebut bertanggung jawab terhadap pertambahan massa ikan (Effendi 1997). Pertumbuhan jaringan atau organ selain dipengaruhi oleh kualitas makanan juga dipengaruhi oleh hormon pertumbuhan. Hormon pertumbuhan meningkatkan transpot asam amino melalui membran atau mempercepat proses kimia sintesis protein sehingga protein jaringan bertambah. Selain itu hormon pertumbuhan juga bekerja pada metabolisme lemak yang bertugas meningkatkan kecepatan pengeluaran lemak dari depot lemak, sehingga memungkinkan lemak tersedia sebagai energi dan selanjutnya mengurangi kecepatan oksidasi asam amino dan akibatnya meningkatkan jumlah asam amino jaringan yang disintesis menjadi protein (Fujaya 2004). KESIMPULAN Gen tiGH diduga telah terintroduksi ke dalam gonad sehingga dapat ditransmisikan pada generasi F 1 . Pada generasi pertama transmisi gen berkisar antara 4,0% – 8,33%. Pertumbuhan bobot antara ikan transgenik dan nontransgenik adalah 1 – 7 kali lipat lebih tinggi dibandingkan dengan nontransgenik pada generasi pertama.