Modifikasi Struktur Etil ρ-metoksisinamat Melalui Reaksi Kondensasi
advertisement

UIN SYARIF HIDAYATULLAH JAKARTA Modifikasi Struktur Etil ρ-metoksisinamat Melalui Reaksi Kondensasi Aldol dengan Etil Metil Keton SKRIPSI PUTRI HAYATI NUFUS 1112102000030 FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN PROGRAM STUDI FARMASI JAKARTA AGUSTUS 2016 UIN SYARIF HIDAYATULLAH JAKARTA Modifikasi Struktur Etil ρ-metoksisinamat Melalui Reaksi Kondensasi Aldol dengan Etil Metil Keton SKRIPSI Diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi PUTRI HAYATI NUFUS 1112102000030 FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN PROGRAM STUDI FARMASI JAKARTA AGUSTUS 2016 ii ABSTRAK Nama Program Studi Judul Skripsi : Putri Hayati Nufus : Strata-1 Farmasi : Modifikasi Struktur Etil ρ-metoksisinamat melalui Reaksi Kondensasi Aldol dengan Etil Metil Keton. Etil ρ-metoksisinamat (EPMS) merupakan senyawa yang terkandung dalam kencur (Kaempferia galanga L) yang memiliki aktivitas sebagai antiinflamasi. Gugus ester pada EPMS merupakan gugus yang kurang stabil karena mudah terhidrolisis. Penelitian ini bertujuan untuk memodifikasi struktur etil ρ-metoksisinamat (EPMS) melalui reaksi kondensasi aldol dengan etil metil keton. Gugus ester pada EPMS akan diubah menjadi gugus keton. Modifikasi EPMS melalui tiga proses yaitu proses hidrolisis menggunakan NaOH, proses oksidasi menggunakan Ca(NO3)2 dan proses kondensasi aldol menggunakan etil metil keton dengan adanya NaOH dalam air. Reaksi dilakukan dengan menstirer campuran pada suhu ruang. Analisis struktur molekul senyawa ditentukan berdasarkan data fisika, GCMS dan 1H-NMR. Hasil hidrolisis EPMS menghasilkan senyawa asam ρ-metoksisinamat (APMS) yang di oksidasi sehingga menghasilkan senyawa 4-metoksibenzaldehid. Senyawa tersebut direaksikan dengan etil metil keton melalui reaksi kondensasi aldol. Setelah dilakukan reaksi selama 24 jam diperoleh senyawa target dengan rendemen 35,26 %. Reaksi kondensasi aldol menggunakan basa NaOH dalam air yang akan merubah senyawa etil metil keton menjadi ion enolat sehingga bereaksi pada gugus karbonil senyawa 4-metoksibenzaldehid. Berdasarkan analisa menggunakan GCMS dan 1HNMR menunjukkan bahwa senyawa target adalah senyawa 1-(4-metoksifenil)-1penten-3-on. Senyawa 1-(4-metoksifenil)-1-penten-3-on merupakan bentuk keton dari etil ρ-metoksisinamat (EPMS) berupa kristal putih hingga kuning dengan titik leleh 53-60οC. Identifikasi senyawa menggunakan KLT dengan eluen heksan-etil asetat (4:1) menunjukkan nilai Rf 0,525. Identifikasi menggunakan GCMS menunjukkan waktu retensi 9,857 dan berat molekul 190 dengan fragmentasi masa pada 161, 133, 118, 103, 89 dan 76. Identifikasi menggunakan 1H-NMR menunjukkan sinyal CH2 pada 2,66 ppm yang membuktikan bahwa gugus ester telah berubah menjadi gugus keton. Kata kunci : Aldehid, etil metil keton, etil ρ-metoksisinamat, hidrolisis, kondensasi aldol, NaOH, oksidasi. vi UIN Syarif Hidayatullah Jakarta ABSTRACT Name : Putri Hayati Nufus Programme Study : Pharmacy Title : Structure Modification of Ethyl ρ-methoxycinnamate Compound through Aldol Condensation Reaction with Methyl Ethyl Ketone. Ethyl ρ-methoxycinnamate (EPMS) is a compound contained in kencur (Kaempferia galanga L) which has anti-inflammatory activity. EPMS ester group is less stable because it is easily hydrolyzed. The aims of this study were to structure modification of ethyl ρ-methoxycinnamate (EPMS) compound through aldol condensation reaction with methyl ethyl ketone. Ester groups on EPMS will be converted into a ketone group. Modifications EPMS through three processes, namely the process of hydrolysis using NaOH, the oxidation process using Ca(NO3)2 and aldol condensation process using methyl ethyl ketone in the presence of NaOH in water. Carried out by stirring the reaction mixture at room temperature. Analysis of the molecular structure of the compound is determined based on the data of physics, GCMS, and 1H-NMR. EPMS hydrolysis produced acid ρ-methoxycinnamate (APMS) compound which are oxidized to produced 4-methoxybenzaldehide compound. This compound is reacted with methyl ethyl ketone through aldol condensation reaction. After reaction for 24 hours is obtained compound with a yield of 35.26%. Aldol condensation reaction using NaOH alkaline water that will change methyl ethyl ketone compounds into the enolate ion to react the carbonyl group in 4methoxybenzaldehide compound. Based on an analysis using GCMS and 1H-NMR showed that the target compound is 1- (4-methoxyphenyl) -1-penten-3-on compound. The 1- (4-methoxyphenyl) -1-penten-3-one compound is a ketone form of ethyl ρmethoxycinnamate (EPMS) in the form of white to yellow crystals with a melting point 53-60οC. The identification of compounds by TLC with eluent hexane-ethyl acetate (4: 1) showed Rf value of 0.525. Identification using GCMS showed a retention time of 9.857 and a molecular weight of 190 with fragmentation period at 161, 133, 118, 103, 89 and 76. Identification using 1H-NMR showed CH2 signal at 2.66 ppm that proves that the ester groups have been transformed into a ketone group. Keywords : Aldehyde, aldol condensation, ethyl p-methoxycinnamate, hydrolysis, methyl ethyl ketone, NaOH, oxidation. vii UIN Syarif Hidayatullah Jakarta KATA PENGANTAR Puji dan syukur penulis panjatkan kehadirat Allah SWT atas pertolongan, rahmat, dan karunia-Nya sehingga penulis dapat menyelesaikan skripsi yang berjudul “Modifikasi Struktur Etil ρ-metoksisinamat Melalui Reaksi Kondensasi Aldol dengan Etil Metil Keton”. Shalawat dan salam senantiasa terlimpah kepada junjungan kita Nabi Muhammad SAW, teladan bagi umat manusia dalam menjalani kehidupan. Skripsi ini disusun untuk memenuhi salah satu syarat menempuh ujian akhir guna mendapatkan gelar Sarjana Farmasi Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri Syarif Hidayatullah Jakarta. Dalam menyelesaikan masa perkuliahan hingga penulisan skripsi ini penulis tentu menemukan berbagai kesulitan dan halangan yang menyertai. Oleh karena itu, penulis tidak terlepas dari bantuan, doa, dan bimbingan dari banyak pihak. Pada kesempatan ini penulis menyampaikan ucapan terima kasih yang sebesar-besarnya kepada : 1. Bapak Dr. Arief Sumantri, SKM, M.Kes selaku Dekan Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri (UIN) Syarif Hidayatullah Jakarta. 2. Ibu Ismiarni Komala, M.Sc., Ph.D., Apt sebagai Pembimbing I dan Ibu Ofa Suzanti Betha, M.Si., Apt sebagai Pembimbing II yang telah memberikan ilmu, nasihat, waktu, tenaga, dan pikiran selama masa perkuliahan hingga penelitian dan penulisan skripsi. 3. Ibu Dr. Nurmeilis., M.Si., Apt selaku Ketua Program Studi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri (UIN) Syarif Hidayatullah Jakarta. 4. Prof. Dr. Atiek Soemiati M.Si., Apt selaku pembimbing akademik yang telah memberikan bimbingan dan bantuan selama masa perkuliahan. 5. Bapak dan Ibu staf pengajar, serta karyawan yang telah memberikan arahan selama masa perkuliahan. 6. Kedua orang tua tercinta, Bapak Drs. H. Munasir dan Ummi Hj. Masturoh yang telah memberikan dukungan material, moral, nasihat-nasihat, serta doa yang tiada pernah putus di setiap sujudnya setiap waktu. viii UIN Syarif Hidayatullah Jakarta 7. Abang Hafiz, Abang Khairul, Abang Fariz, Abang Dillah dan Adik Kiki yang telah memberikan doa dan motivasi selama penulis melaksanakan penelitian dan menyusun skripsi ini. 8. Teman-teman Kingdom : Owi, Beni, Gilman, Mutia, Noni, Atul, Nita, Elsa, Ani, dan Windi yang telah memberikan doa, semangat, serta bantuan selama penyusunan skripsi. 9. Teman-teman seperjuangan Echa, Tania dan Fika atas semangat dan kebersamaan selama perkuliahan hingga saat ini. 10. Teman-teman Farmasi 2012 yang telah memberikan motivasi dan bantuan selama masa perkuliahan dan penyusunan skripsi. 11. Kak Walid, Mba Rani, Ka Eris, Ka Yaenab, Ka Lisna, Ka Tiwi dan Ka Rahmadi yang telah membantua selama melakukan penelitian. 12. Kepada semua pihak yang telah membantu penulis selama ini yang tidak dapat disebutkan namanya satu persatu. Semoga bantuan yang telah diberikan mendapat balasan dari Allah SWT. Penulis menyadari bahwa penulisan skripsi ini masih jauh dari kesempurnaan. Oleh karena itu, saran dan kritik yang bersifat membangun akan penulis nantikan. Akhir kata, semoga skripsi ini dapat bermanfaat bagi pengembangan ilmu pengetahuan. Ciputat, 18 Agustus 2016 Penulis ix UIN Syarif Hidayatullah Jakarta DAFTAR ISI Halaman HALAMAN JUDUL......................................................................................... ii HALAMAN PERNYATAAN ORISINALITAS………………………….… iii HALAMAN PERSETUJUAN PEMBIMBING............................................. iv HALAMAN PENGESAHAN………………………………………………… v ABSTRAK…………………………………………………………………….. vi ABSTRACT……………………………………………………………………. vii KATA PENGANTAR………………………………………………………... viii HALAMAN PERNYATAAN PERSETUJUAN PUBLIKASI…………….. x DAFTAR ISI..................................................................................................... xi DAFTAR TABEL……………………………………………………………. xiii DAFTAR GAMBAR........................................................................................ xiv DAFTAR LAMPIRAN.................................................................................... xv DAFTAR ISTILAH......................................................................................... xvi BAB 1 PENDAHULUAN.................................................................................. 1 1.1 Latar Belakang.................................................................................. 1 1.2 Rumusan Masalah............................................................................. 3 1.3 Tujuan............................................................................................... 3 1.4 Manfaat............................................................................................. 3 BAB 2 TINJAUAN PUSTAKA........................................................................ 4 2.1 Tumbuhan Kencur............................................................................ 4 2.1.1 Klasifikasi............................................................................. 4 2.1.2 Tempat Tumbuh................................................................... 4 2.1.3 Kandungan Kimia................................................................. 5 2.1.4 Manfaat................................................................................. 5 2.2 Senyawa Etil ρ-metoksisinamat....................................................... 6 2.3 Modifikasi Struktur EPMS............................................................... 7 2.4 Optimasi Reaksi Kimia.................................................................... 8 2.5 Hidrolisis.......................................................................................... 9 2.6 Oksidasi Alkena............................................................................... 10 2.7 Kondensasi Aldol............................................................................. 11 2.8 Natrium Hidroksida.......................................................................... 13 2.9 Kalsium Nitrat.................................................................................. 14 2.10Asam Asetat Glasial......................................................................... 14 2.11Etil Metil Keton................................................................................ 15 2.12Iradiasi Microwave........................................................................... 16 2.12.1 Mekanisme Reaksi Secara Polarisasi Dipol......................... 17 2.12.2 Mekanisme Reaksi Secara Konduksi................................... 17 2.13Iidentifikasi...................................................................................... 17 2.13.1 Kromatografi........................................................................ 17 a. Kromatografi Lapis Tipis............................................... 18 b. Kromatografi Gas........................................................... 21 2.13.2 Spektrofotometri................................................................... 22 a. Spektrofotometri Resonansi Magnetik........................... 23 xi UIN Syarif Hidayatullah Jakarta BAB 3 METODOLOGI PENELITIAN.......................................................... 25 2.1 Tempat dan Waktu Penelitian.......................................................... 25 3.1.1 Tempat..................................................................................... 25 3.1.2 Waktu...................................................................................... 25 3.2 Alat dan Bahan................................................................................. 25 3.2.1 Alat......................................................................................... 25 3.2.2 Bahan...................................................................................... 25 3.3 Prosedur Penelitian.......................................................................... 26 3.3.1 Preparasi………………………………………………..…... 26 a. Pengambilan Sampel……………………………..…….. 26 b. Determinasi Tumbuhan……………………………...…. 26 c. Penyiapan Bahan untuk Ekstraksi……………………… 26 d. Pembuatan Plat KLT Preparatif……………………....… 26 3.3.2 Isolasi Etil ρ-metoksisinamat………………………...……... 26 3.3.3 Modifikasi Etil ρ-metoksisinamat .......................................... 27 a. Proses Hidrolisis................................................................. 27 b. Proses Oksidasi.................................................................. 27 c. Proses Kondensasi Aldol……………………………...…. 27 3.3.4 Pemurnian dengan KLT Preparatif……………………...….. 28 3.3.5 Identifikasi Senyawa............................................................... 28 a. Identifikasi Organoleptis.................................................... 28 b. Pengukuran Rf................................................................... 28 c. Pengukuran Titik Leleh..................................................... 28 d. Identifikasi Senyawa Menggunakan GCMS..................... 28 e. Identifikasi Senyawa Menggunakan 1H-NMR…………... 28 BAB 4 HASIL DAN PEMBAHASAN…………………………………...….. 29 4.1 Hasil Isolasi Senyawa Etil ρ-metoksisinamat…………………....… 29 4.1.1 Hasil Determinasi………………………………………...…. 30 4.1.2 Pembuatan Serbuk Simplisia………………………………... 30 4.1.3 Isolasi Etil ρ-metoksisinamat…………………………...…... 30 4.1.4 Identifikasi Senyawa Etil ρ-metoksisinamat………………... 31 4.2 Reaksi Hidrolisis Etil ρ-metoksisinamat………………………….. 32 4.2.1 Identifikasi Senyawa Hasil Hidrolisis EPMS..……………... 34 4.3 Reaksi Oksidasi Asam ρ-metoksisinamat……………………….… 35 4.3.1 Identifikasi Senyawa Hasil Oksidasi APMS……………….. 36 4.4 Reaksi Kondensasi Aldol 4-metoksibenzaldehid………………….. 37 4.5 Identifikasi Senyawa Hasil Reaksi Kondensasi Aldol…………….. 40 BAB 5 KESIMPULAN…………………………………………………….…. 45 5.1 Kesimpulan……………………………………………….………… 45 5.2 Saran……………………………………………………….….…… 45 DAFTAR PUSTAKA........................................................................................ 46 LAMPIRAN....................................................................................................... 51 xii UIN Syarif Hidayatullah Jakarta DAFTAR TABEL Halaman Tabel 4.1 Data pergeseran kimia (δ) spektrum H-NMR etil ρ-metoksisinamat, asam ρ-metoksisinamat, dan 1-(4-metoksifenil)-1-penten-3-on…..……. 43 1 xiii UIN Syarif Hidayatullah Jakarta DAFTAR GAMBAR Gambar 2.1 Gambar 2.2 Gambar 2.3 Gambar 2.4 Gambar 2.5 Gambar 2.6 Gambar 2.7 Gambar 2.8 Gambar 2.9 Gambar 2.10 Gambar 2.11 Gambar 2.12 Gambar 2.13 Gambar 2.14 Gambar 2.15 Gambar 2.16 Gambar 2.17 Gambar 4.1 Gambar 4.2 Gambar 4.3 Gambar 4.4 Gambar 4.5 Gambar 4.6 Gambar 4.7 Gambar 4.8 Gambar 4.9 Gambar 4.10 Gambar 4.11 Gambar 4.12 Gambar 4.13 Gambar 4.14 Gambar 4.15 Gambar 4.16 Gambar 4.17 Gambar 4.18 Gambar 4.19 Gambar 4.20 Halaman Kandungan kimia rimpang kencur………………………………... 5 Jalur asam sikhimat dalam biosintesa fenilpropanoid untuk menghasilkan etil p-metoksisinamat…………………………….... 6 Beberapa trasformasi gugus fungsi dari EPMS………………….... 7 Prinsip reaksi hidrolisis …………………………………………... 9 Mekanisme hidrolisis ester dalam suasana basa ………….……..... 9 Mekanisme hidrolisis ester dalam suasana asam……………….… 10 Reaksi oksidasi alkena …………………………………………... 10 Reaksi pemaksapisahan oksidatif pada disubstitusi ………...…… 11 Reaksi pemaksapisahan oksidatif pada monosubstitusi …………. 11 Reaksi pemaksapisahan oksidatif pada disubstitusi dan monosubstitusi……………...................................................... 11 Mekanisme reaksi kondensasi aldol……………………………... 12 Mekanisme dehidrasi aldol………………………………………. 13 Struktur natrium hidroksida……………………………………… 14 Struktur kalsium nitrat…………………………………………… 14 Struktur asam asetat………...…………….……………………… 15 Struktur etil metil keton………………………………………….. 15 Skema kromatografi lapis tipis……………………………….….. 20 KLT uji pendahuluan oksidasi ………………………………….. 29 Simplisia kencur …………….………………………………..…. 30 KLT isolat kencur …….………………………………………..... 31 Kristal EPMS ……………………………………………………. 31 Pola fragmentasi GCMS etil ρ-metoksisinamat …………….…... 32 Mekanisme reaksi hidrolisis etil ρ-metoksisinamat …….………. 33 KLT senyawa hasil hidrolisis ……………………………………. 33 Senyawa hasil hidrolisis etil ρ-metoksisinamat ………..………... 33 Pola fragmentasi GCMS asam ρ-metoksisinamat ……………..... 34 KLT senyawa hasil oksidasi …………………………………….. 35 Senyawa hasil oksidasi asam ρ-metoksisinamat………..………... 35 Reaksi oksidasi asam ρ-metoksisinamat ……………………….... 36 Pola fragmentasi GCMS 4-metoksibenzaldehid………………… 37 KLT optimasi reaksi kondensasi aldol…………………………… 38 KLT senyawa hasil kondensasi aldol…………………………….. 39 Senyawa hasil reaksi kondensasi aldol………………………..…. 39 Mekanisme reaksi kondensasi aldol senyawa 4-metoksibenzaldehid dengan etil metil keton…………...…..….. 40 KLT semua senyawa………………………………………….…. 41 Pola fragmentasi GCMS 1-(4-metoksifenil)-1-penten-3-on……. 42 Struktur senyawa……………………………………………….... 43 xiv UIN Syarif Hidayatullah Jakarta DAFTAR LAMPIRAN Halaman Lampiran 1. Kerangka Penelitian………………………………………………………….. 51 Lampiran 2. Isolasi Etil ρ-metoksisinamat………………………………………………… 52 Lampiran 3. Determinasi Tanaman Kencur……………………………………………….. 53 Lampiran 4. Spektrum GCMS Senyawa Etil ρ-metoksisinamat…………………………... 54 Lampiran 5. Spektrum GCMS Senyawa Asam ρ-metoksisinamat………………………… 55 Lampiran 6. Spektrum GCMS Senyawa 4-metoksibenzaldehid…………………………... 56 Lampiran 7. Spektrum GCMS Senyawa 1-(4-metoksifenil)-1-penten-3-on………………. 57 Lampiran 8. Spektrum 1H-NMR Senyawa 1-(4-metoksifenil)-1-penten-3-on…………….. 59 Lampiran 9. Spektrum GCMS Hasil Optimasi Reaksi Kondensasi Aldol………………… 62 Lampiran 10. Perhitungan Reaksi Modifikasi Etil ρ-metoksisinamat………………………. 64 xv UIN Syarif Hidayatulah Jakarta DAFTAR ISTILAH APMS : Asam ρ-metoksisinamat EMK : Etil Metil Keton EPMS : Etil ρ-metoksisinamat g : Gram GCMS : Gas Cromatography Mass Spectrometry KLT : Kromatografi Lapis Tipis mg : Mili gram MS : Mass Spectrometry NaOH : Natrium hidroksida NMR : Nuclear Magnetic Resonance UV-Vis : Ultra Violet-Visible xvi UIN Syarif Hidayatullah Jakarta BAB 1 PENDAHULUAN 1.1 Latar Belakang Indonesia merupakan negara yang beriklim tropis dengan keanekaragaman hayati terbesar kedua di dunia setelah Brazil. Indonesia memiliki sekitar 25.00030.000 spesies tanaman yang merupakan 80% dari jenis tanaman di dunia dan 90% dari jenis tanaman di Asia (Pramono E, 2002; Erdelen, 1999). Tanaman merupakan bahan baku yang banyak digunakan sebagai obat herbal. Hal tersebut tentunya menjadi potensi besar yang harus dikembangkan dan dimanfaatkan untuk menunjang sektor kesehatan dalam rangka meningkatkan derajat kesehatan dan kesejahteraan bangsa Indonesia (BPOM RI, 2014). Sekitar 9.600 spesies tanaman merupakan tanaman yang memiliki khasiat sebagai obat dengan kurang lebih 300 spesies tanaman telah digunakan sebagai bahan baku obat tradisional oleh industri di Indonesia (Depkes RI, 2007). Kencur (Kaempferia galanga L.) merupakan salah satu tanaman di Indonesia yang berpotensi sebagai obat. Kencur termasuk ke dalam famili Zingiberaceae dan merupakan tanaman asli India yang penyebarannya sudah memasuki kawasan Asia Tenggara termasuk Indonesia. Kencur secara empiris telah dimanfaatkan dalam mengobati berbagai penyakit seperti radang lambung, radang anak telinga, influenza pada bayi, masuk angin, sakit kepala, batuk, memperlancar haid, mata pegal, keseleo, diare, menghilangkan darah kotor dan mengusir lelah (Al-Fattah, 2011). Sebelumnya telah dilaporkan penelitian mengenai aktivitas kencur, diantaranya adalah aktivitas ekstrak minyak atsiri kencur sebagai antibakteri dan antifungi (Tewtrakul et al., 2005), aktivitas ekstrak etanol kencur sebagai penyembuh luka (Tara et al., 2006), ekstrak air dari kencur yang memiliki aktivitas sebagai antinosiseptif dan antiinflamasi (Sulaiman et al., 2008), aktivitas kencur sebagai antioksidan (Mekseepralard, 2010), aktivitas ekstrak etanol kencur sebagai analgesik dan antiinflamasi (Vittalro et al., 2011) dan efek toksisitas ekstrak metanol kencur terhadap larva dan pupa Anopheles stephensi (Dhandapani et al., 2011). 1 UIN Syarif Hidayatullah Jakarta 2 Kandungan metabolit sekunder ekstrak kencur diantaranya adalah etil pmetoksisinamat (80,05 %), beta-sitosterol (9,88%), asam propionat (4,71%), pentadekan (2,08%), asam tridekanoat (1,81) dan 1,21-docosadiene (1,47%). Etil pmetoksisinamat (EPMS) merupakan senyawa utama dalam kencur yang memiliki aktivitas antiinflamasi melalui penghambatan COX-1 (42,9%) dan COX-2 (57,82%), dengan masing-masing nilai IC50 1,12 μM dan 0,83 μM (Umar et al., 2012). Efek terapi antiinflamasi non steroid (AINS) berhubungan dengan mekanisme kerja penghambatan pada enzim siklooksigenase-1 (COX-1) yang dapat menyebabkan efek samping pada saluran cerna dan penghambatan pada enzim siklooksigenase-2 (COX-2) yang dapat menyebabkan efek samping pada sistem kardiovaskular. Kedua enzim tersebut dibutuhkan dalam biosintesis prostaglandin pada saat terjadi inflamasi (Lelo dan Hidayat, 2004). Oleh karena itu, pada dekade terakhir ini desain dan sintesis obat antiinflamasi khususnya golongan AINS banyak mengambil perhatian ahli kimia medisinal. Maka dilakukan banyak sekali modifikasi pada AINS seperti memberikan elaborasi konjugat gugus tertentu sesuai tujuan khusus (Qandil, 2012). Senyawa etil p-metoksisinamat mudah diisolasi dan merupakan senyawa yang sangat potensial sebagai bahan dasar sintesa karena mempunyai gugus fungsi reaktif seperti ester dan olefin yang mudah ditransformasikan menjadi gugus fungsi yang lain (Surbakti, 2008). Penelitian mengenai modifikasi etil p-metoksisinamat telah banyak dilakukan diantaranya adalah modifikasi melalui reaksi hidrolisis, reaksi transesterifikasi, dan reaksi degradasi sinamat (Mufidah, 2014), reaksi reduksi (Qudsi, 2014), proses nitrasi (Indriyani, 2015; Aulia, 2015) dan reaksi amidasi (Reza, 2015). Namun belum dilakukan penelitian modifikasi etil p-metoksisinamat melalui reaksi kondensasi aldol. Kondensasi aldol merupakan reaksi suatu aldehid yang diolah dengan basa seperti NaOH dalam air, sehingga membentuk ion enolat yang akan bereaksi dengan suatu molekul aldehid lain atau keton dengan cara mengadisi pada karbon karbonil (Fessenden, 1982). Pada penelitian ini akan dilakukan modifikasi etil pmetoksisinamat yaitu dengan merubah gugus ester menjadi gugus keton melalui UIN Syarif Hidayatullah Jakarta 3 reaksi kondensasi aldol. Gugus ester mudah terhidrolisis sehingga dapat merubah etil p-metoksisinamat (EPMS) menjadi asam p-metoksisinamat (APMS). Perubahan senyawa EPMS menjadi APMS dapat menghilangkan aktivitas antiinflamasi (Mufidah, 2014). Pada kurkumin terdapat gugus diketon dan ikatan rangkap yang berperan dalam aktivitas biologis sebagai antiinflamasi, antikanker dan antimutagenik (Da’i, 2003). Senyawa aldehid dalam reaksi kondensasi aldol ini diperoleh dengan terlebih dahulu menghidrolisis etil p-metoksisinamat sehingga membentuk asam pmetoksisinamat yang kemudian akan di oksidasi sehingga didapatkan senyawa aldehid yaitu 4-metoksibenzaldehid. Berdasarkan hasil uji pendahuluan, etil pmetoksisinamat bila langsung di oksidasi akan menghasilkan senyawa lain yang lebih banyak dibandingkan dengan mengoksidasi asam p-metoksisinamat. Oleh karena itu, etil p-metoksisinamat dihidrolisis terlebih dahulu menjadi asam p-metoksisinamat. Senyawa 4-metoksibenzaldehid yang didapat akan direaksikan dengan etil metil keton melalui reaksi kondensasi aldol dengan bantuan basa natrium hidroksida (NaOH) dalam air. Reaksi kondensasi aldol dilakukan dengan menstirer campuran pada suhu ruang. 1.2 Rumusan Masalah Apakah struktur etil p-metoksisinamat dapat dimodifikasi melalui reaksi kondensasi aldol dengan etil metil keton ? 1.3 Tujuan Penelitian Melakukan modifikasi struktur etil p-metoksisinamat melalui reaksi kondensasi aldol. 1.4 Manfaat Penelitian Memberikan data ilmiah tentang metode dan produk modifikasi struktur etil pmetoksisinamat melalui reaksi kondensasi aldol. UIN Syarif Hidayatullah Jakarta BAB 2 TINJAUAN PUSTAKA 2.1 Tumbuhan Kencur Kencur (Kaempferia galanga L.) merupakan tanaman tropis yang banyak tumbuh diberbagai daerah di Indonesia sebagai tanaman yang dipelihara (Barus, 2009). Tanaman ini diperkirakan berasal dari India (Rukmana, 1994). Terdapat dua tipe pertumbuhan, yang pertama berdaun lebar dan terhampar diatas tanah dan yang kedua berdaun sempit dan agak tegak. Bagian dari kencur yang digunakan adalah rimpang (Depkes, 1989). Tanaman kencur tidak berbatang, rimpang bercabang-cabang, akar-akar berbentuk gelendong, kadang-kadang berumbi, panjang 1-1,5 cm. Berdaun sebanyak 1-3 (umunya 2 helai), lebar merata, berbentuk jantung, ujung lancip, bagian atas tidak berbulu, bagian bawah berbulu halus, pinggir bergelombang berwarna merah kecoklatan, bagian tengah berwarna hijau, panjang helai daun 715 cm, lebar 2-8 cm, dan tangkai pendek. Panjang bunga 4 cm dan mengandung 4-12 bunga (Depkes, 1977). 2.1.1. Klasifikasi Klasifikasi Kaempferia galanga L. di dalam dunia botani adalah sebagai berikut (Barus, 2009) : Kerajaan : Plantae Divisi : Spermathophyta Sub divisi : Angiospermae Kelas : Monocotyledonae Bangsa : Zingiberales Suku : Zingiberaceae Subfamilia : Zingiberoideae Marga : Kaempferia Jenis : Kaempferia galanga L. 2.1.2. Tempat Tumbuh Tumbuh di India, Malaysia dan India. Dapat ditanam ditempat rendah dan dipergunungan.Menghendaki tanah yang subur, gembur dan ditempat 4 UIN Syarif Hidayatullah Jakarta 5 yang sedikit terlindung. Di Indonesia, Kencur dapat tumbuh di Sumatra, Jawa, Nusa tenggara, Sulawesi, Maluku, dan Irian (Depkes, 1977). Produksi, mutu dan kandungan bahan aktif didalam rimpang kencur ditentukan oleh varietas, cara budidaya dan lingkungan tempat tumbuhnya (Muhlisah, 1999). 2.1.3. Kandungan Kimia Tanaman kencur terdapat kandungan minyak atsiri 2,4%-3,9%, borneol, kamfer, sineol dan etil alkohol (Depkes, 1989). Dalam penelitian Umar et al. (2012), menyebutkan bahwa kandungan senyawa kimia dalam ekstrak kencur adalah etil p-metoksisinamat (80,05%), asam propionat (4,71%), pentadekan (2,08%), asam tridekanoat (1,81%), 1,21-docosadiene (1,47%) dan beta-sitosterol (9,88). Selain itu, pada penelitian Tewtrakul et al. (2005) juga disebutkan bahwa terdapat kandungan α-pinen, kamphen, karvon, benzen, eukalipton, borneol dan metil sinamat. Kandungan kimia rimpang kencur yang telah dilaporkan oleh Afriastini (1990) yaitu (1) etil sinamat, (2) etil p-metoksisinamat, (3) p-metoksistiren, (4) karen, (5) borneol dan (6) parafin. Gambar 2.1. Kandungan kimia rimpang kencur (Afriastini, 1990). 2.1.4. Manfaat Tanamana kencur banyak digunakan sebagai ramuan obat tradisional dan sebagai bumbu masakan (Barus, 2009).Kencur dapat digunakan sebagai obat batuk, obat gosok (sakit kulit) dan sakit perut (Depkes, 1989). Ekstrak kencur banyak memiliki aktivitas diantaranya yaitu ekstrak alkohol sebagai antiinflamasi dan analgesik (Vittalrao et al., 2011) serta sebagai penyembuh luka (Tara et al., 2006), ekstrak air sebagai antinosiseptif dan antiinflamasi UIN Syarif Hidayatullah Jakarta 6 (Sulaiman et al., 2008), ekstrak metanol sebagai repellent dan memiliki toksisitas terhadap larva dan pupa Anopheles stephensi (Dhandapani et al., 2011), dan ekstrak minyak atsiri kencur meiliki aktivitas antimikroba dan antifungi (Tewtrakul et al., 2005). 2.2 Senyawa Etil p-metoksisinamat Senyawa etil p-metoksisinamat (EPMS) merupakan salah satu senyawa hasil isolasi rimpang kencur (Kaempferia galanga, L) dengan jumlah yang relatif banyak (Barus, 2009). Senyawa EPMS berbentuk kristal putih kekuningan, berbau khas dengan berat molekul 206 g/mol dan memiliki titik lebur 47-520C (Mufidah, 2014). Gambar 2.2 Jalur asam sikhimat dalam biosintesa fenilpropanoid untuk menghasilkan etil p-metoksisinamat (Bangun, 2011). UIN Syarif Hidayatullah Jakarta 7 EPMS termasuk senyawa ester yang memiliki cincin benzena dan gugus metoksi yang bersifat nonpolar serta gugus karbonil yang mengikat etil yang bersifat sedikit polar sehingga dalam ekstraksinya dapat menggunakan pelarut dengan variasi kepolaran. EPMS lebih larut dalam pelarut heksan karena terdapat dua gugus yang mendukung sifat nonpolar sedangkan hanya satu gugus yang mendukung sifat polar (Tufikhurohmah et al., 2008). Etil p-metoksisinamat merupakan turunan asam sinamat sehingga biosintesanya melalui jalur biosintesis asam sikhimat (Bangun, 2011). 2.3 Modifikasi Struktur EPMS Senyawa etil p-metoksisinamat mudah diisolasi dan merupakan senyawa yang sangat potensial sebagai bahan dasar sintesa karena mempunyai gugus fungsi reaktif seperti ester dan olefin yang mudah ditransformasikan menjadi gugus fungsi yang lain (Surbakti, 2008). Derivat EPMS memiliki aktivitas sebagai tabir surya, antara lain S-Sorboil-2-merkaptoetil p-metoksisinamida dan SCrotonil-2-merkaptoetil p-metoksisinamamida (Hanson et al., 2006). Gambar 2.3 Beberapa trasformasi gugus fungsi dari EPMS (Ekowati et al., 2009) Perubahan gugus asam karboksilat APMS menjadi amida menunjukkan aktivitas biologis berupa sedasi pada hewan coba mencit (Ekowati et al., 2009). Perubahan ikatan rangkap vinilik pada APMS menjadi ikatan tunggal dengan reaksi hidrogenasi, akan menurunkan aktivitas analgesik senyawa tersebut (Ekowati et al., 2007). Beberapa penelitian telah dilakukan terkait modifikasi struktur EPMS dengan substitusi gugus amina, diantaranya modifikasi struktur EPMS melalui proses amidasi dengan etanolamin (Barus, 2009) dan amidasi UIN Syarif Hidayatullah Jakarta 8 dietanolamin (Bangun, 2011) dengan cara konvensional dan dengan iradiasi microwave (Ferround et al., 2008; Khalafi et al., 2003). 2.4 Optimasi Reaksi Kimia Menurut Kamus Besar Bahasa Indonesia, optimalisasi berasal dari kata optimal yang berarti terbaik dan tertinggi (Depdikbud, 1995). Reaksi kimia (chemical reaction) yaitu suatu proses dimana zat atau senyawa diubah menjadi satu atau lebih senyawa baru (Chang, 2004). Laju (kecepatan) menyatakan sesuatu yang terjadi persatuan waktu, misalnya perdetik, permenit, dan lain-lain.Yang terjadi dalam reaksi kimia adalah perubahan jumlah pereaksi dan hasil reaksi.(Petrucci, 1987). Kinetika kimia membahas tentang laju reaksi dan mekanisme terjadinya reaksi. Mekanisme adalah serangkaian reaksi-reaksi sederhana yang menerangkan reaksi keseluruhan. Untuk mengetahui mekanisme suatu reaksi, dipelajari perubahan laju yang disebabkan oleh perbedaan konsentrasi pereaksi, hasil reaksi dan katalis. Keterangan yang penting dapat pula diperoleh dari studi tentang suhu, tekanan, pelarut, konsentrasi elektrolit atau komposisi isotopik terhadap laju reaksi (Sukardjo, 1986). Ada enam faktor yang memperngaruhi laju reaksi yaitu (Goldberg, 2002) : 1. Sifat alami reaktan. Sifat ini adalah sifat yang paling tidak dapat dikontrol oleh ahli kimia. 2. Suhu. Secara umum, semakin tinggi suhu sistem, akan semakin cepat reaksi kimia berlangsung. 3. Kehadiran katalis. Katalis adalah zat yang dapat mempercepat reaksi kimia tanpa mengubah komposisinya. 4. Konsentrasi reaktan. Secara umum, semakin tinggi konsentrasi reaktan, akan semakin cepat pula reaksinya. 5. Tekanan reaktan gas. Secara umum, semakin tinggi tekanannya, akan semakin cepat reaksinya. 6. Wujud partikel molekul. Semakin kecil ukuran reaktan padat, semakin kecil wujud partikel molekulnya dan akan semakin cepat reaksinya. pH adalah suatu ukuran keasaman suatu air (larutan). Laju reaksi dalam larutan berair sangat mudah dipengaruhi oleh adanya pH sebagai akibat adanya UIN Syarif Hidayatullah Jakarta 9 proses katalisis. Untuk mengetahui pengaruh pH maka faktor-faktor lainnya yang berpengaruh seperti suhu, kekuatan ionik dan komposisi pelarut harus dibuat tetap (Arisandi, 2008). 2.5 Hidrolisis Hidrolisis merupakan proses transformasi kimia suatu molekul organik berupa RX yang akan bereaksi dengan air sehingga menghasilkan sebuah struktur dengan ikatan kovalen OH. Hidrolisis disebut juga reaksi perpindahan nukleofilik yang menyerang atom elektrofilik.Mekanisme reaksi yang sering ditemui substitusi nukleofilik baik secara langsung maupun tidak langsung dan eliminasiadisi nukleofilik (Larson dan Weber, 1994). RX + H2O ROH + X- + H+ Gambar 2.4 Prinsip reaksi hidrolisis (Larson dan Weber, 1994). Reaksi hidrolisis dapat terjadi dengan katalis basa atau asam.Mekanisme hidrolisis ester dalam suasana basa disebut saponifikasi.Hal tersebut terjadi akibat adanya adisi nukleofilik OH ke karbonil ester, menjadi intermediet alkoksida tetrahedral(1). Kemudian adanya proses tersebut menyebabkan keluarnya ion alkoksi menghasilkan asam karboksilat (2). Ion alkoksida menarik proton dari asam karboksilat menjadi ion karboksilat (3).Setelah itu terjadi protonasi ion karboksilat oleh asam mineral menghasilkan asam karboksilat (4) (Riswiyanto, 2009). Gambar 2.5 Mekanisme hidrolisis ester dalam suasana basa (Riswiyanto, 2009). Mekanisme hidrolisis ester dalam suasana asam dapat dilakukan namun tidak hanya menghasilkan asam karboksilat saja melainkan menghasilkan asam karboksilat dan alkohol.Pada suasana asam, protonasi gugus karbonil terjadi untuk engaktifkan (1).Kemudian terjadi serangan nukleofilik oleh air menjadi UIN Syarif Hidayatullah Jakarta 10 intermediet tetrahedral (2). Hal tersebut menyebabkan terjadinya transfer proton yang kemudian mengubah OR menjadi gugus pergi yang baik (3). Kemudian terjadi pelepasan alcohol menghasilkan asam karboksilat dan katalis asam (4) (Riswiyanto, 2009). Gambar 2.6 Mekanisme hidrolisis ester dalam suasana asam (Riswiyanto, 2009). 2.6 Oksidasi Alkena Alkena dapat dioksidasi menjadi anekaragam produk, bergabung pada reagensia yang digunakan. Reaksi yang melibatkan oksidasi ikatan rangkap karbon-karbon dapat dikelompokkan menjadi dua gugus umum : (1) oksidasi ikatan pi tanpa pemutusan ikatan sigma dan (2) oksidasi ikatan pi yang memutus ikatan sigma (Fessenden, 1982). π (1) σ (2) Gambar 2.7 Reaksi Oksidasi alkena (Fessenden, 1982). Produk oksidasi dengan pemaksapisahan (cleavage) bergantung pada kondisi oksidasi dan struktur alkena. Pertama-tama akan diperhatikan struktur alkena. Wajah strutural alkena yang menentukan produk pemaksapisahan UIN Syarif Hidayatullah Jakarta 11 oksidatif ialah adanya atom hidrogen pada karbon sp2. Jika tiap karbon alkena tidak mengikat atom hidrogen (artinya, tiap atom karbon alkena tersubstitusi), maka pemaksapisahan oksidatif akan menghasilkan sepasang molekul keton. Gambar 2.8 Reaksi pemaksapisahan oksidatif pada disubstitusi (Fessenden, 1982). Sebaliknya, jika tiap karbon alkena mempunyai satu hidrogen yang terikat padanya, maka produk pemaksapisahan oksidatif akan berupa aldehida atau asam karboksilat atau asam karboksilat, bergantung kondisi reaksi (Fessenden, 1982). Gambar 2.9 Reaksi pemaksapisahan oksidatif pada monosubstitusi (Fessenden, 1982). Jika satu sisi ikatan rangkap itu tersubstitusi, sedangkan sisi yang lain termonosubstitusi, maka pemaksapisahan oksidatif akan menghasilkan suatu keton dari sisi disubstitusi, dan suatu aldehida atau asam karboksilat dari sisi monosubstitusi (Fessenden, 1982). Gambar 2.10 Reaksi pemaksapisahan oksidatif pada disubstitusi dan monosubstitusi (Fessenden, 1982). 2.7 Kondensasi Aldol Bila suatu senyawa aldehida dioleh dengan basa seperti NaOH dalam air, ion enolat yang terjadi dapat bereaksi pada gugus karbonil lain dari molekul aldehida yang lain. Hasilnya ialah adisi satu molekul aldehida ke molekul UIN Syarif Hidayatullah Jakarta 12 aldehida lain. Reaksi tersebut disebut reaksi kondensasi aldol.Kata “aldol” yang diturunkan dari aldehida dan alcohol, memerikan produ itu, yang merupakan suatu aldehida β-hidroksi.Suatu reaksi kondensasi ialah reaksi di mana dua molekul atau lebih bergabung menadi satu molekul yang lebih besar, dengan atau tanpa hilangnya suatu molekul kecil (seperti air). Kondensasi aldol merupakan suatu reaksi adisi di mana tidak dilepaskan suatu molekul kecil (Fessenden, 1982). Suatu kondensasi aldol berlangsung dengan mereaksikan aldehida yang diolah dengan larutan natrium hidroksida berair sehingga terbentuk ion enolat. Ion enolat bereaksi dengan suatu molekul aldehida lain dengan cara mengadisi pada karbon karbonil untuk membentuk suatu ion alkoksida, yang kemudian merebut sebuah proton dari dalam air untuk menghasilkan aldol produk itu.Aldehida awal dalam kondensasi aldol harus mengandung satu hidrogen yang berposisi α terhadap gugus karbonil sehingga aldehida ini dapat membentuk ion enolat dalam basa (Fessenden, 1982). (1) (2) (3) Gambar 2.11 Mekanisme reaksi kondensasi aldol (Solomons, 2013) Keterangan : (1) Pembentukan enolat, (2) Adisi enolat, dan (3) Protonasi alkoksida Suatu aldehida tanpa hidrogen α tidak dapat membentuk ion enolat dan demikian tidak dapat berdimerisasi dalam suatu kondensasi aldol.Namun aldehida tersebut dapat dicampur dengan aldehida yang memiliki hidrogen alfa, maka kondensasi antara keduanya dapat terjadi.Reaksi ini disebut kondensasi aldol UIN Syarif Hidayatullah Jakarta 13 silang (cross aldol condensation).Suatu kondensasi aldol silang juga dapat terjadi antara aldol dengan keton (Fessenden, 1982). Suatu senyawa karbonil β-hidroksi, seperti suatu aldol, mudah mengalami dehidrasi, karena ikatan rangkap dalam produk berkonjugasi dengan gugus karbonilnya. Oleh karena itu, suatu aldehida α,β-tak jenuh dapat dengan mudah diperoleh sebagai produk suatu kondensasi aldol. Bila dehidrasi menghasilkan suatu ikatan rangkap yang berkonjugasi dengan suatu cincin aromatik, seringkali dehidrasi itu berlangsung sertamerta (spontan), bahkan juga dalam larutan basa (Fessenden, 1982). Gambar 2.12 Mekanisme dehidrasi aldol (Solomons, 2013). 2.8 Natrium Hidroksida Natrium hidroksida merupakan pellet, serpihan atau batang berwarna putih atau praktis putih yang dapat melebur. Bila dibiarkan di udara, akan cepat menyerap karbon dioksida dan lembab. Natrium hidroksida berupa massa keras, rapuh dan menunjukkan pecahan hablur (Depkes RI, 1995). Natrium hidroksida merupakan basa kuat sehingga biasa digunakan untuk membuat suasana basa dalam suatu reaksi.Pada reaksi kondensasi aldol, natrium hidroksida digunakan untuk membentuk ion enolat sehingga dapat berikatan dengan senyawa elektrofilik (Fessenden, 1982). Sifat-sifat natrium hidroksida adalah sebagai berikut (Depkes RI, 1995; HOPE, 2009) : Rumus molekul : NaOH. Berat molekul : 40 g/mol. Kelarutan : mudah larut dalam air (1 dalam 0,9 bagian pada 20oC, 1 dalam 0,3 pada 100oC) dan etanol (1 dalam 7,2 bagian pada 20oC). pH : 12 (0.05% w/w); 13 (0,5% w/w) dan 14 (5% w/w). Titik lebur : 318oC. UIN Syarif Hidayatullah Jakarta 14 Gambar 2.13 Struktur natrium hidroksida (Pubchem). 2.9 Kalsium Nitrat Kalsium nitrat disebut juga Norgessalpeter (Norwegia sendawa) merupakan senyawa organikdengan rumus Ca(NO3)2. Senyawa ini tidak berwarna dan dapat menyerap kelembaban dari udara dan biasanya ditemukan sebagai tertrahidrat.Sifat-sifat dari kalsium nitrat adalah sebagai berikut (Pubchem) : Rumus Kimia : Ca(NO3)2 Masa molar : 164,088 g/mol (anhidrat), 236,15 g/mol (tetrahidrat). Penampilan : Kristal tidak berwarna sampai putih, padat, dan higroskopis. Masa jenis : 2,504 g/cm3 (anhidrat), 1,896 g/cm3 (tetrahidrat). Titik lebur : 561οC (1042οF; 834οK) (anhidrat), 42,7 C (109οF; 316οK) (tetrahidrat). Kelarutan dalam air : anhidrat : 1212 g/L (20οC), 2710 g/L (40οC); tetrahidrat: 1050 g/L (0οC), 1290 g/L (20οC), 3630 g/L (100οC). Kelarutan : larut dalam ammonia, hampir tidak larut dalam HNO3. Kelarutan dalam etanol : 51,4 g/100 g (20οC); 62,9 g/100 g (40οC). Kelarutan dalam aseton : 16,8 g/kg (20οC) Keasaman (pKa) :6 Gambar 2.14 Struktur kalsium nitrat (Pubchem). 2.10 Asam Asetat Glasial Asam asetat glasial mengandung tidak kurang dari 99,5% dan tidak lebih dari 100,5 % b/b C2H4O2. Asam asetat glasial merupakan cairan bening atau kristal, tidak berwarna, berbau khas, menusuk, dan mempunyai rasa asam jika UIN Syarif Hidayatullah Jakarta 15 dienceran dengan air. Asam asetat glasial mendidih pada suhu lebih kurang 118οC dan mempunyai bobot jenis lebih kurang 1,05 g/cm3 (Depkes RI, 1995).Asam asetat diproduksi untuk cuka konsumsi rumah tangga yang mengandung 3-9% asam asetat glasial.Selain itu, asam asetat juga diproduksi sebagai precursor untuk polivinil asetat dan selulosa asetat.Asam asetat pekat (asam asetat glasial) bersifat korosif dan dapat menyerang kulit (Pubchem). Sifat-sifat dari asam asetat adalah sebagai berikut (Depkes RI, 1995; Pubchem) : Rumus molekul : C2H4O2 Nama lain : Asetil hidroksida (AcOH); asam metanakarboksilat. Berat molekul : 60,05 g/mol. Kelarutan : Dapat bercampur dengan air, etanol, da gliserol. Suhu beku : Tidak lebih rendah dari 15,6οC. Titik lebur : 289 sampai 290 K. pKa : 4,76. Gambar 2.15 Struktur asam asetat (Pubchem). 2.11 Etil Metil Keton Etil metil keton (EMK) atau 2-butanon merupakan senyawa organik berupa cairan bening, berbau tajam, berbau manis seperti butterscotch dan aseton. EMK larut dalam air dan biasanya digunakan sebagai pelarut industri (Pubchem). Sifat-sifat dari etil metil keton adalah sebagai berikut (Pubchem) : Nama Lain :2-butanon, metilpropanon, metil asetoon. Rumus kimia : C4H5O Masa molar : 72,11 g/mol Masa jenis : 0,8050 g/mL Titik lebur : -86C (-123F; 187K). Titik didih : 79,64C (175,35F; 352,79K). Kelarutan dalam air : 27,5 g/100 mL. Gambar 2.16 Struktur Etil Metil Keton (Pubshem). UIN Syarif Hidayatullah Jakarta 16 2.12 Iradiasi Microwave Gelombang mikro merupakan radiasi elektromagnetik yang terletak diantara frekuensi radiasi inframerah dan radio, dengan panjang gelombang mulai dari 1 mm hingga 1 m, frekuensinya mulai dari 300 GHz hingga 300 MHz (Bogdal, 2005; Loupy, 2006). Ketika sebuah bahan logam dipaparkan radiasi microwave, microwave akan secara luas menyebar pada permukaan, namun benda tersebut tidak dipanaskan dengan menggunakan microwave melainkan karena adanya respon dari medan magnet dari radiasi microwave yaitu elektron bergerak bebas pada permukaan bahan, dan aliran electron tersebut dapat menghasilkan panas (Bogdal, 2005). Reaksi dengan menggunakan microwave dapat dikategorikan sebagai green chemistry. Tujuan dari green chemistry adalah untuk mengurangi atau meminimalkan penggunaan dari pelarut yang mudah menguap dalam sintesis modern dan mengurangi penggunaan energi. Pengembangan dari metode sintesis baru bebas pelarut dengan menggunakan bantuan microwave saat ini menjadi topik penting dalam penelitian, karena reaksi bebas pelarut mengurangi penggunaan pelarut, prosedur sintesis dan pemisahan yang lebih sederhana, mencegah pemborosan dan menghindari resiko bahaya atau toksik terkait dengan penggunaan pelarut (Loupy, 2006). Semua peralatan standar (Oven domestik atau reactor lebih spesifik yang didedikasikan untuk sintesis kimia) beroperasi pada frekuensi dari v = 2,45 GHz (setara dengan ƛ = 12,2 cm) untuk mengurangi intervensi dari frekuensi radio dan radar. Reaksi kimia dengan microwave didasarkan pada interaksi dari molekul dengan gelombang oleh efek “microwave dielectric heating”. Fenomena ini bergantung pada kemampuan suatu bahan untuk mengabsobsi radiasi microwave dan mengubahnya menjadi panas. Komponen elektrik dari medan elektromagnetik telah menunjukkan bahwa perannya sangat penting. Dalam hal tersebut, maka reaksi yang terjadi melibatkan dua mekanisme yaitu polarisasi dipolar dan konduksi ionik. Iradiasi dari senyawa polar pada frekuensi microwave meghasilkan orientasi dari dipol atau ion pada medan listrik (Loupy, 2006). Untuk produk cair (contohnya pelarut), hanya molekul polar yang secara selektif mengabsorbsi gelombang mikro, sedangkan molekul nonpolar tidak UIN Syarif Hidayatullah Jakarta 17 bereaksi (inert).Pada konteks dari absorbsi gelombang mikro, telah menunjukkan bahwa titik didih lebih tinggi ditemukan ketika pelarut diberikan iradiasi microwave daripada pemanasan biasa. Efek ini dikenal dengan “super heating effect” yang telah ditujukan untuk penghambatan dari nukleasi dalam pemanasan microwave (Loupy, 2006). 2.12.1 Mekanisme Reaksi Secara Polarisasi Dipolar Prinsip dari mekanisme reaksi polarisasi dipolar adalah adanya interaksi dipol-dipol antara molekul-molekul polar ketika di radiasi dengan microwave. Molekul yang berinteraksi dipol tersebut sangat sensitif terhadap suatu medan magnet yang berasal dari luar sehingga dapat mengakibatkan terjadinya rotasi pada molekul tersebut sehingga menghasilkan sejumlah energi (Lidstrom et al., 2001; Loupy, 2006). 2.12.2 Mekanisme Reaksi Secara Konduksi Mekanisme secara konduksi dapat terjadi pada larutan-larutan yang mengandung ion. Bila suatu larutan mengandung suatu partikel bermuatan atau ion yang berikatan dengan suatu medan listrik maka ion-ion tersebut akan bergerak. Pergerakan tersebut akan menyebabkan terjadinya peningkatan kecepatan dari tumbukanantar molekul sehingga akan merubah energi kinetik menjadi energi kalor (Kingson, 1988). 2.13 Identifikasi 2.13.1 Kromatografi Kromatografi pertama kali dikembangkan oleh seorang ahli botani Rusia Michael Tswett pada tahun 1903 untuk memisahkan pigmen berwarna dalam tanaman dengan cara perkolasi ekstrak petroleum eter dalam kolom gelas yang berisi kalsium karbonat (CaCO3) (Gandjar dan Rohman, 2007). Kromatografi merupakan metode fisika untuk pemisahan komponenkomponen dengan mendistribusikannya diantara dua fase, salah satunya merupakan lapisan stasioner dengan permukaan yang luas dan fase lainnya berupa zat alir (fluid) yang mengalir lambat (perkolasi) sepanjang lapisan stasioner tersebut. Fase stasioner dapat berupa zat padat atau cairan dan fase geraknya dapat berupa cairan atau gas (Underwood, 1989). UIN Syarif Hidayatullah Jakarta 18 Kromatografi dapat dibedakan berdasarkan mekanisme pemisahannya menjadi kromatografi adsorpsi, kromatografi partisi, kromatografi penukar ion, kromatografi pasangan ion dan kromatografi eksklusi ukuran.Berdasarkan pada alat yang digunakan, kromatografi dapat dibagi menjadi kromatografi planar yaitu kromatografi kertas dan kromatografi lapis tipis, kromatografi cair kinerja tinggi (KCKT) dan kromatografi gas (KG) (Gandjar dan Rohman, 2007).Menurut Farmakope Indonesia, jenis-jenis kromatografi tersebut dan kromatografi kolom bermanfaat dalam analisis kualitatif dan kuantitatif yang digunakan dalam penetapan kadar dan pengujian. Kromatografi kertas dan kromatografi lapis tipis umumnya lebih bermanfaat untuk tujuan identifikas karena sederhana dan mudah.(Depkes, 1995). a. Kromatografi Lapis Tipis Kromatografi lapis tipis (KLT) dikembangkan oleh Izmailoff dan Schraiber pada tahun1938 (Gandjar dan Rohman, 2007).Kromatografi lapis tipis merupakan metode pemisahan fisikokimia.Lapisan yang memisahkan terdiri atas bahan berbutir-butir (fase diam) yang ditempatkan pada penyangga berupa pelat gelas atau lapisan yang cocok.Pelat fase diam tersebut diletakkan di dalam bejana tertutup rapat yang berisi larutanpengembang yang cocok (fase gerak) dan terjadi pemisahan dengan caraperambatan kapiler (pengembangan).Selanjutnya senyawa yang tidak berwarna harus ditampakkan (dideteksi) (Stahl Egon dalam Khoirunni’mah, 2013). Fase diam yang digunakan dalam KLT merupakan penjerap kecil dan seragam (uniform) dengan diameter partikel antara 10-30 um. Semakin kecil ukuran dan semakin sempit kisaran ukuran fase diam, maka semakin baik kinerja KLT dalam hal resolusi dan efisiensinya.Penjerap yang paling sering digunakan adalah silika dan serbuk selulosa, sementara mekanisme sorpsi yang utama pada KLT adalah partisi dan absorpsi.Fase gerak pada KLT dapat dipilih dari pustaka, tetapi lebih sering dengan mencoba-coba karena waktu yang diperlukan hanya sebentar.Sistem yang paling sederhana adalah campuran dua pelarut organik karena daya elusi campuran dua pelarut UIN Syarif Hidayatullah Jakarta 19 tersebut mudah diatur sehingga pemisahan dapat terjadi secara optimal (Gandjar dan Rohman, 2007). Pemilihan dan pengoptimasian fase gerak harus memperhatihan hal sebagai berikut : 1) KLT merupakan teknik yang sensitif sehingga fase gerak yang digunakan harus memiliki kemurnian yang sangat tinggi. 2) Daya elusi fase gerak harus diatur untuk memaksimalkan pemisahan dimana harga Rf terletak antara 0,2-0,8. 3) Untuk pemisahan dengan menggunakan fase diam yang bersifat polar seperti silika gel, polaritas fase gerak akan menentukan kecepatan migrasi solut sehingga dapat menentukan nilai Rf. Penambahan pelarut yang bersifat sedikit polar seperti dietil eter ke dalam pelarut non polar seperti metil benzena akan meningkatkan harga Rf secara signifikan. 4) Solut-solut ionik dan polar lebih baik digunakan campuran pelarut sebagai fase geraknya, seperti campuran air dan metanol dengan perbandingan tertentu. Penambahan sedikit asam etanoat akan membuat solut bersifat asam, sedangkan penambahan dengan ammonium akan membuat solut besifat basa (Gandjar dan Rohman, 2007). Penotolan larutan uji dan larutan baku berdasarkan cara yang tertera pada masing-masing monografi dengan jarak antara lebih kurang 1,5 cm dan lebih kurang 2 cm dari tepi bawah lalu lempeng dibiarkan hingga mengering. Ketika bekerja dengan lempeng harus menghindarkan zat penjerap dari gangguan fisik.Pada jarak 10 cm hingga 15 cm diatas titik penotolandiberi tanda.Lempeng ditempatkan pada rak penyangga hingga tempat penotolan terletak disebelah bawah lalu rak dimasukkan ke dalam bejana kromatografi (Depkes, 1995).Bejana kromatografi sebelumnya dijenuhkan dengan uap fase gerak dan tepi bagian bawah pelat yang telah ditotoli sampel dicelupkan kedalam fase gerak kurang lebih 0,5-1 cm. Tinggi fase gerak harus dibawah pelat yang telah berisi totolan sampel (Gandjar dan Rohman, 2007). Bejana di tutup hingga rapat dan dibiarkan hingga fase gerak merambat 10 cm hingga 15 cm di atas titik penotolan, umumnya diperlukan waktu lebih kurang 15 menit hingga 1 jam.Lempeng dikeluarkan dari bejana dan dibuat UIN Syarif Hidayatullah Jakarta 20 tanda batas rambat pelarut. Lempeng dikeringkan di udara dan bercak mulamula diamati dengan cahaya ultraviolet gelombang pendek (254 nm) dan kemudian dengan cahaya ultraviolet gelombang panjang (366 nm). Dilakukan pengukuran jarak tiap bercak dari titik penotolan serta dicatat panjang gelombang untuk tiap bercak yang diamati. Harga Rf bercak ditentukan laludibandingkan antara kromatogram larutan uji dengan larutan baku (Depkes, 1995). Gambar 2.17 Skema kromatografi lapis tipis Pendeteksian bercak-bercak yang umumnya tidak berwarna dapat dilakukan dengan pendeteksian secara kimia, fisika, maupun biologi. Cara kimia dilakukan dengan mereaksikan bercak dengan suatu pereaksi melalui cara penyemprotan sehingga bercak menjadi jelas. Cara fisika digunakan dengan pencacahan radioaktif dan fluoresensi sinar ultra violet (Gandjar dan Rohman, 2007). Mengidentifikasi bercak sangat lazim mengunakan harga Rf (Retordation Factor). Harga Rf mulai dari 0 sampai 1. Faktor-faktor yang mempengaruhi nilai Rf diantaranya struktur kimia dari senyawa yang sedang dipisahkan, tebal dan kerataan dari lapisan penjerap, sifat penjerap, teknik percobaan, pelarut dan derajat kemurniannya, derajat kejenuhan uap pengembang dalam bejana, jumlah cuplikan yang digunakan, kesetimbangan dan suhu (Sastrohamidjojo, 1985). Kromatografi lapis tipis telah luas dipergunakan dan merupakan cara pemisahan yang baik, khususnya untuk kegunaan analisis kualitatif. Kromatografi lapis tipis dapat digunakan untuk memisahkan berbagai senyawa seperti ion-ion organik, senyawa-senyawa organik baik yang UIN Syarif Hidayatullah Jakarta 21 terdapat di alam maupun sintetik dan kompleks senyawa-senyawa organik dengan anorganik (Adnan, 1997).Kromatografi lapis tipis juga telah banyak digunakan untuk analisis obat di laboratorium farmasi (Stahl Egon dalam Khoirunni’mah, 2013). Kromatografi lapis tipismempunyai kelebihan dibandingkan dengan kromatografi kertas yaitu pengerjaannya lebih cepat, hasil pemisahannya lebih sempurnadan kepekaannya lebih tinggi (Adnan, 1997).Kromatografi lapis tipis hanya membutuhkan perlengkapan yang sedikit dan waktu analisis yang singkat (15-60 menit), memerlukan jumlah cuplikan yang sangat sedikit (kira-kira 0,1 g). Selain itu, hasil palsu yang disebabkan oleh komponen sekunder tidak mungkin terjadi, kebutuhan ruangan minimum dan penanganannya sederhana (Stahl Egon dalam Khoirunni’mah, 2013). b. Kromatografi Gas Kromatografi gas (KG) yang dikenalkan pertama kali pada tahun 1950an merupakan suatu teknik instrumental dengan metode yang dinamis untuk pemisahan dan deteksi senyawa-senyawa organik yang mudah menguap dan senyawa-senyawa gas anorganik dalam suatu campuran. Kromatografi gas digunakan untuk analisis sampel-sampel padat, cair, dan gas.Sampel padat dapat diekstraksi atau dilarutkan dalam suatu pelarut sehingga dapat diinjeksikan ke dalam sistem KG, sedangkan sampel gas dapat lagsung diambil dengan penyuntik (syringe) yang ketat terhadap gas.Ruang suntik sampel biasanya berupa lubang yang ditutupi dengan septum atau pemisah karet. Suhu ruang suntik biasanya 10-150C lebih tinggi dari suhu kolom maksimum sehingga seluruh sampel akan segera menguap setelah disuntikkan (Gandjar dan Rohman, 2007). Fase gerak pada KG disebut juga gas pembawa karena digunakan hanya untuk membawa solut ke kolom dan tidak mempengaruhi selektifitas. Gas pembawa biasanya mengandung helium, nitrogen, hidrogen, atau campuran argon dan metana.Helium merupakan gas pembawa yang sering digunakan karena memberikan efisiensi kromatografi yang lebih baik (mengurangi pelebaran pita).Proses pemisahan terjadi pada kolom dimana terdapat fase diam didalamnya.Ada 2 jenis kolom pada KG yaitu kolom kemas (packing UIN Syarif Hidayatullah Jakarta 22 column) dan kolom kapiler (capillary column).Kolom kapiler lebih kecil dibanding kolom kemas.Semakin sempit diameter kolom, maka efisiensi pemisahan kolom semakin besar atau puncak kromatogram yang dihasilkan semakin tajam (Gandjar dan Rohman, 2007). Prinsip KG yaitu solut-solut yang mudah menguap (dan stabil terhadap panas) akanbermigrasi melalui kolom yang mengandung fase diam dengan suau kecepatan yang tergantung pada rasio distribusinya. Pada umumnya solut akan terelusi berdasarkan pada peningkatan titik didihnya, kecuali jika ada interaksi khusus antara solut dengan fase diam. Pemisahan pada kromatografi gas didasarkan pada titik didih suatu senyawa dikurangi dengan semua interaksi yang mungkin terjadi antara solut dengan fase diam. Fase gerak yang berupa gas akan mengelusi solut dari ujung kolom lalu menghantarkannya ke detektor. Penggunaan suhu yang meningkat (biasanya kisaran 50-3500C) bertujuan untuk menjamin bahwa solut akan menguap dan karenanya akan cepat terelusi.Kromatogram hasil pemisahan fisik komponenkomponen oleh KG disajikan oleh detektor sebagai deretan luas puncak terhadap waktu.Waktu dalam kromatogram dapat digunakan sebagai data kualitatif, sedangkan luas puncak dipakai sebagai data kuantitatif (Gandjar dan Rohman, 2007). Beberapa kelebihan kromatografi gas diantaranya pada penggunaan kolom yang lebih panjang dapat menghasilkan efisiensi pemisahan yang tinggi.Fase gas dibandingkan fase cair tidak bersifat reaktif terhadap fase diam dan zat-zat terlarut.Gas dan uap mempunyai viskositas yang rendah, serta kesetimbangan partisi antara gas dan cairan berlangsung cepat, sehingga sensitivitasnya tinggi dan analisis relatif cepat.Adapun kelemahannya yaitu terbatas hanya untuk zat-zat yang mudah menguap (Khopkar, 2003). 2.13.2 Spektrofotometri Spektrofotometri merupakan pengukuran suatu interaksi antara reaksi radiasi elektromagnetik dan molekul atau atom dari suatu zat kimia (Depkes, 1995). Spektrofotometri terdiri Spektrofotometermenghasilkan atas sinar spektrometer dari spektrum dan dengan fotometer. panjang gelombang tertentu dan fotometer merupakanalat pengukur intensitas cahaya UIN Syarif Hidayatullah Jakarta 23 yang ditranmisikan atau yang diabsorpsi.Spektrofotometer tersusun atas sumber spektrum yang kontinyu, monokromator, selpengabsorpsi untuk larutan sampel atau blangko dan suatu alat untuk mengukur pebedaanabsorpsi antara sampel dan blangko ataupun pembanding (Khopkar, 1990). Komponen-komponen pada instrumen spektrofotometri meliputi (Khopkar, 1990): 1. Sumber radiasi. Sumber tenaga radiasi harusstabil. Sumber yang biasa digunakan adalah lampuwolfram. 2. Monokromator. Digunakan untuk memperoleh sumber sinar yang monokromatis. 3. Sel absorpsi. Pada pengukuran di daerah visibel menggunakan kuvet kaca atau kuvetkaca corex, tetapi untuk pengukuran pada UV menggunakan sel kuarsa karena gelastidak tembus cahaya pada daerah ini. 4. Detektor. Detektor radiasi dihubungkan dengan sistem meter atau pencatat. Peranandetektor untuk memberikan respon terhadap cahaya pada berbagai panjanggelombang. Spektrofotometri yang sering digunakan dalam analisis famasi meliputi spektrofotometri serapan ultra violet (UV), cahaya tampak (Visibel), inframerah (IR) dan serapan atom (AAS) (Depkes, 1995). a. Spektrofotometri Resonansi Magnetik Spektrum resonansi magnetik nuklir (NMR) melengkapi spektrum infamerah yang hanya dapat memberikan gambaran mengenai gugus fungsi tetapi hanya sedikit memberi informasi mengenai atom-atom hidrogen dalam sebuah molekul organic (Fessenden, 1986). Kombinasi IR dan data NMR seringkali cukup untuk menentukan secara benar struktur molekul yang tidak diketahui (Pavia et al., 2008). Spektroskopi NMR didasarkan pada penyerapan gelombang radio oleh inti-inti tertentu dalam molekul organik yang berada dalam medan magnet yang kuat (Fessenden, 1986). Radiasi pada daerah frekuensi radio digunakan untuk mengeksitasi atom-atom, biasanya proton-proton atau atom-atom karbon-13, sehingga spinnya berubah dari sejajar menjadi sejajar melawan medan magnet yang digunakan. Rentang frekuensi yang dibutuhkan untuk UIN Syarif Hidayatullah Jakarta 24 eksitasi dan pola-pola pembagian kompleks yang dihasilkan sangat khas pada struktur kimia molekul tersebut (Watson, 2009). NMR dapat menentukan jumlah masing-masing jenis yang berbeda dari inti hidrogen serta memperoleh informasi mengenai sifat dasar dari lingkungan terdekat dari masing-masing jenis. Informasi yang sama dapat ditentukan untuk inti karbon (Pavia et al., 2008). Spektrum NMR biasanya ditentukan dari larutan substansi yang dianalisis, oleh karena itu pelarut yang digunakan tidak boleh mengandung atom hidrogen karena akan mengganggu puncak spektrum. Pelarut yang dapat digunakan seperti tetraklormetana (CCl4) yang tidak mengandung hidrogen atau pelarut yang atom hidrogennya telah diganti menjadi isotopnya yaitu deuterium seperti CDCl3. Atom-atom deuterium mempunyai sifat magnetik yang sedikit berbeda dengan hidrogen sehingga menghasilkan puncak pada area spektrum yang berbeda (Sudjadi, 1983). Instrument NMR terdiri atas komponen-komponen sebagai berikut (Willard et al., 1988) : 1. Magnet untuk memisahkan energi spin nuklir. 2. Paling tidak terdapat dua saluran frekuensi radio, satu untuk stabilisasi medan atau frekuensi dan satu untuk memberikan frekuensi radio untuk energi penyinaran. Yang ketiga dapat digunakan untuk masing-masing inti yang akan dipisahkan. 3. Probe sampel yang mengandung kumparan untuk kopling sampel dengan bidang frekuensi radio. 4. Detektor untuk memproses sinyal NMR. 5. Generator (Sweep Generator) untuk menyapu bersih baik medan magnet amupun frekuensi radio melalui frekuensi resonansi sampel. 6. Rekorder untuk menampilakan spektrum. UIN Syarif Hidayatullah Jakarta BAB 3 METODOLOGI PENELITIAN 3.1 Tempat dan Waktu Penelitian 3.1.1 Tempat Penelitian modifikasi struktur etil p-metoksisinamat melalui reaksi kondensasi aldol dengan etil metil keton dilaksanakan di Laboratorium Penelitian I, Laboratorium Farmakognosi dan Fitokimia, Laboratorium Kimia Obat, dan Laboratorium Analisa Obat dan Pangan Halal, Program Studi Farmasi, Fakultas Kedokteran dan Ilmu Kesehatan. 3.1.2 Waktu Penelitian ini dilaksanakan pada bulan November 2015 sampai dengan Juli 2016. 3.2 Alat dan Bahan 3.2.1 Alat Spektrofotometri 1H-NMR (500 MHz, JEOL), vaccum rotary evaporator (SB-1000 Eyela), digital water bath (SB-100 Eyela), GCMS (AGILENT TECHNOLOGIES), microwave, lemari pendingin, plat alumunium TLC silica gel 60 F254 (Merck), melting point SMP10, oven, timbangan analitik, statif, labu reaksi, corong, corong pisah, hotplate, erlenmeyer, rak, tabung reaksi, chamber KLT, plat kaca, termometer, pipet eppendorf, mikropipet, batang pengaduk, pinset, kertas saring, kapas, aluminuim foil, vial uji, botol, pH meter, labu ukur, gelas ukur, gelas piala, dan magnetik stirrer. 3.2.2 Bahan Senyawa etil p-metoksisinamat hasil isolasi dari kencur (Kaempferia galanga L.), etil metil keton (Merck), natrium hidroksida (NaOH) (Merck), kalsium nitrat (Ca(NO3)2) tetrahidrat (Merck), silica gel 60 GF254 (Merck), asam asetat glasial (Merck), methanol gradient grade for LC (Merck), asam klorida (HCl), etanol p.a (Merck), etil asetat, n-heksan, metanol dan aquadest. 25 UIN Syarif Hidayatullah Jakarta 26 3.3 Prosedur Penelitian 3.3.1 Preparasi a. Pengambilan Sampel Rimpang kencur (Kaemferia galanga L,) diperoleh dari kebun Balitro (Balai Penelitian Tanaman Rempah dan Obat) di wilayah Sukabumi, Jawa Barat pada bulan November 2015. b. Determinasi Tumbuhan Determinasi tumbuhan kencur (Kaempferia galanga L.) dilakukan di Herbarium Bogoriense Bidang Botani, Puslit Biologi, LIPI Cibinong. c. Penyiapan Bahan untuk Ekstraksi Sebanyak 55 kg kencur dibersihkan, dicuci dengan air mengalir, lalu dirajang sekitar 2-3 mm. Kencur dijemur selama 5-6 hari tanpa terkena sinar matahari. Setelah kering, kencur dihaluskan menggunakan blender (Barus, 2009). d. Pembutan Plat KLT Preparatif Sebanyak 5 gram silika gel 60 GF254 ditambakan 11 ml aquades di dalam erlenmeyer lalu kocok dengan kuat hingga tercampur sempurna. Tuangkan bubur silika gel ke atas plat kaca dengan ukuran 10 cm x 10 cm. Keringkan plat KLT preparatif pada suhu ruang selama 2 jam lalu aktivasi dalam oven pada suhu 120οC selama 1 jam (Merck). 3.3.2 Isolasi Etil p-metoksisinamat (Mufidah, 2014) Serbuk simplisia kencur dimaserasi dengan menggunakan pelarut n-heksan yang telah didestilasi dengan waktu perendaman 5 hari sambil sesekali dilakukan pengocokan. Setelah 5 hari disaring sehingga diperoleh ampas dan filtrat. Ampas dilakukan maserasi ulang sebanyak 4 kali hingga hasil maserasi menunjukkan warna hampir jernih. Seluruh filtrat hasil maserasi dipekatkan dengan menggunakan vacuum rotary evaporator. Filtrat pekat didiamkan pada suhu kamar sampai terbentuk kristal. Kristal yang diperoleh dimurnikan dengan menggunakan n-heksan dan direkristalisasi dengan cara melarutkan kristal dalam n-heksan dan beberapa tetes metanol dan kemudian dibiarkan pada suhu kamar UIN Syarif Hidayatullah Jakarta 27 sehingga terbentuk kristal kembali. Kristal dipisahkan dengan penyaringan dan dihitung rendemennya. 3.3.3 Modifikasi Etil p-metoksisinamat a. Proses Hidrolisis Sebanyak 3 gram NaOH (0,075 mmol) dilarutkan dengan etanol pro analisis dalam erlenmeyer dengan bantuan stirrer. Tambahkan senyawa etil pmetoksisinamat sebanyak 10 gram (0,0484 mmol) dan reaksi dijaga pada suhu 60οC di atas hotplate selama 5 jam. Hasil reaksi dilarutkan dengan aquades, kemudian ditambahkan HCl 15 % untuk membentuk endapan APMS hingga tidak ada lagi endapan putih yang terbentuk atau pH mencapai 4. Endapan yang didapat disaring dengan menggunakan kertas saring dan dikeringkan pada suhu ruang (Aulia, 2015). b. Proses Oksidasi Sebanyak 4 gram APMS (0,0224 mmol) ditambahkan 10 gram Ca(NO3)2 (0,0423 mmol) dan 20 ml asam asetat glasial (0,3497 mmol). Campuran reaksi tersebut di iradiasi menggunakan microwave pada 300 watt selama 2 menit. Hasil reaksi segera ditambahkan dengan aquadest dingin lalu dinginkan di dalam kulkas. Hasil reaksi di ekstraksi dengan heksan lalu dipekatkan menggunakan vacuum rotary evaporator (Komala, 2014). c. Proses Kondensasi Aldol Sebanyak 206,2 mg NaOH dilarutkan dengan 1 mL aquadest dalam erlenmeyer dengan bantuan stirrer. Tambahkan campuran 468,8 mg pmetoksibenzaldehid (3,447 mmol) dengan 4,16 ml etil metil keton (46,5345 mmol) (1 : 13,5). secara perlahan lalu stirer selama 24 jam pada suhu ruang. Reaksi di cek menggunakan KLT dan GCMS. Hasil reaksi di partisi dengan aquades-etil asetat. Lapisan etil asetat kemudian dipekatkan dengan vacuum rotary evaporator (Rayar et al., 2015 dengan modifikasi). UIN Syarif Hidayatullah Jakarta 28 3.3.4 Pemurnian dengan KLT Preparatif Beri batas 1 cm pada bawah dan atas KLT perapatif. Totolkan hasil reaksi kondensasi aldol sepanjang batas bawah plat KLT preparatif dan biarkan hingga kering. Masukkan plat KLT preparatif ke dalam gelas beaker yang telah dijenuhkan dengan eluen heksan-etil asetat (4:1) lalu elusi hingga mencapai batas atas. Periksa dan tandai spot dibawah UV 254 nm dan 365 nm. Spot yang terbentuk di kikis lalu di ekstraksi dengan etil asetat dan dibiarkan pada suhu ruang hingga membentuk kristal. Kristal yang terbentuk direkristalisasi dengan menggunakan metanol. 3.3.5 Identifikasi Senyawa a. Identifikasi Organoleptis Senyawa yang didapat dari hasil modifikasi diidentifikasi warna, bentuk dan bau. b. Pengukuran Rf EPMS dan semua senyawa hasil modifikasi di KLT dengan menggunakan eluen heksan-etil asetat (4:1). c. Pengukuran Titik Leleh Senyawa yang didapat dari hasil modifikasi diidentifikasi titik lelehnya menggunakan alat melting point SMP10. d. Identifikasi Senyawa Menggunakan GCMS Kolom yang digunakan adalah HP-5MS (30 m x 0,25 mm ID x 0,25 um), suhu awal 700C selama 2 menit, dinaikkan ke suhu 2850C dengan kecepatan 200C/min selama 20 menit. Suhu MSD 2850C. Kecepatan aliran 1,2 mL/min dengan split 1:100. Parameter scanning dilakukan dari massa paling rendah yakni 35 sampai paling tinggi 550 (Umar et al., 2012). e. Identifikasi Senyawa Menggunakan 1H-NMR Sedikit sampel padat (kira-kira 10 mg) dilarutkan dalam pelarut kloroform bebas proton (khusus NMR), kemudian dimasukkan ke dalam tabung khusus NMR untuk kemudian dianalisis. UIN Syarif Hidayatullah Jakarta BAB 4 HASIL DAN PEMBAHASAN Pada penelitian ini dilakukan modifikasi senyawa etil ρ-metoksisinamat yang diisolasi dari tanaman kencur melalui reaksi kondensasi aldol sehingga merubah gugus ester menjadi gugus keton. Senyawa etil ρ-metoksisinamat terlebih dahulu di ubah menjadi asam ρ-metoksisinamat melalui reaksi hidrolisis. Senyawa asam ρmetoksisinamat yang telah didapat kemudian di oksidasi sehingga diperoleh senyawa aldehid yang direaksikan dengan etil metil keton melalui reaksi kondensasi aldol dengan adanya basa NaOH dalam air. Pada percobaan pendahuluan, reaksi oksidasi langsung pada etil ρmetoksisinamat (EPMS) dapat menghasilkan senyawa aldehid dan beberapa senyawa lain. Pada saat EPMS diubah terlebih dahulu menjadi asam ρ-metoksisinamat (APMS) melalui reaksi hidrolisis maka didapatkan senyawa aldehid dan senyawa lain yang lebih sedikit (gambar 4.1). Senyawa aldehid 1 2 3 4 Gambar 4.1 KLT uji pendahuluan oksidasi dengan eluen heksan-etil asetat (4:1) (visualisasi UV ƛ 254 nm). Keterangan : (1) reaksi oksidasi EPMS, (2) reaksi oksidasi APMS, (3) APMS, dan (4) EPMS 4.1 Hasil Isolasi Senyawa Etil ρ-metoksisinamat Proses isolasi senyawa EPMS dimulai dari determinasi, pembuatan serbuk simplisia rimpang kencur segar, isolasi dan rekristalisasi EPMS, serta identifikasi EPMS. 29 UIN Syarif Hidayatullah Jakarta 30 4.1.1 Hasil Determinasi Pada penelitian ini dilakukan determinasi untuk memastikan kebenaran tumbuhan yang digunakan. Determinasi dilakukan di Herbarium Bogoriense, Pusat Penelitian Biologi LIPI, Bogor, Jawa Barat. Hasil determinasi menunjukkan bahwa sampel merupakan spesies Kaempferia galanga L (Lampiran 3). 4.1.2 Pembuatan Serbuk Simplisia Rimpang Kencur Segar (RKS) Sebanyak 55 kg RKS digunakan dalam penelitian ini. Setelah melalui proses pembuatan simplisia, diperoleh serbuk simplisia kencur sebanyak 7 kg. Simplisia kencur yang didapatkan berwarna kecoklatan (gambar 4.2). Gambar 4.2 Simplisia kencur 4.1.3 Isolasi Etil ρ-metoksisinamat Simplisia RKS yang didapat diekstraksi dengan cara maserasi menggunakan pelarut heksan. Hasil maserasi diperoleh filtrat yang dapat mengkristal pada suhu ruang sehingga memudahkan dalam isolasi. Kristal yang diperoleh direkristalisasi dengan heksan dan metanol sehingga didapatkan kristal yang berwarna putih kekuningan (gambar 4.4). Persen rendemen kristal EPMS yaitu : UIN Syarif Hidayatullah Jakarta 31 Gambar 4.3 KLT isolat kencur dengan eluen heksan-etil asetat (4:1) (visualisasi UV ƛ 254 nm) Gambar 4.4 Kristal EPMS 4.1.4 Identifikasi Senyawa Etil ρ-metoksisinamat Senyawa EPMS dilakukan identifikasi organoleptis, pengukuran titik leleh, dan identifikasi menggunakan GCMS. a. Identifikasi Organoleptis Senyawa Etil ρ-metoksisinamat Senyawa etil ρ-metoksisinamat memiliki karakteristik sebagai berikut: Warna : putih kekuningan Bau : khas Bentuk : kristal b. Pengukuran Titik Leleh Senyawa Etil ρ-metoksisinamat Pengukuran titik leleh menggunakan alat melting point didapatkan rentang titik pada senyawa etil ρ-metoksisinamat yaitu 48-52οC. UIN Syarif Hidayatullah Jakarta 32 c. Identifikasi Senyawa Etil ρ-metoksisinamat Menggunakan GCMS Analisa senyawa etil ρ-metoksisinamat dilakukan dengan menggunakan GCMS. Dari hasil GCMS, didapatkan waktu retensi 9,878 dan memiliki berat molekul 206,1 dengan fragmentasi masa pada 161, 134, 118, 89, dan 63 (lampiran 4). Hasil GCMS tersebut menunjukkan hasil yang serupa seperti hasil dari Mufidah (2014). Adapun fragmentasi yang terjadi pada senyawa etil ρmetoksisinamat adalah sebagai berikut : Gambar 4.5 Pola fragmentasi GCMS etil ρ-metoksisinamat. 4.2 Reaksi Hidrolisis Etil ρ-metoksisinamat Reaksi hidrolisis dilakukan dengan menggunakan katalis basa NaOH dalam pelarut etanol p.a. Mekanisme reaksi hidrolisis diinisiasi oleh protonasi pada karbonil oksigen. Protonasi tersebut membuat gugus karbonil terprotonasi dengan melepaskan proton dari karbon sehingga bersifat lebih elektrofilik dan akan menerima penambahan nukleofil OH (Larson dan Weber, 1994). Pada reaksi hidrolisis EPMS, gugus ester digantikan dengan gugus karboksilat sehingga menghasilkan senyawa asam ρ-metoksisinamat (APMS). Pada reaksi hidrolisis, NaOH dilarutkan kedalam etanol p.a lalu ditambahkan dengan EPMS. Campuran dipanaskan pada suhu 60οC selama 5 jam di atas hotplate. Setelah proses reaksi selesai, hasil reaksi ditambahkan aquadest hingga larut kemudian ditambahkan HCl 15% sampai pH 4 yang ditandai dengan tidak terbentuk UIN Syarif Hidayatullah Jakarta 33 lagi endapan APMS. Penambahan HCl 15% bertujuan untuk mengikat Na+ sehingga terbentuk endapan putih berupa hasil hidrolisis (Mufidah, 2014). Endapan APMS yang didapat disaring kemudian dikering anginkan sehingga didapatkan residu berupa serbuk putih (gambar 4.8). Persen rendemen hasil hidrolisis yaitu : Gambar 4.6 Mekanisme reaksi hidrolisis etil ρ-metoksisinamat (Aulia, 2015). 1 2 Gambar 4.7 KLT senyawa hasil hidrolisis dengan eluen heksan-etil asetat (4:1) (visualisasi UV ƛ 254 nm). Keterangan : (1) EPMS, dan (2) APMS. Gambar 4.8 Senyawa hasil hidrolisis etil ρ-metoksisinamat UIN Syarif Hidayatullah Jakarta 34 4.2.1 Identifikasi Senyawa Hasil Hidrolisis EPMS Senyawa hasil hidrolisis etil ρ-metoksisinamat dilakukan identifikasi organoleptis, pengukuran titik leleh, dan identifikasi menggunakan GCMS. a. Identifikasi OrganoleptisSenyawa Hasil Hidrolisis EPMS Senyawa hasil hidrolisis etil ρ-metoksisinamat memiliki karakteristik sebagai berikut: Warna : putih Bau : tidak berbau Bentuk : serbuk b. Pengukuran Titik Leleh Senyawa Hasil Hidrolisis EPMS Pengukuran titik leleh menggunakan alat melting point didapatkan rentang titik pada senyawa hasil hidrolisis yaitu 171-175οC. c. Identifikasi Senyawa Hasil Hidrolisis EPMS Menggunakan GCMS Analisa senyawa hasil hidrolisis etil ρ-metoksisinamat dilakukan dengan menggunakan GCMS. Dari hasil GCMS, didapatkan waktu retensi 9,592 dan memiliki berat molekul 178 dengan fragmentasi masa pada 161, 133, 116, 101, dan 77 (lampiran 5). Adapun fragmentasi yang terjadi pada senyawa hasil hidrolisis etil ρ-metoksisinamat adalah sebagai berikut : m/z = 76 m/z = 102 Gambar 4.9 Pola fragmentasi GCMS asam ρ-metoksisinamat. UIN Syarif Hidayatullah Jakarta 35 Hasil GCMS tersebut menunjukkan hasil yang serupa dengan hasil dari Aulia (2015). Sehingga senyawa hasil hidrolisis etil ρ-metoksisinamat adalah asam ρ-metoksisinamat. 4.3 Reaksi Oksidasi Asam ρ-metoksisinamat Asam ρ-metoksisinamat memiliki karbon alkena yang dapat dioksidasi. Gugus alkena pada APMS mempunyai satu hidrogen yang terikat padanya, sehingga hasil oksidasi dapat berupa senyawa aldehid. Reaksi oksidasi dilakukan dengan mengiradiasi campuran APMS, Ca(NO3)2 dan asam asetat glasial dengan microwave 300 watt selama 2 menit. Ca(NO3)2 merupakan oksidator yang akan mengoksidasi APMS. Setelah reaksi selesai, hasil reaksi segera ditambahkan aquades dingin dan disimpan didalam kulkas. Hasil reaksi kemudian dipartisi dengan heksan lalu dikeringkan dengan rotary evaporator sehingga didapatkan serbuk berwarna kuning (gambar 4.11). Persen rendemen senyawa aldehid yaitu : 1 2 Gambar 4.10 KLT senyawa hasil oksidasi dengan eluen heksan-etil asetat (4:1) (visualisasi UV ƛ 254 nm).Keterangan : (1) APMS, dan (2) senyawa hasil oksidasi. Gambar 4.11 Senyawa hasil oksidasi asam ρ-metoksisinamat. UIN Syarif Hidayatullah Jakarta 36 MWI 300 watt 2 menit Gambar 4.12 Reaksi oksidasi asam ρ-metoksisinamat 4.3.1 Identifikasi Senyawa Hasil Oksidasi APMS Senyawa hasil oksidasi asam ρ-metoksisinamat dilakukan identifikasi organoleptis dan identifikasi menggunakan GCMS. a. Identifikasi Organoleptik Senyawa Hasil Oksidasi APMS Senyawa hasil oksidasi asam ρ-metoksisinamat memiliki karakteristik sebagai berikut : Warna : kuning Bau : khas Bentuk : serbuk b. Identifikasi Senyawa Hasil Oksidasi APMS Menggunakan GCMS Analisa senyawa hasil oksidasi dilakukan dengan menggunakan GCMS. Dari hasil GCMS, didapatkan beberapa kromatogram dari beberapa senyawa, dimana salah satunya adalah senyawa dengan waktu retensi 6.657 dan memiliki berat molekul 135 dengan fragmentasi masa pada 107, 92, 77, dan 63 (lampiran 6). Berdasarkan hasil GCMS menunjukkan bahwa senyawa hasil oksidasi adalah 4-metoksibenzaldehid. UIN Syarif Hidayatullah Jakarta 37 Adapun fragmentasi yang terjadi pada senyawa 4-metoksibenzaldehid adalah sebagai berikut : m/z = 135 m/z = 106 m/z = 91 m/z = 75 Gambar 4.13 Pola fragmentasi GCMS 4-metoksibenzaldehid 4.4 Hasil Optimasi Reaksi Kondensasi Aldol 4-metoksibenzaldehid Suatu aldehida tanpa hidrogen α dapat dicampur dengan aldehida yang memiliki hidrogen α atau dengan keton sehingga kondensasi antara keduanya dapat terjadi yang disebut dengan reaksi kondensasi aldol silang (cross aldol condensation) (Fessenden, 1982). Senyawa 4-metoksibenzaldehid hasil reaksi oksidasi asam ρmetoksisinamat tidak memiliki atom hidrogen pada C alfa. Pada reaksi ini senyawa aldehid tersebut direaksikan dengan suatu keton yaitu 2-butanon atau etil metil keton (EMK) dengan adanya basa NaOH dalam air. Pada reaksi kondensasi aldol ini, dilakukan denga nmelarutkan NaOH dalam 1 ml aquades. Larutan NaOH kemudian ditambahkan senyawa 4-metoksibenzaldehid yang telah dicampur dengan etil metil keton. Campuran tersebut distirer pada suhu ruang. Reaksi ini dilakukan optimasi untuk mendapatkan hasil modifikasi yang sempurna. Optimasi dilakukan dengan mereaksikan selama 4 jam, 7 jam dan 24 jam. Reaksi dimonitoring dengan menggunakan KLT eluen heksan-etil asetat (4:1) dan GCMS. Berdasarkan hasil KLT, tidak terlihat perbedaan dikarenakan nilai Rf antara senyawa aldehid dan hasil kondensasi aldol yang sama (gambar 4.14). Oleh karena itu harus dilakukan pemeriksaan hasil reaksi menggunakan GCMS. Dari hasil GCMS dapat dilihat perbedaan banyaknya perubahan senyawa aldehid menjadi senyawa UIN Syarif Hidayatullah Jakarta 38 target (lampiran 9). Berdasarkan hasil optimasi, dipilih reaksi selama 24 jam. Hal tersebut dikarenakan senyawa target yang terbentuk lebih banyak. 1 2 3 (a) 4 1 2 3 4 (b) Gambar 4.14 KLT optimasi reaksi kondensasi aldol dengan eluen heksan-etil asetat (4:1) (a) visualisasi UV ƛ 254 nm (b) visualisasi UV ƛ 365 nm. Keterangan : (1) Reaksi selama 4 jam (2) Reaksi selama 7 jam (3) Reaksi selama 24 jam (4) Senyawa aldehid hasil oksidasi APMS Setelah reaksi selesai, warna larutan akan berubah menjadi kuning kecoklatan. Hasil reaksi dipartisi dengan aquades-etil asetat untuk memisahkan senyawa hasil kondensasi aldol. Lapisan etil asetat dikeringkan dengan rotary evaporator sehingga didapatkan cairan merah pekat. Cairan hasil reaksi dimurnikan dengan menggunakan KLT preparatif eluen heksan-etil asetat (4:1). Spot yang terbentuk dikikis lalu diekstraksi menggunakan etil asetat. Lapisan etil asetat di keringkan dengan vacuum rotary evaporator sehingga didapatkan hasil berupa kristal berwarna putih sampai kuning (gambar 4.16). Kristal yang didapat kemudian direkristalisasi dengan menggunakan metanol. Persen rendemen senyawa hasil kondensasi aldol yaitu : UIN Syarif Hidayatullah Jakarta 39 1 2 Gambar 4.15 KLT senyawa hasil kondensasi aldol dengan eluen heksan-etil asetat (4:1) (visualisasi UV ƛ 254 nm). Keterangan : (1) senyawa hasil oksidasi, dan (2) senyawa hasil kondensasi aldol. (a) (b) Gambar 4.16 Senyawa hasil reaksi kondensasi aldol. Keterangan : (a) Sebelum Pemurnian dan (b) Setelah Pemurnian Pada reaksi kondensasi aldol ini, ion hidroksida dari basa NaOH akan mengambil sebuah proton dari C alfa pada etil metil keton untuk membentuk ion enolat (1). Ion enolat tersebut merupakan nukleofil yang akan menyerang karbon karbonil dari senyawa aldehid membentuk ion alkoksida (2). Ion alkoksida kemudian mengambil proton dari molekul air untuk membentuk produk aldol (3). Produk aldol tersebut akan mengalami dehidrasi secara spontan (4). UIN Syarif Hidayatullah Jakarta 40 Gambar 4.17 Mekanisme reaksi kondensasi aldol senyawa 4-metoksibenzaldehid dengan etil metil keton. 4.5 Identifikasi Senyawa Hasil Reaksi Kondensasi Aldol Senyawa hasil reaksi kondensasi aldol 4-metoksibenzaldehid dilakukan identifikasi organoleptis, pengukuran titik leleh, pengukuran Rf, identifikasi menggunakan GCMS dan identifikasi menggunakan 1H-NMR. a. Identifikasi Organoleptis Senyawa Hasil Reaksi Kondensasi Aldol Senyawa hasil reaksi kondensasi aldol memiliki karakteristik sebagai berikut : Warna : putih sampai kuning Bau : khas Bentuk : kristal UIN Syarif Hidayatullah Jakarta 41 b. Pengukuran Rf Senyawa Hasil Hidrolisis, Oksidasi dan kondensasi aldol. Senyawa hasil modifikasi diidentifikasi dengan membandingkan nilai Rf seluruh senyawa yang di KLT menggunakan eluen heksan-etil asetat (4:1) (gambar 4.18). Nilai Rf yang di dapat adalah sebagai berikut : Etil ρ-metoksisinamat = 0,575 Asam ρ-metoksisinamat = 0,1 Senyawa 4-metoksibenzaldehid = 0,5 Senyawa hasil kondensasi aldol = 0,525 1 2 3 4 Gambar 4.18 KLT semua senyawa dengan eluen heksan-etil asetat (4:1) (visualisasi UV ƛ 254 nm). Keterangan : (1) EPMS, (2) APMS, (3) 4-metoksibenzaldehid dan (4) senyawa hasil kondensasi aldol. Berdasarkan nilai Rf dapat diketahui tingkat kepolaran dari masing-masing senyawa. Senyawa etil ρ-metoksisinamat memiliki tingkat kepolaran yang lebih rendah dibanding senyawa yang lain ditandai dengan nilai Rf yang paling tinggi. Senyawa etil ρ-metoksisinamat yang telah dihidrolisis menghasilkan senyawa asam ρ-metoksisinamat (APMS). APMS memiliki tingkat kepolaran yang jauh lebih tinggi dibanding senyawa etil ρ-metoksisinamat dengan nilai Rf 0,1. Pada senyawa 4metoksibenzaldehid diperoleh nilai Rf sedikit lebih rendah dibandingkan dengan EPMS sehingga memiliki tingkat kepolaran sedikit lebih tinggi. Senyawa 4metoksibenzaldehid dengan senyawa hasil kondensasi aldol memiliki nilai Rf hampir sama yakni berturut-turut adalah 0,5 dan 0,525. Hal ini menunjukkan bahwa senyawa tersebut memiliki sedikit perbedaan tingkat polaritas. UIN Syarif Hidayatullah Jakarta 42 c. Pengukuran Titik Leleh Senyawa Hasil Reaksi Kondensasi Aldol Pengukuran titik leleh menggunakan alat melting point didapatkan rentang titik pada senyawa hasil reaksi kondensasi aldol yaitu 53-60οC. d. Identifikasi Senyawa Senyawa Hasil Reaksi Kondensasi Aldol Menggunakan GCMS Analisa senyawa hasil reaksi kondensasi aldol dilakukan dengan menggunakan GCMS. Dari hasil GCMS, didapatkan senyawa dengan waktu retensi 9.857dan memiliki berat molekul 190 dengan fragmentasi masa pada 161, 133, 118, 103, 89 dan 76 (lampiran 7). Berdasarkan hasil GCMS menunjukkan bahwa senyawa hasil reaksi kondensasi aldol 4-metoksibenzaldehid dengan etil metil keton adalah 1-(4metoksifenil)-1-penten-3-on. Senyawa tersebut merupakan bentuk keton dari EPMS dimana tidak terdapat atom O pada etoksi ester. Pengurangan berat molekul EPMS dengan atom O menunjukkan berat molekul senyawa tersebut. m/z = 102 Gambar 4.19 Pola fragmentasi GCMS 1-(4-metoksifenil)-1-penten-3-on. e. Identifikasi Senyawa Hasil Reaksi Kondensasi Aldol Menggunakan 1H-NMR Analisa senyawa hasil reaksi kondensasi aldol juga dilakukan dengan menggunakan 1H-NMR. Interpretasi analisa dari NMR berupa nilai dari pergeseran kimia (δ) pada suatu senyawa dalam satuan ppm (Pavia et al., 2008). Hasil analisis UIN Syarif Hidayatullah Jakarta 43 senyawa hasil kondensasi aldol dengan 1H-NMR (lampiran 8) ditunjukkan pada tabel 4.1 dengan panduan gambar 4.20. Gambar 4.20 Struktur senyawa. Keterangan:(a) Etil ρ-metoksisinamat, (b)Asam ρ-metoksisinamat, dan (c) 1-(4-metoksifenil)-1-penten-3-on Tabel 4.1 Data pergeseran kimia (δ) spektrum 1H-NMR etil ρ-metoksisinamat, asam ρ-metoksisinamat, dan 1-(4-metoksifenil)-1-penten-3-on (CDCl3, 500 MHz). Pergeseran Kimia (δ, ppm) Etil ρ-metoksisinamat Asam ρ-metoksisinamat 1-(4-metoksifenil)-1- (Mufidah, 2014) (Mufidah, 2014) penten-3-on 1 1,33 (t, 3H, J=7,15) - 1,15 (t, 3H, J=7,2) 2 4,25 (q, 2H, J=7,15) - 2,66 (q, 2H, J=7,2) 4 6,31 (d, 1H, J=15,6) 7,63 (d, 1H, J=16,2) 6,63 (d, 1H, J=16,2) 5 7,65 (d, 1H, J=16,25) 6,34 (d, 1H, J=16,2) 7,52 (d, 1H, J=15,6) 7 6,90 (d, 1H, J=9,05) 6,95 (d, 1H, J=9,05) 6,90 (d, 1H, J=9,05) 8 7,47 (d, 1H, J=8,45) 7,47 (d, 1H, J=9,1) 7,49 (d, 1H, J=8,45) 10 7,47 (d, 1H, J=8,45) 7,54 (d, 1H, J=9,1) 7,49 (d, 1H, J=8,45) 11 6,90 (d, 1H, J=9,05) 6,95 (d, 1H, J=9,1) 6,91 (d, 1H, J=9,05) 12 3,82 (s, 3H) 3,82 (s, 3H) 3,83 (s, 3H) Posisi UIN Syarif Hidayatullah Jakarta 44 Spektrum 1H-NMR memberikan sinyal pada pergeseran kimia 1,15 ppm (3H) berbentuk triplet karena berinteraksi dengan sinyal pada 2,66 ppm (2H) berbentuk quartet sehingga disimpulkan ini adalah CH3-CH2-X. Karena sinyal CH2 pada 2,66 ppm maka X adalah C=O. Pada senyawa EPMS, sinyal CH2 lebih downfield karena berikatan dengan oksigen pada gugus ester sehingga menunjukkan sinyal pada 4,25 ppm. Spektrum 1H-NMR memberikan sinyal pada 3,83 ppm (3H) berbentuk singlet. Sinyal ini lebih downfield karena berikatan dengan oksigen (-OCH3, metoksi). Pergeseran kimia 6,63 ppm (1H) berbentuk doublet memiliki hubungan dengan puncak pada pergeseran kimia 7,52 ppm (1H) berbentuk doublet, dengan rentang nilai konstanta kopling yaitu 15,6 – 16,2. Bentuk tersebut adalah olefin dengan proton berkonfigurasi trans. Pada pergeseran kimia 6,90 ppm – 7,49 ppm (4H) merupakan proton-proton dari benzen dengan dua substitusi. Pola sinyal ini menunjukkan bahwa 2 proton yang ekivalen terkopling secara ortho dengan 2 proton yang ekivalen lainnya, yang kemudian menunjukkan bahwa sinyal ini adalah sinyal dari H 7/11dan H 8/10. UIN Syarif Hidayatullah Jakarta BAB 5 KESIMPULAN DAN SARAN 5.1 Kesimpulan Berdasarkan penelitian dapat disimpulkan bahwa : a. Modifikasi senyawa etil ρ-metoksisinamat hasil isolasi dari kencur (Kaempferia galanga L.) telah berhasil dilakukan melalui tiga proses yaitu proses hidrolisis, proses oksidasi dan proses kondensasi aldol. b. Proses hidrolisis etil ρ-metoksisinamat (EPMS) menghasilkan senyawa asam ρmetoksisinamat (APMS) yang di oksidasi sehingga menghasilkan senyawa 4metoksibenzaldehid. Proses kondensasi aldol senyawa 4-metoksibenzaldehid dengan etil metil keton menghasilkan senyawa 1-(4-metoksifenil)-1-penten-3-on dengan rendemen 35,26 %. c. Senyawa 1-(4-metoksifenil)-1-penten-3-on merupakan bentuk keton dari EPMS berupa kristal putih hingga kuning dengan titik leleh 53-60οC. Identifikasi senyawa menggunakan KLT dengan eluen heksan-etilasetat (4:1) menunjukkan nilai Rf 0,525. d. Identifikasi menggunakan GCMS menunjukkan waktu retensi 9,857 dan berat molekul 190 dengan fragmentasi masa pada 161, 133, 118, 103, 89 dan 76. Identifikasi menggunakan 1H-NMR menunjukkan sinyal CH2 pada 2,66 ppm yang membuktikan bahwa gugus ester telah berubah menjadi gugus keton. 5.1 Saran a. Penelitian ini perlu dikembangkan lagi untuk mendapatkan metode reaksi kondensasi aldol dengan waktu yang lebih singkat dan rendemen yang besar. b. Perlu dilanjutkan penelitian untuk menguji aktivitas antiinflamasi senyawa 1-(4metoksifenil)-1-penten-3-on. 45 UIN Syarif Hidayatullah Jakarta DAFTAR PUSTAKA Adnan, M. 1997. Teknik Kromatografi Untuk Analisis Bahan Makanan. Yogyakarta: Penerbit Andi. Al-Fattah, M. H. 2011. Mukjizat Pengobatan Herbal dalam Al-Qur’an. Jakarta : Mirqat. Aulia, N. S. 2015. Modifikasi Struktur Senyawa Etil p-metoksisinamat Melalui Proses Nitrasi dengan Metode Cold Microwave Serta Uji Aktivitas Sebagai Antiinflamasi. Skripsi. Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta. Jakarta. Bangun, R. 2011. Semi Sintesis N,N-Bis(Hidroksietil)-3-(4-Metoksifenil) Akrilamida Dari Etil p-metoksisinamat Hasil Isolasi Rimpang Kencur (Kaempferia galanga L) Melalui Amidasi Dengan Dietanolamin. Medan: Universitas Sumatera Utara. Barus, R. 2009. Amidasi Etil p-Metoksi Sinamat yang Diisolasi dari Kencur (Kaempferia galanga, Linn). Medan: Sekolah Pasca Sarjana Universitas Sumatera Utara. Bogdal, D. 2005. Microwave-assisted Organic Synthesis. Elservier: Academic Press. BPOM RI. 2014. Peraturan Kepala Badan Pengawas Obat dan Makanan Republik Indonesia Nomor 13 Tahun 2014 Tentang Pedoman Uji Klinik Obat Herbal. Chang, R. 2004. Kimia Dasar: Konsep-konsep inti Edisi ketiga Jilid 2. Jakarta : Erlangga. Departemen Kesehatan RI. 1995. Farmakope Indonesia Edisi IV. Jakarta. Depdikbud. 1995. Kamus Besar Bahasa Indonesia. Jakarta : Balai Pustaka. Dhandapani, A.; Shobana K.; Murugan K.. 2011. Larvicidal, Pupicidal And Smoke Toxicity Effect OfKaempferiagalanga To The Malarial Vector, Anopheles Stephensi. The Bio Scan Journal 6(2) : 329-333. Ekowati, J.; Bimo, A. T.; Sukardiman; Siswandono; Sasaki S.; Higashiyama K.; Budiati T. 2012 Synthesis of Thiourea Derivatives of Ethyl pmethoxycinnamate Isolated from K. galanga and Their Chemopreventive Activity Against Fibrosarcoma in Mice. UPPS. Ekowati, J.; Dyah N. W.; Poerwono H.; Siswandono; Budiati T.; Sasaki S.; Yamauchi T.; Higashiyama K. 2009. Structure Modification of p- 46 UIN Syarif Hidayatullah Jakarta 47 methoxycinnamic Acid Isolated from Kaempferia galanga to Improve its antinociceptive activity. Second Collaborative Joint Seminar USM-Unair, Surabaya, Indonesia. Ekowati, J.; Suzana; Dyah N.W.; Susilowaty M. I.; Poerwono H.; Rudyanto M.; Astika G. N.; Syahrani A.; Siswono H.; Budiati T. 2007. Novel Analgesic Compounds From p-methoxycinnamic Acid. First Collabotarive Joint Seminar USM-Unair, Penang, Malaysia. Erdelen WR, Adimihardja K, Moesdarsono H, Sidik. Biodiversity, traditional medicine and the sustainable use of indigenous medicinalplants in Indonesia. Indigenous knowledge and developmentmonitor 1999;7(3):3-6. Ferround, C.; Marie G.; Sthephane U.; Helene B.; Alain G. 2008. Microwaveassisted solvent-free synthesis of N-acetamides by amidation or aminolysis. Tetrahedron Letters 49 (2008) 3004-3008. Fessenden. R. J. dan J. Fessenden. 1982. Kimia Organik. Edisi Ketiga. Jilid 1. Erlangga. Jakarta. Fessenden. R. J. dan J. Fessenden. 1982. Kimia Organik. Edisi Ketiga. Jilid 2. Erlangga. Jakarta. Gandjar, G.H.; Rohman, A., 2007. Kimia Farmasi Analisis. Yogyakarta : Pustaka Pelajar. Goldberg, D. 2002. Kimia Untuk Pemula. Jakarta : Erlangga. Handson, K. M.; Enrico G.; Christoper J. B. 2006. Sunscreen Enhancement of UV-Inducted Reactive Oxygen Species In The Skin. Journal Free Radical Biology and Medicine: 41 (8): 1205-1212. Indriyani, N. K. P. 2015. Modifikasi Struktur Senyawa Etil p-metoksisinamat Melalui Proses Nitrasi Serta Uji Aktivitas Sebagai Antiinflamasi. Skripsi. Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta. Jakarta. Khalafi-Nezhad, A.; Babak M.; Mohammad N. S. R. 2003. Direct Preparation of Primary Amides From Carboxylic Acids and Urea Using Imidazole Under Microwave Irradiation. Tetrahedron Letters 4A (2003) 7325-7328. Khoirumni’mah, Z. 2012. Modifikasi Struktur Senyawa Metil Sinamat Melalui Proses Degradasi Sinamat Serta Uji BSLT (Brine Shrimp Lethality Test) Terhadap Senyawa Hasil Modifikasi. Jakarta: UIN Syarif Hidayarullah. Khopkar, S. M. 2003. Konsep Dasar Kimia Analitik. Jakarta : UI-Press. UIN Syarif Hidayatullah Jakarta 48 Kingston H. M.; Jessie L. B. 1988. Introduction to Microwave Sample Preparation Theory and Practice. ACS publishing. Komala, I. 2014. Evaluasi Pengaruh Modifikasi Struktur Senyawa Etil ρmetoksisinamat (EPMS) yang Diisolasi dari Rimpang Kencur (Kaempferia galanga) Terhadap Aktivitas Antiinflamasinya. Lembaga Penelitian dan Pengabdian kepada Masyarakat (LP2M) UIN Syarif Hidayatullah : Jakarta Larson, R. A.; Eric J. W. 1994. Reaction Mechanism In Environmental Organic Chemistry. United State of America: Lewis Publisher. Lidstrom, P.; Tierney, J.; Wathey, B.; Westman, J. 2001. Microwave Assisted Organic Synthesis- A Review. Tetrahedron, 9225-9283. Loupy, A. 2006. Microwave in Organic Synthesis, Second Edition. Wiley-VCH. Mekseepralard, C.; Narisa K.; Jenny M. W. 2010. Antimicrobial and Antioxidant Activities of Traditional Thai Herbal Remedies for Aphthous Ulcer. Phytother. Res. 24: 1514-1519 (2010). Merck. Making TLC Plate From Bulk TLC Silica Gels. Heidelberg, Germany. Mufidah, S. 2014. Modifikasi Struktur Senyawa Etil p-metoksisinamat yang diperoleh dari Kencur (Kaempferia galangal Linn.) melalui Transformasi Gugus Fungsi Serta Uji Aktivitas Sebagai Antiinflamasi. Skripsi. Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta. Jakarta. Petrucci, R. H. 1987. Kimia Dasar Prinsip dan Terapan Modern Jilid 1. Jakarta : Erlangga. Pramono E. 2002. The commercial use of traditional knowledge andmedicinal plants in Indonesia. Submitted for multi-stakeholderdialoque on trade, intellectual property and biological resourcesin Asia. PubChem. n.d. 2-Butanone. Diakses tanggal 27 Juli 2016. https://pubchem.ncbi.nlm.nih.gov/compound/2-Butanone#section=Top PubChem. n.d. Acetate. Diakses tanggal 27 Juli 2016. http://pubchem.ncbi.nml.gov/compound/acetate#section=Wikipedia PubChem. n.d. Calcium Nitrate. Diakses tanggal 27 Juli 2016. https://pubchem.ncbi.nlm.nih.gov/compound/calcium_nitrate#section=Wi kipedia PubChem. n.d. Sodium Hidroxide. Diakses Tanggal 20 April 2016. https://pubchem.ncbi.nlm.nih.gov/compound/SodiumHidroxide#section=T op UIN Syarif Hidayatullah Jakarta 49 Qudsi, H. 2014. Modifikasi Struktur Senyawa Etil p-metoksisinamat yang Diisolasi dari Kencur (Kaempferia galanga L.) dengan Metode Reaksi Reduksi Serta Uji Aktivitas Sebagai Antiinflamasi. Skripsi. Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta. Jakarta. Rayar, A.; Maite S. V.; Clotilde F. 2015. An Efficient and Selective Microwaveassisted Claisen-Schmidt Reaction For The Synthesis Of Functionalized Benzalacetones. SpringerPlus 4:221. Reza, M. 2015. Amidasi Senyawa Etil p-metoksisinamat Melalui Reaksi Langsung dengan Iradiasi Microwave Serta Uji Aktivitas Sebagai Antiinflamasi. Skripsi. Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta. Jakarta. Riswiyanto. 2009. Kimia Organik. Jakarta: Penerbit Erlangga. Rukmana, R. 1994. Kencur. Yogyakarta: Penerbit Kanisius. Cetakan ke-13. Sastrohamidjojo, H. 1985. Spektroskopi Edisi I. Yogyakarta : Liberty. Solomon, T.W.G.; Fryhle. C. B. 2006. Organic Chemistry. 9th Edition, John Wiley & Sons. Stahl, E. 1969. Thin Layer Chromatography. Springer-Verlag : New York. Stahl, E. 1985. Analisis Obat Secara Kromatografi dan Mikroskopi. Bandung : Institut Teknologi Bandung. Sukardjo. 1986. Kimia Anorganik. Yogyakarta : Bima Aksara. Sulaiman, M.R.; Z.A, Zakaria; I.A.Daud; F.N.Ng ;Y.C.Ng; M.T. Hidayat. 2008. Antinociceptive and Anti-inflammatory activities of The Aqueous extract of Kaempferia galanga leaves in animal models. J.Nat Med 62:221-227. Surbakti, D. Isolasi dan Transformasi Etil p-metoksisinamat dari Kaempferia galanga Linn. Tesis ITB via Perpustakaan Digital ITB (http://digilib.itb.ac.id/ diakses pada 15 Januari 2016). Tara V., S; Sharma C.; Adiga S.; Bairy L. K.; Shenoy S.; Shenoy G. 2006. Wound Healing Activity Of Alkoholic Extract of Kaempferia galanga in Wistar Rats. Indian J.Physiol Pharmacol 50 (40) : 384-390. Tewtrakul, S; Supreeya Y.; Sopa K.; Latthya A. 2005. Chemical Components and Biological Activities of Volatile Oil of Kaempferia galanga Linn. SongklanakrinJ. Sci Technol Vol. 2 (Suppl.2) : Thai Herbs. UIN Syarif Hidayatullah Jakarta 50 Tufikhurohmah, T.; Rusmini; Nurhayati. 2008. Pemilihan Pelarut Optimasi Suhu Pada Isolasi Senyawa Etil Para Metoksi Sinamat (EPMS) Dari Rimpang Kencur Sebagai Bahan Tabir Surya Pada Industri Kosmetik. Umar, M. I.; Mohd Z. A.; Amirin S.; Item J. A. 1; Mun F. Y.; Rabia A.; Ashfaq A. 2012. Bioactivity-Guided Isolation of Ethyl-p-methoxycinnamate, an Anti-inflammatory Constituent, from Kaempferia galanga L. Extracts. Molecules, 17, 8720-8734. Underwood, A.L. 1989. Analisis Kimia Kuantitatif. Jakarta: Erlangga. Vittalro, A. M.; Tara T.; Meena K. K.; K.L Bairy; Smita S. 2011. Evaluation of Antiinflammatory and analgesic activities of alcoholic extract of Kaempferia galanga in rats. Indian J.Physiol Pharmacol 55 (1) : 13-24. UIN Syarif Hidayatullah Jakarta 51 Lampiran 1. Kerangka Penelitian Isolasi Etil ρ-metoksisinamat dari Kencur (Kaempferia galanga L.) Etil ρ-metoksisinamat (EPMS) Reaksi Hidrolisis Reaksi Oksidasi Reaksi kondensasi Aldol Pemurnian dan Identifikasi Senyawa UIN Syarif Hidayatullah Jakarta 52 Lampiran 2. Isolasi Etil ρ-metoksisinamat 55 kg rimpang Bersihkan dari tanah dan Rajang dan kencur segar akar dengan air mengalir kering anginkan Sortasi kering Maaserasi dengan Haluskan Simplisia kencur heksan dengan blender Ampas Filtrasi Filtrat Dipekatkan dengan vacuum rotary evaporator Kristal Fiiltrat pekat diendapkan pada suhu kamar Rekristaisasi Kristal EPMS murni UIN Syarif Hidayatullah Jakarta 53 Lampiran 3. Determinasi Tanaman Kencur UIN Syarif Hidayatullah Jakarta 54 Lampiran 4. Spektrum GCMS Senyawa Etil ρ-metoksisinamat UIN Syarif Hidayatullah Jakarta 55 Lampiran 5. Spektrum GCMS Senyawa Asam ρ-metoksisinamat UIN Syarif Hidayatullah Jakarta 56 Lampiran 6. Spektrum GCMS Senyawa 4-metoksibenzaldehid UIN Syarif Hidayatullah Jakarta Lampiran 7. Spektrum GCMS Senyawa 1-(4-metoksifenil)-1-penten-3-on 57 UIN Syarif Hidayatullah Jakarta (Lanjutan) 58 UIN Syarif Hidayatullah Jakarta Lampiran 8. Spektrum 1H-NMR Senyawa 1-(4-metoksifenil)-1-penten-3-on 59 UIN Syarif Hidayatullah Jakarta (Lanjutan) 60 UIN Syarif Hidayatullah Jakarta (Lanjutan) 61 UIN Syarif Hidayatullah Jakarta 62 Lampiran 9. Spektrum GCMS Hasil Optimasi Reaksi Kondensasi Aldol (1) (2) Reaksi selama 4 jam (1) (2) Reaksi selama 7 jam UIN Syarif Hidayatullah Jakarta 63 (Lanjutan) (2) (1) Reaksi selama 24 jam Keterangan : (1) Senyawa aldehid, (2) Senyawa target UIN Syarif Hidayatullah Jakarta 64 Lampiran 10. Perhitungan Reaksi Modifikasi Etil ρ-metoksisinamat a. Perhitungan Bahan Untuk Reaksi Hidrolisis Etil ρ-metoksisinamat 1) Etil ρ-metoksisinamat o Terpakai = 10 g (BM = 206,24g/mol) o Mol = 2) NaOH o BM = 40 g/mol o Mol = 1,5 x 0,0484 = 0,0726 mol o Massa = mol x BM = 0,0726 x 40 = 2,904 g ≈ terpakai 3 g b. Perhitungan Bahan Untuk Reaksi Oksidasi Asam ρ-metoksisinamat 1) Asam ρ-metoksisinamat o Terpakai = 4 g (BM = 178 g/mol) o Mol = 2) Kalsium Nitrat Tetrahidrat (Ca(NO3)2. 4H2O) o BM = 236,15 g/mol o Mol = 2 x 0,0224 = 0,0448 mol o Massa = mol x BM = 0,0448 x 236,15 = 10,57 g ≈ terpakai 10 gram 3) Asam Asetat Glasial o BM = 60,05 g/mol o ρ = 1,05 g/cm3 o Mol = 16 x 0,0224 = 0,3584 mol o Massa = mol x BM = 0,3584 x 60,05 = 21,52192 g o Volume = ≈ terpakai 20 mL UIN Syarif Hidayatullah Jakarta 65 c. Perhitungan Bahan Untuk Reaksi Kondensasi Aldol 4-metoksibenzaldehid 1) Senyawa 4-metoksibenzaldehid o Terpakai = 468,8 mg = 0,4688 g (BM = 136 g/mol) o Mol = 2) Etil Metil Keton o BM = 72,11 g/mol o ρ = 0,8050 g/mL o Mol = 13,5 x 0,00344 = 0,04644 mol o Massa = mol x BM = 0,04644 x 72,11 = 3,3487 g o Volume = ≈ terpakai 4,1684 mL 3) NaOH o BM = 40 g/mol o Mol = 1,5 x 0,00344 = 0,00516 mol o Massa = mol x BM = 0,00516 x 40 = 0,2064 g ≈ terpakai 206,82 mg UIN Syarif Hidayatullah Jakarta


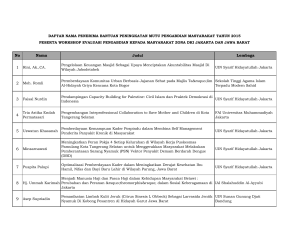
![SINTESIS SEhIYAWA TABIR SURYA TT`RT]NAI\I BENZOFENOI](http://s1.studylibid.com/store/data/000021403_1-08993e9cd2bed24b8ed359829b00854d-300x300.png)







