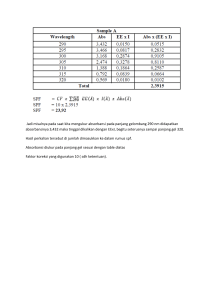
LAPORAN PRAKTIKUM BIOLOGI KIMIA ENZIM DISUSUN OLEH : Nama : Nurrahmi Azriati NPM : A1F018020 Hari,Tanggal : Sabtu, 5 Desember 2020 Pertemuan Ke : 3 (Tiga) DosenPengampu : 1. Nadia Amida, M.Pd 2. Drs. Hermansyah Amir, M.Pd Laboran : Tarmo Sujono, A.Md AsistenPratikum : 1. Weni Inda Sari (A1F017011) 2. Ahmad Mukhlasul Amri (A1F017030) 3. Darma Gusti Lestari (A1F017058) PROGRAM STUDI PENDIDIKAN KIMIA JURUSAN PENDIDIKAN MATEMATIKA DAN ILMU PENGETAHUAN ALAM FAKULTAS KEGURUAN DAN ILMU PENDIDIKAN UNIVERSITAS BENGKULU 2020 I. Tujuan 1. Untuk membuktikan kecepatan reaksi enzimatik 2. Untuk mengetahui pengaruh suhu terhadap kerja enzim II. Latar Belakang Enzim merupakan biokatalisator yang efektif, efisien dan selektif yang akan meningkatkan kecepatan reaksi kimia spesifik secara nyata. Enzim mengkatalisis reaksi tanpa produk samping dan ramah lingkungan sehingga enzim dapat dimanfaatkan untuk tujuan reaksi atau jenis produk yang diharapkan. Enzim adalah suatu kelompok protein yang menjalankan dan mengaturperubahan-perubahan kimia dalam sistem biologi. Reaksi atau proses kimia yang berlangsung dalam sel hidup dikarenakan adanya enzimyangbersifat sebagai katalisator yaitu zat-zat yang dapat mempercepat reaksi tetapi zatitu sendiri tidak ikut bereaksi. Enzim terbagi menjadi dua tipeyaitu: enzim ekstraseluler atau eksoenzim (berfungsi di luar sel) dan enzim intraseluler atau endoenzim (berfungsi dalam sel). Salah satu enzim ekstaseluler adalah enzim amilase yang dapat menguraikan pati menjadi unit-unit gula yanglebih kecil. Kegunaan utama enzim bagi organisme adalah sebagai katalis hayati. Walaupun dalam jumlah yang amat sedikit, katalis mempunyai kemampuan unik untuk mempercepat berlangsungnya reaksi kimiawi tanpa enzim itu sendiri terkonsumsi atau berubah setelah reaksi selesai. Enzim memegang peran penting dalam kehidupan manusia salah satunya adalah enzim amilase. Enzim amilase banyak dimanfaatkan dalam bidang industri tekstil, industri makanan, deterjen dan industri kertas. Selain itu, enzim ini juga di gunakan dalam pengujian limbah cair yang mengandung amilum. Oleh karena itu untuk lebih mengetahui dan memahami kerja suatu Enjim, khususnya kerja enzim amilase yang terdapat pada air liur yang dilarutkan pada pati, maka percobaan ini dilakukan dengan tujuan untuk mengetahui reaksi enzimatik dan juga pengaruh suhu terhadap kerja enzim III. Langkah Kerja Uji Protein Air liur 1. Diambil sebanyak 1 ml air liur orang gemuk dan air liur orang kurus dan dimasukkan ke gelas kimia 2. Diencerkan dengan 100 ml aquades 3. Disiapkan 6 tabung reaksi yang masing-masing ditempatkan dalam penangas air dengan suhu yang berbeda-beda 4. Dimasukkan larutan pati sebanyak 10 tetes dalam tabung B dan tabung U 5. Ditempatkan tabung dalam penangas air pada suhu yang telah ditentukan selama 5 menit 6. Ditambahkan air liur yang telah diencerkan sebanyak 1 ml ke dalam tabung U 7. Dipanaskan kembali dalam penangas air selama 5 menit 8. Ditambahkan 10 tetes larutan lugol 9. Ditambahkan 4 ml aquades 10. Diuji dengan genesis tiap-tiap tabung pada panjang gelombang 680 nm 11. Dicatat absorbansi suhu A blanko o 0 C 0,082 suhu ruang 0,097 o 37 C 0,214 60o C 0,251 o 100 C 0,125 IV. A uji gemuk 0,144 0,061 1,725 0,121 0,055 A uji kurus 0,224 0,075 0,111 0,126 0,053 Pengamatan Pada percobaan kali ini mengenai enzim, kami mengamati bagaimana reaksi enzimatis dan pengaruh suhu terhadap terja enzim. Disini sampel yang kami gunakan adalah air liur orang kurus dan air liur orang gemuk dengan larutan pati, larutan lugol, dan aquades. Untuk mengetahui pengaruh suhu terhadap kerja enzim ini dengan cara diencerkan air liur gemuk dan kurus dengan 100 ml aquadest dan siapkan 6 tabung reaksi dengan suhu berturut-turut adalah 0oC, 25oC, suhu ruang, 37oC, 60oC, dan 100oC dan pada masing-masing tabung diletakkan didalam penangas air yang kemudian dipanaskan selama 5 menit. Kemudian dimasukkan larutan pati sebanyak 10 tetes kedalam tabung U dan tabung B yang ditempatkan dalam penangas air dan dipanaskan selama 5 menit. Lalu dimasukkan air liur yang telah diencerkan kedalam tabung U sebanyak 1 ml dan dipanaskan kembali selama 1 menit kemudian ditambahkan 10 tetes larutan lugol dan 4 ml aquades dan diuji pada panjang gelombang 680 nm dan dicatat absorbansinya. V. Hasil dan Pembahasan 5.1 Hasil pengamatan 5.2 ∆A / menit A Au Au Blanko Gemuk Kurus Gemuk Kurus 0℃ 0,082 0,144 0,224 -0,062 -0,142 Suhu ruang 0,097 0,061 0,075 0,061 0,022 37℃ 0,214 1,725 0,111 -1,511 0,103 60℃ 0,251 0,121 0,126 0,13 0,125 100℃ 0,125 0,055 0,053 0,07 0,072 Suhu Pembahasan Pada percobaan kali ini membahas mengenai enzim yang bertujuan untuk mengetahui reaksi enzimatik dan untuk mengetahui pengaruh suhu terhadap kerja enzim. Enzim adalah biokatalisator yang berfungsi sebagai katalis dalam proses biologis. Enzim yang dikenal luas penggunaannya adalah enzim amilase, lipase, dan protease yang merupakan enzim hidrolitik pemecah senyawa makromolkul karbohidrat, lemak, dan ptotein. Enzim merupakan sekelompok protein yang mengatur dan menjalankan perubahan-perubahan kimia dalam sistem Biologi. Enzim dihasilkan oleh organ-organ pada hewan dan tanaman yang secara katalitik menjalankan berbagai reaksi, seperti hidrolisis, oksidasi, reduksi, isomerasi, adisi, transfer radikal, pemutusan rantai karbon. Secara umum, enzim menghasilkan kecepatan, spesifikasi, dan kedali pengaturan terhadap reaksi dalam tubuh. Enzim berfungsi sebagai katalisator, yaitu senyawa yang meningkatkan kecepatan reaksi kimia (Supriyatna, 2015 : 18-19) Menurut Samsuri (2017 : 20), Enzim merupakan protein yang bersifat katalis, sehingga sering disebut biokatalis. Enzim memiliki kemampuan mengaktifkan senyawa lain secara spesifik dan dapat meningkatkan kecepatan reaksi kimia yang akan berlangsung lama apabila tidak menggunakan enzim. Enzim yang digunakan harus sesuai dengan polisakarida yang akan dihidrolisis. Ada beberapa faktor yang mempengaruhi kerja enzim tersebut diantaranya adalah suhu, pH, dan inhibitor. Pada percobaan ini, yang diamati dalam pengaruh suhu terhadap kerja enzim. Menurut Risnoyatiningsih (2008), bahwa enzim dapat mempercepat reaksi (sebagai Katalis), enzim tidak mengubah kedudukan normal dari keseimbangan kimia Pada percobaan kali ini dilakukan pengujian terhadap enzim amilase dengan sampel air liur orang gemuk dan air liur orang kurus serta menggunakan larutan pati untuk membuktikan reaksi enzimatik yang ada pada sampel tersebut. Dalam air liur terdapat enzim amilase dimana fungsi dari enzim ini adalah untuk mengubah zat pati ke dalam glukosa. Percobaan pertama yang dilakukan pada percobaan adalah memanaskan larutan pati pada dua tabung berbeda, Tujuan dari pemanasan ini adalah untuk memutuskan ikatan karbohidrat di dalam larutan pati. Kemudian ditambahkan larutan air liur yang telah diencerkan ke tabung. Tujuan dari pengenceran ini adalah untuk menurunkan atau mengurangi konsentrasi air liur, sebab nantinya akan dilakukan pengukuran absorbansi, dimana pada genesis, konsentrasi sampel yang digunakan harus kecil. Kemudian, tabung diberi perlakuan suhu yang berbeda-beda dengan dipanaskan lagi selama 5 menit, dan diberi lugol. Fungsi penambahan lugol ini adalah sebagai Kofaktor. Kofaktor merupakan komponen atau senyawa kimia dan nonprotein yang berfungsi untuk mengaktifkan enzim. Setelah ditambahkan lugol, larutan pada tabung berubah warna. Adanya perubahan warna tabung menunjukkan bahwa enzim dari air liur (enzim α-amilase) telah berikatan dengan substrat (larutan pati). Sesuai dengan pernyataan Fessenden (1982), bahwa teori aktivasi enzim ini disebut teori kesesuaian terimbas : E+S ↔ Enzim Substrat E–S → kompleks E–P → kompleks E+P enzim produk enzim-substrat enzim-produk Diduga enzim menyesuaikan diri di sekitar substrat (molekul yang akan dikerjakan) untuk membentuk suatu kompleks enzim substrat. Ikatan-ikatan substrat dapat tegang Oleh gaya tarik menarik antara substrat dan enzim ikatan tegang memiliki energi tinggi dan lebih mudah terpatahkan oleh karena itu, reaksi yang diinginkan berlangsung lebih mudah dan menghasilkan suatu kompleks enzim – produk. Menurut Mahartoharsono (1990), bahwa enzim itu terbagi menjadi dua yaitu keseluruhan enzim dinamakan holo-enzim. Bagian proteinnya dinamakan apo-enzim dan bagian nonproteinnya disebut koenzim. Percobaan selanjutnya adalah melakukan pengujian secara Spektrofotometri untuk menentukan nilai Absorbansi untuk sampel. Setelah dilakukan pengukuran diperoleh nilai Absorbansi pada blanko yaitu pada suhu 0°C (0,082), suhu ruang (0,097), 37°C (0,214), 60°C (0,251), 100°C (0,125). Sedangkan untuk absorban sampel uji air liur gemuk yaitu pada suhu 0°C (0, 144), suhu ruangan (0,061), 37°C (1,725), 60°C (0,121), 100°C (0,055) dan absorban sampel uji air liur kurus yaitu pada suhu 0°C (0,224), suhu ruang (0,075), 37°C (0,111), 60°C (0,126), 100°C (0,053). Dari data Absorbansi yang diperoleh, dapat dihitung nilai selisih serapan antara tabung blanko dan tabung uji dengan rumus : ∆A = AB – AU Sehingga didapatkan nilai ∆A yaitu untuk air liur gemuk pada suhu 0°C (-0,062), suhu kamar (0,061), suhu 37°C (-1,511), suhu 60°C (0,013), suhu 100°C (0,07), dan untuk air liur kurus pada suhu 0°C (-0,142), suhu kamar (0,022), suhu 37°C (0,103), suhu 60°C (0,125), suhu 100°C (0,072) Berdasarkan nilai ∆A yang dihasilkan tersebut, dapat diketahui pengaruh suhu untuk kerja enzim. Dari hasil percobaan dapat diketahui bahwa rata-rata nilai absorbansi orang kurus lebih besar dibandingkan orang gemuk. Kita ketahui bahwa semakin tinggi suhu maka kerja enzim semakin cepat, tetapi apabila suhu sudah mencapai suhu optimum maka enzim akan mengalami denaturasi atau kerusakan. Pada suhu yang terlalu rendah kemantapan enzim tinggi tetapi aktivitasnya rendah, sedangkan pada suhu yang terlalu tinggi aktivitasnya tinggi tetapi kemantapannya rendah. Daerah temperatur saat kemantapan dan aktifitas enzim cukup disebut temperatur optimum, hal ini sesuai dengan literatur dimana menurut Noviyanti (2012), temperatur mempengaruhi aktivitas enzim maka temperatur rendah. Reaksi enzimatik berlangsung lambat, kenaikan akan mempercepat reaksi enzimatik mencapai maksimum, kenaikan temperatur melewati temperatur optimum akan menyebabkan enzim terdenatuasi. Faktor-faktor utama yang mempengaruhi kerja enzim yaitu konsentrasi substrat senyawa inhibitor dan aktivator, pH serta suhu. Berdasarkan hasil pengamatan didapatkan grafik. Berdasarkan grafik dapat diketahui bahwa pada suhu 60°C memiliki nilai absorbansi paling besar. Pada suhu diatas 60°C absorbansi larutan akan semakin turun. Hal ini dikarenakan semakin tinggi suhu maka kerja enzim semakin cepat tetapi apabila suhu sudah mencapai suhu optimum makan enzim akan mengalami denaturasi atau kerusakan sehingga kerja enzim semakin lambat bahkan dapat merusak enzim tersebut. Sedangkan pada suhu rendah aktivitas enzim menurun atau berhenti secara reversible karena molekulmolekul yang memiliki energi kinetik tinggi melampaui energi aktivitas, reaksinya sangat sedikit sehingga reaksi terjadi sangat lambat. VI. Kesimpulan 1. Enzim adalah biokatalisator yang berfungsi sebagai katalis dalam proses biologis. Enzim yang dikenal luas penggunaannya adalah enzim amilase, lipase, dan protease yang merupakan enzim hidrolitik pemecah senyawa makromolkul karbohidrat, lemak, dan ptotein. Pada percobaan kali ini dilakukan pengujian terhadap enzim amilase dengan sampel air liur orang gemuk dan air liur orang kurus serta menggunakan larutan pati untuk membuktikan reaksi enzimatik yang ada pada sampel tersebut. Dalam air liur terdapat enzim amilase dimana fungsi dari enzim ini adalah untuk mengubah zat pati ke dalam glukosa. Kerja enzim dinyatakan sebagai kemampuan enzim tersebut dalam mengubah substrat menjadi produk. Berdasarkan percobaan yang dilakukan kerja enzim dengan suhu yang berbeda-beda 2. Percobaan yang dilakukan adalah memanaskan larutan pati pada dua tabung berbeda, Tujuan dari pemanasan ini adalah untuk memutuskan ikatan karbohidrat di dalam larutan pati. Kemudian ditambahkan larutan air liur yang telah diencerkan ke tabung. Tujuan dari pengenceran ini adalah untuk menurunkan atau mengurangi konsentrasi air liur, sebab nantinya akan dilakukan pengukuran absorbansi, dimana pada genesis, konsentrasi sampel yang digunakan harus kecil. Kemudian, tabung diberi perlakuan suhu yang berbeda-beda dengan dipanaskan lagi selama 5 menit, dan diberi lugol. Fungsi penambahan lugol ini adalah sebagai Kofaktor. Setelah ditambahkan lugol, larutan pada tabung berubah warna. Adanya perubahan warna tabung menunjukkan bahwa enzim dari air liur (enzim α-amilase) telah berikatan dengan substrat (larutan pati). Berdasarkan hasil pengamatan dapat diketahui bahwa pada suhu 60°C memiliki nilai absorbansi paling besar yaitu 0,257°C. Pada suhu diatas 60°C absorbansi larutan akan semakin turun. Hal ini dikarenakan semakin tinggi suhu maka kerja enzim semakin cepat VII. Daftar Pustaka Fessenden, Ralph. 1982. Kimia Organik Jilid 2. Jakarta: Erlangga Mahartoharsono, Soekarsono. 1990. Biokimia 1. Yogyakarta: Ugm Press Noviyanti, Tri., Puji.A, Winda.R. 2012. Pengaruh Temperatur Terhadap aktivitas Enzim Protease dari Daun Sansaking (Pycnarrhena cauliflora Diels). Jurnal Kimia Khatulistiwa. Vol 1. No 1 ISSN : 2303-1077 Risnoyatiningsih, Sri. 2008. Yellow Sweet Potato Starch Hydrolysis Into Glucose Enzymatically. Jurnal Teknik Kimia. Vol 3. No 1 ISSN : 2655-8394 Samsuri, M., Gosan.M, Mardias, Hermansyah.H. 2017. Pemanfaatan Sellulosa Bagas untuk Produksi Ethanol Melalui Sakaritifikasi dan Fermentasi Serentak Dengan Enzim Xylanase. Jurnal Makara. Vol 11. No 1. Supriyatna, Ateng., Dea.A, Ayu.AJ, Dyna.H. 2015. Aktivitas Enzim Amilase, Lipase, dan Protease dai Larva. Jurnal ISTEK. Vol 9. No 2. ISSN : 1979-8911 VIII. Lampiran 1) Rincian Perhitungan Perhitungan ∆A/menit (gemuk) Perhitungan ∆A/menit (kurus) • • Suhu 0℃ ∆A/menit = AB – AU • ∆A/menit = AB – AU = 0,082 – 0,144 = 0,082 – 0,224 = -0,062 = -0,142 Suhu ruang • ∆A/menit = AB – AU • = 0,097 – 0,061 = 0,097 – 0,075 = 0,061 = 0,022 Suhu 37℃ • Suhu 37℃ ∆A/menit = AB – AU = 0,214 – 1,725 = 0,214 – 0,111 = - 1,511 = 0,103 Suhu 60℃ • ∆A/menit = AB – AU • Suhu ruang ∆A/menit = AB – AU ∆A/menit = AB – AU • Suhu 0℃ Suhu 60℃ ∆A/menit = AB – AU = 0,251 – 0,121 = 0,251 – 0,126 = 0,13 = 0,125 Suhu 100℃ ∆A/menit = AB – AU • Suhu 100℃ ∆A/menit = AB – AU = 0,125 – 0,05 = 0,125 – 0,053 = 0,07 = 0,072 2) Jawaban Pertanyaan 1. Mengapa suhu yang lebih tinggi dari suhu optimum menyebabkan enzim terdenaturasi ? 2. Mengapa dalam percobaan enzim digunakan air liur sebagai sampel 3. Bagaimana reaksi kimia yang terjadi antara larutan pati dengan air liur ? Jawaban : 1. Semakin tinggi suhu maka kerja enzim semakin cepat, tetapi apabila suhu sudah mencapai suhu optimum maka enzim akan mengalami denaturasi atau kerusakan. Pada suhu yang terlalu rendah kemantapan enzim tinggi tetapi aktivitasnya rendah, sedangkan pada suhu yang terlalu tinggi aktivitasnya tinggi tetapi kemantapannya rendah. Daerah temperatur saat kemantapan dan aktifitas enzim cukup disebut temperatur optimum, temperatur mempengaruhi aktivitas enzim maka temperatur rendah. Reaksi enzimatik berlangsung lambat, kenaikan akan mempercepat reaksi enzimatik mencapai maksimum, kenaikan temperatur melewati temperatur optimum akan menyebabkan enzim terdenatuasi 2. Karena pada air liur terdapat enzim amilase yang membantu pencernaan makanan didalam mulut sehingga dapat diketahui aktivitas enzim pada suhu tertentu dalam percobaan ini 3. Enzim berasal dari air liur yang mengandung 𝛼-amilase yang berfungsi mengkatalis. Reaksi hidrolisis amilum lalu ditambahkan lugol Lugol → I2 / KI(aq) Dengan reaksi Amilum + I2 → amilum – iod 3) Bukti pustaka Pengaruh temperatur terhadap temperatur optimum tercapai. Kenaikan aktivitas enzim protease Uji pengaruh temperatur terhadap aktivitas enzim dilakukan untuk mengetahui kondisi optimum enzim dalam mendegradasi substrat. Setiap enzim memiliki aktivitas maksimum pada temperatur tertentu, aktivitas enzim akan semakin meningkat . dengan bertambahnya temperatur hingga temperatur di atas temperatur optimum akan menyebabkan aktivitas enzim menurun (Baehaki, 2008). Pengaruh suhu terhadap aktivitas protease ekstrak kasar daun sangsangk dapat dilihat pada Gambar 1 dan Tabel 1 YELLOW SWEET POTATO STARCH HYDROLYSIS INTO GLUCOSE ENZYMATICALLY Sri Risnoyatiningsih Jurusan Teknik Kimia Fakultas Teknologi Industri UPN “Veteran” Jawa Timur Jl. Raya Rungkut Madya Gunung Anyar Surabaya email : [email protected] ABSTRACT Glucose is a monosaccharide found in many fruits, and plants obtained through a process using enzyme hydrolysis of starch saccharide. Sweet potato starch Hydrolisis run with three neck flask equipped with a stirrer. In Liquifikasi stage, three-neck flask is inserted into the starch solution which has been set temperature and the pH was added HCI and in the heat, then added α-amylase enzyme in a certain time. Saccharification second stage, where the results liquification cooled, set the temperature and pH on certain conditions. Then added enzyme giukoamilase by volume according to the specified variable, and incubated at a given time. At a certain time interval was taken a few examples of the analyzed samples will be analyzed glucose levels Process behavior observed in this study were changes in temperature, hydrolysis time and the addition of enzymes, the best hydrolysis results obtained at 60 ° C, pH 4.5 and the addition of 0.7 ml of glucoamylase and time hydrolysis 5 days with glucose levels reaching 5 , 65% and conversion yield of 66.8% and 22.59%. Key words: Sweet Potato Starch, Liquificationi, saccharifictsion, glucose, α-amylase enzyme PENDAHULUAN Tanaman ubi jalar merupakan tanaman yang mudah pemeliharaannya, tahan terhadap kekeringan , murah biaya perawatannya, tidak mengherankan kalau disukai banyak pertani, terutama diusahakan sebagai tanaman palawija, sebagai tanaman gilir setelah padi. Selama ini masyarakat menganggap ubi jalar merupakan bahan pangan dalam situasi darurat (kurang makan), bahkan disebut sebagai makanan kelas bawah. Padahal potensi ekonomi dan sosial ubi jalar cukup tinggi dan juga sudah dikenal pada taraf internasional, seperti di Amerika Serikat atau negara-negara maju lain, ubi jalar dijadikan makanan mewah dan bahan aneka industri, seperti industri fermentasi, textil, lem , kosmetik, farmasi dan sirup. Karbohidrat Karbohidrat merupakan sumber kalori utama bagi manusia selain protein dan lemak. Karbohidrat yang mempunyai rumus empiris (CH2o)n ini juga mempunyai peranan penting dalam menentukan karakteristik bahan makanan, misalnya rasa, warna, tekstur, dan lain-lain. Sedangkan dalam tubuh, karbohidrat berguna untuk mencegah tibulnya pemecahan pemecahan protein tubuh yang berlebihan, kehilangan mineral dan berguna untuk membantu metabolisme lemak dan protein. Di alam, karbohidrat dibentuk dari reaksi CO2 dan H2O dengan bantuan sinar matahari melalui proses fotosintesis dalam sel tanaman yang berkrolofil. Sebagian besar bahan-bahan nabati yang merupakan sumber karbohidrat diperoleh dari serelia, umbi-umbian, dan batang tanaman misanya sagu. Sumber karbohidrat yang mmerupakan bahan makanan pokok di berbagai daerah di Indonesia adalah biji-bijian, khususnya beran dan jagung. Pada umumnya karbohidrat dapat dikelompokkan menjadi 3 bagian, yaitu : a. Monosakarida Merupakan suatu molekul yang terdiri dari 5 atau 6 atom C. Monosakarida yang mengandung satu gugus aldehida disebut aldosa, sedangkan ketosa mempunyai satu gugus keton. Monosakarida dengan 6 atom C disebut heksosa, misal(dekstrosa atau gula anggur), fruktosa (levulosa atau gula buah), dan galaktosa. Sedangkan yang Enzim membantu Enzim dapat mempercepat reaksi (sebagai produk, tetapi akhirnya jumlah produk tetap katalis), enzim tidak diubah oleh reaksi yang sama dengan produk yang diperoleh tanpa dikatalisnya, dan enzim tidak mengubah enzim. Kondisi kedudukan aktifitas enzim normal dari kesetimbangan kimia. Dengan kata lain enzim dapat mempercepat yang pembentukan mempengaruhi diantaranya konsentrasi enzim, konsentrasi substrat, pH, dan suhu. PEMANFAATAN SELLULOSA BAGAS UNTUK PRODUKSI ETHANOL MELALUI SAKARIFIKASI DAN FERMENTASI SERENTAK DENGAN ENZIM XYLANASE M. Samsuri1,2, M. Gozan1, R. Mardias, M. Baiquni, H. Hermansyah1, A. Wijanarko1, B. Prasetya2, dan M. Nasikin1 1. Departemen Teknik Kimia, Fakultas Teknik, Universitas Indonesia, Depok 16424, Indonesia 2. Pusat Penelitian Bioteknologi, Lembaga Ilmu Pengetahuan Indonesia (LIPI), Cibinong, Bogor 16911, Indonesia E-mail: [email protected] Abstrak Bagas merupakan residu padat pada proses pengolahan tebu menjadi gula, yang sejauh ini masih belum banyak dimanfaatkan menjadi produk yang mempunyai nilai tambah (added value). Bagas yang termasuk biomassa mengandung lignoselulosa sangat dimungkinkan untuk dimanfaatkan menjadi sumber energi alternatif seperti bioetanol atau biogas. Dengan pemanfaatan sumber daya alam terbarukan dapat mengatasi krisis energi terutama sektor migas. Pada penelitian ini telah dilakukan konversi bagas menjadi etanol dengan menggunakan enzim xylanase. Perlakuan dengan enzim lainnya saat ini sedang dikerjakan di laboratorium kami mengingat hemisulosa juga mengandung polisakarida lainnya yang dapat didekomposisi oleh berbagai enzim. Hasil penelitian menunjukkan kandungan lignoselulosa pada bagas sebesar lebih kurang 52,7% selulosa, 20% hemiselulosa, dan 24,2% lignin. Hemiselulosa merupakan polisakarida yang dapat dihidrolisis oleh enzim xylanase dan kemudian akan difermentasikan oleh yeast S. cerevisiae menjadi etanol melalui proses Sakarifikasi dan Fermentasi Serentak (SSF). Beberapa parameter yang dianalisis pada penelitian ini antara lain kondisi pH (4, 4,5, dan 5), untuk meningkatkan kuantitas etanol dilakukan penambahan HCl berkonsentrasi rendah (0,5% dan 1% (v/v)) dan bagas dengan perlakuan jamur pelapuk putih (L. edodes) selama 4 minggu. Proses SSF dilakukan dengan waktu inkubasi selama 24, 48, 72, dan 96 jam. Perlakuan dengan pH 4, 4,5, dan 5 menghasilkan konsentrasi etanol tertinggi berturut-turut 2,357 g/L, 2,451 g/L, 2,709 g/L. Perlakuan penambahan HCl konsentrasi rendah mampu meningkatkan produksi etanol, penambahan dengan konsentrasi HCL 0,5 % dan 1 % berturut-turut menghasilkan etanol 2,967 g/L, 3,249 g/L. Perlakuan dengan menggunakan jamur pelapuk putih juga dapat meningkatkan produksi etanol yang dihasilkan. Setelah bagas diberi perlakuan L. edodes 4 minggu mampu menghasilkan etanol dengan hasil tertinggi 3,202 g/L. Abstract Utilization of Bagasse Cellulose for Ethanol Production through Simultaneous Saccharification and Fermentation by Xylanase. Bagasse is a solid residue from sugar cane process, which is not many use it for some product which have more added value. Bagasse, which is a lignosellulosic material, be able to be use for alternative energy resources like bioethanol or biogas. With renewable energy resources a crisis of energy in Republic of Indonesia could be solved, especially in oil and gas. This research has done the conversion of bagasse to bioethanol with xylanase enzyme. The result show that bagasse contains of 52,7% cellulose, 20% hemicelluloses, and 24,2% lignin. Xylanase enzyme and Saccharomyces cerevisiae was used to hydrolyse and fermentation in SSF process. Variation in this research use pH (4, 4,5, and 5), for increasing ethanol quantity, SSF process was done by added chloride acid (HCl) with concentration 0.5% and 1% (v/v) and also pre-treatment with white rot fungi such as Lentinus edodes (L.edodes) as long 4 weeks. The SSF process was done with 24, 48, 72, and 96 hour’s incubation time for fermentation. Variation of pH 4, 4,5, and 5 can produce ethanol with concentrations 2,357 g/L, 2,451 g/L, 2,709 g/L. The added chloride acid (HCl) with concentration 0.5% and 1% (v/v) and L. edodes can increase ethanol yield, The highest ethanol concentration with added chloride acid (HCl) concentration 0.5% and 1% consecutively is 2,967 g/L, 3,249 g/L. The highest ethanol concentration with pre-treatment by L. edodes is 3,202 g/L. Keywords: bagasse, bioethanol, hemicelluloses, SSF, xylanase, S. cerevisiae, Lentinus edodes Produksi Etanol dengan Proses SSF Secara umum sintesis bioetanol yang berasal dari biomassa terdiri dari dua tahap utama, yaitu hidrolisis dan fermentasi. Pada metode terdahulu proses hidrolisis dan fermentasi dilakukan secara terpisah atau Separated Hydrolisys and Fermentation (SHF) dan yang terbaru adalah proses Simultaneous Saccharification and Fermentation (SSF) atau Sakarifikasi dan Fermentasi Serentak (SFS). Satu diantara beberapa keuntungan dari proses SSF adalah hidrolisis dan fermentasi dilakukan dalam satu wadah atau reaktor sehingga dapat berlangsung secara efisien. Hidrolisis bertujuan untuk memecah polisakarida menjadi monosakarida sehingga dapat langsung difermentasi oleh yeast. Pada penelitian ini hidrolisis dilakukan secara biologis, yaitu menggunakan enzim. Enzim merupakan protein yang bersifat katalis, sehingga sering disebut biokatalis. Enzim memiliki kemampuan mengaktifkan senyawa lain secara spesifik dan dapat meningkatkan kecepatan reaksi kimia yang akan berlangsung lama apabila tidak menggunakan enzim. Enzim yang digunakan harus sesuai dengan polisakarida yang akan dihidrolisis biokatalisator yang berfungsi sebagai dkk., katalis sekelompok protein yang mengatur dan dalam proses biologis 2011). (Lehninger, 1982). Enzim yang dikenal menjalankan luas kimia penggunaannya adalah enzim Enzim merupakan perubahan-perubahan dalam sistem Biologi. amilase, lipase, dan protease yang dihasilkan merupakan enzim hidrolitik pemecah hewan senyawa katalitik menjalankan berbagai reaksi, makromolkul karbohidrat, oleh dan organ-organ Enzim tanaman secara lemak, dan ptotein. Berdasarkan hal seperti tersebut maka dilakukan “Uji Aktivitas isomerasi, Enzim Amilase, Lipase, Dan Protease pemutusan rantai karbon (Sumardjo, dari 2009). Ekstrak illucens” Usus untuk Larva mempelajari Hermetia potensi hidrolisis, yang pada adisi, Secara menghasilkan oksidasi, reduksi, transfer radikal, umum, kecepatan, enzim spesifikasi, larva H.illucenssebagai penghasil enzim dan kedali pengaturan terhadap reaksi amilase, lipase, dan protease serta dalam tubuh. Enzim berfungsi sebagai pendegradasi limbah organik.Larva H. katalisator, illucensmemiliki protease, meningkatkan kecepatan reaksi kimia amilase, dan lipase,protease berfungsi (Marks, dkk., 2000). Suatu enzim dapat mengubah protein menjadi asam amino, mempercepat amilase 1011kali lebih cepat dibandingkan ketika enzim mengubah pati menjadi maltosa,dan lipase mengubah lemak reaksi menjadi asam lemak dan gliserol. (Kim, katalis yaitu tersebut senyawa reaksi tidak yang 108sampai menggunakan