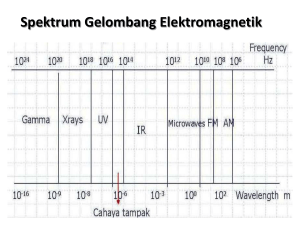
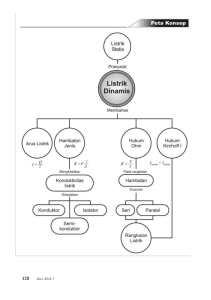
ikatan kimia - ajmainchemistry
advertisement

MODUL 2 IKATAN KIMIA ( MERAMAL BENTUK GEOMETRI MOLEKUL ) Standar Kompetensi ( SK ) : Memahami struktur untuk meramalkan sifat-sifat periodik unsur,struktur molekul, dan sifat-sifat senyawa Kompetensi Dasar ( KD ) : Menjelaskan teori jumlah pasangan elektron di sekitar inti atom dan teori hibridisasi untuk meramal bentuk molekul. Indikator : 1. Menentukan bentuk molekul berdasarkan teori pasangan elektron ( VSPER ). 2. Menentukan bentuk molekul berdasrkan teori hibridisasi. Kegiatan Pembelajaran : 1. TEORI DOMAIN ELEKTRON Domain elektron adalah daerah ( ruang ) di sekitar atom pusat di mana pasangan elektron ditemukan.Pada atom pusat terdapat dua jenis domain elektron yaitu : domain elektron ikatan dan domain elektron bebas. Domain elektron yaitu : Sepasang electron ikatan ( tunggal, rangkap dua atau tiga ) di sebut satu domain Sepasang pasangan electron bebas berarti satu domain Contoh : a. Molekul : H2O Struktur Lewis : …………….. Domain electron : .................... Domain elektron ikatan ( DEI ): ...................... Domain elektron bebas( DEB ): ........................ b. Molekul CO2 Struktur Lewis : …………………. Domain electron : …………………. Domain elektron ikatan( DEI ): …………. Domain elektron bebas( DEB ): ………….. 2. MERUMUSKAN TIPE GEOMETRI SUATU MOLEKUL Prinsip-prinsip dasar teori domain elektron a. b. Antar domain elektron pada kulit atom pusat saling tolak-menolak sehingga domain elektron akan mengatur diri sedemikian rupa sehingga tolak-menolak di antaranya menjadi minimum Urutan kekuatan tolak-menolak di antara domain elektron adalah Gaya tolak-menolak antar DEB > gaya tolak-menolak DEB dan DEI > gaya tolak DEI Ikatan kimia ( bentuk molekul)_2013 Page 1 Tabel 1 : Berbagai bentuk molekul berdasarkan teori pangan elektron Jumlah Domain elektron terikat (DEI) Jumlah Domain elektron Bebas (DEB) Bentuk Molekul Gambar 2 0 Linier B–A–B 2 2 Planar bentuk V 2 3 Linier 3 0 Segitiga datar/Trigonal Planar 3 1 Paramid trigonal 3 2 Planar bentuk T 4 0 Tetra hedron/tetrahedral 4 1 Bidang 4 4 2 Segi 4 planar 5 0 Bipiramid trigonal 5 1 Piramid segi 4 Ikatan kimia ( bentuk molekul)_2013 Page 2 Jumlah Domain elektron terikat (DEI) Jumlah Domain elektron Bebas (DEB) Bentuk Molekul 6 0 oktahedron c. Gambar Untuk meramal bentuk geometri suatu molekul dapat di gunakan persamaan berikut : AXnEm Dengan : A = atom pusat X = atom yang terikat ke atom pusat E = domain elektron bebas n = jumlah DEI m = jumlah DEB Perumusan untuk mencari nilai E : E = ( EV – X ) 2 EV = Jumlah elektron valensi atom pusat X = Jumlah atom terikat pada atom pusat Tipe molekul dapat ditentukan dengan langkah-langkah sebagai berikut : a. Senyawa biner berikatan tunggal Contoh : Tentukan tipe molekul dari 1. NH3 2. CH4 3. XeF4 Jawab : b. Senyawa berikatan rangkap dan atau ikatan kovalen koordinat E = ( EV – X ) 2 EV = Jumlah elektron valensi atom pusat X = jumlah electron terikat(kovalen tunggal atau rangkap) pada atom pusat. Contoh : Tentukan tipe molekul berikut ini : 1. SO3 2. CO2 3. SO2 Jawab : Ikatan kimia ( bentuk molekul)_2013 Page 3 3. Penentuan bentuk molekul dengan teori hibridisasi Hibridisasi adalah proses penggabungan orbital-orbital sehingga terbentuk orbital baru dengan tingkat energi sama. Menurut teori ini kita dapat menentukan bentuk molekul dengan mengikuti langkah-langkah sebagai berikut : 1. Menuliskan konfigurasi elektron dari atom pusat dengan aturan Aufbau dan diagram orbital. 2. Jika jumlah elektron tunggal dari atom pusat, kurang jumlahnya dari unsur yang akan terikat dengan atom pusat, perlu diadakan eksitasi elektron terlebih dahulu. 3. Pasangkan elektron yang berasal dari atom lain ke elektron tunggal yang sudah disediakan oleh atom pusat, lalu gabungkan orbital yang terdapat pada level yang sama, itulah hibridisasinya. 4. Lihat tabel yang tersedia untuk menentukan bentuk molekul. Tabel 2 : Hibridisasi dan bentuk molekul Hibridisasi DEI DEB Bentuk molekul linier sp2 sp2 sp3 sp3 sp3 dsp2 sp3d 2 d sp3 / sp3d2 d2sp3 / sp3d2 d2sp3 / sp3d2 2 3 4 3 2 4 5 6 5 4 0 0 0 1 2 0 0 0 1 2 Linier Segitiga planar Tetrahedron Piramid segitiga Planar bentuk v Segiempat planar Bipiramidal Oktahedron Piramida segiempat Segiempat planar Catatan: Gambar dari bentuk molekul di atas dapat dilihat pada tabel 1. Contoh : Tentukan bentuk molekul BF3, jika diketahui nomor atom B = 5, dan F = 9 dengan teori hibridisasi! Penyelesaian : Ikatan kimia ( bentuk molekul)_2013 Page 4