1. GLIKOLISIS PENDAHULUAN Sebagian besar
advertisement

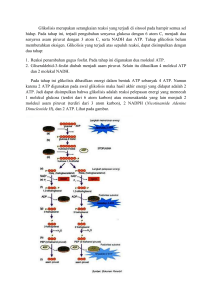
1. GLIKOLISIS PENDAHULUAN Sebagian besar jaringan membutuhkan glukosa meskipun dalam jumlah minimum, terutama otak dan eritrosit. Glikolisis merupakan jalur utama untuk pemanfaatan glukosa dan di sitosol semua sel. Jalur ini merupakan jalur unik, karena jika ada oksigen dapat menggunakan oksigen melalui rantai respirasi dalam mitokondria (erob) atau dapat juga bekerja bila sama sekali tidak ada oksigen (anerob). Namun untuk mengoksidasi glukosa, setelah menjadi piruvat sebagai basil akhir glikolisis membutuhkan tidak hanya oksigen molekuler tapi juga sistem enzim mitokondrial yaitu kompleks piruvat dehidrogenase, siklus asam sitrat dan rantai respirasi KEPENTINGAN BIOMEDIS Glikolisis tidak hanya merupakan jalur utama untuk metabolisme glukosa, tapi juga merupakan jalur utama untuk metabolisme fruktosa dan galaktosa yang berasal dari diet. Dan glikolisis dapat dihasilkan ATP tanpa adanya oksigen, hal ini memungkinkan otot skelet dapat bekerja dengan kecepatan yang tinggi pada keadaan erob dan bila oksigen kurang melakukan glikolisis penting untuk mempertahankan kehidupannya pada episode anoksik. Sebaliknya otot jantung yang teradaptasi untuk keadaan kondisi erob, kemampuan glikolisisnya relatif rendah, dan mempunyai kemampuan bertahan yang rendah pada keadaan iskemia. Penyakit yang jarang ditemukan enzim-enzim tersebut (misalnya piruvat kinase); kondisi ini terutama yaitu kurangnya aktivitas anemia hemolitika atau jika terjadi pada otot skelet (misalnya fosfofruktokiase) menyebabkan kelelahan fatigue. Pada sel kanker yang tumbuh cepat, glikolisis berjalan melebihi kecepatan yang diperlukan oleh siklus asam sitrat. Sehingga akan dihasilkan piruvat lebih banyak dibanding yang dapat dimetabolisme. Selanjutnya akan dihasilkap laktat yang berlebih, yang memberikan sifat asam pada lingkungan tumor tersebut, merupakan suatu keadaan yang dapatditerapkan untuk terapi beberapa kanker. Asidosis laktat hasil dan berbagai kasus dapat terjadi, termasuk akibat defisiensi piruvat dehidrogenase. GLIKOLISIS DAPAT BERFUNGSI PADA KEADAAN ANEROB Pada awalnya, glikolisis ditemukan dari proses fermentasi ragi yang sama dengan pemecahan glikogen dalam otot. Telah diamati bahwa jika otot berkontraksi pada lingkungan anerob, glikogen akan hilang dan laktat akan nampak sebagai produk akhir utama. Jika diberikan oksigen, keadaan aerob kembali dan glikogen ada kembali, sedangkan laktat menghilang. Namun, jika kontraksi terjadi pada keadaan erob laktat tidak tertimbun dan piruvat sebagai produk akhir utama dari glukolisis. Piruvat selanjumya dioksidasi menjadi CO2 dan H20. Dari hasil pengamatan ini dapat dipisahkan metabolisme karbohidrat menjadi fase anerob dan erob. Namun sebenarnya reaksi dalam glikolisis baik ada oksigen atau tidak adalah sama, kecuali pada produk akhir dan ATP yang dihasilkan. Jika oksigen rendah, reoksidasi NADH ujung terbentuk dari NAJD+ selama glikolisis terganggu. Pada keadaan ini NADH direoksidasi bersamaan dengan reduksi piruvat menjadi laktat dan NADH menjadi NAD+. Dengan terjadinya reaksi ini, energi yang dilepaskan akan terbatas. Akibatnya, untuk mendapatkan energi yang cukup, diperlukan glukosa lebih banyak, untuk mengalami glikolisis pada keadaan anerob dibandingkan keadaan erob (lihat gambar dalam lampiran). REAKSI-REAKSI DALAM GLIKOLISIS MERUPAKAN SATU REAKSI UTAMA PENGGUNAAN GLUKOSA Persamaan reaksi glikolisis (glukosa menjadi laktat) adalah sbb. : Glukosa + 2 ADP + 2 Pi 2 laktat + 2 TP + 2 H20 Semua enzim dalam jalur glikolisis terdapat ekstramitokondiral merupakan fraksi sel yang larut dalam sitosol. Sebelum glukosa masuk dalam jalur glikolisis, glukosa mengalami fosforilasi menjadi glukosa -6-fosfat oleh enzim heksokinase. Namun di sel parenkhim hepar dan dalam sel pankreas peran ini dilaksanakan oleh enzim glukokinase yang aktivitasnya dalam hepar dapat diinduksi dan dipengaruhi perubahan status nutrisi. ATP diperlukan sebagai donor fosfat, bereaksi sebagai kompleks Mg-ATP. Reaksi disertai dengan lepasnya energi bebas sebagai panas, sehingga pada keadaan fisiologis, reaksi terjadi irreversibel. Heksokinase dihambat secara alosterik oleh produk yaitu heksosa-6-fosfat. Heksokinase mempunyai afinitas tinggi terhadap substrat glukosa (Km rendah). lni akan menjamin masuknya glukosa ke jaringan walaupun kadar glukosa dalam darah rendah, dengan memfosforilasi semua glukosa yang masuk ke dalam sel, sehingga mempertahankan perbedaan kadar glukosa yang besar antara darah dan lingkungan intrasel. Enzim ini juga bekerja pada anomer glukosa a dan 13 dan juga mengkatalisis fosforilasi heksosa lain tetapi dengan kecepatan yang lebih rendah dibandingkan glukosa. Mg2+ 1) Glukosa + ATP Glukosa-6-fosfat + ADP Fungsi glukokinase juga mengambil glukosa dan darah setelah makan. Glukokinase berbeda dengan heksokinase, is mempunyai Km yang tinggi terhadap glukosa, dan bekerja optimal pada kadar glukosa di atas 5 mmol/L. Enzim ini khusus untuk glukosa. Glukosa-6-fosfat adalah senyawa yang penfing yang menjembatani berbagai jalur metabolik (glikolisis, glukoneogenesis, jalur pentosa fosfat, glikogenesis dan glikogenolisis). Pada glikolisis, Glukosa-6-fosfat diubah menjadi fruktosa-6-fosfat oleh fosfoheksose isomerase, terjadi isomerisasi aldosa-ketosa dan hanya anomer-a dari glukosa-6-fosfat yang dipengaruhi. 2) a-D-glukosa-6-fosfat a-D-fruktosa-6-fosfat Reaksi ini diikuti dengan fosforilasi berikutnya dengan ATP dikatalisis oleh fosfofruktokinase (fosfofruktokinase-1) menghasilkan fruktosa-1,6-difosfat. Fosfofruktokinase adalah enzim allostrik dan dapat diinduksi dan peran utamanya dalam mengatur kecepatan glikolisis. Reaksi ini merupakan reaksi irreversibel pada keadaan fisiologis 3) D-fruktosa-6-fosfat + ATP D-Fruktosa-1,6-difosfat Reaksi selanjutnya Fruktosa-1,6-difosfat dipecah oleh aldolase (fruktosa 1,6-difosfat aldolase menjadi 2 those fosfat, gliseraldehid-3-fosfat dan dihidroksiaseton fosfat 4) D-fruktosa-1,6-difosfat D- gliseraldehid 3-fosfat + dihidroksiaseton fosfat Beberapa macam aldolase telah ditemukan, semua mengandung 4 subunit. Aldolase A terdapat di sebagian besar jaringan, sedang aldolase B terdapat di hepar dan ren. Fruktose 6-fosfat yang terdapat dalam sel terutama dalam bentuk furanosa, tapi bereaksi dengan fosfoheksose isomerase, fosfofruktokinase dan aldolase dalam bentuk konfigurasi cincin terbuka. Gliseraldehid 3-fosfat dapat diubah menjadi dihidroksi aseton fosfat atau sebaliknya oleh enzim fosfotriose isomerase. 5) D-gliseraldehid dihidroksi aseton fosfat Glikolisis berlanjut dengan oksidasi gliseraldehid 3-fosfat menjadi 1,3bisfosfogliserat, dan karena aktivitas fosfotriose isomerase, dihidroksi aseton fosfat juga dioksidasi menjadi 1,3bisfosfogliserat melalui gliseraldehid 3-fosfat. 6) gliseraldehid 3-fosfat + NAD+ + Pi Reaksi ini dipengaruhi 1,3-bisfosfogliserat + NADH + H+ enzim gliseraldehid 3-fosfat dehidrogenase membutuhkan NAD+. Secara struktur enzim terdiri dari 4 polipeptida identik membentuk tetramer. Empat gugus —SH terdapat pada masing-masing polipeptida yang berasal dari residu sistein. Salah satu dari gugus —SH merupakan tapak aktif enzim. Mula-mula substrat bergabung dengan gugus-SH tersebut, membentuk suatu hemiasetal yang kemudian diubah menjadi tiol ester bertenaga tinggi dengan oksidasi; hidrogen yang diambil pada reaksi ini dipindahkan ke NAD+ yang diikat enzim. NADH yang dihasilkan tidak begitu kuat diikat enzim, selanjutnya akan dilepaskan digantikan NAD+. Selanjutnya dengan fosforolisis, Pi ditambahkan membentuk 1,3-bisfosfogliserat dan enzim bebas. Energi yang dilepaskan selama oksidasi disimpan dengan membentuk gugus sulfur berenergi tinggi , yang setelah fosforolisis menjadi gugus fosfat energi tinggi pada posisi 1,3-bisfosfogliserat. Fosfat energi tinggi ini ditangkap sebagai ATP pada reaksi berikutnya dengan ADP oleh pengaruh enzim fosfogliserat kinase melepaskan 3-fosfogliserat. 7) 1,3-bisfosfogliserat + ADP 4 A.3-fosfogliserat + ATP Karen diperoleh 2 molekul triosa fosfat dari 1 molekul glukosa yang mengaiami glikolisis, maka juga dihasilkan 2 molekul ATP per molekul glukosa, sebagai basil fosforilasi pada peringkat substrat. Jika terdapat arsenat, is akan bersaing dengan fosfat anorganik (Pi) menghasilkan 1-arseno-3-fosfogliserat, yang dapat terhidrolisis spontan menghasilkan 3-fosfogliserat dan panas, tanpa menghasilkan ATP. Ini salah satu contoh penting ciari kemampuan arsenat sebagai uncoupler pada oksidasi dan fosforilasi. 3-fosfogliserat selanjutnya diubah menjadi 2-fosfogliserat oleh enzim fosfogliserat mutase sedang 2,3-bisfosfogliserat (difosfogliserat, DPG) adalah senyawaantara pada reaksi ini. 8) 3-fosfogliserat 2-fosfogliserat Langkah berikutnya dikatalisis oleh enolase dan melibatkan reaksi dehidrasi dan distribusi ulang energi dalam molekul, menghasilkan fosfat energi tinggi, pada posisiposisi dengan membentuk fosfoenol piruvat. Enolase dihambat oleh fluorida. Enzim juga tergantung oleh adanya atau Mn++. 9) 2-fosfogliserat fosfoenolpiruvat +H20 Fosfat energi tinggi dari fosfoenolpiruvat clipindahkan ke ADP oleh enzim piruvat kinase menghasilkan 2 molekul ATP. Enolpiruvat yang terbetuk pada reaksi ini secara spontan diubah menjadi piruvat bentuk keto. Ini adalah salah satu reaksi tak terbalikkan (searah) lainnya yang disertai dengan hilangnya energi bebas sebagai panas 10) fosfoenolpiruvat + ADP piruvat + ATP Sekarang status redox pada jaringan menentukan yang man dari kedua jalur ini yang akan berlangsung. Jika keadaan anerob, reoksidasi NADH berlangsung dengan memindahkan reducing equivalent piruvat. Piruvat direduksi oleh NADH menjadi laktat dikatalisis oleh laktat dehidrogenase. Reoksidasi NADH melalui pembentukan laktat memungkinkan glikolisis terjadi tanpa adanya oksigen dengan menghasilkan NAD+ untuk siklus lain yang dikatalisis oleh gliseraldehid 3-fosfat dehidrogenase. Pada keadaan erob, piruvat masuk mitokondria, dan setelah diubah menjadi asetil-KoA dioksidasi menjadi CO2 melalui siklus asam sitrat. Reducing equivalent dari NADH yang terbentuk dalam glikolisis masuk mitokondria untuk dioksidasi melalui 2 shuttle .(Baca topik respirasi seluler) JARINGAN-JARINGAN YANG BEKERJA PADA KEADAAN HIPOKSIA CENDERUNG MENGHASILKAN LAKTAT Lingkungan hipoksia ada pada otot skelet, terutama serabut putih, yang kecepatan bekerjanya tidak dibatasi oleh kapasitas oksigenasi. Peningkatan jumlah laktat dapat diamati di jaringan, darah dan urine. Glikolisis di eritrosit, walaupun pada lingkungan erob, selalu berakhir dengan laktat, karena tidak ada mitokondria tempat enzim untuk reaksi oksidasi piruvat secara erob. Paling sedikit 90% kebutuhan energi total eritrosit mamalia diperoleh dari glikolisis. Disamping otot skelet serabut putih, otot polos dan eritrosit, jaringan lainnya yang biasanya memperoleh sebagian besar dari glikolisis dan menghasilkan laktat adalah otak, traktus gastrointestinal, medula renalis, retina dan kulit. Hepar, ginjal dan jantung biasanya mengambil laktat dan mengoksidasinya, tapi pada keadaan anerob juga menghasilkan laktat. GLIKOLISIS DIATUR PADA TIGA TAHAP YANG MELIBATKAN REAKSI TIDAK SEIMBANG Walaupun sebagian besar reaksi glikolisis adalah dapat dibalikkan, tiga di antaranya adalah reaksi eksergonik dan secara fisiologis talc terbalikkan. Reaksi tersebut adalah yang dikatalisis oleh heksokinase atau glukokinase, fosfofruktokinase dan piruvat kinase yang merupakan tapak utama pengaturan glikolisis. GLIKOLISIS DALAM ERITROSIT Dalam sebagian besar eritrosit mamalia, jalur yang dikatalisis oleh fosfogliserat kinase diarahkan jalur lain dengan proses yang menghasilkan panas dan tidak menghasilkan energi. Reaksi tersebut dikatalisis oleh 2,3-bisfosfogliserat fosfatase. Hilangnya fosfat energi tinggi, berarti tidak dihasilkan ATP jika reaksi melalui jalur ini, yang menguntungkan sel darah merah untuk penghematan, karena memungkinkan glikolisis berjalan jika kebutuhkan ATP minimal. Fungsi 2,3-bisfosfogliserat akan berikatan dengan hemoglobin, menyebabkan turunnya afinitas hemoglobin terhadap oksigen dan menghasilkan 'curve disosiasi oksihemoglobin bergeser ke kanan. Sehingga adanya 2,3-bisfosfogliserat dalam sel akan membantu oksihemoglobin melepaskan oksigen. 1,3-bisfosfogliserat + ADP 4 2,3-bisfosfogliserat 3-fosfogliserat