Semnaskan_UGM / Penyakit Ikan dan Kesehatan - BPPBAP
advertisement

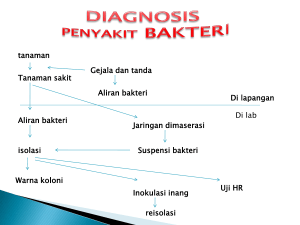
Seminar Nasional Tahunan XI Hasil Penelitian Perikanan dan Kelautan, 30 Agustus 2014 KEMAMPUAN LENDIR IKAN NILA (Tilapia mosambica) MENGHAMBAT PERTUMBUHAN VIBRIO PATOGEN Nurhidayah* dan I.A.K. Kadriah Balai Penelitian dan Pengembangan Budidaya Air Payau (BPPBAP), Maros *e-mail: [email protected] Abstrak Akuakultur memiliki peran penting dalam pengembangan dan pemenuhan permintaan protein hewani. Industri akuakultur secara bertahap berkembang di dunia. Dalam usaha menjaga kesehatan hewan budidaya maka perlu dijaga hubungan antara hewan budidaya, lingkungan dan patogen. Aktivitas antibakteri dalam lendir ikan telah dibuktikan dalam beberapa spesies ikan dan aktivitas dapat spesifik terhadap bakteri tertentu. Penelitian bertujuan untuk mengetahui kemampuan lendir ikan nila dalam menghambat pertumbuhan bakteri Vibrio patogen. Perlakuan yang digunakan adalah Kontrol V. harveyi 107 (A), Kontrol V.harveyi 106 (B), Kontrol V. harveyi 105 (C), V. harveyi 107 + lendir (D), V. harveyi 106 + lendir (E), V. harveyi 105 + lendir (F), Kontrol V. parahaemolyticus 107 (G), Kontrol V. parahaemolyticus 106 (H), Kontrol V. parahaemolyticus 105 (I), V. parahaemolyticus 107 + lendir (J), V. parahaemolyticus 106 + lendir (K), dan V. parahaemolyticus 105 + lendir (L). Pengamatan dilakukan setiap 24 jam hingga 120 jam. Hasil penelitian menunjukkan bahwa pada pengamatan 48 jam lendir ikan nila mulai memperlihatkan kemampuan menghambat pertumbuhan bakteri patogen hingga 120 jam pada perlakuan yang menggunakan bakteri Vibrio harveyi dan Vibrio parahaemolyticus yang dikultur secara bersama baik pada kepadatan 105 CFU/mL, 106 maupun kepadatan 107 CFU/mL. Pada pengamatan 24 jam belum memperlihatkan kemampuan yang optimal dalam menghambat pertumbuhan bakteri patogen. Berdasakan hasil yang diperoleh bahwa lendir ikan nila menunjukkan aktivitas antibakteri yang kuat terhadap bakteri patogen pada lama perlakuan 96 jam. Kata kunci: pertumbuhan, lendir, ikan nila, V. harveyi, V. parahaemolyticus Pengantar Ikan nila (Oreochromis niloticus) merupakan ikan air tawar yang termasuk ke dalam famili Cichlidae dan merupakan ikan asal Afrika (Boyd, 2004). Di Indonesia benih ikan nila secara resmi didatangkan dari Taiwan oleh Balai Penelitian Perikanan Air Tawar tahun 1969. Jenis ini merupakan ikan konsumsi air tawar yang banyak dibudidayakan setelah ikan mas (Cyprinus carpio) dan telah dibudidayakan di lebih dari 85 negara (Dinas Perikanan dan Kelautan Daerah, 2001). Ikan nila cenderung sangat mudah dikembangbiakkan serta sangat mudah dipasarkan karena merupakan salah satu jenis ikan yang paling sering dikonsumsi sehari-hari. Dengan teknik dan cara budidaya ikan nila yang sangat mudah, serta pemasarannya yang cukup luas, menjadikan budidaya ikan nila ini sebagai peluang usaha yang bagus untuk dilakukan, baik skala rumah tangga maupun skala besar. Dalam lingkungan perairan, ikan senantiasa kontak dengan jasad patogen seperti bakteri, jamur, virus maupun protozoa yang mempuyai kemampuan menginfeksi ikan. Masuknya jasad patogen ini ke dalam tubuh ikan tergantung dari kondisi lingkungan, ikan dan organisme patogen. Di lingkungan alam, ikan nila dapat diserang berbagai macam penyakit karena senantiasa kontak dengan jasad patogen seperti bakteri, jamur, virus maupun protozoa yang mempuyai kemampuan menginfeksi ikan. Penyakit tersebut dapat menyerang ikan dalam jumlah besar dan menyebabkan kematian sehingga kerugian yang ditimbulkan sangat besar (Kordi & Ghufran, 2004). Sumber penyakit yang dapat menyebabkan infeksi pada ikan adalah jasad patogen yang dapat dikelompokkan menjadi dua golongan yaitu patogen asli (true pathogen) dan patogen potensial (opportunistic pathogen) (Kordi & Ghufran, 2004). Patogen asli adalah organisme patogen yang selalu menimbulkan penyakit khas apabila ada kontak dengan ikan sedangkan patogen potensial adalah Semnaskan_UGM / Penyakit Ikan dan Kesehatan Lingkungan (PK-07) - 31 PK-07 Seminar Nasional Tahunan XI Hasil Penelitian Perikanan dan Kelautan, 30 Agustus 2014 organisme patogen yang dalam keadaan normal hidup damai dengan ikan, akan tetapi jika kondisi lingkungan menunjang akan menjadi patogen pada ikan (Bennett, 2009). Secara umum faktor-faktor yang terkait dengan timbulnya penyakit merupakan interaksi dari tiga faktor yaitu inang, patogen dan lingkungan atau stressor eksternal yaitu perubahan di lingkungan yang tidak menguntungkan,tingkat higienik yang buruk dan stress (Austin & Austin, 2007). Perkembangan suatu penyakit dalam akuakultur meliputi suatu interaksi yang kompleks antara tingkat virulensi patogen, derajat imunitas inang, kondisi fisiologis dan genetik hewan, stress dan padat tebaran (Irianto, 2004). Mekanisme pertahanan diri organisme inang terhadap organisme patogen dikenal dengan sistem pertahanan tubuh (Kaufmann & Kabelitz, 2010). Pada ikan sistem pertahanan itu berupa lendir, sisik, dan kulit (Bruno & Wood, 1999). Menurut Irianto (2004), sistem imun bawaan antara lain terdiri dari penghalang fisik terhadap infeksi, pertahanan humoral dan sel-sel fagositik. Secara fisiologis, hewan mempunyai pertahanan tubuh non spesifik terhadap suatu infeksi dengan memberikan respon secara langsung terhadap agen asing yang masuk. Pertahanan non spesifik tersebut berupa mukus yang memiliki kemampuan menghambat kolonisasi mikroorganisme pada kulit, insang dan mukosa. Mukus ikan mengandung immunoglobulin alami, bukan sebagai respon dari pemaparan terhadap antigen. Immunoglobulin (antibodi) tersebut dapat menghancurkan patogen yang menginfeksi ikan. Kendala yang dihadapi oleh pembudidaya ikan dan udang adalah adanya serangan penyakit vibriosis yang dapat menyebabkan kematian. Bakteri Vibrio menyerang larva udang yaitu pada saat udang dalam keadaan stress dan lemah, oleh karena itu sering dikatakan termasuk bakteri oportunistik patogen. Vibrio harveyi sampai saat ini masih menjadi spesies utama dari bakteri berpendar yang menjadi agen penyebab penyakit pada budidaya udang yang berakibat kerugian bagi hampir seluruh petani pembudidaya khususnya di wilayah Asia Tenggara (Lavilla-Pitogo et al., 1990; Karunasagar et al., 1994; Liu et al., 1999), termasuk bakteri gram negatif, berpendar dan diketahui menjadi salah satu dari bakteri mikroflora di usus hewan-hewan laut. (O’Brien et al., 1979; Baumann et al., 1980). Vibrio harveyi merupakan bakteri yang membutuhkan sodium klorida untuk hidupnya, berbentuk curverod dan termasuk dalam kelompok bakteri gram negative yang banyak ditemukan pada lingkungan perairan (Farmer et al., 2005) serta dapat memendarkan cahaya sendiri pada kondisi tertentu. Spesies bakteri ini terdistribusi secara luas pada lingkungan akuatik dan diketahui menjadi penyebab utama penyakit kunang-kunang pada organisme laut maupun payau. Selain sebagai penyebab utama, sering kali juga bertindak sebagai agen oportunistik pada infeksi sekunder (Saulnier et al., 2000). Bahan dan Metode Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Mei 2014 di Laboratorium Kesehatan Ikan dan Lingkungan Balai Penelitian dan Pengembangan Budidaya Air Payau menggunakan erlenmeyer volume 250 ml pada masing-masing perlakuan. Perlakuan dan Rancangan Perlakuan yang digunakan pada penelitian ini masing-masing: A = Kontrol V.harveyi 107, B = Kontrol V.harveyi 106, C = Kontrol V.harveyi 105, D = V. harveyi 107 + lendir, E = V. harveyi 106 + lendir, F= V. harveyi 105 + lendir, G = ,Kontrol V. parahaemolyticus 107, H = Kontrol V. parahaemolyticus 106, I = Kontrol V. parahaemolyticus 105 , J = V. parahaemolyticus 107 + lendir, K = V. parahaemolyticus 106 + lendir, dan L = V. parahaemolyticus 105 + lendir. Pengamatan dilakukan setiap 24 jam hingga 120 jam. Prosedur Penelitian Stok isolat bakteri Vibrio pathogen yang digunakan dikeluarkan dari -80°C dan distabilkan pada suhu ruangan. Masing-masing isolat bakteri diambil sebanyak 100 µl dan ditanam ke dalam media Nutrien Broth (NB) volume 50 ml. Diinkubasi bergoyang (shaker) selama 24 jam. Media kultur bakteri patogen diambil sebanyak 1 ml dan dimasukkan ke dalam NB volume 100 ml sesuai perlakuan (A,B,C,H,I dan 32 - Semnaskan_UGM / Nurhidayah dan I.A.K. Kadriah Seminar Nasional Tahunan XI Hasil Penelitian Perikanan dan Kelautan, 30 Agustus 2014 J). Pada perlakuan D,E,F,K,L dan M ditambahkan lendir ikan nila sebanyak 0,5 ml, diinkubasi sambil dishaker selama 4 jam. Sampling dilakukan setiap 24 jam hingga 120 jam pada masing perlakuan dengan cara: diambil 1 ml media kultur bakteri pada masing-masing perlakuan, dimasukkan ke dalam larutan fisiologis volume 9 ml. Dilakukan pengenceran secara bertingkat mulai dari 0-106 atau sesuai kondisi kekeruhan sampel. Sampel yang telah diencerkan ditanam pada media TCBSA sebanyak 0,1 ml pada masing-masing perlakuan dan diinkubasi selama 24 jam. Populasi bakteri yang tumbuh dihitung berdasarkan jumlah koloni bakteri yang tumbuh pada masing-masing cawan petri. Sampling dan Pengamatan Pengamatan dan sampling populasi bakteri dilakukan setiap 24 jam hingga 120 jam pada masingmasing perlakuan. Hasil dan Pembahasan Hasil Waktu Pengamatan (jam) Gambar 1. Kurva pertumbuhan bakteri patogen pada media uji. Kontrol V. harveyi 107 (A), Kontrol V. harveyi 106 (B), Kontrol V. harveyi 105 (C), V. harveyi 107 + lendir (D), V. harveyi 106 + lendir (E), V. harveyi 105 + lendir (F), Kontrol V. parahaemolyticus 107 (G), Kontrol V. parahaemolyticus 106 (H), Kontrol V. parahaemolyticus 105 (I), V. parahaemolyticus 107 + lendir (J), V. parahaemolyticus 106 + lendir (K), dan V. parahaemolyticus 105 + lendir (L) Dari hasil yang diperoleh diketahui bahwa dengan penambahan 0,5 % lendir ikan nila pada kultur bakteri dapat menurunkan populasi bakteri patogen. Pada perlakuan 96 dan 120 jam terlihat perbedaan populasi bakteri yang cukup signifikan antara perlakuan kontrol (tanpa penambahan lendir) dengan perlakuan penambahan lendir ikan nila. Hasil yang sama diperoleh baik untuk perlakuan dengan V. harveyi maupun dengan V. parahaemolyticus. Pada perlakuan 24 – 72 jam belum terlihat adanya perbedaan populasi bakteri yang cukup signifikan antara perlakuan kontrol (tanpa penambahan lendir) dengan perlakuan penambahan lendir ikan nila. Tiga mekanisme utama antagonisme mikroba flora normal terhadap patogen yaitu kompetesi dalam menempati situs perlekatan atau kolonisasi, antagonisme spesifik melalui produksi senyawa penghambat berupa protein spesifik (bakteriosin) dan antagonisme non-spesifik dengan memproduksi berbagai metabolit atau produk akhir yang menghambat mikroba patogen antara lain berupa asam-asam organik dan peroksidase (Irianto,2004). Penelitian yang dilakukan oleh Kasai (2010) menunjukkan adanya protein bioaktif yang ditemukan pada lapisan lendir dari ikan flounder (Platichthys stellatus), yang menunjukkan aktivitas antibakteri terhadap Staphylococcus epidermidis, S. aureus dan methicillin-resistant S. aureus. Penelitian Eissa et al. (2011) mengungkapkan bahwa sampel lendir dari ikan nila (O. niloticus) dan ikan lele (C. gariepinus) menghambat pertumbuhan bakteri baik bakteri Gram positif atau bakteri Gram Semnaskan_UGM / Penyakit Ikan dan Kesehatan Lingkungan (PK-07) - 33 Seminar Nasional Tahunan XI Hasil Penelitian Perikanan dan Kelautan, 30 Agustus 2014 negatif. Lendir Lele (C.gariepinus) sangat efektif selama perlakuan 6 jam pertama dan terus teramati selama 12 sampai 24 jam. Aktivitas ini hampir sama terhadap tiga strain bakteri, sedangkan lendir O. niloticus tidak efektif pada perlkuan 6 jam pertama. Setelah 6 jam pertama aktivitas anti bakteri di lendir nila bekerja dalam menghambat pertumbuhan bakteri untuk semua strain bakteri patogen yang diujikan. Sistem kekebalan tubuh bawaan, terutama permukaan tubuh eksternal, memainkan peran dalam melindungi ikan budidaya yang dibudidayakan secara intensif dan yang dibudidayakan pada suhu rendah. Sistem kekebalan ini akan melindungi dari infeksi karena tidak memadainya respon imun adaptif. Penelitian Palaksha et al. (2008) menunjukkan kemampuan komponen immunitas yang terdapat pada lendir ikan budidaya ekonomis penting, Olive Flounder (Paralichthys olivaceus) dengan mengevaluasi komponen immun dari lendir kulitnya. Pada lendir kulit ikan Olive Flounder terdeteksi enzim lisozim, tripsin-like protease, alkaline phosphatase dan esterase. Lendir kulit menunjukkan aktivitas antibakteri yang kuat terhadap bakteri patogen. Komponen kekebalan utama dari lendir kulit yang diidentifikasi, terlibat dalam kekebalan non-spesifik dari ikan Olive Flounder. Kesimpulan Lendir ikan nila menunjukkan aktivitas antibakteri yang kuat terhadap bakteri patogen pada lama perlakuan 96 hingga 120 jam. Daftar Pustaka Austin, B. & D. Austin. 2007. Bacterial fish pathogens disease of farmed and wild fish, fourth edition. Praxis Publishing. United Kingdom. Hal : 83,161. Bruno, D.W. & B.P. Wood. 1999. Saprolegnia and other oomycetes. In: Woo, P.T.K. & D.W. Brun, editors: Fish diseases and disorder vol.3, viral, bacterial and fungal infections. CABI Publishing. Wallingford. Owon. United Kingdom: 560-569. Boyd, C.E. 2004. Farm level issues in aquaculture certification: tilapia. WWF-US Auburn. Alabama. Dinas Kelautan dan Perikanan Daerah. 2001. Petunjuk teknis pembenihan dan pembesaran ikan nila (Oreochromis niloticus). Propinsi Sulawesi Tengah. Farmer, J. J. & F.W. Hickman-Brenner. 1992. The genera Vibrio and Photobacterium. P:2952–3011. In Balows, A. (Ed). The prokaryotes – a handbook on the biology of bacteria: ecophysiology, isolation, identification, applications. Springer. New York. Lavilla-Pitogo, C.R., M.C.L. Baticados, E.R. Cruz-Lacierda & L.D. Pena. (1990). Occurrence of luminous bacterial disease of Penaeus monodon larvae in the philippines. Aquaculture 91:1–13. Liu, C. & K.K. Lee. 1999. Cysteine protease is a major exotoxin of pathogenic luminous Vibro harveyi in the tiger prawn, Penaeus monodon. Lett. Appl. Microbiol. 28:428–430. Irianto, A. 2005. Patologi ikan teleostei. Gadjah Mada University Press. Yogyakarta. O’Brien, M.G., A.J. Taylor & N.H. Poulter. 1991. Improved enzymatic assay for cyanogenics in fresh and processed cassava. J.Sci. Food. Agric. 56 pp 277-89. Palaksha, K.J., G.W. Shin, Y.R. Kim & T.S. Jung. Evaluation of non-specific immune components from the skin mucus of olive flounder (Paralichthys olivaceus). Fish & Shellfish Immunology Volume 24, Issue 4, April 2008, Pages 479-488. Kordi, K. & M. Ghufran. 2004. Penanggulangan hama dan penyakit ikan, Cetakan Pertama. PT Rineka Cipta. Jakarta. 34 - Semnaskan_UGM / Nurhidayah dan I.A.K. Kadriah Seminar Nasional Tahunan XI Hasil Penelitian Perikanan dan Kelautan, 30 Agustus 2014 Kasai, K., T. Ishikawa, T. Komata, K. Fukuchi, M. Chiba, H. Nozaka, T. Nakamura, T. Sato & T. Miura. 2010. Novel l-amino acid oxidase with antibacterial activity against methicillin-resistant Staphylococcus aureus isolated from epidermal mucus of the flounder Platichthys stellatus. FEBS Journal. 277: 2, 453-465. 41 ref. Karunasagar, I, Pai, R, Malathi, GR. Karunasagar, I. 1994. Mass mortality of Penaeus monodon larvae due to antibiotic-resistant Vibrio harveyi infection. Aquaculture 128: 203–209. Saulnier, D., P. Haffner, C. Goarant, P. Levy & D. Ansquer. 2000. Experimental Infection Models for Shrimp Vibriosis Studies: A Review. Aquaculture 191:133–144. Tanya Jawab Pertanyaan : Bahan aktif apa yang terkandung pada lendir? Jawaban : Belum mengkaji bahan aktif yang terkandung pada lendir. Semnaskan_UGM / Penyakit Ikan dan Kesehatan Lingkungan (PK-07) - 35