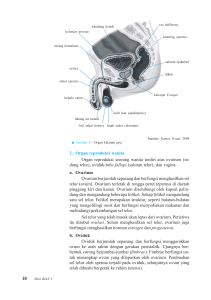
Polimorfisme Genetik Gen Follicie Stimulatying harmone Receptor
advertisement

Polimorfisme Genetik Gen Follicle Stimulating Hormone Receptor
dan Respon Ovarium Terhadap Stimulasi
Follicle Stimalding Hormone
Oleh
: Dr. Daniel Joko Wahyono, M.Biomed
I. Pendahuluan
Follicle stimuloting hormone (FS[D merupakan hormon yang sangat penting dalam
sistem reproduksi mamalia,
pubertas.
Di
yaitu
untuk perkembangan gonad dan pematangan masa
samping itu, FSH juga diperlukan untuk menghasilkan gamet selama masa
subur (Simoni et a1.,1999). FSH menjalankan fungsinya menstimulasi oogenesis melalui
interaksi dengan FSHR pada sel target, yaitu sel-sel granulosa folikel. FSHR merupakan
anggota kelompok reseptor G-protein-coupled (Simoni and Nieschlag, 1995; lvlayorga et
aL.,2000\.
Pada teknologi reproduksi berbantuan seperti intracytoplasmic sperm iniection
(ICSD dan in vitrofertilization
{Vf)
stimulasi ovarium dengan FSH merupakan salah satu
prosedur standar yang harus dijalani oleh wanita yang mengikuti program reproduksi
berbantuan untuk mendapatkan oosit yang meinadai untuk fertilisasi (Lenton et a1.,2000;
Agrawal et a1.,2000; Mayorga et a1.,2000; Subiyanto et aI., 2000). Pengalaman di
beberapa
klinik yang melakukan reproduksi
berbantuan menunjukkan adanya variasi
respons wanita usia reprodukstif terhadap FSH eksogen (Mayorga et a1.,2000; Subiyanto el
aL.,2000).
Saat
ini diketatrui ada tiga SNPs pada gen reseptor FSH, yaitu satu pada promoter
dan dua lainnya pada ekson 10 yang berada pada domain ekstraselular. Situs polimorfik
yang pertama ditemukan pada domain ekstraseluler di posisi aa (kodon) 307, yaitu Alanine
(Ala) atau Threonine (Thr). Situs polimorfik yang lain ditemukan pada domain intraseluler
kodon 680, yaitu Asparagin (Asn) atau Serine (Ser) (Simoni et ol., 1997). Analisis Single
Strand Conforaation Polymorphism (SSCP) dapat digunakan untuk melakukan
variasi alel
l0 yang berkaitan
bio.unsoed.ac.id
Thr307-Asn680 dan Ala307-Ser680. Frekuensi dan distribusi dua variasi
identifikasi dua polimofisme pada ekson
yaitu
dengan
FSHR,
alel
selanjutnya
di analisis dengan
SSCP pada kodon 3A7 dan Restrietion Fragment Length
Polymorphrsn (RFLP) pada kodon 680 (Simoni et a1.,1999).
2. Follicle stimulating hormone GSH)
FSH adalah salah satu hormon gonadotropin yang dihasilkan oleh hipofisa anterior.
Sintesis dan sekresi FSH diatur oleh gonadotropin releasing hormone (GnRH) yang
disekresikan oleh neuron khusus
di
dalam hipotalamus. GnRH menginduksi sekresi
gonadotropin dengan cara perlekatan dekapeptida pada reseptor spesifik pada gonadotropin
hipofisis, kemudian diikuti dengan respons plasma-membran yang menyebabkan
dilepaskannya FSH ke sirkulasi (Yen and Jaffe, 1936). Fungsi utama FSH adalah
menstimulasi maturasi testis
dan ovarium
sertra mengafur gametogenesis dan
steroidogenesis dalam gonad. Mekanisme kerja FSH pada sel-sel gonad berupa umpan
balik negatif. Pada ovarium, FSH menginduksi perkembangan folikel sampai terbentuk
folikel tersier (follicle deGraafl. Folikel tersier kemudian membentuk hormon estrogen
yang kemudian menekan hipofisis anterior sehingga sekresi FSH menjadi terhenti. Pada
testis, target FSH adalah sel sertoli yang terdapat dalam tubuklus senminiferus dan berperan
dalam spermatogenesis (Simoni et
al.,
1997).
FSH disusun oleh dua subunit polipeptida yang terikat satu sama lain dalam il€tan
nonkovalen dengan afinitas tinggi. Kedua subunit yang menyusunnya dikenal sebagai
subunit
a dan p. Subunit o dari hormon FSH mempunyai struktur yang sama dengan
hormon glikoprotein lain, yaitu luteinizing hormone (LH), human chorionic gandotrophin
(hCG) dan thyroid-stimulating hormone GSFD (Yen and Jaffe, 1986; Loumaye et al.,
1998). Sub.unit o mengandung 92 residu asam amino dengan lima ikatan disulfida yang
berkontribusi pada pembentukan struktur tersiernya. Sebaliknya" subunit
p mempunyai
sekuens asam amino yang berbeda-beda dan membawa informasi yang spesifik yang akan
dikespresikan bila telah bergabung dengan subunit a. Subunit p mengandung l l
asam amino dengan enam ikatan disulfida (Loumaye et
adalah 33
kilo Dalton (kDa),
l residu
al., l99S). Berat molekul FSH
berat molekul subunit a adalah 14 kDa.
bio.unsoed.ac.id
glikosilasi
sedangkan
mengandung empat asam amino asparagin yang terikat pada situs
2
FSH
FSH, dan dari
keempat asparagin tersebut dua terletak pada subunit c (Asn 52 dan 78), dan dua lainnya
terletak pada subunit p (Asn
7
dan Asn 24). Kehadiran dan komposisi rantai samping
karbohidrat dan asam sialat yang berbeda-beda pada FSH menentukan lama aktivitas
biologi FSH secara in vivo dan pada akhirnya menentukan kualitas FSH dalam tubuh
(Loumaye
et a1.,1998; Simoni et a1.,1997).
Konsentrasi FSH dalam darah yang tidak mencukupi akibat kurangnya sintesis atau
sekresi FSH menyebabkan kasus infertilitas pada pria dan wanita. Pada wanit4 keadaan ini
ditandai dengan tidak normal atau tidak terjadinya owlasi, sedangkan pada pria keadaan
yang mengakibatkan infertilitas
ini
disebabkan tidak cukup tersedianya spenna yang
bergerak normal. Pemberian preparat FSH, baik tunggal atau dikombinasikan dengan LH,
sangat membantu penanganan kasus-kasus infertilitas pada pria dan wanita (Loumaye et
al.,1998).
Preparat FSH yang pertama kali dijumpai di pasaran dihasilkan dari urin wanita
pasca menopause yang dikenal dengan human menopausal gonadotropiz (HMG). HMG
adalatr sumber FSH eksogen pertama yang dipakai secara klinis untuk stimulasi ovarium
(Simoni et a1.,1997). Tingkat kemanjuran HMG dalam menginduksi ovarium masih rendah
dibandingkan dengan preparat FSH eksogen lainnya, misalnya urofollitropin (uFSH) dan
highly purified urofollitropin (UFSH-FIP) maupun urofollitropin
u dan urofollitropin p
(Lenton et aI., 2000). Urofollitropin dan uFSH-HP merupakan preparat FSH yang
dihasilkan dari proses pemurnian HMG. uFSH dapat diberikan secara subkutan karena
tingkat kemurniannyayang lebih tinggi daripada HMG (Bergh et a1.,1997). Preparat FSH
terakhir yang dijumpai di pasaran saat ini dihasilkan dari teknologi DNA rekombinan yag
dikenal dengan urofollitropin
o dan urofollitropin B
(Loumaye et
rekombinan ini dihasilkan dengan menyisipkan fragmen DNA subunit
al., 1998). Produk
a
dan F gen FSH
manusia ke dalam vektor ekspresi pCLH3AXSV2DHFR (untuk subunit
a) dan vektor
ekspresi pCLH3AXSV2ODC (untuk subunit B), kemudian ditransfeksi ke sel ovarium
hamster (Loumaye et
al., 1998). Follitropin o
dipasarkan dengan nama Gonal-F dan
bio.unsoed.ac.id
follitropin p dipasarkan dengan naman Puregon atau Follistatin @aya and Gunby,1999).
Kedua produk rekombinan FSH manusia yang dihasilkan
ini
benar-benar murni dan
terbebas dari aktivitas LH dan protein urin lainnya (Lenton et a1.,2000)..
3. Aspek Molekul FSHR dan Gen FSHR
FSH bekerja dalam sel melalui reseptor khusus, yaitu FSHR yang terletak secara
ekslusif pada gonad. Ekspresis FSHR pada manusia dan beberapa mamalia lainnya yang
sudah teridentifikasi hanya terdapat pada testis dan ovarium. Pada testis, ekspresi FSHR
secara ekslusif hanya ditemukan pada sel-sel Sertoli, sedangkan pada
ovarium FSHR
hanya diekspresikan pada sel-sel granulosa (Yen and Jaffe, 1986; Simoni et al., 1997;
Heckert and Griswold,
l99l).
FSHR termasuk ke dalam famili reseptor yang membentuk ikatan dengan GTPbinding protein Qrotein G), kompleks protein transmembran yang dicirikan dengan adanya
tujuh heliks hidrofobik yang tersisipkan dalam plasmalemma, domain intraseluler dan
ekstraseluler dengan dimensi yang bervariasi sesuai dengan tipe ligandnya (Gudermawr et
a1.,1995). Bagran intraseluler dari FSHR membentuk ikatan dengan protein G yang setelah
adanya aktivasi reseptor oleh interaksi hormonal dengan domain ekstraseluler menginisiasi
rangkaian peristiwa yang terutama menyebabkan efek biologi spesifik dari gonadotropin.
Diperkirakan FSHR manusia yang terdiri atas domain ekstraseluler, domain
transmembran, dan domain intraseluler disusun oleh 695 asam amino (aa) termasuk 17 aa
pertama yang mengkode suatu signal peptida hidrofobik. Domain eksfaseluler reseptor
terdiri atas 349
aao
domain transmembran terdiri atas264 aa, dan domain intraseluler terdiri
atas 82 aa. Homologi
di
antara spesies mamalia yang berbeda umumnya tinggi dan
mencapai 9O %padadomian transmemban (Simoni et al.,1997).
Domain ekstraseluler disusun oleh beberapa unit pengulangan yang tidak sempurna
yang masing-masingnya terdiri atas 24 residu. Leucine-rich repeot (LRR) ditemukan pada
protein yang terlibat dalam adhesi antara sel tertentu dan interaksi protein-protein pada
spesies
mulai dan yeast sampai manusia (Kobe and Deisenhofer, 1993). Pola LRR sangat
9. Domain
- 8 dan kurang
bio.unsoed.ac.id
conserved pada ekson 2
conserved pada ekson
mengandung beberapa residu sistein yang terutama terletak pada ekson
eksfiaseluler
I dan 10. Delapan
residu sistein yang terutama terletak pada ekson
conserted yang juga terdapat pada reseptor
I
dan 10. Delapan residu sistein sangat
LH (LI{R) dan reseptor TSH (TSI{R),
kemungkinan mempunyai peran penting dalam integritas konformasi domain ekstraseluler
dari semua reseptor hormon glikoprotein (Kobe and Deisenhofer, 1993).
Hasil
perbandingan domain transmembran FSHR, LHR, dan TSHR menunjukkan bahwa domain
transmembran pada segmen
2,3,
dan
4
sangat homolog, sedangkan pada empat segmen
lainnya mempunyai tingkat homologi yang rendah. Residu prolin yang kemungkinan
penting untuk ketepatan insersi protein ke dalam membran diketahui homolog untuk
segmen
ke4, ke-6, dan ke-7 dari
semua reseptor hormon glikoprotein (Simoni et a1.,1997).
Penelitian menggunakan teknik biologi molekuler pada jaringan ovarium
menunjukkan bahwa sel-sel granulosa merupakan satu-satunya sel yang mengekspresikan
FSHR (Camp et a1.,1991). Ekspresi reseptor pada organ wanita seperti halnya pada organ
pria juga bersifat gonad dan cell-specific.Pada pria" ekspresi FSH semra spesifik terikat
pada reseptor yang terletak pada membran sel Sertoli (Kangasniemi et
al., 1990). Hasil
hibridisasi in situ jugamembukrikan bahwa sel-sel Sertoli merupakan satu-satunya sel yang
mengekspresikan FSHRpada testis @oeckers et al.o 1994).
Hasil pemetaan kromosom gen FSHR dengan teknik hibridisasi in situflourescent
menggunakan pelacak cDNA atau
DNA genom dan analisis lingkage menunjukkan bahwa
gen FSHR terletak pada kromosom 2p2l pada manusia (Minegishi e/
al.,l99l;
Kelton et
al.,1992). Gen FSIIR adalah gen salinan tunggal (single copy gene). Hasil analisis restriksi
klon genom menunjukkan panjang gen FSHRpada manusia adalah 54 kpb, sedangkan tikus
adalah 86 kpb. Gen FSHR terdiri atas
dikode oletr ekson
I-
9, sedangkan
transmembran dan domain
1234 pb (Heckert et
l0
ekson dan 9 intron. Domain ekstraseluler FSI{R
C domain ekstraseluler, domain
intraseluler dikode oleh ekson t0 dengan panjang lebih dari
bagian ujung
al., 1992; Gromoll et aI., 1996). Gen manusia mengkode 695 asam
amino, termasuk signal peptida sebesar 17 asam amino. Ukuran intron sangat bervariasi,
intron 7 berukuran 108 pb sedangkan intron
I
berukuran jauh lebih bear yaitu 15 kpb.
bio.unsoed.ac.id
Sekuens konsensus splicing pada batas ekson-intron conserved pada semua ekson. Asam
amino yang terletak pada hampir setiap penghubung ekson/intron adalah Leusin dan
Isoleusin (Simoni et a1.,1997).
4. Polimorlisme Gen FSHR
Situs peta gen pada genom manusia dikenal sebagai polimorfik bila ada probabilitas
yang logis bahwa genom dari dua individu akan berbeda satu dengan lainny4 dimana
sebagian besar variasi tersebut dalam bentuk polimorfisme basa nukleotida tunggal atau
single nucleotide polymorphisns (SNPs) @ruce et al., 2002; Botwell and Sambrook,
2003). Alel adalah perubahan sekuens DNA tertentu yang berbeda dengan sekuens wild
We-nyapada satu lokus gen dalam suatu kromosom. Apabila alel tersebut ditemukan pada
I
lebih dari
persen kromosom dari suatu populasi disebut sebagai polimorfisme genetik
(Nussbaum et al., 2001).
Dewasa ini telah diketahui dengan pasti dua situs polimorfisme pada gen struklur
FSI{R manusia. Polimorfisme ini diketahui dari hasil skrining gen FSI{R pada pasien
disgenesis ovarium, pasien l4tpogonadotropic hypogondism, dan pria infertil. Polimorfisme
pertama ditemukan pada domain ekstraseluler pada kodon 307 (posisi sekuens nukleotida
919) yang dapat ditempati oleh Alanin (GCT) atau Treonin (ACT). Polimorfisme kedua
terletak pada domain transmembran pada kodon 680 (posisi sekuens nukleotida 2039) yang
dapat ditempati oleh Asparagin (AAT) atau Serin (AGT). Pada posisi sekuens nukleotida
919 dan 2039 te4adi perubahan basa nukleotida dari Guanin menjadi Adenin. Kedua situs
polimorfik tersebut terletak pada ekson 10 dan membentuk dua variasi alel pada FSH&
yaitu Thr307/Asn680 dan Ala307/Ser680 (Simoni et al., 1999). SNPs pada ekson l0
<
menghasilkan empat variasi
alel yang dislret dan dicirikan dengan kombinasi
Thr307/Ser680, Ala307/Ser680, Ala307/Asn680, danThr307/Ser680. Kedua variasi alel
yang pertama sangat sering terjadi pada populasi Kaukasi4 masing-masing Thr307/Ser680
dengan frekuensi 60
o/o dan
Ala307/Ser680 dengan frekuensi 40
o/o.
Variasi alel yang lebih
jarang terjadi adalah pada Ala307/Asn680 dan Thr307/Ser680, frekuensinya sangat kecil
yaitu < 5
o/o pada
bio.unsoed.ac.id
populasi Cina. Pada umumnya polimorfisme pada gen FSHR ekson l0
berupa polimorfisme basa nukleotida tunggal atau single nucleotide polymorphisms
6
(SNPs), seperti Thr307Ala" Val34lAla dan Ser680Asn. Ketiga situs polimorfik tersebut
merupakan tipe missense yang tidak menuqiukkan perubahan fenotipe atau tidak
mempunyai efek fenotipe (Themmen et a1.,2000).
Identifikasi kedua polimofisme pada ekson
l0
gen
FSHR ini dapat dilakukan
dengan analisis Polymerase Chain Reaction Single Stranded Conformation Polynorphisms
(PCR-SSCP), sedangkan khusus pada kodon 680 dapat juga dilakukan analisis dengan
PCR-SSCP dan Polymerase Chain Reaction Restriction Fragment lcngth Polynrorphisms
(PCR-RFLP). Oleh karena pada kodon 680 ekson 10 gen FSI{R mempunyai situs restriksi
yang dapat dikenali oleh enzim restriksi Bsr SI, maka posisi ini dapat dianalisis dengan
PCR-RFLP (Simoni et a1.,1999). Penelitian Mayorga et al. Q000) menunjukkan bahwa
wanita dengan genotip Asn/Asn membutuhkan jumlatr ampul FSH paling
sedikit (31,8 +
2,4 ampvl,l ampul = 75 II-D untuk stimulasi ovarium dan wanita dengan genotip Ser/Ser
membutuhkan jumlah ampul FSH terbanyak (46,8 + 5,0 ampul). Hal ini menunjukkan suatu
hubungan yang jelas pada regulasi feedback FSH yang bergantung pada tipe FSHR
(Mayorga et a1.,2000). Residu Asn berkontribusi dalam glikosilasi FSHR dan penting
dalam proses pasca- translasi reseptor dan ekspresi pada permukaan sel. Sebaliknya residu
Ser berkonfibusi dalam fosforilasi yang berpotensi menyebabkan turnover reseptor
(Mayorga et a1.,2000; Davis et a1.,1995).
5. Kesimpulan
FSH menjalankan fungsinya menstimulasi oogenesis melalui interaksi dengan
FSHR pada sel target, yaitu sel-sel granulosa folikel ovarium dan sel-sel sertoli testis.
Variasi uf"t
psnn yang menentukan
sensitivitas ovarium terhadap stimulasi FSH
merupakan wacana baru dalam endokrinologi reproduksi.
Daftar Pustaka
bio.unsoed.ac.id
Agrawal, R., J. Holmes, H.S. Jacobs. 2000. Follicle-stimulating hormone or human menopausal
gonadotropin for ovarian stimulation in in vitro fertilization cycles : a meta-analysis. Fertil
Steril 73: 33843.
Boeckers, T.M., E. Nieschlag M.R. Kreuta M. Bergmann. 1994. Localization of folliclestimulating hormone immunoreactivity and hormone receptor mRNA in testicular tissue of
infertile men. Cell Tissue
Res
278: 595-600.
Botwell, D. and J. Sambrook.2003. DNA Microarrays : A Molecular Cloning Manual. Cold Spring
Harbor Laboratory Press, New York, USA : 400.
Brucg A., A.Johnson, J. Lewis, M. Rafi K. Roberts, P. Walter. 20fi2. Moleculm Biologt of The
Cell.4e ed. Galand Science, New Yorlg USA : 464.
Camp, T.A., J.O. Rahal, I(8. Mayo. 1991. Cellular localization and hormonal regulation of folliclestimllating hormone and luteinizing hormone receptor messenger RNAs in the rat ovary.
Mol Endocrinol 5: 1405-17.
Davis, D., X. Liq D.L. Segaloff. 1995. Identification of the sites of N-linked glycosylation on the
follicle-stimulating hormone (FSH) recepor and assessment of their role in fsh receptor
function. Mol Endocrinol 9 : 159-170.
Day4 S. and J. Gunby. 1999. Recombinant versus urinay follicle-stimulating hormone for ovarian
stimulation in assited reproduction. Hwn Reprod 14 :2207-12.
Ford K.A. and A.R. I"aBarbera. 1988. Follicle-stimulating hormone (FSIT) unmasks specific high
atrnity FSH-binding stes in cell-free membrane preparations of porcine granulosa cells.
Endocrinologt 123 : 237 4-8I.
Gromoll, J., E. Pekel, E. Nieschlag 1996. The structure and organization of the human folliclestimulating hormone receptor GSIIR) gene. Genomics 35 : 308-11.
Gudemrann, T., B. Nuemberg G. Schuktz. 1995. Receptors and G protein as primary components
of transmembrane signal hansduction. I.G-protein-coupled receptors:structure and function.
J Mol Med73:51-63.
Heckkerl L.L. and M.D. Grsiwold. 1991. Expression of follicle-stimulating hormone recepror
mRNA in rat testes dan Sertoli cells. Mol Endocrinol s:670-7.
Heckert, L.L., I.J. Daley, M.D. Griswold. 1992. Strucuhal organization of the follicle-stimularing
hormone receptor gene. Mol Endocrinol 6 : 70-80.
Huhaniemf I., V. Eskol4 P. Pakarinen, T. Matikainen, R. Sprengel. lgg2.'themurine lgteinizing
hormone and follicle-stimulating hormone receptor gene : transcription initiation sitei
putative promoter sequences and promoter activity. Mot Celt Endocriiol 88 : 55-66.
Kangasniemi, M., A. Kaip4 J. Toppari, A. Perhentupa,I. Huhtaniemi, M. Parvinen. 1990. Ceflular
regulation of follicle-stimulating hormone (FSID binding rat somniferous tubules. J Androl
ll
:336-43.
bio.unsoed.ac.id
Keltorq C.A., S.V.Y
th*g, N.P. Nugen! RL. Schweickhardt, J.L. Rosenthal, S.C. Chappl.lgg2.
The cloning of the human follicle-stimulating hormone receptor and its expression in COS7, CHO and Y- I cells. Mol Cell Endoginol t9 : 14 I -5 I .
inhibitor' a protein
lgg3. Crystal structure of porcine ribonuclease
leucine-rich repeats' Nature 366 : 7 514
and J. Deisenhofer
Kobe,
--- - -' B.
-with
.
Lenton,E.,A.Solta&J.Hewitt,A-Thomsorr,W.Davies,N.AshraiV.Sharma"L.Jenner,W.
assited
of ovuiation in women undergoingptnified
Ledger, E. McVeigtr- 2000. -Inducion
highlv
versus
FSH (follitropin alpha)
reproductive techniques
*inu.y fsff
:pgg{lanil;man
(urofofiitropin HP) ' Hum Reprod 15 : 1021-7'
Loumaye,E.,M.Dreano,A.Galazka,C.Howles,L.Ham.A.Eshkol.lgg8.Recombinatfolliclenttt b-iotechnologl product for treatment of
stimulating hormone: development "f ittt
infertility.-Hum Reprod Update 4 : 862-81
2000' Ovarian
H'M' Behre' C' Gassnerr' E' Nieschlag' M' Simoni'
the FSH receptor
on
depends
t" rliiirr.lrtimulating rro*ro* irsrD ltlTrylion
Mayorga, M.P., J. Gromoll,
response
g.notyp"
I
Ai i"a*'nol
aid Metab 85 (9) : 3365-3369'
Y. Ibuki, M' Igarashi' 1991' Cloning and sequencing
Minegishi, T., K. Nakamura" Y. Takakurq
,pNe. Biociem Biopltys Rei commun 175 :1125-30.
human FSH
of
;;;'p;
Willard. 2001. Thompsom&Thompson
Nussbaurrr, R.L., R.R. Mclnnes, H.F.
wB saunders Co', Philadeplhia' USA : 87'
"*"--?tgi.
Simoni, M. and E. Nieschlag. 1995.
clinical
vse- Reprod
Med
Rev
py
4:
: Genetics in Medicine.
and
in therapy : physiological basis' new preparations
t63'167 '
The Follicle-stimulating hormon receptor :
simoni, M., J. Gromoll, E. Nieschlag. 19 9,7.
biochemystry,molecularbiolory,on'''*'"*andpathophysiology.EndocrRevlS:739773.
simoni,M.,J.Gromoll,w.H0ppner.lggg.Mutationanalysisofthefollicle-stimulatinghormone
characterization of two
irir"ttiir-;;, identification and(2):751-755'
GSID receptor in normal *o
J Ctin Endocrinol and Metab U
discrete
Subiyanto,
FSH;;"tpt*
M. Jaffar, I. Yan,
Mal.am Klinik
PNI
isoforms.
g{.
JAYA :
Y*11".
I 1'
{
1
in vitro'
2000. Stimulasi ovarium program fertilisasi
-
receptor
Mutation of gonadotropin and gonadofropin
Themmer\ A.p.N. and I.T. Huhteniemi. 2000.
*d;.il;ht;iolory oif pituitary-gonadal tunction' Endocrine
: elucidatin!'ihe;tt
t"t"t
Rev2l (5):551-583'
Physiologt' Pathophysiologt
Yerf S.S.C. and R.B. Jaffe. 1986. Reprodrctive endocrinolog't' Philadelphia' London'
companv'
ctinicat *;;;;;;;;r-iJ.oiiJ.. w.B. Saunders
bio.unsoed.ac.id
and