kel-09-kromatografi
advertisement

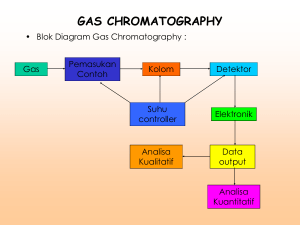
Kromatografi Gas-Cair (Gas-Liquid Chromatography) Kromatografi DEFINISI Kromatografi adalah teknik pemisahan campuran didasarkan atas perbedaan distribusi dari komponenkomponen campuran tersebut diantara dua fase, yaitu fase diam (padat atau cair) dan fase. Kromatografi Pertukaran Ion Padat Gas Cair Plat Kolom Cair Anion Fasa Diam Fasa Gerak Kation Gel Cair GPC Jenis-Jenis Kromatografi Berdasarkan fase gerak yang digunakan, kromatografi dibedakan menjadi dua golongan besar yaitu gas chromatography dan liquid chromatography. Masingmasing golongan dapat dibagi lagi seperti yang telah disebutkan pada definisi di atas. Kromatografi di dalam bentuk tempat Komatografi Kolom : Kromatografi kolom merupakan teknik pemisahan di mana tempat stasioner dalam tabung. Kromatografi Planar Kromatografi Kertas Kromatografi Lapisan Tipis Contoh Chromatography Liquid Chromatography digunakan untuk identifikasi pigmen tumbuhan atau komponen lain Thin-Layer Chromatography Menggunakan lapisan tipis atau gelas kaca untuk memisahkan komponen kimia dan bahan lainnya Gas Chromatography Digunakan untuk menentukan komposisi kimia zat-zat yang tidak diketahui, seperti senyawa berbeda dalam bensin yang ditunjukkan oleh tiaptiap puncak dalam grafik di bawah ini. Paper Chromatography Dapat digunakan untuk memisahkan komponen-komponen tinta, pewarna, senyawa tumbuhan (klorofil), make-up, dan banyak zat lain Kromatografi Gas-Cair Proses Kromatografi Pembawa gas Detektor Kolom Flow Controller Sampel Injeksi GLC sebagai komatografi tak dieal linear Disebut grafik isotermal Koefisien distribusi Suatu tetapan tanpa dimensi, K yang diperoleh dari hukum henry dengan menggantikan tekanan parsial dan fraksi mol suatu zat terlarut dengan dua suku konsentrasi yang sama satuannya. Kesetimbangan dalam perpindahan massa Suatu faktor pelebaran pita dalam kromatografi yang disebakan oleh terhingganya waktu yang diperlukan oleh suatu zat terlarut untuk keseimbangan Dapat dituliskan dari hukum Henry Cl=KCg .... (1) Resolusi Disebut separation Dua zat terlarut yang didasarkan pada waktu-waktu retensi dan lebar pita Aspek-aspek percobaan glc Gas Pembawa (Pengemban) Sistem Pengambilan Sampel Jenis-jenis Detektor : - Konduktivitas Termal - Pengionan Nyala Karakteristik Detektor : - Detektor Integral - Detektor Diferensial - Kepekaan - Stabilitas - Kelinieran - Keserbagunaan - Waktu Respons Kolom : - Kolom Isian - Kolom Kapiler - Pemilihan Fasa Cair Gas pembawa Gas yang telah digunakan dalam GLC : Hidrogen, helium, nitrogen, argon, karbon dioksida, dan uap air. Gas pembawa yang cocok bergantung pada karakteristik detektor tersebut. Gas hidrogen dan helium digunakan pada detektor kinduktivitas termal sedangkan nitrogen digunakan pada detektor pengionan nyala. Sistem pengambilan sampel Sampel-sampel cair : diinjeksikan melalui suatu karet septum dengan memakai suntikan syringe. Sampel-sampel gas : diinjeksikan atau dimasukkan dengan memakai bermacam-macam alat pengambilan sampel gas yang dirancang untuk kromatograf komersial kolom Kolom Kapiler - Merupakan tabung yang panjang dan tipis dari kaca atau bahan lainnya seperti baja tahan karat. - Hanya dapat menangani sampel-sampel yang sangat kecil, dan penggunaannya secara luas menunggu pengembangan detektor yang sangat sensitif. Kolom Isian Fasa stasioner dalam GLC adalah cairan, tetapi cairan itu tidak boleh dibiarkan bergerak-gerak di dalam tabung. Cairan tersebut harus diimobilisasi, biasanya dalam bentuk suatu lapisan tipis dengan luas permukaan besar. Ini paling lazim dilakukan dengan mengimpregnasi suatu bahan padat dengan fase cair kolom diisi. Kolom … (2) Pemilihan fasa cair - Fasa cair stasioner harus dipilih dengan mempertimbangkan masalah pemisahan tertentu. - Fasa cair harus stabil secara termal pada temperatur kolom (kecuali dalam kasus-kasus khusus), tidak bereaksi secara kimia dengan komponen-komponen sampel, memiliki daya pelarut yang cukup untuk sampel. Karakteristik detektor Detektor Integral Memberikan suatu pengukuran setiap saat dari jumlah total bahan yang dielusi yang telah melewatinya sampai waktu itu. Detektor Diferensial Menghasilkan kromatogram familiar yang terdiri dari puncak-puncak dan bukan langkah-langkah. Dibagi menjadi 2 kelas besar : - detektor yang mengukur konsentrasi zat terlarut dengan memakai beberapa sifat fisika dari aliran gas buangan - detektor yang merespons secara langsung zat terlarut dengan demikian berarti mengukur laju alir massanya. Karakteristik detektor … (2) Kromatogram yang diperoleh dengan detektor Integral Kromatogram yang diperoleh dengan detektor diferensial Karakteristik detektor …. (3) Kepekaan Kepekaan detektor menunjukkan suatu batasan yang paling penting pada jumlah zat terlarut yang paling kecil yang dapat ditentukan dengan GLC Rumus umum untuk kepekaan : Stabilitas Garis dasar suatu kromatogram dimaksudkan untuk fluktuasi jangka pendek dari suatu sifat yang sangat acak yang disebut noise. Noise dapat dihubungkan dengan kepekaan, tingkat noise dan batas deteksi. Hubungan antara kepekaan, tingkat noise, dan batas deteksi dapat dirumuskan sebagai berikut. Mengingat kembali definisi kepekaan Jika menggabungkan batas deteksi, Qo, dengan dua kali tingkat noise puncak ke puncak, 2Rn, maka kita bisa tulis Karakteristik detektor … (3) Keserbagunaan Waktu Respons Waktu respons keseluruhan untuk suatu kromatograf adalah fungsi bukan hanya dari detektor itu sendiri, tetapi juga kelembaman komponen-komponen lain. Misalnya perekam. Kelinieran Jenis-jenis detektor Detektor Konduktivitas Termal - Detektor yang banyak digunakan untuk GLC. mengandung : filamen logam yang termistor. - Gas pembawanya adalah hidrogen dan helium - Detektor ini relatif sederhana, tidak mahal, memiliki kepekaan yang cukup bagi banyak kegunaan Alat ini dipanaskan maupun suatu Jenis-jenis detektor …. (2) Detektor Pengionan Nyala Prinsip dasar : 1. Energi kalor dalam hidrogen menyebabkan banyak molekul untuk mengionisasi 2. Gas efluen dari kolom dicampur dengan hidrogen dan dibakar pada ujung jet logam dalam udara berlebih. 3. Potensial diberikan antara jet dan elektroda kedua yang bertempat di atas atau sekitar nyala itu. 4. Ketika ion-ion dibentuk dalam nyala, ruang gas antara kedua elektroda menjadi lebih konduktif, dan arus yang meningkat mengalir dalam sirkuit. 5. Arus melewati resistor, tegangan terbentuk yang dikuatkan untuk menghasilkan isyarat yang diterima perekam. Jenis-jenis detektor … (3) Gambar Detektor Pengionan Nyala Penerapan glc Identifikasi Senyawa Keserbagunaan GLC Pirolisis Kromatografi Gas Analisis Kuantitatif Bergantung pada hubungan antara jumlah suatu zat terlarut dan ukuran dari pita elusi yang dihasilkan. Kromatografi Cair Kromatografi Cair Kromatografi adalah kromatografi dengan fasa gerak berupa zat cair. PROSES-PROSES DISTRIBUSI FASA Adsorpsi Pertukaran Ion Partisi Cair - Cair ADSORPSI Adsorpsi adalah proses pemisahan bahan dari suatu campuran dengan cara pengikatan bahan tersebut pada seluruh bagian adsorben cair yang diikuti dengan pelarutan. ADSORBEN Persyaratan adsorben : Memiliki daya melarutkan bahan yang akan diabsorpsi yang sebesar mungkin (kebutuhan akan cairan lebih sedikit, volume alat lebih kecil). Selektif Memiliki tekanan uap yang rendah Tidak korosif Mempunyai viskositas yang rendah Stabil secara termis Murah Alat Absorpsi Secara Skematis Prinsip Pemisahan Ion Untuk memisahkan sejumlah anion dan kation satu sama lainnya. Anorganik kation dipisahkan pada kolom resin pemisah kation, sementara anorganik anion dipisahkan pada kolom resin pemisah anion. Resin Pemisah Ion Contoh Pemisahan ion Na+, NH4+, K+, Mg2+ dan Ca2+ Resin-SO3-H+ + Na+, NH4+, K+, Mg2+, Ca2+ ↔ Resin-SO3-Na+, NH4+, K+, Mg2+, Ca2+ + H+ Partisi Cair - Cair Teknik ini tergantung pada partisi zat padat diantara dua pelarut yang tidak dapat bercampur salah satu diantaranya bertindak sebagai fasa diam dan yang lainnya sebagai fasa gerak. Kromatografi Cair-Cair Kromatografi Cair-Cair Ada dua macam sistem penggunaan dalam kromatografi cair-cair : 1. kromatografi fasa normal fase gerak → non polar ( ex: heksana, isopropil-eter) fase diam → sangat polar (ex: air) digunakan untuk memisahkan senyawa polar, sebab senyawa polar akan tertahan lebih lama didalam kolom yang polar, sedangkan senyawa yang non-polar akan keluar lebih awal dari dalam kolom. 2. Kromatografi fasa terbalik fase gerak → polar ( ex: air, metanol) fase diam → non polar (ex: hidrokarbon oktadekana) digunakan untuk memisahkan senyawa-senyawa non polar. Analisa Kualitatif Dasarnya adalah waktu retensi atau volume retensi suatu senyawa. Membandingkan t atau V senyawa dalam sampel yang dianalisis dengan t atau V suatu senyawa standar (yang telah diketahui) Analisis Kuantitatif Metode pengukuran tinggi puncak Tinggi puncak suatu kromatogram akan sebanding dengan kadar senyawa yang membentuk kromatogram tersebut. Pengukuran tinggi puncak didasarkan pada rumus pengukuran tinggi suatu segitiga, yaitu suatu garis tegak lurus dari titik tengah alas kromatogram sampai dengan perpotongan sisi segitiga kromatogram tersebut. Analisis Kuantitatif (lanjutan) Metode pengukuran luas puncak Dapat memberikan hasil yang lebih akurat jika dibandingkan dengan cara pengukuran tinggi puncak. Luas puncak diukur seperti menghitung luas segitiga yaitu : Rumus tersebut memberikan hasil yang baik jika kromatogramnya berbentuk lancip. Cara lain menggunakan rumus : Analisis Kuantitatif (lanjutan) Analisis Kuantitatif (lanjutan) Metode gunting dan timbang Kromatogram yang telah digambarkan pada kertas digunting sesuai bentuknya, kemudian guntingan-guntingan kertas kromatogram ini ditimbang. Berat dari masingmasing guntingan kromatogram ini akan sebanding dengan kadar senyawa yang membentuk kromatogram tersebut. Analisis Kuantitatif (lanjutan) Metode Integrator Integrator adalah peralatan elektronik yang sering dijumpai pada peralatan kromatografi yang modern. Alat ini akan mengubah tanda-tanda listrik dari detektor menjadi suatu gambaran kromatogram sekaligus menghitung luas kromatogram yang dibentuk secara elektronik. Kromatografi Kertas fase diam → kertas serap Fase gerak → pelarut atau campuran pelarut yang sesuai. Jarak relative pada pelarut disebut sebagai nilai Rf. Untuk setiap senyawa berlaku rumus sebagai berikut: Rf=jarak yang ditempuh oleh senyawa jarak yang ditempuh oleh pelarut Kromatografi Kertas (lanjutan) Kromatografi Kertas Dua Arah Digunakan dalam menyelesaikan masalah pemisahan substansi yang memiliki nilai Rf yang sangat serupa. Menggunakan dua pelarut yang berbeda Kromatografi Lapis Tipis Menggunakan sebuah lapis tipis silika atau alumina yang seragam pada sebuah lempeng gelas atau logam atau plastik yang keras. Fase diam → Jel silika (atau alumina) atau substansi yang dapat berpendarflour dalam sinar ultra violet. Fase gerak → pelarut atau campuran pelarut yang sesuai. Kromatografi Lapis Tipis (lanjutan) Sebuah garis menggunakan pinsil digambar dekat bagian bawah lempengan dan setetes pelarut dari campuran pewarna ditempatkan pada garis itu. Ketika bercak dari campuran itu mengering, lempengan ditempatkan dalam sebuah gelas kimia bertutup berisi pelarut dalam jumlah yang tidak terlalu banyak. Perlu diperhatikan bahwa batas pelarut berada di bawah garis dimana posisi bercak berada. Menutup gelas kimia untuk meyakinkan bawah kondisi dalam gelas kimia terjenuhkan oleh uap dari pelarut. Untuk mendapatkan kondisi ini, dalam gelas kimia biasanya ditempatkan beberapa kertas saring yang terbasahi oleh pelarut. Kondisi jenuh dalam gelas kimia dengan uap mencegah penguapan pelarut. Kromatografi Lapis Tipis (lanjutan) Perhitungan nilai Rf Nilai Rf untuk setiap warna dihitung dengan rumus sebagai berikut: Sebagai contoh, jika komponen berwarna merah bergerak dari 1.7 cm dari garis awal, sementara pelarut berjarak 5.0 cm, sehingga nilai Rf untuk komponen berwarna merah menjadi: Analisis Sampel yang Tidak Berwarna 1.Menggunakan pendarflour Fase diam pada sebuah lempengan lapis tipis seringkali memiliki substansi yang ditambahkan kedalamnya, supaya menghasilkan pendaran flour ketika diberikan sinar ultraviolet (UV). Pendaran ini ditutupi pada posisi dimana bercak pada kromatogram berada, meskipun bercakbercak itu tidak tampak berwarna jika dilihat dengan mata. Ketika sinar UV diberikan pada lempengan, akan timbul pendaran dari posisi yang berbeda dengan posisi bercak-bercak. Bercak tampak sebagai bidang kecil yang gelap. Analisis Sampel yang Tidak Berwarna 2. Penunjukkan bercak secara kimia Dalam beberapa kasus, dimungkinkan untuk membuat bercak-bercak menjadi tampak dengan jalan mereaksikannya dengan zat kimia sehingga menghasilkan produk yang berwarna. Sebuah contoh yang baik adalah kromatogram yang dihasilkan dari campuran asam amino. Kromatogram dapat dikeringkan dan disemprotkan dengan larutan ninhidrin. Ninhidrin bereaksi dengan asam amino menghasilkan senyawa-senyawa berwarna, umumnya coklat atau ungu. Dalam metode lain, kromatogram dikeringkan kembali dan kemudian ditempatkan pada wadah bertutup (seperti gelas kimia dengan tutupan gelas arloji) bersama dengan kristal iodium. Uap iodium dalam wadah dapat berekasi dengan bercak pada kromatogram, atau dapat dilekatkan lebih dekat pada bercak daripada lempengan. Substansi yang dianalisis tampak sebagai bercak-bercak kecoklatan. Kromatografi Kolom Kolom kromatografi berkerja berdasarkan skala yang lebih besar menggunakan material terpadatkan pada sebuah kolom gelas vertikal. Penggunaan kolom Misalnya memisahkan campuran dari dua senyawa yang berwarna, yaitu kuning dan biru. Warna campuran yang tampak adalah hijau. Pertama penutup kran dibuka untuk membiarkan pelarut yang sudah berada dalam kolom mengering sehingga material terpadatkan rata pada bagian atas, dan kemudian tambahkan larutan secara hati-hati dari bagian atas kolom. Lalu buka kran kembali sehingga campuran berwarna akan diserap pada bagian atas material terpadatkan, sehingga akan tampak seperti gambar disamping. menamambahkan pelarut baru melalui bagian atas kolom, jangan sampai merusak material terpadatkan dalam kolom. Lalu buka kran, supaya pelarut dapat mengalir melalui kolom, kumpulkan dalam satu gelas kimia atau labu dibawah kolom. Karena pelarut mengalir kontinyu, anda tetap tambahkan pelarut baru dari bagian atas kolom sehingga kolom tidak pernah kering. Perubahan yang mungkin terjadi sejalan perubahan waktu High Performance Liquid Chromatography (HPLC) Peralatan HPLC secara prinsip terdiri dari : Tempat pelarut Pompa Tempat injeksi sampel Kolom Detektor Rekorder i High Performance Liquid Chromatography (HPLC) [lanjutan] 1. Fasa mobile (pelarut) pelarut yang digunakan harus dilakukan degassing untuk mengeluarkan gas terlarut yang tidak diinginkan. 2. Sistem pompa ada dua jenis pompa, yang mendasari pemakaiannya yaitu : tekanan tetap dan volume tetap. 3. Flow controller (pengendali aliran) untuk menstabilkan aliran fasa mobile akibat adanya perubahan tekanan gas, temperatur dan viskositas. 4. Kolom Tidak memerlukan temperatur yang tinggi, karena sifat ikatan kimia terhadap fasa stasioner sangat sensitif terhadap temperatur yang tinggi. High Performance Liquid Chromatography (HPLC) [lanjutan] 5. Detektor karakteristik detektor untuk HPLC - sensivitasnya tinggi - respon yang menyeluruh terhadap sampel - tidak meruska sampel - tidak sensitif terhadap perubahan temperatur dan kecepatan aliran fasa mobile - dapat beroperasi secara terus menerus. 6. Rekaorder Mengeluarkan output berupa kromatogram. Keuntungan HPLC Cepat Resolusi Sensitivitas detektor Kolom yang dapat digunakan kembali Ideal untuk zat bermolekul besar dan berionik Mudah rekoveri sampel SEKIAN DAN TERIMAKASIH Pertanyaan Fase diamnya dari GLC Mengapa larutan fase stasioner (khotib) Dampak pembuatan kromatografi sempit dan tebal Perbedaaan adsorpsi dari spektrokospi dengan kromatografi (Daudi) Keunggulan antara kromatografi dan spektrokospi. (Daudi) Bahwa metode ada kesamaannya yaitu analisis senyawa dengan tingkat pemisahan yang lebih akurat, tapi perbedaannya deteksi sampe yang digunakan berbeda, yaitu stre menggunakan sinar, kromatografi dengan fase cair dan gas.