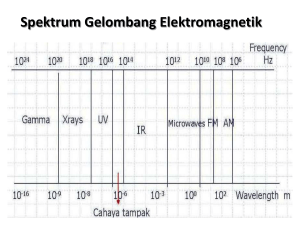
Bilangan kuantum
advertisement

Atom netral Ion bermuatan listrik positif : melepas elektron negatif ; menerima elektron Atom Inti atom o proton o neutron Elektron Contoh: 11 23 Na p = 11 e = 11 n = 12 Percobaan Lempeng emas ”Oleh Rutherford” menggunakan lempeng emas kemudian di tembakan sinar laser Kesimpulan Rutherford: 1. Atom sebagian besar merupakan ruang hampa. 2. Atom terdiri dari inti dimana massa dan muatan positif dipusatkan. 3. Elektron bergerak disekitar inti atom. Rutherford : Atom terdiri dari inti atom sebagai pusat massa dan terpusat muatan positif, sedang electron bergerak disekitar inti menurut lintasan–lintasan tertentu. Elektron–elektron dalam atom hanya dapat menempati lintasan-lintasan tertantu, dan dapat berpindah dari satu lintasan kelintasan yang lain, tetapi tidak dapat berada pada sembarang kedudukan. Keadaan elektron dalm suatu lintasan dapat ditunjukan oleh 4 macam bilangan kuantum yang dimilikinya yaitu: Bilangan kuantum Utama (n) Bilangan kuantum Azimut (l) Bilangan kuantum Magnetik (m) Bilangan kuantum Spin (s) Menggambarkan besarnya tingkat tenaga yang dimiliki oleh suatu elektron dalam atom. Hubungan antara impuls putar dan gerakan suatu elektron dalam suatu tingkat tenaga (lintasan) dapat dinyatakan dalam persamaan berikut : Dengan n = 1,2,3 ....... adalah bilangan kuantum utama ,yang mengkuantisasikan Impuls putar gerakan elektron dalam suatu lintasan . Bilangan kuantum ini juga melukiskan ”besarnya ukuran lintasan elektron dalam atom ( jarak inti elektron). Lintasan dengan n = 1 disebut lintasan K Lintasan dengan n = 2 disebut lintasan L Lintasan dengan n = 3 disebut lintasan M dst disebut N, O, P,dan Q Menyatakan ukuran dan tingkat energi orbital Memiliki nilai bilangan bulat positif (1,2,3,…dst) Semakin besar nilai n, semakin besar ukuran orbital (semakin besar jarak rata2 elektron dalam orbital dari inti atom) Nilai n menunjukkan kulit atom Bilangan kuantum ini diberi lambang ℓ ,dan dikenal pula sebagai bilangan kuantum orbital. Bilangan kuantum azimut memberikan gambaran tentang kuantisasi implus putar gerakan elektron dalam suatu sub lintasan. Menggambarkan tingkat energi elektron pada subkulit Suatu tingkat tenaga dengan bilangan kuantum n akan memiliki sejumlah sub lintasan, dimana masing-masing sub lintasan akan memiliki bilangan kuantum azimut yang berbeda. Harga bilangan kuantum azimut 0,1,2,3.... ( n-1) Sub kulit elektron: • s (sharp) • p (principal) • d (diffuse) • f (fundamental) Elektron pada subkulit s ℓ = 0 Elektron pada subkulit p ℓ = 1 Elektron pada subkulit d ℓ = 2 Elektron pada subkulit f ℓ = 3 Bentuk orbital biasanya dinyatakan dgn s,p,d,f Kulit M, maka nilai n = 3 dan ℓ = 0, 1, dan 2 karena mempunyai subkulit s, p, dan d. Kulit N, maka nilai n = 4 dan ℓ = 0, 1, 2, dan 3 karena mempunyai subkulit s, p, d, dan f. Jadi nilai bilangan kuantum azimut tidak mungkin sama atau lebih besar dari bilangan kuantum utamanya. Maksimal nilai ℓ = n – 1 Pengisian elektron dalam atom berlangsung menurut urutan tingkat tenaga orbital–orbital atom. Urutan tingkat tenaga orbitalorbital atom adalah : 1s<2s<2p<3p<3p<4s<3d<4p<4d dst. 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p10 7s2 5f14 6d10 7p6 Bilangan ini mempunyai lambang m Bilangan kuantum magnetik menunjukkan arah orbital elektron Bilangan kuantum magnetik menyatakan jumlah orbital pada sub kulit elektron Bilangan kuantum magnetik menunjukan adanya beberapa sub–sub lintasan dengan tenaga yang sama sebagai penyusun suatu sub lintasan. Harga Sub kulit S P d f m pada berbagai subkulit Harga ℓ 0 1 2 3 Harga m Jumlah Orbital 0 1 –1, 0, +1 3 –2, –1, 0, +1, +2 5 –3, –2, –1, 0, +1, +2, +3 7 Disamping bergerak mengelilingi inti, elektron-elektron dalam atom berotasi, sehingga akan menimbulkan implus putar rotasi elektron. Implus putar ini besarnya juga terkuantisasi . S = +1/2 disebut bilangan kuantum spin positif. (+ ½) berarti bahwa rotasi elektron searah dengan rotasi atom keseluruhan, sedangkan bilangan kuantum negatif (- ½) berarti bahwa rotasi elektron berlawanan dengan rotasi atom secara keseluruhan. menunjukkan arah perputaran elektron pada sumbunya arah rotasi : searah jarum jam (nilai s = + ½ dan dalam orbital dituliskan dengan tanda panah ke atas atau berlawanan arah jarum jam). berlawanan arah jarum jam (nilai s = - ½ dan dalam orbital dituliskan dengan tanda panah ke bawah) Menyatakan bahwa didalam suatu atom tidak boleh ada 2 elektron atau lebih yang memilki keempat bilangan kuantum sama. Kalau ada dua elektron memiliki n,l,dan m sama ; maka mereka harus mempunyai spin berlawanan, 2 elektron semacam ini “ berpasangan”. 1. 2. 3. Tentukan harga bilangan kuantum n, ℓ, m dari elektron-elektron pada sub kulit 3p. Suatu atom memiliki elektron terakhir pada n=3, ℓ =1, m=1, dan s= -1/2. Berapa jumlah elektron atom tsb? 20 Tuliskan konfigurasi elektron unsur 40 Ca