OKSIDASI BIOLOGI
advertisement

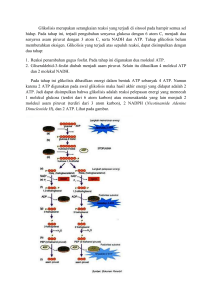
BIOENERGETIKA DAN FOSFORILASI OKSIDATIF T. HELVI MARDIANI Bagian Biokimia Fakultas Kedokteran Universitas Sumatera Utara Pendahuluan Bioenergetika atau termodinamika biokimia memberikan prinsip dasar untuk menjelaskan mengapa sebagian reaksi dapat terjadi sedangkan sebagian yang lain tidak. Sejumlah sistem non biologik dapat menggunakan energi panas untuk melaksanakan kerjanya, namun sistem biologi pada hakekatnya bersifat isotermik dan memakai energi kimia untuk memberikan tenaga bagi proses kehidupan. Prinsip reaksi oksidasi reduksi yaitu reaksi pengeluaran dan perolehan elektron berlaku pada berbagai sistem biokimia dan merupakan konsep penting yang melandasi pemahaman tentang sifat oksidasi biologi. Ternyata banyak reaksi-reaksi oksidasi dalam sel hidup dapat berlangsung tanpa peran molekul oksigen. Mitokondria sebagai organella pernapasan sel, dikatakan demikian karena didalamnya berlangsung sebagian besar peristiwa penangkapan energi yang berasal dari oksidasi dalam rantai pernapasan sel. Sistem dalam mitokondria yang merangkaikan respirasi dengan produksi ATP sebagai suatu zat antara berenergi tinggi dikenal dengan fosforilasi oksidatif. Fosforilasi oksidatif memungkinkan organisme aerob menangkap energi bebas dengan proporsi yang lebih besar bila dibandingkan dengan organisme an aerob. BIOENERGETIKA DAN FOFORILASI OKSIDATIF Hukum termodinamika Organisme hidup mengubah energi yang diperolehnya dari makanan untuk berbagai tujuan seperti pemeliharaan sel, reproduksi dan berbagai kerja baik fisik maupun kimia. Dalam banyak reaksi biokimia, energi dari reaktan diubah dengan sangat efisien menjadi bentuk yang berbeda. Dalam fotosintesa, energi cahaya diubah menjadi energi ikatan kimia. Dalam mitokondria, energi bebas yang terkandung dalam molekul kecil dari bahan makanan diubah mnjadi suatu alat tukar energi dalam bentuk adenosin trifosfat ( ATP ). Energi ikatan kimia yang terkandung dalam ATP selanjutnya digunakan dalam berbagai cara dan tujuan. Dalam kontraksi otot, energi ATP diubah oleh miosin menjadi energi mekanik. Membran dan organel sel mempunyai pompa yang menggunakan ATP untuk transport molekul dan ion. ATP juga digunakan untuk berbagai aktiviatas sel lainnya. Bioenergetika atau thermodinamika biokimia menerangkan berbagai macam perubahan energi yang menyertai reaksi-reaksi biokimia. Energi bebas adalah bahagian energi total yang dapat digunakan untuk kerja-kerja bermanfaat, difungsikan berdasar hukum thermodinamika pertama dan kedua. Hukum thermodinamika pertama menyatakan jumlah energi dalam suatu sistem dan lingkungannya adalah tetap. Hukum kedua menyatakan bahwa suatu proses dapat berlangsung spontan hanya bila jumlah entropi (tingkat kekacauan) suatu sistem dan lingkungannya bertambah. Suatu masalah dalam menggunakan entropi sebagai kriteria apakah suatu reaksi kimia dapat berjalan spontan, ialah bahwa perubahan entropi reaksi kimia tidak dapat diukur secara langsung. Kesukaran ini diatasi ©2004 Digitized by USU digital library 1 dengan menggunakan fungsi thermodinamika lain yang disebut energi bebas ( G ) dengan persamaan : tG = tH - T tS . tG adalah perubahan energi bebas suatu sistem yang mengalami perubahan pada suatu tekanan (P) dan suhu (T) yang tetap. tH adalah perubahan entalpi (kandungan panas) sistem dan tS perubahan entropinya. Perubahan entalpi dinyatakan sebagai : tH = tE – PtV, karena perubahan volume, tV dalam reaksi biokimia kecil sehingga tH hampir sama dengan tE, maka : tG = tE - T tS . Berlawanan dengan perubahan energi dalam sistem (tE ), perubahan energi bebas (tG ) suatu reaksi adalah kriteria yang berharga untuk menentukan apakah reaksi tersebut dapat berlangsung dengan spontan. Suatu reaksi dapat berlangsung spontan hanya bila tG negatif. Bila tG nol, sistem berada dalam keseimbangan dan bila positif, diperlukan masukan energi bebas untuk menggerakkan reaksi tersebut. ATP merangkai proses eksergonik dan endergonik Proses dimana berlangsungnya reaksi-reaksi yang melepaskan energi bebas (eksergonik) selalu dirangkaikan dengan proses yang reaksi-reaksinya memerlukan energi bebas (endergonik). Reaksi eksergonik adalah reaksi dalam proses katabolisme yaitu reaksi-reaksi pemecahan atau oksidasi molekul bahan bakar sedangkan reaksi sintesa yang membangun berbagai substansi terdapat dalam proses anabolisme. Untuk merangkaikan kedua proses eksergonik dan endergonik harus ada senyawa antara dengan potensial energi tinggi yang dibentuk dalam reaksi eksergonik dan menyatukan senyawa yang baru dibentuk tersebut kedalam reaksi endergonik, sehingga energi bebasnya dialihkan antara dua proses tersebut. Senyawa antara yang dibentuk tidak perlu mempunyai hubungan struktural dengan reaktan-reaktan yang bereaksi. Dalam sel hidup, reaksi oksidasi yang melepas energi bebas selalu disertai dengan peristiwa fosforilasi yang membentuk senyawa dengan potensial energi lebih tinggi. Senyawa pembawa atau senyawa antara energi tinggi yang utama adalah ATP . ATP adalah nukleotida yang terdiri dari adenin , ribosa dan trifosfat . Bentuk aktif ATP adalah kompleksnya bersama dengan Mg2+ atau Mn2+. Sebagai pengemban energi, ATP kaya energi karena unit trifosfatnya mengandung dua ikatan fosfoanhidrida. Sejumlah besar energi bebas dilepaskan ketika ATP dihidrolisis menjadi adenosin difosfat (ADP) dan ortofosfat (Pi) atau ketika ATP dihidrolisis menjadi adenosin monofosfat (AMP) dan pirofosfat (Ppi). ATP memungkinkan perangkaian reaksi yang secara termodinamik tidak menguntungkan menjadi reaksi yang menguntungkan. Reaksi pertama dalam lintasan glikolisis yaitu fosforilasi glukosa menjadi glukosa 6 fosfat adalah reaksi yang endergonik (tGº = + 13,8 kj/mol), agar reaksi dapat berlangsung harus terangkai dengan reaksi lain yang lebih eksergonik yaitu hidrolisa gugus terminal fosfat ATP (tGº = - 30,5 kj/mol ) sehingga rangkaian reaksi yang dikatalisa oleh heksokinase tersebut berlangsung dengan mudah dan sangat eksergonik (tGº = - 16,7 kj/mol ). Konversi antar ATP, AMP dan ADP adalah mungkin. Enzym adenilat kinase (miokinase) mengkatalisis reaksi : ATP + AMP ⇔ ADP + ADP. Reaksi ini mempunyai fungsi antara lain, memungkinkan fosfat energi tinggi dalam ADP untuk digunakan dalam sintesa ATP, memungkinkan AMP yang terbentuk dari beberapa reaksi aktivasi yang melibatkan ATP difasforilasi ulang menjadi ADP dan memungkinkan peningkatan konsentrasi AMP (ketika ATP terpakai habis) sebagai sinyal metabolik untuk menaikkan kecepatan reaksi-reaksi katabolik (menghasilkan ATP). Beberapa reaksi biosintesis dijalankan oleh nukleotida trifosfat yang analog dengan ATP, yaitu guanosin trifosfat (GTP), uridin trifosfat (UTP) dan sitidin trifosfat (CTP). Bentuk difosfat nukleotida-nukleotida ini disebut dengan GDP, UDP dan CDP dan bentuk- ©2004 Digitized by USU digital library 2 bentuk monofosfatnya dengan GMP, UMP dan CMP. Transfer gugus fosforil terminal dari satu kelain nukleotida dapat terjadi dengan bantuan enzym nukleosida difosfat kinase seperti reaksi-reaksi ATP + GDP ⇔ ADP + GTP dan ATP + GMP ⇔ ADP + GDP. Berbagai senyawa dalam sistem biologi mempunyai potensi fosforil yang tinggi. Ternyata, beberapa diantaranya, seperti fosfoenolpiruvat, karbamoil fosfat, 1, 3 bifosfogliserat, asetil fosfat dan kreatin fosfat mempunyai potensial pemindahan fosfat yang lebih tinggi dari ATP, hal ini berarti senyawa-senyawa tersebut dapat memindahkan gugus fosforilnya ke ADP untuk membentuk ATP. Potensial transfer fosforil senyawa-senyawa terfosforilasi yang penting secara biologis seperti glukosa 1 fosfat, fruktosa 6 fosfat, glukosa 6 fosfat dan gliserol 3 fosfat lebih rendah dari ATP. Posisi ATP yang berada ditengah-tengah dari molekul-molekul terfosforilasi tersebut, memungkinkan ATP berfungsi secara efisien sebagai pengemban gugus fosforil. ATP sering disebut senyawa fosfat berenergi tinggi dan ikatan fosfoanhidridanya disebut sebagai ikatan berenergi tinggi. Senyawa-senyawa tinggi energi adalah senyawa yang banyak melepaskan enegi bebas ketika mengalami hidrolisis. Istilah ikatan berenergi tinggi sering disimbolkan dengan ~ P dan menunjukkan senyawa yang punya potensial transfer fosforil tinggi. Ada tiga sumber utama ~ P yang mengambil bagian dalam penangkapan energi yaitu peristiwa fosforilasi oksidatif, sumber ~ P yang paling besar pada organisme aerobik, sumber energi bebas untuk menggerakkan proses ini berasal dari reaksi-reaksi oksidasi rantai pernapasan. Sumber kedua adalah glikolisis, membentuk total dua ~ P yang terjadi pada reaksi pemecahan glukosa menjadi laktat. Sumber ketiga adalah siklus asam sitrat, dimana satu ~ P dihasilkan langsung pada konversi suksinil ko-A menjadi suksinat. Senyawa biologi penting lainnya yang digolongkan sebagai senyawa energi tinggi adalah yang mengandung ikatan tiol ester, mencakup koenzym A, protein pembawa asil, senyawa ester asam amino, S-adenosilmetionin, uridin difosfat glukosa dan 5.fosforibosil.1.pirofosfat. Reaksi oksidasi molekul bahan bakar dimana NADH dan FADH2 adalah pengemban elektron utama Kemotrop memperoleh energi bebas dari oksidasi molekul bahan bakar, seperti glukosa dan asam lemak. Pada organisme aerob, akseptor elektron terakhir adalah oksigen. Transport elektron dalam reaksi-reaksi oksidasi tidak langsung dari molekul bahan bakar atau dari produk pemecahannya ke oksigen. Substrat-substrat yang dioksidasi memindahkan elektronnya kepengemban-pengemban khusus yaitu nukleotida piridin atau flavin. Pengemban yang tereduksi ini kemudian memindahkan elektron potensi tingginya ke oksigen melalui rantai pernapasan yang terdapat pada sisi dalam membran mitokondria. Gradien proton yang terbentuk sebagai hasil aliran elektron dalam rantai pernapasan ini yang kemudian mendorong sintesis ATP dari ADP dan ortofosfat ( Pi ). Proses ini yang disebut fosforilasi oksidatif, yang menjadi sumber utama ATP pada organisme aerob. Selain itu, elektron potensi tinggi yang berasal dari oksidasi molekul bahan bakar dapat digunakan pada reaksi-reaksi biosintesa yang memerlukan daya pereduksi. Nikotinamid adenin dinukleotida (NAD+) adalah pengemban elektron utama pada oksidasi molekul bahan bakar. Bagian reaktif dari NAD+ adalah cincin nikotinamidnya, suatu derivat piridin. Pada oksidasi substrat, cincin nikotinamid NAD+ menerima satu ion hidrogen dan dua elektron, yang ekivalen dengan satu ion hidrida(H-). Bentuk tereduksi pengemban ini disebut NADH. Pada dehidrogenasi diatas, satu atom hidrogen dari subsrat dipindahkan langsung ke NAD+, sedangkan yang ©2004 Digitized by USU digital library 3 lainnya terdapat dalam pelarut sebagai proton. Kedua elektron yang dilepaskan oleh substrat dipindahkan kecincin nikotinamid. Pengemban elektron utama lainnya pada oksidasi molekul bahan bakar adalah flavin adenin dinukleotida (FAD). Bentuk tereduksinya adalah FADH2. Bagian reaktif dari FAD adalah cincin isoaloksazinnya. FAD, seperti juga NAD+, dapat menerima dua elektron. Tetapi tidak seperti NAD+, FAD mengambil proton dan juga ion hidrida. Rantai pernapasan dan fosforilasi oksidatif NADH dan FADH2 yang terbentuk pada reaksi oksidasi dalam glikolisis, reaksi oksidasi asam lemak dan reaksi-reaksi oksidasi dalam siklus asam sitrat merupakan molekul tinggi energi karena masing-masing molekul tersebut mengandung sepasang elektron yang mempunyai potensial transfer tinggi. Bila elektron-elektron ini diberikan pada oksigen molekuler, sejumlah besar energi bebas akan dilepaskan dan dapat digunakan untuk menghasilkan ATP. Adanya perbedaan potensial oksidasi reduksi (E0’) atau potensial transfer elektron memungkinkan elektron mengalir dari unsur yang potensial redoks lebih negatif (afinitas elektronnya lebih rendah) ke unsur yang potensial redoksnya lebih positif (afinitas elektronnya lebih tinggi). Aliran elektron ini akan melalui komplek-komplek protein yang terdapat pada membran dalam mitokondria dan menyebabkan proton terpompa keluar dari matriks mitokondria. Akibatnya terbentuk kekuatan daya gerak proton yang terdiri dari gradien pH dan potensial listrik transmembran yang kemudian mendorong proton mengalir kembali kedalam matriks melalui suatu kompleks enzym sintesa ATP. Jadi, oksidasi dan fosforilasi terangkai melalui gradien proton pada membran dalam mitokondria. Fosforilasi oksidatif merupakan proses pembentukan ATP akibat transfer elektron dari NADH atau FADH2 kepada oksigen melalui serangkaian pengemban elektron. Proses ini adalah sumber utama pembentukan ATP pada organisme aerob. Pembentukan ATP dalam glikolisis sempurna glukosa menjadi CO2 dan H2O, dari 30 ATP yang terbentuk 26 ATP berasal dari proses fosforilasi oksidatif. Komplek-komplek enzym yang terangkai pada membran dalam mitokondria untuk pengangkutan elektron dari molekul NADH atau FADH2 ke oksigen molekuler dimana terbentuk sejumlah ATP dan molekul air dikenal dengan rantai pernapasan. Komplek enzym tersebut adalah NADH-Q reduktase, suksinat-Q reduktase, sitokrom reduktase dan sitokrom oksidase. Suksinat-Q reduktase, berbeda dengan ketiga komplek yang lain, tidak memompa proton. Dalam fosforilasi oksidatif, daya gerak elektron diubah menjadi daya gerak proton dan kemudian menjadi potensial fosforilasi. Fase pertama adalah peran komplek enzym sebagai pompa proton yaitu NADH-Q reduktase, sitokrom reduktase dan sitokrom oksidase. Komplek-komplek transmembran ini mengandung banyak pusat oksidasi reduksi seperti flavin, kuinon, besi-belerang, heme dan ion tembaga. Fase kedua dilaksanakan oleh ATP sintase, suatu susunan pembentuk ATP yang digerakkan melalui aliran balik proton kedalam matriks mitokondria. Elektron potensial tinggi dari NADH masuk rantai pernapasan pada NADH-Q reduktase atau disebut juga dengan NADH dehidrogenase atau komplek I. Langkah awal adalah pengikatan NADH dan transfer dua elektronnya ke flavin mononukleotida (FMN), gugus prostetik komplek ini, menjadi bentuk tereduksi, FMNH2. Elektron kemudian ditransfer dari FMNH2 keserangkaian rumpun belerang besi (4Fe-4S), jenis kedua gugus prostetik dalam NADH-Q reduktase. Elektron dalam rumpun belerangbesi kemudian diangkut ke ko-enzym Q, dikenal juga sebagai ubiquinon. Ubiquinon mengalami reduksi menjadi radikal bebas anion semiquinon dan reduksi kedua terjadi dengan pengambilan elektron kedua membentuk ubiquinol (QH2) yang terikat enzym. Pasangan elektron pada QH2 dipindahkan ke rumpun belerang besi (2Fe-2S) kedua yang ada pada NADH-Q reduktase, dan akhirnya ke Q yang bersifat mobil ©2004 Digitized by USU digital library 4 dalam inti hidrofobik membran dalam mitokondria. Aliran dua elektron ini menyebabkan terpompanya empat H+ dari matriks kesisi sitosol membran dalam mitokondria, dengan mekanisme yang belum diketahui. Ubiquinol ( QH2 ) juga merupakan tempat masuk elektron dari FADH2 enzymenzym flavoprotein kerantai pernapasan. Suksinat dehidrogenase merupakan bagian dari komplek suksinat-Q reduktase atau disebut juga komplek II, suatu protein integral membran dalam mitokondria. FADH2 tidak meninggalkan komplek, elektronnya ditransfer kerumpun belerang-besi dan kemudian ke Q untuk masuk dalam rantai pernapasan. Enzym-enzym flavoprotein lain seperti gliserol fosfat dehidrogenase dan asil-ko-A dehidrogenase yang membentuk gugus prostetik tereduksi FADH2, elektronnya dipindahkan ke flavoprotein kedua yang disebut flavoprotein pemindah elektron atau ETF (electron transferring flavoprotein). Selanjutnya ETF memberikan elektronnya kerumpun belerang besi dan Q untuk masuk rantai pernapasan dalam bentuk QH2. Berbeda dengan komplek I, komplek II dan enzym lain yang mentransfer elektron dari FADH2 ke Q tidak memompa proton karena perubahan energi bebas dari reaksi yang dikatalisanya terlalu kecil. Itulah sebabnya, ATP yang terbentuk pada oksidasi FADH2 lebih sedikit dari pada melalui NADH. Pompa proton kedua dalam rantai pernapasan adalah sitokrom reduktase atau ubiquinol-sitokrom c reduktase atau komplek sitokrom bc1 atau disebut juga komplek III. Sitokrom merupakan protein pemindah elektron yang mengandung heme sebagai gugus prostetik. Komplek III ini berfungsi mengkatalisir transfer elektron dari QH2 kesitokrom c dan secara bersamaan memompa proton sebanyak dua H+ melewati membran dalam mitokondria. Ada dua sitokrom yaitu b dan c1 dalam komplek ini, juga mengandung protein Fe-S dan beberapa rantai polipeptida lain. Heme pada sitokrom b berbeda dari heme yang ada pada sitokrom c dan c1 yang terikat secara kovalen berupa ikatan tioester pada proteinnya. Sitokrom oksidase, komponen terakhir dari tiga pompa proton dalam rantai pernapasan, mengkatalisis transfer elektron dari ferositokrom c kemolekul oksigen sebagai akseptor terakhir. Sitokrom oksidase mengandung dua gugus heme yang berbeda dari heme pada sitokrom c dan c1 karena gugus rantai samping hemenya dan ikatannya pada enzym secara non kovalen. Heme komplek ini dikenali sebagai heme a dan heme a3, karenanya komplek ini juga disebut sitokrom aa3. Selain heme komplek ini juga mengandung dua ion tembaga, dikenal dengan CuA dan CuB. Ferositokrom c memberikan satu elektronnya kerumpun heme a- CuA dan satu lagi kerumpun heme a3- CuB dimana oksigen direduksi melalui serangkaian langkah menjadi dua molekul H2O. Molekul oksigen merupakan ekseptor elektron terminal yang ideal. Afinitasnya yang tinggi terhadap elektron memberi daya gerak termodinamik yang besar untuk fosforilasi oksidatif. Terjadi pemompaan proton empat H+ kesisi sitosol dari membran. Sejumlah ATP yang dibentuk pada peristiwa fosforilasi oksidatif dirantai pernapasan tidak begitu pasti karena stoikiometri pompa proton, sintesa ATP dan proses transport metabolite tidak harus dalam jumlah bulat atau bernilai tetap. Menurut perkiraan saat ini, jumlah H+ yang dipompa dari matriks kesisi sitosol membran oleh Komplek enzym I, III dan IV per pasangan elektron, masing-masing adalah 4, 2 dan 4. Sintesa ATP digerakkan oleh aliran kira-kira tiga H+ melalui ATP sintase. Sedangkan untuk mengangkut ATP dari matriks kesitosol memerlukan satu H+ tambahan. Dengan demikian terbentuk kira-kira 2,5 ATP sitosol akibat aliran sepasang elektron dari NADH ke oksigen. Untuk elektron yang masuk pada tahap komplek III, misalnya yang berasal dari oksidasi suksinat, hasilnya adalah kira-kira 1,5 ATP per pasangan elektron. Kecepatan fosforilasi oksidatif ditentukan oleh kebutuhan ATP. Transport elektron terangkai erat dengan fosforilasi, elektron tidak mengalir melalui rantai ©2004 Digitized by USU digital library 5 pernapasan ke oksigen bila tidak ada ADP yang secara simultan mengalami fosforilasi menjadi ATP. Fosforilasi oksidatif memerlukan suplai NADH atau sumber elektron lain dengan potensial tinggi, oksigen, ADP dan ortofosfat. Faktor terpenting dalam menentukan kecepatan fosforilasi oksidatif adalah kadar ADP. Kecepatan konsumsi oksigen oleh mitokondria meningkat tajam bila ditambahkan ADP dan kembali kenilai semula bila ADP yang ditambahkan sudah difosforilasi menjadi ATP. Pengaturan oleh kadar ADP ini disebut pengaturan respirasi. Kepentingan fisiologis mekanisme pengaturan ini jelas, kadar ADP meningkat bila ATP dipakai dan dengan demikian fosforilasi oksidatif terangkai dengan penggunaan ATP. Elektron tidak mengalir dari molekul bahan bakar kemolekul oksigen bila sintesa ATP tidak diperlukan. Transfer elektron dalam rantai pernapasan dapat dihambat oleh banyak inhibitor spesifik. Inhibitor-inhibitor ini dibagi menjadi tiga golongan yaitu inhibitor rantai pernapasan, inhibitor fosforilasi oksidatif dan pemutus rangkaian (uncoupler) fosforilasi oksidatif. Amobarbital (barbiturat), pierisidin A (antibiotik), insektisida dan rotenon (racun ikan) menghambat transfer elektron dalam NADH-Q reduktase dengan menyekat pemindahan elektron dari Fe-S ke Q. Karboksin dan TTFA menghambat aliran elektron dalam suksinat-Q reduktase, sedangkan malonat merupakan inhibitor kompetitif dari enzym suksinat dehidrogenase. Dimerkaprol dan antimisin A menghambat elektron dari sitokrom b dalam sitokrom reduktase. Racun klasik seperti H2S, karbon monoksida (CO), sianida (CN-) dan azida (N3-) menghambat sitokrom oksidase dan dapat menghentikan respirasi secara total. Oligomisin (antibiotik) menghambat fosforilasi dan dengan begitu juga menghambat oksidasi sedangkan atraktilosida dan asam bongkrek menghambat pengangkutan ADP kemitokondria dan ATP keluar mitokondria, sehingga menganggu fosforilasi oksidatif. Senyawa-senyawa pemutus rangkaian memisahkan proses oksidasi dalam rantai pernapasan dengan proses fosforilasi. Pemisahan ini menyebabkan respirasi menjadi tak terkendali, karena konsentrasi ADP dan ortofosfat tidak lagi membatasi laju respirasi . senyawa-senyawa ini antara lain adalah dinitrofenol, dinitrokresol, pentaklorofenol dan yang memiliki daya paling kuat sampai seratus kali lebih besar dari yang lain adalah CCCP (klorokarbonil sianida phenilhidrazon). Elektron dari NADH sitosol Membran dalam mitokondria tidak permeabel terhadap NADH dan NAD+. NADH yang terbentuk pada glikolisis disitosol, pada oksidasi gliseraldehid 3-fosfat, harus dioksidasi kembali menjadi NAD+ untuk kelangsungan glikolisis. Bagaimana NADH sitosol dapat dioksidasi melalui rantai pernapasan bila tidak dapat masuk kemitokondria? Pemecahannya adalah elektronnya saja yang dibawa melintasi membran mitokondria. Salah satu pembawa adalah gliserol 3-fosfat yang dapat menyebrangi membran luar mitokondria. Langkah pertama dalam sistem ini adalah pemindahan elektron dari NADH ke dihidroksiaseton fosfat membentuk gliserol 3fosfat yang dikatalisa oleh gliserol 3-fosfat dehidrogenase. gliserol 3-fosfat berdifusi kedalam mitokondria dan dioksidasi kembali menjadi dihidroksiaseton fosfat pada permukaan luar membran dalam mitokondria. Sepasang elektron dari gliserol 3fosfat ditransfer kegugus prostetik gliserol dehidrogenase mitokondria. Enzym ini berbeda dengan enzym serupa yang ada disitosol, karena menggunakan FAD dan bukan NAD sebagai akseptor elektron selain itu juga merupakan protein transmembran. Dihidroksiaseton fosfat yang terbentuk kemudian berdifusi kembali kedalam sitosol untuk melengkapi sistem angkut ini. Flavin tereduksi dalam mitokondria memindahkan elektronnya kepembawa elektron Q dan masuk rantai pernapasan dalam bentuk QH2. Akibatnya hanya terbentuk 1,5 ATP dan bukan 2,5 ATP bila NADH sitosol yang dioksidasi dalam rantai pernapasan diangkut oleh gliserol 3-fosfat. Penggunaan FAD memungkinkan elektron dari NADH sitosol ditranspor ©2004 Digitized by USU digital library 6 kedalam mitokondria melawan gradien konsentrasi NADH , walaupun untuk itu , sistem angkut ini harus merugi satu ATP dibanding bila sistem menggunakan NAD+. Sistem angkut ini terutama berperan pada otot terbang serangga yang dapat mempertahankan kecepatan fosforilasi oksidatif yang sangat tinggi . Dalam jantung dan hati, elektron dari NADH sitosol dibawa kedalam mitokondria melalui sitem angkut malat-aspartat, yang menggunakan dua penggemban membran dan empat enzym. Diawali dengan transfer elektron dari NADH sitosol ke oksaloaetat, membentuk malat, yang kemudian melintasi membran dalam mitokondria dan dioksidasi kembali melalui NAD+ dalam matriks mitokondria membentuk NADH. Karena oksaloasetat yang dibentuk tidak mudah melintasi membran dalam mitokondria, diperlukan reaksi transaminasi untuk membentuk aspartat, yang dapat diangkut kesisi sitosol. Berbeda dari sistem angkut gliserol fosfat , NADH hanya dapat dibawa kedalam mitokondria bila ratio NADH / NAD+ disitosol lebih tinggi dari pada dimatriks mitokondria. Protein pengangkut dalam mitokondria Mitokondria merupakan organel yang berbentuk lonjong, biasanya dengan panjang kurang lebih dua mikrometer dan diameter setengah mikrometer. Mitokondria mengandung susunan rantai pernapasan, enzym-enzym siklus asam sitrat dan enzym-enzym oksidasi asam lemak. mitokondria memiliki dua sistem membran, membran luar dan membran dalam yang luas dan berlipat-lipat. Lipatanlipatan pada membran dalam disebut krista. Dua kompartemen dalam mitokondria yaitu ruang antar membran (ruang antara membran dalam dan membran luar mitokondria) dan matriks yang dibatasi membran dalam. Membran luar cukup permeabel untuk sebagian besar molekul kecil dan ion, karena mengandung banyak porin, suatu protein transmembran dengan pori besar. Sebaliknya hampir tidak ada ion atau molekul polar yang dapat menembus membran dalam. Sekelompok besar protein transport mengangkut metabolit seperti ATP dan sitrat, melalui membran dalam kedalam matriks dan sebaliknya. Kedua sisi membran dalam disebut sisi matriks (sisi negatif) dan sisi sitosol (sisi positif) karena potensial membran antara dua sisi tersebut. Sisi ruang antar membran dikatakan sisi sitosol karena dapat dicapai oleh hampir semua molekul kecil dalam sitosol. ATP dan ADP tidak berdifusi bebas melintasi membran dalam mitokondria. Suatu protein transport spesifik, ATP-ADP translokase (pembawa adenin nukleotida), memungkinkan molekul yang tinggi muatan ini menyebrangi sawar permeabilitas membran dalam mitokondria. Aliran ATP dan ADP terangkai secara antiport, ADP masuk matriks bila ATP keluar matriks mitokondria, dan sebaliknya. Pertukaran ATPADP sangat banyak mengunakan energi, kurang lebih seperempat energi yang dihasilkan pada transfer elektron melalui rantai pernapasan. Beberapa protein pengangkut atau pengemban mitokondria lain untuk ion dan metabolite bermuatan bekerja dengan cara simport dan antiport. Pengemban fosfat, bekerja bersama dengan translokase ATP-ADP, menyebabkan pertukaran antara Pi (sebagai ion H2PO4-) dengan OH- atau simport dari Pi dan H+. Kerjasama kedua pengangkut ini, menyebabkan pertukaran ADP dan Pi sitosol dengan ATP matriks, disertai masuknya satu H+. Pengemban dikarboksilat, memungkinkan malat, suksinat dan fumarat dikeluarkan dari mitokondria secara antiport dengan Pi. Pengemban trikarboksilat, mengangkut sitrat dan satu proton masuk mitokondria secara antiport dengan malat. Pengemban piruvat, membawa masuk piruvat dari sitosol kematriks mitokondria secara simport dengan H+ atau secara antiport dengan OH-. Pengangkut α ketoglutarat, membawa masuk α ketoglutarat secara antiport dengan malat. Protein-protein pengangkut mitokondria ini dan lebih dari lima yang lainnya mempunyai struktur yang sama. Membran dalam mitokondria bersifat permeabel bebas terhadap molekul kecil yang tidak bermuatan, seperti air, oksigen, CO2, NH3 ©2004 Digitized by USU digital library 7 dan asam monokarboksilat (seperti 3-hidroksibutirat, asetoasetat, dan asetat ), sedangkan asam lemak rantai panjang masuk mitokondria dengan pembawa karnitin. Kreatin fosfat mengangkut fosfat energi tinggi Gerakan ulang alik kreatin fosfat memungkinkan pemindahan cepat fosfat energi tinggi dari mitokondria kesitosol. Gerakan ini menguatkan fungsi kreatin fosfat sebagai pendapar energi dengan bekerja sebagai suatu sistem yang dinamis untuk pemindahan fosfat energi tinggi dari mitokondria pada jaringan yang aktif seperti otot jantung dan otot skelet. Jumlah ATP pada otot hanya mencukupi untuk menopang aktivitas produksi selama kurang dari satu detik. Otot vertebrata mengandung gudang fosfat energi tinggi dalam bentuk kreatin fosfat (fosfokreatin), yang dapat dengan mudah mentransfer fosfat energi tingginya ke ADP membentuk ATP. Kreatin fosfat mempertahankan konsentrasi ATP tinggi selama periode kerja otot. Kreatin kinase yang ada pada ruang antar membran mitokondria, mengkatalisa pemindahan fosfat energi tinggi dari ATP kepada kreatin. Selanjutnya, kreatin fosfat yang terbentuk diangkut kesitosol melalui porin (pori-pori protein) yang terdapat pada membran luar mitokondria. Isozym kreatin kinase yang berbeda mengantarai pemindahan fosfat energi tinggi ke dan dari berbagai sistem yang menggunakan atau menghasilkannya. CKa, kreatin kinase yang bertanggung jawab terhadap kebutuhan ATP yang besar, seperti kontraksi otot. CKc, kreatin kinase untuk mempertahankan keseimbangan antara kreatin dan kreatin fosfat, juga keseimbangan ATP dan ADP. CKg, kreatin kinase yang menggabungkan glikolisis pada kreatin untuk sintesa kreatin fosfat. Dan CKm, kreatin kinase mitokondria yang memperantarai pembentukan kreatin fosfat dari ATP yang terbentuk melalui fosforilasi oksidatif. Kreatin fosfat + ADP + H+ ⇔ ATP + kreatin, energi bebas standart hidrolisa kreatin fosfat adalah –10,3 kkal/mol, dibandingkan dengan hidrolisa ATP yang –7,3 kkal/mol maka, perubahan energi bebas standart pada pembentukan ATP dari kreatin fosfat adalah –3 kkal/mol. Potensial transfer fosforil kreatin fosfat yang lebih tinggi dari ATP, menyebabkan kreatin fosfat menjadi dapar fosfat energi tinggi yang sangat efektif. Kesimpulan 1. Reaksi berlangsung spontan bila terjadi pelepasan energi bebas (tG negatif) yaitu reaksi tersebut bersifat eksergonik, dan jika tG positif, reaksi hanya berlangsung bila diperoleh energi bebas, reaksi ini bersifat endergonik. 2. ATP adalah zat perantara penukar energi bebas, yang merangkaikan prosesproses yang bersifat eksergonik dengan proses-proses yang bersifat endergonik. 3. Enzym oksidase dan dehidrogenase memiliki peran utama dalam proses rantai pernapasan. 4. Komplek-komplek enzym dalam rantai pernapasan menggunakan potensial energi dari gradien proton untuk mensintesa ATP dari ADP dan Pi. Dengan demikian jelas terlihat bahwa rangkaian reaksi oksidasi terangkai erat dengan fosforilasi. 5. Terdapat sejumlah senyawa kimia yang dapat menghambat rangkaian reaksi oksidasi dan peristiwa fosforilasi atau memutus rangkaian oksidasi dan fosforilasi. 6. Terdapat protein pengangkut khusus untuk perlintasan beberapa ion dan metabolit pada membran mitokondria. ©2004 Digitized by USU digital library 8 DAFTAR PUSTAKA - Champe P C PhD, Harvey R A PhD. Lippincott’s Illustrated Reviews: Biochemistry 2nd .1994 : 61 – 72 - Lehninger A, Nelson D, Cox M M. Principles of Biochemistry 2nd 1993 : 364 - 394 - Murray R K, et al. Harper’s Biochemistry 25th ed. Appleton & Lange. America 2000 : 123 - 148 - Stryer L.1995. Biochemistry 4th : 184 – 187 ; 443 – 451 ; 488 – 498 ; 529 - 553 ©2004 Digitized by USU digital library 9