- Free Documents
advertisement

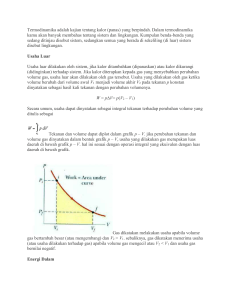
A. KONSEP DASAR TERMODINAMIKA . Sistem dan Lingkungan Sistem adalah sesuatu yang menjadi subjek pembahasan. Lingkungan adalah segala sesuatu yang berada diluar sistem. . KESETIMBANGAN Ada macam kesetimbangan dalam termodinamika a. kesetimbangan mekanis b. kesetimbangan termal c. kesetimbangan kimia Jika macam kesetimbangan itu terpenuhi, maka sistem berada dalam keadaan setimbang termodinamik. . KALOR Kalor merupakan energi yang berpindah akibat perbedaan suhu antara sistem dan lingkungannya. . USAHA DAN KAPASITAS KALOR Usaha gas dapat dihitung dengan persamaan W F x s F gaya. Gaya yang diberikan gas dapat ditentukan F dari hubungan p tekanan gas p A A luas penampang Jadi, W F x s W p A s atau W p A s A s V jadi, W p V W usaha J p tekanan N/m V perubahan volume m . KALOR JENIS Kalor jenis c adalah kapasitas kalor persatuan massa . C Rumus c atau Q mcT m . KAPASITAS KALOR MOLAR kapasitas kalor molar gas adalah banyaknya kalor yang diperlukan untuk manaikkan suhu mol gas sebesar K Ada macam kalor molar gas, yaitu a. kalor molar pada volume tetap CV,m b. Kalor molar pada tekanan tetap CP,m Rumus a. Kalor molar pada volume tetap CV,m ,, b. Kalor molar pada tekanan tetap CP,m ,, . TETAPAN LAPLACE Tetapan LAPLACE adalah perbandingan antara kapasitas kalor pada tekanan tetapCp dengan kapasitas kalor pada volume tetapCv. Proses termodinamika Ada proses perubahan kedaan termodinamika, yaitu a. Proses IRAVERSIBEL proses yang berlangsung secara spontan pada satu arah dan tidak dapat terjadi pada arah sebaliknya. b. Proses REVERSIBEL proses yang selalu berada dalam keadaan setimbang temodinamik. Proses termodinamik dapat berupa Pemuaian ekspansi Pemampatan kompresi Pemanasan Pendinginan Macammacam proses termodinamika . Proses Isotermal proses perubahan tingkat keadaan suatu gas yang berlangsung pada suhu tetap. Rumus . diagram pV untuk proses isotermal . Proses Isobarik Proses perubahan tingkat keadaan suatu gas yang berlangsung pada tekanan konsta. Rumus W pV V usaha yang dilakukan dalam proses isobarik . Proses Isokhorik Proses perubahan tingkat suatu gas yang berlangsung pada volume konstan. diagram proses isokhorik . Proses Adiabatik Proses perubahan tingkat keadaan sistem dimana selama proses tersebut tidak ada kalor yang masuk atau keluar dari sistem. Rumus diagram proses adiabatik Mesin Kalor Mesin kalor adalah mesin yang merubah energi panas menjadi energi mekanik. Energi mekanik diperoleh dari energi termal dengan membiarkan sejumlah kalor mengalir dari temperatur tinggi ke rendah. Rumus W Qh Qc W kerja mekanik Qh suhu tinggi Qc suhu rendah efisiensi kalor Skema mesin kalor Siklus Carnot Siklus Carnot adalah mesin kalor hipotesis yang beroprasi dalam suatu siklus reversibel. Mesin ini merupakan mesin kalor yang ideal, sehingga tidak mungkin digunakan di kehidupan nyata. Siklus carnot terdiri dari proses Isotermal dan proses adiabatik reversibel atau isentropik entropi konstan. Diagram proses siklus CARNOT MESIN PENDINGIN Mengalirkan kalor dari tempat dingin ke tempat panas. Suhu dalam mesin pendingin jauh lebih rendah dari pada suhu udara ruangan. Rumus skema mesin pendingin Contoh mesin pendingin Hukumhikum termodinamika Hukum I Termodinamika ketika kalor Q diberikan pada sistem, sebagian kalor yang diberikan digunakan untuk menaikkan energi dalam sebesar U, sedangkan sisanya keluar dari sistem ketika sistem itu melakukan usaha W terhadap lingkungannya Dirumuskan QUW Skema perjanjian HUKUM I TERMODINAMIKA Hukum II Termodinamika Faktanya, nilai efisiensi mesin kalor tak mungkin mencapai dan tidak mungkin bisa membuat mesin yang mengubah seluruh kalor Qh menjadi kerja W. Macammacam perumusan Hukum II Termodinamika . Perumusan Kelvin Planck adalah mustahil bagi sistem manapun untuk merubah seluruh kalor yang diserapnya darii reservoir suhu tinggi menjadi mekanik Faktanya, kita dapat menggerakkan mobil hanya dengan mendinginkan udara disekitar mobil. . Perumusan Clausius tidak mungkin membuat mesin yang kerjanya hanya menyerap kalor dari reservoir yang bersuhu rendah dan memindahkan kalor ini ke reservoir yang bersuhu tinggi tanpa adnya usaha dari luar Usaha dari luar misalnya energi listrik atau energi Mekanik. . Hukum II Termodinamika dalam bentuk Entropi Entropi adalah ukuran keteraturan atau ketidakteraturan suatu sistem. suatu proses hanya dapat terjadi jika tingkat ketidakteraturan suatu keadaan menuju ke tingkat ketidakteraturan yang lebih besar Rumus S Sakhir Sawal Proses REVESIBEL adalah proses ideal yang tak pernah terjadi di alam ini. Semua proses di alam semesta bersifat irevesibel sehingga entropi total alam semesta selalu meningkat. sebuah proses alami yang bermula dalam suatu keadaan kesetimbangandan berakhir dalam satu kesetimbangan lain akan bergerak dalam arah yang akan menyebabkan entropi sistem dan lingkungan akan bertambah atau tetap Sekian