Vitamin
advertisement

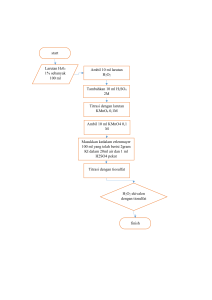
Laporan Praktikum Biokimia Hari/ tanggal Waktu PJP Asisten : Selasa/ 17 Desember 2013 : 13.00-14.40 WIB : Puspa Julistia Puspita, S. Si, M. Sc. : Resti Siti Muthmainah, S. Si. Lusianawati, S. Si. VITAMIN Kelompok 7 Ayu Septra Wulandari Yaya Nugraha Diana Agustini Raharja J3L112029 J3L112089 J3L112168 PROGRAM KEAHLIAN ANALISIS KIMIA PROGAM DIPLOMA INSTITUT PERTANIAN BOGOR BOGOR 2013 Pendahuluan Vitamin merupakan golongan senyawa organik sebagai pelengkap makanan yang sangat diperlukan oleh tubuh (Suhardjo 1886). Vitamin memiliki peran sangat penting untuk pertumbuhan, pemeliharaan kesehatan, dan fungsi-fungsi tubuh lainnya agar metabolisme berjalan normal. Vitamin dibagi menjadi dua golongan utama, yaitu vitamin yang larut dalam air yang meliputi vitamin B dan C, serta vitamin yang larut dalam lemak yang meliputi vitamin A, D, E, dan K (Poedjiadi 1994). Vitamin yang larut dalam air di sebut prakoenzim. Vitamin-vitamin ini dapat bergerak bebas dalam badan, darah, dan limfa. Vitamin yang larut dalam air mudah rusak dalam pengolahan dan mudah hilang atau terlarut bersama air selama pencucian bahan. Vitamin ini di dalam tubuh disimpan dalam jumlah terbatas dan kelebihan vitamin akan dikeluarkan atau diekskresikan melalui urin, oleh karena itu untuk mempertahankan saturasi jaringan vitamin ini harus sering dikonsumsi (Poedjiadi 1994). Golongan vitamin yang larut dalam lemak di sebut alosterin. Vitamin setelah diserap dalam tubuh akan disimpan dalam jaringan-jaringan lemak terutama hati. Vitamin-vitamin ini tidak diekskresikan, sehingga di dalam tubuh akan disimpan dalam jumlah banyak dan kemungkinan terjadinya toksisitas jauh lebih besar daripada vitamin yang larut dalam air (Poedjiadi 1994). Kebanyakan vitamin yang larut dalam air berperan sebagai kofaktor enzim tertentu dalam mengkatalisis berbagai reaksi biokimia. Vitamin A dan D mempunyai sifat menyerupai hormon, vitamin E memiliki sifat antioksidan, dan vitamin K diperlukan bagi biosintesis faktor pembekuan darah (Winarno 1984). Tujuan Percobaan dilakukan untuk menentukan kandungan vitamin C dalam tablet vitamin C dan sari buah jeruk dengan cara iodometri tidak langsung. Metode Bahan-bahan yang digunakan, yaitu tablet vitamin C, sari buah jeruk, akuades, H2SO4 2 N, iod 0,01 N, tiosulfat 0,01 N, dan indikator larutan pati. Alatalat yang digunakan, yaitu buret dan alat-alat gelas. Penentuan vitamin C dalam tablet. Sebanyak 50 mg sampel tablet vitamin C dilarutkan dalam 5 mL akuades dingin yang telah dididihkan dan diencerkan sebanyak 10 kali. Sebanyak 5 mL sampel yang telah diencerkan dimasukkan ke dalam erlenmeyer, ditambahkan dengan 3 mL H2SO4 2 N, dan 10 mL larutan iod 0,01N sehingga warnanya menjadi cokelat. Larutan dititrasi dengan tiosulfat 0,01 N sampai menjadi kuning kehijauan. Beberapa tetes indikator larutan pati ditambahkan ke dalam erlenmeyer sehingga warna yang terbentuk menjadi biru kehitaman dan dititrasi kembali sampai menjadi tidak berwarna. Larutan blanko (tanpa sampel) dikerjakan seperti sampel dan juga dititrasi dengan tiosulfat 0,01 N. Penentuan vitamin C dalam sari jeruk. Percobaan dilakukan seperti penentuan vitamin C dalam tablet untuk minuman sari jeruk sebanyak 5 mL. Hasil Berikut ini hasil yang diperoleh dari percobaan yang telah dilakukan pada penentuan kandungan vitamin C. Tabel 1 Data hasil penentuan kadar vitamin C dari sampel tablet dan sari jeruk Volume tiosulfat (mL) Volume Kadar vitamin C terkoreksi (mL) (mg) Awal Akhir Terpakai Blanko 0,00 9,40 9,40 Tablet 1 0,00 4,70 4,70 4,70 41,36 Tablet 2 0,00 4,60 4,60 4,80 42,24 Sari jeruk 1 5,30 10,40 5,10 4,30 37,84 Sari jeruk 2 4,60 9,90 5,30 4,10 36,08 Contoh perhitungan pada tablet 1: Volume terkoreksi = volume terpakai blanko – volume terpakai sampel = 9,40 mL – 4,70 mL = 4,70 mL Kadar vitamin C = volume terpakai x 0,88 mg/mL x faktor pengenceran = 4,70 mL x 0,88 mg/mL x 10 = 41,36 mg Bahan Pembahasan Vitamin C termasuk vitamin yang larut dalam air. Vitamin C atau asam askorbat merupakan asam gula yang banyak terdapat pada buah-buahan. Vitamin C dapat membantu menjaga daya tahan tubuh terhadap penyakit. Struktur vitamin C dapat dilihat pada gambar 1. Gambar 1 Struktur Vitamin C (Hart 2003) Sumber vitamin C terbaik ialah berasal dari sayuran dan buah-buahan seperti melon, jeruk, stroberi, papaya, brokoli, belimbing, kubis, asparagus, dan aneka sayuran hijau. Penetapan kadar vitamin C dalam suatu bahan dapat dilakukan dengan cara titrimetri. Reaksi yang dijalankan dengan titrasi yaitu suatu larutan ditambahkan dari buret sedikit demi sedikit sampai jumlah zat-zat yang direaksikan tepat menjadi ekivalen. Ketika tampak telah ekivalen maka penambahan titran harus dihentikan yang di sebut dengan titik akhir titrasi. Larutan yang digunakan untuk menitrasi dan diletakkan dalam buret di sebut titran sedangkan larutan yang dititrasi oleh penitran di sebut dengan titrat (Harjadi 1993). Titrasi redoks dapat dibedakan menjadi beberapa cara berdasarkan pemakaiannya, yaitu Na2S2O3 sebagai titran yang di sebut juga dengan iodometri tidak langsung, I2 sebagai titran yang di sebut juga dengan iodometri langsung, suatu oksidator kuat sebagai titran dengan oksidator kuat dapat berupa KMnO4, K2Cr2O7, atau Ce (IV), serta suatu reduktor kuat sebagai titran (Harjadi 1993). Percobaan yang dilakukan merupakan titrasi redoks dengan metode iodometri tidak langsung yang menggunakan Na2S2O3 sebagai titran. Penambahan larutan H2SO4 dilakukan terlebih dahulu sebelum larutan iod pada pembuatan titrat untuk membuat larutan iod tidak mengalami oksidasi. Vitamin C atau asam askorbat (C6H8O6) ditambahkan dengan larutan iod berlebih, kemudian vitamin C dioksidasi oleh I2 dengan reaksi dapat dilihat pada gambar 2. C6H8O 6 + I2 C6H6O 6 + 2HI Gambar 2 Reaksi vitamin C dengan larutan iod (Khoplar 1990) Sisa I2 yang tidak bereaksi dengan asam askorbat kemudian dititrasi dengan tiosulfat dengan reaksi dapat dilihat pada gambar 3. 2Na2S2O3 + I2 Na 2S4O6 + 2NaI Gambar 3 Reaksi tiosulfat dengan sisa larutan iod (Khopkar 1990) Reaksi tiosulfat dengan larutan iod berjalan cepat dan bersifat unik karena oksidator lain tidak mengubah S2O32- menjadi S4O62- melainkan menjadi SO32seluruhnya atau sebagian menjadi SO42-. Titrasi dapat dilakukan tanpa indikator dari luar, karena warna I2 yang dititrasi itu akan lenyap jika titik akhir tercapai. Warna mula-mula yaitu cokelat agak tua menjadi lebih muda, kemudian kuning, kuning muda, dan seterusnya sampai akhirnya lenyap. Jika diamati dengan cermat perubahan warna tersebut, maka titik akhir dapat ditentukan dengan cukup jelas, namum lebih mudah dan lebih tegas jika ditambahkan amilum ke dalam larutan sebagai indikator. Amilum dengan I2 membentuk suatu kompleks berwarna biru kehitaman yang masih sangat jelas sekalipun I2 sedikit sekali. Larutan iod yang terikat hilang bereaksi dengan titran pada titik akhir sehingga warna biru lenyap mendadak dan perubahan warnanya tampak sangat jelas. Penambahan amilum ini harus menunggu sampai mendekati titik akhir titrasi, yaitu jika iod sudah tinggal sedikit yang tampak dari warnanya yang kuning muda atau kuning kehijauan. Tujuannya ialah agar amilum tidak membungkus iod dan menyebabkan sukar lepas kembali. Hal ini akan berakibat warna biru sulit sekali lenyap sehingga titik akhir tidak kelihatan tajam lagi. Jika iod masih banyak sekali maka dapat menguraikan amilum dan hasil penguraian ini mengganggu perubahan warna pada titik akhir. Titrasi harus dilakukan dengan cepat untuk meminimalisasi terjadinya oksidasi iodida oleh udara bebas. Pengocokan pada saat melakukan titrasi iodometri tidak langsung dilakukan untuk menghindari penumpukan tiosulfat pada area tertentu. Penumpukan konsentrasi tiosulfat dapat menyebabkan dekomposisi tiosulfat untuk menghasilkan belerang. Reaksi terbentuknya belerang dan larutan menjadi bersifat koloid karena keruh oleh kehadiran belerang dapat dilihat pada gambar 4. 2- S2O3 + 2H+ H2SO3 +S Gambar 4 Reaksi tiosulfat ketika tidak dilakukan pengocokan (Khopkar 1990) Titrasi larutan blanko dilakukan untuk menentukan jumlah I2 total yang bereaksi dengan tiosulfat. Titrasi pada larutan sampel dengan tiosulfat menunjukkan jumlah I2 yang tidak bereaksi dengan vitamin C, sehingga jumlah I2 yang bereaksi dengan vitamin C dapat diketahui dari selisih antara volume larutan blanko dengan volume tiosulfat yang terpakai untuk sampel. Kadar vitamin C pada tablet dan sari buah jeruk didapatkan dari selisih antara volume titran pada larutan blanko dengan volume titran sampel yang kemudian dikalikan dengan 0,88 mg/mL dan dikalikan dengan faktor pengencerannya. Nilai 0,88 mg/mL menunjukkan bahwa 1 mL tiosulfat 0,01 N setara dengan 0,88 mg vitamin C dalam 1 mL. Berdasarkan stoikiometri, jika 1 mL tiosulfat dengan konsentrasi 0,01 N maka 1 mL vitamin C memiliki konsentrasi 0,01 N. Nilai 0,01 N vitamin C dengan melakukan konversi satuan maka akan diperoleh kadar vitamin C sebesar 0,88 mg dengan perhitungan dapat dilihat pada gambar 5. Gambar 5 Perhitungan untuk memperoleh 0,88 mg vitamin C Berdasarkan hasil percobaan diperoleh kadar vitamin C pada tablet 1 dan tablet 2 kurang dari 50 mg per tablet dengan yang tertera pada kemasan tablet vitamin C. Hal ini dikarenakan vitamin C mudah teroksidasi. Tempat pengemasan pada tablet vitamin C tidak tertutup rapat atau transparan sehingga cahaya mudah masuk, akibatnya kadar vitamin C dapat berkurang akibat teroksidasi. Sari buah jeruk 1 dan 2 lebih besar dari 35,71 mg per 5 mL minuman sari buah jeruk. Minuman sari buah jeruk yang tertera pada kemasan mengandung 1000 mg vitamin C dalam 140 mL yang menunjukkan terdapat 35,71 mg vitamin C dalam 5 mL. Hasil yang diperoleh lebih besar dibandingkan dengan yang tertera di kemasan yang dapat disebabkan oleh adanya kealahan dalam melakukan titrasi, seperti penambahan titran yang berlebih sehingga terjadi kesalahan titrasi positif. Penentuan kadar vitamin C dalam suatu bahan terutama produk makanan maupun minuman ini sangat penting dalam bidang industri agar kadar vitamin C yang tedapat di dalam suatu produk dapat memenuhi kebutuhan akan vitamin C yang diperlukan oleh konsumen. Kebutuhan akan vitamin C diperlukan, karena vitamin C berperan penting dalam oksidasi fenilalanina menjadi tirosin, mereduksi ion feri menjadi fero dalam saluran pencernaan, mengubah asam folat menjadi bentuk aktif asam folinat, serta sintesis hormon-hormon steroid dari kolesterol. Penyakit atau gejala yang tampak yang disebabkan oleh defisiensi vitamin C di antaranya skorbut, pendarahan gusi, mudah terjadi luka dan infeksi tubuh, dan jika sudah terjadi sukar disembuhkan. Selain itu, terjadinya hambatan pertumbuhna pada bayi dan anak-anak, pembentukan tulang yang tidak normal pada bayi dan anak-anak, serta kulit mudah mengelupas. Vitamin sangat penting bagi tubuh, akan tetapi apabila kelebihan ataupun kekurangan vitamin ini memiliki dampak buruk bagi kesehatan tubuh. Vitamin A memiliki fungsi untuk melindungi mata, membangun sel-sel kulit, menjaga tubuh dari infeksi, membatu pertumbuhan tulang dan gigi. Sumber-sumber vitamin A dapat diperoleh dari ikan, telur, susu, hati, daging sapi, wortel, labu, dan bayam. Dampak kekurangan vitamin A ialah adanya gangguan pada mata, rentan terhadap penyakit infeksi, dan masalah pada kulit, sedangkan dampak kelebihan vitamin A ialah menimbulkan keracunan, kerusakan hati, kelelahan, nyeri persendian, dan kulit kering. Vitamin B kompleks yaitu B1, B2, B3, B6, dan B12 memiliki manfaat yang cukup besar untuk metabolisme pembentukan energi yang diperlukan sel-sel otak seperti menjaga kesehatan, mendorong nafsu makan, memproduksi energi, membantu pembentukan antibody dan saraf, meningkatkan nafsu makan, mencegah anemia, menjaga kesehatan jantung, serta meningkatkan kekebalan tubuh. Sumber-sumber vitamin B di antaranya padi-padian, daging, makanan laut, ungags, produk susu, telur, brokoli, kacang-kacangan, dan produk fermentasi kedelai. Dampak kekurangan vitamin B di antaranya mudah terjangkit penyakit beri-beri, mudah terjena infeksi, masalah kulit, diare, dermatitis, sariawan, nafsu makan turun, mengganggu sustem syaraf dan daya ingat, anemia, serta cepat lelah, sedangkan kelebihan vitamin ini maka tubuh akan membuangnya bersama urin. Dampak terburuk dari kelebihan vitamin yaitu dapat mengakibatkan kerusakan saraf seperti lumpuh, mati rasa, dan gagal ginjal. Vitamin D memiliki manfaat di antaranya meningkatkan penyerapan kalsium dan fosfor yang berguna untuk kekuatan tulang dan gigi, mengatur kadar kalsium dalam darah, dan mengatur produksi hormon. Sumber-sumber vitamin D di antaranya produk susu, minyak ikan, tempe, tahu, telur, dan sinar matahari pagi. Dampak kekurangan vitamin D ialah masalah pada tulang dan gigi serta masalah pertumbuhan, sedangkan dampak kelebihan vitamin D di antaranya nyeri tulang, lemah otot, mual, cepat lelah, dan kehilangan nafsu makan. Vitamin E memiliki manfaat untuk kesehatan kulit, melindungi tubuh dari radikal bebas, mengurangi risiko penyakit jantung dan kanker, serta menguatkan sel darah merah. Sumber vitamin E di antaranya kacang-kacangan, sayur, gandum, ikan, susu, dan alpukat. Dampak kekurangan vitamin E di antaranya merusak imunitas tubuh dan memperlambat perkembangan syaraf otot, sedangkan dampak kelebihan vitamin E di antaranya hipertensi, lemah otot, dan mudah terkena risiko pendarahan dalam tubuh. Simpulan Berdasarkan percobaan yang telah dilakukan dapat disimpulkan bahwa kandungan vitamin C dalam tablet 1 sebesar 41,36 mg dan tablet 2 sebesar 42,24 mg per tablet, sedangkan kandungan vitamin C dalam minuman sari jeruk 1 sebesar 37,84 mg dan minuman sari jeruk 2 sebesar 36,08 mg dalam 5 mL minuman sari jeruk. Daftar Pustaka Harjadi W. 1993. Ilmu Kimia Analitik Dasar. Jakarta: Gramedia Pustaka Utama. Hart H, Leslie EC, David JH. 2003. Kimia Organik. Achmadi SS, penerjemah; Jakarta: Erlangga. Terjemahan dari: Organic Chemistry. Ed. Ke-11. Khopkar SM. 1990. Konsep Dasar Kimia Analitik. Saptorahardjo A, penerjemah; Jakarta: UI Press. Terjemahan dari: Basic Concepts of Analytical Chemistry. Poedjiadi A. 1994. Dasar-Dasar Biokimia. Jakarta: UI Press. Suharjdo. 1886. Pangan, Gizi, dan Pertanian. Jakarta: UI Press. Winarno FG. 1984. Kimia Pangan dan Gizi. Jakarta: Gramedia Pustaka Utama.