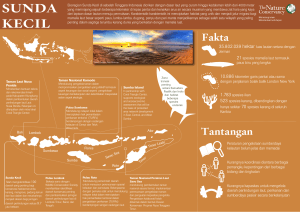
③ laut dan atmosfer sebagai suatu sistem geokimia
advertisement

① PENDAHULUAN P engetahuan geokimia berasal dari dua buah disiplin ilmu yaitu ilmu geologi dan kimia, tetapi bukan merupakan penggabungan ilmu, namun geokimia merupakan disiplin ilmu yang membantu menjelaskan fenomena geologi yang terjadi. Dengan perkataan lain, pengetahuan mengenai bumi yang dilihat dari aspek kimianya. Nah, untuk itu, tentu saja kita harus mengerti dan memahami ilmu geologi lebih dahulu. Halmana “geology”, adalah ilmu yang mempelajari segala sesuatu yang berkenan dengan gejala-gejala yang terjadi di bumi, baik yang diakibatkan oleh gerakan bumi maupun penyusunan kimia di alam secara mandiri. Intinya geologi (geo=bumi dan logos= ilmu/pengetahuan), yakni pengetahuan bumi yang menyelidiki struktur bumi dengan tiga lapisan, yaitu kerak bumi, mantel dan inti bumi. Ketiga lapisan ini memiliki struktur-lapisan yang berbeda dengan didominasi oleh unsur kimia tertentu. Jadi dengan perkataan lain geologi adalah pengetahuan tentang susunan zat yang terbentuk dari bumi. Bahkan geologi pun merupakan pengetahuan yang mempelajari sejarah perkembangan bumi serta mahkluk yang pernah hidup di bumi. Oleh karenanya geologi itu sendiri terdiri dari banyak cabang juga, seperti: Mineralogi, Petrologi (petros=batuan dan logos= ilmu),Palaentologi (palaios=purba, ontos=mahkluk), sedimentologi, geomorfologi, geofisika, geokimia dan geoteknik. Geokimia ialah pengetahuan yang mempelajari bentuk,sifat dan fungsi serta aksi- reaksi kimia alam yang ada ~1~ di bumi. Hakikinya, Geokimia adalah ilmu yang mempelajari kandungan unsur dan isotop dalam lapisan bumi, terutama yang berhubungan dengan kelimpahan (abundant), penyebaran serta hukum-hukum yang mengaturnya. Dari dasar ini berkembang beberapa cabang ilmu geokimia di antaranya, geokimia panas bumi, geokimia mineral, geokimia petroleum dan geokimia lingkungan. Buku yang ditulis ini akan menguraikan tentang geokimia laut, pengetahuan ini dipandang penting pada dekade belakang ini, dikarena ilmuan dunia dan ahli ekonomi berpandangan bahwa laut memiliki sumberdaya alam yang menjamin keberlangsungan hidup manusia di muka bumi. Para ahli geologi berasumsi bahwa zat besi adalah unsur kimia terbesar pada lapisan bumi. Logam ini terpusat di inti bumi. Senyawa magnesium silikat, yang mengandung magnesium, silikon, dan oksigen, menjadi penyusun utama lapisan mantel. Sebagian besar dari unsur-unsur penyusun tersebut telah tercipta di ruang angkasa sejak jutaan tahun silam. Gambar 1.1 memperlihatkan secara global komposisi kimia penyusun bumi. Dimana zat besi mendominasi meliputi 35% dari total zat kimia di bumi, zat besi ini di dalamnya juga ada kobalt dan mangan. Oleh karenanya di kerak samudera gabungan antara besi dan mangan disebut sebagai kerak kobalt yang kaya akan Fe-Mn. Oksigen menduduki posisi kimia kedua terbanyak sesudah besi, hal itu menunjukan diplanit bumi terdapat banyak makhluk hidup dan proses fotosintesis oleh butir hijau daun yang memproduksi oksigen cukup berpolah. Kemudian urutan komposisi kimia penyusun bumi terbesar sampai terkecil adalah magnesium (Mg) meliputi 17%, silikon (13%), ~2~ nikel (2,7%), belerang (2,7%), kalsium (0,6%), aluminium (0,4%) dan unsur-unsur lain. Gambar 1.1. Komposisi Kimia Penyusun Kulit Bumi Buku yang disajikan ini akan membahas tentang geokimia yang meliputi : sejarah perkembangan ilmu geokimia; laut dan atmosfer merupakan suatu sistem geokimia; sumber-sumber material yang masuk laut; kesetimbangan thermodinamika; kinetika dan kristalisasi; kelarutan gas di laut; sedimen laut, air antara sedimen dan proses diagenesis; biomineralisasi; dan kerak kobalt di laut yang memiliki nilai ekonomis tinggi. Intinya dalam buku ini mengulas sifat kimia di laut, interaksi kimia dan faktor-faktor pembatas serta pembentukan sedimen yang berlangsung jutaan tahun silam. Kemudian bahasan tentang transpor/pemindahan zat kimia serta reaksi yang mungkin dan yang sudah terjadi. Pada dasarnya, geokimia dari sudut ilmu, banyak membicarakan ~3~ tentang perubahan kimia secara alamiah bertalian dengan prinsip termodinamika dan kinetika reaksi kimia. Praktisnya geokimia berasal dari pengetahuan geologi dan kimia, kemudian para ahli seperti: Georg Bauer dan Nicolas Steno (1800-an) memperluas kedua pengetahuan ini untuk tujuan meneliti kejadian-kejadian di bumi selain secara fisika tetapi reaksi kimia yang terjadi. Dalam pengembangan ilmu ini turut terlibat para ahli geologi, kimiawan, fisikawan, metematikawan dan para ahli biologi. Lahirnya geokimia sebagai cabang ilmu geologi baru menyebabkan munculnya metoda dan data observasi baru mengenai berbagai hal yang banyak menarik perhatian para ahli sedimentologi dan mineralogi. Sebagian besar riset geokimia pada mulanya diarahkan pada riset kuantitatif untuk mengetahui penyebaran unsur-unsur kimia di alam, termasuk penyebarannya dalam pebatuan sedimen. Lambat laun data tersebut menuntun para ahli untuk memahami apa yang disebut sebagai siklus geokimia (geochemical cycle) serta penemuan hukum-hukum yang mengontrol penyebaran unsur dan proses-proses yang menyebabkan timbulnya pola penyebaran unsur seperti nikel, kobalt, mangan, besi, logam mulia, silicon, karbon, magnesium, kalsium, karbonat dan sebagainya. Berkembangnya kimia moderen pemahaman geokimia makin meluas dan pemanfaatannya makin signifikan, sehingga mereka berasumsi bahwa perbedaan ketiga habitat, yaitu lautan, atmosfer dan daratan hanya dipisahkan oleh sebaran, komposisi dan reaksi kimia saja. Bahkan dalam analisa mereka ketiga habitat ini memiliki mahkluk hidup berbeda. Pengetahuan itulah sampai saat ini tetap diakui kehidupan yang ada di laut, darat dan atmosfir berbeda sifat ~4~ dan bentuknya. Pembentukan kimia yang terjadi di ketiga habitat tersebut menjadikan sebagai objek riset yang sangat strategis dan bermanfaat bagi umat manusia. Baru-baru ini, kimia nuklir (nuclear chemistry) menyumbangkan sebuah “jam” dan “termometer” yang pada gilirannya membuka era riset baru terhadap sedimen. Unsurunsur radioaktif, khususnya 14C dan K, memungkinkan dilakukannya metoda penanggalan langsung terhadap batuan sedimen tertentu. Metoda 14C, yang dikembangkan oleh Libby, dapat diterapkan pada endapan resen. Metoda 40K/40Ar terbukti dapat diterapkan pada glaukonit, felspar autigen, mineral lempung, dan silvit yang ditemukan dalam endapan tua. Analisis isotop dapat digunakan untuk menentukan temperatur purba. Metoda Urey—berdasar-kan nisbah 16 O/18O yang merupakan fungsi dari temperatur—dapat dipakai untuk menaksir temperatur pembentukan cangkang fosil yang ada dalam endapan di laut. Meskipun “jam” dan “termometer” tersebut masih memperlihatkan kekeliruan, namun harus diakui bahwa keduanya telah memberikan kontribusi yang berarti terhadap pembelajaran sedimentasi dan sedimen. Van’t Hoff adalah orang pertama yang memanfaatkan azas fasa untuk mempelajari kristalisasi larutan garam dan pembentukan endapan garam. Mulanya penelitian eksperimental terhadap campuran yang dapat menghasilkan kristal, terutama sistem silikat pada temperatur tinggi, dilakukan oleh para ahli petrologi batuan beku dan metamorf. Baru pada beberapa dasawarsa terakhir ini saja, hal itu menarik perhatian para ahli sedimentologi. Sebagai contoh, Carmichael dan Eugster (1987) memakai cara itu untuk meneliti endapan non-marin dan mineral-mineral yang ~5~ mencirikan pembentukan sungai hijau di Wyoming dan Colorado. Zen (1959) menunjukkan bahwa azas fasa yang diajukan oleh Gibbs dapat diterapkan untuk menganalisis hubungan antara mineral lempung dan mineral karbonat. Hasil penelitian Zen kemudian diterapkan oleh Peterson (1962) terhadap larutan karbonat di bagian timur Tennessee. Perkembangan metoda yang relatif baru itu dapat dibaca dalam karya tulis Eugster (1971). Berbagai kajian teoritis dan eksperimental tentang stabilitas mineral pada berbagai kondisi oksidasi-reduksi (Eh) dan pH dilakukan oleh Garrels dan beberapa ahli lain (Garrels dan Christ, 1965). Penelitian aspek-aspek geokimia sedimen banyak menambah pengertian kita tentang endapan sedimen. Buku-buku yang membahas tentang topik-topik geokimia sedimen antara lain adalah Geochemistry of Sediments karya Degens (1965) dan Principles of Chemical Sedimentology karya Berner (1971). Aplikasi atau contoh nyata yang dapat dilihat dari geokimia salah satunya adalah metode yang digunakan oleh sedimentologist dalam mengumpulkan data dan bukti pada sifat dan kondisi depositional batuan sedimen, yaitu analisis kimia dari pebatuan, melingkupi geokimia isotop, termasuk penggunaan penanggalan radiometrik, untuk menentukan usia batu, dan kemiripan dengan daerah sumber. Metode ini pertama kali dipakai pada tahun 1970-an dimana penelitian sedimentologi mulai beralih dari makroskopis dan fisik ke arah mikroskopis dan kimia. Dengan perkembangan teknik analisa dan penggunaan katadoluminisen dan mikroskop elektron memungkinkan para ahli sedimentologi mengetahui lebih baik tentang aspek geokimia. Perkembangan yang pesat ini memacu kita untuk mengetahui hubungan antara diagenesis, pori-pori dan pengaruhnya ~6~ terhadap evolusi porositas dengan kelulusan batupasir dan batugamping. Saat ini berkembang perbedaan antara makro sedimentologi dan mikro sedimentologi. Makro sedimentologi berkisar studi fasies sedimen sampai ke struktur sedimen. Di sisi lain, mikro sedimentologi meliputi studi batuan sedimen di bawah mikroskop atau lebih dikenal dengan petrografi. Akhir-akhir ini riset dan pengamatan terhadap sumber minyak bumi dilakukan pendekatan dengan prinsip geokimia. Dalam pidato ilmiah saudara Dr. Eddy Ariyono Subroto pada tanggal 30 September 2011, disaat pengukuhan sebagai Guru Besar Fakultas Ilmu dan Teknologi Kebumian (FITB) institut teknologi Bandung, Dengan pidato ilmiah yang berjudul "Peran Geokimia Petrolium Dalam Usaha Eksplorasi Migas di Indonesia". Dia menjelaskan, kebutuhan energi di dunia semakin meningkat tajam, tak terkecuali di Indonesia. Untuk mengatasi hal tersebut, pemerintah juga menggali potensi energi dari yang tidak konvensional. Eksplorasi energi tersebut menjadikan ilmu geokimia sebagai ilmu yang penting dan sangat diperlukan. Tahun 2008 penulis menjadi salah seorang delegasi RI pada konfrensi “International Seabed Authority/ISA” di Kingston, Jamaica. Disaat itu ada sesi seminar tentang mineral dan nodul polimetalik di dasar laut. Dalam seminar itu terungkap begitu besar nilai ekonomi yang terkandung pada kerak kobalt yang kaya akan ferromanganese. Dalam diskusi terungkap bahwa untuk mengeksplorasi dan eksploitasi kerak samudera itu di perlukan pengetahuan geokima, agar zat kimia secara individu dapat diprakirakan nilai ekonominya dengan pasti. ~7~ Ilmu geokimia sendiri kemudian terus berkembang, sehingga tidak saja berupa ilmu tradisional atau ilmu yang mendasarkan analisisnya dari data kualitatif, tetapi juga menjadi arah kuantitatif. Saat ini muncullah pemodelan cekungan (basin modelling) berbasis geokimia. Dengan adanya pemodelan ini, ilmu geokimia berperan semakin signifikan. Dia lebih pertegas lagi, Jika di masa lampau suatu pemboran boleh dilakukan hanya dengan justifikasi ilmu geofisika, maka sekarang keikutsertaan ilmu geokimia sudah menjadi keharusan. Dengan demikian pengetahuan geokimia akan makin berperan dalam menentukan potensi sumberdaya alam secara kuantitatif maupun kualitatif. Para ilmuan dunia mengakui bahwa Indonesia adalah negara kepulauan terbesar di dunia, sehingga dalam konferensi PBB pada tanggal 10 Desember 1982 di Montego Bay Jaimaika yang dikenal sebagai United Nations Convention on the Law of the Sea/UNCLOS ke III memutuskan Indonesia sebagai “archipelago State”. Karena memiliki ribuan pulau dengan garis panjang pantai 95.181 km2. Keberdaan sebagai negara kepulauan menunjukan Indonesia memiliki wilayah laut lebih luas dari wilayah daratan (kontinental), implikasinya kekayaan alam di laut lebih banyak dari di daratan. Kekayaan yang dimiliki di laut tidak hanya hayati dan nir-hayati yang ada di badan air tetapi mineral yang ada di dasar laut dan di tanah bawah dasar laut sangat berpolah. Pengajaran geokimia laut sangat berarti bagi para pemangku kepentingan di laut (stakeholder) baik dosen, mahasiswa, pengusaha tambang, pembisnis dan para pengambil kebijakan. Karena pengetahuan dasar tentang geokimia laut sangat membantu kelancaran dalam rangka ~8~ prediksi potensi, kegiatan riset, peluang usaha dan kemungkinan peristiwa alam yang akan terjadi di laut. Berbicara geokimia laut tidak terlepas dari pembahasan mineral, baik yang terkandung dalam air laut maupun “seabed minerals”. Kandungan mineral yang ada di landas kontinen wilayah perairan laut Indonesia sangat berlimpah baik jenis maupun jumlah. Analisis ekonomi (suatu prediksi) mineral yang ada di dasar laut dan tanah di bawah dasar laut memiliki nilai ± 330 miliar US$ (Rompas dkk, 2013). Diterbitkan buku ini merupakan salah satu usaha mempercepat pembangunan ekonomi di Indonesia dan akan menambah khazanah berpikir bagi para ilmuan kelautan, geologi dan pembisnis tambang. Disamping itu buku ini menjadi bahan bacaan bagi para mahasiswa dan para dosen. Barangkali buku ini dapat juga dijadikan buku ajar di perguruan tinggi sekaligus berperan buku pinter bagi siswa dan mahasiswa. Tidak berlebihan dapat disimpulkan bahan bacaan ini merupakan bahan bacaan yang langka atau kurang ilmuan Indonesia menulisnya. ~9~ ② SEJARAH PERKEMBANGAN ILMU GEOKIMIA B erjalannya waktu dan sejarah mengajarkan kepada kita, bahwa kemajuan suatu negara termasuk kemajuan budaya sangat tergantung pada keberadaan kekayaan sumberdaya alam dari negara tersebut. Sebagian besar dari kekayaan itu terdapat di dalam bumi, lapisan-lapisan batuan yang ada dalam bumi termasuk dalam nodule yang ada di dasar laut dan tanah dasar laut berguna bagi kehidupan manusia. Bahkan di badan air proses kimia mineral yang berinteraksi dengan aspek biologi dapat mendatangkan energi untuk keperluan hidup manusia, oleh karenanya ada bagian ilmu yang membahas khusus untuk itu, yaitu disebut “biogeokimia”. Sebelum masuk ke pengetahuan dan perkembangan geokimia, kita ketahui lebih dahulu bagaimana bumi yang kita tempati, struktur lapisannya dan zat-zat apa yang mendominasinya. Bumi tempat kita tinggal saat ini merupakan salah satu anggota tata surya dengan matahari sebagai pusatnya. Jarak bumi dengan matahari sekitar 150 juta km. Bumi berbentuk bulat pepat dengan jari-jari ± 6.370 km. Bumi merupakan planet dengan urutan ketiga dari delapan planet yang dekat dengan matahari. Bumi diperkirakan telah terbentuk sekitar 4,6 milyar tahun yang lalu, dan merupakan satu-satunya planet yang dapat dihuni oleh berbagai jenis mahluk hidup. Permukaan bumi terdiri dari daratan dan lautan. Jika bumi ~ 10 ~ diiris maka akan tampak lapisan-lapisan seperti pada gambar di bawah ini : Gambar 2.1 Struktur lapisan bumi Sumber: Ensiklopedia Lapisan bumi dibagi menjadi tiga bagian, yaitu sebagai berikut : 1.) Kerak bumi Kerak bumi adalah lapisan terluar bumi yang terbagi menjadi dua kategori, yaitu kerak samudera dan kerak benua. Kerak samudera mempunyai ketebalan sekitar 5-10 km sedangkan kerak benua mempunyai ketebalan sekitar 20-70 km. Tebal lapisan kerak bumi mencapai 70 km dan merupakan lapisan tanah dan batuan .Lapisan ini menjadi tempat tinggal bagi seluruh mahluk hidup. Suhu di bagian bawah kerak bumi mencapai 1.100 derajad Celcius. Lapisan ~ 11 ~ kerak bumi dan bagian di bawahnya hingga kedalaman 100 km dinamakan litosfer. Unsur-unsur kimia utama pembentuk kerak bumi adalah: Oksigen (46,6%), Silikon (27,7%), Aluminium (8,1%), Besi (5,0%), Kalsium (3,6%) Natrium (2,8%), Kalium (2,6%) dan Magnesium (2,1%). Unsur–unsur tersebut membentuk satu senyawa yang disebut dengan batuan (Skinner dan Brian, 1976). 2.) Selimut atau Selubung Mantel. Selimut merupakan lapisan yang terletak di bawah lapisan kerak bumi. Lapisan ini dikenal juga sebagai lapisan Pyrosphere. Tebal selimut bumi mencapai 2.900 km dan merupakan lapisan batuan padat. Suhu di bagian bawah selimut bumi mencapai 3.000 derajat Celcius. Mantel ini terdiri dari besi dan mineral SIMA. Density sekitar 3.5 SG. Tekanan dari lapisan diatasnya membuat lapisan ini selalu dalam kondisi solid, tapi tetap bisa melelehkan batuan. Lapisan mantle paling luar sekitar 200 km dinamai dengan asthenosphere. Pada lapisan ini tekanan dan suhu berada pada kondisi berimbang sehingga lapisan ini bersifat plastis. 3.) Inti Bumi. Inti bumi terdiri dari material cair, dengan penyusun utama logam besi (90%), nikel (8%), dan lain-lain yang terdapat pada kedalaman 2900–5200 km. Lapisan ini dibedakan menjadi lapisan inti luar dan lapisan inti dalam. Lapisan inti luar tebalnya sekitar 2.000 km dan terdiri atas besi cair yang suhunya mencapai 2.200 oC. Inti dalam merupakan pusat bumi berbentuk bola dengan diameter sekitar 2.700 km. Inti dalam ini terdiri dari nikel dan besi yang suhunya mencapai 4500oC. ~ 12 ~ Berdasarkan penyusunnya lapisan bumi terbagi atas litosfer, astenosfer, dan mesosfer. Litosfer adalah lapisan paling luar bumi (tebal kira-kira 100 km) dan terdiri dari kerak bumi dan bagian atas selubung. Litosfer memiliki kemampuan menahan beban permukaan yang luas misalkan gunungapi. Litosfer bersuhu dingin dan kaku. Di bawah litosfer pada kedalaman kira-kira 700 km terdapat astenosfer. Astenosfer hampir berada dalam titik leburnya dan karena itu bersifat seperti fluida. Astenosfer mengalir akibat tekanan yang terjadi sepanjang waktu. Lapisan berikutnya mesosfer. Mesosfer lebih kaku dibandingkan astenosfer namun lebih kental dibandingkan litosfer. Mesosfer terdiri dari sebagian besar selubung hingga inti bumi. Permukaan bumi ini terbagi atas kira-kira 20 pecahan besar yang disebut lempeng. Ketebalannya sekitar 70 km. Ketebalan lempeng kira-kira hampir sama dengan litosfer yang merupakan kulit terluar bumi yang padat. Litosfer terdiri dari kerak dan selubung atas. Lempengnya kaku dan lempeng-lempeng itu bergerak diatas astenosfer yang lebih cair. Arus konveksi memindahkan panas melalui zat cair atau gas, yang membuat lempeng-lempeng dapat bergerak, yang dapat menimbulkan getaran yang terjadi dipermukaan bumi. Pergerakan dan pembentukan senyawa kimia pada lapisan-lapisan tersebut yang terjadi secara alamiah merupakan dasar utama pengembangan ilmu geokimia. Dengan mengetahui jenis lapisan dan ketebalannya maka sudah dapat prakirakan besaran potensi enerji, mineral dan gas yang tersedia di bumi. Perkembangan geokimia, historisnya diawali dari sejarah perkembangan geologi, dimana pengetahuan purbakala apa yang terjadi di muka bumi selalu dihubungkan ~ 13 ~ dengan kepercayaan tahyul. Misalnya peristiwa gempa bumi yang terjadi di daerah pedalaman Afrika, bangsa Mozambigue beranggapan bahwa bumi karena kedinginan dan demam. Demikian juga penduduk pedalaman di Peru (Amerika Selatan) menduga gempabumi yang terjadi karena dewa bumi sedang menari. Semua anggapan-anggapan itu digugurkan dengan munculnya ahli geologi, seperti Hution (1726-1729); Cuvier (1830) dan Lyell (1830). Para ahli geologi menjabarkan secara jelas perkembangan evolusi bumi dan peristiwa di bumi adalah akibat gerakan bumi yang mengelilingi matahari. Gerakan bumi ini berjalan lambat tetapi dapat memisahkan pulau yang satu dengan yang lain. Pengetahuan “geologi” menceritakan segala fosil-fosil sejak purbakala yang mendiami bumi, fosil-fosil itu merupakan sedimen yang terendap dalam waktu lama jutaan tahun silam, sehingga membentuk lapisan-lapisan keras sampai bisa terbentuknya pebatuan/kerak. Sedimen tersebut dapat berasal dari bahan mineral yang ada di atmosfir jatuh ke bumi dan ada juga makhluk hidup (flora dan fauna) yang mati dan mengendap sejak ribuan tahun silam. Sehingga dalam geologi dikenal lapisan strata menurut waktu pengendapan (periode). Seperti Prakambrium dan Kambrium. Istilah “Kambrium” menunjukan batuan-batuan yang tertua yang mengandung fosil berlimpah. Pembagian prakambrium dan kambrium, bertolak dari waktu nol, yaitu dihitung dari tahun kelahiran Jesus Kristus (Isa Al-masih). Periode prakambriun di asumsikan hanya satu lapisan batu tertua yang biasanya berada di bawah lapisan batuan yang berfosil (Katili dan Marks, 1959). Bertolak teori geologi pelbagai jenis pebatuan yang ada menurut stratifikasi, pembentukan lapisan itu tidak lepas dari ~ 14 ~ suatu reaksi kimia alam yang berlangsung lama. Reaksi kimia menjadikan sedimen yang mengeras jadi batu dikarenakan mengandung kapur (kalsium/Ca), silikat dan fosfat. Demikian pula karena fosil yang mengendap dari mahkluk hidup maka di dalamnya ada unsur karbon, misalnya teori minyak bumi menjelaskan bahwa minyak bumi itu terbentuk berasal dari fosil plankton yang mengendap cukup lama di kerak bumi. Karena pembentukan pebantuan, nodul (bongkahan) dan gas-gas yang ada di bumi akibat interaksi kimia satu dengan yang lain membentuk senyawa baru yang berfaedah bagi kehidupan, itulah pengetahuan geokimia. Oleh karenanya akar ilmu geokimia (geochemistry) adalah geologi dan kimia, kemudian dikembangkan oleh praktisi ilmuan, seperti Georg Bauer, Nicolas Steno dan beberapa ahli geologi. Mereka mempelajari sifat elemen kimia dan mengembangkan daya nalarnya untuk mengetahui proses reaksinya yang terjadi secara alamiah di bumi. Akhir abad ke 18 pengetahuan geologi dan kimia moderen tumbuh secara cepat, seorang ilmuan bernama Antoine Lavoisier menulis hasil risetnya dalam sebuah buku yang menceritakan keberadaan kimia yang masuk ke laut, atmosfir, tanah dan dipebatuan, dan terjadi modifikasi menjadi unsur kimia tertentu. Dasar temuan itu ilmu geokimia dikembangkan oleh ilmuan kimia moderen, antara lain: Humphry Davy dan John Dalton. Walaupun terjadi perdebatan serius oleh para ilmuan geologi, akhirnya mereka coba mempelajari sifat dan struktur kimia kristal serta timah dalam mineralogy. Awal memperkenalkan terminologi Geokimia adalah kimiawan Swiss CF Schonbein di tahun 1838, ilmu ini merupakan disiplin ilmu tersendiri yang dapat dipakai untuk ~ 15 ~ pelbagai bidang, kini pengetahuan geokimia dipakai dimanamana dan telah menjadi cabang ilmu yang berfaedah pada pengetahuan ilmu alam. Hasil survey beberapa laboratorium geofisika seperti : “Geological Survey” Amerika Serikat pada tahun 1884; Carnegie Institution of Washington , DC , pada tahun 1904 dan di beberapa negara Eropa ,terutama Norwegia dan Uni Soviet , antara sekitar 1910 dan 1925. Data-data hasil survey mereka membuka khazanah riset dan dipakai oleh ahli geologi untuk memperkirakan komposisi rata-rata kerak lapisan bumi. Abad kedua puluh , jalannya geokimia telah dipandu oleh beberapa kemajuan teknologi . Yang pertama adalah penemuan dari seorang pakar bernama Max von Laue di tahun 1912 dia membuktikan bahwa dalam kristal ada substansi atom dapat berfungsi sebagai kisi difraksi untuk menyebarkan seberkas sinar - X . Bertolak hasil temuan ini, ilmuan William L. Bragg mencoba membuktikan struktur kimia garam yang ada dikarang . Selanjutnya di tahun 1920, Victor M. Goldschmidt dan rekan-rekannya di University of Oslo berhasil menentukan struktur sejumlah besar mineral umum , dan dari struktur ini , dirumuskan prinsip-prinsip tentang kimia dan distribusi unsur-unsur dalam senyawa alami. Akhir-akhir ini banyak pengetahuan geokimia dimanfaatkan oleh ahli perminyakan, tidak hanya digunakan untuk prediksi kandungan minyak dan gas tetapi segi pemanfaatan produk itu lebih luas. Oleh karenanya mereka menggunakan istilah geokimia petroleum. Geokimia petroleum (minyak dan gas bumi) adalah penerapan prinsipprinsip kimia yang mempelajari tentang asal, migrasi, ~ 16 ~ akumulasi dan alterasi dari petroleum, selain itu menerapkan konsep-konsepnya dalam rangka eksplorasi petroleum yang lebih efektif. Walaupun sebenarnya pengetahuan dan eksplorasi minyak dan gas bumi telah berlangsung sejak zaman dahulu, namun begitu, seiring berkembangnya waktu, ilmu semakin berkembang, dengan lahirnya teknologi-teknologi terbarukan sehingga semakin memudahkan dalam eksplorasi minyak dan gas bumi untuk memenuhi kebutuhan energi. Dengan kemajuan teknologi , akhirnya pengetahuan geokimia mampu menyelidiki dan prediksi kimia bagian lapisan bumi yang tidak dapat diakses, sampai saat ini ilmu ini lebih banyak dipergunakan ketimbang geofisika. Geokimia laut objek studinya yang lebih luas , termasuk penguraian elemen utama ; gas-gas terlarut, organik, radionuklida, padatan tersuspensi, zat yang dikeluarkan dari gunung api di dasar laut, sedimen dan mineral di dasar dan tanah dibawah laut. Disamping itu geokimia diapliksaikan pada teknologi terapan radioaktif. Perkembangan kimia nuklir (radio aktif isotop) bermula pada akhir abad kesembilan belas, oleh Marie dan Pierre Curie. Oleh karena itu satuan mengukur radioaktif menggunakan satuan curie. Peneliti bernama Alfred O.C. Nier dari Minnesota universitas melakukan penelitian selama 3 tahun (1936-1939) telah menemukan kandungan isotop dari 25 elemen, akhirnya di tahun 1947 isotop diaplikasikan pada massa spektrometer. Sampai saat ini prinsip-prinsip dari pengetahuan geokimia masih relevan pada penerapan isotop, seperti pada spektrofotometer dan radiologi kedokteran, penggunaan kimia nuklir di pelbagai ~ 17 ~ senjata yang mematikan manusia. Bahkan sampai saat ini pengetahuan geokimia terus berkembang. Massuk keabad dua puluh pengetahuan geokimia lebih khusus geokimia laut makin berkembang pesat, terutama diaplikasikan pada eksplorasi kerak samudera yang mengandung kobalt kaya akan manganese. Pebatuaan tersbut sangat tersohor sebagai sumberdaya alam laut yang memiliki nilai ekonomi tinggi , banyak diminati oleh negaranegara maju. Sering mereka menyebut pebatuan Fe-Mn adalah pengganti minyak bumi sebagai penghasil devisa negara. Masyarakat dunia telah menyadari bahwa daratan kita semakin sempit, dikarenakan adanya pertambahan penduduk dan kegiatan pembangunan pemukiman serta aktifitas industri. Semua faktor ini mempengaruhi kegiatan ekonomi di daratan, alternatif satu-satunya menggali atau memanfaatkan sumberdaya alam yang ada di laut dalam rangka mengisi devisa negara. . ~ 18 ~ ③ LAUT DAN ATMOSFER SEBAGAI SUATU SISTEM GEOKIMIA B ab ini akan mengulas bagaimana kedudukan geokimia dalam hubungan antara laut dengan atmosfer. Tapi sebelum masuk lebih dalam uraian tentang samudera (laut), kita harus pahami lebih dahulu bahwa samudera itu secara geologi masuk kedalam lapisan hidrosfer. Planit bumi yang kita tempati lebih dari 70% didiami air sedang daratan luasnya relatif kecil. Barangkali juga ini mempertanda kehidupan mahkluk di dalamnya membutuhkan air yang cukup banyak bagi keberlanjutan hidupnya. Apabila kita melihat planit bumi dimana samudera digambar dengan warna biru tua, maka terkesan pada kita adalah betapa luasnya samudera itu jika dibandingkan dengan daratannya, yakni 71% muka bumi ditutupi dengan lapisan air yang kita sebut hidrosfer. Secara fisik permukaan bumi ditinjau dari kedudukan garis lintang, berbeda daerah yang satu dengan yang lain (lihat Tabel 3.1). Hidrosfer sangat penting bagi kehidupan dibumi. Tak ada mahluk hidup yang dapat hidup tanpa air. Hidrosfer juga dapat meredam teriknya panas matahari, karena energi cahaya matahari digunakan untuk menguapkan air. Dengan hidrosfer terjadi pula sirkulasi air. Akibat dari adanya siklus air ini, maka ada berbagai macam aliran air yang dikenal antara lain, air laut menjadi bertambah asin, terbentuknya sungai-sungai, danau-danau dan air tanah. Erosi juga dapat mengubah permukaan tanah dan membentuk pebatuan sedimen. ~ 19 ~ Tabel 3.1. Distribusi Perairan Laut dan Daratan Garis Lintang ( 0) 90-85 85-80 80-75 75-70 70-65 65-60 60-55 55-50 50-45 45-40 40-35 35-30 30-25 25-20 20-15 15-10 10-5 5-0 90-00 Belahan Bumi Utara Perairan Daratan Perairan Daratan Perairan (106km2) (106km2) ( %) (%) (106km2) 0,979 …… 100,0 ….. ….. 2,545 0,384 85,2 12,8 ….. 3,742 1,112 77,1 22,9 0,522 4,414 2,326 65,5 34,5 2,604 2,456 6,116 28,7 71,3 6,816 3,123 7,210 31,2 69,8 10,301 5,399 6,613 45,0 55,0 12,006 5,529 8,066 40,7 59,3 13,388 6,612 8,458 43,8 56,2 14,693 8,411 8,016 51,2 48,8 15,833 10,029 7,627 56,8 43,2 16,483 10,806 7,943 57,7 42,3 15,782 11,747 7,952 59,6 40,4 15,438 13,354 7,145 65,2 34,8 15,450 14,981 6,164 70,8 29,2 16,147 16,553 5,080 76,5 23,5 17,211 16,628 5,332 75,7 24,3 16,808 17,387 4,737 78,6 21,4 16,792 154,695 100,281 60,7 39,3 206,364 6 2 Total Perairan Laut 361,059 X 10 km , 70,8% Total Daratan 148,892 X 106km2 , 29,2% Sumber: Kossinna, 1921 dalam Sverdrup dkk, The Oceans, 1962. ~ 20 ~ Belahan Bumi Selatan Daratan Perairan (106km2) ( %) 0,978 ….. 2,929 ….. 4,332 10,7 4,136 38,6 1,756 79,5 0,032 99,7 0,006 99,9 0,207 98,5 0,377 97,5 0,594 96,4 1,173 93,4 2,967 84,2 4,261 78,4 5,049 75,4 4,998 76,4 4,422 79,6 5,062 76,9 5,332 75,9 48,611 80,9 Daratan (%) 100,0 100,0 89,3 61,4 20,5 0,3 0,1 1,5 2,5 3,6 6,6 15,8 21,6 24,6 23,6 20,4 23,1 24,1 19,1 Disamping itu akibat erosi bisa terancaman kehidupan manusia, seperti peristiwa banjir bandang di Manado, Jakarta, daerah pantura dan di daerah lain di Indonesia (peristiwa tahun 2014), peristiwa ini berakibatkan hilang nyawa manusia, kerugian material dan terganggu aktifitas perekonomian. Adanya aliran air ini juga ke laut menjadikan raut muka bumi di laut lebih “rata” daripada diatas tanah. Proses perubahan itu melibatkan pengetahuan geokimia, olehnya antar laut dan atmosfer merupakan satu sistem yang tak terpisahkan Sesungguhnya berapa volume air yang ada di dunia ini? Suatu pertanyaan yang sangat menarik. Memang banyak pendapat yang bermunculan, tapi consensus para ahli diperkirakan sebanyak 1,35. 1012 m3. sebagian besar terdiri dari air asin sebanyak 97,2%. Sedang yang berupa air danau, sungai, air tanah dan uap air (awan) hanya sebesar 0,6%. Lapisan air yang menyelimuti permukaan bumi disebut hidrosfer, dimana hidrosfer di muka bumi dikelompokkan menjadi dua, yaitu perairan darat dan perairan laut. Laut merupakan sekumpulan air yang sangat luas di muka bumi yang memisahkan atau menghubungkan suatu pulau atau benua dengan pulau atau benua lainnya. Perairan laut tidak hanya terdiri atas laut itu sendiri tetapi juga terdiri atas samudera, teluk, dan selat. Intinya komposisi kimia relatif di laut didominasi oleh enam unsur utama ( Na , Mg , Ca , K , Cl , dan S ) . Pada awal 1819 profesor Kimia di Jenewa, Alexander Marcet mengatakan dalam publikasinya bahwa , enam unsur ini hampir sama di seluruh perairan laut di dunia . Senyawa-senyawa ini biasa di kalkulasikan sebagai “salinitas” . Dari keenam unsur kimia yang selalu ada di laut, hanyalah kalsium memperlihatkan variasi kecil tetapi dapat diukur. Berangkat dari keterangan ilmiah ini, maka seorang ahli oseanografi yang sangat terkenal, W. Dittmar pada tahun 1873 melakukan riset secara detail. Peneliti ini menggunakan ~ 21 ~ contoh air laut sebanyak 77 contoh diambil dari beberapa perairan di Samudera Pasifik, Hindia dan Atlantik melalui suatu ekspedisi yang dilakukan oleh H.M.S. Challenger. Ia mendeterminasi tentang garam-garam, sulfat, magnesium, kalsium dan kalium (potassium) dan jenis kimia lainnya dalam takaran garam per kilogram (‰). Tabel 3.2 berikut ini disajikan hasil kajian Dittmar tentang kimia utama terdapat di air laut pada standar konsentrasi Cl = 19.00 ‰, angka Cl ini merupakan nilai tengah rasio antar perbedaan ion dan total padatan terlarut. Tabel.3.2. Kimia Utama yang Terkandung di Air Laut No 1 2 3 4 5 6 7 8 9 10 11 12 Ion Nilai Cl = 19‰ % Cl 18,980 55,04 Br 0,065 0,19 SO42,649 7,68 CO3 0,00 HCO3 0,140 0,41 F0,001 0,00 H3BO3 0,026 0,07 ++ Mg 1,272 3,69 Ca++ 0,400 1,16 ++ Sr 0,013 0,04 + K 0,380 1,10 Na+ 10,556 30,61 ∑ 34,482 ‰ Sumber: Sverdrup dkk, 1962. The Ocean. - Air yang ada di perairan laut tidak berbentuk air murni namun bersenyawa dengan beberapa garam, para ahli telah sepakat ukuran garam-garam yang terlarut di dalam air laut menggunakan satuan salinitas (salinity). Salinitas di laut umumnya berkisar antara 33 – 37 ‰ tergantung pada kondisi ~ 22 ~ wilayahnya, yakni wilayah yang banyak curah hujan, muara sungai, limpasan es dan salju, dan daerah yang setengah tertutup (semi-enclosed). Khusus di laut merah sering terjadi proses penguapan (evaporasi) yang sangat cepat, kadar salinitasnya dapat mencapai 40‰. Pengikatan ion dalam tingkat tertentu, untuk pasangan ion antara delapan ion terlarut paling banyak dalam air laut, yaitu Na+ , K+, Ca2+, Cl-, HCO3-, CO32- dan SO42-, yang membentuk lebih 99% total ion terlarut. Data konsentrasi dan keseimbangan untuk interaksi antara empat kation dan empat anion larutan yang telah digunakan untuk menghitung hasil pada tabel-tabel berikut. Tabel 3.3. Distribusi ion di Unsur Utama pada Anion di Air Laut Ion Konsentrasi (mol) Ion bebas (%) Dengan SO42- Dengan HCO3- Dengan CO32- Kalsium, Ca2+ Magnesium,Mg2+ + Natrium, Na + Potasium, K 0,0104 0,0540 0,4752 0,0100 91 87 99 99 8 11 1,2 1 1 1 0,001 - 0,2 0,3 - Sumber: Svedrup dkk (1962) Tabel 3.4. Distribusi ion di Unsur Utama pada kation di Air Laut Ion 2- Sulfat, SO4 Bikarbonat, Karbonat Konsentra si (mol) Ion bebas (%) Dengan 2+ Ca (%) Dengan 2+ Mg (%) Dengan + Na (%) Denga n K+ (%) 0,0284 0,00238 0,000,269 54 69 9 3 4 7 21,5 19 7 21 8 17 0,5 - Sumber: Svedrup dkk (1962) Zat terlarut kebanyakan mempunyai waktu residen lebih lama daripada waktu pengadukan. Hal ini memungkinkan terjadi karena siklus ulang di dalam perairan, ~ 23 ~ terutama karena keterlibatannya dalam reaksi biologi. Disamping itu, dapat terjadi juga pertukaran di sepanjang dasar laut dan bidang batas udara-laut. Zat terlarut itu pada akhirnya akan berpindah dari larutan air ke sedimen di dasar laut dan batuan melalui proses bolak-balik. Proses tersebut termasuk penyerapan dan “scavenging” unsur-unsur minor, formasi pembentukan kerangka, reaksi diagenetika di sedimen, penimbunan partikel di lingkungan sekitar lingkaran anoxic, serta reaksi pada saat aktivitas hidrotermal. Kadar garam air laut rata-rata adalah + 3%, sebagian besar berupa garam dapur (NaCl) sebanyak 85%, garam inggris (MgSO4) sebanyak 10%, dan inilah yang membuat air laut terasa agak pahit. Adapun 5% lainnya terdiri dari berbagai mineral antara lain Calsium, Kalium, Bromida dan lain-lain. Laut mempunyai kedalaman dasar yang berbeda-beda. Dasar laut membentuk lereng mulai garis pantai ke arah tengah laut. (gambar 3.1) Kedalaman laut makin bertambah dengan makin jauh jaraknya dari daratan pantai. Gambar 3.1. Zona Kedalam Laut Bertolak pada gambar diatas ternyata di laut ada 4 zona yang memiliki karakteristik berbeda, yaitu: ~ 24 ~ a. Zona litoral atau zona pasang surut, merupakan wilayah laut yang berada di antara pasang naik dan pasang surut air laut. Zona ini sering disebut dengan daerah pantai. b. Zona neritik, merupakan wilayah laut yang berada di antara garis pantai kedalaman 200 m. Pada zona ini sinar matahari masih dapat menembus ke dalam. Ikan dan sejenisnya serta tumbuhan laut banyak dijumpai pada zona ini. c. Zona batial, merupakan wilayah laut yang berada pada kedalaman 200–2.500 m. Pada zona ini sinar matahari sudah tidak mampu menembus ke dalam sehingga organisme laut tidak sebanyak pada zona neritik. Zona batial biasanya merupakan lereng benua (continental slope) yang curam dan berbatasan dengan landas benua (continental shelf). d. Zona abisal, merupakan wilayah laut yang mempunyai kedalaman lebih dari 2.500 m. Suhu pada wilayah ini sangat dingin. Hewan laut yang dapat hidup hanya terbatas, tumbuhan laut sudah tidak ada. Gambaran secara keseluruhan fisik laut (relief) perlu juga kita ketahui agar proses interaksi kimia sebagai proses geokimia lebih mudah dipahami oleh pembaca. Relief dasar laut (morfologi) adalah perbedaan tinggi dan rendah permukaan laut. Halmana relief merupakan bentuk kekasaran permukaan bumi, baik berupa tonjolan, gunung, dataran, atau cekungan yang terjadi karena adanya pengaruh tenagatenaga pembentuk muka bumi, baik tenaga endogen maupun tenaga eksogen. Bentuk muka bumi di lautan tidak seruncing dan sekasar relief di daratan. Keadaan ini sebagai akibat dari erosi di dalam lautan dan oleh adanya pengikisan yang berlangsung lama oleh arus laut di dasar perairan (lihat gambar 3.2). ~ 25 ~ Gambar 3.2. Morfologi Dasar Laut Sumber: Skinner ( 1976) Gambar diatas memperlihatkan beberapa bagian dasar laut, yaitu (a) Landas Kontinen (Continental Shelf) adalah bagian dari benua yang terendam oleh air laut. Untuk menentukan apakah dasar laut merupakan kelanjutan dari suatu benua, biasanya dilihat dari struktur batuan pembentuknya (kondisi geologi). Yang paling mudah diamati, landas kontinen memiliki kedalaman tidak boleh lebih dari 150 meter. Sedangkan Batas Landas Kontinen merupakan batas dasar laut yang sumberdaya alamnya dapat dikelola oleh negara yang bersangkutan; (b) Lereng kontinen (continental slope) merupakan kelanjutan dari continental shelf dengan kemiringan antara 4% sampai 6%. Kedalaman lereng benua lebih dari 200 meter. Daerah ini meluas dari patahan beting sampai pada kedalaman rata-rata 2 km. Daerahnya curam dengan kemiringan rata-rata 1:2 sampai 1:40, dan mencakup luas 13% dari luas permukaan bumi; (c) ~ 26 ~ Jurang submarine (submarine canyon) adalah lembah yang dalam (tenggelam) dan lebar. Yang dimaksud lembah tenggelam adalah lembah lembah sungai yang tergenang air laut sebagai akibat penenggelaman daratan. Contoh: lembahlembah sungai purba di Laut Jawa dan Selat Karimata; (d) kontinen landai (continental rise), punggung bukit lautan yang terbentuk di dasar laut, mirip tanggul raksasa, panjangnya bisa ribuan kilometer; (e) Mid ocean ridge, merupakan kumpulan gunung-gunung vulkanik dari dasar lautan yang bagian-bagian badan dan puncaknya mencapai permukaan laut dan membentuk pulau-pulau. Mid ocean ridge ini banyak terdapat di tengah samudra pasifik; (f) Guyot, yaitu gunung di dasar laut yang bentuknya serupa dengan “seamount” tetapi bagian puncaknya datar. Banyak terdapat di lautan pasifik. Sedang Seamount adalah gunung di dasar laut dengan lereng yang curam dan berpuncak runcing serta kemungkinan mempunyai tinggi sampai 1 km atau lebih tetapi tidak sampai ke permukaan laut; dan (g) Palung (trench) adalah lembah yang sangat dalam dan memanjang di dasar laut serta memiliki lereng yang curam. Palung ini merupakan bentukan morfologi dasar laut yang berbentuk seperti saluran atau parit yang sangat dalam yang pada umumnya terdapat pada perbatasan antara benua dengan kepulauan. Trench ini memiliki tingkat kedalaman yang tinggi, sebagai contoh sebagian dari ava trench memiliki kedalaman 7.700 meter Setelah kita ketahui secara bentuk kimia utama dan bentuk laut serta bagian-bagiannya, sekarang ini marilah lihat bentuk dan karakteristik atmosfer. Kata atmosfer berasal dari bahasa Yunani, dari kata atmos yang berarti udara dan spheira yang berarti lapisan. Jadi, atmosfer adalah lapisan udara yang menyelubungi bumi. Atmosfer tersusun oleh sejumlah zat yaitu: Nitrogen (N2) sebesar 78,08%, Oksigen (O2) sebesar 20,94%, Argon (Ar) ~ 27 ~ sebesar 0,90%, Karbondioksida (CO 2) sebesar 0,03% dan sisanya terdiri atas gas lainnya dengan jumlah sedikit. Sifat fisik atmosfer, yakni (1) merupakan campuran berbagai gas yang tidak berwarna dan tidak terlihat oleh mata; (2) Memiliki berat sehingga memiliki juga tekanan udara; (3) Mengembang jika terkena panas dan mengerut ketika dingin; (4) Jika terjadi perbedaan tekanan, maka terjadilah pergerakan udara yang disebut angin yang bergerak dari tekanan tinggi ke tekanan rendah; dan ke (5) Tidak berbau, tidak berwarna, dan tidak bisa dirasakan Atmosfer merupakan udara yang menyelubungi bumi dan sangat berguna bagi keberlangsungan kehidupan di bumi karena beberapa sebab: ① atmosfer mampu melindungi bumi dari pancaran radiasi matahari yang bersuhu 6000 derajat Kelvin; ② atmosfer berperan penting dalam siklus hidrologi pada proses penampungan air dari permukaan bumi (daratan dan lautan); ③ atmosfer mengandung oksigen yang dibutuhkan makhluk hidup untuk bernapas; dan ke ④ atmosfer merupakan medium tempat bercampurnya pelbagai unsur kimia yang berdampak pada kualitas udara. Sudut pandang profil temperatur vertikal, maka atmosfer dapat dibagi menjadi empat lapisan yang berbeda yaitu troposfer, stratosfer, mesosfer, dan termosfer. Puncak dari lapisan-lapisan tersebut adalah tropopause, stratopause, mesopause, dan termopause (gambar 3.3). Troposfer merupakan lapisan terbawah dari atmosfer terdapat pada ketinggian dari 8 km di daerah kutub dan 16 km di ekuator. Ruang terjadinya sirkulasi dan turbulensi seluruh bahan di atmosfer atau dapat dikatakan sebagai daerah interaksi kimia, sehingga menjadi salah satu lapisan yang mengalami pembentukan dan perubahan cuaca seperti angin, awan, presipitasi, badai, kilat dan guntur. Secara umum panas bumi yang terjadi akibat oleh jumlah zat rumah kaca berlimpah akan bertumpuk di lapisan ini sehingga sinar ~ 28 ~ matahari masuk ke bumi, pantulan baliknya terhambat terhalang oleh gas rumah-kaca di lapisan ini. Gambar 3.3. Bentuk Lapisan Atmosfer Sumber: Skinner ( 1976) Kecepatan angin pada lapisan ini bertambah dengan naiknya ketinggian dan di troposfer ini pemindahan energi berlangsung. Radiasi surya menyebabkan pemanasan permukaan bumi yang selanjutnya panas tersebut diserap oleh air untuk berubah menjadi uap. Akibat proses evaporasi, energi panas diangkat oleh uap ke lapisan atas yang lebih tinggi berupa panas laten. Setelah terjadi pendinginan berlangsung proses kondensasi. Pada lapisan ini suhu udara turun dengan bertambahnya ketinggian (dT/dz < 0) atau pada keadaan lapse rate (Suhu udara turun dengan bertambahnya ketinggian). Rata-rata lapse rate seluruh dunia pada keadaan normal adalah -6.5 derajatK, setiap kenaikan ketinggian 1 km. Pada atmosfer normal, suhu troposfer berubah dari 15 0C pada permukaan laut menjadi -600C di puncak troposfer. ~ 29 ~ Lapisan di atasnya dengan suhu tetap atau meningkat disebut stratofer kisaran ketinggiannya antara 12-50 km diatas permukaan laut. Lapisan ini terdiri dari 3 wilayah antara lain Stratofer bawah ketinggiannya 12-20 km daerah isotermis, Stratosfer tengah ketinggiannya 20-35 km daerah inversi suhu, Stratosfer atas ketinggiannya 35-50 km daerah inversi suhu yang kuat. Lapisan ini tidak mengalami turbulensi maupun sirkulasi. Stratosfer merupakan lapisan atmosfer utama yang mengandung gas ozon. Lapisan dengan suhu menurun di ketinggian 50-80 km disebut mesosfer dengan perubahan suhu terhadap ketinggian adalah lapse rate. Pada lapisan ini suhu udara sekitar -50C pada lapisan hingga -950C pada puncaknya. Tidak mengalami turbuleni atau sirkulasi udara. Merupakan daerah penguraian O2 menjadi atom O. Batas atasnya adalah lapisan mesopause dengan perubahan suhu terhadap ketinggian mulai bersifat isotermal. Lapisan di atasnya dengan suhu yang meningkat disebut termosfer. Lapisan ini ditandai dengan beberapa ciri yaitu memiliki ketinggian 80 km hingga batas yang sulit ditentukan karena sangat jarangnya partikel gas yang mencapai lapisan ini. Di atas termosfer adalah ionosfer, merupakan puncak atmosfer yang langsung bersentuhan dengan ruang hampa udara. Lapisan ini merupakan tempat berlangsungnya proses ionisasi gas ionasasi gas N2 dan O2 sehingga lapisan ini disebut ionosfer. Dimana diatas ketinggian 100km pengaruh radiasi uv dan sinar x makin kuat. Lapisan terdekat bumi, troposfer, mengandung 6/7 bagian dari massa total atmosfer yang relatif tercampur secara sempurna, sangat basah, dan merupakan pusat aktivitas dan pembentukan awan maupun hujan. Seperti uraian diatas, kimia-kimia utama di laut yang relatif konstan berdiam di perairan laut walaupun kecil jumlahnya, kecuali kalsium (Ca2+) yang sangat bervariasi rasionya namun bisa diterah atau dapat diukur. Zat kimia di ~ 30 ~ laut yang konstan disebut sebagai senyawa “konservatif”. Senyawa-senyawa itu dapat berubah kuantumnya jika ada pemasukan air murni ke laut, seperti dari sungai, danau dan sebagainya. Umumnya para ahli geokimia menaruh perhatian pada elemen minor dilaut seperti B , Li , Sb , U , dan Br dan juga kimia konservatif , yang sering bervariasi secara dramatis relatif terhadap salinitas. Kekuatan pengikatan kimia sangat tergantung pada ion, dimana kation dan anion dalam larutan mengalami tarikan dan atau tolakan elektrostatik bergantung pada muatan tiap ionik. Interaksi tersebut adalah kabalikan proporsi terhadap kuadrat jarak antara ion dan sangat kecil dalam larutan yang sangat encer ketika ionnya jauh terpisah. Akan tetapi, dalam larutan asin seperti air laut, interaksi antara ion terlarut tidak dapat diabaikan. Interkasi tersebut menentukan spesifikasi zat terlarut dan pengaruhnya mengurangi kemampuan ionion dalam reaksi kimia organik atau biologi. Di laut ada juga unsur kimia nir-konservatif yang memegang peranan dalam proses biologi di laut. Kadar garam yang ada di laut umumnya diterah dengan satuan salinitas dalam takaran per mil (‰).Dengan demikian , air laut yang memiliki total kandungan garam terlarut dari 3,45 % berat memiliki salinitas 34,5 ‰ . Menurut McSween dkk (2003) perairan laut terbuka dan normal salinitas bervariasi dari 33 ‰ sampai 38 ‰, kecuali di laut mati kadar garamnya tinggi bisa mencpai 45‰. Ion dengan garam ionik yang kuat (elektrolit yang kuat) seperti natrium klorida mempunyai satu-satunya interaksi yaitu tarikan elektrostatik dan atau tolakan antara ion yang bersifat independen, dan lingkaran hidrasi yang tetap. Beberapa ion membentuk pasangan ion ketika lingkaran hidrasi ion unsur besar dan hasilnya dapat berupa spesies netral atau bermuatan. Pasangan ion jarang terbentuk ~ 31 ~ antara dua monovalen, biasanya terbentuk antara dua ion polivalen atau antara satu ion polivalen dan satu ion monovalen. Walaupun tidak ada bagian yang jelas antara pembentukan ion kompleks dan pasangan ion, terdapat dua perbedaan prinsip: pertama, ikatan dalam ion kompleks adalah kovalen, bukan elektrovalen seperti pada pasangan ion. Kedua, bila ion kompleks terbentuk dalam larutan, lingkaran hidrasi dwikutub atau lebih ion tunggal akan membuat gabungan kompleks untuk membentuk selimut penyatuan hidrasi. Sesungguhnya, jika sebagian jumlah total ion terlarut berinteraksi dengan ion-ion lain dalam larutan, ion tersebut tidak bebas untuk terlibat dalam reaksi kimia. Besarnya interaksi dan pengaruhnya pada reaktivitas kimia jenis terlarut bergantung pada sifat ion-ion yang terlibat. Umumnya untuk konsentrasi larutan adalah sama terhadap air laut, dan proporsi konsentrasi total jenis ionik yang bebas bereaksi berkurang dengan bertambahnya muatan. Konsentrasi efektif akan kurang variasinya dibandingkan dengan konsentrasi sebenarnya. Konsentrasi efektif (dikenali sebagai aktivitas keseimbangan larutan) hakekatnya berada dalam larutan 70% konsentrasi yang sesungguhnya, disamping itu terdapat beberapa ion-ion multivalen yang kompleks meliputi 5-10%, contohnya Al3+. Sedang untuk ion kurang berinteraksi, seperti Na+ adalah merupakan subyek pada interaksi elektrostatik Mula-mula diperkirakan bahwa zat-zat kimia yang menyebabkan air laut asin berasal dari darat yang dibawa oleh sungai-sungai yang mengalir ke laut, entah itu dari pengikisan pebatuan di darat, dari tanah longsor, dari air hujan atau dari gejala alam lainnya, yang terbawa oleh air sungai ke laut. Jika hal ini benar tentunya susunan kimiawi air sungai tidak akan berbeda dengan susunan kimiawi air laut. Namun menurut teori, zat-zat garam tersebut berasal dari dalam dasar laut ~ 32 ~ melalui proses outgassing, yakni rembesan dari kulit bumi di dasar laut yang berbentuk gas ke permukaan dasar laut. Bersama gas-gas ini, terlarut pula hasil kikisan kerak bumi dan bersama-sama garam-garam ini merembes pula air, semua dalam perbandingan yang tetap sehingga terbentuk garam di laut. Kadar garam ini tetap tidak berubah sepanjang masa. Artinya kita tidak menjumpai bahwa air laut makin lama makin asin. Zat-zat yang terlarut yang membentuk garam, yang kadarnya diukur dengan istilah salinitas dapat dibagi menjadi empat kelompok, yakni: 1. Konstituen utama : Cl, Na, SO4, dan Mg. 2. Gas terlarut : CO2, N2, dan O2. 3. Unsur Hara : Si, N, dan P. 4. Unsur Runut : I, Fe, Mn, Pb, dan Hg. Konstituen utama merupakan 99,7% dari seluruh zat terlarut dalam air laut, sedangkan sisanya 0,3% terdiri dari ketiga kelompok zat lainnya. Akan tetapi meskipun kelompok zat terakhir ini sangat kecil persentasenya, mereka banyak menentukan kehidupan di laut. Sebaliknya kepekatan zat-zat ini banyak ditentukan oleh aktivitas kehidupan di laut. Hakikinya, salinitas merupakan jumlah dari seluruh garam-garaman dalam gram pada setiap kilogram air laut. Secara praktis, adalah susah untuk mengukur salinitas di laut, oleh karena itu penentuan harga salinitas dilakukan dengan meninjau komponen yang terpenting saja yaitu klorida (Cl). Kandungan klorida ditetapkan pada tahun 1902 sebagai jumlah dalam gram ion klorida pada satu kilogram air laut jika semua halogen digantikan oleh klorida. Penetapan ini mencerminkan proses kimiawi titrasi untuk menentukan kandungan klorida. Salinitas ditetapkan pada tahun 1902 sebagai jumlah total dalam gram bahan-bahan terlarut dalam satu kilogram air laut jika semua karbonat dirubah menjadi oksida, semua bromida dan yodium dirubah menjadi klorida dan semua ~ 33 ~ bahan-bahan organik dioksidasi. Selanjutnya hubungan antara salinitas dan klorida ditentukan melalui suatu rangkaian pengukuran dasar laboratorium berdasarkan pada sampel air laut di seluruh dunia dan dinyatakan sebagai: S (o/oo) = 0.03 +1.805 Cl (o/oo) Simbol o/oo (dibaca per mil) adalah bagian per seribu. Kandungan garam 3,5% sebanding dengan 35o/oo atau 35 gram garam di dalam satu kilogram air laut. Persamaan tahun 1902 di atas akan memberikan harga salinitas sebesar 0,03o/oo jika klorinitas sama dengan nol dan hal ini sangat menarik perhatian dan menunjukkan adanya masalah dalam sampel air yang digunakan untuk pengukuran laboratorium. Oleh karena itu, pada tahun 1969 UNESCO memutuskan untuk mengulang kembali penentuan dasar hubungan antara klorinitas dan salinitas dan memperkenalkan definisi baru yang dikenal sebagai salinitas absolut dengan rumus: S (o/oo) = 1.80655 Cl (o/oo) (1969) Namun demikian, dari hasil pengulangan definisi ini ternyata didapatkan hasil yang sama dengan definisi sebelumnya. Definisi salinitas ditinjau kembali ketika cara untuk menentukan salinitas dari pengukuran konduktivitas, temperatur dan tekanan dikembangkan. Maka sejak tahun 1978, didefinisikan suatu satuan baru yaitu Practical Salinity Scale (Skala Salinitas Praktis) dengan simbol S, sebagai rasio dari konduktivitas. Hakiki, salinitas dari suatu sampel air laut ditetapkan sebagai perbandingan dari konduktivitas listrik (K) sampel air laut pada temperatur 15oC dan pada tekanan satu atmosfer terhadap larutan kalium klorida (KCl), dimana bagian massa KCl adalah 0,0324356 pada temperatur dan tekanan yang sama. Rumus dari definisi ini adalah: S = 0.0080 - 0.1692 K1/2 + 25.3853 K + 14.0941 K3/2 - 7.0261 K2 + 2.7081 K5/2 ~ 34 ~ Dari penggunaan definisi baru ini, dimana salinitas dinyatakan sebagai rasio, maka satuan ‰ (permil) tidak lagi berlaku, praktis nilai 35 ‰ berkaitan dengan nilai 35 dalam satuan. Beberapa oseanografer menggunakan satuan "psu" dalam menuliskan harga salinitas, yang merupakan singkatan dari "practical salinity unit". Karena salinitas praktis adalah rasio, maka sebenarnya ia tidak memiliki satuan, jadi penggunaan satuan "psu" sebenarnya tidak mengandung makna apapun dan tidak diperlukan. Pada kebanyakan peralatan yang ada saat ini, pengukuran harga salinitas dilakukan berdasarkan pada hasil pengukuran konduktivitas. Salinitas di daerah subpolar (yaitu daerah di atas daerah subtropis hingga mendekati kutub) rendah di permukaan dan bertambah secara tetap (monotonik) terhadap kedalaman. Di daerah subtropis (atau semi tropis, yaitu daerah antara 23,5 o 40oLU atau 23,5o - 40oLS), salinitas di permukaan lebih besar daripada di kedalaman akibat besarnya evaporasi (penguapan). Di kedalaman sekitar 500 sampai 1000 meter harga salinitasnya rendah dan kembali bertambah secara monotonik terhadap kedalaman. Sementara itu, di daerah tropis salinitas di permukaan lebih rendah daripada di kedalaman akibatnya tingginya presipitasi (curah hujan). Besaran senyawa kimia di laut bervariasi dan sangat tergantung pada kondisi atmosfer, terlihat korelasi positif antar samudera dan atmosfer. Gambar berikut memberikan ilustrasi bagaimana interaksi positif antar daerah permukaan laut (atmosfer) dengan kedudukan kimia di laut. Air menguap ke udara membawa beberapa senyawa kimia, apalagi jika udara itu telah terpolusi oleh kimia logam, maka zat-zat kimia tersebut akan bersama uap air akan terkondensasi yang akhirnya akan jatuh ke laut dan mengendap sebagai sedimen dan membentuk lapisan keras (kerak) (lihat gambar warna hitam). Adanya sirkulasi hidrotermal terjadilah pengikisan pebatuan, mineral dalam batuan kerak lautan mengakibatkan ~ 35 ~ pemasukan unsur klorida, sulfat serta gas-gas ke dalam perairan laut sehingga elemen kimia di laut lebih kompleks. penguap an 1 Cuaca } Batuan di daratan kondensasi penguapa n sendimen 4 subduksi photosintesa penghancur bahan larutan hidrothermal Kepermukaa 3 aerosol oceanic Perubahan gas organism kepermukaan n Gerakan pengendap debu an pore waterpenghancuran bakteri air 2 nutrien exchang e Gambar3.4. Ilustrasi Atmosfer dan Laut Suatu Sistem Sumber: Rompas dkk (2009) Selain itu oleh adanya gerakan bumi apalagi wilayah perairan laut Indonesia terdapat lempengan bumi yang mudah bergerak berakibatkan penambahan unsur kimia di laut. Pebatuan sedimen maupun partikel-partikel hasil vulkanik di dasar laut dipindahkan secara langsung keatas (uplit) atau ke atas permukaan laut maupun oleh subduksi ke dalam mantel bumi. Elemen-elemen naik keatas dan adanya pengaruh cuaca partikel-pertikel itu jatuh sebagai sedimen dan batuan ke dalam kerak melalui proses magmatik, dan ~ 36 ~ membentuk macam bentuk batuan (igneous) dan membebaskan gas-gas vulkanik kedalam perairan. Partikel-partikel dari udara masuk kedalam laut membawa pelbagai elemen kimia, ada yang bentuk padatan, cair dan gas. Semua elemen kimia itu akan berasosiasi dengan elemen di laut, bahkan ada yang dimanfaatkan oleh organisme hidup untuk keperluan kehidupannya. Sebagian partikel itu jatuh sebagai sedimen dan mengendap di dasar laut, kemudian diluruhkan oleh mikroorganisme sehingga menjadi bahan nutrien bagi percepatan proses fotosintesa. Adanya aliran air sungai maupun air permukaan tanah (run off) membawa elemen kimia yang menambah kekayaan kimia di lautan. Bahan-bahan yang dihantar oleh aliran sungai ada yang bentuk padatan maupun berbentuk senyawa. Sedimen laut dan batuan igneous mempunyai komposisi elemen kimia yang sangat kompleks, halini berlaku tidak hanya unsur utama limestone, sandstone dan shales, melainkan berlaku juga untuk elemen unsur minor. Hampir semua sedimen terigen di bagian lapisan pelagis terdiri atas bahan-bahan yang berukuran kecil. Ada dua cara bahan tersebut sampai ke permukaan, pertama adanya bantuan arus turbulensi dan aliran gravitasi dan kedua melalui gerakan es yaitu bahan glasial yang dibawa oleh bongkahan es ke laut lepas dan mencair. Bongkahan es besar yang mengapung bongkahan es kecil dan pasir dapat ditemukan pada sedimen pelagis yang berjalan beberapa ratus kilometer dari daerah gletser atau tempat asalnya. Selain zat-zat terlarut ini, air juga mengandung butiranbutiran halus dalam suspensi. Sebagian dari zat ini akhirnya terlarut, sebagian lagi mengendap ke dasar laut dan sisanya diurai oleh bakteri menjadi zat-zat hara yang dimanfaatkan tumbuhan untuk fotosintesis Unsur terlarut kebanyakan mempunyai waktu residen lebih lama dari pada waktu pengadukan. Hal ini memungkinkan terjadi karena siklus ulang di dalam perairan, ~ 37 ~ terutama karena keterlibatannya dalam reaksi biologi. Disamping itu, dapat terjadi juga pertukaran di sepanjang dasar laut dan bidang batas udara-laut. Unsur terlarut, pada akhirnya akan berpindah dari larutan air ke sedimen di dasar laut dan batuan oleh prosesproses perubahan yang reversible. Proses tersebut termasuk penyerapan dan “scavenging” unsur-unsur minor, formasi material kerangka, reaksi diagenetik dengan sedimen, penyimpanan dalam lingkaran anoxic, serta reaksi pada saat aktivitas hidrotermal. Interaksi kimia di dasar laut dalam periode yang cukup panjang bisa mengakibatkan polimetalik nodul yang keras. Elemen kimia di laut sejak bumi awal sampai sekarang sangat berbeda, apalagi laut merupakan wadah terbesar yang dapat menampung pelbagai kimia, baik dari daratan, udara maupun dari dasar lautan. Gambar berikut ini memperlihatkan lempengan kerak bumi dengan kandungan elemen kimia yang terdapat pada setiap lapisan. Pebatuan Vulkanik: Fe,Cu, Mn, Co, Cd, Zn, Ni, He, La, Nd, dsb Senyawa organik Batuan Granit: Si, Al, K, Ar, Ni, Cd, Pb, Au, Fe, dsb. Pebatuan sedimen: Ca, C, S, Na, Mg, K, Fe , Cd, P, , Cl,Co dsb. Gambar. 3.5. Sumber Elemen Kimia di Laut ~ 38 ~ Bahan-bahan ini hadir di badan air, akibat dari kejadian gerakan bumi akan melepaskan elemen kimia ke perairan laut, yang kemudian kimia tersebut sebagian dimanfaatkan oleh organisme perairan, sebagian diuraikan oleh mikroorganisme dan yang lain akan tertinggal sebagai sedimen. Hein (2004) kobalt yang kaya akan senyawa ferromaganese yang ada dilaut sesungguhnya berasal dari “seamount”; punggung laut (ridge) dan tanah keras didasar laut, selain itu pula bisa zat kimia ini hadir di laut oleh adanya gerakan bumi mengeluarkan magma. Tetapi tidak hanya cobalt saja, namun senyawa titanium, cerium, nikel, platinum, Mg, thallium dan tellurium dapat terjadi. Kobalt kaya akan Fe-Mn, para ilmuan geokimia laut menyebut sebagai kerak dan bongkahan kobalt atau Fe-Mn. Karena kerak tersebut belakangan ini telah menjadi perhatian khusus oleh ISA, karena sumber ekonominya sangat besar, maka penulis membahas khusus di bab 11 (bagian akhir). Sejak pertengahan 1970-an , ahli geokimia secara bertahap menemukan bahwa sejumlah trace elemen , seperti Sr , Cd , Ba , dan Cr , juga kehadiran zat kimia yang berhubungan dengan nutrien di laut , meskipun tidak begitu jelas dalam banyak kasus bagaimana elemen ini terlibat dalam proses secara biokimia di laut. Dari sudut pandang geokimia , gradien terukur sangat penting untuk kemampuan kita melacak jalur dan proses biologi , sedimen , dan perilaku sirkulasi di lautan . McSween dkk (2003) telah melakukan penelitian terhadap kimia dilaut dan teridentifikasi kelimpahan serta sifat sejumlah elemen di laut dalam, seperti terlihat pada tabel 3.5 berikut. Sejumlah elemen itu dikelompok ke dalam kimia konservatif dan nir-konservatif. Juga gas-gas terlarut ( O2 , CO2 , H2S , dan beberapa gas yang bebas N2 dan N2O , yang terlibat dalam proses metabolisme. Pola kelimpahan sangat menentukan sebagian besar kelarutan senyawa kimia di laut. ~ 39 ~ Tabel 3.5 Kelimpahan dan Sifat Beberapa Kimia di Laut Kosentrasi di Permukaan Kosentrasi di Kedalaman Unsur Sifat -1 Li 178 µg Kg Konservatif 1 -1 B 4.4 mg Kg Konservatif 1 C 2039178 µmol 2264 µmol Kg-1 (714 Nutrien m) N (N2) 560 µmol Kg-1 (995 m) GasNonnutrien -7 -1 (NO3-) <3 X 10 mol Kg 41 µmol Kg-1 (891 M) Nutrien -1 O(O2) 205 µmol Kg 47 µmol Kg-1 (891 m) Hub. Nutrien -1 F 1,3 mg Kg konservatif Na 10, 781 g Kg-1 Konservatif -1 Mg 1,284 g Kg Konservatif Al 1,0 µg Kg-1 0,6 µg Kg-1 (1000 m) ? -1 100,8 µ mol Kg (891 m) Si 2,0 µg Kg-1 Nutrien -1 -1 2,84 µ mol Kg (891 m) P 0,08 µg Kg Nutrien S 2,712 g Kg-1 Konservatif Cl 19, 353 g Kg-1 Konservatif -1 K 399 mg Kg Konservatif 413,6 mg Kg-1 (1000 m) Ca 417,6 mg Kg-1 Konservatif 2 -1 -1 Cr 268 ng Kg 296 ng Kg (1000 m) Hub. Nutrien -1 -1 Mn 34 ng Kg 38 ng Kg (985 m) Hub. Nutrien Fe 8 ng Kg-1 45 ng Kg-1 Hub. Nutrien Ni 146 ngKg-1 566 ng Kg-1 (985 m) Hub. Nutrien -1 -1 Cu 34 ng Kg 130 ng Kg (985 m) Hub. Nutrien Zn 6-7 ng Kg-1 438 ng Kg-1 (985 m) Hub. Nutrien -1 -1 As 1,1 ng Kg 1,8 µg Kg (1000 m) Hub. Nutrien Br 67 mg Kg-1 Konservatif Rb 124 µg Kg-1 Konservatif -1 -1 Sr 7,404 mg Kg 7,720 mg Kg (700 m) Hub. Nutrien Cd 0,3 ng Kg-1 117 ng Kg-1 (985 m) Hub. Nutrien -1 Sn 1,0 ng Kg Antropogenik -1 -1 I 48 µg Kg 60 µg Kg (1036 m) Hub.Nutrien Cs 0,3 µg Kg-1 Konservatif Ba 4,8 µg Kg-1 13,3 µg Kg-1 (997 m) Hub.Nutrien -1 -1 Hg 3 ng Kg 4 ng Kg (1000 m) Hub. Nutrien Pb 13,6 ngKg-1 4,5 ng Kg-1 (1000 m) Antropogenik U 3,2 µg Kg-1 Konservatif Sumber : McSween dkk, 2003. GEOCHEMISTRY Pathways and Processes. ~ 40 ~ Keterangan : Hub.Nutrien : Dalam hubungan dengan nutrisi di Laut 1) Angka yang diperkirakan karena sangat sedikit kandungannya. 2) Kalsium mudah berubah karena dalam kaitan dengan karbonat, diperkirakan zat itu mendekati konservatif. Banyak kimia di laut berperan sebagai penyuplai makanan di laut, halmana jenis tumbuhan umumnya berada di daerah permukaan laut (zona neritik), oleh adanya sinar surya proses fotosintesis dapat berlangsung, beberapa jenis kimia memperlancar proses biologi tersebut. seperti fosfat , nitrat , silika terlarut ( ΣSi ) , dan karbon anorganik terlarut (ΣCO2 = CO2 + HCO3 - + CO32 - ) . Hasil fotosintesa itu di makan oleh hewan termasuk zooplankton, yang kemudian dikonversi menjadi bahan organik dalam tubuh organisme. Setelah organisme itu mati dan kotorannya akan mengendap didasar perairan, yang selanjutnya di luruhkan oleh mikroba. Peluruhan zat tersebut hasilnya merupakan elemen penting sebagai nutrien di laut. Bertolak dari tabel 3.5, ternyata organisme hidup berperan penting pada kelimpahan zat kimia di laut. Beberapa zat kimia yang bersifat hara (nutrien) dan zat yang ada hubungannya dengan nutrien khususnya 5 elemen, yaitu Fosfat , nitrat , silika , Zn , dan Cd makin berkurang ke area permukaan air dan sering disebut sebagai “biolimiting” faktor bagi konstituen di laut. Salah satu dari ke 5 zat kimia itu, yakni fosfat merupakan elemen penting bagi organisme dalam rangka proses metabolisme, karenanya fosfat adalah unsur “biolimiting”. Kalau silika dalam bentuk SiO2 merupakan penyuplai pembentukan kulit keras pada organisme diatom dan radiolaria. Tetapi tidak untuk skleton, karena membutuhkan senyawa kalsium karbonat. Elemen nitrat merupakan pembatas pada banyak spesies besar tetapi tidak untuk marga “bluegreen algae”, ~ 41 ~ biasanya pengambilan nitrogen tetap (fix nitrogen) ada dalam bentuk N2. Unsur kadmium (Cd) dan seng (Zn) umumnya akan makin berkurang mendekati permukaan, karena banyak dimanfaatkan oleh organisme bersama-sama dengan fosfat. Kehadiran unsur karbon di laut, bukan merupakan faktor pembatas biologi (biolimiting), dimana meskipun di air permukaan konsentrasi karbon sedikit dibandingkan pada perairan dalam, organisme hanya memanfaatkan 10% saja, dan mereka tinggalkan sebesar 90% dari karbon yang terlarut. Salah satu cara untuk melihat sifat bukan pembatas biologi adalah membandingkan kelimpahan dengan unsur pembatas biologi (biolimiting). Halmana perbandingan unsur fosfor, nitrogen dan karbon di dalam jaringan organisme, umumnya tetap, yakni 1:15: 105 [fosfor:nitrogen:karbon]. Perbandingan ini sering disebut sebagai rasio “Redfield”. Mengapa disebut rasio “Redfield” karena diambil dari nama seorang ahli geokimia yakni Alfred C. Redfield dialah yang pertama kali menetapkannya. Suatu hal yang tidak mengherankan lagi, perbandingan atom P : N di perairan dalam adalah 01:15 . Sedang perbandingan P : C di perairan dalam sebesar 1:1000, ini menunjukan bahwa 90% tidak dalam bahan organik, memang ada sebagian terikat sebagai karbonat tetapi relatif kecil. Setiap empat karbon dalam bahan organik, rata-rata satu atom dikombinasikan dengan ion kalsium dan terikat secara biokimia dalam bentuk karbonat. Dalam kaitan suatu sistem antar laut dan atmosfer, kita lihat di atmosfer ada tiga komponen reaktif utama yaitu oksigen , air , dan karbon dioksida, ketiganya berperan dalam pertukaran di udara dan lautan. Aktifitas pertukaran tergantung pada kesetimbangan atau faktor kinetika pada distribusi elemen, yang akhirnya berpengaruh pada komposisi kimia laut. ~ 42 ~ Walaupun beberapa reaksi fotokimia yang terjadi di bagian atas atmosfer yakni pada ketinggian 12 Km, atau yang dikenal sebagai lapisan troposfer (lihat gambar 3.3) sangat mempengaruhi proses geokimia yang terjadi di bumi. Wilayah ini mengandung banyak massa gas dan akibat pengaruh dari siner surya ke bumi maka pertukaran udara di troposfer dan laut mudah terjaling baik. Holland (1978) menyajikan massa udara di daerah troposfer, konstituen ini sangat mempengaruhi pertukaran zat di laut. Tabel 3.6 menyajikan komposisi zat di atmosfer tepatnya pada wilayah troposfer. Tabel 3.6 Komposisi Unsur Udara di Atmosfer No Unsur di udara KONSENTRASI (ppm) 1 2 3 4 5 6 7 8 9 Nitrogen (N2) Oksigen (O2) Argon Air Karbon dioksida Neon Helium Gas Methan (CH4) Krypton 78,084 (±0,004) X 104 20,946 (±0,002) X 104 9340 (± 10) 40 – 4X 104 320 18,18 (±0,04) 5,24 (±0,04) 1,4 1,14 (±0,01) Sumber: Holland (1978). The Chemistry of the Atmosphere and Oceans. Selain jenis unsur yang tercantum dalam tabel 3.6 , ada banyak gas dengan konsentrasi < 1 ppm . Variasi dalam beberapa ini , seperti ozon ( O3 ) , dapat memiliki efek yang signifikan pada organisme , tapi jarang memiliki peran yang terukur dalam mengendalikan lingkungan geokimia. Gas-gas penting (juga disebut langka) merupakan “senyawa inert” tidak memiliki kecendrungan membentuk senyawa walaupun adanya pengaruh sinar surya, atau membentuk pebatuan. Secara pelan-pelan unsur-unsur itu akan terakumulasi di atmosfer dengan bertambahnya waktu. ~ 43 ~ ④ SUMBER MATERIAL DI LAUT U mumnya sumber material alam yang ditransfer kedalam laut berasal dari batuan di daratan dan di dalam laut sendiri. Bahan yang berasal dari batuan di daratan biasanya melalui peluruhan oleh sinar matahari (tumbukan batu) dengan suhu rendah, tapi kalau bersumber dari aktivitas vulkanik (gunung berapi) biasanya lewat proses dengan suhu tinggi. Kemudian material berasal dari polutan sebagai akibat dari macam-macam antropogenik biasanya juga melibatkan suhu dan sirkulasi udara. Banyak jenis material yang menjadi sumber terus menerus masuk ke laut sebagian besar terjadi di daerah permukaan seperti: partikel, bahan terlarut dan gas. Kenyataan perairan laut di dunia pengtransferan material melalui beberapa cara masuk ke badan air laut, yakni melalui aliran sungai (fluvial), udara (atmosfer, seperti uraian bab terdahulu) dan daratan (glacial). Semuanya itu sangat tergantung pada ruang dan waktu. Sebagai contoh transpor melalui atmosfer di daerah lintang rendah adalah sangat kuat, dimana debu yang ada terus-menerus akan masuk ke permukaan laut, sesekali ada tekanan kuat. Material yang berasosiasi di udara di semua permukaan laut satu saat akan tiba di laut , walaupun kadang-kadang konsentrasinya rendah. Bahan yang berasal dari aliran sungai cukup banyak di dunia, tapi yang dari daratan yang ada es (glacial) relatif tidak terlalu banyak. Pemindahan material lewat air dalam bentuk es biasanya dengan cara fisik tergantung pada keadaan iklim. Daerah yang polar biasanya berada di “interglacial” dan daerah yang diselimuti es (gunung es). Garrels dan Mackenzie (1977), memperkirakan material berasal dari pebatuan yang ~ 44 ~ masuk ke samudera melalui aliran sungai ada sekitar 20 X 1014 g Tahun-1, dimana 90% berasal dari antartika. Ada juga transpor material melalui aliran “run-off” masuk ke lingkungan laut. Pemindahan material itu merupakan bagian yang menarik bagi geokimia, halmana pemindahan material melalui “glacial” kurang mendapat perhatian, tapi pemindahan melalui aliran sungai dan atmosfer sangat menarik. Menurut Tissot dan Welte (1984) keberadaan karbon organik di bumi bisa bersumber dari dua sistem siklus yang terjadi, yakni secara biologi dan secara geokimia. Iluistrasi model siklus yang terjadi terlihat pada gambar berikut. Gambar 4.1, Dua Model Siklus Karbon Organik di Bumi Keterangan OM= organic material Sumber: Tissort dan Welte (1984). Transpor Melalui Aliran Sungai Sungai banyak terkandung komponen baik organik maupun nir-organik, ada yang bentuk partikel maupun bahan terlarut. Umumnya material melalui sungai sangat ~ 45 ~ mempengaruhi reaksi kimia di laut, khususnya “trace element”. Suatu data dasar memperlihatkan proses pemasukan material lewat sungai sangat erat keterkaitannya dengan kimia (chemical signals) Material yang ada di air dan lingkungan perairan berasal dari atmosfer dan/atau melalui aliran permukaan tanah (run-off), sirkulasi air tanah dan pemasukan lewat larutan buangan. Larutan dan partikel yang ada di sungai merupakan bahan berasal dari batuan akibat pengikisan oleh sinar matahari, dekomposisi dari bahan organik, dekomposisi bahan di atmosfer (basa dan kering), dan juga pencemaran. Banyak faktor yang membuat komposisi material yang ada di badan air sungai, tetapi intinya semua bahan itu ada dalam bentuk partikel dan terlarut, nanti dalam periode tertentu proses reaksi kimia berlangsung. Pola aliran sungai sangat berhubungan dengan jenis batuan, struktur geologi, bentuk erosi dan sejarah pembentukan kerak bumi. Sistem pengaliran yang berkembang pada permukaan bumi secara regional dikontrol oleh kemiringan lereng, jenis dan ketebalan lapisan batuan, struktur geologi, jenis dan kerapatan vegetasi serta kondisi iklim. Bentuk erosi sangat tergantung struktur partikelnya. Pola pengaliran pada batuan yang berlapis sangat tergantung pada kondisi topografi, geologi (jenis, sebaran, ketebalan dan bidang perlapisan batuan serta geologi struktur seperti sesar, kekar, arah dan bentuk perlipatan), iklim, serta vegetasi yang terdapat di dalam DAS bersangkutan. Zat kimia utama yang masuk ke sungai dan dialirkan ke laut secara global di sajikan pada tabel 4.1 berikut. Kandungan rata-rata yang ada di sungai dan di air laut jumlahnya berbeda. Sangat menarik perhatian , halmana di sungai umumnya didominasi oleh kalsium dan bikarbonat, sedangkan di air laut adalah natrium (sodium) dan klorida yang punya peran penting pada kelarutan zat-zat lain, seperti garam. ~ 46 ~ Tabel 4.1 Komposisi Zat Utama di Sungai Mengalir ke Laut zat Na+ K+ Ca2+ Hg2+ ClSO42HCO-3 SiO3-2 TDS Atlantik Hindia Kutub Utara 4,2 8,5 8,8 1,4 2,5 1,2 10,5 21,6 16,1 2,5 5,4 1,3 5,7 6,8 11,8 7,7 7,9 15,9 37 94,9 63,5 9,9 14,7 5,1 78,9 154,9 123,7 Pasifik Rata-rata di sungai Rata-rata di air laut 5,2 1,2 13,9 3,6 5,1 9,2 53,4 11,7 195,3 5,3 1,5 13,3 3,1 6,0 8,7 51,7 10,7 101,5 10733 399 412 1294 19344 2712 142 - Sumber: Chester dan Jickells ( 2012) TDS = Total padatan terlarut Hakekatnya, variasi zat yang ada di sungai lebih banyak di bandingkan yang terkadung di air laut, hal itu dapat dilhat pada tabel diatas. Maybeck (1981) mengatakan secara garis besar ranking variasi zat yang terlarut di sungai adalah sebagai berikut: Cl-> SO42-> Ca2+= Na+> Mg2+> HCO3-> SiO2> K+ . Sejumlah perairan di muka bumi kita intinya berbasis pada jumlah ion yang dikandung ( salinitas) dan saling berintegrasi deengan pelbagai variasi ion yang ada atau rasio ion (ionic ratios). Gibbs (1970) telah melakukan kajian tentang dua sifat air yang berlainan, dan sebagai kesimpulan zat Ca2+ banyak di air tawar sedang Na+ lebih banyak di perairan salinitas yang tinggi. Dia juga telah meneliti tentang anion di kedua perairan yang sifat berbeda, yaitu unsur HCO3untuk air tawar dan Cl- untuk perairan air laut. Zona permukaan air umumnya ion komponen disitu berasal dari luar. Seperti adanya curah hujan (precipitation) dan hasil pengikisan batuan oleh cuaca, dan ada juga proses alamiah yang terjadi di dalamnya. Menurut Gibbs (1970) selama penguapan (evaporation) akan terjadi peningkatan ~ 47 ~ kristalisasi kadar garam di perairan, sehingga akan mempengaruhi nilai salinitasnya. Hasil riset Stallard dan Edmond (1983), menunjukan sungai di lembah Amazon kadar garamnya relatif tinggi, diakibatkan penguapan oleh adanya panas matahari dan juga adanya unsur karbonat. Kalau kita gunakan ion Cl- sebagai referens di laut, maka siklus garam di permukaan laut Amazon dapat di simpulkan yang sangat berlimpah adalah Na +, Mg2+ dan SO42dan sesudah itu Cl- ( Stallard dan Edmond, 1981), dan biasanya yang menjadi penghambat siklus ini adalah aliran sungai yang berasal dari lembah. Dalam kenyataan muara sungai dekat pantai , material yang dominan adalah Na (sodium), yaitu meliputi 50% berada di daerah permukaan. Kemudian ada 15 % zat Ca dan K, ini merupakan akibat siklus asli di sungai, dan kurang lebih 3% akan hilang masuk ke daerah laut. Menurut Chester (1990), umumnya sungai yang membawa material Na dan Mg sangat sedikit jika di bandingkan dengan kandungan sebagai hasil peleburan batuan oleh sinar matahari. Gibbs (1970) mendukung bahwa kandungan Na, K, Mg dan Ca sekitar 80% berasal dari tanah dibawah sungai. Hakekatnya, disaat keadaan di dominasi curah hujan berlimpah atau luapan “presipitasi” sangat tinggi, total ion relatif rendah, dimana perbandingan Na/(Na+Ca) juga Cl/(Cl+HCO3-) akan relatif tinggi. Dalam keadaan demikian peluruhan akibat pemanasan sinar matahari bersifat rendah dan percepatan penguapan yang terjadi adalah rendah. Sebaliknya bila di dominasi penguapan dan proses kritalisasi, maka total ion sangat tinggi dan rasio Na/(Na+Ca) juga Cl/(Cl+HCO3-) adalah tinggi. Keadaan ini memperlihatkan peluruhan kimia akibat sinar matahari sangat intensif dan kecepatan penguapan tinggi. Tetapi bila di dominasi dengan bebatuan, jumlah ion tidak terlalu banyak serta rasio Na/(Na+Ca) juga Cl/(Cl+HCO3-) juga relatif rendah. Pada kondisi demikian, daerah itu terjadi ~ 48 ~ peluruhan berasal dari sinar matahari sangat intensif dan penguapan rata-rata rendah. Bertolak dari dimensi dominan seperti uraian diatas, maka kondisi permukaan air menyangkut keberadaan ion dan perbandingan zat-zat tersebut merupakan bahan diskusi yang menarik. Sebagai ilustrasi respek dari ketiga keadaan tersebut di sungai disajikan pada tabel 4.2. (hasil riset Maybeck, 1981) Berangkat dari tabel tersebut, sungai yang mengalir ke teluk Kanada relatif air murni dengan kandungan total ion hanya sekitar 19 mg l-1 , dimana kehadiran elemen utama melalui hujan, kecuali tidak ada hujan , maka tidak ada pemasukan ion. Kalau di sungai Mackenzie tipe sungai didominasi batuan, kandung zat yang masuk berasal dari sedimen dan kristalisasi dari udara, nilai kandung total ion ada sebanyak 207 mg l-1 . Beberapa sungai kandungan total ion dan rasio Na(Na+Ca) relatif tinggi, seperti di sungai Colorado kandungan total ion adalah hampir 700 mg l-1 , dan kandungan Na+ agak lebih tinggi sedikit dari ion Ca2+ . Dengan demikian sungai tersebut bersifat “saline” (agak asin) karena terjadi penguapan dan kristalisasi. Tabel 4.2 Rata-rata Konsentrasi Elemen Utama di Sungai No Mengalir Kebeberapa Tipe Penampungan. (mg l-1) Sungai Sungai Colorado Elemen Aliran sungai ke teluk Kanada Mackenzie didominasi pebatuan 1 Na+ 0,60 7,0 2 K+ 0,40 1,1 3 Ca2+ 3,3 33 4 Mg2+ 0,7 10,4 5 Cl 1,9 8,9 6 SO421,9 36,1 7 HCO310,1 111 8 TIC 18,9 207 Keterangan: TIC= total ionic content Sumber : Chester dan Jickells ( 2012) ~ 49 ~ dengan situasi penguapan & kristalisasi 95 5 83 24 82 270 135 694 Indonesia dikenal sebagai negara kepulauan memiliki banyak sungai yang bermuara ke perairan laut Nusantara, dari sekian banyak sungai hanya ada 10 sungai yang dikategorikan sungai terpanjang, yaitu: 1. Sungai Kapuas, di Kalimantan barat, dengan panjang total hingga 1.178 km, Sungai Kapuas tercatat sebagai sungai terpanjang di Indonesia, 2. Sungai Mahakam terletak di Kalimantan Timur, dengan panjang 920 km, 3. Sungai Barito terletak di Kalimantan tengah dengan panjang 909 km, 4. Sungai Batanghari terletak di pulau Sumatera tepatnya di provinsi Jambi, memiliki panjang sungai 800 km dan lebar sungai berkisar antara 200 – 650 meter, 5. Sungai Musi terletak di Palembang (Sumatera Selatan) memiliki panjang 750 km, 6. Sungai Membramo terletak di Papua. Sungai ini memiliki panjang sampai 670 km, 7. Sungai Bengawan Solo, terletak di pulau Jawa dengan panjang sungai mencapai 548,53 km yang mengalir di Provinsi Jawa Tengah dan Jawa Timur, 8. Sungai Digul terletak di Papua memiliki panjang 546 km, 9. Sungai Indragiri terletak di dengan panjang sungai ini mencapai 500 km, dan ke 10. Sungai Kahayan terletak di Palangkaraya Kalimantan tengah memiliki panjang hingga 250 km. Semua sungai-sungai melewati aliran dengan kondisi pebatuan, hujan dominan dan proses penguapan relatif tinggi. Dengan demikian rata-rata sungai tersebut kandungan ion total relatif tinggi. Di Indonesia cukup banyak sungai kecil yang bermuara ke daerah pantai, seperti Bali, 15 sungai; Bengkulu, 22 sungai; DKI, 13 sungai; Jambi, 10 sungai; di Jawa barat ada 27 sungai; di Jawa tengah, 21 sungai; di Jawa Timur ada sebanyak 22 sungai; di Kalimatan barat, 17 sungai; di Kalimantan Selatan, 25 sungai; Kalimatan tengah, 8 sungai, di Kalimatan timur, 10 sungai; di Lampung, 10 sungai; di Maluku, 10 sungai; di Aceh, 10 sungai; di NTB ada sebanyak 19 sungai; Di Papua ada 10 ~ 50 ~ sungai; di Riau, 10 sungai; Sulawesi Tengah ada 11 sungai ; Sulawesi Selatan, 12 sungai ; Sulawesi tengara, 8 sungai; Sulawesi utara ada sebanyak 15 sungai; Sumatera Barat, 23 sungai; Sumatera Selatan, 11 sungai; Sumatera Utara, 11 sungai dan Yogyakarta ada sebanyak 18 sungai. Dikatakan sebagai sungai kecil karena ukuran panjang relatif tidak terlalu panjang dan pada umumnya kedalam berkisar pada 0,2-3 m. Namun demikian sungai-sungai tersebut ada dominan terjadi hujan atau adanya “presipitasi”; dominasi daerah bebatuan dan dominasi penguapan dan proses kritalisasi. Ratusan sungai yang mengalir ke perairan laut nusantara suatu pertanda material seperti: partikel, material terlarut dan senyawa polutan lainnya sangat berpotensi. Sehingga tingkat kualitas dari sudut pandang geokimia akan cepat berubah di setiap tahun. Berbagai referens menyatakan ada hubungan erat kondisi geologi didaerah penangkapan air dengan kimia perairan. Seperti seorang profesor bidang geokimia yang bernama M. Maybeck, mengatakan bahwa kecepatan pengadukan kimia berasal dari batuan kerak kulit bumi yaitu: pertama, kimia yang teraduk berasal dari sedimen memberikan kontribusi sebesar 90%, dan kurang lebih 66% merupakan turunan dari deposit karbonat. Kedua, kecepatan peluruhan oleh adanya matahari memperlihatkan bahwa penguapan > batuan karbonat > batuan kristal > butiran batu karang dan pasir. Keadaan lingkungan di Indonesia dibelakangan ini sangat dikuatirkan, dimana banyak hutan dan daerah pertanian berubah fungsi, terkadang terjadi “tandus” bahan geologi utama adalah partikel tanah dan batu. Apabila partikelpartikel itu diangkut oleh air permukaan di waktu hujan (runoff) maka akan tiba di muara sungai di daerah pantai, dalam periode tertentu muara sungai akan membentuk delta. ~ 51 ~ Delta merupakan suatu wilayah perairan terbentuk dari endapan sedimen yang dialirkan oleh sungai, dalam waktu lama terjadi deposit yang menumpuk sehingga di muara sungai ada tumpukan tanah yang membentuk huruf “Y” (lihat gambar 4.2). Seorang sejarawan terkenal yaitu Herodotus, melihat bentuknya delta yang terjadi disungai Nil seperti huruf “Y” , mereka mengatakan itu bentukan Yunani sehingga mereka simbol “Δ”, sampai sekarang ini simbol ini dipakai di dunia. Gambar 4.2. Pembentukan Delta Pembentukan delta di daerah pantai membawa konsekuensi garis pantai akan berubah dan komposisi kimia juga berubah, sehingga total ion berubah pula. Dalam tabel berikut disajikan komposisi ion utama di sungai yang mengalir ke perairan laut setelah melewati berbagai tipe pebatuan. Tabel 4.3. Komposisi Ion Utama di Sungai Dialirkan ke Laut (mg l -1) ion Batuan Plutonik dan metamorpik tinggi Na+ Memang sejak semula ion ini sudah ada di Batuan vulkanik ~ 52 ~ Batuan sedimen pengaruhi oleh air laut K+ 1,0 1,5 1,0 2+ Ca 4,0 8,0 30 2+ Mg 1,0 3,0 8,0 ClMemang sejak semula ion ini sudah ada dipengaruhi oleh air di laut SO422,0 6,0 25 HCO3 15, 45 100 TIC 30 70 175 Sumber: Maybeck (1981). TIC = total ionic content. Material yang merupakan dari kerak bumi dan peluruhan dari batuan oleh sinar matahari diidentifikasi sebagai ∑ konsentrasi kation, diberi simbol TZ +. Stallard dan Edmond telah melakukan kajian, alhasil telah teridentifikasi bahwa: ⁕ Sungai yang mengandung ∑ konsentrasi kation dengan kisaran 0< TZ+<200 µeq l-1 adalah sungai yang relatif kaya silika sedang elemen utama lain kurang. Umumnya aliran air melalui daerah pebatuan . ⁕ Sungai yang mengandung ∑ konsentrasi kation dengan kisaran 200< TZ+<450 µeq l-1 adalah sungai yang silikanya berasal dari pengikisan batuan karang, dan sungai tersebut kaya akan kandungan silika. Pada sungai ini tendensinya muatan kation kurang banyak, relatif ada di dalam Na dan K, juga relatif ada di dalam Ca - Mg dibandingkan dengan sungai yang penuh pebatuan. ⁕ Sungai yang mengandung ∑ konsentrasi kation dengan kisaran 450< TZ+<3000 µeq l-1 adalah sungai dengan airnya melalui sedimen laut atau daerah tanah dasar merah (red bed), kaya akan kation dari karbonat asalnya dari batu karang lunak yang mudah hancur dan sedikit ada penguapan. Sungai ini memiliki kandungan Ca dan Mg dan salinitasnya cukup tinggi. Karena melalui pebatuan karang yang mudah ~ 53 ~ hancur dan kurang terjadi penguapan maka ion SO42- adalah tinggi. ⁕ Sungai yang mengandung ∑ konsentrasi kation dengan kisaran 4TZ+>3000 µeq l-1 adalah sungai yang terusmenerus penguapan dan kaya Na dan Cl. Umumnya elemen dominan dan “ trace elements” yang ada di sungai nantinya akan dialiri ke daerah pantai (laut) dianggap sebagai partikel di sungai (the particulate river signal), dan beberapa referens mengatakan sebagai bahan partikel sungai atau RPM (river particulate material). Bahan partikel ini berasal dari padatan yang tersuspensi di badan air, misalnya suspensi sedimen. RPM, mengandung variasi komponen yang terserap dalam bentuk berbagai ukuran partikel. Komponenkomponen itu berasal dari pelbagai sumber pengikisan batuan, termasuk: pertama, daerah tanah yang gundul (feldspars), daerah yang kondisi setengah subur (amphiboles), daerah yang banyak patahan batu (pyroxenes) dan daerah yang banyak mineral (micas). Kedua, aluminosilika, seperti mineral tanah liat; kuartz; karbonat; hydro oksida dari Al, Fe dan Mn; serta pelbagai komponen organik. Komposisi mineral yang ada pada RPM sesungguhnya agak homogen bercampur dengan tanah dari sungai, tetapi setiap sungai memiliki mineral spesifik di dalam RPM. Dalam studi Konta (1985) melaporkan bahwa: ① Mineral di tanah lebih dominasi oleh komponen kristalin, walaupun distribusi secara sendiri-sendiri berbeda. Intinya, sungai di daerah tropis relatif tinggi peluruhan mineral oleh sinar matahari, sungai ini termasuk sungai tipe kaolin pada RPM, sedang sungai di daerah subtropis termasuk tipe “mortmorillonite”. ② Tanah kuarsa tidak ada sungai yang tidak memiliki RPM. ~ 54 ~ ③ Mineral kristalin pada RPM termasuk asam plagioklas, K dan bahan-bahan dari daerah setengah subur, dan ④ kemungkinan ada juga calcite dan atau dolomit pada RPM. Sungai merupakan media transpor material kearah laut yang telah berlangsung jutaan tahun silam. Karbon organik seperti terlukis pada gambar 4.1 bisa berlansung selama proses transport material baik lewat aliran air permukaan tanah (run-off), saluran air maupun sungai. Memang prinsip dasar teori fluida, air akan mengalir dari dataran tinggi (tempat tinggi) ke bagian wilayah yang rendah. Selama dalam proses pengaliran air sejak mengalirnya air permukaan tanah (run-off) maupun dari daerah pengunungan atau dataran tinggi, proses pengikisan di pebatuan maupun partikel tanah akan membawa pelbagai bahan kimia termasuk mineral. Disamping itu ada juga material yang diangkut oleh angin melalui udara. Zat-zat kimia yang diangkut oleh sungai maupun angin lewat atmosfer akan mengendap di dasar samudera menjadi suatu lapiran kerak samudera. Dengan adanya bantuan mikroba bahan-bahan itu akan terakumulasi di lapisan sedimen. Semua mineral yang disebut ini akan dialirkan oleh sungai ke arah laut, sehingga perairan laut, khususnya daerah pantai komposisi elemen sangat bervariasi sangat tergantung dari tipe tanah, kontur daratan dan aktivitas yang terjadi di kontinental. Umumnya aliran sungai melewati lokasi pemukiman, kluster industri maupun daerah pertanian akan membawa bahan organik yang cukup banyak, sehingga mempengaruhi komposisi kimia di perairan. Chester (1990) mengatakan umumnya sungai di dunia terdapat komposisi seperti pada tabel 4.4 ~ 55 ~ Tabel 4.4. Komposisi rata-rata Unsur di bebatuan, Tanah dan yang Terlarut di Sungai Daratan Sungai Unsur Batuan Tanah Terlarut Partikel -1 -1 -1 (µg g ) (µg g ) (µg l ) (µg g-1) Ag Al As Au B Ba Br Ca Cd Ce Co Cr Cs Cu Er Eu Fe Ga Gd Hf Ho K La Li Lu Mg Mn Mo Na Nd Ni P Pb Pr Rb Sb Se Si Sm Sr Ta 0,07 69300 7,9 0,01 6,5 445 4 4500 02 86 13 71 3,6 32 3,7 1,2 35900 16 6,5 5 1,6 24400 41 42 0,45 16400 720 1,7 14200 37 49 610 16 9,6 112 0,9 10,3 275000 7,1 278 0,8 0,05 71000 6 0,001 10 500 10 15000 0,35 50 8 70 4 30 2 1 40000 20 4 0,5 14000 40 25 0,4 5000 1000 1,2 5000 35 50 800 35 150 1 7 330000 4,5 250 2 0,3 50 1,7 0,002 18 60 20 13300 0,02 0,08 0,2 1 0,035 1,5 0,004 0,001 40 0,09 0,008 0,01 0,001 1500 O,o5 12 0,001 3100 8,2 0,5 5300 0,04 0,5 115 0.1 0,007 1,5 1 0,004 5000 0,008 60 <0.002 ~ 56 ~ 0,07 94000 5 0,05 70 600 5 21300 1 95 20 100 6 100 3 1,5 48000 25 5 6 1 20000 45 25 0,5 11800 1050 3 7100 35 90 1150 100 8 100 2,3 18 285000 7 150 1,25 Tb Th Ti Tm U V Y Yb Zn 1,05 9,3 3800 0,5 3 97 33 3,5 127 0,7 9 3000 0,6 2 90 40 90 0,001 0,1 10 0,001 0,24 1 0,004 30 1 14 5600 0,6 3 170 30 3,5 250 Sumber : Martin &Whitfield (1983) disitasi oleh Chester (1990) Material yang ada di sungai sebagai elemen kimia dengan komposisi yang bervariasi masuk ke laut, tidak semua sungai langsung ke arah laut terbuka. Tapi ada juga kawasan pantai didiami daerah estuari, dimana di wilayah (zona) ini merupakan filter alamiah. Unsur-unsur seperti terterah pada tabel 4.4. bila masuk di zona estuari akan tercampur, dan dalam waktu beberapa hari atau mingguan ada yang berbentuk larutan dan partikel, semuanya bisa tenggelam ke daerah itu. Namun sedimen yang berasal dari aliran “run-off” akan masuk ke sistem estuari bersifat statis, tetapi bisa oleh adanya proses kimia dan biologi masuk dalam suatu siklus sehingga menjadi deposit komponen. Secara singkat ilustrasinya di sajikan pada gambar 4.3 berikut. ZONA PERCAMPURAN DI ESTUARI S ‰ 35 SUNGAI LAUT S‰ 0 p kd d SEDIMEN ESTUARINE REACTIVITY Gambar 4.3. Skema Pemasukan Material ke Wilayah Estuari Zona estuari memiliki peran penting dalam pembentukan/penyusunan geokimia di laut, khususnya ~ 57 ~ sumber material itu berasal dari sungai, tanda ini menunjukan material dalam bentuk partikel maupun terlarut terasosiasi secara fisika, kimia dan biologi di daerah estuari. Pemisahan material dalam fase partikel dan terlarut didefinisikan koefisien alamia adalah: kd = X/C, dimana X merupakan konsentrasi peluang perubahan elemen pada fase partikel, sedang C adalah konsentrasi elemen terlarut. Muara sungai dekat estuari, biasanya sirkulasi terjadi akibat adanya aliran/arus sungai, tetapi di estuari dekat mulut sungai dapat terjadi lapisan air berkadar garam tinggi, sering disebut “salt wedge of estuary” (lapisan tebal garam estuari). Sifatnya kadar garam itu berada dibawah lapisan air tawar, karena densitas masing-masing lapisan berbeda, maka akan terjadi dua lapisan di mulut sungai. Adanya aliaran pasang air laut memungkinkan percampuran secara bertahap lapisan air tawar di permukaan perairan muara sungai, jika ada gerakan ombak kemungkinan akan terjadi lapisan air asin naik ke lapisan air tawar, sehingga terjadilah percampuran air, maka lapisan air tawar di permukaan akan menurun densitasnya , sebaliknya salinitasnya naik. Meade (1972) dan Potsma (1980) mengatakan distribusi suspensi partikel di eustuari sangat dipengaruhi oleh dinamika sirkulasi yang terjadi. Dalam kenyataan tenaga arus pasang dapat membuat goyangan di muara sungai, pada keadaan demikian memungkinkan terjadi pengadukan tidak penuh, banyak ahli mengatakan/istilahkan “partially stratified”. Pecampuran yang terjadi akibat dorongan atau difusi oleh arus eddy, maka lapisan air asin di bawah akan ke permukaan (upward), sebaliknya air tawar di permukaan akan ke bawah (downward). Suspensi yang diangkut oleh sungai melewati daerah estuari dan akhirnya terjadi percampuran ke perairan laut. Secara garis besar konsentrasi bahan terlarut di sungai dan di laut di bumi kita ini, disajikan di tabel 4.5 ~ 58 ~ Tabel 4.5. Konsentrasi Zat Terlarut di Sungai dan Laut di belahan bumi SUNGAI TERLARUT µg l-1 Ag Al As Au B Ba Br Ca Cd Ce Co Cr Cs Cu Er Eu Fe Ga Gd Hf Ho K La Li Lu Mg Mn Mo Na Nd Ni P Pb Pr Rb Sb Sc Si Sm Sr Ta Tb Th Ti Tm U V Y Yb Zn 0,3 50 1,7 0,002 18 60 20 13.300 0,02 0,08 0,2 1 0,035 1,5 0,004 0,001 40 0,09 0,008 0,01 0,001 1500 0,05 12 0,001 3100 8,2 0,3 3300 0,04 0,5 115 0,1 0,007 1,5 1 0,004 5000 0,008 60 <0,002 0,001 0,1 10 0,001 0,24 1 0,004 30 PARTIKEL µg g-1 0,07 94000 5 0,05 70 600 5 21500 1 95 20 100 6 100 3 1,3 4800 23 5 6 1 20000 45 25 0,3 11800 1050 3 7100 35 90 1150 100 8 100 2,5 18 285000 7 150 1,25 10 14 5600 0,4 3 170 30 3,5 250 PERAIRAN LAUT TANAH DI LAUT BADAN AIR DALAM (µg g-1) µg l-1 0,04 0,3 1,5 0,004 4440 20 67000 41200 0,01 0,001 0,05 0,3 0,4 0,1 0,0008 0,0001 2 0,03 0,0007 0,007 0,0002 380000 0,003 180 0,0002 6 1,29 X 10 0,2 10 2 1,077 X 10 0,003 0,2 60 0,003 0,0006 120 0,24 0,0006 2000 0,0005 8000 0,002 0,0001 0,01 1 0,0002 3,2 2,5 0,0013 0,0008 0,1 Sumber : Chester dan Jickells ( 2012) ~ 59 ~ 0,1 95000 13 0,003 220 1500 100 10000 0,23 100 55 100 5 200 2,7 1,5 60000 20 7,8 4,5 1 28000 45 45 0,5 18000 6000 8 20000 40 200 1400 200 9 110 0,8 20 283000 7 250 1 1 10 5700 0,4 2,0 150 32 3 120 Masuk Material dari Atmosfer Material yang ada di daerah troposfer ada dalam ukuran 0,1 - 10µm, dan lama tinggal di udara relatif singkat kurang lebih beberapa hari. Sangat berbeda dengan material yang diangkut oleh sungai, harus melalui peluruhan dan modifikasi di zona estuari. Hanya yang menarik material yang diangkut oleh udara di atmosfer dapat menyebar kemana-mana dan langsung jatuh ke permukaan laut. Material yang ada di udara terus meningkat di akhir-akhir ini, karena adanya pencemaran dan aktivitas gunung berapi (vulkanik). Material di udara berbentuk padatan dan cairan yang tergabung sebagai gas, biasanya dikenal sebagai “aerosol”. Menurut Prospero dkk (1983) bahwa tipe aerosol yang udara dapat diklasifikasi: a) aerosol alamiah, seperti; residu semprotan, debu mineral yang ditiupkan angin, debu gunung berapi, bahan biogenik, asap dari pembakaran lahan dan partikel berubah jadi gas. b) antropogenik aerosol seperti: emisi partikel antropogenik dan bahan hasil konversi gas, misal buangan industri ke udara. Atmosfer adalah lapisan gas yang melingkupi sebuah planet, termasuk bumi, dari permukaan planet tersebut sampai jauh di luar angkasa. Di bumi, atmosfer terdapat dari ketinggian 0 km di atas permukaan tanah, sampai dengan sekitar 560 km dari atas permukaan bumi. (lihat 3.3). Atmosfer Bumi terdiri atas nitrogen (78.17%) dan oksigen (20.97%), dengan sedikit argon (0.9%), karbondioksida (variabel, tetapi sekitar 0.0357%), uap air, dan gas lainnya. Lapisan troposfer berada pada level yang terendah dari atmosfer, lapisan ini dianggap sebagai bagian atmosfer yang paling penting, karena berhubungan langsung dengan permukaan bumi yang merupakan habitat dari berbagai jenis mahluk hidup termasuk manusia, serta sebagian besar iklim berlangsung pada lapisan troposfer. Susunan kimia udara troposfer terdiri dari 78,03% nitrogen, 20,99 oksigen, 0,93% ~ 60 ~ argon, 0,03% asam arang, 0,0015% nenon, 0,00015% helium, 0,0001% kripton, 0,00005% hidrogen, serta 0,000005% xenon. Secara global Troposfer terbagi ke dalam empat lapisan, yaitu : ① Lapisan Udara Dasar, tebal lapisan 1 – 2 meter di atas permukaan bumi. Pada lapisan udara ini tergantung dari keadaan fisik muka bumi, dari jenis tanaman, ketinggian dari permukaan laut dan lainnya. Biasanya lapisan inilah yang disebut sebagai iklim mikro, yang mempengaruhi kehidupan tanaman dan ekosistem laut. ② Lapisan Udara Bawah, lapisan udara ini dinamakan juga lapisan-batasan planiter (planetaire grenslag, planetary boundary layer). Tebal lapisan ini 1 – 2 km. Di sini berlangsung berbagai perubahan suhu udara dan juga menentukan iklim serta dalam lapisan ini polutan relatif banyak (terlarut dan partikel debu) ③ Lapisan Udara Adveksi (Gerakan Mendatar), lapisan ini disebut juga lapisan udara konveksi atau lapisan awan, yang tebalnya 2 – 8 km. Di dalam lapisan udara ini gerakan mendatar lebih besar daripada gerakan tegak. Hawa panas dan dingin yang beradu di sini mengakibatkan kondisi suhu yang berubah-ubah. Pada lapisan ini peluang besar terjadi konversi kimia ke bentuk gas. ④ Lapisan Udara Tropopouse, merupakan lapisan transisi antara lapisan troposfer dan stratosfer terletak antara 8 – 12 km di atas permukaan laut (dpl). Pada lapisan ini terdapat derajat panas yang paling rendah, yakni antara – 46 o C sampai – 80o C pada musim panas dan antara – 57 o C sampai – 83 o C pada musim dingin. Suhu yang sangat rendah pada tropopouse inilah yang menyebabkan uap air tidak dapat menembus ke lapisan atmosfer yang lebih tinggi, karena uap air segera mengalami kondensasi sebelum mancapai tropopouse dan kemudian jatuh kembali ke bumi dalam bentuk cair (hujan) dan padat (salju, hujan es). Di zona ini biasanya terjadi percampuran antara material terlarut, ~ 61 ~ partikel primer, pertukaran agregat dan kondensasi. (lihat gambar 4.4). Sebagai gambaran hubungan antara proses yang terjadi di udara dan material yang naik ke atmosfer, disajikan kedalam gambar 4.4 berikut. KIMIA BERUPA GAS DAN MUDAH MENGUAP UAP PANAS PERLAHAN BERUBAH UAP KONDENSASI PARTIKEL PRIMER DEBU OLEH ANGIN EMISI UAP AIR LAUT GUNUNG BERAPI AWAL PERCAMPURAN TERJADI KONDENSASI KOAGULASI PARTIKEL DARI TUMBUHAN Menetes PERTUKARAN AGREGAT KOAGULASI KOAGULASI HUJAN SEDIMENTASI 0,002 0,01 0,1 PARTIKEL µm PARTIKEL HALUS 1 2 10 100 PARTIKEL KASAR Gambar 4.4. Skema Proses Kehadiran Partikel dan Endapan ke Laut (Modifikasi dari Chester, 1990) Bertolak dari gambar diatas, intinya partikel yang naik ke atmosfer dikategorikan ke dalam dua kelompok besar, yakni: partikel halus berdiameter < 2 dan partikel kasar berukuran >2. Partikel yang naik ke troposfer sumber utama berasal dari proses pembakaran seperti: kegiatan antropogenik (buangan industri, dan sebagainya), emisi dari letusan gunung berapi, pembakaran lahan dan hutan. Partikel-partikel ini terakumulasi di udara, dan ada juga berbentuk gas akan terjadi coagulasi menjadi partikel primer. ~ 62 ~ Partikel kasar naik ke troposfer oleh adanya kegiatankegiatan yang terjadi di permukaan bumi, itupun tergantung pada kondisi suhu, misalnya debu dari kerak bumi dan uap garam dapat terjadi pada proses suhu rendah, sedang dengan suhu tinggi seperti debu berasal pembakaran industri dan buangan gas kendaraan bermotor. Maring & Duce (1997) telah melakukan penelitian tentang aerosol di udara seputar Atlantik utara, dimana dia temui partikel berdiameter .40 µm; ada semburan uap air laut; partikel debu mineral; partikel yang memang sudah ada di troposfer; dan ada partikel berdiameter <0,06 µm. Partikel yang sudah ada di troposfer mengandung banyak jenis kimia tetapi lebih di dominasi adalah sulfat (85%). Sedang partikel Tabel 4.6. Estimasi Emisi Partikel di Atmosfer ( 10 12 g thn-1) SUMBER 1 Kegiatan Manusia: Partikel langsung Partikel bentuk gas: • Dikonversi menjadi Sulfat • lain-lain Total Di alam: Partikel langsung: • Pembakaran hutan • Emisi gunung berapi • Vegetasi • Debu mineral (hancuran oleh matahari) • Garam dari laut Partikel bentuk gas: •Dikonversi menjadi Sulfat • Lain-lain Total Jumlah Keseluruhan Produksi Global 2 3 30 200 30 280 5 25 250 500 200 36 10 75 300 1000 335 135 1250 1530 Keterangan: (1) Prospero dkk, (1983); (2) Nriagu (1979) dan (3) Lantzy & Mackenzi (1979) disitasi oleh Chester (1990). ~ 63 ~ yang berukuran <0,06 µm diperkirakan dari debu daratan, uap asin dari laut, proses biologi di darat, dan polutan, semua partikel itu naik ke troposfer terjadi koagulasi. Semua partikel yang ada di troposfer (terkoagulasi) akan jatuh ke laut oleh air hujan. Sebagaimana uraian diatas jelas bagi kita bahwa material gas dan partikel yang masuk ke atmosfer berasal dari alam dan aktivitas manusia (antropogenik), dimana proses yang berlangsung bisa terjadi dengan suhu rendah atau tinggi tergantung pada zat itu berikatan dengan inangnya. Beberapa sumber material yang naik ke atmosfer dapat berasal dari alam dan antropogenik, diuraikan sebagai berikut: Sumber alamiah Berasal dari kerak bumi, muka bumi kita dapat menyuplai partikel dan gas ke atmosfer. Umumnya partikel (tumbukan batu) sebagai deposit di permukaan bumi akan terangkut melalui cara mekanik yaitu adanya angin. Komponen-komponen ini adalah penting dan banyak sebagai aerosol di permukaan laut. Berasal dari laut, sama seperti kerak bumi dapat berbentuk partikel dan gas. Material partikel dapat terbentuk dari garam laut lewat proses mekanik (secara fisik). Penguapan dari permukaan laut akan menjadi bentuk gas dan masuk ke atmosfer. Demikian juga dari aktivitas gunung berapi berupa erupsi (pembakarannya dengan suhu tinggi) dimana erupsinya dapat menyuplai material partikel, seperti abu bersama-sama gas . Kemudian dalam fase gas lewat proses kondensasi bisa menjadi elemen yang mudah menguap. Di daerah biosphere, dapat menyuplai material ke atmosfer, seperti vegetasi melalui pembakaran dengan suhu tinggi, dan juga bisa berasal adanya penguapan dari tumbuhan dipermukaan bumi dan dari tanah. ~ 64 ~ Kemungkinan pula bisa dari luar angkasa, tetapi sangat kecil jumlahnya masuk ke atmosfer, seperti meteor kecil (cosmic spherules) dan juga bisa radioaktif berasal dari sinar meteor. Sumber antropogenik Material berasal dari antropogenik masuk ke atmosfer dalam bentuk partikel dan gas, seperti hasil pembakaran fosil (minyak bumi), tambang dan proses penggilingannya, buangan bersifat debu, produk kimia, penggunaan kimia di bidang pertanian dan dapat juga berasal dari industri serta aktivitas sosial lainnya. Secara umum emisi yang naik ke atmosfer sebagai siklus debu di alam disajikan pada tabel 4.7 berikut ini. Tabel. 4.7 Siklus Debu secara Global di Troposfer Rata-rata Deposit 10-6 g cm2 thn-1 1012 g thn-1 Wilayah Laut Angin pasat di Bagian Utara Angin pasat di Atlantik Utara Atlantik Selatan Samudera India Pasifik Utara: - Barat Pasifik Utara - Timur dan tengah Pasifik utara Pasifik Selatan Seluruh Pasifik Keseluruhan Perairan Laut Sumber: Prospero dkk (1983) 82 85 450 12 100 – 400 18 – 37 336 5000 11-62 5-64 300 30 18 350 816 – 1135 Tabel diatas memperlihatkan bahwa debu di daerah barat pasifik utara ( ± 300 x 1012 g thn-1), asalnya dari padang pasir Asia, sama halnya di Atlantik utara tropis berasal dari padang Sahara. Intinya debu secara global lebih kurang berkisar (800 – 1100) x 1012 g thn-1. ~ 65 ~ Jumlah mineral aerosol yang ada pada atmosfer di atas Samudera Atlantik sebagian besar akan jatuh ke perairan sebagai elemen di laut. Material yang tertangkap di udara sesungguhnya bersumber dari daerah daratan seputar samudera Atlantik yang kemudian adanya tiupan angin tersebar ke daerah lain (Chester, 1990). Untuk gambaran global kandungan mineral aerosol di daerah kutub utara. Atlantik dan kutub selatan dapat dilihat pada tabel 4,8 Tabel 4.8 Mineral Dalam Aerosol di Kutub Utara, Atlantik dan Kutub Selatan Wilayah Laut Konsentrasi mineral aerosol -3 ( µg m dalam udara) Bagian kutub Utara: Variable: kabut - Atlantik utara bagian barat -0,1 — -2,5 - Atlantik utara, angin pasat <1.0 - > 103 di timur barat daya - Atlantik selatan, angin -0,1 — -1,0 pasat di Selatan timur daya - Atlantik Selatan, Bagian <0,1 barat Bagian Kutub Selatan <0,01 Sumber: Chester (1990) Wilayah kutub utara banyak partikel di atmosfer sehingga udaranya mirip kabut karena adanya percampuran antara mineral dan polutan yang berasal Eurasia (Amerika bagian timur dan Eropa tengah). Kalau di Atlantik utara bagian barat ( pada lintang utara 650 – 400 ) konsentrasi mineral aerosol di udara diperkirakan < 0,5 µg m-3 , sebagian besar bahan-bahan itu berasal dari polutan yang ada di Amerika dan Eropa. Konsentrasi yang tinggi di Atlantik disebabkan adanya angin pasat dari arah utara-timur yang melewati pantai Afrika barat, ~ 66 ~ angin itu membawa material debu yang berasal dari padang sahara. Daerah kutub selatan memperlihatkan konsentrasi mineral aerosol relatif kecil (atau berkurang) dibandingkan dengan daerah Atlantik, halmana udara yang berasal dari sahara dengan membawa material banyak, melewati ekuator, tetapi oleh adanya angin pasat selatan-barat, secara dramastis partikel-partikel itu jatuh sebelum tiba di kutub selatan. Mineral aerosol di udara diatas Samudera India diperkirakan bersumber dari padang pasir di bagian utara samudera India. Sebagai contoh, yang dilaporkan oleh Chester dan Jickells (2012) konsentrasi dengan nilai rata-rata 16µg m-3 di udara diatas Laut Arabian utara di hantar oleh angin ke Samudera India. Daerah Samudera Pasifik bagian utara telah dilakukan kajian lewat proyek SADS ( the SEAREX Asian Dust Study), alhasil kegiatan projek ini telah memperlihatkan data bahwa, aerosol yang ada di lapisan troposfer di atas samudera Pasifik sebagian besar di suplai dari padang pasir Asia. Menurut Uematsu dkk, (1983) distribusi mineral aerosol di udara bisa melalui dua cara, yaitu (1) konsentrasi menurun secara gradien dari daratan Asian dan konsentrasi tinggi pada daerah lintang tengah (500 LU dan 200LU) dengan rata-rata mineral aerosol di udara adalah 0,79 µg m-3. Kemudian menurun menjadi 0,26 µg m-3 pada 110LU, dan kalau di katulistiwa rata-rata konsentrasi di udara adalah 0,07 µg m-3 . (2) Mineral aerosol yang di transpor ke permukaan Pasifik utara sangat bervariasi , itu biasanya terjadi pada bulan Februari, sedang bulan-bulan yang lain relatif rendah semua aerosol itu bersumber dari daratan Asia. Kalau bagian Pasifik Selatan, tersedia data dari hasil kajian SPAN (South Pasific Aerosol Network), dimana pada katulistiwa dan pada 150LS mineral aerosol di temui sekitar 0,23 µg m-3 , kemudian lebih ke selatan lagi kemungkinan konsentrasinya di udara akan menurun, diperkirakan ± 0,01 ~ 67 ~ µg m-3. Menurut Chester dan Jickells (2012) udara di daerah pasifik, khususnya diatas Samoa (Amerika) konsentrasi mineral aerosol relatif rendah, tetapi konsentrasi kelihatan tinggi berada di daerah samudera Pasifik selatan, tepatnya udara diatas pulau Norfolk, yakni berkisar 0,79 µg m-3. Halmana wilayah ini sangat dekat dengan daratan Australia, jadi prakiraan sumber debu yang ada berasal daerah daratan. Hasil penelitian LIPI menyatakan debu yang ada di udara samudera Pasifik Selatan terutama di seputar wilayah Indonesia, Fuji, Papua New Quinea, kepulauan Solomo dan Filipina, umumnya berasal dari daratan utama pulau-pulau negara tersebut, apalagi pada waktu-waktu tertentu dipengaruhi oleh erupsi gunung vulkanik. Misalnya erupsi gunung Sinabung (di tanah Karo), Gunung berapi (Jawa tengah), gunung Kelud (Jawa Timur), gunung Lokon (Tomohon) dan ada dua gunung di Filipina yang meletus dua tahun lalu. Semua material itu di hantar oleh angin sehingga jatuh di prmukaan samudera Pasifik. Hakekatnya, debu yang berada di udara permukaan laut perairan laut dunia konsentrasinya berbeda-beda sangat tergantung pada ruang dan waktu, kalau di bagian pasifik Selatan kandungan mineral aerosol di udara adalah ≤ 10-3 µg m-3 sedang di bumi bagian Timur utara Atlantik udaranya banyak dipengaruhi oleh pantai barat Afrika dihantar oleh angin pasat, kandungannya agak tinggi > 103 µg m-3. Umumnya udara diatas permukaan laut/samudera banyak bersumber pada padang pasir dan tanah gersang di daerah daratan, seperti di daerah Atlantik kelihatan konsentrasi tinggi itu berada di lintang rendah (0-350N), sedang padang pasir di utara Afrika ke barat akan mempengaruhi tingginya konsentrasi di wilayah Pasifik (pada lintang menengah, 20-500N). Secara global distribusi mineral aerosol mengandung garam air laut tinggi, itu dapat terjadi oleh adanya dorongan angin yang kuat, halmana mineral aerososl itu berasal dari ~ 68 ~ padang pasir dan daerah tanah gersang pada wilayah lintang rendah, tabel 4.9 menyajikan informasi tentang konsentrasi uap garam air laut dan mineral aerosol yang berada di udara bawah troposfer. Kejadian uap air naik ke atmosfer bisa melewati beberapa cara, yakni oleh adanya gelombang besar menghantam pemecah ombak sehingga terjadi butiran air atau gelembung-gelembung , dan gelembung itu diangkut oleh angin naik ke bagian troposefer. Seperti apa yang dikemukakan oleh Blanchard (1983) semprotan air laut memungkinkan produksi butiran-butiran air-laut, dan butiran itu akan berperan penting penyediaan uap-asin aerosol. Dimana adanya tumbukan gelombang pada pemecah ombak, badan kapal di laut, dan atau tembok-tembok di pelabuhan, mengakibatkan kekuatan arus edy makin kuat. Kemudian disertai angin yang kencang menyebabkan butiran air terangkut ke atmosfer. Dalam beberapa referens menyimpulkan bahwa ukuran garam air laut berkisar <0,2 µm sampai > 200 µm , tetapi hampir 90 persen garam air laut di perairan laut dunia memiliki ukuran antara 2-20 µm. Walaupun demikian dalam riset mereka telah terbukti jumlah garam-air laut yang naik ke atmosfer relatif sedikit jumlahnya. Tabel 4.9 Konsentrasi Uap air Laut dan Mineral Aerosol di bawah Troposfer Nilai Tengah Konsentrasi (µg m-3 Daerah Laut udara) 0 Mineral aerosol 0 Atlantik Utara, 22 – 64 N 0 0 Atlantik Utara, 0 – 28 N 0 0 Atlantik Selatan, 5 – 35 S 0 0 Atlantik Selatan, 5 – 35 S termasuk tanjung harapan. 0 0 Pasifik, 28 N – 40 S Laut Mediterania 0 0 Samudera India, 15 S- 7 N Sumber: Prospero dkk (1983) ~ 69 ~ Uap air laut 1,30 36,6 1,35 1,22 6,71 11,2 9,06 11,3 0,58 4,57 7,20 8,44 6,98 3,52 Jadi dapat dikatakan mineral aerosol di atmosfer berasal dari garam-air laut itu sangat tergantung pada angin dan kedudukan lintang. Umumnya angin yang bertiup di permukaan laut adalah 5 sampai 35 m s-1 , dan makin cepat angin bertiup maka peluang partikel uap air laut naik ke atmosfer makin besar. Partikel uap air laut yang naik ke troposfer unsur sulfat adalah sangat penting, seperti (NH4)2SO4 bersifat aerosol utama. Sulfat yang ada di permukaan laut bisa juga berasal dari alam dan polutan yang ada di daratan. Kemudian sulfat yang ada di permukaan laut bisa langsung membentuk garam-air laut atau dapat terbentuk dari bentuk gas ke partikel melalui reaksi kimia. Persenyawaan antar garam air laut dengan sulfat sebagai aerosol laut di perkirakan adalah SO42- : Na+, dan rasionya dalam air laut adalah 0,25. Memang ada juga sulfat tanpa garam laut, tetapi itu hanya kekecualian saja dan jarang terjadi. Kandungan Kimia Pada Laut Aerosol Tabel 4.10 disajikan keadaan konsentrasi beberapa zat kimia yang ada di aerosol laut, data-data ini di kumpulkan dari beberapa referens. Memang dalam realita besaran kandungan zat kimia sangat tergantung pada lokasi dan cara pemindahan zat itu (dari dan ke) atmosfer. Disamping itu ada juga kandungan zat kimia telah lama sudah berada di daerah itu, namun demikian tabel 4.10 memberikan gambaran global zat-zat utama pada aerosol laut. Komposisi kimia pada aerosol laut umumnya berasal dari partikel ukuran besar yang kemudian adanya reaksi percampuran senyawa, maka terurai menjadi bagian-bagian kecil. Walaupun partikel itu dalam ukuran kecil, tapi punya peran sebagai indikator, pembentuk aerosol di atmosfer, dan zat-zat itu tergantung pada sumber mineralnya. Seperti, fraksi yang ada tidak berasal dari mana-mana, atau memang ~ 70 ~ sudah ada disitu, hal itu di sebut sebagai faktor pengkayaan (enrichment factor = EF), dimana dapat dikalkulasi dengan persamaan berikut: EF sumber = (E/I)udara / (E/I)sumber 4.1 Dimana (E/I)udara adalah perbandingan antara elemen E dengan indikator elemen I yang ada di aerosol. Sedangkan (E/I)sumber adalah rasio konsentrasi material sumber. Tabel 4.10 Kisaran Konsentrasi Zat Kimia di Aerosol Laut. Zat Kimia Estimasi Rata-rata Kisaran Konsentrasi (ng m-3 di udara) Al 1 – 104 Fe 1 – 104 Mn 0,1 - 102 Cu 0,1 – 101 Zn 0,1 – 102 Pb 0,1 – 102 Sumber: Chester dan Jickells ( 2012) Kandungan kimia seperti terterah pada tabel diatas berasal dari dua sumber, yaitu dari kerak bumi dan permukaan samudera. Kerak bumi adalah merupakan benda padat yang terdiri dari endapan dan batu-batuan, yang dapat terangkut ke atmosfer melalui proses penguraian oleh sinar matahari, dan atau aktivitas gunung berapi (vulkanik), dimana erupsinya naik ke lapisan troposfer, seperti baru-baru terjadi di Indonesia, erupsi gunung Sinabung ( provinsi Sumatera Utara) yang terjadi di akhir tahun 2013, kemudian erupsi gunung Kelud (Jawa Timur) yang mengeluarkan udara panas bercampur material naik ke lapisan troposfer, peristiwa ini terjadi di awal tahun 2014. Memang wilayah Indonesia tidak bisa di sangkal komponen kimia yang naik ke lapisan ~ 71 ~ troposfer umumnya berasal dari aktivitas vulkanik, karena Indoneisa sebagai negara kepulauan terbesar di dunia yang memiliki jumlah gunung api terbanyak di dunia. Seperti aluminium (Al) adalah contoh material yang bersumber dari batu-batuan atau dari tanah keras, bisa terlepas dari batuan melalui suatu proses (lihat uraian sebelumnya), proses peluruhannya disebabkan pelbagai faktor, hal itu dapat di hitung dengan persamaan berikut: EFbatuan = (E/Al)udara/(E/Al) batuan 4.2 Dimana, (E/Al)udara adalah perbanding konsentrasi antara elemen E dan Al di aerosol, sedang (E/Al) batuan adalah perbandingan konsentrasi yang ada di kerak batuan. Kandungan aluminium pada batuan asli umumnya mengandung >10, tetapi jika nilai EF batuan terdapat 10 sampai 5 X 103 di aerosol artinya pengkayaan yang terjadi tidak terkontrol, halmana di sebut AEE (anomalously enriched elements), Tetapi bila nilai 1 sampai 10 yang ada di aerosol menunjukan tidak ada pengkayaan, disebut sebagai NEE (non-enriched elements). Keberadaan nilai NEE di atmosfer adalah merupakan hal biasa, tetapi nilai AEE dengan variasi komposisi dapat merubah konsentrasi di aerosol, pada peningkatan nilai AEE merupakan hal yang menarik untuk di teliti atau didiskusikan. Debu dan gas yang telah berasosiasi di atmosfer sumbernya bermacam, seperti vulkanik, minyak bumi (fossil fuel) dan industri. Sampai sekarang konsentrasi tetap di udara atmosfer di dunia nilai selalu berubah-ubah. Namun demikian para ahli geokimia memperkirakan suatu kisaran rata-rata dalam kurun waktu 5 tahun penelitiannya. Dalam tabel 4.11 di tampilkan emisi partikel di atmosfer yang berasal dari alam maupun antropogenik. ~ 72 ~ Tabel 4.11. Emisi partikel di Atmosfer Bersumber Dari Alam dan Antropogenik (108g th-1) Unsu r Kimia Debu di Daratan Debu Vulkanik Gas Vulkanik Buangan Industri Minyak bumi ∑ Minyak bumi + Industri Faktor penganggu di atmosfer (%) Al Ti Sm Fe Mn Co Cr V Ni Sn Cu Cd Zn As Se Sb Mo Ag Hg Pb 35650 13275 8,4 4000 12000 72000 15 0 0 0 1600 5200 15 23000 12000 3600 5 12 29 32 9 3,2 7 3200 10700 39 19000 87750 2,1 75000 0 0 52 0 1800 0,04 3000 160 3100 63 4250 30 0,005 24 20 44 161 40 84 0,05 650 290 940 323 500 150 0,000 1000 1100 2100 346 500 83 9 600 380 980 812 200 2,4 0,005 400 30 430 1363 50 93 0,012 2200 430 2630 1897 100 0,4 0,001 40 15 55 2346 2,5 108 0,14 7000 14000 8400 2786 250 3 0,10 620 160 780 3390 25 1 0,13 50 90 140 3878 3 0,3 0,013 200 180 380 4474 9,5 1,4 0,02 100 410 510 8333 10 0,1 0,000 40 10 50 27500 0,5 0,1 6 50 60 110 14583 0,3 8,7 0,001 16000 4300 20300 30 0,012 Sumber: Lantzy & Mackenzie (1979) disitasi oleh Chester (1990). Pelbagai unsur kimia yang naik ke atmosfer bisa terjadi reaksi membentuk senyawa tertentu, tapi ada juga dalam bentuk utuh. Semua unsur kimia itu merupakan faktor pengganggu di atmosfer. Banyak referens menyatakan unsur kimia yang menjadi faktor pengganggu disebut sebagai “atmospheric Interference factor” (AIF). Faktor pengganggu ~ 73 ~ atau yang mengatur elemen di udara dapat dihitung dengan persamaan berikut: AIF = (Ea ∕ En) X 100 4.3 Dimana Ea adalah jumlah (∑) zat yang terkandung pada emisi antropogenik, sedang En memperlihatkan jumlah emisi dari alam. Berangkat dari tabel diatas terlihat, ada tiga kelompok zat kimia, yaitu ❶ Al, Ti, Fe, Mn dan Co semua memiliki nilai AIF (faktor pengaruh di atmosfer) adalah < 100, dan zat dari alam lebih mendominasi di atmosfer. ❷ terdiri dari Cr, V dan Ni yang memiliki nilai AIF pada kisaran 100 – 500 halmana lebih didominasi dari emisi antropogenik, walaupun ada juga dari alam tapi tidak melebihi nilai 5 dibandingkan dengan antropogenik. Dan kelompok ke ❸ Sn, Cu, Cd, Zn, As, Se, Mo, Hg dan Pb kelompok ini memiliki kisaran 500 – 35000 kelompok ini sebagian besar berasal dari emisi antropogenik. Emisi yang masuk ke atmosfer secara umum dari beberapa data penelitian dan pernyataan para ahli geokimia laut di dunia, bahwa kandungan emisi terbanyak berada di belahan bumi utara yaitu ± 90%, sedang sisa 10% ada di belahan bumi bagian selatan katulistiwa. Dalam laporan Weisel dkk (1984) bahwa estimasi sumber zat secara global yang naik ke atmosfer disajikan pada tabel 4.12, dan hal menarik ketersediaan data logam mikro bersumber dari permukaan perairan laut. Data dalam tabel 4.12 terlihat unsur kimia logam mikro seperti : Al, Fe, Mn dan Co di atmosfer hampir 90% berasal dari alam yang disumbangkan dari debu batuan, sedang zat kimia K dan Mg umumnya (± 80%) bersumber dari garam laut. Kemudian unsur V (± 24%), Cu (23 %) dan Pb (69%) merupakan hasil proses alamiah yang bersumber dari permukaan samudera. Kecuali unsur kimia Cu di duga ~ 74 ~ Tabel 4.12. Secara Global Sumber logam mikro yang naik ke Atmosfer (109 g th-1) Zat ALAM ANTROPOGENIK *) Kimia Samudera Debu Vulkanik Vegetasi Minyak bumi Lain-lain Al 200 20000 700 40 2000 2000 Co 0,2 7 0,1 0,04 0,9 2 Cu 5 10 6 0,9 2 50 K 30000 6000 200 100 200 200 Fe 50 10000 300 20 2000 4000 Mg 100000 3000 80 20 300 200 Mn 7 200 9 5 8 400 Pb 8 3 0,4 0,2 4 400 Se 0,0005 7 0,2 0,002 0,6 0,4 V 10 30 0,2 0,2 20 2 Zn 8 80 10 10 80 200 Cd 0,4 0,005 0,1 0,05 0,2 5 Sumber: Weisel dkk (1984). *) Sebagai nilai yang diperkirakan pada butiran air dalam bentuk gelembung yang naik ke udara. dapat berasal dari kegiatan vulkanik, tapi relatif kecil yaitu ≥ 5%. Kalau menurut Nriagu (1979) bahwa vegetasi di daratan memiliki kemampuan menyumbang unsur Zn, nilainya di perkirakan 20 persen. Secara umum dapat dikatakan, unsur logam mikro seperti Al, Fe, Mn, Co dan Sc merupakan sumbangan dari batu-batuan melalui proses alamiah, dan zat-zat itu bukan merupakan pengkayaan dari atmosfer. Tetapi aktivitas vulkanik dan vegetasi di daratan merupakan proses pengkayaan secara alamiah, dan jumlah bervariasi tergantung dari anomali pengkayaan zat (anomalously enriched elements). Kalau zat kimia Na, K, Mg dan beberapa logam mikro (trace metal) di atmosfer adalah sumbangan dari garam laut. Namun demikian semua zat-zat itu menjadi aerosol di udara akan jatuh kembali ke laut, memang ada sebagian ~ 75 ~ besar aerosol, mineral dan logam mikro yang bersumber dari permukaan laut satu berpindah tempat ke laut lain akibat dihantar oleh angin pasat. Suatu ilustrasi tentang proses terjadi pengkayaan logam mikro di atmosfer yang bersumber dari permukaan samudera, disajikan dalam gambar 4.5 berikut ini. Aerosol Lapisan organik Me Partikel Me Me Organik Pengikatan anorganik Partikel anorganik Serap Lapisan mikro Mikroba PERAIRAN Terlarut Logam mikro Pengikatan organik tidak dipermukaan air Pengikatan bahan organik di permukaan Ilustrasi Proses Pengkayaan Partikel di Atmosfer berasal dari Permukaan Samudera. Gambar 4.5. Samudera merupakan wilayah luas dan terbuka memungkinkan terjadinya butiran air yang bisa naik ke atmosfer. Butiran air/gelembung terbentuk akibat adanya angin dan gerakan glombang besar, apalagi ombak itu melewati tanggul pemecah ombak, jumlah butiran air yang akan naik ke atmosfer makin signifikan. ~ 76 ~ Umumnya pengkayaan di atmosfer bersumber dari samudera bisa berasal dari bahan organik dan partikel yang ada di lapisan mikro. Organik alam yang ada dipermukaan sangat bervariasi senyawanya di dalam butiran yang ada di lapisan mikro, seperti: padatan suspensi, organik karbon dan partikel terlarut, fosfat organik dan anorganik, bahan organik berbentuk nitrogen (termasuk nitrat), bakteri dan organisme mikro lainnya, bahan cemar (polutan) dan logam mikro. Intinya pengkayaan logam mikro di lapisaan mikro (lihat gambar) fenomenanya tidak stabil, dan frekuensi kehadiran logam mikro sangat tergantung dari bentuk dan sifat bahan organik yang ada di permukaan. Kemudian proses pengikatan bahan organik dan partikel logam mikro di lapisan mikro cukup tinggi dibandingkan dengan yang ada di bagian perairan. Walaupun sesungguhnya peluang pengkayaan di perairan variasi luas. Hakekatnya, partikel ada dalam bentuk debu, mineral aerosol dan logam mikro yang bersumber dari samudera memiliki kisaran ≤ 10-3 m-3 sampai ≥ 103 µg m-3 (bersumber dari daerah padang pasir). Secara global sumber debu yang menjadi mineral aerosol di atmosfer sekitar 100 sampai 800 g th-1 , dan prinsipnya sumber utama partikel sebagai laut aerosol ada tiga, yaitu dari kerak bumi, permukaan paerairan samudera dan antropogenik. Semua partikel dan aerosol akan turun ke laut melalui proses kondensasi atau adanya proses presipitasi (lihat gambar 4.3) Material bersumber dari hidrothermal Lapisan dasar laut dan tanah di dasar laut (sea bed) terdapat komposisi sebagai batuan keras lava yang tersusun pada lapisan pertama sebagai sedimen (kerak samudera pertama) dan lapisan ke dua dasar sebagai lapisan batu keras laut terbentuk oleh adanya vulkanik, dan lapisan ke tiga adalah lapisan gabbro (lihat gambar 4.6). ~ 77 ~ Secara umum aktivitas vulaknik dimulai dari gas vulkanik yang berakumulasi di dalam dapur magma berfungsi sebagai motor penggerak magma. Dalam kegiatannya ataupun bila terjadi peningkatan kegiatan gas-gas vulkanik tersebut akan keluar ke permukaan terlebih dahulu karena lebih ringan daripada material dalam bentuk cair/fluida atau padat. Kerak samudra, merupakan benda padat yang terdiri dari endapan di laut pada bagian atas, kemudian di bawahnya batuan batuan vulkanik dan yang paling bawah tersusun dari batuan beku gabbro dan peridolit. Oksidasi di Air Laut Permukaan Laut SEDIMEN (Lapisan 1) Hidrotermal terendam Transfer panas dan zat kimia Dominasi logam Fe Padatan Batuan Vulkanik (Lapisan 2) Dolit Pengeluaran gas MAGMA ASTENOSFER GABBRO (Lapisan 3) MOHO MANTLE Gambar 4.6. Lapisan Kerak Samudera (Dasar laut dan Tanah di bawahnya) Celah yang ada di bawah badan air laut atau geyser disebut sebagai ventilasi hidrotermal. Celah itu terbentuk akibat lempengan kerak samudera bergerak tanpa henti dan bertabrakan dengan gunung laut. ~ 78 ~ Komposisi kimia di landas kontinen dan di badan air berbeda, karenanya pembentukan sedimen dan pertukaran kimia perbedaan itu yang berperan penting, biasanya melalui proses “diagenesis” dan adanya aktivitas biota perairan, maka membentuk sedimen di dasar perairan, apalagi partikel yang keluar melalui ventilasi hidrotermal akan makin cepat membentuk suatu bongkahan keras (nodul) Lapisan kerak samudera sangat dipengaruhi oleh lapisan vulkanik, komposisi kimia yang dikandung di landas kontinen telah tersusun ribuan tahun, yang mula-mula zat-zat itu ada dalam batuan gabbro dan predolit. Semakin bertambah tahun lapisan-lapisan makin keras, apalagi jika di seputarnya atau didalam samudera terdapat gunung berapi. Sebagai contoh Indonesia pada wilayah perairan laut banyak di temui gunung berapi (misalnya daerah kepulauan Sangihe, kabupaten Banten, gunung anak Karatau). Disamping itu di pinggiran daerah pantai Indonesia banyak ditemui gunung berapi aktif, lava gunung berapi antar satu dengan yang lain saling berhubungan. Pergeseran material di lapisan bawah tanah memungkin terjadi, sehingga membentuk lapisan tebal yang keras di dasar laut. Dalam lapisan itu mengandung zatzat kimia, seperti: Al, Fe, Ni, Mg, Co, Pb dan sebagainya. Karena asosiasi yang kuat maka membentuk suatu manganes nodule. Gambar diatas terlihat magma merupakan sumber panas dalam bentuk cair dan gas naik ke lapisan dua melewati lapisan dolit, pada lapisan dua terbentuk batuan hidrothermal. Dalam periode panjang membentuk suatu lapisan yang disebut sebagai sedimen, halmana pada lapisan ini banyak terdapat logamfero dan logam lainnya. Zat kimia yang ada di lapisan ini berasosiasi sering membentuk suatu nodul manganese. Elderfield (1976) mengatakan bahwa ada perbedaan antara “geotermal” dan “hidrotermal”, halmana kalau geotermal sumber panasnya bisa langsung masuk ke dalam sirkulasi air ~ 79 ~ tanpa pemindahan kimiawi, pelapukan dari batuan kerak samudera atau dari partikel akan jatuh ke dasar membentuk sedimen (jadi sedimen itu bersifat mineral). Tetapi hidrotermal selain panas yang ada terjadi juga transfer kimiawi. Seperti unsur Hg, Ce dan B, bersumber dari mantel (kulit) berubah bentuk gas dan juga gas radiogenik ( 3H) ditransfer ke sirkulasi air, walaupun akhirnya zat-zat itu akan membentuk sedimen di dasar perairan. Jadi jelas terlihat aktivitas hidrotermal bisa sebagai penghasil batuan samudera yang baru di pusat punggung dasar laut, dan dalam waktu lama akan membentuk lapisan keras sehingga tersusun nodul mangan. Secara umum gambaran komposisi nodul mangannes dan batuan keras yang tersusun pada daerah landas kontinen disajikan pada tabel 4.13 berikut ini. Tabel 4.13 Kelimpahan zat Mn, Fe, Ni, Co dan Cu pada nodul Mangan dan Batuan ( satuan berat dalam %) Mn Fe Ni Co Cu Mn/Fe Kedalaman Seamounts Datar an Punggung laut aktif 14,62 15,810,35 1 1,15 0,058 0,92 1872 17,17 11,81 0,641 0,347 0,087 1,53 0,45 15,15 19,15 0,306 0,40 0,081 0,80 2870 Punggu ng laut lainnya 19,74 20,08 0,336 0,570 0,052 0,98 1678 Pinggiran kontinen Pinggiran Seamount Abysal 38,69 1,34 0,121 0,011 0,082 28,8 3547 15,65 19,32 0,296 0,419 0,078 0,81 1694 16,78 17,27 0,540 0,256 0,370 0,97 4460 Sumber: Murton, B.J. dkk (2004) Interaksi antara batuan lava dengan air laut dapat terjadi dengan kisaran temperatur luas dan periode yang panjang, aktivitas itu bisa melalui beberapa alur sebagai berikut: (1) adanya aktivitas hidrotermal dengan suhu tinggi dapat menghancurkan kerak batuan di dasar laut, kemudian pada punggung dasar laut dengan suhu tidak terlalu tinggi bisa terjadi interkasi dengan air laut; (2) dengan suhu rendah pelapukan batuan dapat terjadi, dan zat-zat hasil pelapukan dapat berasosiasi dengan air laut dalam waktu yang tidak ~ 80 ~ terlalu lama; dan ke (3) hasil yang dikeluarkan oleh lava panas dapat masuk ke dasar perairan atau tanah di dasar perairan. Chester dan Jickells ( 2012) menyatakan unsur kimia yang dikandung oleh batuan di dasar samudera bisa berbentuk unsur utama dan minor, disajikan pada tabel 4.14. dan tabel 4.15 berikut ini. Tabel 4.14. Unsur Kimia Utama di Bebatuan Dasar Samudera Senyawa SiO2 TiO2 Al2O3 Fe2O3 FeO MnO MgO CaO Na2O K2 O H2O(∑) P2O3 Batuan di pulau Oseanik Rata-rata batuan tolelitik 49,36 2,50 13,94 3,03 8,53 0,16 8,48 10,30 2,13 0,38 0,26 Rata-rata batuan alkali 46,46 3,01 14,64 3,37 9,11 0,14 8,19 10,33 2,92 0,84 0,37 Batuan di Punggung Atlantik Batuan Batuan tolelitik Alumina 50,47 48,13 1,04 0,72 15,93 17,07 0,95 1,17 7,88 8,65 0,13 0,13 8,75 10,29 11,38 11,26 2,60 2,39 0,10 0,09 0,59 0,29 0,11 0,10 Sumber: Chester dan Jickells ( 2012) Tabel 4.15. Kimia Minor di Bebatuan Dasar Samudera (µg g-1) Unsur Batuan Batuan Batuan Batuan di Batuan di diPunggung SamuderaIndia Pulau Tonga alkali tolelitik Atlantik Fe Mn Cu Ni Co Ca Cr V Ba Sr 82600 1084 36 51 25 22 67 252 498 815 76800 1239 77 97 32 17 297 292 14 130 63616 87 123 41 18 292 289 12 123 Sumber: Chester dan Jickells ( 2012) ~ 81 ~ 68282 90 242 23 20 347 340 131 54008 51 25 30 13 75 230 13 115 Zat kimia baik berbentuk utama (major) maupun minor sebagaimana terterah pada table diatas (Tabel 4.14 dan 4.15) memiliki kemampuan bersenyawa satu dengan yang lain, bahkan bisa membentuk ikatan yang kompleks berwujud mineral. Interaksi kimia-kimia tersebut dapat terjadi di badan/kolom air atau dapat juga di sedimen. Keberadaan zat kimia, baik organik maupun anorganik di samudera akan menentukan dan sebagai pengendali kehidupan di samudera dan penyusunan kerak samudera. Berbicara kerak/bongkahan di dasar samudera, secara umum lapisan kerak ada yang bersifat keras dan ada juga lunak, artinya masik mengandung sejumlah air (larutan kental), hal ini disebut sebagai hidrogenetika. Walaupun kerak yang bersifat larutan dengan viskositas tinggi itu, akan menjadi keras oleh adanya reaksi oksidasi. Dalam kenyataan di sedimen, kerak samudera ataupun bongkahan abisal terdapat beberapa lapisan, lapisan yang bagian atas biasanya berupa partikel halus sebagai endapan berasal dari badan air, yang kemudian diikuti lapisan pebatuan keras berasal dari vulanik. Intinya pada lapisan batuan keras di lapisan dua (batuan vulkanik) berinteraksi dengan air laut merupakan suatu sumber material dari aktivitas hidrotermal dimana akan membentuk cadangan geokimia di landas kontinen. Rekasi kimia yang terjadi yang menyusun beberapa komponen dan tenggelam di dasar perairan sangat tergantung pada volume air dan aktivitas. Secara umum proses pembentukan batuan keras samudera maupun batuan-batuan baru yang tersusun di punggung dasar laut sebagai akibat adanya aktivitas hidrotermal. Mula-mula di dasar laut membentuk asap putih dan makin bertambah waktu kelihatan seperti asap hitam, akhirnya zat-zat itu mengeras menjadi bahan mineral di dasar perairan sampai membentuk nodul. ~ 82 ~ ⑤ KESETIMBANGAN THERMODINAMIKA T ermodinamika merupakan suatu kajian yang menyangkut perubahan energi yang menyertai suatu proses perubahan fisik atau kimia ataupun s benda. Konsep utama yang digunakan adalah hukum kekalan energi yang menyatakan bahwa energi adalah kekal adanya, energi hanya ditransformasikan dari satu bentuk ke bentuk yang lain. Suatu perubahan zat menjadi zat lain, bisa jadi zat atau benda semula mengalami degradasi (peluruhan) kandungan energi dalamnya karena pada proses tersebut energinya dipindahkan ke zat/benda lain atau dilepaskan ke lingkungan. Bentuk kesetimbangan kimia di perairan alamiah sangat kompleks karena material yang ada berasal dari pelbagai sumber. Mengidentifikasi komposisi kimia yang ada disertai kesetimbangannya, dapat dilakukan dengan pendekatan seperti berbentuk zat tunggal atau terdiri beberapa senyawa, sifat senyawa padat atau cair, di troposfer tertutup atau terbuka, dan apakah sifat kimia itu mudah dipengaruhi oleh cahaya atau tidak. Proses perubahan fisika maupun kimia kebanyakan berlangsung bolak-balik. Pada awalnya proses berlangsung ke arah hasil, tetapi begitu molekul hasil terbentuk, maka proses ke arah yang berlawanan akan berlangsung. Ketika proses kedua arah yang berlawanan tersebut mempunyai laju yang sama dan konsentrasi zat tidak berubah lagi dengan bertambahnya waktu, saat itulah kesetimbangan dinamika tercapai. Kesetimbangan tersebut bersifat dinamis karena kedua proses dengan arah berlawanan tersebut tetap ~ 83 ~ berlangsung walaupun tidak menghasilkan perubahan konsentrasi. Termodinamika merupakan suatu instrumen untuk meramal apakah suatu proses yang belum kita ketahui dapat dilaksanakan atau tidak. Termodinamika dapat menjelaskan mengapa proses pertumbuhan dan reproduksi sistem hayati seperti manusia, hewan dan tumbuhan dapat terjadi. Kita akan dapat mengerti mengapa reaksi fotosintesis dapat berlangsung dan mengapa pula ikan dapat bernafas dalam air. Bertolak dari pemikiran itu, timbulah beberapa pertanyaan mendasar bagi kita, seperti: mengapa bila ada oksigen, besi lama kelamaan akan berkarat; mengapa gas O2 bisa menjadi H2O dengan sendirinya pada suhu rendah. Kalau di atmosfer, mengapa gas O2 menjadi gas ozon (O3) atau sebaliknya dapat terjadi. Semua perubahan yang dipertanyakan tadi, bisa dijawab dengan menggunakan konsep termodinamika. Memang pengetahuan termodinamika banyak di gunakan sebagai kurikulum di ilmu keteknikan (misalnya, fakultas teknik), karena pengetahuan pemindahan bentuk benda satu ke bentuk lain memerlukan perubahan energi “transfer energy”. Menurut Thomas (1992), Transfer kalor didefinisikan sebagai pemindahan energi dari satu tempat ke tempat lain dalam satu sistem yang disebabkan oleh perbedaan suhu. Menurut teori, termodinamika terdiri dari dua suku kata yakni. Termo dan dinamika. Termo dalam bahasa Yunani mengartikan sebagai panas atau kalor, sedang dinamika bermakna kekuatan atau tenaga. Pengertian termodinamika secara harfiah yaitu perubahan kalor menjadi kekuatan atau tenaga. Aspek yang terkandung dari makna tadi melibatkan peristiwa konversi energi. Tetapi adanya perkembangan ilmu dan teknologi yang begitu pesat, maka aspek yang terlibat makin beragam seperti: Pengetahuan tentang pemindahan panas umumnya digunakan pada ~ 84 ~ disiplin ilmu kimia, “aerospace”, lingkungan, mekanikal, teknik nuklir, refigerasi, polimer dan sebagainya. Namun demikian, pengetahuan kelautan lebih khusus untuk siklus energi berasal dari nurtrien di laut juga akan menggunakan teori panas dan persamaannya, penulis mencoba aplikasikan ke dalam sistem geokimia di laut. Ada tiga prinsip dalam hukum termodinamika yang berkembang sampai saat ini, yakni Hukum termodinamika pertama, dipelajari prinsip kekelan energi, sedangkan hukum termodinamika kedua, membahas arah suatu perubahan, proses atau peristiwa yang memperlihatkan kecenderungan dari pergerakan semesta ke arah tidak teratur, hukum termodinamika II digunakan sebagai alat untuk menilai dan mengukur tingkat kespontanan dari proses atau perubahan tersebut. Sedang untuk hukum termodinamika ketiga, memberikan prinsip dasar dari kedua hukum tersebut (termodinamika I dan II) sebelumnya dengan menjelaskan derajat ketidakteraturan pada kondisi temperatur (suhu) 0oK absolut. Jadi menurut hukum termodinamika ke III, kristal murni berada pada suhu absolut 00K memiliki keteraturan struktur tertinggi, dan menurut konvensi ditetapkan NOL. Intinya para ahli merumuskan persamaan tentang termodinamika, yakni sebagai energi konservasi. Hukum termodinamika adalah: (5.1) Catatan: rata-rata perubahan energi = 0 Dimana Ẻ0 dan Ẻ1 merupakan pemindahan energi masuk dan keluar ke dalam sistem. Δ Ẻ3 / Δt adalah perubahan energi yang tersimpan di dalam sistem. Untuk analisis pemindahan kalor di dalam perubahan suatu larutan (fluida), ada dua rumusan dasar, yaitu: (1) prinsip massa konservasi dengan persamaan berikut, ~ 85 ~ (5.2) Ke (2) hukum Newton kedua, dengan persamaannya sebagai berikut, (5.3) Dimana M adalah produk dari komponen x dari velosity µ dan massa m Hakekatnya, berbicara termodinamika tidak terlepas pemahaman tentang panas secara alamiah, cara kerjanya dan identifikasi pengaruhnya pada sistem alam. Hukum-hukum tentang panas dalam kaitan dengan termodinamika yang di aplikasikan pada geokimia merupakan pusat diskusi dalam bab ini. Sebagai sasaran pembahasan dalam bagian ini yaitu membicarakan hal yang berkaitan dengan temperatur, panas dan hal-hal yang mempengaruhi kesetimbangan kimia di laut termasuk kimia potensial, entropy dan enthalpy. Intinya untuk mengetahui rumusan dasar dari pertukaran energi di alam akibat pengaruh suhu, tekanan, volume, entropy dan komposisi kimianya. Suhu Dan Rumus Persamaannya. Dalam kehidupan keseharian kita, dimana suhu sangat berhubungan dalam tubuh kita, terkadang suhu dapat mengendalikan aktivitas keseharian, tergantung rasa kita apakah panas atau dingin. Batasan suhu tinggi atau rendah tidak hanya dengan perasaan tetapi sebaiknya dianalisa dengan pendekatan prinsip geokimia, jelas bagi kita untuk mendefinisikan suhu tidak hanya dengan dua alasan seperti: (1) Sulit menentukan konsep suhu hanya dengan cara prediksi melalui pengamatan ~ 86 ~ subjektif. Oleh karenanya penentuan skala suhu haruslah menggunakan dasar matematika; ke (2) Agak sulit bagi kita menentukan panas (kalor), secara kuantum masuk kedalam tubuh kita akibat suhu. Sesungguhnya pemahaman panas perlu pendekatan sifat termodinamika. Sebagai contoh ada dua sistem tertutup dengan kondisi homogen, dimana setiap sistem terdiri dari zat tunggal dengan sifak fisiknya, pasti tidak akan terjadi proses reaksi kimia dengan sempurna. Untuk itu dengan pendekatan termodinamika dapat menjelaskannya sifat intensif dari kedua sistem, kemungkinan akibat tekanan dan viskositas, sehingga berpengaruh pada kecepatan akustik dan volume molar. Dalam teori tekanan di simbolkan dengan “p” sedang Volume dengan simbol “v” Seandainya kita tempatkan dua kontainer berdekatan secara spontan terjadi pertukaran tekanan dan volume molar kedalam sistem itu tetapi jika dibiarkan dalam beberapa saat, pasti tidak akan tejadi perubahan. Pada kondisi itu kedua kontainer dalam kesetimbangan panas (thermal equilibrium). Untuk itu mengukur tekanan dan volume molar diberi label P1, V1 dan p1, v1 , tidak bisa dipungkiri secara umum harapan P1 akan sama dengan p1 demikian juga pada volume molar V1 akan berimbang dengan v1 . Jikalau kita pisahkan sistem itu, kemungkinan salah satu sistem akan berubah, ditandai dengan nilai P2 , V2 dan sudah pasti ada kesetimbangan panas dengan p1,dan v1 halini menunjukan bahwa kemungkinan kombinasi P dan V adalah stabil. Perubahan yang terjadi biasanya menimbulkan panas atau sering disebut “suhu”, kalau suhu ada dalam kesetimbangan di katakan “isotherm”, secara empiris rumus kesetimbangan suhu di gambarkan sebagai berikut: f (p, v¯ ) = t atau F(P, V¯ ) = T, (5.4) ~ 87 ~ Apabila t=T , akan memperlihatkan sifat intensif dari suatu sistem ada dalam kesetimbangan termal. Dalam kenyataan di alam banyak sistem yang sama, maka rumus ini dapat dikembangkan. Kalau ada gas pada tekanan rendah maka persamaannya adalah PV¯ = RT, dimana R adalah konstanta gas (1,987 cal mol−1K−1). Kemudian pada daerah tekanan tinggi yang mengandung banyak atom per molekul maka berlaku persamaan Van der Waals, yaitu: (P + a/V¯ 2)(V¯ − b) = RT, (5.5) Di mana nilai a dan b adalah konstanta empiris. Jadi hakekatnya perubahan tekanan di suatu tempat akan mempengaruhi suhu (temperatur) sehingga dapat dikembangkan persamaan yang terterah diatas. Sebagai contoh, kalau kita memindahkan sesuatu benda atau objek dari satu tempat ke tempat lain maka akan keluarkan gaya, jumlah kalor yang keluar adalah dw , maka fungsi gaya itu adalah sebagai berikut: dw = F dx (5.6) dimana F adalah gaya sedang dx menunjukan tempat yang berpindah. Merupakan suatu konsensus bahwa, dw akan positif jika terjadi perpindahan atau gaya, sedang nilai negatif adalah tempat dimana benda itu di pindahkan. Dalam setiap gerakan selalu ada kekuatan (gaya), maka persamaan umum adalah : dw = ΣFi dxi. (5.7) Gaya merupakan tekanan hirostatik, P, seperti tekanan, tegangan permukaan, tarikan listrik atau gradien magnit. Keseluruhan pekerjaan itu dikaitkan dengan thermodinamika, dapat digunakan dengan rumus persamaan dw . ~ 88 ~ Apabila dihubungkan dengan geokimia , dimana pertukaran volume di nyatakan dV diterapkan pada tekanan hidrostatik, maka persamaannya adalah sebagai berikut: dw = PdV. (5.8) Jadi berbicara geokimia dalam kesetimbangan termodinamika sesungguhnya berhubungan akan dengan tekanan dan volume. Kalau perhitungan thermodinamika didasarkan pada tekanan dan volume kemungkinan kesalahannya kecil, tetapi jika penerapan pada geologi, karena ada pengaruh gerakan yang signifikan, seperti letusan vulkanik dengan gas yang meluas tersebar dan gas-gas lain yang signifikan pengaruhnya, maka agak sulit dievaluasi, sebab tekanan tidak sama di semua tempat dan gas tidak dalam kesetimbangan mekanis dengan lingkungannya. Hukum Pertama Termodinamika Hukum pertama termodinamika merupakan bentuk lain dari hukum kekekalan energi. Dalam suatu sistem yang terisolasi jumlah energi total selalu tetap. Jika antara sistem dan lingkungan terjadi pertukaran kalor atau kerja, maka menurut hukum pertama termodinamika jumlah total energi, yaitu energi sistem ditambah energi lingkungan harus selalu tetap. Kita tahu alam semesta yang merupakan ciptaan Tuhan, mempunyai energi yang konstan. Berdasarkan asas kekekalan energi (nanti diuraikan berikut), kita tidak mungkin bisa menciptakan/membuat dan memusnahkan suatu energi yang dapat kita lakukan hanyalah mengubah suatu bentuk energi tersebut menjadi sebuah bentuk energi yang lain. Secara ilustrasi kondisi energi di alam seperti terlihat pada gambar 5.1 . Masuk dan keluar energi adalah perubahan energi yang tersimpan di dalam sistem. ~ 89 ~ Sebelum lebih lanjut membahas tentang hukum termodinamika, marilah kita pelajari tentang hukum kekekalan energi, apa yang dimaksud dengan kerja dan kalor serta fungsi keadaan (lingkungan). Gambar 5.1. Ilustrasi Kerja energi di Alam ① Hukum Kekekalan Energi: Prinsip hukum kekekalan energi yaitu dalam setiap proses, energi tidak dapat dimusnahkan maupun diciptakan. Energi dapat dipertukarkan dari satu bentuk ke bentuk lain atau dialihkan dari satu sistem ke sistem lain dalam bentuk kerja atau kalor, tetapi jumlah energinya tak pernah berubah. Marilah kita ketahui bentuk-bentuk energi yang lazim terlibat yaitu energi kinetik, Ek =½ m.V2. (5.9) dimana m adalah massa benda dan v kecepatannya. Satuan energi dinamakan SI adalah joule (J). 1 J= 1 kg.m2.det-2 Suatu benda juga memiliki energi karena lokasinya. Energi ini dinamakan energi potensial (Ep) dengan persamaan sebagai berikut: Ep = mgh (5.10) halmana g adalah percepatan gravitasi, yang nilainya berdasar percobaan adalah 9,81 m.det-2 untuk massa di bumi, sedang h merupakan ketinggian benda. ~ 90 ~ Jadi hukum kekekalan energi : E total = Ek + Ep = tetap (5.11) Laju produksi atau penggunaan energi disebut daya. Satuan SI untuk daya adalah watt (J.det-1) Prinsip yang menjadi dasar dari perkembangan termodinamika adalah hukum kekekalan energi. Prinsip ini berlaku baik pada mahkluk hidup maupun benda mati seperti kontainer (pada percobaan James Joule), gas, logam, dan sebagainya. Bila kita ambil contoh pada benda mati seperti batu, yang kita letakan pada suatu tempat dengan ketinggian tertentu maka batu itu memiliki energi potensial. Selanjutnya bila batu kita jatuhkan dari ketinggian tertentu maka batu akan bergerak dengan kecepatan tertentu, keadaan ini menunjukan bahwa saat ini batu memiliki energi kinetik. Proses perubahan energi pada gerakan batu tadi adalah perubahan dari energi potensial menjadi energi kinetik yang dikatakan sebagai peristiwa transformasi energi. Energi yang dimiliki batu tadi secara keseluruhannya tetap hanya bentuk energinya berubah. ② Pengertian Kerja dan Kalor (Panas) Kerja mekanik terbentuk apabila sebuah gaya bekerja pada suatu jarak yang tertentu. Besar kerja dinyatakan sebagai hasil perkalian antara gaya dan jarak. Satuan SI untuk kerja adalah Joule (J), ini diambil dari nama James Joule sebagai penemu teori hukum termodinamika. Besaran Joule ini berhubungan gaya satu newton (N) yang bekerja pada jarak satu meter (m). Oleh karena itu 1 Joule = 1 newton X 1 meter (atau Kerja = gaya X jarak). Kerja dapat dinyatakan sebagai segala bentuk alih energi yang dapat ditimbulkan melalui pengangkatan atau penurunan beban. Kalor adalah energi yang dipindahkan sebagai akibat adanya perbedaan suhu. Energi berupa kalor selalu berpindah dari benda yang panas (suhu lebih tinggi) ke benda yang dingin (suhunya lebih rendah). Kalau kita lihat dari segi ~ 91 ~ molekul, hal ini berarti bahwa molekul dari benda panas akan memberikan sebagian energi kinetiknya kepada molekul benda dingin ketika kedua benda itu bersentuhan. Akibatnya, energi kinetik rata-rata dari molekul benda panas akan berkurang dan suhunya turun, sedang suhu benda dingin akan naik karena energi kinetik rata-rata molekulnya bertambah. Kalor akan mengalir antara kedua benda tersebut sampai suhunya sama. Banyaknya kalor q. Yang dibutuhkan untuk mengubah suhu zat, tergantung pada besarnya perubahan suhu, jumlah zat dan jenis zat (jenis molekul). Kapasitas kalor adalah banyaknya kalor yang dibutuhkan untuk menaikkan suhu suatu zat 10C; sudah barang tentu kapasitas kalor bergantung pada jumlah zat kapasitas kalor spesifik atau kalor jenis. Pengertian kalor jenis adalah jumlah kalor yang dibutuhkan untuk menaikkan suhu 1 gram zat 10C. Kapasitas kalor molar adalah banyaknya kalor yang diperlukan untuk menaikkan suhu 1 mol zat 10C Menurut sejarahnya banyaknya energi kalor dinyatakan dalam satuan kalor. Satu kalori adalah jumlah kalor yang dibutuhkan untuk menaikkan suhu 1 gram air dari 14,50C ke 15,50C. yang perlu diingat satuan kalori bukan satuan SI. Dalam percobaan Joule memperlihatkan kerja ditimbulkan dengan jalan melepaskan beban karena efek gravitasi kerja tersebut diubah menjadi kalor yang direkam melalui adanya kenaikan suhu air dalam wadah percobaan. Hasil menunjukan bahwa jumlah joule kerja yang dihasilkan beban selalu kira-kira 4,15 kali lebih besar dari jumlah kalor yang diserap oleh air. Percobaan Joule ini menegaskan bahwa kerja mekanik dapat diubah menjadi kalor, dan menyatakan bahwa kalor serta dapat diukur dengan menggunakan satuan yang sama yaitu joule atau kalori. Secara empirik percobaan itu memperlihatkan bahwa : 1 kal = 4,184 J dan 1 kkal = 4,184 kJ. ~ 92 ~ ③ Pengertian sistem, Lingkungan dan Fungsi Keadaan. Sistem dalam termodinamika didefinisikan sebagai sejumlah materi atau daerah dalam ruang yang dijadikan sebagai objek studi. Massa atau daerah yang berada di luar sistem disebut sebagai lingkungan. Bidang yang bersifat riil maupun imaginer yang memisahkan sistem dan lingkungan disebut sebagai batas. Batas ini dapat berupa batas tetap (fixed boundry) atau batas berubah (movable boundry). Dalam bidang kimia, yang dimaksudkan dengan sistem adalah suatu reaksi kimia zat-zat yang kita reaksikan. Sedangkan tabung reaksi atau gelas kimia beserta segala sesuatu di sekelilingnya merupakan lingkungan (lihat gambar 5.1). Intinya sistem yang dimaksud diatas, ada empat tipe, yaitu sistem terbuka, tertutup, terisolasi dan adiabatik, perbedaan dari keempatnya terletak pada interaksi antara sistem dan lingkungannya. Sistem terbuka memiliki ciri yang memungkinkan adanya perpindahan massa dan kalor, baik masuk atau keluar. Contohnya, reaksi yang berlangsung dalam gelas piala dimana materi atau massa dan kalor dapat dengan mudah masuk dan keluar dari sistem ke lingkungan dan sebaliknya. Untuk sistem tertutup, cirinya adalah tidak dapat terjadi aliran massa namun aliran kalor masih dimungkinkan. Sebagai contoh apabila kita panaskan gas di dalam tabung silender yang tertutup dengan sumber kalor (bunsen misalnya), maka volume gas di dalam tabung silinder akan memuai sebagai akibat dari peningkatan suhu gas yang diterimanya melalui dinding yang dipanaskan tadi. Kemudian suatu sistem disebut sistem terisolasi, bila tidak dimungkinkan adanya aliran baik massa atau kalor yang terjadi antara sistem dan lingkungan. Suatu sistem disebut adiabatik, bila sistem tersebut tidak memungkinkan kalor keluar dari sistem ke lingkungan. Besaran ekstensif adalah variabel yang ukurannya ditentukan oleh jumlah atau kuantitas dari sistem. Sebaliknya besaran intensif adalah variabel yang tidak ~ 93 ~ tergantung pada jumlah atau kuantitas sistem atau dengan pengertian lain nilainya tetap pada berbagai jumlah atau kuantitas sistem. Contoh besaran (ukuran) ekstensif dan intensif dapat dilihat pada tabel 5.1 berikut. Tabel 5.1 Ukuran Besaran Intensif dan Ekstensif Besaran Tekanan, Densitas, Suhu, Viskositas, intensif Tegangan permukaan, Kalor Jenis Besaran Volume, Massa, Energi, Energi bebas ekstensif Gibbs, Entalpi, Entropi, Energi dalam, Kapasitas kalor. Setiap sitem memiliki karakteristik, misalnya satu balok es memiliki massa volume, suhu, densitas, kekerasan dan tekanan. Kumpulan nilai atau harga dari seluruh karakteristik yang dimiliki sistem tadi mendefinisikan apa yang disebut sebagai keadaan. Sifat dari sistem yang hanya ditentukan oleh keadaan sistem, dan tidak ditentukan oleh cara mencapai keadaan tersebut disebut sebagai fungsi keadaan. Gas ideal dengan massa tertentu akan memiliki hubungan dengan sifat tekanan, volume dan suhu. Paling tidak dua sifat yang diperlukan untuk mendefinisikan keadaan gas ideal, misalnya tekanan dan volume, maka dari hubungan tekanan volume dapat diketahui suhu gas. Kronologis penemuan hukum termodinamika, diawali dengan pengujian bertahun-tahun di sekitar tahun 1940-an oleh seorang ahli kimia berkebangsaan Inggris, yaitu James Joule. Hasil percobaan ini di publikasi resmi pada tahun 1947 dalam bentuk jurnal ilmiah. Oleh karenanya satuan dari energi dipakai ukuran Joule. Joule melakukan percobaan dengan memindahkan air kedalam kontainer (wadah) dan ada juga wadah lain yang bersifat terisolasi . Salah satu wadah di putar airnya dengan menggunakan alat pedal sepeda yang terbuat dari besi ~ 94 ~ sedang wadah yang satu tidak diberi perlakuan.. Sambil uji berjalan suhu (temperatur) di kedua wadah itu di monitoring. Hasil uji itu sangat mengejutkan , menyimpulkan bahwa ada sejumlah energi spesifik dalam proses itu berlangsung, namun kedua suhu relatif sama. Perubahan spesifik itu terjadi adalah merupakan fungsi energi potensial. Sebagai contoh jika kita melemparkan potongan (balok) timah ke atas meja, maka energi terjadi tidak hanya gaya pemindahan benda itu saja, tapi ada energi potensial bertambah berasal dari dalam balok itu (tergantung pada suhu, tekanan dan komposisi benda itu). Pemindahan air ke wadah yang dilakukan Joule tidak hanya perubahan tempat air itu, tapi ada internal energi (energi dalam) dari air tersebut, semuanya dapat di terah dengan suhu. Fungsi energi merupakan energi internal di dalam sistem, diberi simbol E, rumus sederhananya adalah sebagai berikut: dE = −dw. (5.12) Energi yang terjadi pada pengujian itu, ada dua dugaan yakni: pertama, di bagian dinding pada wadah yang airnya tidak dipindahkan ada berhubungan dengan suhu, energi yang ada merupakan transfer energi, disebut sebagai panas atau kalor. Pemindahan energi (panas) menyangkut dengan pemindahan suatu massa yang masuk ke dalam sistem (Thomas, 1992). Jadi menurut penjelasan Joule panas yang ada bukan dari gaya pemindahan melainkan berasal dari cahaya yang masuk ke dalam sistem. Kedua, panas yang ada di wadah pemindahan adalah berasal dari gaya kerja itu. Bertolah dari dua cara pengujian itu pada intinya sistem yang terjadi bersifat tertutup dimana kedua wadah itu ada dinding yang tidak bisa ditembus, disebut sebagai adiabatic (lihat penjelasan diatas). Jadi pengujian Joule membuktikan tidak terjadi pemindahan panas di kedua sistem itu. Para ahli geokimia juga beranggapan di alam terbuka bisa terjadi ~ 95 ~ adiabatic, namun sifat nir-adiabatic dapat terjadi tergantung pada sifat dan bentuk dinding pemisahnya. Pada rumus di sebut diatas sebagai hukum termodinamika pertama, dimana proses panas yang berkerja di keadaan adiabatic atau panas yang bertambah hanya dari internal sistem, bukan dari luar. Pertukaran panas secara internal sama dengan panas yang diperoleh (dq) sedang panas yang diperoleh dari gaya kerja adalah (−dw), persamaannya adalah sebagai berikut: dE = dq − dw. (5.13) Dimana pada dE ada sejumlah energi di dalam sistem itu (internal energi) halmana total perubahan energi di dalam sistem itu adalah: dE = Eakhir – Eawal = ΔE. (5.14) dimana nilai ΔE. Tidak tergantung dari kedua sistem itu berlangsung, sebaliknya berbeda dengan nilai dq dan dw ada sejumlah panas yang masuk relatif makin bertambah dengan panas internal. Jadi berbicara soal panas maka proses ini dikatakan sebagai “energy transfer”. Secara integral nilai dq dan dw tergantung dari E awal dan E akhir. Dalam percobaan Joule seperti uraian diatas adalah sustu sistem yang terisolasi, dimana jumlah energi total selalu tetap. Jika antara sistem dan lingkungan terjadi pertukaran kalor atau kerja, maka menurut hukum termodinamika pertama jumlah total energi yaitu energi sistem di tambah energi lingkungannya harus selalu tetap (rumus 5.14). Apabila nilai dq positif artinya energi diserap sistem, sedang nilai negatif menunjukan sistem melepaskan energi. Demikian pula, jika nilai dw positif artinya sistem dikenai kerja sistem, tapi bila negatif artinya sistem melakukan kerja. Simbol E adalah energi dalam (internal energi) dari sistem. Sedang ΔE perubahan energi dalam dari sistem. Termodinamika tidak berhubungan dengan teori mengenai struktur zat. Pengetahuan termodinamika telah berkembang sebelum adanya teori atom moderen, tetapi kita ~ 96 ~ sekarang telah mengetahui bahwa energi dalam merupakan banyaknya energi total yang dimiliki partikel suatu zat. Energi dalam ini berhubungan dengan ikatan kimia, energi kinetik, translasi, energi vibrasi yang berhubungan dengan ikatan, energi rotasi molekul-molekul poliatomik, energi ikatan antar molekul dan seterusnya. Energi dalam merupakan fungsi keadaan. Ini berarti nilai dari energi dalam tergantung pada keadaan sistem dan bukan tahapan yang dilaluinya. Nilai dari ΔE perubahan energi dalam, nilai ini tergantung dari keadaan awal dan akhir saja. Namun demikian internal energi merupakan kombinasi variable intensif dan variable ekstensif. Tabel 5.2 memperlihatkan hubungan bentuk energi dalam dan pasangan variable intensif0ekstensifnya. Tabel 5.2 Jenis Energi dan Bentuk Variabelnya Jenis Energi Variabel Variable Kerja intensif ekstensif Mekanik Tekanan (p) Volume P dV Termal Temperatur Entropi (S) T dS Kimia Potensial Kimia Mol (n) Δ dn (µ) Listrik Tegangan Muatan (Q) E dQ Grativitasi Medan Tinggi Mg dh gratifitasi Untuk dq dan dw, nilainya tergantung dari keadaan dan lintasan yang dipilih dalam proses transformasi yang terjadi. Bila sistem selama proses transformasi mengatasi reaksi kimia, maka keadaan awal dan akhir terlihat adanya perbedaan komposisi kimia. Untuk komponen dq disebut kalor reaksi. Apabila perubahan keadaan tidak diikuti dengan kerja, maka dw= 0 dan ΔE = q. Contoh yang paling umum adalah proses yang terjadi pada volume tetap. Perlu kita ~ 97 ~ ketahui bahwa proses yang terjadi di laboratorium dilakukan pada tekanan konstan. Pada kondisi tekanan tetap, dw=pΔV, p adalah tekanan dan ΔV adalah perubahan volume yang timbul. Dalam situasi sperti ini maka nilai ΔE: ΔE = dq-dw (lihat rumus 5.13), dengan dw=pΔV, maka ΔE=qv – pΔV (perubahan internal energi pada p tetap), sehingga qv = ΔE + pΔV. Pembahasan tentang hukum termodinamika tidak akan terlepas dengan pembicaran soal entalpi dan entropi. Untuk itu mari kita pelajari apa yang di sebut entalpi dan entropi. Entalpi (H) adalah jumlah energi yang dimiliki sistem pada tekanan tetap. Entalpi dirumuskan sebagai jumlah energi yang terkandung dalam sistem (E) dan kerja (W), persamaannya sebagai berikut: H=E+W (5.15) Dimana W = P × V : W = kerja sistem (joule), V = volume (liter) dan P adalah tekanan (atm). Seperti hukum kekekalan energi (lihat rumus 5.11), bahwa energi tidak dapat diciptakan dan tidak dapat dimusnahkan, tetapi hanya dapat diubah dari bentuk energi yang satu menjadi bentuk energi yang lain. Nilai energi suatu materi tidak dapat diukur, yang dapat diukur hanyalah perubahan energi (ΔE). Demikian juga halnya dengan entalpi, entalpi tidak dapat diukur, kita hanya dapat mengukur perubahan entalpi (ΔH) persamaan rumus entalpi adalah : ΔH = Hp – Hr (5.16) Dimana: ΔH adalah perubahan entalpi, sedang Hp = entalpi produk dan Hr = entalpi reaktan atau pereaksi. Apabila H produk > H reaktan, maka ΔH bertanda positif, berarti terjadi penyerapan kalor dari lingkungan ke sistem. Sebaliknya jika H reaktan > H produk, maka ΔH ~ 98 ~ bertanda negatif, berarti terjadi pelepasan kalor dari sistem ke lingkungan. secara matematis, perubahan entalpi (ΔH) dapat diturunkan kalkulasi matematis adalah sebagai berikut. H = E + W (1) . Pada tekanan tetap: ΔH = ΔE + PΔV (2); ΔE = q + W (3) dan Wsistem = –PV (4). Substitusi persamaan (3) dan (4) dalam persamaan (2): H = (q + W) + PΔV; H = (q – PΔV) + PΔV sehingga H = q.Jadi, pada tekanan tetap, perubahan entalpi (ΔH) sama dengan kalor (q) yang diserap atau dilepas. Sebagai ilustrasi agar lebih di pahami bagaimana hubungan entalpi dengan kerja endoterm dan eksoterm secara kimiawi (lihat gambar berikut). Gambar 5.2. Reaksi Endoterm dan Eksoterm dalam hubungan Entalpi. Dimana, (a). Reaksi kimia yang membutuhkan atau menyerap kalor disebut reaksi endoterm. Contoh: Reaksi pemutusan ikatan pada molekul unsur H2 adalah: H2 → 2 H ΔH = +a kJ. Reaksi endoterm dengan ΔH bertanda positif (+). (b). Reaksi kimia yang membebaskan kalor disebut reaksi eksoterm. Contoh: ~ 99 ~ Reaksi pembentukan ikatan pada molekul unsur H2 adalah: 2H → H2 ΔH = –a kJ. Reaksi eksoterm dengan ΔH bertanda (–). Entropi adalah salah satu besaran termodinamika yang mengukur energi dalam sistem per satuan temperatur yang tak dapat digunakan untuk melakukan usaha kerja. Mungkin manifestasi yang paling umum dari entropi adalah (mengikuti hukum termodinamika), entropi dari sebuah sistem tertutup selalu naik dan pada kondisi transfer panas, energi panas berpindah dari komponen yang bersuhu lebih tinggi ke komponen yang bersuhu lebih rendah. Umumnya beranggapan bahwa entropi itu mengukur perubahan yang tidak keberaturan (disorder) di dalam sistem. Pada suatu sistem yang panasnya terisolasi, entropi hanya berjalan satu arah (bukan proses reversibel/bolakbalik). Entropi suatu sistem perlu diukur untuk menentukan bahwa energi tidak dapat dipakai untuk melakukan kerja pada proses-proses termodinamika. Proses-proses ini hanya bisa dilakukan oleh energi yang sudah diubah bentuknya, dan ketika energi diubah menjadi kerja/usaha, maka secara teoritis mempunyai efisiensi maksimum tertentu. Selama kerja/usaha tersebut, entropi akan terkumpul pada sistem, yang lalu terdisipasi dalam bentuk kalor buangan. Pada termodinamika klasik, konsep entropi didefinisikan pada hukum kedua termodinamika, yang menyatakan bahwa entropi dari sistem yang terisolasi selalu bertambah atau tetap konstan. Maka, entropi juga dapat menjadi ukuran kecenderungan suatu proses, apakah proses tersebut cenderung akan "terentropikan" atau akan berlangsung ke arah tertentu. Entropi juga menunjukkan bahwa energi panas selalu mengalir secara spontan dari daerah yang suhunya lebih tinggi ke daerah yang suhunya lebih rendah. ~ 100 ~ Hukum Kedua Termodinamika Banyak peristiwa alam yang terjadi disekitar kita tidak cukup dijelaskan dengan hukum pertama termodinamika. Rumusan hukum tersebut tidak memberikan penjelasan mengenai arah dari dapat/atau tidaknya suatu proses berlangsung, fenomena ini disebut derajat kespontanan. Sebagai contoh keseharian kita dimana sebuah kolam tidak akan membeku di musim panas. Jika sebuah benda panas berinteraksi dengan benda dingin, maka tak terjadi bahwa benda panas tersebut semakin panas dan benda dingin semakin dingin, meskipun proses-proses tersebut tidaklah melanggar hukum kekekalan energi yang dinyatakan sebagai hukum pertama termodinamika. Hukum kedua termodinamika berkaitan dengan apakah proses-proses yang dianggap taat azas dengan hukum pertama, terjadi atau tidak terjadi di alam. Hukum kedua termodinamika seperti yang diungkapkan oleh Clausius mengatakan, “Untuk suatu mesin siklis maka tidak mungkin untuk menghasilkan efek lain, selain dari menyampaikan kalor secara kontinu dari sebuah benda ke benda lain pada temperatur yang lebih tinggi". ( Prof. Rudolf Clausius, yang menemukan peristiwa spontan yang tidak beraturan) Bertolak dari siklus Carnot, yakni siklus hipotesis yang terdiri dari empat proses terbalikkan, yaitu pemuaian isotermal dengan penambahan kalor, pemuaian adiabatik, pemampatan isotermal dengan pelepasan kalor dan pemampatan adiabatik; jika integral sebuah kuantitas mengitari setiap lintasan tertutup adalah nol, maka kuantitas tersebut yakni variabel keadaan, mempunyai sebuah nilai yang hanya merupakan ciri dari keadaan sistem tersebut, tak peduli bagaimana keadaan tersebut dicapai. Variabel keadaan dalam hal ini adalah entropi. Perubahan entropi hanya tergantung pada keadaan awal dan keadaan akhir dan tak tergantung pada proses yang menghubungkan keadaan awal dan keadaan akhir sistem ~ 101 ~ tersebut. Hukum kedua termodinamika dalam konsep entropi mengatakan, "Sebuah proses alami yang bermula di dalam satu keadaan kesetimbangan dan berakhir di dalam satu keadaan kesetimbangan lain akan bergerak di dalam arah yang menyebabkan entropi dari sistem dan lingkungannya semakin besar". Jika entropi diasosiasikan dengan kekacauan (tak beraturan) maka pernyataan hukum kedua termodinamika di dalam proses-proses alami cenderung bertambah ekivalen dengan menyatakan, kekacauan dari sistem dan lingkungan cenderung semakin besar. Sebagai contoh, bila kita menyebarkan wangi parfum. Molekul penyususun parfum akan menyebar memenuhi seluruh ruang pada saat disemprotkan. Kecenderungan pergerakan dari molekul-molekul parfum untuk menyebar memenuhi ruangan merupakan ciri peristiwa spontan. Di dalam ekspansi bebas, molekul-molekul gas yang menempati keseluruhan ruang kotak adalah lebih kacau dibandingkan bila molekul-molekul gas tersebut menempati setengah ruang kotak. Jika dua benda yang memiliki temperatur berbeda T1 dan T2 berinteraksi, sehingga mencapai temperatur yang serba sama T, maka dapat dikatakan bahwa sistem tersebut menjadi lebih kacau, dalam arti, pernyataan "semua molekul dalam sistem tersebut bersesuaian dengan temperatur T adalah lebih lemah bila dibandingkan dengan pernyataan semua molekul di dalam benda A bersesuaian dengan temperatur T1 dan benda B bersesuaian dengan temperatur T2". Pada tahun 1850, Rudolf Clausius seorang profesor Jerman menemukan sifat keadaan yang berkaitan dengan peristiwa perubahan spontan. Beliau menyimpulkan suatu besaran entropi , yang dalam bahasa Yunani “εντροπία [entropía], εν- [en-] (masuk) dan τροπή [tropē]” yang artinya mengkonversi, tapi banyak ahli kimia menyebut sebagai ~ 102 ~ “pemberi arah”. Pada saat itu Clausius menyadari bahwa entropi, S, merupakan ukuran derajat tidak beraturan. Esensi dari hukum kedua termodinamika adalah mendefinisikan sifat baru, entropi (S) yang merupakan fungsi keadaan. Nilai entropi maksimum dicapai pada kondisi keseimbangan untuk sistem terisolasi. Apabila di dalam sistem terisolasi (yang mencakup sistem dan lingkungan) proses yang spontan terjadi, misalnya sejumlah kalor , dqrev dipindahkan ke dalam sistem secara “reversibel” (perubahan yang sangat lambat jalannya) pada suhu T, entropi yang timbul akibat proses pada sistem tersebut didefinisikan sebagai: dS = (dq/T)rev (5.16) Dimana T adalah panas yang ditimbulkan pada sistem yang prosesnya bersifat reversible. Performan kerja pada sistem biasanya menggambarkan panas yang hilang pada sistem, jika nilainya negatif untuk kerja selanjutnya. Pertukaran entropi keseluruhan didefinisikan sebagai: dS = dq/T − dq/T = 0. (5.17) Dengan perkataan lain entropi adalah energi termal yang diserap oleh sistem dalam kondisi keseimbangan dibagi dengan suhu sistem. Perubahan entropi total dapat dijadikan ukuran spontanitas suatu reaksi dengan mengukurnya pada sistem terisolasi. Untuk proses spontan, perubahan entropi untuk terisolasi bernilai positif yaitu: ΔStotal =ΔSsis + ΔSling > 0 (5.18) Untuk memudahkan pengertian persamaan diatas, maka sebagai contoh: Satu gram es 0oC dimasukan ke dalam 4 gram air 10oC. Bila diketahui kalor spesifik air 1 kal/g oC dan ~ 103 ~ lebur es 80 kal/g. Apakah proses peleburan es merupakan peristiwa spontan ?. Penyelesaiannya adalah: pada proses pendinginan air sebanyak 4 gram dari 10oC menjadi 0oC akan dilepaskan kalor sebanyak = 4 gX 10oC X 1 kal/g oC= 40 kal. Jumlah es yang dapat melebur dengan 40 kal yang diperoleh dari pelepasan energi oleh air adalah: 40 kal = = 0,5 g 80.kal/g dqrev ΔSes = = T ΔSes = 0,5 X 80 g.kal/g = 0,1465 kal/K 273 K - dqrev/T = - CdT/T= -Cln 283/273 =0,1439 kal/K Dimana C = 4 kal/K untuk 4 gram sampel. Maka perubahan entropi total adalah: ΔStotal = ΔSes + ΔSair = 0,1465 kal/K – 0,1439 kal/K = 0,0026 kal/K = 0,0109 J/K Diperoleh ΔStotal> 0, berarti proses peleburan es adalah spontan. Energi Bebas dan Perubahan Spontan Bertolak dari hasil soal diatas, terlihat kriterian spontan ditentukan dengan mengetahui nilai ΔStotal atau ΔSuniversium. Untuk mengetahui nilai ΔStotal berarti harus diketahui nilai ΔSlingkungan yang secara praktek sulit dihitung karena harus diketahui secara pasti bagaimana interaksi yang terjadi antara sistem dan lingkungan. Yang kita perlukan sekarang adalah suatu kriteria yang dapat digunakan hanya kepada sistem itu sendiri. Untuk itu dikemukakan suatu ~ 104 ~ besaran termodinamika baru yang disebut energi bebas yang dicirikan oleh simbol G. Energi bebas terdiri dari: Energi bebas Helmholtz Energi bebas Gibss : A= U- TS : G= H – TS Fungsi hukum energi bebas dari Helmholtz, analogi dengan persamaan yang ada dalam proses entalpi, yakni: dE ≤ TdS − PdV.. Dengan kondisi isothermal maka didefinisikan sebagai berikut: d(E − TS) ≤ −PdV. (5.19) dimana fungsi F = E – TS sering disebut sebagai “Helmholtz function”, Walaupun demikian banyak literatur mengatakan sebagai Energi bebas Helmholts “Helmholtz free energy” atau fungsi kerja. Hanya disayangkan banyak simbol yang dipergunakan pada energi dalam, entalphi dan energi bebas Helmholtz , akhirnya mengukur perubahan energi lebih dikenal dengan “energi bebas Gibbs” yang di beri simbol “G”. Tapi pemakaian simbol ini tidak merupakan standar internasional. Kalau ilmuan di Amerika energi bebas Gibbs diberi simbol F, sedang untuk energi bebas Helmhots adalah A. Untuk proses pada suhu dan tekanan konstan digunakan energi bebas Gibbs, yang perubahannya ditunjukan oleh persamaan: ΔG = ΔH – TΔS (5.20) Kespontanan suatu proses dengan demikian dapat diukur dengan satu kriteria, yaitu perubahan energi bebas Gibbs (ΔG). Ketetapannya adalah untuk suatu proses yang terjadi pada suhu dan tekanan di dalam suatu sistem tertutup, perubahan secara spontan akan disertai oleh penurunan energi bebasnya. ~ 105 ~ ΔG < 0 Proses spontan Berangkat dari persamaan energi bebas Gibbs, ada dua unit energi yang merupakan perubahan energi bebas, yang pertama adalah ΔH dan yang kedua TΔS. Halmana ΔH kita kenal sebagai kalor reaksi pada tekanan konstan atau entropi, sedangkan TΔS adalah perkalian antara suhu dengan nilai entropi dalam sistem (K X J/K) sehingga TΔS pun merupakan ukuran energi yang disebut sebagai energi pengorganisasian sistem atau organizational energy of a system. Penggunaan kriteria baru ini menentukan perubahan yang bersifat spontan dapat ditentukan dengan melihat tanda ΔH dan ΔS yang kemungkinan prosesnya dapat dilihat pada tabel 5.3 berikut ini. Tabel 5.3. Kriteria Perubahan Spontan ΔG = ΔH – TΔS ( lihat. 5.20) Kasus 1 ΔH - ΔS + ΔG - 2 - - + 3 + + + - + 4 Hasil Spontan pada seluruh kisaran suhu Spontan pada suhu rendah Nonspontan pada suhu tinggi Nonspontan pada suhu rendah Spontan pada suhu Tinggi Non spontan pada seluruh suhu Contoh reaksi 2H2O(g)2H2(g)+O2(g) H2O (I) H2O (p) 2NH3(g)N2(g)+3H2(g) 3O2(g)2O3(g) Agar lebih dipahami konsep perubahan spontan, diberikan contoh soal, yakni ada reaksi disosiasi AB (g) A(g) + B(g). Apakah cenderung berjalan spontan pada suhu tinggi atau suhu rendah. Penyelesaian : Reaksi ini melibatkan pemecahan ikatan antara A dan B, maka energi harus diserap oleh sistem jadi ΔH>0. Karena 2 mol gas dihasilkan dari 1 mol gas maka terdapat kenaikan ketidak teraturan dari reaksi tersebut sehingga ΔS>0. Persamaannya adalah sebagai berikut: ~ 106 ~ ΔG = ΔH – TΔS = ? (+) (+) (+atau-) (-) = spontan (+)= tidak spontan Spontanitas reaksi pada suhu tertentu akan tergantung pada nilai relatif ΔH terhadap TΔS. Kita dapat prediksi bahwa makin tinggi suhu reaksi nilai TΔS akan makin besar (sementara ΔH tidak terlalu dipengaruhi suhu), sehingga operasi dan persamaan tersebut akan menghasilkan nilai ΔG < 0. Dengan demikian reaksi-reaksi disosiasi dari tipe akan cenderung spontan pada suhu yang tinggi. Perubahan Energi Bebas Standar, ΔG0. Seperti halnya ΔH, ΔU dan ΔS, energi bebas dari bahan kimia tergantung pada keadaannya. Untuk dapat menggunakan kaidah ini dalam suatu perhitungan diperlukan konvensi untuk menetapkan keadaan standar bagi energi bebas suatu zat. Konvensi keadaan standar untuk suatu zat adalah: -Padatan: senyawa/bahan murni pada tekanan 1 atm -Cairan: senyawa/bahan murni pada tekanan 1 atm - Gas : gas ideal pada tekanan 1 atm. - Terlarut : larutan ideal pada konsentrasi 1 M Perubahan energi yang dihasilkan bila pereaksi dan produk berada pada keadaan standar disebut sebagai perubahan energi bebas standar, ΔG0. Untuk reaksi suatu senyawa yang dibentuk dan unsur-unsurnya, maka ΔG0 mencerminkan nilai energi bebas pembentukan standar dari senyawa tersebut yang disimbolkan oleh nilai ΔG0. Bila senyawa yang dibentuk jumlahnya satu mol (yang biasanya ditampilkan pada data tabel termodinamika), umunya digunakan tanda garis pada bagian atas simbol (overbar) ΔG0. Berdasarkan konvensi, energi bebas pembentukan standar unsur pada keadaan bentuknya yang paling stabil ~ 107 ~ pada tekanan 1 atm didefinisikan besarnya = Nol pada suhu tertentu. Beberapa contoh dituliskan pada tabel 5.4 sebagai berikut. Tabel 5.4. Nilai ΔHf0, ΔGf0 dan ΔSf0 beberapa Zat Br2(g) Br2(I) C (berlian) Grafit I2 (g) I2 (p) ΔHf0, kJ/mol ΔGf0 kj/mol 30,71 0 1,88 0 62,26 0 3,14 0 2,85 0 19,37 0 ΔSf0, J mol1 -1 K 245,35 152,30 2,43 5,69 260,58 116,7 Beberapa sifat ΔG yang harus diperhatikan adalah: 1. ΔG adalah suatu besaran yang bersifat ekstensif 2. ΔG akan berubah tanda bila proses berjalan sebaliknya 3. ΔG untuk seluruh proses bersih dapat diperoleh dengan menjumlahkan nilai-nilai ΔG dari masingmasing. Energi Bebas dan Kesetimbangan Seperti uraian di atas bahwa ΔG < 0 maka proses berjalan spontan dan sebaliknya. Suatu keadaan harus dapat kita jelaskan bila suatu proses mempunyai nilai ΔG = 0. Keadaan ini disebut keadaan setimbang, bila suatu sistem dalam keadaan setimbang akan terdapat suatu kecenderungan yang sama (equal) dari suatu proses untuk bergerak ke arah produk atau ke arah pereaksi. Apabila dalam keadaan kesetimbangan terjadi perubahan yang sangat kecil dari variabel percobaan misalnya suhu atau ~ 108 ~ tekanan, maka perubahan tersebut tidak akan mengganggu perubahan bersihnya. Jika terjadi keseimbangan, ilustrasinya disajikan pada gambar 5.3 berikut: ΔH, TΔS ΔH ΔG < 0 ΔG > 0 ΔG = 0 TΔS SUHU (K) Gambar 5.3. Perubahan Energi Bebas Sebagai Fungsi Suhu Melihat pada gambar 5.3, di garis pertama memperlihatkan variasi suhu terhadap perubahan enthalpi , dan garis vertikal menunjukan hasil perkalian TΔS. Garis ΔH akan mempunyai kemiringan positif pada suatu kasus dan negatif pada kasus yang lain, tapi pada umumnya kemiringan bersifat datar (gradual). Dapat dikatakan bahwa ΔH tidak sensitif terhadap perubahan suhu. Kemiringan dari garis T ΔS diduga lebih curam. Jarak vertikal dari garis TΔS terhadap ΔH menunjukan nilai ΔG= ΔH – TΔS. Dimulai dari sebelah kiri gambar, nilai ΔG akan positif dan besar. Besarannya nilai ΔG akan menurun dengan meningkatnya suhu. Pada sisi kanan gambar, nilai TΔS melebihi ΔH sehingga nilai ΔG menjadi negatif. Pada perpotongan kedua garis tersebut, biasanya nilai ΔG = 0, dan sistem tersebut pada keadaan seimbang. ~ 109 ~ Peristiwa transisi fasa adalah suatu proses yang berada dalam keseimbangan. Dengan demikian fenomena kesetimbangan pada gambar 5.3 dapat dimanfaatkan untuk menghitung entropi pada peristiwa tersebut. Hakekatnya, seandainya gambar 5.3 adalah gambar yang menjelaskan mengenai pencairan es. Bila kita mulai dengan air dengan wujud padat dan cairan pada keadaan standarnya (misalnya pada tekanan 1 atm), maka titik perpotongan dari dua garis adalah pada 273, 15 K, suhu ini merupakan titik cair normal es. Pada 273, 15K cairan air berada pada kesetimbangan dengan wujud padat. Perubahan entropi, ΔS 0 untuk pencairan/peleburan es (kalor lebur molar es pada 273, 15K adalah 6,02 kJ/mol), maka dapat ditentutukan sebagai berikut: Tampak bahwa untuk proses transisi fasa, persamaan dapat di-modifikasi. Untuk proses umum transisi fasa seperti peleburan dan pembekuan, penguapan dan kondensasi, perubahan entropi pada proses tersebut dinyatakan dengan rumus: ΔG = ΔH – TΔS = 0 ΔS = atau ~ 110 ~ ΔS0tr = Secara matematis menghitung entropi didasarka pada rumus diatas, pertanyaan berapa entropi penguapan molar standar air pada 1000C . Enthalpi penguapan molar standar pada suhu 1000C adalah 40,7 kJ/mol. Penyelesaian sebagai berikut: Persamaan kimia proses tersebut adalah : H2O (C, 1 atm) H2O (g, 1 atm) Tabel berikut di sajikan beberapa nilai perubahan entropi molar standar untuk fasa, yakni: Tabel 5.5. Perubahan Entropi Molar Standar Untuk Transisi Fasa Bahan Ttrs ΔH0trs ΔS0trs J mol-1 kJ/mol 1K Penguapan: Aseton 320 30,25 91,9 Etanol 351 39,33 112.1 n-heksana 342 28,58 83.6 timbal 2042 179,41 88,6 Peleburan: Benzena 279 9,83 35,2 Kamper 452 6,86 15,2 Timbal 601 4,77 7,9 merkuri 234 2,30 9,8 Hukum Ketiga Termodinamika Meskipun nilai absolut dari kebanyakan sifat-sifat termodinamika tidak dapat ditentukan, adalah mungkin untuk memperoleh nilai absolut dari entropi untuk berbagai ~ 111 ~ bahan. Hal ini dimungkinkan oleh hukum ketiga termodinamika menyatakan bahwa: “Entropi suatu kristal sempurna yang murni pada suhu NOL absolut adalah NOL.” Kristal sempurna pada suhu nol absolut menunjukan tingkat paling teratur yang mungkin diperoleh untuk suatu sistem termodinamika. Jika suhu naik dari suatu nilai yang dekat dengan O K. Maka entropi akan naik. Entropi absolut selalu bernilai posistif. Bila terdapat lebih dari satu bentuk fase padatan (alotropi), maka akan terdapat entropi transisi pada suhu dimana bentuk pada suhu yang rendah akan berubah menjadi fase padatan baru. Kenaikan drastis yang lain dari entropi dapat terjadi titik cair padatan, dan masih lebih besar lagi pada titik didih cairan keragaman nilai entropi absolut dengan suhu. ~ 112 ~ ⑥ KINETIKA DAN KRISTALISASI T idak semua proses reaksi geokimia mengikuti hukum kesetimbangan karena proses-proses itu sangat kompleks, seperti kristalisasi dari magma dan pembentukan kembali kristal batuan metamorf (batuan ubahan) umumnya di kendalikan oleh aktivitas kinetika atau laju reaksi. Apalagi penyusunan kristal dari material kecil (mineral) selalu melalui suatu proses yang membutuhkan suhu tertentu sehingga terbentuk partikel padatan yang struktur sangat kuat. Berikut ini kimiawan ahli geokimia McSween, dkk (2003) melukiskan suatu contoh kristal yang terbentuk dari partikel/mineral kecil, melalui suatu proses nukleasi, seperti gambar berikut: Gambar 6.1. Struktur Kristal pyroxena C2/c . Sumber: McSween dkk (2003), ~ 113 ~ Secara geometri M1 dan M2 adalah kation yang dikelilingi oleh enam atom oksigen dan kesemua atom itu membentuk tetrahidral (T). Bentuk diatas tersusun kurang lebih 100 bentuk kristal yang dibantu dengan atom silicon, sehingga tersusun struktur yang padat. Uraian berikut akan membahas tentang kinetika dan kristalisasi, kedua aspek ini saling keterikatan ditinjau dari sudut pandang kimia. Halmana kinetika kimia mempelajari laju (kecepatan) dan mekanisme reaksi. Laju reaksi dinyatakan sebagai perubahan konsentrasi atau tekanan dari produk atau reaktan terhadap waktu. Perubahan konsentrasi lazim dinyatakan dalam satuan mol L-1 atau M, atau dengan kata lain adalah kecepatan berkurangnya pereaksi atau bertambahnya produk reaksi dinyatakan dlm molar/detik (mol.L−1.s−1). Sedang yang dimaksud dengan mekanisme reaksi adalah seperangkat proses dasar yang menjelaskan kemolekulan reaksi. Suatu reaksi sering kali tersusun dari serangkaian langkah reaksi. Urutan langkah-langkah terjadinya reaksi ini dikenal sebagai mekanisme reaksi. Sedang kristalisasi adalah proses penyusunan kristal dari bentuk atom dan ion menjadi struktur yang padat dan morfologinya berbeda-beda. Pengetahuan tentang kinetika kimia dirintis oleh Peter Waage pada tahun 1864, sehingga terbitnya hukum aksi massa, yang menyatakan bahwa kecepatan suatu reaksi kimia secara proporsi dengan kuantitas zat yang bereaksi ( setiap reaksi kimia, jumlah massa sebelum dan sesudah reaksi selalu sama). Prinsip dari persamaan Laju adalah persamaan yg mengaitkan laju reaksi dengan konsentrasi molar pereaksi dgn pangkat yang sesuai, seperti persamaan berikut: dX/dt = V = k. [A]a.[B]b (6.1) Dimana k, (tetapan Laju) adalah tetapan perbandingan antara laju reaksi dan hasil kali konsentrasi jenis zat yang ~ 114 ~ mempengaruhi laju reaksi. Hakekatnya: Tetapan laju = koefisien laju = laju reaksi jenis Kristal adalah zat padat yang mempunyai bentuk bangun beraturan yang terdiri dari atom-atom, molekul atau ion dengan susunan teratur, dan polanya berulang melebar secara tiga dimensi (lihat gambar 6.1). Jadi kristalisasi adalah proses pembentukan padatan kimia dari unsur kimia mikro/partikel kecil melalui pembekuan atau reaksi kimia. Seorang ahli keturunan Jerman yaitu Van’t Hoff yang mulamula memanfaatkan azas fasa untuk mempelajari kristalisasi larutan garam dan pembentukan endapan garam. Dia meneliti bagaimana kecepatan reaksi kimia dari ion garam yang terkecil sampai membentuk endapan berbentuk kristal. Pada intinya penyusunan atom sehingga menjadi padatan biasanya mengikuti kaidah penggabungan volume, yaitu volume dua gas yang bereaksi (pada suhu dan tekanan sama) merupakan nisbah dari bilangan-bilangan bulat yang sesderhana. Demikian pula, nisbah volume setiap produk (gas, cair dan padatan) terhadap volume dari masing-masing komponen itu yang bereaksi merupakan nisbah dari bilanganbilangan bulat yang sederhana. Sebagaimana penjelasan diatas, bahwa laju reaksi adalah penambahan konsentrasi produk atau pengurangan konsentrasi reaktan per satuan waktu, maka berdasarkan jumlah molekul yang bereaksi dikenal ada tiga kelompok yaitu: (1) reaksi unimolekuler (hanya 1 mol) reaktan yang bereaksi, contoh: N2O5 → N2O4 + ½ O2. (2) reaksi bimolekuler ada 2 mol reaktan yang bereaksi, contoh: 2HI → H2 + I2. (3) reaksi termolekular ada 3 mol reaktan yang bereaksi, contoh 2NO + O2 → 2NO2. . Kalau didasarkan pada banyaknya fasa yang terlibat, maka dikenal reaksi homogen dan heterogen. Secara kuantitatif, kecepatan reaksi kimia ditentukan oleh orde ~ 115 ~ reaksi (n), yaitu jumlah dari eksponen konsentrasi pada persamaan kecepatan reaksi. n = umumnya bilangan bulat kecil (1,2,3…) dalam hal tertentu bisa berupa pecahan atau nol. Jadi orde reaksi dapat diuraikan sebagai berikut: 1. Reaksi Orde Nol; pada reaksi orde nol, kecepatan reaksi tidak tergantung pada konsentrasi reaktan.Persamaan laju reaksi orde nol dinyatakan sebagai berikut: A – A0 = – k0 . t (6.2) A = konsentrasi zat pada waktu t A0 = konsentrasi zat mula – mula Contoh reaksi orde nol ini adalah reaksi heterogen pada permukaan katalis. 2. Reaksi Orde Satu; pada reaksi orde satu, kecepatan reaksi berbanding lurus dengan konsentrasi reaktan. Persamaan laju reaksi orde satu dinyatakan sebagai berikut: ln = k1 (t – t0) (6.3) Bila t = 0 –> A = A0 ln [A] = ln [A0] - k1 t [A] = [A0] e-k1t 3. Reaksi Orde Dua; persamaan laju reaksi untuk orde dua dinyatakan sebagai berikut : -dA [A]2 -dA/ 2 [A] = k2 t 1 /[A] - 1/[Ao] = k2 (t – t0) / dt = k2 (6.4) Dalam proses kinetika (laju rekasi) temperatur sangat mempengaruhi kecepatan reaksi. Kalau bab-bab terdahulu menjelaskan perubahan bentuk senyawa kimia oleh adanya suhu rendah. Tapi suatu kenyataan kinetika banyak berperan aktif pada proses geokimia dengan suhu tinggi termasuk ~ 116 ~ kristalisasi dari magma atau rekristalisai dari batuan ubahan (metamorf). Halmana kecepatan reaksi (r) X →Y + Z, dapat dilukiskan sebagai : −dX/dt = k(X)n, Dimana X adalah konsentrasi reaktan pada waktu “t” dan k merupakan nilai konstanta, sedang “n” menunjukan orde reaksi. Untuk kecepatan pengendalian proses magma atau sistem metamorf sangat tergantung pada nilai konstanta temperatur. Hubungan antara rata-rata nilai konstanta dan temperatur mengikuti rumus Arrhenius sebagai berikut: k=A exp(−∆G¯*/RT), (6.5) dimana A faktor frekuensi, ∆G¯* adalah energi aktivasi R adalah konstanta molar gas, dan T adalah suhu absolut. Karena terjadi tabrakan dua molekul maka kecepatan reaksi sesuai dengan frekuensi tabrakan tersebut. Faktor frekuensi (A) menunjukan jumlah waktu per detik molekul atom pada reaksi penuh. Walaupun demikian tidak semua peristiwa tabrakan dapat menyebabkan reaksi, karena kemungkinan tabrakan antar molekul tidak cukup energi untuk bereaksi. Olehnya setiap reaksi yang terjadi ada batas nilai energi yang dibutuhkan. Secara teori transformasi satu zat ke zat lainnya melalui rekasi kimia selalu diiringi dan dipengaruhi oleh perubahan energi. Energi yang menggerakan suatu reaksi kimia disebut “energi aktivasi” (activation energy) yakni energi bebas yang keluar untuk melakukan proses reaksi (Ea). Dimana (−∆G¯*/RT) menunjukan fraksi reaksi atom yang memiliki energi tinggi melebihi energi rata-rata masuk ke dalam sistem untuk mendorong suatu reaksi kimia. Berbicara tentang energi bebas ada yang disebut “faktor Boltzmann” (sifatnya mirip dengan distribusi Boltzmann pada hukum statistika). Bentuk eksponensial negatif dari faktor Boltzmann ~ 117 ~ berhubungan dengan temperatur tinggi dalam sistem, sangat tergantung pada nilai ∆G¯*, dan kecepatan konstanta boleh berubah adanya perubahan temperatur. Prinsip teori tabrakan pada laju reaksi ialah suatu reaksi antara atom, ion, dan/atau molekul harus melalui tabrakan antar partikel. Teori tabrakan mengatakan bahwa laju reaksi berbanding lurus dengan jumlah tabrakan yang terjadi antara molekul-molekul zat yang bereaksi tiap detik (faktor frekuensi/A). Laju reaksi berbanding lurus dengan frekuensi tabrakan yang terjadi (A), fraksi molekul teraktifkan (f), dan peluang untuk bertabrakan (p). Frekuensi tabrakan bergantung pada konsentrasi zat yang terlibat dalam reaksi. Kenaikan konsentrasi zat yang bereaksi memperbesar jumlah tabrakan per satuan waktu. Akan tetapi, harus diingat bahwa tidak semua tabrakan yang efektif. Agar tabrakan efektif, zat-zat yang bereaksi harus (1) memiliki energi minimum tertentu yang dibutuhkan untuk penyusunan partikel-partikel kembali, dan (2) mempunyai orientasi yang sesuai satu sama lain pada saat bertabrakan. Bagian yang akan bertabrakan dengan efektif bergantung pada sifat pereaksi dan suhu. Energi yang harus dimiliki suatu molekul agar dapat bereaksi disebut energi aktivasi hipotesis (Ea). Laju reaksi bergantung pada hasil kali frekuensi tabrakan dengan fraksi molekul yang berenergi ≥Ea. Semakin besar energi aktivasi semakin kecil fraksi molekul dan semakin lambat reaksi berlangsung. Dalam kecepatan reaksi, hakekatnya hanya sebagian kecil dari tabrakan efektif yang akan menghasilkan reaksi. Jika dua molekul reaktan bertabrakan dengan pergerakan yang lambat, awan elektron molekul yang satu tidak dapat memasuki molekul lainnya sehingga tidak terjadi perubahan kimia. Sebaliknya, bila tabrakan keras (gaya tabrakan cukup besar),molekul-molekul akan saling berdekatan dan awan elektron saling mempengaruhi. Hal ini ~ 118 ~ menimbulkan pemutusan dan pembentukan ikatan, dan reaktan pun berubah menjadi produk. Terdapat gaya kinetik minimum yang harus dimiliki suatu molekul untuk mengatasai gaya tolak diantara awan-awan elektron pada saat bertabrakan. Energi kinetik minimum ini disebut energi aktivasi. Pada suatu reaksi kesetimbangan A + B2 ⇆ AB + B, kita misalkan reaksi kekanan melibatkan perubahan energi E1. Reaksi sebaliknya melibatkan perubahan teori keadaan transisi, pada reaksi ini dapat digambarkan sebelum A dan B membentuk AB dan B akan terdapat transisi A-B-B. A + B-B Reaktan A- B–B A–B+B Produk Keadaan transisi (6.6) Suatu reaksi akan berlangsung melalui keadaan transisi yang memiliki energi E1 lebih besar daripada keadaan awal (reaktan) dan E1 lebih besar daripada keadaan (produk). Ilustrasinya pada gambar berikut memperlihatkan koordinat rekasi yang ditentukan oleh energi potensial. Koordinat reaksi adalah parameter yang terus bervariasi, dan setiap nilai sesuai dengan seperangkat atom atau molekul sistem reaksi sepanjang jalannya reaksi. A—B--B A—B--B EP reaksi EP reaksi ke kiri ke kanan EP reaksi ke kanan Produk AB + B △E rekasi △E rekasi Reaktan A + B EP reaksi ke kiri Reaktan AB + B (a) (b) Koordinat Reaksi Produk A + B Gambar 6.2. Koordinat Energi Potensial Untuk reaksi Keterangan: (a) reaksi endoterm dan (b) reaksi eksoterm. ~ 119 ~ Penggabungan/difusi Kejadian suatu reaksi kimia pada prinsipnya merupakan penggabungan dua unsur kimia. Walaupun penggabungan (difusi) secara fisik kelihatan reaksi kimia mudah berlangsung, namun reaksi kimia itu diatur dengan energi aktivasi. Energi aktivasi atau energi pengaktifan adalah energi minimum yang harus dimiliki oleh molekul pereaksi agar menghasilkan tabrakan yang efektif. Komponen kecil dapat bergerak bebas dipermukaan (difusi permukaan) di antara partikel-partikel kecil (difusi antar pertikel) atau cairan (difusi volume). Penggabungan zat kimia itu (padat maupun cair) dapat berkembang oleh suhu tinggi. Berkaitan dengan difusi volume, dimana penggabungan dapat terjadi antar atom atau ion yang sama (misalnya zat oksigen bergabung dengan oksigen lain di senyawa lain). Bisa terjadi interdifusi, dimana satu atom atau ion dapat bergabung dengan sistem berlawanan (misalnya, Mg – Fe pertukaran olivin). Umumnya, proses interdifusi dapat menurunkan kecepatan penggabungannya. Dalam persamaan Fick, pemindahan materi didalam suatu media dapat berlangsung terus-menerus. Proses pemindahan antar dua zat akan menyangkut dengan koefisien difusi (D), dimana pengukuran penggabungan hanya dapat menggunakan ” tracer koefisien difusi ( D * )”, suatu teknologi menggunakan isotop (misalnya, 18O bergerak melalui ikatan oksigen pada silikat ). Kalau koefisien interdifusi (D1-2) adalah merupakan interaksi ion satu dengan ion lainnya. Secara empiris hal itu dapat dihitung dengan “trace koefisien” dari setiap jenis di dalam sistem itu: D1–2 = (n1D1* + n2D2*)/(n1 + n2). Memang pada sangat kompleks sistem geologi penggabungannya untuk dianalisa oleh karenanya ~ 120 ~ menghitung D1–2 sangat sulit , karena kita harus terlebih dahulu mengumpulkan sejumlah data eksperimen untuk memperkirakan koefisien tracer dalam sistem yang reaksi. Oleh karena itu dalam kimia geologi dilakukan pendekatan alternatif yaitu cara konvensional pengikatan kimia, dengan asumsi difusi yang terjadi adalah secara mekanik (fisik), seperti analisa yang dilakukan pada pengikatan atom logam dan batuan, akibat pengikatan ion membentuk mineral atau pembentukan struktur kristal. Penggabungan volume pada unsur padat terjadi pemindahan atom atau ion yang tidak sempurna seperti struktur kristal. Bentuk fisik kristal akan terdapat kekosongan atom pada kisi-kisi tertentu, diantara kisi-kisi itu terdapat elektri netral. Frenkel menyatakan kisi-kisi itu terbentuk karena ditinggalkan oleh ion sehingga terjadi kekososngan, tapi Schottky mengatakan jumlah kation dan anion dalam posisi sama sehingga terjadi kekosongan. Dalam kristal murni terdapat juga di bagian luar (extrinsic) yang cacat (kekosongan), hal ini disebabkan oleh ion-ion asing yang bermuatan berbeda dengan ion asli sehingga ion asing menempatinya. Karena prinsip kesetimbangan tidak terpenuhi maka terjadi kekosongan pada struktur kristal, seperti penggabungan Fe3 + menjadi olivin biasanya menempati tempat kosong dalam kristal memerlukan kation. Secara umum diketahui bahwa kristal non-stoikiometri juga memiliki kekosongan. Jadi kristal mengandung intrisik dan ekstrinsik yang cacat, pembentuknya atau penggabungannya tergantung pada suhu, namun lebih efektifnya proses penggabungan atom pada suhu tinggi. Seandainya suhu diturunkan maka peluang terjadi pemasukan ion asing makin besar dan proses intrinsik akan terjadi sebaliknya. Mekanisme difusi ekstrinsik mungkin mendominasi sistem alam , karena kebanyakan mineral mengandung ~ 121 ~ banyak kotoran , dan suhu untuk sebagian besar proses geologi kurang dari yang dibutuhkan untuk mekanisme intrinsik. Biasanya makin banyak bagian yang cacat akan berperan penting pada proses penggabungan volume, termasuk dislokasi , perpindahan bidang kisi , dan berbagai macam cacat planar , seperti batas-batas kembar dan susunan yang tidak teratur dan termasuk patahan kecil. Bagian yang cacat merupakan saluran efektif untuk penggabungan/difusi ( sering disebut “short circuits”) di mana saluran ini dapat mengontrol kelimpahan sampai pada bagian kristal yang terjadi kekosongan, walaupun kekosongan yang panjang sulit untuk model kuantitatif. Lingkaran lobang kecil terkadang dianggap sebagai cacat panjang, sehingga mengkaburkan antar difusi volume dan difusi bunderen kecil. Banyak ahli geokimia percaya bahwa perpindahan massa atom pada batuan metamorf yang efektif berasal dari butiran padat. Meskipun gagasan ini mungkin benar dalam banyak kasus , namun proses pengikatan material sangat tergantung pada kekuatan kimiawi dan efektifitas suhu di lingkungannya. Nukleasi Bertolak dari perspektif termodinamika terbentuknya kristal adalah hal yang menajubkan, karena proses nukleasi dari fase produk volume kecil diinisiatif menjadi kristal (padatan besar). Pengertian nukleasi adalah proses penyusunan atom/ion membentuk suatu inti struktur material yang padat, contohnya pembentukan kristal. Sangat sulit dimengerti bahwa inti kristal dapat terbentuk oleh adanya fluktuasi pemanasan yang bersifat sementara. Karena belum ada penelitian yang secara rinci mengamati pembentuk kristal inti. Kekuatan pendorong untuk nukleasi sama halnya dengan prinsip kecepatan proses lainnya mengikuti sistem ~ 122 ~ kesetimbangan. Secara umum dapat dikatakan kekuatan pendorong terbentuknya inti kristal adalah sangat jenuh (supersaturation) terhadap kosentrasi dan kesetimbangannya. Dalam studi geokimia sering dikatakan suatu penyimpangan dari kesetimbangan dalam cara lain, yaitu, kondisi dibawa pendinginan (△T), ini merupakan parameter untuk melihat kesetimbangan antara suhu penampilan pertama dari fase dan suhu di mana itu benar-benar muncul Sebagai contoh, dalam magma, kristalisasi biasanya gagal terjadi karena adanya suhu tinggi melelehkan batuan, nilai △T adalah sama dengan suhu minus di bawah suhu leleh. Nukleasi Pada Situasi cair Suatu pengikatan kimia yang terjadi di saat penurunan derajat bebas dalam sistem dilukiskan secara deferensial dengan persamaan berikut: (6.7) Dalam prakteknya , persamaan diatas melukiskan setiap fase penyusunan selalu mengikuti sifat termodinamika kimia. Jika pengikatan satu fase dengan fase yang lain dengan termodinamika bersifat diskontunitas, hal itu menunjukan tidak ada kontribusi energi dalam sistem itu. Harus diakui bahwa tidak mudah memberikan penjelasan antara fase satu dengan yang lain dalam kaitannya sifat termodinamika diskontunitas. Atom-atom pada permukaan tetesan atau kristal bagian dalamnya tidak disertai dengan pengikatan yang seragam . Penyusunan struktur terganggu oleh adanya pengikatan yang tidak teratur, hal tersebut membutuhkan peningkatan energi bebas. Umumnya energi bebas dipermukaan jumlahnya sedikit karena jumlah atom pada fase pengikatan lebih banyak dari yang ada didalamnya. ~ 123 ~ Dapat diprediksi selama nukleasi sumbangan rata-rata inti kristal atau tetesan (droplet) adalah sangat kecil. Energi bebas dipermukaan yang menghambat proses kinetika, keadaan demikian disebut sebagai pendinginan (undercooling). Suatu energi bebas akan berasosiasi dengan kondisi minimal maka akan terbentuk pertikel juga minimal. Untuk itu diperlukan suatu kekuatan baru mendorong pembentukannya, kekuatan itu disebut sebagai kekuatan tensional (δ). Hakekatnya tegangan permukaan hanya berlaku pada fase cair tidak berlaku pada fase padat. Kekuatan tensional akan hilang pada nukleasi di kristal. Tegangan permukaan dapat dipandang sebagai ukuran perubahan energi bebas karena peningkatan permukaan partikel di daerah A , yaitu Apabila “G” didefrensialkan maka dapat dimodifikasi dengan persamaan berikut: Dimana △Gvol simbol yang berkaitan dengan suhu, tekanan dan komposisi yang ada dalam volume keseluruhan. Jadi unutk inti keseluruhan dengan radius “r” di rumuskan sebagai berikut: (6.8) Dimana △G adalah energi bebas per volume. Karena σ selalu positif maka radius kecil energi permukaan lebih ~ 124 ~ mendominasi tapi jika radius besar akan didominasi oleh volume. Kondisi yang tidak stabil implikasinya jika radius r naik sampai pada keadaan radius kritis (r crit) energi bebas akan meningkat dalam proses nukleasi, dan apabila energi bebas cenderung menurun sampai pada radius kritis (rcrit) maka pembentukan inti akan makin kecil. Untuk lebih jelasnya, berikut ini dibuat contoh soal yaitu, umpamanya pembentukan inti “forsterit” pada Mg2SiO4 cair. Dengan asumsi sebagai pendingin 10 ° C dan energi permukaan 103 ergs cm-2 (= 2.39 × 10-5 kal cm-2) serta radius kristis pada inti olivin dibawah kondisi, pertanyaannya bagaimana energi bebas pada inti dengan radius bervariasi ?. ΔGv pada olivin dengan suhu 2063 K (10 K di bawah cairan forsterit) adalah -1,738 cal cm-3. Didasarkan pada rumus 6.8, maka subsitusinya mengikuti persamaan berikut: (6.9) Jika r = 2 × 10−5 cm, maka ΔGtotal adalah 6.18 × 10−14 cal. Nukleasi pada padatan Sesungguhnya proses nukleasi pada materi padatan dapat saja terjadi namun prosesnya lebih rumit. Berbicara pemindahan fasa pada material padat tidak terlepas dengan perubahan volume melalui fase reaktan. Hal ini menimbulkan masalah ruang untuk memasukan energi. Jadi harus ada energi tambahan ke dalam sistem, sehingga energi bebas akan berbentuk persamaan ini: ΔGtotal = 4π/3r 3(ΔGv + ΔGs ) + 4πr 2σ, Dimana ΔGs adalah energi regangan Nukleasi pada batuan metamorf mungkin selalu heterogen. Seperti butiran kecil, dislokasi dan daerah rentang ~ 125 ~ yang merupakan faktor pembentuk inti, dalam hal ini pada sistem proses nukleasi dapat menurunkan energi bebas. Sebuah contoh menarik nukleasi pada padatan dengan yang berada di larutan-padat, seperti pyroxene dan feldspars biasanya proses yang terjadi lambat. Gambar berikut memperlihatkan percobaan solvus (padatan dalam larutan) yang ada didalam NaAlSi3O8-KAlSi3O8. Gambar 6.3. Diagrama Percobaan Tentang Solvus dan Spinodal Keterangan: Grafik bagian atas memperlihatkan diagram T-Xor pada sistem “feldspar” alkali dengan bentuk reaksi Solvus dan Spinodal. Sedang grafik dibawahnya adalah diagrama Ĝ-Xor memperlihatkan pergerakan suhu, dimana titik a1-a2 adalah lokasi solvus sedang grafik lengkung b1-b2 merupakan garis spinodal. Gambar diatas menunjukan “feldspars” alkali yang homogen dengan kondisi solvus merupakan bagian padatan sedang pendinginan sehingga terbagi ke dalam dua bagian (lihat titik a1 dan a2), nukleasi di bagian luar sistem padatan ~ 126 ~ bisa juga homogen ataupun heterogen. Dalam gambar 6.3. grafik lengkung kearah bawah (a1-a2) menunjukan kondisi suhu pada felspars alkali, sehingga pada titik A1 –A2 adalah bentuk suhu relatif stabil. Bentuk nukleasi yang lain, oleh adanya percepatan reaksi bisa membentuk A1 dan A2 dengan komposisi yang stabil, kondisi ini sering disebut “spinodal” (gambar 6.3. bagian atas). Disamping itu oleh adanya keterbatasan solvus dan campuran suhu yang rendah terbentuklah dua titik, yaitu b1 dan b2. (δ2ĜδX2=0) yang membentuk lengkungan spinodal. Apabila komposisi feldspar berlebihan di antara titik B1 dan B2 dimana isi berfluktuasi (contoh pada x1 dan x2), maka energi bebas akan hilang dan feldspare akan menjadi homogen. Artinya dalam kondisi itu tidak terjadi percampuran situasi seperti ini disebut “dekomposisi spinodal”. Jadi pada fase homogen spinodal sangat terbatas (b1 ke b2) dan pada lokasi titik x1 dan x2 kondisi relatif stabil. Disamping itu pada titik x3 dan x4 kondisinya tidak terjadi percampuran/pengikatan. Permasalahan, antar homogen dan fase diluar percampuran perbedaan energi adalah kecil, sebab adanya atom yang tidak kesesuaian maka komposisi antara x1 dan x2 adalah kecil sehingga energi yang masuk kecil. Oleh karena itu , pada batas antaranya tidak terjadi percampuran (difusi) dengan demikian kelihatan dekomposisi spinodal utama tidak melibatkan nukleasi. Sehingga komposisi antara titik A1 dan A2 terjadi kestabilan yang kuat (sangat padat). Penyusunan keseluruhan “feldspars” pada letak solvus dan spinodal (lihat gambar 6.3: grafik antara titik A1 dan B1 atau A2 dan B2) dengan pengontrolan larutan padat solvus mengakibatkan tidak terjadi percampuran. Hal ini dikarenakan struktur yang tidak cocok sehingga kinetika (laju reaksi) terhambatdan kerja nukleasi juga lambat. Larutan padatan pada fase solvus kinetikanya sangat susah mengakibatkan pengikatan lambat, barangkali ~ 127 ~ pengaruhnya temperatur, waktu dan pemindahannya. Secara ilustrasi di lukiskan pada gambar 6.4, berikut. Gambar 6.4. Hubungan Suhu, Waktu dan Kecepatan Berpindah Sumber : Marine Geochemistry oleh Chester dan Jickells (2012) Gambar diatas memperlihatkan suatu percobaan untuk melihat sintesis kerja kinetika yang dipengaruhi oleh suhu dan waktu. Terlihat dua grafik yang melengkung (bergaris dan hitan) adalah bentuk produk yang dimulai dari 1% sampai bisa mencapai 99% dengan mengikuti prinsip kesetimbangan yang dipengaruhi atau dikontrol oleh nukleasi homogen atau dekomposisi spinodal. Sebagai contoh, pada kondisi proses pendinginan yang lambat (slow cooling) lebih kearah nukleasi homogen ketimbang dekomposisi spinodal. Sebaliknya pada tingkat pendinginan yang benar (tidak lambat dan tidak cepat) cenderung ke arah dekomposisi spinodal. Tetapi dengan kondisi pendingin yang cepat dekomposisi spinodal akan sempurna, dimana tidak terjadi lagi percampuran atau terjadi padatan kuat. ~ 128 ~ Perkembangan Pembentukan Kristal Pembentukan kristal dari partikel mikro sampai terbentuknya padatan yang kuat sangat tergantung pada : ❶ reaksi kimia pada lapisan pembatas (interface) antara kristal dan disekitarnya; ❷ difusi komponen ke dan dari lapisan pembatas; ❸ panas yang keluar dari pembatas pada saat proses kristalisasi; ❹ Bahan sekitar yang menyusun struktur kristal itu. Kalau pembentukan kristal pada mineral silika melalui hanya proses pada butir 1 dan 2 saja. Kemudian dua butir terakhir merupakan pengaruh lingkungan sekitarnya lebih kuat daripada penyusunan inti kristal yang dikendalikan oleh reaksi pembatas. Sebaliknya, jika pemindahan komponen ke pembentukan inti kristal berlangsung cepat artinya proses penggabungan berlangsung baik. Kecuali antara kristal dan sekitarnya komposisinya sama, maka lapisan pembatas tidak melakukan difusi dan pembentukan tidak terjadi meskipun panas laten kristalisasi dibutuhkan. Sesungguhnya panas laten itu sangat penting bagi proses pembentukan kristal. Pengendalian oleh lapisan pembatas lebih efekti pada sistem beku seperti pada sistem metamorf, namun faktor sekitarnya cukup berperan. Gradien konsentrasi yang terjadi akibat pengendalian pembentukan dan pemindahan komponen ke dan dari sekitarnya untuk kristalisasi tidak bisa mengimbangi atau adanya penolakan di lapisan pembatas, olehnya proses pembentukan terlambat. Apabila terjadi adveksi cairan akan cenderung merusak gradien sehingga kecepatan pembentukan terhambat. Halmana lapisan pembatas sebagai pengendali proses pembentukan dan komponen pembentukan kristal serta gerakan dari sekitarnya relatif kurang, maka keadaan seperti ini tidak dipengaruhi oleh pemindahan cairan. Lapisan Pembatas Sebagai Pengendali Pembentukan Kecepatan pengendalian oleh lapisan pembatas sangat tergantung keberadaan atom yang melekat dan terlepas dari ~ 129 ~ kristal. Kecepatan pengambilan (ra) dinyatakan dalam persamaan berikut: ra = ν exp(−ΔG*/RT), dimana v adalah atom yang bergerak, sedang ΔG* adalah energi aktivasi , Persamaan ini sama dengan persamaan pada kecepatan pemisahan atom (rd) yaitu rd = ν exp(−[ΔG′ + ΔG*]/RT), Dimana ΔG′ adalah kekuatan pendorong termodinamika. Pada tingkat pembentukan, Y, adalah (ra - rd) kali ketebalan lapisan ( σ0), dan atom yang ada permukaan berhasil dalam pengikatannya (f) sehingga dapat dijabarkan dalam persamaan berikut: Y = σ0 fν exp(−ΔG*/RT)[1 − exp(−ΔG′/RT)]. (6.10) Persamaan diatas memperlihatkan kecepatan nukleasi sangat variatif dibawah kondisi dingin, halmana jika ΔG′ adalah nol maka kondisi pendingin nol juga, tetapi kalau sistem ada pada tataran kesetimbangan suhu maka pembentukan akan naik sebab ΔG′ naik. Namun demikian pada saat pendingin derajatnya membesar, pembentukan mulai menurun sebab ΔG′ mulai kelihatan, hal itu menunjukan atom mulai berpindah sehingga viskositas (kekentalan) cairan makin bertambah. Oleh karenanya pendingin pada tingkat pertama mulai naik sampai mencapai maksimum, yang akhirnya akan turun karena kecepatan nukleasi sudah tidak ada. Para ahli kimia menyadari bahwa setiap mekanisme pembentukan di kendalikan oleh lapisan pembatas , seperti terlukis pada huruf f didalam persamaan 6.10 diatas. Karena atom dapat diambil kapan saja maka lapisan pembatas bisa tentukan keberlanjutan pengikatannya itu. Jika nilai f=1 pada semua pendingin mengakibatkan pembentukan relatif cepat. Dalam model lapisan tersebar (layer-spreading) di lapisan ~ 130 ~ pembatas adalah datar, kecuali pada tahap-tahap pengambilan satu atom di tempat tertentu. Contoh ilustrasinya seperti gamabr berikut (gambar 6.5) berikut: Gambar 6.5. Mekanisme Pembentukan Kristal pada model Lapisan Datar Sumber: Chester (1990). Keterangan: (a) adalah nukleasi di permukaan kristal, dimana satu atom ada dibagian ujung, sedang (b) adalah kedudukan atom dislokasi dan akan menempel pada bagian lain struktur kristal. Jadi f < 1 memperlihatkan disuatu lapisan tebal tersebar satu atom secara lateral dan satu atom lagi bertambah di bagian ujung dari lapisan pembatas. Halmana atom yang berada di bagian ujung lapisan pembatas akan membentuk spiral. Suatu percobaan yang dilakukan oleh Kirkpatrick dkk, (1976) mereka mengamati kerja perkembangan benih kristal yang berada pada variasi pendingin, yang diukur adalah kecepatan pemindahan atom pada bagian luar lapisan pembatas. Alhasil percobaannya menunjukan lapisan pembatas sebagai pengendali pembentukan agak sulit untuk memecahkan atom yang ada di luar, karena tidak memiliki △G dan ΔG′ sebagiamana yang terlukis pada persamaan 6.10. Teori Stokes – Einstein pada saat terjadi kekentalan (η) secara eksponensial memungkinkan terjadi pengantian kedudukan atom sebagaimana tersirat pada persamaan 6.10. ~ 131 ~ Walaupun secara matematis agak sulit terjadi karena reaksinya agak kompleks tapi dengan logika hal itu bisa terjadi. Suatu hal yang pasti pembentukan kristal dapat cepat terjadi dibawa kondisi pendingin dengan tingkat kekentalan yang rendah (△G dan ΔG′ adalah rendah). Dengan demikian dapat disimpulkan bahwa nilai Yη /T sama dengan nilai f yaitu mengukur kemampuan pengikatan atom pada kristal. Artinya Yη /T merupakan suatu mekanisme pembentukan kristal. Dimana pembentukan bisa terjadi bentuk garis lurus horisontal, pada dislokasi bisa terjadi garis melengkung yang positif, dan atau garis kurva positif pada perkembangannya. Suatu perhitungan yang dilakukan oleh Kirkpatrick (1974), dengan memplotkan data kekentalan pada cairan pendingin, yaitu suatu cairan dibawah kondisi pendingin (500C), η sama dengan 19 poise (g cm-1 detik-1). Sedang menggantikan nilai pembentukan adalah 9 × 10-3 cm detik –1 di dalam pendingin, maka di jabarkan pada persamaan berikut: Yη / △T = 3,4 × 10-3 g sec -2 deg -1 Sebagai contoh, sebuah kristal dari planet pluto dengan derajat kecil membentuk batuan vulkanik, dengan pendingin hanya 10C, berapa besar pembentukan di kristal bagi luar dalam satuan sentimeter ? . Jika dugaan Y pada △T = 10C, maka persamaannya adalah Yη / △T =6,6 X 10-5 T. atau dengan kata lain △T =10C, Yη / △T =6,6 X 10-5g sec-2 . Karena η = 15 poise pada 10C dibawa kondisi pendingin. Jadi kecepatan rata-rata dalam 106 sec selama 10 hari, perkembangan kristal yang terjadi adalah 1 cm. Hal yang harus diingat, batu pluto yang sesungguhnya memiliki suhu ±1390°C melebihi suhu magma sehingga nilai kekentalan rendah, oleh karenanya proses penggabungan dapat terjadi pada magma multikomponen. ~ 132 ~ Difusi sebagai Pengendali Pembentukan Kecepatan difusi sebagai pengendali pada pembentukan akan mengikuti hukum Ficks pertama dan kedua. Halmana kecepatan pembentukan dikendalikan cepatnya atom bergabung pada lapisan pembatas, dan itu tergantung cuaca disaat itu. Hakekatnya, kecepatan pembentukan terletak pada keadaan difusi dengan persamaan kesetimbangan masa, karena kecepatan atom mendekati ke lapisan pembatas lewat cara difusi harus sama dengan atom yang melekat pada lapisan pembatas. Secara umum persamaan kecepatan pembentukan (Y) didalam kondisi pengendalian difusi (penggabungan) adalah sebagai berikut: Y = k(D/t)1/2 (6.11) Dimana k adalah nilai kontanta dari konentrasi yang terlibat, sedang D adalah koefisien penggabungan (difusi yang lambat), dan t adalah waktu. Sesungguhnya pembentukan struktur atau termal yang dihasilkan oleh difusi dapat mempengaruhi pertumbuhan menyebabkan bentuk kristal rusak. Ketika permukaan kristal menjadi tidak stabil ,tonjolan mulai berkembang . Panas dan komponen ditolak selama prose pembentukan kristal sehingga dapat terjadi pengembangan tambahan struktur di sekitarnya. Hal ini dapat menghasilkan bentukan struktur kuat dan kristal dendritik. Meningkatnya pendingin, maka D akan menurun dan nilai Y akan naik sehingga perbandingan D/Y turun. Beberapa Aplikasi Kinetika Dalam sistem geokimia banyak terjadi interaksi kinetika berlangsung secara bersamaan . Dimana kecepatan reaksinya akan berjalan lambat dan proses itu dikenal sebagai ratelimiting step. Proses kinetika disini banyak factor yang ~ 133 ~ mempengaruhinya, seperti suhu lingkungan. Contohnya model kinetika yang terjadi pada proses kristalisasi seperti ilustrasi sebagai berikut: Aragonit ⇆ kalsit adalah sebagai rate-limiting step Semua kalsit dipermukaan bumi kondisi termodinamikanya adalah stabil, tapi argonit hanya stabil pada tekanan tinggi, tapi pada batuan metarmorf terkadang bisa terangkat jika tekanan tinggi. Apabila alur kinetika, reaksi balik dari aragonit ke kalsit maka proses pengakatannya dapat dikendalikan. Selama kalsit mengalamai diagenesis bisa mengantikan posisi aragonit di daerah luar kristal sehingga keberlanjutan ubahan (metamorf) aragonit mengambarkan kondisi yang tidak biasanya. Misalnya pada suhu rendah (200oC) memungkinkan penempatan kembali aragonit hanya beberapa hari walaupun reaksi yang berlangsung lebih lambat karena ketiadaan air. Apabila aragonit terlarutkan dan terjadi penguapan maka akan terbentuk benih baru kalsit. Sebaliknya dari aspek pengetahuan perminyakan bahwa ubahan aragonit dikonversi ke kalsit halitu menunjukan kalsit mengantikan kedudukan arogonit. Jadi dapat simpulkan bahwa batuan ubahan (metamorf) tidak memiliki pori-pori untuk masuknya cairan disaat ada proses pengangkatan. Suatu percobaan yang dilakukan oleh William Carlson dan John Rosenfeld (1981), mereka menyimpulkan bahwa nukleasi kalsit bukanlah “rate-limiting step “ (tahap membatasi kecepatan ), karena sebagian diganti aragonit biasanya dikelilingi oleh banyak butir kalsit kecil . Gambar berikut memberikan ilustrasi dari proses dimaksud. Dalam gambar 6.6. memperlihatkan bagaimana faktor penghambat pembentukan struktur kristal dibawa kondisi pendingin, bereaksi dengan kecepatan yang berbeda ~ 134 ~ sehingga pelbagai bentuk terjadi seperti bentuk memanjang, kerangka keras, berbentuk kotak dan berbentuk bola. Cairan Suhu Padatan Berat % An Gambar 6.6. Diagram T-Xan pada sistem albite-anorthite. Sumber: Chester dan Jickells (2012) Berangkat dari uraian diatas dapat disimpulkan, bahwa faktor kinetika sangat penting pada proses geologi sampai dengan suhu tinggi. Dalam setiap proses pemindahan atom, aspek energi keaktifan merupakan hal utama yang diperhatikan, karena energi aktif berkurang proses pembentukan akan berkurang. Kemudian pada proses pembentukan dengan kondisi pendinginan sering tidak mengikuti kaidah kesetimbangan kimia. Dalam keadaan sistem suhu tinggi maka ada tiga proses yang terjadi, yaitu: 1. Nukleasi merupakan pengendalian utama dalam proses pembentukan kristal, dan penggabungan sebagai respons dari energi potensial dari kimia. ~ 135 ~ Penggabungan volume selalu mengikuti hukum pertama dan kedua dari hukum Ficks. 2. Proses nukleasi bisa berlangsung pada konsidi homogen maupun heterogen, namun energi bebas dipermukaan sering dihambat sampai pada tingkat kritis. 3. Pembentukan/perkembangan kristal dikendalikan oleh laju reaksi (kinetika), biasanya lapisan pembatas menentukan kecepatan nukleasi, dan pada posisi dislokasi grafik perkembangannya bisa membuat grafik melengkung tidak regresi. ~ 136 ~ ⑦ KELARUTAN GAS DI PERAIRAN LAUT K andungan gas di perairan laut sebagian besar berasal dari atmosfer. Halmana di atmosfer sendiri terdapat campuran gas major, minor dan trace, kelimpahannya seperti terlihat pada tabel berikut: Tabel 7.1. Gas Non-variabel di Atmosfer Gas Konsentrasi Gas Konsentrasi (%) (ppm) N2 78,084 Ne 18,18 O2 20,946 He 5,24 CO2 0,033 Kr 1,14 Ar 0,934 Xe 0.087 H2 0,5 CH4 2,0 N2O 0,5 Sumber: Richards (1965) disitasi oleh Chester dan Jickells (2012) . Pemasukan gas dari udara ke perairan atau sebaliknya dari perairan naik ke udara (exchange across) akan melalui suatu lapisan di permukaan air yang disebut sebagai “interface”. Secara umum gas dari atmosfer ditransfer ke dalam perairan laut biasanya akan melalui proses mekanik ( fisikal), seperti pengadukan, gerakan angin, ombak dan sebagainya. Beberapa gas konservatif memang sudah ada di dalam perairan laut, tapi banyak juga gas masuk melalui proses biologi (seperti proses fotosintesis pada hayati laut) dan kimiawi (seperti aktifitas vulkanik gunung berapi di dasar ~ 137 ~ laut). Jumlah kelarutan gas di perairan laut merupakan suatu hal penting, dari sudut pandang geokimia, karena proses yang terjadi merupakan siklus biogeokimia laut. Secara global dapat dikatakan ada dua gas yang sangat penting dalam proses pemindahan yaitu oksigen (O2) dan karbon dioksida (CO2), dan kedua gas tersebut mendapat perhatian dalam pembahasan bagian ini. Proses kelarutan gas di laut dapat dikatakan sangat mudah mekanismenya bisa melalui difusi langsung maupun melalui mekanik, misalnya gas-gas konvensional seperti oksigen, nitrogen dan argon. Kalau zat oksigen bersifat difusi langsung, zat itu mudah bersenyawa dengan hydrogen, atau dapat pula merupakan hasil proses fotosintesis. Dimana bantuan sinar matahari dengan sinar ultra akan merangsang kerja butir hijau untuk memproduksi glukosa dan oksigen. Demikian pula zat nitrogen bisa langsung oleh tumbuhan untuk kepentingan tumbuh, sedang gas argon pada umumnya melalui penyerapan dengan beberapa unsur yang ada di kolom air. Hakekatnya untuk menghitung tingkat kelarutan gas, ada pelbagai bentuk persamaan yang dikemukakan oleh para ilmuan, namun harus diingat bahwa kelarutan gas tersebut sangat dipengaruhi oleh temperatur (suhu) dan salinitas. Menurut Weiss (1970) berbagai persamaan menghitung kelarutan gas di perairan laut yang bersumber dari udara basa, jumlah kelarutannya sangat tergantung pada faktor suhu dan salinitas. Halitu dapat di jabarkan sebagai berikut: C = A1 + A2(100/T)+ A3 (T/100)+ A4(T/100)+ S‰ [B1+B2(T/100)+B3(T/100)2] (7.1) Dimana C adalah kelarutan gas di perairan laut bersumber dari udara bertekanan 1 atmosfer, A dan B berisikan jumlah setiap gas dan kecepatan kelarutannnya, sedang T adalah suhu absolut dan S (‰) adalah salinitas. ~ 138 ~ Data hasil hitungan dari rumus 7.1 disajikan pada tabel 7.1 berikut ini, yang memperlihatkan kelarutan oksigen dalam satuan µmol dalam kg-1 pada pelbagai (variasi) suhu dan salinitas. Dalam table yamg di kemukakan oleh Kester (1975) menunjukan bahwa semakin bertambah nilai salinitas daya kelarutan oksigen makin menurun. Demikian juga dengan suhu, makin naik suhu daya kelarutan oksigen makin kecil. Sebelum membahas lebih lanjut bagaimana mekanisme difusi gas ke laut, marilah kita lihat faktor-faktor sebagai pengendali pada pertukaran gas di samudera dan atmosfer. Besaran kelarutan gas di perairan laut merupakan faktor kontrol penting bagi pengikatan kimia di dalam samudera. Hakekatnya partisi gas dari atmosfer ke perairan laut merupakan fungsi dari suhu, salinitas dan tekanan. Suatu hal yang menarik adalah bagaimana pengaruh tekanan terhadap percampuran gas, misalnya di atmosfer. Halmana tekanan gas yang terjadi pada suatu volume campuran merupakan bagian dari tekanan dari setiap gas (individu gas). Konsep ini juga berlaku pada kelarutan molekul gas di dalam perairan. Untuk itu hukum Henry menjabarkan hubungan antara tekanan gas di dalam larutan (PG) dan konsentrasinya (CG), yakni: P G = KG C G (7.2) Dimana KG adalah konstanta hukum Henry, merupakan kecepatan transfer proporsi gas dari atmosfer ke tekanan dari kedua tempat, yaitu: atmosfer (p) dan di laut (P), halmana tekanan parsial di kedua tempat (udara dan laut) diasumsi ada dalam kesetimbangan [ p =P]. Biasanya pemindahan gas, cairan dan padat dari udara ke air atau sebaliknya, selalu melalui suatu lapisan ”interface” (sebagimana uraian diatas), jika perpindahan yang terjadi hanya beberapa puluh μm cenderung terakumulasi di lapisan ”interface” tersebut. ~ 139 ~ Tabel 7.2. Kelarutan Oksigen di Perairan Laut (µ mol Kg-1) Salinitas ‰ Sumber: Kester (1975) disitasi oleh Chester dan Jickells (2012) ~ 140 ~ Gas-gas dipindahkan ke perairan melalui ”interface” adalah suatu difusi molekul. Prosesnya dua arah meskipun terjadi kejenuhan bila konsentrasi gas dalam air dalam keadaan kesetimbangan dengan konsentrasi gas di atmosfir. Ketebalan lapisan batas tidak konstan, yaitu akan berkurang dengan meningkatnya turbulensi dalam air sehingga pertukaran gas terjadi secara cepat pada saat badai (terjadi agitasi) daripada cuaca tenang. Daya larut gas diperairan sangat tergantung pada suhu, yaitu proses kelarutan akan lebih baik di air dingin (suhu rendah) daripada di air hangat. Jika temperatur air meningkat dalam kondisi kesetimbangan akan diperoleh net fluks gas dari laut ke udara. Kelarutan gas dalam air juga akan meningkat dengan kenaikan tekanan, kelarutan bervariasi terbalik dengan salinitas, semakin tinggi salinitas semakin kurang kelarutannya. Persamaan kecepatan pertukaran gas, F, yaitu gas yang melalui batas udara air adalah: F = K(T)w∆C (7.3) K, adalah konstanta kecepatan perpindahan, yaitu laju saat perpindahan terjadi. ∆C, adalah perbedaan konsentrasi yang menyebabkan terjadi fluks gas melalui ”interface”. Biasanya K dalam Cm/jam-1, sedang C dalam ml/L-1 dan F dalam ml.Cm-2 yaitu unit volume kali unit luas dalam unit waktu. Persamaan reaksi diatas berjalan sedemikian rupa sehingga K konstan (K dikenal sebagai koefisien pertukaran). Halmana ∆C adalah perbedaan konsentrasi yang dikendalikan oleh “fluks” dan konstanta proposional. Dalam keadaan nilai ~ 141 ~ ∆C sama dengan nol saat itu terjadi jenuh tetapi pertukaran gas masih terjadi dan kedua arah reaksi adalah sama. K(T)w adalah keterikatan fluks dan perbedaan konsentrasi yang menggambarkan suatu kecepatan gerak (velositas) dan bisa juga sebagai koefisien pemindahan gas (kecepatan transfer atau kecepatan seher/piston). Untuk kondisi normal, harga K(T)w berkisar antara beberapa sentimeter sampai beberapa puluh sentimeter per jam dan bertambah besarnya dengan kecepatan angin. Sebagai perbedaan konsentrasi (∆C) persamaannya adalah sebagai berikut: ∆C = CaH-1 – Cw (7.4) Dimana Ca dan Cw adalah konsentrasi didalam udara dan di perairan, sedang H adalah nilai kontanta hukum Henry (melukiskan kesetimbangan antara konsentrasi gas di udara dengan konsentrasi gas bentuk nir-ion di perairan). Untuk total kecepatan transfer (pemindahan) gas di rumuskan sebagai berikut: 1/ K(T)w = 1/αkw + 1/Hka (7.5) Dimana ka dan kw adalah kecepatan transfer dari gas yang tidak dapat bereaksi di dalam udara dan di perairan. Sedang α adalah faktor reaksi kimia gas yang ditransfer ke perairan. Kemudian H adalah konstanta hukum Henry sebagai terlukis pada rumus 7.4. Menurut pendapat Liss (1983) pengukuran timbal-balik kecepatan transfer gas (udaraperairan) dengan adanya resistansi pertukaran gas adalah sangat mudah. Halmana persamaan 7.5 telah mengambarkan bagaimana resistensi pertukaran gas yaitu 1/ K(T)w = R(T)w, 1/αkw = rw dan 1/Hka = ra, jadi persamaannya adalah: R(T)w = rw + ra ~ 142 ~ (7.6) Untuk itu sebagai kontrol resitensinya ada pada nilai rw dan ra dengan demikian disimpulkan ada dua kelompok gas dalam proses pertukarannya, yakni: 1. Gas dalam keadaan ra > rw memperlihatkan gas umumnya memiliki nilai H rendah (kelarutan di air tinggi), artinya partisi gas lebih dominan masuk ke perairan. Gas-gas yang masuk kedalam kelompok ini seperti SO2, NH3 dan HCl. 2. Gas dalam keadaan rw > ra memperlihatkan rw resistensi dominan pada transfer. Jadi umumnya gas memiliki nilai H tinggi (kelarutan di air rendah), dalam kelompok ini termasuk O2, CO2, CO, CH3, CH3I, MeI, Me2S dan gas-gas yang lemah. Hakekatnya gas pada kelompok ini umumnya gasgas yang penting pada proses siklus geokimia. Pertukaran atau transfer gas sebagaimana yang diuraikan diatas melalui “interface” proses pertukaran gas sangat tergantung pada: a. Perbedaan konsentrasi antara yang ada di udara dan di air yang akan melewati “interface” yaitu setiap aliran (fluks) dikendalikan oleh setiap gradien konsentrasi ( koefisien difusi molekul); dan b. Koefisien transfer (kecepatan gerak putaran/piston). Pertukaran gas tergantung pada kecepatan angin, suhu, dan daya kelarutan, kecepatan difusi dan reaksi kimia setiap gas. Dalam tabel 7.2 disajikan kecepatan difusi dan kelarutan gas di perairan laut pada suhu berbeda. ~ 143 ~ Tabel 7.3. Daya Larut dan difusi beberapa Gas di Laut O0C 240C Gas Daya Larut Daya Larut Koefisien difusi Koefisien difusi 3 -1 -5 2 -1 (Cm L ) (x 10 Cm s ) (Cm3 L-1) (x 10-5Cm2s-1) He 7,8 2,0 7,4 4,0 Ne 10,1 1,4 8,6 2,8 N2 18,3 1,1 11,8 2,1 O2 38,7 1,2 23,7 2,3 Ar 42,1 0,8 26,0 1,5 Kr 85,6 0,7 46,2 1,4 Xe 192 0,7 99 1,4 Rn 406 0,7 186 1,4 CO2 1437 1,0 666 1,9 N2O 1071 1,0 476 2,0 Sumber: Broecker dan Peng (1982) Gas-gas yang ada di udara difusi ke dalam air laut terbagi dalam dua kategori yaitu: 1. Kelarutan gas dengan reaksi kimia yang rendah, seperti: N2, O2, Ar dan gas mulia lain. 2. Kelarutan gas dengan reaksi yang tinggi, seperti : SO2, NO2 dan NH3. Tiga perempat massa gas di atmosfer berada di bawah 10 km dan tidak menunjukan variasi dalam proporsi unsurunsur utamanya, yaitu nitrogen (77%) oksigen (21%) dan argon (1%) dan gas-gas minor (1%), sedang gas rumah kaca seperti CO2 secara normal hanya 0,035% dari total gas yang ada di atmosfer. Disamping itu terdapat juga gas-gas yang minor (trace) seperti hydrogen sulfida (H2S), Amonia dan methan. Konsentrasi gas-gas di atmosfer bergantung pada volumenya dan asupan gas dari industri dan aktifitas manusia yang ada di bumi. ~ 144 ~ Meskipun karbon dioksida merupakan gas paling mudah larut diantara gas utama, konsentrasinya di dalam air laut sangat kecil. Mengapa? Karena gas karbon dioksida cepat bereaksi dengan air (H2O) membentuk senyawa bikarbonat dan karbonat. Kedua senyawa itu berperan sebagai penyangga keasaman (pH buffer), model reaksinya adalah sebagai berikut: CO2 (gas) + H2O ↔ H2CO3 ↔ H+ +HCO3 (7.7) Grafik di bawah ini memperlihatkan kedudukan gas-gas utama di atmosfer. 1.0 0.1 0.01 0.001 0.0001 N2 O2 Ar CO2 Gambar 7.1 Proporsi Volume dari 4 Gas di atmosfer. (Sumber data The Open University, 1996) Keterangan: Bersama-sama ke empat gas tersebut berjumlah 99% Sisanya terbentuk dari gas-gas minor. ~ 145 ~ Skala vertikal pada gambar diatas memperlihatkan tekanan parsial yang identik dengan komposisi persentase didasarkan pada volume. Sebagai contoh pada gas Oksigen dengan komposisi 21% akan menyebabkan tekanan parsial sebesar 0,21 atm. Demikian pula gas nitrogen dengan komposisi sebesar 77% kedudukan tekanan adalah 0,77 atm. Keempat gas utama ini memegang peran dalam sirkulasi udara di atmosfer sedang gas-gas minor atau trace biasanya volumenya akan bertambah jika adanya aktifitas manusia termasuk industri yang memproduksi gas-gas tersebut. Disamping gas-gas utama itu, terdapat pula gas-gas tambahan sebagai asupan dari industri seperti SO2 , Kloroflorokarbon (CFC), Poliklorin bipenil (PCB). Gas-gas tambahan ini merupakan polutan di atmosfer. Bahkan gas CFC dan CO2 merupakan gas rumah kaca yang mempengaruhi pemanasan global. Gas-gas tersebut berpotensi merusak lapisan oxon (O3) sehingga mengakibatkan penetrasi sinar ultra violet ke permukaan bumi makin bertambah, akhirnya berakibat fatal terjadinya pencarian es dan salju di daerahdaerah kutub. Penambahan gas-gas rumah kaca ini merupakan pembicaraan serius di dunia internasional dan telah menjadi kekuatiran manusia. Sebab akan meningkatkan jumlah volume air di laut akibat es yang ada di daerah kutub akan mencair sehingga akhirnya dapat menegelamkan pulau-pulau kecil dan merusakan garis pantai. Disamping itu, adanya gas-gas rumah kaca terjadilah perubahan iklim yang ekstrim, seperti musim panas yang terlalu panjang mengakibatkan kekeringan, dan jika musim hujan menyebabkan banjir yang sulit dikendalikan. ~ 146 ~ 100 10.0 1.0 0.1 N2 2 O2 Ar CO2 (ml/L-1 pada 240C) Gambar 7.2. Kesetimbangan Konsentrasi 4 Gas di Laut Pada suhu 24 derajat Celcius. (Sumber The Open University, 1996). Beberapa hal yang mengontrol pertukaran udara-laut CO2 adalah solubility pump, biological pump dan physical pump. Solubility pump adalah kemampuan memompa gas karbon dioksida merupakan fungsi dari suhu perairan, DIC (dissolved inorganic carbon), TA (total alkalinitas) dan angin (piston velocity). Aliran udara itu sendiri ditentukan oleh gradien tekanan parsial CO2 (pCO2). Jika pCO2 di atmosfer ~ 147 ~ lebih tinggi dari permukaan laut, maka laut berperan sebagai penyerap (atau penerima), namun sebaliknya jika pCO2 di atmosfer lebih rendah maka laut berperan sebagai pelepas. Perairan tropis yang memiliki suhu permukaan laut yang relatif tinggi cenderung menurunkan daya larut gas sehingga pCO2 di permukaan laut tinggi. Biological pump adalah besaran produksi karbon dioksida di perairan yang dihasilkan oleh aktifitas biologis seperti adanya foto sintesis alga makro dan mikro, biota perairan yang mati dan tenggelam yang akhirnya terjadi peluruhan di dasar perairan. Dimana partikel organik karbon yang dihasilkan itu (setelah terjadi mortalitas dan dekomposisi) akan di transfer ke dasar perairan yang tidak bisa kembali ke permukaan. Dengan demikian, biological pump efektif terjadi di perairan dalam setelah melewati lapisan termoklin. Perairan dangkal ataupun lapisan yang masih bias bercampur (mix-layer) masih memungkinkan terjadi proses remineralisasi sehingga gas karbon diaokside itu bisa dilepaskan kembali ke permukaan. Sintesis Joint Global Ocean Flux Study (JGOFS) di AS telah melaporkan bahwa dari 1000 unit karbon yang diserap di permukaan laut, maka hanya 1 unit yang berhasil tenggelam ke perairan dalam dan terkubur pada kedalaman 1000 meter atau lebih. Physical pump adalah proses penenggelaman karbon dioksida diperairan dilakukan secara fisikal, misalnya CO2 yang di dasar perairan akan naik ke permukaan oleh gerakan “upwelling” atau sebaliknya oleh gerakan “downwelling”. Pemindahan gas dari udara ke perairan laut maupun sebaliknya akan melalui suatu lapisan dipermukaan air. Secara teoritis jumlah pemindahan gas tergantung pada kecepatan transfer gas dan lajunya perubahan gas dalam bentuk gas lain. Tetapi proses ini berlangsung pada daerah “interface”, secara teori ada 3 model pertukaran gas pada wilayah “interface”, yakni: ~ 148 ~ 1. Model lapisan yang stagnan (Stagnant film model), halmana proses transfer akan dikendalikan oleh difusi molekul gas itu. 2. Model pembaharuan permukaan (Surface renewal model), yaitu dalam lapisan stagnan, pada saat-saat tertentu terjadi gelembung di permukaan air dan secara bertahap terjadi transport gas, dan kecepatannya tergantung pada lapisan dimana akan diletakan gas itu. 3. Model batas lapisan (boundary-layer model), memang konsep teori ini relatif lebih kompleks (ribet) dipermukaan, biasanya ada gaya panas menjadikan pertukaran gas. Secara ilustrasi digambarkan pada gambar 7.3 berikut ini. αp Cs Batas Lapisan stagnan Z K e d a l a m a n Fluks = D Cs – αp Z Lapisan tercampur Kecepatan perputaran = D/Z Gambar 7.3. Model Batas Lapisan Stagnan (Sumber: Broecker dan Peng, 1974) Ilustrasi diatas memperlihatkan model lapisan stagnan (stagnant film model/SFM), dimana kecepatan transfer molekul gas antara udara ke perairan laut dikontrol oleh ketebalan batas lapisan stagnan, dan apabila telah melewati lapisan itu maka air dibawahnya diasumsikan telah terjadi percampuran. D adalah difusi molekul gas, Z adalah ketebalan lapisan sedang Cs adalah konsentrasi gas dibawah lapisan, ~ 149 ~ sedangkan α adalah daya kelarutan gas dan p adalah tekanan gas di udara. Hakekatnya difusi gas yang terjadi diperairan laut sangat tergantung pada beberapa faktor yakni: ➊. Kecepatan difusi gas ke perairan laut dipengaruhi oleh suhu, seperti terlihat pada tabel 7.2, halmana bertambah suhu daya difusi makin berkurang. ➋. Ketebalan lapisan. Apabila ketebalan lapisan bertambah konsekuensi waktu difusi gas akan bertambah juga. Intinya rerata kecepatan pemindahan gas ke perairan laut tergantung pada ketebalan lapisan dan agitasi air laut oleh gerakan angin dan kecepatan angin dan derajat ketebalan lapisan. ➌. Perbedaan konsentrasi antara di udara dan di perairan laut. Perbedaan besar, artinya gradien konsentrasi besar dan difusi molekul transfer sangat cepat. Oksigen Kelarutan gas di perairan alamiah termasuk laut nampaknya gas oksigen merupakan bagian yang penting dan signifikan perannnya bagi ekosistem perairan. Kebanyakan perubahan konsentrasi oksigen di perairan diakibatkan adanya bahan cemar berbentuk senyawa organik. Halmana proses penyerapan bahan organik dilakukan oleh bakteri yaitu dalam rangka peluruhan bahan organik ini dibutuhkan suatu oksidasi dengan memanfaatkan oksigen yang tersedia di perairan. Sisi lain kandungan oksigen berlimpa disebabkan adanya hasil proses fotosintesis yang dilakukan oleh fitoplankton dan atau alga hijau, disamping itu pula oleh adanya difusi gas dari udara melalui “interface”. Oleh karena itu kelarutan oksigen (dissolved oxygen) sering dijadikan indikator dari adanya pencemaran di lingkungan. Satuan yang digunakan untuk mengukur adanya perubahan oksigen di perairan para ahli ~ 150 ~ menggunakan istilah “ Biochemical Oxygen Demand” dan “Chemical Oxygen Demand” Selain adanya difusi kandungan oksigen dari udara, diperairan dapat juga asupan oksigen dari hasil kerja fotosintesis dari mikroorganisme seperti fitoplankton dan juga oleh rumput laut. Daya kelarutan oksigen di perairan tergantung juga pada kadar klorida di dalam air, tabel 7.3 berikut ini memperlihatkan daya kelarutan oksigen pada pelbagai kandungan klorida di perairan. Mengapa daya larut oksigen di perairan tawar dan perairan laut berbeda ?. Hal itu di sebabkan adanya kandungan Cl di laut cukup tinggi, sehingga proses kelarutan oksigen menjadi terhalang, untuk itu tabel 7.3 memperlihatkan hubungan antar klorida dengan daya larut gas oksigen Permukaan air laut kandungan oksigen dapat dikatakan lewat jenuh, hal ini terjadi karena pembebasan oksigen pada saat terjadinya proses fotosintesis. Biasanya oksigen yang terikat dengan massa air diperlihatkan adanya gelembung udara (bulb). Gelembung-gelembung udara yang terbentuk di puncak gelombang yang didorong ke bawah ke dalam kolom air, dan sebagian gas yang ada digerakkan ke dalam larutan oleh pertambahan tekanan hidrostatik. Konsentrasi oksigen terlarut dalam keadaan jenuh bervariasi tergantung dari suhu dan tekanan atmosfer. Pada suhu 200C dengan tekanan satu atmosfer konsentrasi oksigen terlarut dalam keadaan jenuh adalah 9,2 ppm, sedang pada suhu 500C dengan tekanan atmosfer yang sama tingkat kejenuhannya hanya 5,6 ppm. Semakin tinggi suhu air, semakin rendah tingkat kejenuhan Kelarutan oksigen di perairan sangat berperan penting terhadap proses korosi (pengkaratan) pipa besi di dalam air. Kecepatan proses korosi besi yang ada di laut sangat tergantung dari jumlah konsentrasi oksigennya, makin banyak kandungan oksigen proses korosinisasi akan makin cepat. ~ 151 ~ Tabel 7.4. Daya kelarutan Oksigen di perairan dengan pelbagai konsentrasi Klorida. Konsentrasi Klorida (Cl) di air (mg/l) Perbedaan/100mg Klorida 0 5 10 15 20 0 Temp.( C) Kelarutan Oksigen (mg/l) 0 14,6 13,8 13,0 12,1 11,3 0,017 1 14,2 13,4 12,6 11,8 11,0 0,016 2 13,8 13,1 12,3 11,5 10,8 0,015 3 13,5 12,7 12,0 11,2 10,5 0,015 4 13,1 12,4 11,7 11,0 10,3 0,014 5 12,8 12,1 11,4 10,7 10,0 0,014 6 12,5 11,8 11,1 10,5 9,8 0,014 7 12,2 11,5 10,9 10,2 9,6 0,013 8 11,9 11,2 10,6 10,0 9,4 0,013 9 11,6 11,0 10,4 9,8 9,2 0,012 10 11,3 10,7 10,1 9,6 9,0 0,012 11 11,1 10,5 9,9 9,4 8,8 0,011 12 10,8 10,3 9,7 9,2 8,6 0,011 13 10,6 10,1 9,5 9,0 8,5 0,011 14 10,4 9,9 9,3 8,8 8,3 0,010 15 10,2 9,7 9,1 8,6 8,1 0,010 ~ 152 ~ Lanjutan Tabel 7.4 16 10,0 17 9,7 18 9,5 19 9,4 20 9,2 21 9,0 22 8,8 23 8,7 24 8,5 25 8,4 26 8,2 27 8,1 28 7,9 29 7,8 30 7,6 31 7,5 32 7,4 33 7,3 34 7,2 9,5 9,3 9,1 8,9 8,7 8,6 8,4 8,3 8,1 8,0 7,8 7,7 7,5 7,4 7,3 9,0 8,8 8,6 8,5 8,3 8,1 8,0 7,9 7,7 7,6 7,4 7,3 7,1 7,0 6,9 8,5 8,3 8,2 8,0 7,9 7,7 7,6 7,4 7,3 7,2 7,0 6,9 6,8 6,6 6,5 ` ~ 153 ~ 8,0 7,8 7,7 7,6 7,4 7,3 7,1 7,0 6,9 6,7 6,6 6,5 6,4 6,3 6,1 0,010 0,010 0,009 0,009 0,009 0,009 0,008 0,008 0,088 0,088 0,008 0,008 0,008 0,008 0,008 Lanjutan Tabel. 7.4 Konsentrasi Klorida (Cl) di air (mg/l) 0 5 10 15 0 Temp. ( C) Kelarutan Oksigen (mg/l) 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 20 Perbedaan/100mg Klorida 7,1 7,0 6,9 6,8 6,7 6,6 6,5 6,4 6,3 6,2 6,1 6,0 5,9 5,8 5,7 5,6 Ket.: Tekanan pada 760 mm Hg. Menghitung O2 dengan rumus= S’=S(P-p)/(760-p). Dimana S larut pada tekanan 760 mm, dan p lebih dari 1000 meter, suhu berada dibawah dari 250C. ~ 154 ~ Kelarutan gas-gas umumnya berkurang dengan bertambahnya temperature dan salinitas, tetapi dapat meningkat dengan pertambahan tekanan. Distribusi gas-gas pada daerah lautan yang lebih dalam terjadi karena arus dan turbulensi dibandingkan karena difusi molekuler. Distribusi ke bawah biasanya perlahan dan membutuhkan waktu bertahun-tahun. Pada kedalaman yang jauh, oksigen secara kontinu dikonsumsi lewat respirasi hewan dan penguraian tumbuhan oleh mikroba detritus. Akan tetapi oksigen tidak hilang karena pencampuran ke bawah dan difusi oksigen terlarut dari permukaan, juga adanya produk dari aktifitas fotosinsis. Lapisan minimum oksigen terbentuk bila penyerapan oksigen terlarut terjadi maksimum relative terhadap laju pengurangannya dan umumnya itu terjadi diantara kedalaman 500 – 1000 meter. Di beberapa daerah seperti di Samudera Hindia bagian utara dan Samudera Pasifik Selatan, airnya mengandung sedikit oksigen dan dibagian-bagian tertentu bisa terjadi kekosongan oksigen (anoxic), tetapi di kedalaman yang jauh makin jauh ke arah laut lepas tingkat oksigen akan naik lagi. Hal ini terjadi karena masukan air yang dingin dengan membawa oksigen yang banyak dari daerah kutub. Nitrogen Gas nitrogen sangat penting di perairan karena derivat gas ini merupakan pembentuk dasar senyawa organik, seperti penyusun komposisi protein. Gas ini dapat dimanfaatkan sebagai nutrisi bagi kelancaran proses sintesis oleh tumbuhan air dan fitoplankton,. Tetapi sering derivat nitrogen dapat juga merupakan bahan cemar (polutan) di lingkungan, seperti ammonia (NH3). Nitrogen yang ada di udara ada dalam bentuk senyawa N2 maupun senyawa yang lebih kompleks, beberapa referensi dari para ahli lingkungan senyawa ini di atmosfir ada sebanyak 78% dan yang lainnya ada di kulit bumi dan di dalam perairan. Atmosfer kita kandungan nitrogen ada sekitar 80% sedang ~ 155 ~ oksigen kurang lebih 20%. Nitrogen sebagai gas tidak merupakan signifikansi bagi indikator kualitas perairan (water quality), tetapi dapat berperan nyata bila nitrogen berubah menjadi nitrat. Halmana senyawa itu merupakan elemen esensial bagi penyuburan perairan. Menurut konstanta hukum Henry, kelarutan gas nitrogen di dalam air bisa mencapai 15,1 mg/l pada suhu 20oC. Bila nitrogen sebagai gas N2 daya reaksi kelarutan di perairan bersifat rendah, tetapi apabila berbentuk gas NO2 dan NH3 reaktivitasnya termasuk tinggi atau cepat. Gas nitrogen terlarut (N2) jarang digunakan dalam proses-proses biologi karena hanya beberapa fitoplankton ( terutama Cyanophaecea atau alga hijau-biru) mampu menggunakannya, yaitu mengubahnya menjadi senyawa nitrogen organik yang diperlukan bagi pertumbuhan. Sebagian besar nitrogen di lautan berbentuk nitrat (NO3) yang diperoleh dari penguraian bahan organik di daratan, senyawa ini terbentuk akibat dari bantuan nitrobakteri atau bakteri pengurai nitrogen. Nitrogen merupakan faktor pembatas yang utama di perairan laut terbuka. Akan tetapi apabila terjadi kondisi keterbatasan nitrogen yang ekstrim, mikro organisme sejenis Trichodesmium dapat memanfaatkan nitrogen terlarut di dalam perairan laut. Di perairan Samudera Pasifik dan Atlantik, organisme tersebut melakukan fiksasi nitrogen (nitrogen fixing) untuk meningkatkan produktifitas primer sehingga melampaui batas nitrat di perairan Pertukaran ini mengubah rasio karbon terhadap nitrogen, fosfat dan besi pada fitoplankton (lihat gambar 7.4). Kondisi ini juga memberikan sebuah mekanisme yang efisien untuk mengekspor karbon dan elemen-elemen yang menyertainya ke perairan laut dalam (deep sea). Adanya elemen fosfor, besi dan lainnya akan mampu mengndalikan kecepatan produktivitas primer di dalam air. Akan tetapi ~ 156 ~ penambahan nitrogen juga berpengaruh secara signifikan terhadap siklus biogeokimia secara lokal maupun regional. Karbon dioksida (CO2) Karbon dioksida masuk ke biosfer bisa melalui fotosintesis dari tumbuhan laut dan hasil penguraian karbon berasal dari sel tumbuhan dan hewan. Penguraian bahan organik dapat menurunkan kandungan oksigen di air, sebaliknya akan menaikan gas karbon dioksida di dalam kolum air. Gas-gas itu bisa ke luar ke atmosfer. Gas karbon dioksida di udara dapat berasal dari berbagai sumber antara lain, hasil pembakaran fosil dan buangan industri. Gas ini termasuk gas rumah kaca yang sering dibicarakan keberadaannya di udara, karena dapat mempengaruhi temperatur udara dan perubahan cuaca. Memang belum ada penelitian yang detil menghitung berapa besaran difusi karbon dioksida secara langsung ke air laut atau berapa jumlah gas per luas persegi serapan fitoplankton di laut. Namun demikian para ahli memprakirakan pelepasan dan penyerapan karbon dioksida di udara mencapai kesetimbangan pada masa pra-industri, emisi gas CO2 antropogenik meningkat secara drastis di atmosfir, tetapi laut memiliki kemampuan menyerap gas rumah kaca itu. Dugaan ahli sekitar 6 peta gram karbon per tahun (Pg C/Y) karbon dioksida di lepaskan ke atmosfir akibat pembakaran bahan fosil (1 peta gram= 1 gigaton= 1000 juta ton). Meningkatnya konsentrasi karbon dioksida di atmosfir mengakibatkan gradien tekanan parsial antara atmosfir dan laut mengalami perubahan. Kenaikan jumlah emisi gas rumahkaca ke atmosfer berdampak signifikan pada kehidupan manusia dan kehidupan di perairan laut, akibat perubahan cuaca (efek Elnino dan La nina). Data Global Carbon Project (GCP) tahun 2007 melaporkan bahwa dari total emisi karbon global ke atmosfer (9,1 Pg C per tahun, 1 Pg sama dengan 10 pangkat 15 gram atau 1 ~ 157 ~ milyar ton) maka 26% diserap oleh lautan global, 29% oleh daratan (hutan) dan sisanya terakumulasi di atmosfer (45%). Dalam hal ini telah terjadi peningkatan akumulasi CO2 di atmsofer, yaitu pada tahun 1960 berkisar 40% dan pada tahun 2008 meningkat 45%. Gambar 7.4. Diagrama CO2 dan pCO2 di Permukaan Laut Ketika karbon membutuhkan δ11Calkalin, δ13CKalsit, δ11N dan akibat pengaruh suhu di permukaan (Andersen Andersen dan Malahoff. 1977) Diagrama pada gambar 7.4. menunjukan bahwa karbon dioksida yang berada di udara dapat di serap oleh hayati laut (alga) dalam ikatan δ11Calkalin, δ13CKalsit kemudian dibantu oleh hara nitrogen. Disamping itu suhu permukaan laut berpengaruh pada tingkat penyerapan karbon dioksida di laut. ~ 158 ~ Udara yang kering dan normal, kandungan gas karbon dioksida hanya terdapat sejumlah 0,0314% dari total gas keseluruhan di udara. Karena konsentrasi yang sangat kecil, maka pada air murni (khusus air bebas alkalinitas) kandungannya sangat rendah walaupun gas itu memiliki sifat mudah larut kedalam air. Ironinya, karbon dioksida bebas yang tinggi di dalam air akan menghambat pernafasan biota perairan, bahkan dapat memberikan efek yang fatal, yaitu kematian. Oleh karenanya disarankan kandungan gas ini tidak boleh melebihi 25 ppm di dalam air. Hampir semua karbon dioksida dalam air laut menyatu dengan air sebagai asam karbonat dan produk disosiasi yang lain. Sesungguhnya prinsip dasar sistem karbon dioksida (CO2) di perairan laut adalah sebagai berikut: (a) CO2 saat pertukaran gas udara/ perairan “interface” keadaan di atmosfer ada dalam setimbang dengan di perairan laut, jadi CO2 (gas) ⇆ CO2 (terlarut) (7.8) (b) Pembentukan hidrat dari CO2 terlarut, yaitu CO2 + H2O ⇆ H2CO3 (7.9) (c) Asam karbonat berdisosiasi membentuk sebagai berikut: H2CO3 ⇆ HCO3¯ (ion bikarbonat) (7.10) HCO3¯ ⇆ H+ + CO32-(ion karbonat) (7.11) Kalau demikian sistem karbon dioksida di perairan maka total karbon inorganik (∑CO2) adalah: ∑CO2 = c CO2 + c H2CO3 + c HCO3¯ + c CO3¯ ~ 159 ~ (7.12) Kemampuan kelarutan gas ini mengikuti kaidah pada rumus 9.1 diatas. Sedang proses pembentukan sebagai bahan penyangga derajat keasaman di perairan (buffer capacity) telah di uraikan pada bab 6. Walaupun konsentrasi gas ini relatif kecil di atmosfir dibandingkan dengan gas-gas lainnya, tetapi laut mampu menyerap karbon dioksida sebesar ± 2,2 peta gram per tahun setara dengan emisi total karbon antropogenik. Kelarutan ini gas karbon dioksida dari kegiatan antropogenik sangat mempengaruhi pada reservoir karbon yang ada di laut. Gas karbon dioksida mudah larut di dalam air dingin dibandingkan dengan air hangat. Kelarutan gas meningkat terhadap tekanan. Tekanan parsial (pCO2) pada lapisan permukaan laut dan udara akan menentukan arah pertukaran gas. Apabila pCO2 rendah akan menyerap karbon dioksida di atmosfir. Sebaliknya apabila pCO2 tinggi akan melepaskan karbon dioksida ke atmosfir. Proses pertukaran ini juga ditentukan oleh kandungan karbon anorganik terlarut (Disolved inorganic carbon/ DIC) dan total alkalinitas. Bila DIC semakin tinggi pCO2 permukaan laut akan meningkat. Tetapi bila total alkalinitas semakin meningkat akan menyebabkan penurunan pCO2 permukaan laut. Pasokan nutrient dari daratan ( misalnya: sungai dan air run off) akan mempercepat aktivitas proses fotosintesis yang di barengi oleh menurunnya DIC. Namun demikian pasokan dari daratan juga membawa DIC dan total alkalinitas yang memiliki dampak berbeda terhadap pCO2 di perairan pesisir. Karbon dioksida di atmosfir (udara) dan ditransfer ke dalam perairan laut (lihat gambar 7.4) Alkalinitas total sangat penting dalam pembentukan fisikokimia air laut dan merupakan faktor kritis yang berperan terhadap proses kimia dan biologi di perairan laut. Burke dan Atkinson (1988) memberikan beberapa alasan mengapa? Alkalinitas merupakan faktor penting di perairan laut, yakni: ~ 160 ~ ① bahwa HCO3- dan CO32- adalah ion asam lemah yang merupakan major anion di perairan laut, dengan demikian memiliki kemampuan merubah alkinitas total (HCO3- → CO32- ), ② Adanya curah hujan menurunkan kadar kalsium karbonat dalam alkalinitas total, sehingga pengukuran alkalinitas total sama halnya dengan mengukur kalsium dan karbon dioksida yang ada dalam proses biogeokimia, ③ bahwa respirasi komunitas biologi dan netfotosintesis dapat merubah konsentrasi DIC, halmana DIC suatu sampel air dapat diterah dengan pengukuran pH dan alkalinitas total. Hakekatnya, alkalinitas merupakan suatu faktor dalam sistem karbon dioksida di perairan; seperti, terjadi perubahan nilai alkalinitas akan mempengaruhi kesetimbangan karbon dioksida di laut dan atmosfer serta kelarutan dan bentuk karbonat biogenik. Jadi dapat dikatakan alkalinitas adalah salah satu parameter yang digunakan untuk melihat siklus karbon global di laut. Seperti diuraikan di atas gas karbon dioksida di dalam air laut sangat kecil, di permukaan hanya terdapat sekitar 1 atom karbon dari 200 yang berbentuk molekul CO2 terlarut, tetapi di laut dalam bisa mencapai 3 atom dari 200 molekul yang terlarut. Perubahan konsentrasi yang terlarut di dalam air laut sangat di tentukan oleh aktivitas manusia (antropogenik), makin besar aktivitas manusia membuang gas karbon dioksida dan atau bahan organik maka peluang kelarutan gas di perairan laut akan makin besar. Kelarutan gas karbon dioksida di perairan laut dan tawar sangat berbeda, gas karbon dioksida di laut mudah terjadi pelarutan oleh karena adanya reaksi ikatan bikarbonat dan karbonat, tetapi di perairan tawar yang kandungan ~ 161 ~ salinitasnya sangat rendah, yaitu <5 ‰ peluang kelarutan kecil. Sebaliknya jika di dalam perairan terjadi perombakan bahan organik dan memproduksi gas karbon dioksida, di perairan tawar gas tersebut cepat terjadi penguapan ke udara, tetapi di perairan laut gas tersebut akan diikat oleh air membentuk ikatan karbonat dan bikarbonat . Lapisan Campuran Interface ATMOSFIR NUTRIEN Permukaan Laut CO2 CO2 NUTRIEN Anorganik terlarut Fitoplankton Kecil Bakteri Organik Terlarut Fitoplankton Besar Bakteri Zooplankton T Partikulat Organik THERMOHALINE Partikulat organik Organik terlarut Bakteri Remineralisasi Organik terlarut BENTHOS Gambar 7.5 Mekanisme Kelarutan CO2 di Air Laut dan difusi Dari atmosfir melalui interface. Sumber: Rompas dkk (2009) Gambar diatas memperlihatkan, bahwa gas karbon dioksida masuk ke laut bisa melalui difusi langsung gas tersebut kemudian bersenyawa dengan air membentuk ikatan karbonat (ikatan senyawa ini kekuatannya relatif kurang). Disamping itu bisa masuk melalui senyawa bahan organik dalam hal ini bakteri akan berperan meluruhkan bahan-bahan tersebut sehingga terbentuk gas karbon dioksida. Tetapi gas ~ 162 ~ ini tidak bebas terlepas ke udara karena di laut adanya senyawa penyangga keasaman yang disebut sebagai karbonat dan bikarbonat. Senyawa karbonat dan bikarbonat ini yang berperan penting menstabilkan reaksi keasaman di perairan laut, oleh karenanya di laut memiliki daya penyangga yang tinggi (buffer capacity), suatu indikasi yang dilihat, bahwa laut dalam keadaan normal kedudukan derajat keasaman (pH) ada di atas 7.3, berbeda dengan perairan tawar, dalam keadaan normal pH berada pada 6,4. Fitoplankton mengambil nutrien dan karbon dioksida melalui proses fotosintesis, dimana karbon dioksida yang diserap oleh butir hijau daun, kemudian ditopang oleh beberapa nutrien seperti nitrogen dan fosfat akan pmemproduksi glukosa, zat ini merupakan produksi energi pertama, oleh karenanya fitoplankton di sebut sebagai komponen produktivias pertama. Laju pengambilan nutrien disebut kinerja produktivitas primer, zooplankton memanfaatkan fitoplankton (primary productivity) kemudian bahan-bahan organik yang telah mati akan diurai (luruhkan) oleh mikroorganisme (bakteri) membentuk senyawa amoniak dan hidrogen sulfida. Bahan organik yang dihasilkan melalui jejaring makanan (food web) yang berada di bagian atas badan air laut (zona diatas garis termoklin) dimanfaatkan oleh biota perairan, bagian lainnya akan tenggelam ke dasar laut. Sebagian dari karbon ini kemudian mengalami proses mineralisasi (reminalisasi) menjadi karbon dioksida. Sebagian kecil lainnya terkubur dalam sedimen di dasar laut atau samudera. ~ 163 ~ Gambar 7.6. Perombakan Bahan Organik di Dasar Perairan Bahan organik yang tenggelam ke dasar lautan memiliki peluang remineralisasi, membentuk senyawa Hidrogen Sulfida (H2S), Nitrat, ferri dan ferro, mangan yang merupakan nutrien bagi fitoplankton. Semua senyawa-senyawa ini dapat naik ke permukaan apabila ada peristiwa upwelling (pengadukan ke atas), dan peluang pembentukan karbon dioksida relatif kecil. Adanya pengadukan ke atas akibat arus dan angin, senyawa dalam bentuk gas seperti hidrogen sulfida dan amoniak cepat menguap ke udara, tetapi bila terjadi gas karbon dioksida, gas ini cepat terikat dalam senyawa karbonat dan bikarbonat di dalam air laut. Oleh karenanya peluang pelepasan gas karbon dioksida ke udara dari air laut dapat dikatakan tidak ada, kalau pun ada peluang kecil sekali. Hampir semua kawasan lautan, ketersediaan nutrient berupa nitrat, fosfat dan silika sebagai pengendali aktifitas biologi, contohnya di Samudera Pasifik utara, sub artik (mintakat yang terletak diantara perbatasan lintang tengah ke arah kutub utara atau lintang 55o – 60o utara) dan katulistiwa, serta wilayah Samudera bagian selatan. Semua kawasan ~ 164 ~ memiliki karakteristik konsentrasi nutrien yang tinggi akan tetapi kandungan klorofilnya rendah. Sehingga semua perairan seperti itu diindikasikan kegiatan proses fotosintesis rendah. Keselurahan wilayah laut ± 30% masuk ke dalam kategori ”nutrien tinggi-klorofil rendah” (High nutrient-low cholophyll). Hal inilah yang membingungkan para ilmuan, perlu ada kajiankajian yang lebih mendalam, agar pertanyaan yang besar ini dapat terjawab secara ilmiah. Zat nitrat, fosfat dan silika merupakan zat hasil degradasi bahan organik dan anorganik. Seperti fosfat lebih banyak bersumber dari pebatuan ketimbang hasil uraian bahan organik, sebaliknya nitrat lebih banyak sebagai hasil penguraian bahan organik ketimbang dari pebatuan. Kalau zat silika merupakan hasil uraian bahan organik dan anorganik berimbang di perairan, artinya zat tersebut di perairan tertentu banyak disumbangkan oleh aktivitas vulkanik, tetapi di perairan tertentu merupakan hasil uraian biota perairan, seperti kerang-kerangan lebih dominan, atau ada di perairan tertentu konsentrasinya 50% disumbang oleh bahan organik dan sisanya berasal dari udara dan aktivitas vulkanik. Hidrogen Sulfida dan Methan Kelarutan gas hidrogen sulfida dan methan kandungnya sangat sedikit (trace) dan pelarutannya dapat melalui tanah di sepanjang pinggiran pantai ataupun melalui difusi dari atmosfer ke permukaan air. Gas-gas itu merupakan reduksi sulfat dan karbon dioksida. Walaupun gas H2S tergolong sebagai gas yang konsentrasi relatif kecil, tapi gas ini sangat berbahaya bagi kehidupan biota diperairan. Dalam jumlah sedikit bisa mematikan ikan atau menghambat pertumbuhan. Demikian juga gas methan, gas ini adalah hasil degradasi bahan organik dan bisa juga bersumber dari perut bumi. Kedua gas ini merupakan zat polutan yang berbahaya bagi kehidupan organisme perairan. ~ 165 ~ Bahan organik baik yang berasal dari kondisi alamiah maupun berasal dari antropogenik (limbah rumah tangga) akan terjadi peluruhan (terurai) oleh adanya mikroorganisme baik melalui tanah maupun di dalam air laut. Halmana mikroorganisme mengoksidasi bahan organik tersebut dengan memanfaatkan anion sulfat atau kelarutan karbon dioksida sebagai penerima elektron (electron acceptors), alhasilnya mereduksi sulfur sebagai H2S dan mereduksi karbon sebagai CH4. Kedua gas ini kurang menguntungkan bagi kualitas air, tetapi dibalik itu kedua gas tersebut merupakan indikator umum terhadap adanya pencemaran dari bahan organik. Kehadiran gas-gas ini di perairan laut akan memberikan efek toksik (racun) bagi organisme yang hidup di permukaan air, Walaupun demikian kedua gas tersebut dapat hilang jika adanya aerasi air atau turbulensi di perairan. ~ 166 ~ ⑧ SEDIMEN DI LAUT M aterial berupa padatan dan larutan yang masuk ke laut akan berakhir menjadi sedimen, prosesnya disebut sedimentasi. Dalam hal ini zat-zat atau material akan terlibat pada proses biologi maupun kimia yang terjadi selama material itu tenggelam kedalaman laut. Dengan demikian dapat didefinisikan sedimen laut sebagai akumulasi dari mineral-mineral dan pecahan-pecahan batuan yang bercampur dengan hancuran cangkang dan tulang dari organisme laut serta beberapa partikel lain yang terbentuk lewat proses kimia yang terjadi di laut. Sebelum mencapai dasar laut dan menjadi sedimen, zat tersebut melayang-layang di dalam laut. Setelah mencapai dasar lautpun , sedimen tidak diam tetapi sedimen akan terganggu ketika hewan laut dalam mencari makan. Sebagian sedimen mengalami erosi dan tersuspensi kembali oleh arus bawah sebelum kemudian jatuh kembali dan tertimbun. Terjadi reaksi kimia antara butir-butir mineral dan air laut sepanjang perjalannya ke dasar laut dan reaksi kimia tetap berlangsung pengendapannya. Ketika air laut terperangkap di antara butiran mineral reaksi kimia terjadi, apalagi proses oksidasi terjadi, seperti pada pebembentukan senyawa ferromangan dari zat besi. Untuk mengetahui bagaimana mekanisme pengendapan material itu, seyogianya perlu kita ketahui bagaimana tipologi dasar pantai serta pembentukan sedimen itu dalam konteks samudera secara menyeluruh. Tinjauan secara morfologi dasar laut (relief), sesungguhnya dasar laut dikategorikan ke dalam tiga topologi daerah, yaitu margin kontinen (continental margins), dasar lembah-samudera( ocean-basin floor) dan punggung dasar laut ~ 167 ~ (mid-ocean ridge). Betuk dan gambaran umum kawasan dasar laut dapat dilihat pada gambar 8. Daratan Punggung Dasar Samudera Pantai tipologi Gunung di dasar Laut Kontinen Margin Dasar lembah samudera Abisal Palung Gambar 8.1. Tipologi Dasar Samudera Kontinen margin atau pinggiran benua seperti terlihat pada gambar diatas, yaitu termasuk didalamnya landasan kontinen (continental shelf), lereng benua (continental slope) dan landasan berbukit (continental rise). Landasan kontinen adalah wilayah laut yang dangkal di sepanjang pantai dengan kedalaman kurang dari 200 meter, dengan kemiringan kira-kira 8,4% atau sekitar 0o7’ atau 2m/km. Landasan kontinen merupakan dasar laut dangkal di sepanjang pantai dan menjadi bagian dari daratan. Contohnya Landas kontinental benua Eropa barat sepanjang 250 km kearah barat. Dangkalan sahul yang merupakan bagian dari benua Australia dan Pulau Irian, Landas kontinen dari Siberia kearah laut Arktik sejauh 100 km, dan dangkalan Sunda yang merupakan bagian dari benua Asia yang terletak antara Pulau Kalimantan, Jawa, dan Sumatera. ~ 168 ~ Lereng benua merupakan kelanjutan dari landas kontinen dengan kemiringan antara 4% sampai 6%. Kedalaman lereng benua lebih dari 200 meter. Daerah ini meluas dari patahan beting sampai pada kedalaman rata-rata 2 km. Daerahnya curam dengan kemiringan rata-rata 1o – 35o atau 1:2 sampai 1:40, mulai dari tepi dangkalan benua kearah laut lepas dan mencakup luas ± 13% dari luas permukaan bumi, kedalamannya antara 200 – 1800 meter dan terbentuk sebagai hasil sedimentasi dan sesar. Sedang landasan berbukit adalah transisi antara benua dengan samudera, mempunyai kemiringan 1:50 sampai 1:800 dengan rata-rata 1:150. Tanjakan continental merupakan tempat pengumpulan sedimen yang berasal dari daratan. Banyak di belahan dunia terdapat jurang di bagian tepi samudera (submarine canyon) membentuk lereng benua dan landasan berbukit/tanjakan yang palungnya bentuk seperti bentuk penampang lembah (V- shape valley) disebut sebagai “trench” dan kalau penampang bentuk seperti U disebut “trough”. Jurang di tepian samudera atau “submarine canyon” merupakan hal menarik untuk diketahui, karena transpor material dari landasan/paparan ke laut sampai ke laut dalam, melalui saluran jurang tersebut. Bentuk saluran pada jurang tepian samudera yang berada di kawasan paparan benua bentuk dan arah alur pemasukan material di sajikan pada gambar 8.2 . Material yang berasal dari daratan masuk ke laut yang kemudian oleh adanya arus air yang kuat akhirnya bahanbahan itu terangkut ke tengah samudera di bagian dasar mengendap menjadi sedimen. Tipe dan struktur “Submarine Canyon”, kalau di Indonesia banyak terdapat di laut Jawa karena merupakan daerah paparan Sunda. Dalam gambar terlihat ada panah merah bagian tengah, halitu memperlihatkan bagaimana lumpur dari daratan mengalir ke landasan kontinen dan masuk ke samudera. ~ 169 ~ Gambar 8.2. Bentuk “Submarine Canyon” Paparan tepian yang berbentuk “trench” (palung) banyak terdapat di samudera Pasifik (Chester, 1990) mengelilingi lembah samudera. Diperkirakan panjangnya sampai 4500 km, dan biasa lebarnya berukuran sedang, yaitu < 100 km. Landas tepian ini berhubungan erat dengan daratan, terkadang pembentuknya sebagai akibat dari gerak tektonik di lautan. Umumnya palung terjadi dasar laut sangat dalam dan berdinding curam, yang semakin ke dasar semakin menyempit. Palung ini berperan penting sebagai penangkap material dari kawasan landas kontinen ke arah laut, biasanya palung ini bisa membentuk landasan berbukit (continental rise) jika telah terjadi penimbunan sedimen. Dasar lembah samudera (the ocean basin floor) letaknya berhubungan dengan margin kontinen. Kalau di samudera Hindia, Atlantik dan Pasifik utara dasar lautnya banyak ditemui paparan abisal. Di paparan daerah ini umumnya lapisan sedimen di dasar laut sangat tebal bisa mencapai > 1000 m, halmana material yang berasal dari margin kontinen di transport ke daeah abisal oleh suatu gerakan arus yang kuat, dimana arus itu membawa material dengan kekeruhan yang tinggi sehingga makin bertambah waktu terbentuklah suatu lapisan dasar laut yang tebal, itulah disebut sedimen. Jadi, material yang berasal dari margin kontinen dipindahkan ke dataran abisal membentuk lapisan tebal bisa juga berasal dari daratan dan dihantar oleh arus dasar sampai ke curam abisal. Sedimen yang terendam pada bagian bibir abisal itu, umumnya ~ 170 ~ material itu melalui daerah “hemi-pelagic” , yaitu suatu daerah di badan air dibawah daerah pelagik. Intinya lapisan yang ada di bibir abisal merupakan tanggul penahan sedimen yang akan masuk ke lubuk abisal. Di samudera Atlantik dan Hndia tanggul penahan itu banyak di temui tetapi di samudera Pasifik relatif sedikit. Apabila material didaerah telah berlimpah akan masuk ke daerah palung abisal oleh adanya gerakan arus. Palung abisal adalah dasar laut sangat dalam dan berdinding curam, yang semakin ke dasar semakin menyempit. Palung sempit dan tidak terlalu curam disebut “trench” (lihat gambar 8.1). Gundukan di daerah abisal dapat membentuk bukit atau gunung kecil di dasar laut yang puncaknya tidak muncul di permukaan laut, biasanya wilayah ini hampir 80% menutupi dasar laut di beberapa Samudera . Disamping itu didasar laut ditemui “seamounts” yaitu gunung di dasar laut dengan lereng yang curam dan berpuncak runcing serta kemungkinan mempunyai tinggi sampai 1 km atau lebih tetapi tidak sampai ke permukaan laut. Pembentukan gundukan tanah tersebut oleh adanya gerakan magma di dasar laut, gunung didasar laut ini banyak terdapat di samudera Pasifik. Punggung didasar samudera atau “mid oceanic ridge”, merupakan punggungan yang terbentuk akibat tenaga tektonik vertikal di tengah samudera sehingga bentuknya memanjang . Bentuk punggungan tersebut adalah wajah dipermukaan bumi, seperti wilayah daratan provinsi Sulawesi utara terdapat banyak bukit dan pengunungan dan hampir semua wilayah Indonesia timur ditemui kawasan pergunungan, gambaran seperti itu sama halnya wajah didasar samudera Atlantik, Antartika, Hindia dan Pasifik. Bahkan di dasar samudera Pasifik ada “mid oceanic ridge” (lihat gambar 8.3) mencakup luas lebih dari 60.000 km, serta beberapa punggung dasar laut ketinggiannya dari dasar laut bisa mencapai puncak 3.000 meter. Memang punggung dasar samudera sangat kompleks di ~ 171 ~ belahan bumi, bahkan ada dapat memisahkan dasar samudera oleh adanya punggung yang tinggi oleh karena itu sering disebut wajah wilayah pararel di dasar samudera. Bertolak dari teori pembentukan punggung dasar laut yaitu adanya gerakan sel-sel dari mantel bumi yang bersifat panas keluar dari dasar samudera, secara perlahan-lahan membentuk bukit kecil dan dibagian ujung menjadi retah oleh adanya gerakan magma, akhirnya jumlah material tanah yang panas makin bertambah sehingga membentuk gundukan tanah yang banyak. Gambar 8.3 memperlihatkan bagaimana gerakan magma membentuk punggung dasar laut . Pulau Bukitan Tengah Laut Gunung Paparan Abisal di Bawah Laut Magma Gambar 8.3. Dasar Samudera Dengan Pembentukan “Mid-ocean ridge” Material tanah di bagian puncak punggung berpindah tempat ke samping sehingga membentuk “trench”. Makin bertambah waktu material tanah dari tanah dibawah dasar laut naik kerpermukaan dasar laut oleh adanya gaya magma akhirnya membukit sehingga akan bergeser ke daerah sekitarnya, gundukan tanah ini bisa membentuk gunung laut ~ 172 ~ (seamount, lihat gambar). Biasanya lapisan tanah yang terbentuk itu menjadikan kerak yang baru yang bersifat keras. Menurut para ahli geofisika bahwa kecepatan pembentuk lapisan keras itu sangat lambat hanya beberapa centimeter dalam setahun, walaupun demikian penimbunan material berasal dari tanah dibawah dasar laut berjalan terus sepanjang tahun. Suatu dugaan punggung dasar laut di samudera Atlantik, samudera India bisa terbentuk 1-2,5 cm per tahun, sedang di bagian timur samudera Pasifik bisa mencapai 5 cm setiap tahun (Chester dan Jickells, 2012). Hasil kajian ahli gempa mengatakan lembah samudera umurnya relatif masih mudah ditinjau dari waktu geologi, kemudian melalui pembuktian dengan data sedimen dari proyek pengeboran dasar laut (DSDP/Deep Sea Drilling Project) memperlihatkan bahwa pembentuk lapisan keraksamudera terjadi pada miliaran tahun lalu diperkirakan pada abad pertengahan “jurassic”, dan pembentukan memang paten akibat dari gaya tektonik membentuk lempengan/plate teknonik (Chester dan Jickells, 2012). Sampai saat ini telah diakui permukaan bumi setebal 100-150 km mudah bergerak dan terus bergeser, di bumi kita ada 6-7 patahan bumi yang asli, olehnya tidak dapat dipungkiri gempa bumi sering terjadi. Lempengan patahan bumi memiliki batas masingmasing, hakekatnya jenis batasan itu menurut Jones (1978) ada tiga jenis yang diketahui, yakni: ① Batas konservatif, halmana setiap lempengan tidak terjadi gesekan atau merusak satu sama lain. ② Batas konstruktif, dimana lempengan itu aktif bergerak membentuk bukit baru sehingga menjadi lempengan baru. Oleh demikian batas konstruktif adalah sumber lempengan (crust). ③ Batas destruktisf, halmana batas lempengan itu bergerak dan menabrak lempengan lain, sehingga batasan lempengan bisa membentuk “trench” dan ~ 173 ~ pulau atau kumpulan gunung mudah. Jadi adanya gerakan maka pinggiran lempengan yang rusak akan tenggelam masuk kedalam “trench” dan kembali ke mantel bumi. Proses tenggelamnya material lempengan yang rusak merupakan hal yang menarik karena tanah yang kembali ke mantel bumi adalah sedimen yang akan terakumulasi di dasar laut. Implikasinya ke proses geokimia telah terjadi penumpukan sedimen di dasar laut, kemudian ditambahnya material yang tenggelam dari badan air maka terjadi suatu siklus geokimia di laut. Prinsip dasar yang harus kita ketahui bahwa sedimen adalah material bahan padat, berasal dari batuan yang mengalami proses pelapukan; peluluhan (disintegration); pengangkutan oleh air, angin dan gaya gravitasi; serta pengendapan atau terkumpul oleh proses atau agen alam sehingga membentuk lapisan-lapisan di permukaan bumi yang padat atau tidak terkonsolidasi (Bates dan Jackson, 1987). Sedang pernyataan Boggs (1986) bahwa sedimen permukaan dasar laut umumnya tersusun oleh: material biogenik yang berasal dari organisme; material autigenik hasil proses kimiawi laut (seperti glaukonit, garam, fosfor); material residual; material sisa pengendapan sebelumnya; dan material detritus sebagai hasil erosi asal daratan (seperti kerikil, pasir, lanau dan lempung) Hakekatnya semua samudera di dunia ditutupi oleh sedimen, entah bersumber dari material di permukaan air yang tenggelam atau akibat hasil destruktif lempengan dan erosi gunung-gunung di dasar laut. Lapisan sedimen itu sangat bervariasi tergantung lokasinya, seperti: di samudera Pasifik terdapat lapisan sedimen rata-rata setebal < 1 km, dan di samudera Atlantik di temui rata-rata > 1 km. Tetapi secara rata-rata ketebalan sedimen di semua samudera diperkirakan 500 meter (Chester, 1990). Intinya laut merupakan wadah ~ 174 ~ penampung partikel baik berasal dari atmosfer yang tenggelam ke dasar laut, material yang dihantar oleh aliran sungai, dan atau aliran air “run off”. Material-material tersebut mengandung pelbagai elemen kimia masuk ke samudera dan ditambah lagi elemen kimia bersumber dari batuan di dasar laut maka pertukaran reaksi kimia di dasar laut merupakan suatu proses geokimia. Prinsipnya sedimen yang di jumpai di dasar laut dapat berasal dari beberapa sumber yaitu : 1. Lithogeneuos sedimen yaitu sedimen yang berasal dari erosi pantai dan material hasil erosi daerah up land. Material ini dapat sampai ke dasar laut melalui proses mekanik, yaitu tertransport oleh arus sungai dan atau arus laut dan akan terendapkan jika energi tertrransforkan telah melemah. 2. Biogeneuos sedimen yaitu sedimen yang bersumber dari sisa-sisa organisme yang hidup seperti cangkang dan rangka biota laut serta bahan-bahan organik yang mengalami dekomposisi. 3. Hidreogenous sedimen yaitu sedimen yang terbentuk karena adanya reaksi kimia di dalam air laut dan membentuk partikel yang tidak larut dalam air laut sehingga akan tenggelam ke dasar laut, sebagai contoh dan sedimen jenis ini adalah magnetit, phosphorit dan glaukonit. 4. Cosmogenous sedimen yaitu sedimen yang bersal dari berbagai sumber dan masuk ke laut melalui jalur media udara/angin. Sedimen jenis ini dapat bersumber dari luar angkasa, aktifitas gunung api atau berbagai partikel darat yang terbawa angin. Material yang berasal dari luar angkasa merupakan sisa-sisa meteorik yang meledak di atmosfir dan jatuh di laut. Sedimen yang bersal dari letusan gunung berapi dapat berukuran halus berupa debu volkanin, atau berupa fragmen-fragmen aglomerat. Sedangkan sedimen yang bersal ~ 175 ~ dari partikel di darat dan terbawa angin banyak terjadi pada daerah kering dimana proses eolian dominan namun demikian dapat juga terjadi pada daerah sub tropis saat musim kering dan angin bertiup kuat. Dalam hal ini umumnya sedimen tidak dalam jumlah yang dominan dibandingkan sumber-sumber yang lain. Secara singkat, sedimen di lembah dasar laut yang berasal dari aktivitas hidrotermal kaya akan elemen logam, dapat membentuk batuan keras di lapisan dasar laut sehingga menjadi gundukan tanah membentuk gunung dan tersebar di samudera. Punggung gunung tersebut biasanya telah terakumulasi dengan karbonat sedimen sehingga sebaran gundukan gunung di samudera mengandung tanah liat dan sedimen karbonat. Biasanya pembentukan kumpulan gundukan tanah diatur atau dikontrol oleh faktor kimia, fisika dan biologi. Kegiatan pembentukan gundukan sehingga menjadi suatu lempengan akan berbeda dari satu lokasi ke lokasi lain dan sangat tergantung pada lingkungannya. Dengan demikian lapisan sedimen di dasar laut sangat bervariasi, bisa berbentuk landasan yang mudah hancur, ukurannya berubah, bentukannya yang curam dan lempengan berukuran memanjang sehingga mngendalikan sirkulasi air di laut dalam yang akhirnya berdampak pada pembentukan sedimen. Telah diketahui banyak arus berasal dari perairan yang dangkal membawa material dan kelarutan pelbagai elemen di masuk ke perairan dalam yang akhirnya menyusun deposit sedimen sehingga bisa membentuk lapisan sedimen tebal, biasanya lapisan tersebut tersusun dalam waktu 120 juta tahun (Davies & Gorsline, 1976). Selama periode itu penyusunan sedimen di lingkungan laut umumnya bahan-bahan itu kaya akan karbonat dan silika serta membentuk suatu lapisan tertentu, tetapi dalam suatu waktu terjadi kekurangan unsur itu akibat dari pengikisan oleh arus atau adanya reaksi kimia yang berlangsung di dasar perairan. Juga kemungkinan hilang senyawa itu dari sedimen yang paten oleh terjadi evolusi ~ 176 ~ tektonik di lembah dasar laut. Perubahan sedimen didasar perairan bisa juga di sebabkan oleh adanya perubahan cuaca secara global, bahan-bahan itu terangkut ke badan air laut dan terjadi interaksi kimia di perairan, terkadang dengan adanya suatu gerakan arus yang kuat bahan-bahan itu naik sampai ke permukaan air (peristiwa up welling), mengakibatkan perairan itu subur, proses produksi primer di laut makin cepat terjadi. Banyak kejadian di laut terjadi kematian ikan secara massal, karena akibat proses up welling, banyak gas-gas beracun di dasar laut naik ke badan laut bahkan sampai ke permukaan, misalnya tahun 2012 terjadi kematian ikan secara massal di perairan Bali, hasil kajian oleh Badan Penelitian dan Pengembangan KKP, ternyata oleh adanya proses pengangkutan material dari dasar laut bersamaan dengan gasgas beracun seperti amoniak dan asam sulfida ke daerah permukaan air. Sedimen di laut tersusun oleh pelbagai senyawa yang ada dilingkungan, namun demikian secara pasti penyusunannya di daerah dekat pantai dan di daerah laut dalam akan berbeda. Dengan demikian sedimen di laut dapat di kategorikan ke dalam dua rezim yang berbeda, yaitu: ① Sedimen dekat pantai, sedimen di rezim ini banyak dipengaruhi oleh bahan-bahan dari daratan. Secara umum aspek fisika, kimia dan biologi deposit material di kawasan estuari, dune, teluk, lagun, delta, daerah yang terkena pasang, bagian depan kontinen dan pinggiran pantai sangat bervariasi dan sangat berbeda dengan rezim di laut dalam. Sesungguhnya Sedimen di daerah pingiran pantai rentan terkena dampak oleh dua kekuatan yaitu alamiah dan antropogenik. ② Sedimen laut dalam, dalam rezim ini biasanya berada pada kedalaman > 500 meter, material-material yang terdeposit dikendalikan oleh material berasal dari ~ 177 ~ daratan juga. Oleh karena ada aktivitas biologi, dan terjadi penenggelaman material berasal dari atmosfer ke permukaan air dan langsung kedasar perairan. Diperkirakan hampir 50% sedimen di laut dalam berasal dari atmosfer masuk melalui permukaan laut, sifat kimia material itu sangat berbeda dengan sedimen dari daratan. Disamping itu sedimen di laut dalam bisa juga berasal dari aktivitas gunung berapi. Dengan demikian karakteristik sedimen di rezim laut dalam bisa dilihat dari ukuran material dan kecepatan akumulasinya. (a) Sedimen di laut dengan fraksinya berasal dari daratan umumnya lebih didominasi oleh tanah lempung dengan ukurannya kecil yakni sedimen berdiameter <2 µm. Tanah lempung memiliki daya viskositas tinggi sehingga tanah ini tidak mudah menjadi ukuran pertikel kecil seperti pasir. Umumnya tanah lempung mudah bersenyawa dengan air, dalam larutan kental tanah ini berwarna kecoklatan. Sedimen tersebut kurang-lebih 6070% mengandung material “non-biogenic”, sangat berbeda dengan sedimen yang ada di daerah dekat pantai, kalau sedimen di dekat pantai terdapat pelbagai variasi ukuran dan lebih didominasi bahan “biogenic”. Umumnya komponen fraksi tanah liat yang padat berukuran kecil banyak terdapat di laut, seperti disajikan pada tabel 8.1. ~ 178 ~ Tabel 8.1. Sedimen Laut Berukuran <2µm dan Suspensi Material dari Sungai Tipe sedimen Lokasi Sedimen pelagis Samudera Atlantik Samudera Pasifik Samudera India Pantai Atlantik di US Dasar jurang perairan Meksiko Dasar jurang perairan california Landasan Sahul Australia 33 buah sungai di US Sedimen pinggiran pantai Partikel dari sungai Berat (%) fraksi <2µm 58 61 64 2 27 19 72 37 Sumber: Chester (1990) (b) Kecepatan akumulasi sedimen di laut biasanya dilakukan dengan pengukuran menggunakan radio aktif seperti 14C, 3 H atau dari uranium lainnya, dan melihat fosil yang ada. Perbedaan data di beberapa samudera di sajikan pada tabel 8.2 berikut. Tabel 8.2. Kecepatan Akumulasi Bahan dari Daratan Di Sedimen Laut Dalam 3 Wilayah Samudera Rata-rata akumulasi (mm/10 Tahun) a b Pasifik Selatan 0,45 1,0 Pasifik Utara 1,5 5,8 Atlantik selatan 1,9 6,0 Atlantik Utara 1,8 5,7 Samudera India 4,4 Keterangan: a) data dari Goldberg & Griffin (1964) b) data dari Ku dkk (1968) Walaupun kedua sumber data pada tabel 8.2 agak berbeda, karena metoda pendekatan agak berbeda. Namun demikian simpulan yang dapat ditarik dari tabel itu, bahwa kecepatan akumulasi material menjadi sedimen di laut dalam ~ 179 ~ relatif lambat dimana < 10 mm di daerah pelagis bisa mencapai 1000 tahun. Hakekatnya kecepatan akumulasi membentuk sedimen di laut dalam tergantung pada kondisi lingkungan, menurut beberapa sumber pustaka akumulasi tertinggi biasanya di landasan “hemi pelagic” yakni > 10 mm per 1000 tahun. Kemudian adanya perpindahan ke arah daerah pelagik, maka kecepatan makin berkurang yakni 0,5 mm per 1000 tahun seperti yang terjadi di lembah Atlantik tengah. Walupun demikian menurut Ku dkk, (1968) terkadang nilai 3 kecepatannya agak naik ( 1 mm/10 tahun) di daerah yang agak jauh, dan prakiraan rata-rata kecepatan akumulasi sedimen non karbonat di laut dalam bisa mencapai 2 mm per 1000 tahun. Alhasil beberapa ahli mengatakan material yang terakumulasi di sedimen laut dalam kecepatan rata-rata hanya beberapa milimeter per tahun, tetapi bertolak belakang dengan di daerah dekat pantai, dimana akumulasi dapat terjadi beberapa milimeter dalam pertahun dan deposit terbentuk ada dalam bentuk non-karbonat. Bagaimana Batuan Sedimen Terbentuk ? Batuan sedimen terbentuk dari batuan-batuan yang telah ada sebelumnya oleh kekuatan-kekuatan seperti pelapukan, gaya-gaya air, pengikisan-pengikisan, angin, arus serta proses litifikasi, diagnesis, dan transportasi, maka batuan ini terendapkan di tempat-tempat yang relatif lebih rendah letaknya, seperti di laut Mula-mula sedimen merupakan butiran, partikel dan batuan-batuan lunak, akan tetapi karena proses diagnesis sehingga batuan-batuan lunak tadi akan menjadi keras. Proses diagenesis adalah proses yang menyebabkan perubahan pada sediment selama terpendamkan dan terlitifikasikan. Pengertian litifikasi adalah proses perubahan material sedimen menjadi batuan sedimen yang kompak. ~ 180 ~ Proses diagenesis ini dapat merupakan kompaksi yaitu pemadatan karena tekanan lapisan di atas atau proses sedimentasi yaitu perekatan bahan-bahan lepas tadi menjadi batuan keras oleh senyawa kimia misalnya senyawa kapur atau silisium. Sebagian batuan sedimen terbentuk di dalam samudera. Beberapa zat ini mengendap secara langsung oleh reaksi-reaksi kimia misalnya garam (CaSO4.nH2O), adapula yang diendapkan dengan pertolongan jasad-jasad, baik tumbuhan maupun hewan. Batuan endapan yang terbentuk secara kimiawi hakekatnya pengikat material oleh reaksi kimia sehingga membentuk padatan keras. Prinsip dasar proses diagnesis memiliki tahapantahapan sebagai berikut: a) Eoldiagenesis, tahap ini merupakan tahap awal dari pengendapan sedimen. Dimana terjadi pembebanan, yang menyebabkan adanya kompaksi pada tiap lapisan sedimennya. Pada tahap ini proses kompaksi mendominasi; b) Mesodiagenesis = earlydiagenesis, tahap mesogenesis ini terjadi setelah melewati tahap eoldiagenesis. Pada tahap ini, kompaksi yang sangat kuat disertai dengan proses peleburan, menyebabkan kenaikan suhu dan tekanan yang memicu terjadinya “dissolution”/pelarutan. Pada tahap ini proses yang mendominasi adalah pelarutan. c) Latelydiagenesis, Jika proses peleburan berjalan terus maka terjadilah butiran sedimen, biasanya disebut latelydigenesis. Apabila kompaksi terus berlanjut, hingga pada suhu 150 derajat celcius. Proses diagenesis akan berhenti dan digantikan menjadi proses metamorfisme. d) Telodiagenesis, tahapan ini terjadi setelah tahap mesodiagenesis terjadi pengangkatan, dalam proses pengangkatan ini, keberadaan berbagai jenis air (air meteorik, air tanah, dll) mempengaruhi susunan ~ 181 ~ komposisi kimia batuan, sehingga memungkinkan terjadinya authigenesis (pengisian mineral baru). Lapisan horizontal yang ada di batuan sedimen disebut “bedding”. Bedding terbentuk akibat pengendapan dari partikelpartikel yang terangkut oleh air atau angin. Kata sedimen sebenanrya berasal dari bahas latin ”sedimentum” yang artinya endapan. Batas-batas lapisan yang ada di batuan sedimen adalah bidang lemah yang ada pada batuan dimana batu bisa pecah dan fluida bisa mengalir. Selama susunan lapisan belum berubah ataupun terbalik maka lapisan termuda berada di atas dan lapisan tertua berada di bawah. Prinsip tersebut dikenal sebagai prinsip superposition. Susunan lapisan tersebut adalah dasar dari skala waktu stratigrafi atau skala waktu pengendapan. Pengamatan pertama atas fenomena ini dilakukan oleh Nicolaus Steno di tahun 1669. Beliau mengajukan beberapa prinsip berkaitan dengan fenomena tersebut. Prinsip-prinsip itu adalah prinsip horizontality, superposition, dan original continuity. Prinsip “horizontality” menjelaskan bahwa semula batuan sedimen diendapkan dalam posisi horizontal. Pembentuk batuan sedimen adalah partikel-partikel atau sering disebut sedimen yang terbentuk akibat hancuran batuan yang telah ada sebelumnya seperti batuan beku, batuan metamorf, dan juga batuan sedimen sendiri. Disamping sedimen-sedimen di atas, adapula sejenis batuan sejenis batuan endapan yang sebagian besar mengandung bahan-bahan tidak larut, misalnya endapan puing pada lereng pegunungan-pegunungan sebagai hasil penghancuran batuan-batuan yang diserang oleh pelapukan, penyinaran matahari, ataupun kikisan angin. Batuan yang demikian disebut eluvium dan alluvium jika dihanyutkan oleh air, sifat utama dari batuan sedimen adalah berlapis-lapis dan pada awalnya diendapkan secara mendatar. Lapisan-lapisan ini tebalnya berbeda-beda dari beberapa centimeter sampai beberapa meter. ~ 182 ~ Di dekat muara sungai endapan-endapan itu pada umumnya tebal, sedang semakin ke laut endapan-endapan ini akan menjadi tipis dan akhirnya hilang. Di dekat pantai, endapan-endapan itu biasanya merupakan butir-butir besar sedangkan ke arah laut kita temukan butir yang lebih halus lagi. Dengan demikian dapat katakan lapisan-lapisan dalam sedimen itu disebabkan oleh beda butir batuan yang diendapkan. Biasanya di dekat pantai akan ditemukan batupasir, lebih ke arah laut batupasir ini berganti dengan batulempung, dan lebih dalam lagi terjadi pembentukkan batugamping (Katili dan Marks). Ada dua tipe sedimen yaitu: detritus dan kimiawi. Detritus terdiri dari partikel-partikel padat hasil dari pelapukan mekanis. Sedimen kimiawi terdiri dari mineral sebagai hasil kristalisasi larutan inorganik atau organik. Partikel sedimen diklasifikasikan menurut ukuran butir, gravel (termasuk bolder, cobble dan pebble), pasir, lanau, dan lempung. Adanya gerakan air partikel/butiran berasal dari daerah kontinental, pelagis dan abrasi di bukitan yang ada didasar laut di transpor ke tempat lain akan membentuk lempengan tipis, makin bertambah waktu makin menebal. Sedang proses litifikasi dari sedimen menjadi batuan sedimen terjadi melalui kompaksi dan sementasi. Intinya, batuan sedimen dapat dibagi menjadi 3 golongan yakni: 1. Batuan sedimen klastik, terbentuk dari fragmen batuan lain ataupun mineral 2. Batuan sedimen kimiawi, terbentuk karena penguapan dan pelapukan 3. Batuan sedimen organik, terbentuk dari sisa-sisa kehidupan hewan/ tumbuhan Batuan Sedimen Klastik terbentuk akibat pengendapan kembali detritus atau pecahan-pecahan batuan asal, dapat berupa batuan beku, sedimen atau metamorf. Berbagai macam proses yang terjadi sebelum terbentuknya batuan sedimen klastik, diantaranya : (1). Pelapukan ~ 183 ~ (Weathering) yaitu proses yang merubah ukuran dan komposisi dari batuan dan terjadi dekat permukaan bumi akibat perbedaan temperatur dan iklim; (2) Erosi yaitu proses yang menyebabkan hilangnya partikel (clasts) batuan dari permukaannya oleh tenaga eksogen (air, angin, atau es): (3). Deposisi yaitu proses akhir dari transportasi yang menempatkan partikel batuan di atas permukaan bumi, dan membentuk fondasi untuk proses sedimentasi: (4). Kompaksi yaitu proses penyatuan pada material-material sedimen sehingga jarak antar material semakin dekat dan menyebabkan sedimen dapat menjadi kompak, dan ke (5) Litifikasi yaitu terjadinya proses sementasi atau perekatan pada material-material yang telah mengalami proses kompaksi membentuk batuan sedimen Berdasarkan ukuran partikel dari sedimen klastik, sedimen-sedimen dapat dibedakan sebagai berikut. Tabel 8.3. Klasifikasi ukuran partikel Di sedimen klastik. Nama Partikel Boulder/Bongkah Cobble/Kerakal Pebble/Kerikil Sand/Pasir Silt/Lanau Clay/Lempung Ukuran >256 mm 64 – 256 mm 2 – 64 mm 1/16 – 2mm 1/256 – 1/16 mm <1/256 mm Sedimen Gravel Gravel Gravel Sand Silt Clay Sumber: dikutip dari pelbagai pustaka ~ 184 ~ Nama batu Konglomerat dan Breksi (tergantung kebundaran partikel) Sandstone Batu lanau Batu lempung Pembentukan sedimen di laut dalam Proses pembentukan sedimen di laut dalam ada kaitannya dengan jalannya transpor material dan distribusi ke pelbagai tempat di samudera. Secara sederhana pemindahan material ke samudera tergantung pada situasi yang ada, intinya ada lima tipe mekanisme pemindahan sedimen di laut dalam. Gravitasi arus, kecepatan pemindahan material ke samudera tergantung pada daerah landasannya, apakah agak miring, sedikit terjal dan bagaimana gaya aliran arusnya. Namun demikian arus dengan kekeruhan tinggi agak lebih cepat ke arah samudera terbuka. Arus yang keruh membawa suspensi sedimen membentuk lapisan di laut dalam, ada yang bersifat sementara, kecepatan arus tinggi dan kepadatan arusnya. Umumnya suspensi yang merupakan kekeruhan itu akan di transport ke laut dalam melalui “submarine canyon” (ilsutrasinya dapat dilihat pada gambar 8.2). Biasanya bahanbahan itu akan melapisi pasir didasar laut sehingga terbentuk lapisan baru sebagai lapisan “interbed”. Jadi kekeruhan yang diangkut oleh arus akan membentuk sedimen di daerah landasan berbukit (continental rise) dan lapisan abisal di lantai laut dalam. Arus di dasar laut, Intinya arus di dasar lautan signifikan bagi pergerakan sedimen yang ada di dasar laut dalam. Arus yang membawa material berukuran butiran kecil dalam jumlah yang banyak sehingga terlihat kekeruhan tinggi, material itu akan mengendap di dasar laut membentuk tumpukan dan gundukan di dasar laut. Arus di dasar laut biasanya sangat kuat di daerah bagian barat lautan, dan oleh adanya gerakan arus ini peluang menyusun sedimen sebagai lapisan di dasar laut mudah terjadi. Arus bagian tengah di laut, arus ini merupakan arus yang paten di laut, biasanya membawa berbagai jenis material masuk ke lautan. Seperti material yang berasal dari pinggiran ~ 185 ~ pantai, suspensi material sedimen dari lembah di dasar laut dan komponen hydrotermal. Bermula pemindahan material berasal dari lembah bagian pinggir kemudian diangkut oleh arus bagian tengah yang akhirnya material itu tiba di bagian tengah laut membentuk gundukan di dasar laut. Arus permukaan dan dekat dengan permukaan, Umumnya arus permukaan dan arus dekat permukaan membawa material berbagai bentuk yang bersumber dari atmosfer, melalui “run-off”, butiran kecil dari daratan. Material tersebut diangkut oleh arus ke tengah lautan yang akhirnya tenggelam, ada pula material dalam perjalanan tenggelam di daerah sekitar pinggiran pantai. Pemindahan material secara vertikal, karena samudera itu begitu luas maka proses pemindahan material dapat juga dikendalikan oleh material karbon yaitu melalui proses biologi atau reaksi kimia atau lebih dikenal sebagai “global ocean flux”. Dalam proses ini, material yang terangkut tadi akan berasosiasi di laut masuk ke siklus biogeokimia yang akhirnya membentuk material berbentuk karbon. Kemudian senyawa karbon berbentuk partikel akan tenggelam ke dasar perairan yang akhirnya bahan-bahan ini akan memegang peran penting dalam proses kimiawi di laut. Namun demikian sebagian material itu akan terangkut oleh arus bagian dalam laut di transpor ke tengah samudera yang akhirnya akan tenggelam di laut dalam. Bertolak dari perbedaan transpor material seperti uraian diatas, dalam kenyataan ada perbedaan vektor transpor dalam rangkah pemindahan material, yakni: (1) pindahnya bahan itu berasal dari pinggiran tumpukan gunung di dasar; (2) adanya pengikisan di bagian permukaan dasar laut (lateral sea-bed); (3) pindahnya bahan di bagian tengah laut; (4) pemindahan bahan di permukaan air dan ke (5) pemindahan terjadi secara vertikal (tenggelam atau naik kepermukaan akibat gerakan arus). Kesemuan material yang masuk ke samudera akan menyusun lapisan di atas dasar lautan, biasanya lapisan ini merupakan ~ 186 ~ media interaksi kimia dan proses biologi di sistem lingkungan dasar laut. Hakekatnya, material yang telah masuk ke laut, entah melalui pelbagai alur pemindahan pasti akan berinteraksi dengan lingkungan samudera, yang perlu diperhatikan adalah komposisi kimia yang ada di sedimen dasar laut. Interaksi kimia di dasar laut ada beberapa pertimbangan, yakni: ➊ Material padatan berasal dari daratan/kontinen mengandung pelbagai kimia, dan begitu bahan-bahan itu ke laut maka terjadilah percampuran komposisinya dan tersebar jauh ke laut. ➋ Pasti pemindahan material ke laut tergantung pada variasi kecepatan sesuai dengan mekanisme transpor. ➌ Hal yang menarik lagi ketarikan relatif dari dasar laut dan partikel yang tenggelam, yang umumnya komposisi kimia di sedimen laut dalam adalah “non biogenous”. Mengapa komposisi sedimen di laut dalam berbentuk lebih dominan nir-biologi, ada beberapa alasan antara lain; (1) sesungguhnya material sampah yang membentuk gundukan di dasar laut ukurannya tidak tentu dan miskin akan logam, umumnya pemindahan itu melalui permukaan melewati zona pantai, ke (2) biasanya material ke badan air ada berbentuk partikel dan kelarutan yang menyerap senyawa dari air laut dan tenggelam ke dasar membawa beberapa elemen kecil (trace element) sehingga menambah elemen di dasar, dimana material itu tidak diikat oleh material di dasar lautan. Prinsip dasar bahwa material yang ditranspor ke laut bisa melalui 3 mekanisme, yaitu: ① “Suspended load” mekanisme transpor dimana partikel tersebut dibawa bersama-sama dengan air secara keseluruhan, ukuran partikel bergantung dari kepadatan mereka dan ~ 187 ~ kecepatan arus, dimana kecepatan arus yang lebih tinggi dapat membawa lebih besar dan partikel yang lebih padat. ② “Bed load”merupakan mekanisme transpor dimana partikel yang lebih kasar dan padat bergerak sepanjang dasar perairan baik secara menggelinding, bergeser maupun meloncat-loncat karena pengaruh tumbukan diantara partikel dan turbulensi tetapi selalu kembali ke dasar. Mekanisme transpor dapat berubah dari suspended loadmenjadi bed loaddan sebaliknya karena adanya perubahan kecepatan aliran. ③ “Dissolve load” dimana berbagai ion masuk ke perairan melalui proses weathering, mekanisme transpor ini tidak terlihat (invisible) dimana ion-ion tersebut larut di dalam air. Dissolve loadsebagian besar terdiri dari HCO-3(ion bikarbonat), Ca+2, SO4-2, Cl-, Na+, Mg+2, dan K+. Ion ini akhirnya terbawa ke lautan dan umumnya menyusun kadungan garam di lautan. Klasifikasi sedimen di laut secara umum. Sebelum masuk ke pembahasan jenis sedimen di laut, perlu diketahui pola gerak pemindahan sedimen dalam aliran air dibedakan menjadi tiga jenis, yaitu : Sedimen merayap (bed load) yaitu material yang terangkut secara menggeser atau menggelinding di dasar aliran. Sedimen loncat (saltation load) yaitu material yang meloncat-loncat bertumpu pada dasar aliran. Sedimen melayang (suspended load) yaitu material yang terbawa arus dengan cara melayang-layang dalam air Uraian-uraian diatas tentang relief dasar laut dan pola gerak sedimen merupakan gambaran bagi kita bagaimana bentuk sedimen di laut. Secara garis besar bentuk sedimen di laut adalah sebagai berikut: ~ 188 ~ 1. Sedimen dekat pantai Sedimen pantai merupakan deposit material berasal dari pinggiran kontinen yang mengandung pelbagai jenis kimia di lingkungan, mulai dari senyawa kimia yang sifatnya toksik sampai nir-toksik. Sediment itu seperti batu kerikil, pasir, endapan tanah dan lumpur semua material itu tersusun membentuk komponen di daerah biogenous, agak becek dan lapisan yang agak keras. Di daerah mengandung unsur biologi (biogenous) terdapat konsentrasi karbon organik yang tersusun pada sedimen, dan di saat tertentu karbon itu bisa berkurang. Secara umum sedimen di kawasan pantai banyak di pengaruhi oleh daratan sehingga bentuk butiran partikel seperti diuraikan dalam skala Wenworth, ilustrasi seperti berikut ini. Lempung keras 0% 100% Lempung Lempung agak berpasir Lanau mendekati Lempung Lempung, Lanau dan Pasir 0% Pasir Pasir sedikit lanau Lanau agak berpasir 100% Pasir berbatu Lanau 100% 0% Endapan padat Gambar 8.4. Bentuk Sedimen Didasarkan Skala Wenworth Bertolak dari gambar diatas terlihat sedimen berbentuk lempung bisa menjadi endapan yang padat, dan endapan padat bisa menjadi lapisan pasir berbatu. Proses ini dapat ~ 189 ~ berlangsung oleh adanya reaksi kimia dan biologi di dasar perairan. Secara fisik sedimen dapat dilihat teksturnya, yakni ada yang ukuran butir (grain size), bentuk pertikel (partikel shape), struktur sedimen, komposisi mineral serta kandungan biota. Dari berbagai sifat fisik tersebut ukuran butir menjadi sangat penting karena umumnya menjadi dasar dalam penamaan sedimen yang bersangkutan serta membantu analisa proses pengendapan karena ukuran butir berhubungan erat dengan dinamika transportasi dan deposisi. Intinya di sedimen pantai mengandung material dengan ukuran bervariasi, yakni dalam bentuk partikel kecil dan butiran yang padat dengan energi rendah di lingkungan dan pasir dengan energi tinggi di lingkungan. Sedimen yang berbentuk agak berbecek lumpur kecepatan akumulasi membentuk sedimen relatif tinggi, yakni lebih besar beberapa milimeter per tahun. Biasanya akumulasi ini merupakan tipe deposit, tetapi deposit ini kurang mengandung karbonat. 2. Sedimen laut dalam Bertolak dari beberapa mekanisme transpor material ke samudera seperti yang diuraikan diatas, pada tipe sedimen yang bersumber dari pelagik dan hemi-pelagik akan terdeposit dan membentuk lapisan sedimen di dasar laut. Sedimen hemi-pelagik laut dalam Sesungguhnya sedimen ini bersumber dari daerah pinggiran kontinen termasuk lapisan dataran di kawasan abisal. Material sebagai sedimen yang bersumber dari daerah daratan pada pinggiran pantai dan juga dari dasar perairan membuat airnya keruh, diangkut oleh arus ke wilayah hemipelagik. Material yang melayang di perairan mengandung banyak senyawa anorganik akan tenggelam ke bagian dasar laut menyusun suatu lapisan. Lapisan yang terbentuk itu memiliki struktur tanahnya meliputi tanah lempung yang agak berlumpur, tanah berasal dari daratan kutub, lumpur yang ~ 190 ~ keruh dan pasir mineral lapisan ini di sebut sebagai sedimen hemi-pelagik. Semua sedimen hemi-pelagik berisikan variasi biologi membentuk suatu ekosistem tersendiri di dasar laut. Kecepatan material menyusun sedimen hemi-pelagik di laut dalam bisa mencapai 10 mm per 1000 tahun, dan terkadang sedimen itu berisi 1-5% bahan karbon organik. Apabila tanah lempung yang ada di hemi-pelagik memperlihatkan warna abu-abu kehijauan serta ada lapisan oksidasi berwarna merah dibawahnya, hal itu menunjukan ada pengurangan kondisi di sedimen tersbut. Sedimen pelagik laut dalam Sedimen yang terbentuk di dasar laut dalam bersumber dari permukaan samudera. Terkadang sedimen itu tidak ada di dasar laut akibat efektivitas gerakan arus dasar laut, menurut Davies dan Laughton (1972) sedimen bersumber dari daerah pelagik turunnya ke dasar perairan disaat tidak ada arus. Material yang tenggelam ke dasar seperti gelembung yang jatuh secara vertikal akan menumpuk dan menutup dasar laut. Jadi intinya sedimen pelagik akan ke dasar jatuh secara vertikal, berbeda dengan sedimen hemi-pelagik dimana pada hemi-pelagik sedimennya bisa berasal dari dasar perairan naik ke atas oleh adanya gerakan arus dalam. Sedimen Pelagik Laut mengandung bahan anorganik Sedimen yang berukuran < 2 µm diperkirakan sebagian besar mengandung fraksi non-biogenous (±60%), sedang fraksi biogenous hanya < 30%. Biasanya sedimen itu berasal dari permukaan air berupa partikel tanah liat, secara ringkas sedimen tersebut dikatakan sebagai tanah lempung dilaut dalam. Material berasal dari daratan tersuspensi di perairan dengan periode waktu panjang umumnya dalam waktu 1000 tahun hanya beberapa milimeter, sedimen ini sebagai sedimen pelagik. Sebetulnya sedimen ini banyak mengandung unsur karbon organik, tetapi proses penenggalaman material ini ke dasar perairan terjadilah peluruhan disaat awal sedimen berada ~ 191 ~ dipermukaan air, sehingga begitu masuk ke dasar laut bahan karbon organik hanya tertinggal 0,1 – 0,2 %. Proses pengendapan bahan tanah lempung biasanya disertai dengan proses oksidasi karena umumnya tanah lempung mengandung unsur besi, disaat unsur besi menjadi “ferri” akan terlihat air berwarna merah, oleh karenanya sering disebut sebagai tanah lempung merah. Beberapa ahli mengatakan tanah lempung berwarna merah ini merupakan komponen utama penyusun sedimen bersifat tanah keras dan bersifat tanah lunak. Sedimen laut dalam bersumber pelagik mengandung unsur biologi. Biasanya sedimen ini mengandung > 30% biogenous, banyak ahli mengatakan sebagai “ooze” (lumpur cair yang halus) dan sedimen ini terbagi kedalam tipe “calcareous” dan “siliceous”. Tipe “calcareous oozes” umumnya berisi >30% karbonat skletal yang menunjukan material sedimen mengandung banyak organisme sampai pada “formaminiferal ooze” (terkadang disebut “globigerina ooze” jika sesudah semua berbentuk “foram”), “nanofissil ooze” (atau coccolith ooze) dan “pteropod ooze”. a. Globigeina ooze, Globigerina adalah dari salah satu group organisme yang bersel tunggal yang dikenal sebagai poraminifera. Sisa-sisa organisme ini membentuk ooze yang menutupi 35% bagian permukaan dasar laut yang kebanyakan dijumpai pada daerah-daerah panas di dunia. b. Coccolith ooze, sedimen mengandung organisme yang ukuran kecil, berasal dari kerang-kerangan, organisme berkulit keras. c. Pteropod ooze, Pteropod adalah golongan mollusca yang bersifat sebgai plankton dimana tubuh mereka meiliki kulit yang mengandung zat kapur. Ooze ini menutupi hanya 1% permukaan laut walaupun terkadang mereka sudah tercampur dengan ooze yang dari jenis lain. ~ 192 ~ Tipe “siliceous ooze” pada tipe ini material yang tertinggal ± > 30% mengandung silika yang tergolong pada “diatom ooze”, “radiolaria ooze” dan juga red “clay ooze”. a. Diatom ooze, diatom adalah golongan tumbuhan yang bersel tunggal memiliki kulit yang mengandung silica, ooze yang terbentuk menutupi 9% dasar laut. Mereka banyak dijumpai pada daerah dingin yang bersalinitas rendah seperti daerah samudera Hindia pada bagian paling selatan. b. Radiolaria ooze, merupakan golongan protozoa bersel satu yang endapannya menutupi 1-2% permukaan dasar laut. c. Red Clay ooze, bentuk ooze ini mempunyai kandungan silica yang tinggi, tapi asalnya sampai saat ini belum diketahui. Diduga butiran halus ooze yang terdapat di laut dalam berasal dari sedimen biogenous tetapi mengalami perubahan yang besar di dalam laut karena pengaruh tinggi tekanan dan konsentrasi asam karbon. Endapan tanah lempung merah (red clay) ini banyak dijumpai di samudera Hindia bagian timur. Sebaran Sedimen di Laut Sedimentasi adalah proses pengendapan sedimen, termasuk semua aktivitas yang mempengaruhi dan merubah sedimen menjadi timbunan sedimen atau batuan sedimen. Batuan sedimen merupakan batuan yang terbentuk dari akumulasi material hasil rombakan batuan yang sudah ada sebelumnya atau hasil aktivitas kimia maupun biologi, yang diendapkan pada cekungan sedimentasi yang kemudian mengalami pembatuan sehingga membentuk lapisan tertentu di dasar laut. Berbagai jenis sedimen yang telah diuraikan diatas (seperti: sedimen lithogeneous, hydrogenous, siliceous, calcareous, terrigenous, glacial) secara ilustrasi sebaran sedimen laut itu di perairan dunia dapat dilihat pada gambar 8.5. dan gambar 8.6. ~ 193 ~ Gambar 8.5. Sebaran sedimen laut secara umum di perairan Dunia Sumber: Davies dan Gorsline, (1976). Suatu penelitian oseanografi oleh HMS Challenger dikoordinasi seorang peneliti berkewargaan Kanada yaitu John Murray di tahun 1876 merupakan penyelidikan awal tentang sedimen laut dalam. Sedimen laut dalam dapat di bagi menjadi dua yaitu: Sedimen Biogenik Pelagis, dengan menggunakan mikroskop terlihat bahwa sedimen biogenik terdiri atas berbagai struktur halus dan kompleks. Kebanyakan sedimen itu berupa sisa-sisa fitoplankton dan zooplankton laut yang terdeposit di dasar laut. Pembentukan sedimen ini tergantung pada beberapa faktor seperti kimia air dan kedalaman serta jumlah produksi primer di permukaan air laut. Jadi,keberadan mikrofil dalam sedimen laut dapat digunakan untuk menentukan kedalaman air dan produktifitas permukaan laut pada zaman dulu. ~ 194 ~ Sedimen Terigen Pelagis, hampir semua sedimen terigen di lingkungan pelagis terdiri atas materi-materi yang berukuran sangat kecil. Ada dua cara materi tersebut sampai ke lingkungan pelagis. Pertama dengan bantuan arus turbiditas dan aliran grafitasi. Kedua melalui gerakan es yaitu materi glasial yang dibawa oleh bongkahan es ke laut lepas dan mencair. Bongkahan es besar yang mengapung, bongkahan es kecil dan pasir dapat ditemukan pada sedimen pelagis yang berjarak beberapa ratus kilometer dari daerah gletser atau tempat asalnya. Bertolak dari gambar diatas, ternyata perairan laut di dunia, material yang terdeposit di permukaan dasar laut lebih didominasi oleh batuan lempung dan “calcareous oozes”. Kemudian sedimen “calcareous oozes” lebih banyak menutupi daerah permukaan dasar laut di kedalaman < 3-4 km. Sedimen yang berwujud “siliceous oozes” ada di seputar lintang tinggi yakni di Antartika dan Pasifik utara (daerah ini juga banyak diatom oozes selain siliceous oozes) serta banyak ditemui di samudera pasifik daerah katulistiwa (radiolarian oozes). Kalau timbunan sedimen glacial di temui di pinggiran Antartika dan di Atlantik Utara. Dalam gambar yang tidak diberi warna adalah sedimen pinggiran pantai atau margin laut. Sedimen yang terdeposit daerah ini lebih banyak di pengaruhi dari daratan. Sedimen lithogenous banyak ditemui di daerah Pasifik utara, sedang bentuk sedimen hydrogenous banyak ditemui di daerah Pasifik selatan. ~ 195 ~ Gambar 8.6 Sebaran Sedimen di Laut Dalam Sumber: Chester dan Jickells (2012) Beberapa peneliti Indonesia telah melakukan penelitian tentang sebaran sedimen di permukaan dasar laut secara terpisah-pisah berdasarkan lokasi kajian, seperti: Helfinalis peneliti dari Pusat Penelitian Oseanografi LIPI, melakukan penelitian sedimen di perairan laut Jawa. Alhasilnya, endapan sedimen di permukaan dasar hanya beberapa sentimeter berwarna coklat kekuningan, hal itu memberi indikasi suplai sedimen dari daratan melalui sungai cukup tinggi. Endapan sedimen di dasar perairan sekitar Kalimantan selatan yang dekat dengan daratan ditemukan endapan lumpur yang encer di permukaan dengan warna coklat dan di lapisan bawahnya lanau lumpuran. Kemudian Sebaran suspensi permukaan berkisar antara 0.018 gr/l terendah ditemukan di sebelah Selatan Pulau kalimantan hingga 0.053 gr/l tertinggi di sebelah barat dari pulau Kalimantan selatan. Sebaran suspensi di kedalaman perairan bagian tengah berkisar antara 0.023 gr/l terendah di sebelah barat Pancel hingga 0.051 gr/l tertinggi yang tersebar di sebelah barat dari pulau Kalimantan ~ 196 ~ selatan. Sebaran suspensi di kedalaman perairan bagian dasar berkisar antara 0.022 gr/l terendah yang didapatkan disebelah barat daya dari pulau Kalimantan selatan hingga 0.051 gr/l tertinggi yang tersebar di sebelah barat dari pulau Kalimantan selatan. (gambar 8.7) Gambar 8.7. Sebaran suspensi di permukaan dasar perairan laut Jawa tengah dan Kalimantan selatan, September 2004 Hasil penelitian Isnaniawardhani (2012) di perairan Madura bagian utara ditemui sedimen dipermukaan dasar laut terdiri dari lempung, lempung-lanauan dan lanau-pasiran, yang umumnya ditemui pecahan cangkang mikroorganisme. Kemudian penelitian di perairan laut Paya, kabupaten Karimun ~ 197 ~ Provinsi Kepulauan Riau, dilakukan oleh Rifardi (2012), ternyata sebaran sedimen di permukaan dasar laut di temui tekstur lanau, lumpur dan perpasir dengan pelbagai ukuran (lihat gambar 8.8). Gambar 8.8. Sebaran Sedimen di Permukaan Dasar Laut Bebrapa peneliti telah melakukan kajian tentang foraminifera sebagai bagian bahan yang tersusun di dasar laut (biostratifikasi), seperti: Loeblich dan Tappan (1994) telah melakukan riset taksonomi foraminifera di paparan Sahul dan Laut Timor, dimana mereka temui ada 946 spesies foraminera di sedimen. Kemudian Natsir dan Rubiman (2010) mengidentifikasi 37 spesies foraminifera bentik di Laut Arafura ~ 198 ~ pada kedalaman antara 29 dan 341 m. Sedang di Teluk Ambon oleh Natsir (2010) berhasil menemukan 61 spesies foraminifera bentik dari 29 sampel sedimen dasar laut pada kedalaman 2650m. Untuk perairan teluk Tomini, dilaporkan oleh Tri Dewi dan Hanafi (2013) bahwa foraminifera di sedimen didominasi oleh foraminifera plangtonik (>90%), seperti Globorotalia menardii, Orbulina universa, Globigerinoides ruber dan lain-lain sebagai penciri sedimen laut dalam. Di sisi lain, foraminifera bentik ditemukan dalam jumlah sedikit (<10%) yang diwakili oleh Cibicidoides wuellerstorfi, Ceratobulimina pacifica, Pyrgo sp., Bolivinita quadralatera, Uvigerina peregrina. Dengan demikian penelitian tentang sedimen di dasar laut dalam dekade terakhir ini di Indonesia makin berkembang. Komposisi Kimia di Sedimen Laut Akhirnya material yang masuk ke laut akan tenggelam ke dasar laut, tetapi tidak berujung pada penimbunan saja namun berjalannya waktu terjadi pemindahan oleh adanya arus, atau bahkan melalui proses siklus geokimia di lingkungan laut. Dalam suatu proses sedimentasi, material yang masuk ke laut berakhir menjadi sedimen. Dalam hal ini zat yang ada terlibat proses biologi dan kimia yang terjadi sepanjang kedalaman laut. Sebelum mencapai dasar laut dan menjadi sedimen, zat tersebut melayang-layang di dalam laut. Setelah mencapai dasar laut, sedimen tidak diam tetapi sedimen akan terganggu ketika hewan laut dalam mencari makan. Sebagian sedimen mengalami erosi dan tersuspensi kembali oleh arus bawah sebelum kemudian jatuh kembali dan terendap. Terjadi reaksi kimia antara butir-butir mineral dan air laut sepanjang perjalanannya ke dasar laut dan reaksi tetap berlangsung penimbunan, yaitu ketika air laut terperangkap di antara butiran mineral. Proses pengendapan material (partikel dan larutan) umumnya akan membentuk batuan sedimen (lapisan sedimen ~ 199 ~ yang padat). Batuan sedimen (batuan reservoir) adalah suatu batuan yang terbentuk dari hasil akumulasi partikel silikat (terigen atau klastik) dan alokem (non-klastik) yang tertransportasikan oleh gravitasi, angin, air, atau es dan melalui presipitasi pada larutan cair. Partikel (sedimen) klastik terbentuk akibat pengendapan kembali detritus atau pecahan-pecahan batuan asal, dapat berupa batuan beku, sedimen atau metamorf. Berbagai macam proses yang terjadi sebelum terbentuknya batuan sedimen klastik, diantaranya: : ➊. Pelapukan (Weathering) yaitu proses yang merubah ukuran dan komposisi dari batuan, halmana proses itu terjadi pada permukaan bumi akibat perbedaan temperatur dan iklim. ➋. Erosi yaitu proses yang menyebabkan hilangnya partikel (clasts) batuan dari permukaannya oleh tenaga eksogen (air, angin, atau es). ➌. Deposisi yaitu proses akhir dari transportasi yang menempatkan partikel-partikel di permukaan bumi, dan membentuk fondasi untuk proses sedimentasi. ➍. Kompaksi yaitu proses penyatuan pada material-material sedimen sehingga jarak antar material semakin dekat dan menyebabkan sedimen dapat menjadi kompak. ➎. Litifikasi yaitu terjadinya proses sementasi atau perekatan pada material-material yang telah mengalami proses kompaksi membentuk batuan sedimen. Pada prinsipnya batuan sedimen disusun oleh material sebagai berikut : (1) fragmen silikat dan butiran yang bersosiasi dengannya, (2) material hasil presipitasi kimia dan biokimia, contohnya senyawa karbonat (kimia dan biokimia klastik) (3) fragmen allochem dari material yang terpresipitasi lebih awal. Ahli geologi sering menyebut “fragmen silikat” adalah detritus atau material terigeneous (terigen), termasuk di dalamnya: gravel, pasir, silt, dan lempung hasil rombakan material silikat atau batuan. Kalau fragmen allochem merupakan fragmen yang terbentuk lebih awal hasil prespitasi (peluruhan) kimia atau biokimia, misalnya material karbonat ~ 200 ~ berupa fosil cangkang , non skeletal, grain (karbonat rombakan) seperti: oolit, ooid, pisoid, peloid, dan sebagainya. Semua proses sedimentasi sampai terbentuk batuan sedimen akan melibatkan reaksi kimia yang kompleks, sehingga tidak bisa dipungkiri sedimen mengandung pelbagai elemen kimia. Pengetahuan tentang komposisi kimia yang tersimpan pada sedimen merupakan data dasar dalam mengsintesa pelbagai reaksi kimia yang akan terjadi di perairan. Untuk itu dari berbagai sumber hasil riset ilmiah yang dilakukan oleh para ilmuan disajikan pada tabel 8.4. Tabel diatas memperlihatkan data kompilasi dari pelbagai sumber material, baik dari kontinen, udara maupun partikel dari sungai, dimana data itu menunjukan tipe sedimen laut secara global, seperti lumpur tepian, lempung laut dalam dan deposit karbonat laut dalam. Tabel berikut (table 8.5) memperlihatkan komposisi elemen secara umum di sedimen utama di laut dalam. ~ 201 ~ Tabel 8.4 Komposisi elemen di sedimen laut dan beberapa material di daerah daratan (µg g-1) Elemen Ag Al As Au B Ba Br Ca Cd Ce Co Cr Cs Cu Er Eu Fe Ga Ge Gd Hf Batuan daratan 0,07 67300 7,9 0,01 65 448 4 45000 0,2 56 13 71 3,6 32 3,7 1,2 35000 16 1,5 6,5 5 Tanah daratan 0,05 71000 6 0,001 10 500 10 15000 0,35 50 6 70 4 30 2 1 40000 20 x 4 --- Material sungai 0,07 94000 5 0,05 70 600 5 21500 1 95 20 100 6 100 3 1,5 48000 25 --5 6 Partikel debu --82000 ----------------23 79 --47 ----48000 --------- ~ 202 ~ Lumpur tepian --84000 5 --------29000 ----13 60 --50 ----65000 --------- Lempung laut dalam 0,1 95000 13 0,003 220 1500 100 10000 0,23 100 55 100 5 200 2,7 1,5 60000 20 1,2 7,8 4,5 Karbonat laut dalam --20000 1,0 --55 190 70 312400 0,23 35 7 11 0,4 50 1,5 0,6 9000 13 0,3 3,8 0,41 Ho In K La Li Lu Mg Mn Mo Na Nd Ni P Pb Pr Rb Se Sb Sc Si Sm Sn Sr Ta Tb Th 1,6 0,1 24000 41 42 0,45 16400 720 1,7 14200 37 49 610 16 9,6 112 0,05 0,9 10 275000 7,1 2 278 0,8 1,08 9,3 0,6 --14000 40 25 0,40 5000 1000 1,2 5000 35 50 800 35 --150 0,01 1 7 330000 4,5 0,1 250 2 0,7 9 1 --20000 45 25 0,5 11800 1050 3 5300 35 90 1150 100 8 100 --2,5 18 285000 7,0 --150 1,2 1 14 ----20000 --------865 1,8 5100 --73 --52 ------------------------- ~ 203 ~ ----25000 --79 --21000 850 1 40000 --35 550 22 --------12 250000 --2 160 ------- 1,0 0,08 25000 45 45 0,5 18000 6000 8 40000 40 200 1400 200 9 110 4,5 0,8 20 283000 7,0 1,5 250 1 1 10 0,8 0,02 2900 10 5 0,5 --1000 3 20000 14 35 350 9 3,3 10 0,5 0,15 2 32000 3,8 0,x 2000 0,x 0,6 --- Ti Tm U V Y Yb Zn Zr 3800 0,5 3 97 33 3,5 127 165 5000 0,6 2 90 40 --90 300 5600 0,4 3 170 30 3,5 250 --- 5700 ----120 ----75 --- 5000 ----145 ----92 240 5700 0,4 2 150 32 3 120 150 770 0,1 --20 42 1,5 35 20 Sumber: Data dari laporan Martin & Vhitfield( 1983); Murphy ( 1985) dan Vadepohl (1960) disitasi oleh Chester dan Jickells (2012) ~ 204 ~ Tabel 8.5. Komposisi Zat Kimia di Sedimen Laut Dalam ( % berat oksidasi) Senyawa Calcareous Lempung Siliceous Rerata lithogeneous Samudera SiO2 26,96 55,34 63,91 42,72 TiO2 0,38 0,84 0,65 0,59 Al2O3 7,97 17,84 13,30 12,29 Fe2O3 3,00 7,04 5,66 4,89 FeO 0,87 1,13 0,67 0,94 MnO 0,33 0,48 0,50 0,41 CaO 0,30 0,93 0,75 0,60 MgO 1,29 3,42 1,95 2,18 Na2O 0,80 1,53 0,94 1,10 K2O 1,48 3,26 1,90 2,10 P2O3 0,15 0,14 0,27 0,16 H2O 3,91 6,54 7,13 5,35 CaCO3 50,09 0,79 1,09 24,87 MgCO3 2,16 0,83 1,04 1,51 C. organik 0,31 0,24 0,22 0,27 N. organik --0,016 0,016 0,015 Total 100 100 100 100 ∑ Fe2O3 3,89 8,23 6,42 --Sumber : El Wakeel dan Riley (1961) Ukuran berat (%) dikalkulasi dari luas tutupan sedimen di dasar laut (calcareous, 48,7%; lithogeneous, 37,8% dan siliceous, 13,5%). Kalau melihat table di atas, ternyata sedimen di samudera elemen CaCO3 , SiO2 dan Al2O3 mendominasi pada komposisi kimia di batuan sedimen. Dalam table 8.6, memperlihatkan komposisi trace elemen yang terdeposit di laut dalam. ~ 205 ~ Tabel 8.6. Konsentrasi Trace Elemen yang Tersimpan di Laut Dalam Trace elemen Lumpur dipantai Karbonat Lempung laut laut dalam dalam Atlantik Cr 100 11 86 V 130 20 140 Ga 19 13 21 Cu 48 30 130 Ni 55 30 79 Co 13 7 38 Pb 20 9 65 Zn 95 35 130 Mn 850 1000 4000 Fe 69900 9000 82000 Sumber: Chester dan Jickells (2012) Lempung laut dalam Pasifik 77 130 19 570 293 116 162 --12500 65000 ~ 206 ~ Sedimen di bukitan dasar laut 55 450 --730 430 105 --380 60000 180000 Nodule Ferromanganese 10 590 17 3300 5700 3400 1500 3500 220000 140580 Tabel diatas menunjukan bahwa elemen Fe dan Mn mendominasi pada pelbagai jenis sedimen seperti: lumpur di pantai, lempung laut dalam, karbonat laut dalam, sedimen di bukitan dasar laut serta bongkahan (nodule) ferro-manganese di dasar laut dan tanah di dasar laut. Seluruh table disajikan diatas memperlihatkan secara umum komposisi kimia yang terdeposit (tersimpan) di sedimen laut, dan hal itu memperlihatkan secara global bagaimana keadaan geokimia di sedimen laut serta merupakan data dasar dalam mengestimasi kandungan kimia di perairan, termasuk elemen kecilnya (trace-element). Intinya mineral yang ada pada lempung, biogenous karbonat dan opal (sedimen banyak pecahan kulit organisme), komposisi kimianya di kendalikan oleh sedimen penyusun mineral itu. Bertolak dari komposisi mineral ini, maka terjadi pelbagai interaksi kimia sehingga membentuk pelbagai jenis sedimen, seperti: tipe lempung, tipe “carbonat oozes” dan tipe “siliceous oozes”. Jika dilihat rerata dari ketiga table diatas dapat disimpulkan bahwa unsur kimia aluminium terkonsentrasi pada lempung, kalau elemen kalsium terdapat dalam sedimen karbonat, sedang unsur silicon terkonsentrasi pada “siliceous oozes”. Kemudian pada table 8.5 terlihat ada unsur Mn dan Fe masuk sebagai elemen utama di sedimen laut dalam, walaupun unsur-unsur itu merupakan trace elemen karena kedua unsur itu sangat penting sebagai agen larutan logam. Didasarkan pada tabel 8.6 terlihat kecenderungan naik jumlah dan sebaran trace elemen di sedimen laut dalam, bertolak dari table itu dapat disimpulkan sebagai berikut: (a) Secara umum, tipe sedimen karbonat sangat miskin trace elemen jika dibandingkan pada sedimen lempung, kecuali unsur Sr. (b) Kandungan trace elemen seperti Cr, V dan Ga di lumpur pantai relatif sama jumlahnya dengan yang ada pada lempung laut dalam. ~ 207 ~ (c) Agak berbeda dengan kandungan Mn, Cu, Ni dan Pb, dimana relatif tinggi di daerah lempung laut dalam, dibandingkan yang dikandung oleh lumpur di pantai. (d) Terjadi perbedaan trace elemen yang ada di lumpur laut dalam di daerah Pasifik jumlahnya lebih besar ketimbang yang terkandung di Atlantik. (e) Kandungan trace elemen yang ada pada nodul (bongkahan) ferromanganese konsentrasinya tinggi dibandingkan dengan konsentrasi pada lempung di laut dalam, apalagi konsentrasi Cr, V dan Ga sangat sedikit di lempung laut dalam. (f) Sedimen di bukitan dasar laut aktif memproduksi metalliferous, seperti Fe, Mn, Cu, Zn, dan Co dan kandungnya relatif tinggi ketimbang yang dikandung pada lempung laut dalam. (g) Kandung trace elemen yang dikandung oleh lempung laut dalam tidak sebesar yang tersimpan di tanah daratan, sebab kemampuan akumulasi kimia trace elemen di laut sangat lambat. Bertolak tabel-tabel diatas ternyata variasi elemen di permukaan dasar laut sebagai akibat reaksi kimia (peluruhan, interaksi dan akumulasi) bahan-bahan cangkang, sisa organisme dan elemen yang ada di material itu, seperti terlihat pada kandungan yang ada di lumpur dan lempung di laut dalam. Kandungan yang ada di metalliferous pada daerah di bukitan dasar laut, bermula dari sedimen laut, baik bersumber dari pelagis maupun oleh gerakan sentrafugal, masing-masing memiliki fraksi kimia tertentu, yang kemudian berinteraksi dengan senyawa kimia yang ada di skeletal yang mengendap di dasar, maka terbentuklah senyawa logam yang kompleks. Prinsipnya, sedimen laut terbentuk oleh adanya material yang masuk ke laut(bisa dari sungai, udara dan air hujan) semua bahan-bahan itu merupakan signal kimia yang ~ 208 ~ terdeposit di dasar laut, oleh adanya pelbagai organisme yang ada di dasar perairan mengakibat reaksi kimia dan membentuk pelbagai jenis sedimen sampai terbentuk lapisan keras mengandung logam. Ada dua hal yang mendasar untuk melihat bagaimana? komposisi kima yang terjadi di sedimen: ① Apakah bentuk signal kimia yang dikandung oleh partikel dan larutan yang masuk ke laut ? ② Bagaimana setiap signal kimia mengikat kimia lainnya yang merupakan suatu karakteristik kimia laut membentuk sedimen atau lapisan sedimen. Hakekatnya, setiap komponen kimia akan berinteraksi dengan pelbagai bentuk sedimen yang ada di perairan pada kondisi cuaca normal atau bisa melalui proses yang terjadi di setiap elemen kimia sehingga membentuk komponen di sedimen laut. Dengan adanya proses interaksi kimia itu, maka terbnetuk empat jenis sedimen, yakni lithogeneous, biogenous, hydrogenous dan cosmogeneous (lihat uraian terdahulu). Sesungguhnya sedimen dilaut terbentuk sangat tergantung pada topografi dasar laut, arus, angin dan gerakan sentrifugal. Dengan demikian sedimen di perairan dunia secara global dapat disimpulkan sebagai berikut: (a) Sebagian besar di permukaan dasar perairan dunia ditutupi sedimen, rerata 500 m, (b) Sedimen di tepian pantai depositnya sangat bervariasi. Kalau sedimen di laut dalam, lebih dari 50% menutupi perairan dunia, umumnya deposit yang terbentuk tergantung pada kelandaian pantai dan biasanya akumulasi yang terjadi sangat lambat. Sedimen laut dalam yang tergolong pada tipe “hemi-pelagik”, mekanisme pembentukannya, berasal dari daerah kontinen diangkut lewat dasar perairan, sedang tipe ~ 209 ~ pelagik umumnya dari permukaan laut jatuh ke dalam perairan dan terdeposit di dasar laut. (c) Jenis sedimen “calcareous oozes” banyak ditemui di permukaan dasar perairan dengan kedalaman < 3-4 km. Sedang sedimen “siliceous oozes” banyak di pinggiran laut yang terletak di lintang tinggi. (d) Intinya, komponen sedimen laut dapat di kategorikan ke dalam fase “aqueous” (interstitial water), lithogenous, hydrogenous, biogeneous dan cosmogeneous. (e) Daerah lumpur pinggiran pantai dan lempung laut dalam konsentrasi trace elemen, relatif diisi oleh: Mn, Cu, Ni, Co dan Pb. Sedimen yang pada dipermukaan dasar laut ada kecenderungan membentuk blok-blok sedimen keras bahkan membentuk lapisan tertentu. Terbentuk lapisan itu tidak hanya oleh kimia yang ada di reservoir tetapi dapat juga dari kerak bumi samudera yang terlepas elemennya dan berintegrasi dengan komposisi kimia yang ada di sedimen. Upaya negara-negara di dunia dalam rangka memajukan perekonomiannya dan untuk memenuhi kehidupan masyarakat, pelbagai kegiatan pembangunan digalahkan, sehingga beberapa dekade belakangan ini lompatan jumlah material, baik berupa partikel maupun fluida yang masuk ke perairan laut tidak dapat dihindarkan, hal ini dapat kita bayangkan laut dengan sistem kimianya akan bekerja keras untuk mengatasinya. Intinya, proses penimbunan material menjadi endapan sedimen dan peluruhan zat-zat ataupun daur ulang sedimen yang ada di dalamnya adalah berbicara soal geokimia laut. Oleh karena itu pengetahuan geokimia sangat dibutuhkan bagi kebutuhan pembangunan secara umum. Geokimia adalah pengetahuan tentang bagaimana sistem kimia di laut sebagai pengendali berbagai proses di laut, sejak dari tenggelamnya atau mengendap material ke laut ~ 210 ~ sampai interaksi kimia yang terjadi, baik di badan air maupun yang ada didasar laut. Selanjutnya bagaimana peristiwa persenyawaan kimia sehingga membentuk kerak samudera. Semuanya merupakan lingkup pengetahuan geokimia. Kalau zat kimia itu melakukan aksi-reaksi yang berhubungan dengan organisme di laut maka halitu disebut sebagai proses biogeokimia di laut. Konsentrasi kimia yang ada di badan air berperan sebagai pengendali sistem kimia di laut adalah merupakan kombinasi elemen yang masuk dari luar, baik bersumber dari sungai maupun dari atmosfer (kelimpahan geokimia), serta sejumlah zat kimia yang keluar akibat dari reaktivitas samudera. Memang tidak dipungkiri, banyak zat kimia di parairan laut juga berasal bebatuan didalamnya, maupun aktivitas vulkanik yang terjadi di bawah tanah dasar laut. Semua zat-zat itu bersama-sama membentuk sedimen di dasar laut. Dalam kegiatan aksi-reaksi zat-zat tersebut di sedimen, ada yang bersifat meluruhkan zat, namun ada yang melakukan daur ulang bahkan daur ulang bisa juga bersumber dari magma yang keluar dari gunung di dasar laut. Secara ilustrasi model daur ulang yang terjadi di permukaan dasar laut dan di seputar gunung di dasar laut seperti terlihat pada gambar 8.9. Dalam gambar tersebut memperlihatkan bagaimana material yang mengendap membentuk sedimen di dasar laut yang kemudian oleh adanya reaksi alam ( reaksi H2O, weathering, dan interaksi zat lain) maka zat-zat itu bisa terurai bagi kepentingan penyusunan kembali sedimen baru dalam pelbagai bentuk, seperti mineral. Menurut Whitfiel (1979) disitasi oleh Chester dan Jickells (2012), bahwa lebih kurang ratusan jenis zat tedensi akumulasi di dalam sistem. ~ 211 ~ Gambar 8.9. Proses Daur Ulang Sedimen di Pemukaan Dasar Laut dan di Gunung di dasar Laut. (Degens dan Mopper disitasi oleh Chester dan Jickells (2012) ~ 212 ~ Hakekatnya, elemen yang diambil dari endapan sedimen akan bersenyawa membentuk suatu fase padat merupakan afinitas pengikatan bahan padat yang diekspresikan dengan koefisien pembagi yaitu Kr. Dimana koefisien itu dikalkulasi antara konsentrasi yang ada di badan air dengan yang ada di bebatuan, sebagai log Kr. Sebetulnya Kr itu berlangsung selama proses daur ulang terjadi di endapan. Menurut Whitfiled dan Turner (1979) disitasi oleh Chester dan Jickells (2012) bahwa pemisahan antara fase padat dan larutan merupakan suatu model elektrostatik, dimana fungsi elektronegatif adalah Qro, yakni melukiskan suatu reaksi oksidasi pada kisi-kisi mineral. Jadi elektronegatif ini berhubungan dengan koefisien pembagi (Kr). Dengan demikian fungsi eletroknegatif (Qro) dan koefisen pembagi (Kr) adalah suatu konsep untuk menghitung konsentrasi di badan air yang dikendalikan geokimia. Kesimpulannya, konsentrasi kandungan zat di badan air dikendalikan kelimpahan yang ada di bebatuan (kelimpahan geokimia) dan yang terserap membentuk lapisan keras di sedimen (reaktivitas laut) ~ 213 ~ ⑨ AIR ANTARA DI SEDIMEN DAN DIAGENESIS A ir antara di sedimen (interstitial waters ) adalah cairan atau larutan yang menempati ruang pori antara partikel dibatuan dan atau sedimen. Larutan ini berperan mempercepat proses diagenetik disedimen. Endapan dari daerah kontinen atau berasal dari pantai akan masuk keperairan dan bercampur dengan air laut, pada fase ini memungkinkan terjadi interaksi sehingga mampu mengencerkan material/partikel termasuk bahan berasal dari hidrotermal, akhirnya material itu akan masuk ke badan air laut menjadi sedimen laut. Dengan demikian interaksi itu berpeluang air masuk kedalam sedimen, sehingga diantara sedimen itu terdapat air, cairan tersebut sebagai airinterstisial. Pada air-interstisial disedimen mengandung elemen kimia , fisika dan biologi yang aktif. Reaksi kimia lewat aktifitas biologi akan berakibat perubahan fase mineral dan komposisi elemen di sedimen, halmana perubahan yang terjadi itu disebut “diagenesis”. Bener (1980) yang pertama menggunakan istilah itu, dimana diagenesis merupakan jumlah total proses perubahan di sedimen atau bebatuan sedimen, walaupun pada akhirnya material itu akan terdeposisi kembali di perairan. Diagenesis awal, Karbon organik yang tersimpan atau diawetkan dalam sedimen merupakan komposisi bahan organik yang sangat kompleks, sebagian besar biostratifikasi itu ada dalam kondisi kurang oksigen, olehnya unsur oksigen merupakan agen pengokidasi. Dalam oksidasi karbon organik ada yang berperan sebagai penerima (akseptor) elektron dan yang lain kehilangan elektron, atau terjadi reduksi-oksidasi ~ 214 ~ (redoks). Menurut Stumm dan Morgan (1996) bahwa proton dan elektron aktif dalam larutan, dimana proses asam-basa akan terjadi pemindahan proton, reaksinya seperti berikut: pH = − log10 aH+ (9.1) dimana, ion hydrogen akan tinggi pada pH rendah dan sebaliknya akan turun jika pH naik. Jadi nilai pH merupakan pengatur kesetimbangan asam-basa. Terkadang perubahan nilai akan berpengaruh pada intensitas kerja redoks. Reaksi redoks akan melibatkan transfer elektron dan p, seperti persamaan berikut. p = − log10 ae− (9.2) dimana larutan ini dapat menerima atau transfer elektron. Karena p merupakan variabel dari kesetimbangan redoks. Jika nilai p relatif tinggi ada kecenderungan oksidasi juga tinggi. Hakekatnya, redoks adalah reaksi oksidasireduksi, biasanya digambarkan sebagai dua separuh-reaksi, yaitu reaksi oksidasi dikatakan sempurna apabila redoks terjadi duakali. Sebagai Ilustrasi, ambil contoh reduksi Fe 3+ pada bahan organik menurut Drever (1982) sebagaimana persamaan berikut. 4Fe3+ + C + 2H2O 4Fe2+ + CO2 + 4H+. (9.3) Persamaan ini memperlihatkan dalam molekul tak ada satupun baik oksigen maupun elektron yang terjadi, karena telah dipecahkan menjadi setengah reaksi. Reaksi yang ada hanyalah Fe dan C, dengan demikian: 4Fe3+ + 4e− 4Fe2+ Dimana Fe3+ berubah menjadi Fe2+ dan, ~ 215 ~ (9.4) (C) + 2H2O CO2 + 4H+ + 4e− (9.5) Hal ini memperlihatkan oksigen berinteraksi dengan karbon membentuk CO2. Walaupun demikian setengah reaksi kimia tidak lengkap sebab larutan tidak bermuatan elektron bebas. Secara teoritis kimia redoks adalah mengukur kimia elektron di setengah-sel. Jadi nilai Eh mengambarkan aktifitas elektro dalam volt, dimana h menunjukan nilai Eh yang merupakan standar elektroda hydrogen. Dengan demikian aktivitas elektron (p) adalah electron relatif dalam larutan, yaitu suatu dimensi jumlah atau dalam volt (Eh), dimana reaksi antar p dan Eh diuraikan dalam persamaan berikut: (9.6) dimana, F adalah Konstanta “Faraday”, R = konstanta gas dan T adalah suhu absolut. Jadi pada suhu 25 0C nilai Eh = 0,059 p. Dengan demikian nilai Eh analog dengan pengukuran pH. Walaupun demikian mengukur nilai Eh dalam oksidasi di perairan alam dalam hubungan reaksi pasangan redoks sulit diaplikasikan. Tapi menurut Stumm dan Morgan (1996) maupun Drever (1982) bahwa nilai itu penting untuk membedakan antara elektroda yang mengukur nilai Eh dan nilai Eh merupakan hasil kalkulasi dari aktivitas redoks. Secara umum konsep keberadaan redoks (redox conditions), jika nilai Eh (redoks potensial) positif memberi indikasi oksidasi terjadi, tapi bila negatif maka telah terjadi reduksi, dengan demikian dapat dikatakan nilai Eh tinggi di separuh-reaksi memperlihatkan telah terjadi oksidasi, sebaliknya bila nilai Eh rendah terjadi reduksi. Tetapi jika suatu setengah-reaksi Eh tinggi di kombinasikan dengan ~ 216 ~ setengah reaksi Eh dengan nilai rendah, maka proses oksidasi dapat terjadi, situasi ini disebut proses diagenetik di sedimen dengan perantara redoks. Bertolak dari persamaan (9.1), Eh dapat dikonversi ke unit energi, hal ini disebut “thermodinamika”, tetapi proses reaksi yang terjadi tidak membutuhkan kinetika. Keberadaan nilai Eh di sedimen mengandung bahan organik yang diproduksi oleh bakteri nir-fotosintetis, Namun dalam proses diagenetik secara garis besar membutuhkan oksigen, dan oksigen diperairan umumnya berasal dari hasil fotosintetis. Tetapi di sedimen proses oksidasinya bisa berjalan halmana oksigen bisa berasal dari bahan organik yang dikandungnya.. Peleburan bahan organik biasanya dilakukan oleh bakteri, sedang bakteri itu dalam melakukan peleburan bahan organik memerlukan oksidasi atau menerima elektron, halini memperlihatkan bila p rendah akan menghasilkan energi rendah. agar reaksi tetap berjalan membutuhkan suatu energi yang cukup, karena mikro organisme yang akan melalukan peleburan bahan organik membutuhkan energi untuk proses metaboliknya. Diagenesis sedimen secara reaksi redoks harus ada ketersediaan beberapa elemen agar proses akan berjalan baik , telah diketahui beberapa elemen seperti: C, N, O, S, Fe dan Mn aktif terlibat dalam proses redoks di akuatik, walaupun sesungguhnya masih ada beberapa komponen kecil (trace element) yang dibutuhkan. Intinya kegiatan itu memerlukan beberapa elemen untuk membantu kerja mikroba dalam rangka mempercepat proses redoks. Secara singkat reaksireaksi yang terjadi disajikan pada table 9.1 dan gambar 9.1 yang dikutip dari Stumm dan Morgan (1996) adalah sebagai berikut. ~ 217 ~ Tabel 9.1. Reaksi Reduksi-Oksidasi di Lingkungan pada pH 7. P A B C D E F G H J L ¼O2(g) + H+(aq) + e ½ H2O 1/5NO-3(aq) + 6/5H+(aq) + e 1/1ON2(g) + 3/5H2O ½Mn (IV)O2(s) + ½HCO-3(aq) + e ½Mn(II)CO3(s)+ H2O 1/8 NO-3(aq) + 5/4H+(aq) + e 1/8NH+4(aq) + 3/8H2O FeOOH(s) + HCO-3(aq) + 2H+(aq) + e FeCO3(s) + 2H2O ½CH2O + H+(aq) + e ½CH3OH 1/8CO2(g) + H+(aq) + e 1/8HS-(aq) + ½H2O 1/8CO2(g) + H+(aq) + e 1/8CH4(g) + ¼H2O 1/6N2 + 4/3H+(aq) + e 1/3NH+(aq) ¼CH2O(aq) + ¼H2O ¼CO2(g) + H+(aq) + e Sumber: Stumm dan Morgan (1996) ~ 218 ~ +13,75 +12,65 +8,9 +6,15 -o,8 -3,01 -3,75 -4,13 -4,68 -8.2 Kombinasi setengah reaksi dalam proses diagenesis menghasilkan sejumlah energi oleh karenanya nilai Eh dan p akan bervariasi. Contoh yang dapat dilihat pada ilustrasi di gambar 9.1, dalam fase oksidasi bahan organik oleh adanya kelarutan oksigen (A + L) dapat menurunkan nilai p dan Eh. Struktur keseluruhan diagenesis bisa dilihat pada gambar 9.1., sebagai contoh lihat kotak kombinasi yang ada dalam gambar, proses kimia yang terjadi kecenderungan menghasilkan banyak energi sedang energi yang digunakan untuk kebutuhan reaksi itu sangat sedikit. Prinsipnya diagenesis dimulai dengan respirasi aerobic (A+L), kemudian denitrifikasi (B+L) dan seterusnya. Hakekatnya, proses diagenetik di sedimen dimana peleburan bahan organik selalu dikendalikan oleh redoks, beberapa kejadian reaski disedimen oleh redoks di sajikan pada table 9.1 dan gambar 9.1. Bertolak dari situ ternyata secara umum proses diagenetik adalah proses katabolik, dan secara alamiah tergantung dari agen oksidan untuk membakar bahan organik. Penguraian bahan organik di sedimen membutuhkan elektron dari pelbagai oksidan yang terjadi di air-interstisial, dan ketika oksigen ada, maka sedimen itu sebagai penerima oksigen. Selama proses diagenetik berlangsung, maka akan terjadi penurunan produksi energi per mol dalam karbon organik, sedang energi itu sangat dibutuhkan bagi kegiatan oksidatif. Jadi apabila oksigen semakin habis maka mikroba sebagai penerima elektron akan berkurang sehingga termodinamikanya turun (. Froelich dkk., 1979; Galoway dan Bender, 1982; Wilson dkk., 1985). Mekanisme reaksi yang terterah pada gambar 9.1 diatas, bisa terjadi dalam kondisi aerob (membutuhkan oksigen) dan anaerob (tidak dibutuhkan oksigen), uraian berikut menjelakan bagaimana proses aerob dan anerob yang akan terjadi. ~ 219 ~ Gambar 9.1. Susunan Proses Diagenesis di Sedimen Dengan Bantuan Mikroba Sumber : Chester dan Jickelss (2012) Metabolisme aerobik, organisme aerobik akan menggunakan oksigen yang terlarut di air-interstisial untuk menghancurkan bahan organik. Peleburan bahan organik ini diawal proses diagenesis akan melalui suatu komposisi yang disebut “redfield”, yakni (CH2O)106(NH3)16(H3PO4). Selanjutnya untuk proses oksidasi bahan organik oleh organisme aerob persamaan reaksinya adalah sebagai berikut: ~ 220 ~ 5(CH2O)106(NH3)16(H3PO4)+690O2 530CO2 + 80HNO3+5H3PO4+610H2O (9.7) Dalam hubungan reaksi karbon dioksida dimana peluruhan karbonat dan amoniak untuk menjadi nitrat diperlukan proses oksidasi, rekasi ini di sebut “nitrifikasi”. Dibawah kondisi oksit, bagi organisme dan plankton yang telah mati kelihatannya mulai rusak oleh adanya aktifitas bakteri, disaat ini tahap terjadinya susunan diagenetik. Seperti yang dikatakan oleh Bender dan Heggie (1984), kurang lebih >90% karbon organik tersebar di dasar laut akan mulai terurai oleh adanya dukungan oksigen. Dengan demikian oksigen merupakan oksidan pertama perusak bahan organik. Selama oksigen tersedia cukup walaupun redoks potensialnya rendah, kondisi ini cukup mampu membantu untuk kelancaran diagenesis berikutnya. Selanjutnya, jika oksigen terlarut kehabisan, namun dekomposisi bahan organik tetap berlangsung, halitu dikarenakan tersedianya oksidan sekunder, keadaan ini disebut “suboxic diagenesis”. Metabolime anerob, apabila kandungan oksigen menurun maka terjadilah proses metabolism anaerob, atau proses penggunaan oksigen bersumber dari oksidan sekunder yaitu: nitrat, MnO2, Fe2O3 atau FeOOH dan sulfat. Nitrat, Menurut Berner (1980) ketika kelarutan oksigen turun sampai 5%, maka nitrat menjadi penerima elektron, persamaan reaksinya seperti berikut: 5(CH2O)106(NH3)16(H3PO4)+472HNO3 276N2+ 520CO2 + 5H3PO4+886H2O (9.8a) Nitrogen oksida (N2O) diketahui umum sebagai gas rumah-kaca, dalam reaksinya di alam akan menghasilkan senyawa tertentu, dimana nitrogen organik akan membentuk senyawa amonia, proses ini disebut sebagai “denitrification”. ~ 221 ~ Persamaan reaksi oksidasi sebagai berikut: 5 NH3 + 3 HNO3 pada molekul nitrogen adalah 4N2 + 9H2O (9.8b) Reaksi oksidasi diatas memanfaatkan oksidan sekunder, produk nitrogen ini mempercepat susunan diagenesis. Dengan demikian seluruh nitrogen yang memanfaatkan nitrat sebagai oksidan sekunder, hal ini tumpa-tindi dengan MnO2, tetapi bagi nitrogen prosesnya berkaitan dengan ammonia sedang MnO2 direduksi sebelum nitrat menjadi N2 tidak membutuhkan proses oksidasi. Nampaknya oksidan sekunder yang digunakan adalah berasal Mn (IV), Fe(III) dan sulfat, dimana senyawa ini membutuhkan elektron untuk peluruhan bahan organik dengan stoichiometri “redfield”. Seperti berikut: . Oksidasi mangan (CH2O)106(NH3)16(H3PO4) + 236MnO2 + 472 H+ 236Mn2 + 106CO2 + 8N2 + H3PO4 + 336 H2O. (9.9) Oksidasi besi (CH2O)106(NH3)16(H3PO4) + 212Fe2O3 + 484 H+ 424Fe2+ + 106 CO2 + 16NH3 + H3PO4 + 530 H2O (9.10) Sulfat (CH2O)106(NH3)16(H3PO4) + 55SO4 16NH3 + H3PO4 +55S-+ H3PO4 + 530 H2O (9.11) Kalau sulfat terjadi reduksi maka methan biogenik akan terjadi dua tipe rekasi seperti berikut: CH3COOH Atau, CO2 + 8H2 CH4 + CO2 CH4 + 2H2O ~ 222 ~ (9.12a) (9.12b). Prinsip dasar proses diagenesis secara umum membutukan oksidan dari pelbagai sumber seperti susunan urutan adalah sebagai berikut: oksigen nitrat Mangan oksida oksida besi sulfat. Dengan asumsi diagenetik di sedimen laut sebagai penerima elektron adalah O2, NO3, Fe2O3 (atau FeOOH) and SO42− , dan bahan organik (komposisi di redfield) sebagai pemberi elektron serta oksidan adalah faktor pembatas untuk proses selanjutnya. Walaupun demikian tidak selamanya peleburan bahan organik akan mengikuti urutan tersebut, sebagai contoh pada reduksi sulfat tidak didahului bentuk gas methan. Oremland dan Taylor (1978) mempertegas bahwa dalam dua proses dapat terjadi secara serentak, tapi keduanya tidak saling membutuhkan. Suatu proses diagenesis di sedimen sangat tergantung pada kondisi lingkungan, dalam kaitan itu Berner (1981), menjelaskan hubungan antara lingkungan dengan diagenesis yang akan berlangsung, yakni: Lingkungan oksit, yaitu pada air-interstisial di sedimen ada oksigen terlarut dimana proses diagenesis yang terjadi dalam kondisi aerob. Melalui kondisi itu sedimen di samudera dalam hanya terdapat sedikit bahan organik, reaksi kimia yang terjadi disana seperti pada perasamaan 9.7. Hakekatnya oksigen yang tersedia itu disuplai dari hasil perombakan bahan organik yang ada atau yang terdapat di sedimennya. Lingkungan anoksit, yaitu air-interstisial di sedimen tidak mengandung oksigen, proses diagenesis yang terjadi memanfaatkan oksidan sekunder melalui metabolism anaerob. Sesungguhnya pada lingkungan anoksit dikategorikan kedalam beberapa tipe: Nir-Sulfat berada di lingkungan oksit, yaitu lingkungan yang berisikan larutan nir-sulfida, keadaan ini banyak ditemui di sedimen laut dalam, keadaan itu disebut sebagai lingkungan suboksit. Halmana proses diagenesis disedimen dalam suasana ~ 223 ~ oksit, dan oksidan diharapkan dari hasil peluruhan karbon organik di sedimen. Dalam lingkungan ini, proses pada nitrat, Mangan oksida dan besi oksida akan menggunakan oksidan sekunder, tapi susunan yang diharapkan bukan sebagai sulfat. Untuk proses reaksi kimia yang terjadi dapat dilihat pada persamaan 9.8 sampai dengan 9.10. diatas. Lingkungan sulfat, yaitu proses diagenesis, dimana sulfat di rombak menjadi senyawa H2S dan HS- melalui metabolisme oleh kerja bakteri. Sebetulnya di air-interstisial sedimen dan di air laut terkandung konsentrasi sulfat yang tinggi. Namun pada saat proses transpor bahan organik dari wilayah kontinen banyak konsentrasi sulfat tertahan di sedimen pantai, sehingga konsentrasi sulfat di laut dalam relatif sedikit. Proses diagenesis di lingkungan sulfat di sajikan pada persamaan 9.11 (lihat diatas). Sesungguhnya produk sulfat sangat penting diperhatikan, karena zat ini beracun bagi banyak organisme dan mudah bereaksi dengan logam sehingga membentuk sulfida yang sulit larut, seperti besi sulfida didalamnya termasuk FeS2 (polysulfida pyrite) dan “markasit diamorph”; Chamosit; glauconit; mangan sulfida (MnS). Lingkungan nir-sulfida methan, yaitu proses peleburan bahan organik di sedimen dengan reaksi diagenesis melalui penggunaan oksigen, mangan oksida, besi oksida dan sulfat yang proses lanjutnya akan membentuk gas methan, reaksi kimia yang terjadi seperti terlukis pada persamaan 9.12a dan 9.12b. Secara umum proses diagenetik disedimen mengunakan pelbagai oksidan dan urutannya sebagai berikut: Oksigen Nitrat Mangan oksida Besi oksida Sulfat Unsur oksigen diperlukan untuk respirasi mikroba dalam rangka proses dekomposisi bahan organik, sedang unsur nitrat, mangan, besi dan sulfat merupakan hasil reduksi bahan organik berfingsi sebagai oksidan sekunder. Kecepatan peleburan dan jumlah konsentrasinya sangat tergantung pada ~ 224 ~ ketersediaan bahan organik di sedimen, dan setiap sedimen yang terkubur dan terdeposit bisa melalui zona perjalanan seperti diurai diatas. Sudut pandang diagenetik vertikal zonasi sedimen, menurut Froelich dkk. (1979) hasil kajiannya di samudera Atlantik ekuator timur, pada sedimen hemi-pelagik suboksit akan terlihat suatu lapisan agak terang kekuning-kuningan setebal 35Cm yang berisikan sedikit karbon organik (± 0,20,5% per berat), kemudian lapisan dibawahnya adalah terigenous sedimen berwarna agak hijau kegelapan, berisikan karbon organic ± 0,5 sampai >1%. Prinsip dasar keadaan larutan di air-interstisial di sedimen diuraikan sebagai berikut: ① Kelarutan nitrat makin bertambah sampai di permukaan sedimen, dan bila terjadi pengurangan maka lapisan air-interstisial akan berwarna hijau agak kekuningan (transisi lithologikal). ② Kelarutan Mn2+ sangat lambat di permukaan tetapi akan bertambah dengan bertambahnya masuknya ke sedimen sehingga membentuk partikel/butiran, dan akan menghilang dengan makin ke poros. ③ Kelarutan Fe2+ kosentrasinya sangat sedikit sekali, tapi ketika kosentrasi nitrat mulai turun, konsentrasi besi mulai naik. ④ Kelarutan sulfat tidak ada perbedaannya di dasar perairan sampai menghilangnya di sedimen. Senyawa yang berperan dalam proses diagenesis menurut zonasi dan profil air-interstisial di sedimen suboksit dilukiskan pada gambar berikut. ~ 225 ~ Sumber: Chester dan Jickells (2012) Zona 1., Di zona ini terdapat variasi oksigen yang cukup dalam rangka peluruhan bahan organik, bentuk reaksi yang terjadi disajikan pada rumus 9.7. Dimana oleh adanya proses oksidasi pada nitrat di bahan organik akan terurai menjadi amoniak. Zona 2 dan 5., Konsentrasi nitrat di bawah maksimum dan akan naik secara linear, walaupun dizona ini tidak terjadi produksi dan di zona 5 nitrat kosong, keadan ini denitrifikasi, rekasi kimianya yang terjadi seperti pada rumus 9.8. Zona 3 dan 4., Dalam zona ini terjadi tumpah-tindi dengan zona 2 dan 5. Kalau di zona 4 oksidasi karbon organik di lakukan oleh mangan oksidasi di air-interstisial, reaksi kimianya seperti terlihat pada persamaan 9.9. Halmana Mn di reduksi ~ 226 ~ menjadi Mn2+ tapi relatif sebagai oksidasi Mn(IV). yang kemudian dikonversi sebagai MnO2 di zona 3. Zona 6 dan 7., Di daerah zona 7 oksidasi organik karbon melalui reduksi feri oksida dan hasil ini untuk konsumsi bagi daerah diatas zona 7 dan didalam zona 6. Didasarkan pada mintakad (perwilayahan) maka susunan diagenetik pada sedimen hemi-pelagik yang memanfaatkan oksidan secara berturut-turut adalah sebagai berikut: oksigen > nitrat ≅ mangan oksida > besi oksida > sulfat. Sesungguhnya penyusunan sedimen dibawah keadaan anoksit di perairan relatif kurang di dunia. Karena pada kenyataan lingkungan di dasar laut dapat terjadi oksidasi pada bahan organik di lapisan sedimen. Walaupun lingkungan sedimen sangat tertutup, tapi suplai oksigen dari badan air cukup besar dan bisa bersumber dari air-interstisial di sedimen. Oksigen yang terlarut di air-interstisial di sedimen dapat berkurang mengakibatkan kondisi anoksit sehingga berpengaruh pada proses diagenetik. Disamping itu, sesungguhnya di kolom (badan) air dapat terjadi pertukaran situasi anoksit dan oksit oleh adanya agitasi air, sehingga memungkinkan adanya suplai oksigen ke perairan, juga tengelamnya unsur karbon memberi peluang oksidatif terjadi. Menurut Muller and Mangini (1980) bahwa sedimen setebal 1-4 cm membutuhkan oksigen sebesar 103 per tahun untuk proses penyusunan sedimen. Jadi ketebalan lapisan oksit di permukaan sedimen di daerah pinggiran pantai cenderung naik, namun mendekati daerah pelagik terjadi penurunan. Suatu pernyataan Burdige (2007), katanya bahan karbon (C) organik yang ada di sedimen tersebut jumlahnya <0,25 sampai 20% dari berat kering. Sedang hasil kajian Seiter dkk. (2004) rata-rata bahan karbon organik di laut dalam (>4000 m) di permukaan sedimen (±5 cm) ada sekitar 0,5% ~ 227 ~ berat kering, tetapi di laut dangkal sebesar 1,5% berat kering. Jadi kandungan karbon organik di laut dangkal lebih banyak dari yang dikandung oleh sedimen di laut dalam. Untuk ketebalan lapisan oksit diperairan dangkal tidak melebihi 1 cm, sedang dilaut dalam ditemui ada sekitar 20 cm (Soetart dkk. 1996). Samudera Pasifik bagian timur ketebalan lapisan oksit di sedimen ditemui sangat bervariasi (Lyle, 1983). Lapisan oksit di suatu sedimen berpengaruh langsung pada proses diagenetik, sebab kandung oksigen sangat membantu pada percepatan reaksi. Kalau keadaan ada dalam pada situasi oksit, artinya terjadi pertukaran oksigen halitu menunjukan potensi redoks positif, tapi jika terjadi penurunan oksigen, kondisi ada pada anoksit, artinya potensi redoks negatif. Apabila di sedimen terjadi oksidasi indikasinya, warna sedimen ada pada coklat-kemerahan, tapi bila oksigen kurang warna sedimen akan berwarna abu-abu ke hijauan. Hubungan kecepatan redoks di sedimen laut dengan ketebalan lapisan oksit di permukaan sedimen adalah sebagai berikut: Sedimen anoksit, umumnya terdapat di kawasan pantai atau daerah yang terisiolasi dan diselokan/kubangan didasar laut, dimana sedimennya terdapat kandungan organik karbon sebesar 10%. Sedimen dekat pantai, biasanya lapisan oksit tidak melebihi beberapa sentimeter, dan lapisannya berwarna coklat. Sedimen ini berisi 5% organik karbon, tapi akumulasi sedimen di daerah ini relatif lebih cepat. Sedimen “hemi-pelagik”, kecepatan deposit relatif agak berkurang dibandingankan dengan sedimen di pantai, sedimennya berisi organik karbon sebesar 2%, dan ketebalan lapisan oksit hanya beberapa sentimeter saja. Sediment pelagik, Kecepatan penyusunan sedimen ini lambat mengandung organik karbon sebesar 0,5%, tapi ada di beberapa tempat di perairan laut dunia ditemui hanya 0,1 – ~ 228 ~ 0,2% (Burdige, 2007). Di sedimen pelagik ini ditemui lapisan oksit pada kedalaman 1 m sampai mendekati 10 meter. Suatu hal yang menjadi perhatian bahwa diagenesis awal di sedimen laut adalah susunan mintakad (zona) vertikal, dimana secara lateral susunan zona diagenetik di samudera adalah sebagai berikut: dekat pantai hemi-pelagik pelagik. Dalam proses diagenetik kandungan bahan organik di sedimen merupakan faktor penting untuk di determinasi (perhatikan), karena bahan organik itu berperan aktif sebagai faktor penentu pada besaran distribusi, penghambatan dan pengendapan di sedimen, secara khusus akan diuraikan sebagai berikut. Bahan organik di sedimen adalah suatu hal yang sangat penting, tidak hanya sebagai sumber siklus karbon global di laut, tapi merupakan penggerak diagenesis awal serta bahan organik itu berperan penting dalam perputaran kimia di laut. Bertolak dari kajian Burdige (2007), secara global bahan organik yang mengendap atau terkubur di laut disajikan pada table 9.2 berikut ini. Tabel 9.2. Karbon Organik yang terendap di Laut Kedalaman Area Laut (%) Karbon organik (Km) Terendap (% dalam kelompok) 0 – 0,2 7 152 (50%) 0,2 – 2 9 96 (31%) >2 84 61 (21%) Sumber: Burdige (2007). Sedimen di pantai jumlah bahan organik relatif kurang, karena di daerah ini banyak ditemui partikel pasir. Namun demikian ada sejumlah bakteri dapat menguraikan bahan ~ 229 ~ organik yang berasosiasi dengan partikel pasir sehingga kawasan ini relatif oksit. Bertolak dari table 9.2 terlihat bahan organik didominasi di perairan dangkal khususnya di delta, tetapi di perairan terbuka pada kedalaman >2km karbon organik yang terlarut dan mengendap ada sebesar 21% . Sedang menurut Lampitt dan Antia (1997) bahwa aliran bahan organik di perairan 2000 meter diduga sebesar 340 X 1012 gC/tahun (lihat table berikut). Tabel. 9.3. Estimasi Aliaran Karbon di Laut. Aliran Gross Ton Karbon/Thn Produktivitas primer di laut 36 Produksi dari eupotik zona 4,5 Ada disedimen kedalaman 0,34 2000 m. Sumber : Lampitt dan Antia (1997). Jadi kurang lebih 20% karbon akan mengendap di laut sebagai sedimen, tetapi bahan organik yang mengendap diperairan laut dalam (4km) di sebagian besar (±63%) samudera di dunia jumlah karbon yang ditemui adalah <5%. Kehadiran partikel organik sebagaimana yang diuraikan di bab 4, material itu bersumber dari daratan, permukaan laut dan antropogenik. Dimana material bahan organik dari atmosfer dan aliran sungai ada sejumlah 216 sampai 180 X 1012 per tahun, sedang dari laut itu sendiri sebagai hasil fotosintesis hanya 1% bahan organik. Bahan organik berasal dari luar laut umumnya agak sulit terdegradasi jika di bandingkan dengan hasil fotosintesa, bahkan ada juga tidak bisa terdegradsi. Misalnya, lignin dan beberapa komponen phenol yang dihantar oleh sungai masuk kedalam laut. Komponen phenol dan lignin berasal dari bahan-bahan, seperti tumbuhan, kayu olahan manusia dan plastik-plastik hitam yang mengandung karbon harus melalui ~ 230 ~ proses peluruhan oleh bakteri. Hampir semua partikel-partikel organik itu mengendap (terkubur) dekat di daerah kontinen, khusus terendap di daerah delta akan masuk ke laut sebagai sedimen di dasar laut diperkirakan ada sekitar >10%. Bahan organik yang masuk ke laut sebagai bahan timbunan sedimen merupakan hal yang menarik perhatian, sebab bahan-bahan itu yang akan melakukan proses diagenesis. Hakekatnya sedimen dilaut yang diketahui umum, ada dua kategori yaitu sedimen dekat pantai dan sedimen di laut dalam, keduanya memiliki sifat dan karakter berbeda dalam penyusunan sedimen. Sedimen dekat pantai, materialnya berasal dari daerah pantai dan bahan organik hasil fotosintesa. Kalau sedimen dekat pantai biasanya akumulasi deposit sangat cepat terjadi, dan kandungan bahan organik yang dikandungnya kurang lebih 1-5%. Sebagian bahan organik ini akan mengakibatkan daerah anoksit, tapi ada sebagian organik di manfaatkan untuk kebutuhan fotosintesis, misal, Calvert dan Price (1970) melaporkan di Namibian shelf kaya akan lumpur diatom dan bahan organik yang dikandung ada diatas 25%. Daerah ini ditemui cukup tersedia unsur oksigen. Sedimen di laut dalam, materialnya lebih banyak dari atmosfer, hasil fotosintesis dan unsur logam dari kerak samudera, umumnya sedimen ini kurang bahan organik diperkirakan ada sebesar 0,5% (Seiter dkk., 2004). Bahan-bahan organik sebagian besar berasal dari air hujan masuk ke laut dan proses penengelaman bahan organiknya agak lambat yaitu <1% di laut terbuka, tapi kalau bersumber dari delta deposit yang terbentuk agak cepat yaitu >50%. Bahan-bahan organik yang terakumulasi ini walaupun relatif kurang namun proses diagenetik akan berjalan sempurna. Intinya, bahan organik yang tersimpan di sedimen terdiri dari molekul asam amino (termasuk protein) karbohidrat dan lipida termasuk lignin (karbohidrat plus). ~ 231 ~ Namun demikian bahan organik berasal dari fitoplankton yang tenggelam menjadi sedimen cukup banyak di laut. Secara umum bahan organik akan masuk ke dalam proses diagenesis awal membentuk “karogen” dalam wujud amorphous (amorf) yang mengandung konsentrasi hidrokarbon dengan berat molekul tinggi dan sangat kental. Semua bahan organik akan terkubur di sedimen laut dalam (>1 km) biasanya proses itu melibatkan reaksi kimiawi, jika suhu naik akan mengalami proses peleburan. Untuk proses diagenesis, katagenesis dan metagenesis, dilukiskan dalam gambar 9.3. Metagenesis Katagenesis Diagenesis Organisme hidup Karbohidrat Lignin Protein Molekul Lainnya Mikroba , degradasi Polimerisasi kondensasi Sedimen baru terbentuk Zona berbentuk minyak Zona berbentuk Gas Rangka karbon Asam FulviK Asam Humik Humin Kerogen Degradasi Termal Lipida Fosil Geokimia Molekul terikat Hidrokarbon BM rendah Dan sedang Retakan Retak Minyak mentah Hidrokarbon BM Tinggi Methan Hidrokarbon Gas Residu karbon Gambar 9.3. Bahan Organik di Sedimen Pada Tahap Diagenesis, Katagenesis dan Metagenesis Sumber : Tissot dan Welte ( 1984) disitir oleh Chester dan Jickells (2012) Gambar diatas terlihat, pada fase diagenesis terjadi pada kedalam dibawah 1000 meter, sedang katagenesis di kedalaman beberapa kilometer, di daerah itu biasanya suhu naik dan tekanan naik, kemudian lanjut ke fase metagenesis atau “metamorfis” (Tissot dan Welte, 1984). ~ 232 ~ Hakekatnya, variasi karbon organik bersumber dari pelbagai jaringan dengan pelbagai ukuran yang masuk ke laut akan tenggelam dan menyusun lapisan sedimen, dimana sebagian menjadi makanan organisme bentik dan sebagian akan masuk kedalam siklus oksigen dan karbon global. Dengan demikian terkuburnya bahan organik di laut merupakan suatu hal yang menarik untuk diteliti, karena dalam proses penyusunan dan peluruhannya akan berhubungan dengan reaksi kimiawi. Menurut Burdige (2007) dalam proses “biodegradable” ada tiga proses yang memegang peran penting, yakni: (1) Peluruhan bahan organik menghasilkan produk berbagai karakter material; (2) Adanya bakteri peluruhan dari fraksi material itu dapat terjadi dan ke (3) secara fisikal peluruhan bahan organik itu bisa terganjal akibat substrat inorganik dan atau organik. Pengikatan bahan organik di permukaan, partikel lempung bisa menghalangi proses peluruhan, atau dapat juga partikel itu menghalangi kerja bakteri atau enzim yang ada didalam bahan organik itu (Hedges dan Keil, 1995; Lee dkk, 2004). Artinya adanya pertukaran karakter kimia yang ada di permukaan lempung itu bisa menganjal proses peluruhan. Konsentrasi oksigen sangat berarti bagi proses peluruhan di sedimen, karena umumnya sedimen di laut dalam, lingkungannya adalah anoksit, misalnya di laut hitam. Berbicara konsentrasi oksigen di dasar laut sama halnya berbicara organik karbon di sedimen, sebab untuk menghancurkan bahan organik itu diperlukan sejumlah oksigen. Ketersediaan oksigen di lingkungan sedimen sematamata hanya dipergunakan peluruhan bahan organik, halmana bahan organik menerima elektron sehingga proses diagenesis berlangsung. Intinya, peluruhan bahan organik di bawah kondisi oksit dan anoksit, kecepatannya berbeda. Apabila kondisi anoksit atau kurang oksigen bahan organik sulit terurai (Middleburg and Levin, 2009). ~ 233 ~ Menyangkut kandungan oksigen di sedimen, menurut Burdige (2007), bahwa ada dua faktor yang berperan di dalam bahan organik yang terendap, yaitu pertama, ketersediaan oksigen di dalam bahan organik itu.; kedua, adanya redoks di lingkungan yang akan mempercepat peluruhan bahan organik. Inti dari diagenesis yang terjadi dialam adalah sebagai berikut: ① Diagenesis awal di sedimen laut prinsipnya melalui suatu seri penggunaan oksidan untuk keperluan peleburan karbon organik seperti berikut: Oksigen nitrat MgO2 besi oksida sulfat Dari uraian diatas terlihat bahwa konsumsi oksigen di laut merupakan indikator siklus biogeokimia secara global. Oleh karenanya unsur oksigen punya arti penting dalam proses biogeokimia di laut. Halmana oksigen bisa didapatkan lewat proses fotosintesis dari tumbuhan termasuk fitoplankton dan difusi langsung dari atmosfer (lihat bahasan di bab 7). Dalam proses denitrifikasi membutuhkan oksigen yang cukup, dimana beberapa peneliti menggemukakan bahwa di laut lebih-kurang 60% hilang karena digunakan pada denitrifikasi dan aktifitas biologi lainnya, dan yang tertinggal di badan air hanya 30% (oksigen kurang) sedang ada di dalam bahan organik yang terkubur sebanyak 10%. ② Proses diagenetik melalui oksidan akan berjalan sempurna, karena oksigen factor utama penggerak lajunya diagenesis. ③ Banyak bahan organik masuk mengikut pelbagai aliran, secara ilustrasi dilukiskan pada gambar 9.4. dimana karbon organik sebelum terendap di laut umumnya akan melewati daerah kontinen dan delta. Pemasukan bahan organik bersumber dari atmosfer (lewat hujan) atau di hantar ~ 234 ~ oleh arus, aliran sungai ke laut, dan terjadi endapan di dasar laut dalam, merupakan diagenetik bersifat vertikal. ④ Proses diagenesis sangat tergantung pada jumlah bahan organik yang tersedia di permukaan sedimen. Secara umum pengurangan oksigen dan bahan organik dimulai dari pinggiran kontinen ke samudera terbuka, artinya proses diagenetik yang terjadi adalah bersifat lateral. Dengan proses ini berakibat secara perlahan akan terjadi: (1) sedimen Lembah anoksit Zona produktivitas tinggi Dataran Abysal Pelagik Gambar 9.4. Ilustrasi Proses Terendap Bahan Organik di Laut Sumber Hedges and Keil (1995) disitasi oleh Chester dan Jickells (2012). dekat pantai lingkungannya ada lapisan anoksit, dan lapisan itu akan terus ke laut sampai pada beberapa millimeter dipermukaan sedimen adalah lapisan anoksit. (2) sedimen dekat pantai hanya sedikit lapisan oksitnya. (3) sedimen hemipelagik di laut dalam hanya memiliki sedikt lapisan oksit yang diperoleh dari hasil reduksi nitrat, mangan oksida dan besi oksida. (4) sesungguhnya pelagik sedimen di laut dalam tidak terjadi proses diagenesis, sebab oksigen yang ada ~ 235 ~ digunakan untuk peluruhan organik karbon yang ada dipermukaan sedimen. Jadi sedimen banyak mengandung batu (shelf) dan di bagian miring, halmana bahan organik disitu akan terhambat proses diagenetiknya karena akibat pengikatan material yang ada di permukaan sedimen. Prinsip dasar, semua bahan organik yang masuk dari pelbagai aliran (seperti terlihat di gambar 9.4), akan berubah bentuk fisiknya menjadi larutan, yang kemudian larutan ini melalui air-interstisial atau secara bersama-sama akan membentuk komposisi mineral di sedimen. Dengan demikian fraksi elemen yang ada di badan air maupun yang terkandung di air-interstisial akan digunakan untuk mempercepat proses diagenesis sehingga jumlah elemen yang ada di bahan organik maupun di badan air akan habis. Mekanisme masuknya air-interstisial ke laut diuraikan sebagai berikut. bahan organik itu berasal dari daerah pelagik jatuh kedasar (vertikal), selama proses berlangsung partikel makin berkurang karena telah terjadi suatu reaksi kimia antar airlaut dan elemen yang ada di bahan organik itu. Akhirnya bahan-bahan itu akan ke dasar perairan. Bahan organik yang ada di atas sedimen laut dengan ketebalan kurang lebih > 10 sentimeter akan terurai oleh adanya oksigen, proses ini disebut awal diagenesis, bila proses ini berjalan terus maka bahan organik tersebut akan terendap, bertambahnya waktu lapisan itu akan mengeras membentuk pebantuan sedimen. Disaat diagenetik awal proses berlangsung, kimia yang ada di air-interstisiaal berperan penting bersama-sama sejumlah komponen kimia dalam siklusnya di badan air. Komponen kimia tersebut adalah: (a) bioaktif atau labile dari elemen C, N, P bersama Ca (kalsium karbonat) dan Si (opal). Komponen kimia tersebut relatif sedikit jumlahnya yang akan mengendap di sedimen laut, karena ada sebagian jumlahnya akan melakukan siklus alamiah. (b) Sesungguhnya oksidan yang digunakan untuk menghancurkan bahan organik adalah oksigen, nitrat, Mn dan FeO2 serta sulfat. Konsumsi nitrat dan ~ 236 ~ sulfat di sedimen biasanya melalui suatu siklus biogeokimia yang menggunakan ion dari komponen itu.(c) Logam kecil, dalam proses peleburan bahan organik dengan menggunakan oksidan biasanya ditopang dengan sejumlah logam kecil (trace) yang ada di air-interstisial serta komponen kimia lainnya dibadan air, saat bahan itu di transpor ke dasar perairan, misalnya mangan oksida. Asosiasi antar logam dengan bahan elemen-elemen tersebut untuk peleburan bahan organik, secara umum disebut recycling. (d) Dalam proses diagenesis awal berlangsung, ada beberapa elemen yang agak sulit dilebur, seperti Na, K dan Mg. Elemen-elemen ini akan berinetraksi dengan mineral aluminosilikat dalam siklus biogeokimia yang akhirnya akan tenggelam ke dasar lautan. Penyusunan elemen di air-interstisial secara garis besar mekanismenya ada hubungan dengan faktor: ① masuknya larutan berasal dari air laut ② Proses pemindahan ke dalam sedimen melalui difusi ③ reaksi yang terjadi antara air laut dengan batuan vulkanis yang padat (baslt), dimana bisa berlangsung pada suhu tinggi maupun rendah. ④ proses reaksi berlangsung di dalam sedimen ⑤ reaksi yang terjadi antar sedimen dan air laut. Intinya, penyusunan elemen yang dikandung oleh airinterstisial, semuanya elemen berasal dari air laut dan masuk ke sedimen secara difusi, konsentrasi bervariasi halitu sangat tergantung pada milieu dari sedimen itu. Proses difusi air laut beserta beberapa komponen ke sedimen, secara matematis agak sulit di hitung. Tapi dengan melihat pengembangan model reaksi yang berlangsung di sedimen maka dugaan besaran dapat dideteksi. Untuk mengetahui sifat reaksi dari beberapa kimia yang ada di air- ~ 237 ~ interstisial dalam sedimen, secara ilustrasi diuraikan sebagai berikut. Perubahan komposisi kimia di dalam air-interstisial lebih banyak pengaruhnya bahan organik yang masuk secara vertikal dari pada horizontal, walaupun demikian proses diagenetik yang berlangsung adalah sama. Intinya, airinterstisial masuk ke sedimen akibat dari pemanasan sehingga berubah menjadi larutan, kemudian oleh adanya tekanan akan merembes ke sedimen (transport secara fisikal) atau dapat pula dengan proses difusi. Hakekatnya, masuknya melalui transpor fisikal dan difusi akan menaikan konsentrasi atau potensi kimia akan bertambah. Secara matematis difusi suatu larutan akan mengikuti persamaan hukum Fick adalah sebagai berikut: Pertama, (9.13) Kedua, (9.14) Dimana J= difusi komponen; i= massa/area/waktu; c= konsentrasi massa dalam volume. Sedang D= koefisien difusi massa per luas/waktu, dan x adalah kenaikan massa maksimum. Rumus pertama Fick digunakan untuk perhitungan pada sistem aliran tetap tapi rumus kedua, digunakan pada kondisi dimana aliran difusi tidak tetap. Sebelum menggunakan persamaan Fick perlu diketahui jumlah sedimen, air-interstisial dan air laut. Caranya, keluarkan air-interstisial dari sedimen sehingga bisa dihitung besaran difusi air-interstisial dengan hukum Fick. Material padat yang terpisah dengan air adalah merupakan efek porosity. Rasio antara panjang difusi yang berliku-liku dengan difusi yang sifat lurus di sebut tortuosity (θ) (Berner, 1980). Umumnya tortuosity digunakan untuk mengukur perubahan ~ 238 ~ listrik di sedimen dan air-interstisial di sedimen. Untuk melihat hubungan antar sedimen dan air-interstisial dilukiskan rumus sebagai berikut: (9.15) Dimana ϕ adalah porosity dan F adalah faktor pembentukan (F = R/R0, halamana R= daya elektrik di sedimen; Ro= daya air-interstisial). Faktor pembentuk sedimen di laut biasanya sekitar 1 – 10, sedang effective diffusion coefficient (D’) sedimen melebihi dari larutannya, yakni >10. Untuk menghitung koefisien efektif dari difusi dapat digunakan dengan rumus sebagai berikut: (9.16) Dimana D adalah koefisien difusi dalam larutan, ϕ adalah porosity dan Θ = tortuosity. Untuk menghitung difusi komponen di sedimen, Gieskes (1983) membuat rumusan reaksi kimianya, dengan anggapan transpor bahan secara vertikal melalui airinterstisial, maka aliran kimia yang terjadi dapat hitung menggunakan rumus sebagai berikut: (9.17) Dimana Jb adalah massa aliran, p = porosity , Z = kedalaman dalam cm, u adalah kecepatan relatif air-interstisial ke sedimen dalam cmb s− 1 ( kecepatan adveksi), C adalah ~ 239 ~ konsentrasi massa dalam mol cmp−3 dan Db koefisien difusi ke sedeimen. Untuk kesetimbangan larutan adalah sebagai berikut: (9.18) Dimana R adalah kimia yang masuk dengan kecepatan reaksi mol cmb−3S −1. Jika densitas air-interstisial dan padatan tidak terjadi perubahan, maka diberikan rumusan berikut: (9.19) Apabila di hubungan dengan rumus (9.18), maka terbentuklah persamaan berikut: (9.20) Dan ketika tetap stabil atau tidak terjadi peubahan, maka terjadilah persamaan: (9.21) Menurut Gieskes (1983), jika kecepatan sedimentasi dan fluktuasi suhu tetap selama 10-12 menit dengan asumsi permukaan sedimen tetap stabil, maka kecepatan akumulasi 20 meter per satu menit. Gieskes melukiskan keadaan konsentrasi dihubungkan dengan keadalaman di ilustrasikan pada gambar berikut. ~ 240 ~ Gambar 9.5. Profil Konsentrasi larutan Kalsium di air- interstisial menurut Kedalamannya (Data yang diperoleh lewat pengeboran ke bagian dasar lautan) . Didasarkan pada gambar diatas kelarutan kalsium (Ca) di air-interstisial akan berpengaruh pada tiga peubah (variabel) yaitu: difusi (Db), kecepatan rekasi (R), dan adveksi (u), jadi untuk dugaan tentang difusi-adveksi dan reaksi di dalam grafik itu dapat dijelaskan sebagai berikut: Kasus pertama, terhadap kecepatan difusi adalah R = 0, Db = f(z) dan u = 0,artinya tidak terjadi reaksi dan adveksi. Dengan demikian difusi (Db) terjadi penurunan dengan bertambahnya kedalaman, dalam gambar terlihat grafik naik. Kasus kedua, tentang kecepatan reaksi, dimana R ≠0, Db adalah tetap dan u = 0. Kondisi ini menunjukan kalsium mulai keluar dari larutan, jadi sumber kalsium disekitarnya makin sedikit jumlahnya. ~ 241 ~ Kasus ketiga, tentang kecepatan adveksi adalah nol (R = 0), Db adalah tetap dan u ≠ 0. Keadaan ini memperlihatkan tidak terjadi reaksi dan koefisien difusi tetap, dalam gambar terlihat kurva adveksi relatif naik. Pernyataan Gieskes (1983) terhadap profil konsentrasi dan kedalaman Ca dan Mg di air-interstisial adalah sebagai berikut: Pertama tentang hubungan linear antara ΔCa dan ΔMg, dimana R = 0. Bertolak dari persamaan 9.21, dengan asumsi R = 0 maka profil Ca dan Mg komponen ini akan masuk secara konservatif, yakni masuk melalui air-interstisial dengan tidak terjadi reaksi. Dengan demikian keadaan disekitar sedimen adalah batuan kecil vulkanik dan air laut itu sendiri yang masuk. Kedua, hubungan non-linear antara ΔCa dan ΔMg, terjadi reaksi di sedimen yaitu R ≠ 0, pada kondisi ini persamaan 9.21 menghitung konsentrasinya harus gunakan geometri. Sesungguhnya proses diagenesis bahan organik (C,N dan P) di sedimen telah melebar jauh sehingga melibatkan unsur non biogenik di poros serta beberapa elemen yang hanya bisa terurai oleh adanya cahaya matahari, seperti Na+, K+ and Mg2+ serta silika. Pelbagai riset telah dilakukan, ternyata komposisi kimia di sedimen cukup banyak elemen yang tersusun bahkan sampai pelbagai bahan dari vulkanik. Salah satu hasil penelitian Sayles (1979), yang dilakukan di Samudera Atlantik bagian utara dan selatan ternyata ditemui senyawa kimia sebagai berikut: 1) Pada air-interstisial kaya akan Na+, Ca2+ and HCO3-, tetapi di air laut kandungan K+ dan Mg2+ menurun. Namun di beberapa titik sampling terlihat kandungan SO42− agak tinggi, halitu barangkali ada peran sulfat sebagai penerima elektron dalam oksidasi bahan organic. 2) Proses pengurangan dan pengkayaan elemen terlihat sangat bervariasi, misalnya elemen Na+ relatif ~ 242 ~ sedikit walaupun ada peningkatan di antara air dengan bertambahnya kedalaman, sebaliknya pada sedimen dengan ketebalan 15-30 cm, konsentrasi kation utama di air-interstisial menurun sangat drastik. 3) Hakekatnya kandungan Mg2+, K+, Ca2+ dan HCO3tergantung dari kondisi geografis, dimana airinterstisial di sedimen dekat pantai relatif tinggi tetapi di laut dalam rendah. Hal ini dikarenakan pada air-interstisial disedimen pada perairan dengan kedalaman sekitar 1-2 m umumnya kaya akan unsur kalsium, natrium dan bikarbonat, tapi unsur kalium dan magnesium telah habis. Terjadi pengurangan elemen K+ karena telah berasosiasi dengan mineral yang ada di lempung, seperti apa yang dikemukakan oleh Mackenzie dan Kump (1995) bahwa dalam air interstisial di laut dalam, umumnya kandungan kalsium memperlihatkan kecenderungan naik, sebaliknya elemen magnesium menurun. Dimana secara teoritis bahwa: pertama, pembentukan dolomit membutuhkan unsur magnesium kalsit yang diambil dari shell yang mengandung karbonat; kedua, serapan elemen magnesium pada fase opal, akan menurunkan kandungan magnesium di airinterstisial sedimen yang mengandung silika. Selain ada perubahan elemen magnesium dan kalsium, juga sering terjadi penurunan nilai δ18 O di air-interstisial. Menurut Lawrence dkk (1975) reaksi karbonat pada diagenesis opal agak sulit dijelaskan, namun intinya nilai-nilai δ18 O merupakan hasil reaksi dari batuan vulkanik di bawah tanah atau yang tersebar di sedimen. Hasil temuan Gieskes (1983) tentang profil beberapa unsur kimia yang berasal dari bahan vulkanik terdapat dalam disedimen dilukiskan pada gambar berikut. ~ 243 ~ Alkalinitas K e d a l a m a n (M) Sulfat (mM) Strontium (mM) Kalium (mM) Kalsium dan Magnesium (mM) Silika (mM) Gambar 9.6. Profil Beberapa Elemen Kimia di Airinterstisial didasarkan pada Kedalamannya. (Data di dapatkan lewat pengeboran/drilling: dimana lapisan pertama berwarna coklat berisi lumpur terigen dan lempung; kedua lempung pelagik, abu, siliceous; ketiga, lumpur berbatu, lempung berbatu, lumpur berbatu, calcareous, dan pasir berbatu; empat, lempung calcareous berbatu, glauconite, lumpurbatu; dan ke lima, lumpur butiran vulanik dan ada rembesan air. Sumber: Gieskes (1983). Bertolak pada gambar diatas proses geokimia yang terjadi dapat di uraikan sebagai berikut: (1) Kosentrasi maksimum strontium merupakan rekristalisasi karbonat pada cairan nanofossil (nanofossil ooze), umumnya pada fase ini dimulainya pembentukan mineral baru; ~ 244 ~ (2) Konsentrasi kalium menurun dengan bertambah kedalaman, hal itu mengindikasi adanya pengikatan elemen kalium oleh pembentukan tanah liat (lempung); (3) Profil sulfat menunjukkan penurunan dengan kedalaman, menunjukkan bahwa telah terjadi reduksi sulfat dalam kolom sedimen; (4) Profil kalsium dan magnesium diinterpretasikan sebagai proses tenggelamnya kandungan Mg dengan bertambah kedalaman, dan telah berintegrasi dengan kalsium dan butiran vulkanik lainnya, meskipun dalam profil lain memperlihatkan adanya penambahan ion di sedimen dan di butiran vulkanik didasar lautan. Air-interstisial memiliki peran utama dalam proses diagenetik bahan-bahan organik di sedimen yang dibantu oleh elemen oksigen. Pelbagai uraian diatas dapat disimpulkan sebagai berikut: 1. Air-interstitial di sedimen laut sesungguhnya berasal dari air laut, masuknya melalui beberapa cara, seperti difusi, fisik akibat tekanan dan perbedaan suhu. 2. Kondisi eksternal dari air-interstisial di sedimen dipengaruhi oleh lingkungan di dasar perairan dan kolom air di atasnya. 3. Reaksi yang berlangsung di sedimen- air interstisial biasanya sangat dipengaruhi oleh keberadaan komposisi kimia yang ada di badan air, intinya pemindahan unsure-unsur itu mengikuti kaidah dari konsentrasi tinggi ke konsentrasi rendah. 4. Reaksi yang berlangsung pada air-interstisial paling intens biasanya di kedalaman 30-50 cm di atas kolom sedimen. 5. Kecepatan difusi ke sedimen sangat tergantung pada bahan-bahan yang tenggelam membentuk sedimen, dan lingkungan awal sedimen didasar perairan. ~ 245 ~ 6. Bahan-bahan yang masuk ke sedimen dengan pelbagai elemen yang terkandung dikenal ada dua sifat alirannya, yaitu aliran primer, umumnya material berasal dari vulkanik atau disebut “hidrotermal” terlarut di perairan serta mengendap di dasar perairan berinteraksi dengan elemen yang tersedia di alam, masuk ke air-interstisial. Selanjutnya aliran sekunder, melalui bahan-bahan organik dari pelbagai sumber masuk ke dalam airinterstisial di sedimen. Misalnya bahan-bahan yang dialirkan oleh sungai, berasal dari atmosfer, semuanya akan diurai di badan air bahkan terendap di dasar perairan, hasil peleburan itu bersifat amorf masuk ke sedimen sebagai air-interstisial. Sehingga Bruland (1983) mengatakan bahwa elemen-elemen itu sebagai tambahan bagi proses diagenetik. Berbagai reaksi kimia yang sangat kompleks yang terjadi di sedimen, air-interstisial maupun di antara muka sedimen dan air laut berpotensi membentuk komposisi kimia di cadangan sedimen (yang telah terendap di dasar). Reaksi kimianya telah di uraikan diatas, dan untuk model diagenesis mangan di sedimen laut disajikan bahasan berikut. Burdige dan Gieskes (1983) mengatakan model kualitatif diagenetik mangan (Mn) di pori-pori mengikuti model persamaan berikut: (9.22) (9.23) Dimana, Db adalah koefisien difusi sedimen, Cp adalah konsentrasi Mn di pori-pori air, Cs adalah konsentrasi Mn ~ 246 ~ dalam fase padat, w adalah tingkat sedimentasi, φ adalah porositas dan R (z) adalah ekspresi tingkat baik untuk oksidasi atau pengurangan. Istilah φ / (1 × φ), melukiskan cm3 porewater / cm3 sedimen , nilai ini digunakan untuk mengkonversi konsentrasi Mn antara fase padat dan cair. Sehubungan dengan model Mn ini dengan asumsi bahwa proses diagenetik yang terjadi ada sebagi berikut: 1. Diagenesis “Steady-state” yang berlangsung. 2. Vertikal gradien jauh lebih penting daripada gradien horisontal sering gradient horizontal diabaikan. Air Laut Antarmuka air-sedimen Zona Oksidasi Zona oksidasi Mn Reaksi Redoks Zona Reduksi Mn Zona Keseimbangan Gambar 9.7. Model zona Diagenetik Mn. 3. 4. 5. 6. Sumber : Burdige and Gieskes (1983) Difusi di “porewater” terjadi melalui proses molekuler, yaitu difusinya mengikuti hukum Fick. Porositas dan koefisien difusi konstan dengan kedalaman. Sifat adveksi konstan sampai pada tingkat sedimentasi. Umumnya fase padat dapat diabaikan ~ 247 ~ 7. Bertambah waktu pasokan Mn ke permukaan sedimen tetap konstan 2+ 8. Serapan Mn dapat diabaikan 9. Di zona reduksi Mn oksigen sangat terbatas sehingga biodegradasi diabaikan. Realita reaksi yang terjadi di alam memperlihatkan bahwa peubah (variabel) Db berbeda tentang difusi ion bebas di air laut, karena efek “tortuosity” pada partikel di sedimen. Berkaitan dengan itu, maka persamaan berikut menjelaskan prosesnya: (9.24) Dimana F adalah 'faktor pembentukan ', yang diukur sebagai persentase resivitasi sedimen dengan resistivitas di pori-air (porewater). Berdasarkan pada persamaan 9.23 dan 9.24 dimana R(x) itu menunjukan ekspresi pada tingkat oksidasi maupun reduksi. Dengan adanya luas permukaan cukup, maka pengendapan Mn dan oksidasi merupakan suatu proses pseudo-orde pertama, sehingga, (9.25) Untuk mengambarkan bagaimana oksidasi yang terjadi pada kondisi ini, dengan asumsi bahwa reaksi yang terjadi adalah hidro oksida (MnOx). Oleh karenanya mekanisme pengurangan Mn akan sebanding dengan jumlah Mn di bahan padat yang tersedia (dugaan yang terjadi adalah hidro-oksida), dengan demikian, Rred (z) dapat dinyatakan sebagai (9.26) Apabila di gabungkan rumus pada 9.22 dan 9.23 maka di peroleh persamaan berikut: Pertama, untuk zona oksidasi (L1 ≤ z ≤ L2), ~ 248 ~ (9.27) (9.28) Kedua, untuk zona reduksi (L2 ≤ z ≤ L3), (9.29) (9.30) Dari persamaan pada keadaan di zona oksidasi dan reduksi, secara ringkas persamannya adalah sebagai berikut: (9.31) (9.32) (9.33) (9.34) Dimana, (9.35) Halamana dengan suatu asumsi, jika 4Dbkox > w2, adveksi pada “porewater” tidak berpengaruh pada difusi, maka : ~ 249 ~ = Kred/W Lox = L2 – L1 (9.36) (9.37) Wn, Wt% K e d a l a m a n (cm) (A) Gambar 9.8. Model Diagenesis Mangan di Sedimen Laut Grafik (A), garis yang terputus-putus (titik-titik) adalah “porewater”, sedang garis normal adalah fase padat. Sumber : (Burdige dan Gieskes, 1983). Grafik diatas merupakan hasil analisis dengan menggunakan persamaan 9.31 dan 9.39, dimana: Db = 71,6 3 -3 cm2/tahun; w = 3 cm 10 /Tahun; φ = 0,8; ρ-sedimen = 2,6 cm ; L1 = 20 cm; L2 = 30 cm; Cos = 0,1% berat; Kox = 5 per tahun dan Kred = 1.50 × 10-3/Tahun. ~ 250 ~ Konsentrasi Mangan Kedalaman (B) Gambar 9.9. Model Diagenesisi Mn di sedimen Laut Menurut Froelich dkk, (1979) (Grafik B) (9.37) (9.38) (9.39) ~ 251 ~ Perhitungan aktual menggunakan dua peubah (Kox dan Kred) dimasukan kedalam persamaan maka hasilnya model diagenesis Mn baik larutan maupun padatan terlihat pada gambar 9.8 (grafik A). Sedang grafik (B) adalah model diagenesis Mn yang dilukiskan oleh Froelich dkk, (1979). Migrasi Mn pasca-pengendapan dikaitkan dengan model adalah sebagai berikut: Sedimen terkubur dalam kondisi di bawah batas redoks, padat Mn oksida akan direduksi menjadi Mn2+, selama proses oksidasi dan pengendapan. Kemudian sedimentasi berlangsung terus terjadi pengendapan di zona oksidasi yang akhirnya akan masuk ke wilayah redoks dan Mn terperangkap di zona sempit di batas redoks (lihat gambar 9.7). . ~ 252 ~ ⑩ BIOMINERALISASI B iomineralisasi berkaitan dengan mineral yang ada di jaringan organisme seperti rangka (tulang, gigi dan kulit) serta cangkang yang hidup maupun terdeposit (fosil) sebagai sedimen di dasar laut, dari jaringan itu merupakan sumber pembentukan mineral di laut. Banyak organisme hidup sebagai pembentuk mineral, produk mineral itu disebut mineral biogenik atau “biomineral” yang tersusun dari material berisikan matriks organik yang sangat kecil ukurannya (nano atau mikro) atau sering disebut kristalin mineral. Mekanisme biomineral dalam organisme, seperti mineral kalsium, silika dan fosfat, serta trace elemen seperti Fe, Na+,Mg2+ dan juga kalium di tulang dan kulit diatom yang mengalami nukleasi masuk ke dalam pori-pori di dalam seratserat kolagen. Nukleasi dikatalisasi oleh adanya grup ester fosfat dan grup karboksilat (Duda dan Pajak, 2004). Pertumbuhan atau mineralisasi terjadi diseluruh serat kolagen dan atau menghubungkan serat-serat kolagen satu sama lain membentuk apatit tulang atau rangka organisme; apatit tulang atau rangka ini dikenal dengan hidroksiapatit biologik. Disamping gugus karbonat (CO32+), terdapat gugus fosfat (PO43-) yang merupakan impuritas tulang. Gugus-gugus tersebut secara struktur dan fisik bersifat tidak stabil dan sangat reaktif. Sifat reaktif tersebut memberikan sifat-sifat fisikokemikal, biologik, fungsional, dan kemikal yang penting dalam pembentukan dan disolusi kristal di dalam jaringan biologik Prinsip dasar, biomineralisasi adalah proses pembentukan mineral sebagai bahan abiotik yang sebetulnya bermula dari organisme hidup. Mineral-mineral yang terbentuk itu, sering membentuk ciri berstruktur seperti ~ 253 ~ cangkang dan tulang biota (skeletal) , dimana proses itu menghasilkan rangka bermineral yang terjadi sepanjang 550 juta tahun silam. Contoh: lapisan besi, dan emas yang ada di sedimen berasal dari biota lewat proses biokimia dan perombakan yang melibatkan bakteri . Mineral-mineral yang bersumber dari unsur biologi seringnya mempunyai kegunaan khusus seperti penderia magnet di dalam bakteria magnetotaktik (Fe3O4), piranti penderiaan graviti (CaCO3, CaSO4, BaSO4), serta penyimpanan dan mobilisasi besi (Fe2O3•H2O di dalam protein ferritin). Dari segi pengagihan taksonomi, biomineral yang paling umum ialah garam-garam fosfat dan karbonat kalsium yang digunakan bersama-sama polimer organik, seperti kolagen dan kitin untuk menyokong pada percepatan pembentukan batuan sedimen. Sesungguhnya komposisi material pada biomineral berasal dari tulang, gigi, enamel, staolit, otolit, kulit moluska dan krustasea, tulang ekor ikan, kulit telur, rangka silika spongs, alga, radiolarian, foraminifera dan kulit diatom mengandung silika, juga mineral besi hasil pembentukan oleh bakteri (Lowestam dan Weiner, 1989; Fortin dkk, 1997; Fortin dan Beveridge, 2000; Lower dkk, 2001 ; Mann, 2001; De Yoreo dan Dove, 2004). Karena adanya ketarikan biomineral tersebut, yakni bahan organik diubah bentuk menjadi unsur abiotik bernilai ekonomis tinggi, maka beberapa dekade belakangan ini para ilmuan memandang pengetahuan biogeokimia sangat penting untuk melihat bagaimana evolusi kebumian, pelbagai mineral yang ada di dasar laut yang bersumber dari organisme hidup pada jutaan tahun silam, membentuk lapisan mineral yang memiliki nilai ekonomis tinggi. Perkembangan pengetahuan biogeokimia belakangan ini sangat pesat, ditandai dengan berbagai judul riset di bidang ini dengan melibatkan para ilmuan interdisplin, seperti ahli biologi, kimia, fisika dan kebumian (earth sciences). Memang disadari antar bumi dan pelbagai kehidupan bisa bermunculan ~ 254 ~ unsur-unsur baru yang merupakan sumberdaya alam yang sangat bermanfaat, diantaranya biomineralisasi. Disiplin ilmu ini telah dikembangkan oleh para ilmuan muda, bahkan banyak dari mereka telah berhasil mengaplikasikan riset dengan menggunakan metoda piranti komputer. Tetapi sesungguhnya terbitan buku pertama tentang “biomineralization” sudah sejak tahun 1824 oleh seorang pakar dari Jerman bernama W.J. Schmidt. Kemudian di awal tahun 1980-an bermunculan pelbagai tulisan ilmiah tentang “calcification”, dimana menceritakan bagaimana proses biologi terjadi pada pengkapuran yang berisikan mineral. Lebih dalam kajiannya ternyata mineral biogenik itu diliputi oleh kation, halini dikenal sebagai biomineralisasi, karya tulis itu antara lain : Lowenstam dan Weiner, 1989; Leadbeater dan Riding, 1989; Bäuerlein, 2000 dan Mann, 2001. Sebelum menanjak ke pembahasan lebih dalam tentang biomineral, kita perlu ketahui bagaimana evolusi biomineral dalam sejarahnya. Ada seorang ahli dari Belanda bernama Nicolaas Tinbergen sangat terkenal sebagai ahli biologi dalam prediksi dan perkembangan lanjut maklum hidup. Dia telah mempelajari bagiamana fungsi organisme yaitu molukuler dan fisiologi ditinjau dari sudut biomineralisasi. Dalam kesimpulan dia bahwa berbicara biomineralisasi tidak akan terlepas dengan pengetahuan biologi dan kimia, termasuk dalamnya bakteri sebagai peluruh sel-sel organisme. Rangka biota dan cangkang yang terdeposit di dasar perairan dalam periode geologi yang panjang, secara alamiah terjadi pengikatan kimia sehingga membentuk lapisan keras (lihat uraian pada bab 8). Di tinjau dari segi evolusi rangka organisme, secara phylogenetik dan fossil di sajikan pada gambar 10.1. Bentukan mineral mula-mula terjadi pada organisme prokaryotik yang kemudian ke eukaryotik proses ini terjadi kurang lebih lebih 3500 juta lalu (Weiner dan Dove, 2003). Kemudian diakhir era “Precambrian” dan khusus pada ~ 255 ~ “Cambrian” kira-kira 540 juta tahun silam, telah terbentuk 64 jenis mineral yang berbeda bersumber dari pelbagai phylum (Knoll, 2003). Sesungguhnya biomineral tidak hanya di produksi oleh biota tetapi dapat juga bersumber dari kerak bumi, dan bentuknya tergantung pada jenis, ukuran, kristalinitas, isotop dan trace elemen yang menyusun komposisinya. Gambar 10.1. Skala Geologi 1000 tahunan dan Kejadian Evolusi [Era Mesoproterozoic (1600-1000 juta tahun yang lalu) dan Paleoproterozoic (2500-1600 juta tahun lalu). Sedang Proterozoic dan Archean (>2500 juta tahun lalu), tidak terlihat pada gambar. Sumber : Remane (2000) ~ 256 ~ Prinsip dasar proses biomineral dari skeletal membutuhkan energy dan energy itu digunakan pada proses metabolik organisme pembentuk kerangka tubuh dan cangkang. Bongkahan sebagai mineral bisa diproduksi oleh hewan, tumbuhan dan bakteri, tetapi jelas bagi kita bahwa penyusun mineral dari organisme (prokariotik dan eukariotik) mengeluarkan energy cukup besar, dan hal itu tergantung pada lingkungan. Namun demikian proses yang berlangsung bertalian dengan interaksi kimia sebagai pembentuk mineral. Mekanisme penyusunan biomineral melibatkan pelbagai senyawa di lingkungan maupun proses biokimia di dalam tubuh organisme itu, seperti asupan nutrisi di organisme, fotosintesis serta kerja enzim yang memproduksi butiran kristal mineral. Bertolak dari gambar diatas, terlihat organisme yang hidup jutaan tahun yang lalu telah menyusun lapisan kerak samudera dengan pelbagai mineral yang padat, belakang ini para ilmuan menyebutnya sebagai “nodule” di dasar laut dan tanah di dasar laut. Suatu kehebatan yang harus kita kagumi para ahli paleosenografi mampu menelusuri peristiwa jutaan tahun yang lalu dalam struktur fosil yang ditinggalkan oleh organisme laut. Secara phylogenik organisme eukariotik sebagai penyusun kerangka mineral telah teridentifikasi lewat kajian oleh para ilmuan. Phylogenik dan model sebaran penyusun kerangka mineral itu di ilustrasikan dalam gambar 9.2. Gambar tersebut menyerupai bentuk pohon memperlihatkan jalannya (roadmap) evolusi skeletal, hakekatnya ada tiga biomineral skeletal, yaitu kalsium karbonat dan silika merupakan jumlah terbanyak, sedang kalsium fosfat relatif sedikit jumlahnya , biomineral ini tersebar luas, tetapi proses pembentuknya tergantung pada organisme eukariotnya dengan proses biokimia yang terjadi. ~ 257 ~ Gambar 10.2. Phylogenik Molekul Eukariotik Penyusun Kerangka Mineral [ C= mineral kalsium karbonat; P= mineral Kalsium fosfat; S= opal silika] Sumber: Mishler dkk (1994) Khusus untuk tumbuhan; tentang “opisthokonts” (Giribet, 2001); dan Baldauf (2003) untuk Eucarya; dan Lowenstam and Weiner (1989) disitir dan diramuh oleh Knoll (2003). Mineral bisa berasal batuan yang terlepas akibat sinar matahari dan beberapa sumber dipindahkan oleh sungai atau jatuh dari atmosfer. Dengan demikian komposisi kimianya ~ 258 ~ sangat kompleks dan peluruhannya dipengaruhi oleh temperatur, pH, tekanan parsial dan CO2 dari udara. Material ini terlarut membentuk endapan sebagai batuan sedimen. Selain itu, mineral laut dapat juga ditransformasi secara pasif diagenesis membentuk struktur, yaitu bersumber dari organisme prokariot dan eukariot. Kedua kelompok organisme ini memiliki kemampuan menyusun skeletal mineral yang terakumulasi di sedimen laut. Rangka karbonat Seperti pada gambar 10.2, ada delapan kelompok organisme ( Opisthokont, Heterokont, Alveolate, Cercozoan, Discicristate, Amoebonozoan, Excavate dan plant) lima diantaranya berisikan kerangka mineral dan endapan kalsit atau aragonit. Namun demikian yang menjadi pertanyaan bagi kita, berapa banyak rangka karbonat yang terbentuk pada spesies eukariot ?, jawabannya, sangat tergantung pada struktur skeletal dan proses biokimianya. Telah diketahui ada dua taxa yang secara orginal dapat menghasilkan rangka CaCO3, yaitu echinodermata dan foraminifera. Biomineralisasi karbonat dari kelompok “foram” berbeda antar cerozoan dan opisthokon, tetapi bagi kelompok echinodermata dan ascidian jelas memiliki mineral yang sama, kedua kelompok ini mengandung “deuterotome kalsifit” walaupun bentuk anatomi skeletal berbeda, yakni berbentuk spikula pada ascidian sedang pada echinordemata ditandai “stereo” (Knoll, 2003). Suatu dugaan rangka karbonat yang ada pada eukariot ada sekitar 20-80 , termasuk ada 20 sesungguhnya dari metazoa (kalau pada Cnidaria hanya 8) (Romano dan Caims, 2000), ada 4 pada tumbuhan (alga hijau dan alga merah), dan pada cercozoan, haptophyte, heterokont, dan pada alveolate (di dinoflagelatta mengandung kalsifit). Menurut Besgtson dan Conway (1992) keanekaragaman rangka pada batuan Cambrian rendah yang bentuk endapan ~ 259 ~ skeletal dengan lapisan terputus-putus disitu terdapat banyak biomineralisasi karbonat berasal dari demospongs. Intinya pada phylogenic, menjelaskan suatu evolusi rangka karbonat, mekanisme lewat system molekuler sama. Pembentukan rangka membutuhkan endapan mineral, dan endapan itu di kendalikan oleh system biologi. Biokomposit rangka organisme terdiri dari matriks organik, yaitu protein kolagen dan substansi inorganik ( protein nonkolagen). Kolagen dalam bentuk lamela-lamela ini membentuk rangka yang padat (kompak). Di antara lamela matriks, terdapat osteosit yang menerima dan mentransmit nutrien. Selain kolagen, di matriks organik tulang juga berupa protein nonkolagen akan berperan di dalam remodelling (pembentukan rangka). Dalam biomineralisasi skeletal membutuhkan kalsium dan karbonat, dimana kedua unsur ini sebagai inti mineral untuk pertumbuhan rangka. Cangkang moluska ialah bahan komposit biogenik yang telah menarik banyak minat dalam bidang sains, karena sifatnya yang luar biasa serta cirinya yang unggul untuk mengkaji biomineralisasi. Beratnya terdiri daripada 95-99% kalsium karbonat dan 1-5% yang tertinggal merupakan komponen organik. Dalam biomineralisasi cangkang moluska, protein-protein khusus bertanggungjawab mengarahkan penukleusan hablur, fasa, morfologi, serta dinamika pertumbuhan dan akhirnya memberikan cangkang itu kekuatan mekanik yang luar biasa. Proses biologi pada eukariot baik bersifat photoautotropik maupun heterotropik membutuhkan ion Ca 2+ dan enzim tertentu. Hasil studi dari Weiner and Wagner (1999), menyimpulkan bahwa pada organisme pembentuk karbonat terjadi sintesa asam protein dan glikoprotein menjadi mineral sebagai diagenetik pertumbuhan Kristal. Jadi banyak hewan dan bakteria bukan pembentuk rangka tetapi memiliki peran sintesa karbonat dalam proses biomolekul. Walaupun secara biokimia ada juga molekul yang dapat menghambat ~ 260 ~ mineral CaCo3, Martin (1995) mendukung adanya pengurangan mineral pada rangka, melalui “anti-calcifying” di makromolekuler sehingga terjadi penghambatan pertumbuhan Kristal. Sebab di samudera yang mengandung banyak “proterozoic” biasanya cepat terjadi kalsifikasi pada sel dan jaringan, terkadang molekul itu menghambat pertumbuhan rangka, hal ini disebut sebagai anti-kalsifikasi. Menurut Luo dkk (1997) kalau pada moluska dan cnidarians ada aktivitas biokimia yang bekerja sebagai kekebalan terhadap “anticalcifying”. . Dengan demikian banyak rangka calcareous terbentuk hasil kerjasama molekul dan proses fisiologi pada organisme eukariot. Intinya rangka strukturnya tidak homogen tergantung proses biokimia pada pembentukan kerangka karbonat. Rangka silika Biomineralisasi silika di bumi lebih banyak dilakukan oleh organisme akuatik, seperti diatom, radiolaria dan sinurophyta multi sel yang berongga (Lowenstam dan Weiner, 1989). Organisme itu memproduksi rangka bagian dalam dan luarnya sampai tersusun massa tubuhnya, dan fenomena ini lebih banyak dilakukan oleh diatom. Gambaran secara elektro mikroskopi yang dilakukan oleh Sumper dan Kröger (2004) disajikan pada gambar 10.3. Pembentukan massa biosilika dimulai dari bentuk ukuran nano secara perlahan-lahan terbentuklah rangka dinding kulitnya, proses yang berlangsung ini dikontrol dengan mekanisme biokimia. Jadi kulit diatom terdiri dari nano silika yang tersusun membentuk ikatan SiO2 organik. ~ 261 ~ Gambar 10.3. Struktur kulit luar beberapa Jenis diatom. (a) Cylindrotheca fusiformis; b,c) Coscinodiscus asteromphalus; d,e) Thalassiosira pseudonana. Sumber: Sumper dan Kröger (2004) Rangka silika opaline banyak terdapat pada organisme eukariot, kurang lebih lima atau enam kelompok dari delapan kelompok besar ditemukan rangka silika. Secara biologikal sebaran rangka SiO2 berbeda dengan rangka CaCO3. Halmana biomineralisasi silika endapannya hanya pada intrasel. Dengan demikian ukurannya mikroskopis, umumnya banyak ditemui pada “cercozoan” (radiolarian dan sejenisnya), “ebridian” dan “heterokon”. Tetapi di hewani rangka siliceous hanya ada pada rongga spikula dan sedikit di kopepoda ( Sullivan dkk, 1975), juga ada di intrasel bagian epidermis larva brachiopoda (Williams dkk, 2001) . Kalau di tumbuhan, biomineralisasi karbonat laut dan phytolith mineral berisi silika, di alga airtawar terjadi di jaringan tumbuhan bagian luar, seperti pada rumputan, sedges dan “sphenopsid” genus Equisetum (Rapp dan Mulholland, 1992), kecuali choanoflagellate dan spongs memang telah ~ 262 ~ mengandung endapan silika, diperkirakan 8-10 kali lebih besar dari organisme eukariotik. Apabila terjadi kerusakan mineral di dalam tubuh organisme, dibutuhkan silika transpor ke bagian sel itu (berasal dari deposit silika yang tersedia pada gelembung air di perairan), dimana yang berperan disini adalah enzim. Silika di gelembung air, biasanya bersumber dari pelbagai molekul, dimana adanya polimerisasi molekul asam silisik, poliamin dan silaffin di diatom (Korning dkk, 2001). Intinya, setiap organisme menyusun rangka silika mineral selalu di kendalikan dengan proses biokimia. Polimerisasi asam silikik bisa terjadi dalam tiga tahap, yakni: ①. Asam silikik dari kelompok“silanol” yang berukuran kecil akan membentuk “dimer” ; “trimer” dan siklus oligomer. Jenis asam oligosilikik berkemampuan membentuk ikatan “siloxane” atau Si-O-Si sebagai bentuk maksimal, dan dalam polisilikik ini merupakan inti pada rangka silika. ② polimerisasi berjalan terus inti itu berkembang menjadi bentuk bola kecil (lihat gambar 9.4) halmana asam silikik berbentuk monomerik sampai oligomerik akan membentuk partikel. dan ke ③ massa polysiklikik ini berkembang terus sehingga terjadi pekat berwujud gel yang akhirnya terjadi ikatan silika yang kuat, maka tersusunlah kulit diatom. Biomineral yang terjadi berisikan matriks kimia organik dan atau inorganik dalam pelbagai bentuk tergantung pada interaksi mineral yang terjadi. Silika pada organisme dilaut lebih banyak (± giga ton per tahun) dari silika yang dikandung oleh manusia (diperkirakan hanya mega ton), umumnya silika di perairan alam ada dalam bentuk asam silikik dan terdeposit di sedimen. Biomineral silika yang di alam mekanisme pembentukan secara diagenesis, mula-mula unsur kimia organik (protein dan karbohidrat) melalui reaksi biokimia sehingga terbentuk senyawa kimia kompleks (larutan), dan larutan itu terdapat juga ion-ion lain seperti: Li+, Na+, K+ dan ~ 263 ~ karbonat. Proses biokimianya berlangsung terus dan dipengaruhi kondisi lingkungan, larutan itu berubah jadi gel (terjadi pengentalan), biasanya pada keadaan berbentuk gel ini makin jelas terlihat senyawa silika, berkat bantuan reaksi biokimia, suhu dan tekanan maka terbentuk endapan silika di sedimen. Gambar 9.4 memberikan Ilustrasi proses pembentuk butiran silika membentuk rangka. Gambar 10.4. Proses terbentuk rangka silika Silika dalam bentuk SiO4 (tetrahedron) dan SiO6 (octahedron) merupakan unsur pembentuk struktur rangka organisme, senyawa itu bersama dengan material silika berbasis zeolite membentuk endapan yang tidak berbentuk (amorf) di dasar perairan. Material yang “amorphous” biasanya ada dalam ikatan Si−O−Si atau ikatan yang terpisah berbentuk Si−O, bentuk struktur kimia silika amorf seperti terlihat pada gambar 10.5. berikut ini. Gambar 10.5. Struktur Ikatan Silika Penyusun Rangka ~ 264 ~ Senyawa silika dalam ikatan Si-O- grup dengan adanya pengentalan dua senyawa asam silikik , mekanisme reaksi yang terjadi seperti dilukiskan pada gambar 10.6. Gambar 10.6. Mekanisme Pengentalan Dua Asam Silikik Senyawa kimia silika seperti yang ada di gambar 9.5., halmana senyawa Si (OH)4 di bawa kondisi pH normal akan mengalami reaksi seperti berikut: Si(OH)4 + Si(OH)4↔ (HO)3Si–O–Si(OH)3 + H2O (10.1) Apabila terjadikan tabrakan dua molekul asam silikik (yang bermuatan ion dan non-ion) maka menurut perry (2003), reaksinya akan terjadi demikian: Si(OH)4 + Si(OH)3O−↔ (HO)3Si–O–Si(OH)3 + OH− ~ 265 ~ (10.2) Proses pembentukan silika oleh organisme atau sering disebut biosilika bisa bersumber dari pelbagai organisme, seperti radiolaria, diatom, plankton dan sebagainya, walaupun secara global kandungan biomineral silika lebih sedikit jika dibandingkan dengan biogenik CaCO3. Beberapa contoh organisme yang mampu memproduksi silika (biosilika), disajikan pada gambar berikut. Gambar 10.7. Silika bersumber dari beberapa organisme. (sumber: Perry, 2003) Silika dalam suatu ikatan kimia kompleks merupakan polimer alam (natural) seperti agarose, hialuronat, fibrin, kolagen ataupun gelatin akan mengalami metabolisme dalam tubuh sehingga membentuk lapisan kulit dan rangka silika tubuh. ~ 266 ~ Rangka fosfat Mineralisasi kalsium fosfat membentuk granula kecil merupakan fosfat yang tenggelam dan tersimpan di laut ( Lowenstam & Weiner, 1989). Rangka fosfat yang terbentuk berasal dari hewan sangat terbatas, kecuali pada branchipoda dan beberapa jenis organisme bertulang belakang. Sebagian besar sumber itu melalui metabolisme bisa merupakan nutrient fosfat bagi rangka. Apalagi sebagiannya digunakan untuk perbaikan perbaikan sel tubuh organisme. Walaupun rangka fosfatik berbeda dengan evolusi pembentukan kalsium karbonat, tetapi dalam proses pembentukan mineral selalu melewati proses biokimia. Hal yang menarik di semua organisme eukariot terjadi transport kalsium dan ini merupakan pengendali bagi pembentukan fosfat secara molekuler. Endapan fosfat dan CaCO3 pada hewan merupakan tanda bahwa molekul bisa menyumbangkan mineral. Memang berbeda endapan mineral berasal dari organisme bertulang belakang (vertebrat) dan moluska, namun kuncinya pembentukan rangka tergantung pada proses biokimia dan jumlah tulang yang dimiliki oleh hewan itu. Biomineral Utama Mineral di laut terdiri pelbagai jenis, kurang lebih ada 64 jenis yang telah ditemui, tetapi ada beberapa jenis yang mendominasi atau disebut juga sebagai biomineral utama. Kation kalsium banyak terdapat pada organisme, hampir 50% biomineral yang diketahui mengandung kalsium (Lowenstam dan Weiner, 1989). Ternyata kalsium punya peran penting pada metabolisme sel (Lowenstam dan Margulis, 1980; Simkiss dan Wilbur, 1989) halamana banyak dipakai untuk kalsifikasi. Pelbagai sumber menyatakan bahwa kalsium bisa berasosiasi dengan fosfat, karbonat, oksalat dan mineral lainnya. Tabel 10.1 berikut memperlihatkan nama dan komposisi kimia biomineral. ~ 267 ~ Tabel 10.1. Nama dan Komposisi Kimia Mineral Hasil Mineralisasi Secara Biologi Nama Kimia Bentuk Senyawa Karbonat Kalsit Mg-Kalsit Aragonit Vaterit Monohydrokalsit Protodolomite Hydrocerussite Amorphous Kalsium Karbonat (ada 5 bentuk) Fosfat Octakalsium fosfat Brushite Francolite Carbonated-hydroxylapatite (dahllite) Whitlockite Struvite Vivianite Amorphous kalsium fospat (ada 6 bentuk) Amorphous kalsium Pyrofosfat Sulfat Gypsum Barite Celestite Jarosite Sulfida Pyrite Hydrotroilite Sphalerite Wurtzite Galena Greigite Mackinawite Amorphous Pyrrhotite Acanthite Arsenat Orpiment As2S3 Hydrat Silika Amorphous Silika ~ 268 ~ CaCO (MgxCa1 )CO CaCO CaCO CaCO3·H2O CaMg(CO3)2 Pb3(CO3)2(OH)2 CaCO3·H2O or CaCO3 3 x 3 3 3 Ca8H2(PO4)6 CaHPO4·2H2O Ca10(PO4)6F2 Ca5(PO4,CO3)3(OH) Ca18H2(Mg,Fe)2 +2(PO4)14 Mg(NH4)(PO4)·6H2O Fe3+2(PO4)2·8H20 bervariasi Ca2P2O7·2H2O CaSO4·2H2O BaSO4 SrSO4 KFe3+3(SO4)2(OH)6 FeS2 FeS·nH2O ZnS ZnS PbS Fe3S4 (Fe,Ni)9S8 Fe1−xS (x = 0−0.17) Ag2S As2S3 SiO2·nH2O Klorida Atacamite Fluorida Fluorite Hieratite Logam Sulfur Oksida Magnetite Amorphous Ilmenite Amorphous Besi Oksida Amorphous Manganes Oksida Hydroksida & Hydrous Oksida Goethite Lepidocrocite Ferrihydrite Todorokite Birnessite Organik Kristal Earlandite Whewellite Weddelite Glushinskite Manganese Oxalate Sodium urate Asam Urik (asam urat) Kalsium tartrat Kalsium malat Paraffin Hydrocarbon Guanine Cu2Cl(OH)3 CaF2 K2SiF6 S Fe3O4 Fe+2TiO3 Fe2O3 Mn3O4 α-FeOOH γ-FeOOH 5Fe2O3·9H2O (Mn+2CaMg)Mn3+4O7·H20 Na4Mn14O27·9H2O Ca3(C6H5O2)2·4H2O CaC2O4·H2O CaC2O4·(2+X)H2O (X<0.5) MgC2O4·4H2O Mn2C2O4·2H2O C5H3N4NaO3 C5H4N4O3 C4H4CaO6 C4H4CaO5 C5H3(NH2)N4O Sumber : Lowenstam dan Weiner (1989), Simkiss dan Wilbur (1989), Mann (2001), Weiner and Addadi (2002) Hal yang menarik dari biomineral kimia organik dari tubuh biota setelah terurai dapat menyusun endapan di dasar laut yang memiliki nilai ekonomis tinggi. Endapan mineral itu berbentuk amorf biogenik, seperti granula (butiran halus) hidro-besifosfat yang bersumber dari kulit holothurians, Molpadia ( Lowenstam dan Rossman 1975). Contoh butiran material amorf yang terdapat di kulit holothurian. ~ 269 ~ Gambar 10.8. Endapan Butiran Hydrous Besi Fosfat pada Kulit Holothurian Sumber: Weiner dan Dove (2003) . Mineral kalsium karbonat banyak dikandung oleh organisme baik dalam jumlahnya maupun sebaran pada pelbagai taxa (Lowenstam dan Weiner, 1989). Telah diketahui ada delapan polimer kalsium karbonat, dimana tujuh berbentuk kristalin sedang yang satu berbentuk amorf (butiran kecil tidak berbentuk). Kemudian ada tiga polimer mengandung kalsium karbonat murni, yakni: Kalsit, aragonit dan vaterit. Selain itu dua senyawa monohidrokalsit dapat membentuk kalsium karbonat stabil yang berisi satu molekul H2O setiap kalsium karbonat (Addadi dkk, 2003) Kurang lebih ada 25% tipe biogenik mineral adalah fosfat, kecuali “struvite” dan “brushite”. Fosfat mineral yang diproduksi oleh biota sangat berlimpah, senyawa itu ada dalam ikatan karbonat hidroksiapatit, sering disebut “dahllite”, dan mineral-mineral itu banyak ditemui di tulang dan gigi, tapi kalau pada brachiopoda ada di inarticulate shell. Kristal biogenik karbonat apatit biasanya berbentuk lempengan tipis dan kecil (± 2-4 nm tebalnya dan ada juga beberapa bisa sampai 10 nm agak panjang dan lebar). Memang umumnya mineral berbentuk kristal dapat terjadi melalui sistem “hexagonal crystallography” (Stumm, 1992). ~ 270 ~ Kalau melihat pada table 9.1 diatas terlihat setiap klas mineral berisikan satu atau lebih H2O atau gugus hidroksil, dan hampir 60% biomineral berisi hydrat. Kemudian bentuk pertama kristalin biomineral karbonat adalah fase hidrat, jika senyawa itu berisikan anhidrat maka perkembangan inti akan terhambat, karena energy kurang serta air yang ada bisa menghambat pertumbuhan. Untuk biomineral besi agak sulit di prediksi jenisnya sebab kebanyakan mineral itu ada dalam ikatan oksida, hidroksil dan sulfida (Bazylinski dan Moskovitz, 1997). Menurut Konhauser (1998) ada beberapa mineral besi sulfat (FeS) dan fosfat yang terdapat di permukaan bumi bisa memperkaya mineral di sedimen. Namun demikian mineral yang tersedia kurang lebih 40% berasal dari organisme (Bazylinski and Frankel, 2003). Mineral bersifat inorganik berasal dari permukaan tanah dapat berasosiasi dan masuk ke biomineralisasi. Demikian juga Kirschvink dan Hagadorn (2000), mempertegas bahwa mineral itu dapat menarik biomineral dan mineral besi secara umum lewat aktivitas mineralisasi. Dalam table 10.1. terlihat ada satu grup “organik” mineral walaupun pembentukannya kontradiksi dengan proses fase kristallin oleh organisme. Namun dapat dipastikan mineral-mineral itu akan kembali terbentuk lewat fraksinasi. Kecuali DNA telah diketahui ditransformasi ke fase kristalin melalui bakteri. Prinsip Dasar Biomineralisasi Pengaturan secara biologi pada proses mineralisasi diatur oleh dua kelompok, yaitu tergantung pada kebebasan biologikal dan mediasi matrik organik. Prinsipnya biomineralisasi sangat tergantung pada lokasi, yaitu: (1) bagaimana bentuk apakah konsentrasi ion atau fase padat serta dimana biomineral itu terbentuk; (2) tipe translokasi yang terjadi; (3) letak dan bentuk produk terjadi. Hakekatnya ~ 271 ~ aktivitas biomineralisasi akan dikendalikan oleh biologikal, seperti mekanisme transport dan hidrasi di lingkungan biasanya memberi efek sedikit elemen kimia. Endapan mineral dapat terjadi karena interaksi antara aktivitas biologi dan lingkungan, sering disebut sebagai “biologically induced” mineralisasi. Dalam kondisi ini permukaan sel merupakan tempat pertumbuhan inti mineral dan perkembangannya. Mineral yang terdeposit melalui proses metabolisme dan didukung oleh proses “redox” (reduksi oksidasi) yang dikendalikan oleh pH, pCO2 maka organisme boleh mengsekresikan mineral dan terdeposit dilingkungan (McConnaughey, 1989; Fortin dkk, 1997 dan Tebo dkk, 1997). Proses mineralisasi di tubuh organisme seperti terlihat pada ilustrasi di gambar 10.9. berikut ini. Nukleat di episel Produk organik Keterangan Aktif memompa Difusi pasif Sekresi Nukleat terangkat menjadi partikel Gambar 10.9. Skematik “biologically induced” mineralisasi Sumber: Weiner dan Dove (2003) Partikel mineral akan keluar dari kulit sel melalui suatu mekanisme seperti ilustrasi diatas, halmana adanya aktivitas memompa dari tubuh (proses metabolism) maka terjadi pengeluaran bahan organik atau sekresi bahan organik yang ~ 272 ~ bermuatan mineral, yang kemudian akan terlepas ke lingkungan perairan dan menjadi endapan sedimen ( Knoll 2003; Van Cappellen 2003). Prinsip dasar, komposisi mineral yang keluar sebagai proses rangsangan secara biologi ada dalam berbagai jenis mineral disertai bentuk bermacammacam pula. Kemudian mineral ini akan mengendap dan berubah menjadi bahan kimia anorganik yang tersusun sebagai batuan sedimen. Aktivitas proses mineralisasi oleh organisme terjadi langsung pada inti, dan inti itu akan bertumbuh sehingga membentuk morphologi tertentu, akhirnya terdeposit di lingkungan. Harus disadari, mekanisme biomineralisasi di dalam tubuh organisme sangat rumit, namun demikian pelbagai biota mampu memproduksi butiran mineral sebagai awal pembentukan mineral di sedimen. Proses biomineral biasanya terjadi di intrasel dan tersimpan pada bagian-bagian sel tertentu, kemudian terlepas melalui kulit yang pada akhirnya akan terlepas ke lingkungan perairan. Mineralisasi dapat berlangsung di sel bagian luar yakni adanya suatu matriks makromolekul berasal dari protein, polisakarida dan glikoprotein secara bersama-sama atau berintegrasi menyusun mineral, tetapi proses ini dikendalikan oleh kegiatan biokimia (metabolism) di sel bagian dalam tubuh. Intinya penyusunan komposisi biomineral dilakukan oleh asam amino (protein) lebih khusus lagi “aspartate” dan grup fosforil (Swift dan Wheeler, 1992). Matriks molekul yang terbentuk itu berasal dari: pertama, adanya difusi ion di cairan dengan kekentalannya tinggi di dalam tubuh, kemudian secara aktif sel itu memompa kation melalui membrane sel dan akan terkumpul di suatu bagian tertentu (Simkiss, 1986)( lihat gambar 10.10,a), kedua, Kation yang ada terkonsentrat di sel sehingga terjadi gelembung kecil yang bermuatan kation, gelembung ini dipompa ke luar sehingga terbentuklah matriks organik (gambar 10.10,b). Akhirnya terbentuklan tulang muda berisi ~ 273 ~ mineral sehingga berkembang menjadi lempengan “epiphyseal” (Ali, 1983) Pompa aktif Gradien difusi Sekresi Matriks organik Matriks organik Gambar 10.10 Mekanisme Penyusunan Mineral di inti sel bagian luar. a). Kation yang dipompa keluar sel melalui membrane dan cairan itu keluar secara difusi pasif. b) Kation dalam cairan terkumpul (terkonsentrat) di sel dan membentuk gelembung kemudian dikeluarkan ke sel bagian luar. Material ini yang akan menjadi biomineral. Sumber: Weiner dan Dove (2003) Mekanisme itu terjadi juga pada larva bulubabi (sea uchin) dimana kalsium kabonat yang ada di dalam tubuh membentuk gelembung cairan yang akhirnya terjadi Kristal kalsit ( Beniash dkk, 1999) Dalam bentuk anion akan berpindah secara pasif yang akhirnya akan berubah menjadi kation yang menyusun matriks organik di sel bagian luar. ~ 274 ~ Kedua proses (gambar 9.10 a dan b) bekerja aktif di sel bagian luar pada nukleasi episel menyuplai matriks organik dan berkembang sehingga terjadi penumpukan mineral. Hampir semua struktur yang terbentuk lewat proses di sel bagian luar diawali dengan pembentukan matriks yang berasal dari jaringan epithel multisel yang mengeluarkan bahan organik. Watabe dan Kingsley (1989) mempertegas lagi bahwa jaringan-jaringan itu memfasilitasi pembentukan rangka secara masif. Contoh-contoh organisme yang mengalami proses seperti itu, yakni foraminifera, kulit moluska, statolit pada cephalopoda, rangka luar dari bry0zoa, skleraktin di karang dan tulang dan gigi pada biota air (Bettencourt dan Guerra, 2000; Constantz dan Meike, 1989; Zeebe dan Sanyal, 2002; Erez, 2003; Lowenstam dan Weiner 1989 dan Veis 2003) Kita pahami sekarang bahwa mekanisme penyusunan mineral diawali dengan pembentukan matriks organik kemudian masuk dalam suatu siklus kerja tubuh. Ada beberapa penelitian yang dilakukan oleh para ilmuan, ternyata banyak bahan organik, protein β-kitin dan serat sel lunak yang berasosiasi dengan mineral aragonite. Adanya aktivitas kimiawi yaitu reaksi asam terjadi sehingga membentuk struktur mineral. Menurut Levi-Kalisman dkk, (2001) struktur dilapisan kedua dikulit moluska mengandung matriks protein dan cairan asam kental menyerupai kulit yang lunak seperti gel disebut “nacreous layer” . Gambaran umum bentuk “nacreous layer” disajikan pada gambar 10.11. Terlihat pada gambar diantara lapisan kitin dan sel makro berasam terdapat serat yang lunak berbentuk gel. Struktur di sel makro berasam ini yang tersusun dari matriks protein dapat mengeluarkan mineral. Tetapi dari sisi lain kondisi itu, bertolak belakang, dengan lazim yang berlaku di proses biomineral, dimana komposisi asam amino tersusun berbentuk larutan ada di dalam matriks. Dikotomi ini memperlihatkan bahwa fiksasi protein berjalan cepat dan ~ 275 ~ -kitin Glikoprotein yang terhambat Glikoprotein berlimpah Serat lunak berbentuk gel Gambar 10.11. Bentuk lapisan kulit yang lunak “nacreous layer” Sumber: Levi-Kalisman dkk, (2001) berlangsung terus sehingga terjadi protein yang mengandung asam yang tinggi (Gotliv dkk, 2003). Suatu hal yang menarik pada kulit moluska, kandungan protein yang mengandung asam tinggi merupakan fraksi yang mendominasi penyusunan struktur kulit dan mekanisme berlangsung terus-menerus. Mineralisasi yang terjadi di ekstrasel merupakan fungsi matriks protein yang bekerja seperti bentuk “bottleneck”, yaitu reaksi biokimia yang menghasilkan cairan matriks protein terus bertambah, sedang produksi mineral sangat sedikit, sehingga bahan organik itu terjadi penumpukan di bagian lapisan kulit tertentu. Beberapa ahli telah melakukan kajian tentang kemampuan protein membentuk inti mineral, seperti Belcher dkk (1996), Falini dkk (1996) dan Gotliv dkk (2003) menyimpulkan proses penyusunan mineral ada berbagai cara, tetapi di tubuh moluska untuk penyusunan inti mineral diperlukan aragonit khusus yang merangsang proses ~ 276 ~ tumbuhnya mineral. Hal yang menarik disini, disaat Weiss dkk (2002) mengadakan uji in vitro dengan cara memasukan inti aragonit melalui amorphous kalsium karbonat dan salah satu bagian tidak diberi amorphous kalsium karbonat, ternyata yang terjadi di larva moluska, produksi kulitnya (shell) diperlukan amorphous kalsium karbonat. Dengan demikian disimpulkan penyusunan biomineral di moluska tidak hanya bersumber dari matriks protein tetapi diperlukan aragonite agar pertumbuhannya cepat berlangsung. Mineralisasi intersel, Proses pembentukan mineral dalam sel dapat terjadi pada setiap organisme di suatu komoditas, halmana pembentukan mineral dari setiap organisme terjadi di ekstrasel. Bagi semua mahklub hidup aktivitas tumbuh kompartemen sel yang satu dengan yang lain saling berhubungan dan berinteraksi dalam pertumbuhan sel. Sebagai ilustrasi pengontrolan secara biologi pembentukan mineral dalam sel disajikan pada gambar 10.12. Pompa aktif Difusi pasif Gambar 10.12. Mineralisasi intersel. [ Substrat inti mineral ada di bagian epithel sel, kemudian Kation dipompa keluar sel, biomineral diluar sel itu bertumbuh] Sumber: Weiner dan Dove (2003) Inti mineral yang ada disubstrat pada ephitel mengeluarkan nukleasi dan berkembang di permukaan sel bagian luar, disana terjadi interaksi antar sel sehingga dengan leluasa menyusun ~ 277 ~ rangka. Namun demikian sesungguhnya penyusunan polymorph dan biomineral diawali dari bagian epidermis sel organisme itu. Sebagai contoh, terjadinya “calcareous” alga dimana inti dan pertumbuhan kalsit dengan c-axis terjadi di pendikular permukaan sel (Borowitzka, 1982). Aktivitas penyusunan mineral di setiap sel akan melalui alur metabolism dalam tubuh, dimana unsur makro dan mikro elemen akan berintegrasi membentuk sel baru, sedang sel yang lama akan didorong ke luar tubuh. Mineralisasi intrasel, Proses ini terjadi antar sel, yakni sebagai pembentukan mineral di dalam sel (seperti uraian diatas) yang kemudian antar sel itu terjadi interaktif atau saling tukar-menukar ion bahkan saling mengikat membentuk inti mineral, secara umum inti biomineral antar sel terjadi di vesikel atau vacuola. Komposisi biomineral dan bentuknya sangat tergantung pada pembentukan kristal pada kompartemennya. Biasanya perkembangan itu dikendalikan oleh kondisi lingkungan serta muatan kation dan anion pada biomineral yang ada dalam matriks organik. Pengaruh kondisi lingkungan dalam penyusunan matriks organik di membrane sel, seperti pH, tekanan karbon dioksida (pCO2) serta komposisi minor dan trace elemen. Sejumlah lipida yang ada di vesikel akan membantu matriks organic dalam rangka pengendapan bahan itu sehingga membentuk struktur mineral. Dalam gambar 9.13 terlihat secara garis besar bagaimana skenario pembentukan biomineral oleh antar sel sehingga terjadi ekstrasel (sel baru dibagian luar sel). Sebagai gambaran umum cara kerja antar sel diilustrasi di gambar 10.13 berikut ini: ~ 278 ~ (A) (B) Pompa Aktif Difusi pasif Akumulasi matriks organik Sekresi Gambar 10.13. Alur Kerja antar sel pada biomineralisasi di vesikel Keterangan: (A) inti biomineral [ 1. Interaksi di sel dan lingkungan; 2. Terjadi sekresi; 3a. senyawa organic telah dikeluarkan; 3.b. material penyusun mineral organik]. (B) tipe mineral membentuk biomineral di sel [ 1. Pertumbuhan di setiap sel sedang 2. Struktur mineral padat. Sumber: Weiner dan Dove (2003) Adanya reaksi biokimia dalam tubuh organisme maka senyawa yang terbentuk akan keluar dari membrane sel membentuk struktur di sel luar sebagai cikabakal mineral. Sebagai contoh di haptophyta alga, penyusunan awal terbentuknya kristal kalsit sampai bagian ujungnya sel pada antara sel di dalam tubuh, kemudian bahan itu keluar dari membrane sel. Menurut Watabe dan Kingsley (1989) mekanisme zat sebagai pembentuk biomineral yang keluar dari membrane, ada dua cara, yakni: pertama, apabila biomineral yang sudah siap di vesikel/vacuola akan keluar melalui membrane; kedua, plasma membran telah bergabung . ~ 279 ~ membentuk biomineral (bersifat premature) maka membran itu akan pecah sehingga keluar. Ada beberapa jenis organisme tertentu, biasanya di bagian luar sel telah tersedia larutan lipida, jika inti mineral keluar dari membran sel langsung terjadi interaksi dengan lipida yang akhirnya mengendap. Seperti terlihat pada gambar 9.13 (A), struktur “coccolith” Haptophyta alga telah matang langsung ditutup oleh sel. Intinya, mineral silika di alga berpengaruh pada vesikel sehingga amorphbous silica itu merupakan pendorong utama penyusunan biomineral di sel (Watabe and Kingsley, 1989).”coccolith” adalah kelompok fitoplankton terdiri dari banyak sel memiliki kemampuan menghasilkan butiran kalsit untuk rangka bagian luar. Berkaitan dengan biomineral di vesikel, aktivitasnya dimulai dari adanya interaksi antara biomineral dengan organik matriks di ekstrasel (sel luar) sehingga membentuk struktur ekstrasel yang padat. Di lingkungan ini beberapa foraminifera mulai menyusun kristal. Kemudian kristal bertumbuh oleh adanya masukan bahan organik sehingga terjadi penumpukan yang akhirnya akan keluar melalui membrane sel (exocytosis), sebagian kristal akan membentuk struktur kulit (Hemleben dkk, 1986) Menurut Markel (1986), kalau echinodermata memiliki kemampuan menyusun biomineral sampai beberapa sentimeter panjangnya pada kulit bagian luarnya. Tetapi kalau bulubabi (sea urchin) walaupun struktur spikulanya terdapat banyak amorphous kalsium karbonat namun produk mineralnya hanya kristal-kristal kecil (single crystal), dan perkembangan menjadi kristalografi sangat lambat (Beniash dkk, 1997; Beniash, 1999; Wilt 2002). Dalam kenyataan tidak semua proses penyusunan mineral di antar sel akan menjadi ekstrasel, kalau kita lihat pada gambar 9.13 (b) dimana biomineral di vesikel bisa membentuk di antar sel tetapi tetap tidak menyebar dan hanya tetap tinggal di kulit saja, hal ini menarik , barangkali ada ~ 280 ~ sesuatu produk kimia dibentuk oleh bakteri yang menghambatnya. Sesungguhnya diseputar membran ada gaya magnetik dari kristal euhedral untuk memproduksi mineral baru (Bazylinski, 1996; Schüler and Frankel, 1999; Bazylinski and Frankel, 2003). Jenis radiolaria juga dapat melakukan proses biomineral di antar sel, halmana pada sitoplasma dapat terjadi spikula silika, yang kemudian secara sedikit-sedikit akan membentuk kompartemen sitoplasmik (Simkiss dan Wilbur, 1989). Tumbuhan juga bisa terjadi proses mineral di antar sel yakni menyusun kalsium sebagai kristal oksalat (Raven dkk,. 1982; Webb 1999; Skinner and Jahren 2003). Demikian pula di kulit diatom dapat terjadi proses mineral, disini terjadi dua proses, yaitu pertama terjadi polimerisasi silika sehingga membentuk matriks organik polypeptida (Swift and Wheeler, 1991, 1992; Kröger dkk. 1999, 2002). Kemudian kedua, silika akan keluar kepermukaan membrane sel dan membentuk bingkai intrasel (Garrone dkk, 1981). Kalsit pada ”coccolith” adalah kelompok fitoplankton yang dapat memproduksi kalsit biasanya berukuran 1-10 μm, kelompok ini mampu menyusun biomineral dengan sistem organik. Di samudera terbuka “coccolithophere” berlimpah, sebab dalam kehidupannya di laut berperan sebagai produksi primer dan bisa melakukan fiksasi karbon. Apabila kelompok fitoplankton ini mati dan tenggelam ke dasar laut akan cepat terakumulasi sebagai “calcareous oozes” dan kapur, dengan demikian proses ini sering disebut sebagai biogeokimia. Umumnya sedimen yang terbentuk oleh “coccolith” umurnya sangat panjang dan merupakan fossil di laut, oleh karenanya banyak riset bersifat multidisplin dilakukan pada bidang ini, seperti aspek biologi, palaeontologi, lingkungan, geologi dan sebagainya. Secara biologi “coccolithophere” adalah filum Haptophyta, diantara filum ini ada beberapa genera diantaranya: Phaeocystis, Prymnesium, Pavlova dan ~ 281 ~ Chrysochromulina tidak mengandung kalsium. Jenis-jenis ini terdapat kloroplas berwarna emas kecoklatan dan memiliki flagela. Bila ditinjau segi fosilnya, pembentukan endapan yang terbentuk diperkirakan terjadi pada periode Precambrian (>600 juta tahun) namun mineral yang tersusun berasal dari kloroplas, sebagai proses endosimbiose kedua, penyusunan itu terjadi diperkirakan di akhir Plaeozoic yaitu kira-kira 300 – 400 juta tahun yang lalu (Medlin dkk, 1997). Data belakangan sebagai hasil kajian, menurut Edvardsen dkk (2000) dan Fujiwara dkk (2001) ternyata ada satu genera dari filum Haptophyta bisa menghasilkan kalsium. Ada pula data geologi yang berbeda dengan pernyataan diatas, dimana coccolith mulai menyusun endapan terjadi di akhir periode Triassic diperkirakan pada 200 juta tahun lalu (Bown 1998a,b). Halamana golgi di tubuh mulai terjadi proses endosimbiose dan mengeluarkan kalsik, dengan demikian kalsik coccolith terjadi de novo (peluruhan) tapi tergantung dari grup biomioneralisasinya. Dua dekade belakang ini kajian biomineral dari coccolith berkembang cepat, seperti yang dilakukan oleh de Vrind-de Jong dkk, (1986, 1994), Westbroek dkk, (1989), Pienaar (1994), de Vrindde Jong and de Vrind (1997), Young dkk, (1999), and Marsh (2000). Bahkan dari peneliti tersebut ada yang mengatakan bahwa produksi biomineral dari coccolith lebih tinggi dari organisme lain. Halmana mekanisme biomineralisasi dikendalikan dengan aktivitas biologi di vesikel intrasel. Dengan demikian mekanisme pembentukan biomineral berasal dari coccolith merupakan suatu hal sangat menarik untuk diteliti. Sesungguhnya hal yang menarik dari coccolithophore dalam proses biomineral, yaitu dalam model biomineralisasi diketahui ada dua tipe yang berbeda didasarkan dari siklus hidupnya (Life cycle), yaitu diploid dan haploid. Berikut ini diagrama kedua siklus hidup coccolith (gambar 10.14). ~ 282 ~ MEIOSIS (Sel diploid mengalami mitosis menjadi 4 sel haploid) N 2N Haploid holococcolith Diploid heterococcolith MITOSIS MITOSIS (2 haploid menjadi satu sel diploid) Kombinasi coccosphere Heterococcocolith Holococcocolith Gambar 10.14. Siklus Hidup “Coccolithophore” [ Pemecahan sel secara aseksual pada coccolith diploid dan haploid, sehingga menghasilkan heterococcolith dan holococcolith] Sumber : Young dan Henriksen (2003) Gambar diatas terlihat siklus hidup dari sel eukariot yang terdiri dari diploid dan haploid. Dimana diploid adalah setiap kromosom ada dua sel yang di beri tanda 2N sedang haploid adalah setiap kromosom hanya satu sel saja di beri symbol N. Transisi dari sel diploid ke haploid biasanya melalui meiosis, tetapi jika terjadi pemecahan sel dari haploid ke diploid harus melalui “syngamy”. Secara umum, pemecahan sel organisme hanya melalui satu fase, tetapi pada haptophyta yang terjadi adalah dua fase dan pengembangan kedua sel itu adalah sama serta pemecahan itu melalui pasangan aseksual (Mitosis). Pada dasarnya pemecahan sel pada coccolith dapat terjadi di dua fase (diploid dan haploid) tapi memiliki sifat berbeda, sehingga akan berdampak pada pembentukan biomineral juga yakni ~ 283 ~ akan berbeda (Billard, 1994;Young dkk. 1999; Cros dkk. 2000; Geisen dkk. 2002; Cros dan Fortuño 2002). Kristal kalsit (± 0,1 μm) yang dibentuk pada fase diploid menjadi heterococcolith adalah sangat terbatas jumlahnya, hanya < 100, tetapi pada fase haploid menjadi holococcolith bisa mencapai beberapa ratus bahkan sampai seribuan. Dalam ilustrasi di gambar 9.14, terlihat coccosphere di heterococcolith banyak holococcolith yang mengelilinginya, halmana ada coccolith yang ditambahkan ke coccosphere di bagian permukaan diperkirakan sekelompok sel diploid yang membungkus heterococcolith, sedang kalau dua sel haploid menjadi diploid dan membentuk kulit holococcolith melalui “syngamy” (Geisen dkk. 2002). Dengan demikian dapat dikatakan siklus hidup coccolithophores sangat bervariatif, seperti pada genera Pleurochrysis dan Emiliania dalam proses menjadikan heterococcolith, kalsit yang ada hanya pada fase diploid sedang haploid tidak ada. Jelas bagi kita bahwa pengembangan sel diploid akan terbentuk struktur heterococcolith, sedang struktur dari holococcolith bersumber dari sel haploid. Bahasan berikut akan melihat bagaimana biomineralisasi pada heterococcolith dan holococcolith ditinjau dari aspek biokimia. Heterococcolith biomineralisasi, prinsip dasar dalam proses pembentukan mineral oleh organisme berasal dari molekul organik yang ada di inti sel yang kemudian tumbuh menjadi suatu matriks organik (seperti uraian diatas) yang pada akhirnya akan membentuk Kristal. Khusus pada organisme kelompok coccolith, diawal bahan organik itu membentuk kristal terdapat polisakarida yang kompleks (FichtingerSchepman dkk, 1981; Marsh dkk, 1992; Marsh, 1994; Ozaki dkk, 2001 dan Marsh dkk. 2002). Bermula inti sel yang spesifik akan mengeluarkan kristalografi dan terjadi pengikatan dengan bahan organik lainnya membentuk suatu matriks organik, dimana organik-organik ini yang akan menjadi kompartemen ~ 284 ~ penyusunan mineral. Dalam ukuran yang lebih besar akan membentuk morfologi biomineral (Mann, 1993). Prinsip dasar yang harus kita ketahui bahwa pembentukan mineral dari matriks organik tidak sama dengan organisme lain seperti moluska dan diatom Sebab di coccolith protein organik berasosiasi dengan gugus polisakarida. Seperti penelitian yang dilakukan oleh Fichtinger-Schepman dkk, (1981) terhadap jenis, Emiliania huxleyi dimana ada satu gugus polisakarida dengan rantai asam galakturonik yang kompleks berada di bagian belakang “mannose” sebagai gugus ester mengikat sulfat. Tetapi kalau di jenis Pleurochrysis carterae, terdapat 3 tipe gugus polisakarida, halmana dua tipe gugus polisakarida berperan mengikat kalsium dan akan membentuk beberapa coccolith, sedang satu gugus lainnya berperan penting pada intisel (Marsh dkk. 2002). Kelompok coccolith yang terbentuk merupakan suatu gambaran adanya fotosintesis alga yang berlimpah di samudera, umumnya coccolith itu melalui biosintesa menghasilkan nutrient N (nitrogen) dan P (fosfat). Matriks organik yang tersusun di coccolith akan menjadi cikal-bakal kristal mineral, namun proses ini membutuhkan enzim tertentu sehingga proses biokimia akan berjalan baik untuk membentuk biomineral. Struktur coccolith asli (proto-coccolith) sesungguhnya terdapat sedikit kristal kalsit yang berbentuk vertikal dan bergaris-garis yang berorientasi C-axis (struktur V/R), kemudian berkembang menjadi heterococcolith. Kelompok coccolith yang mengumpal dan padat disebut sebagai bentuk coccosphere. Sumber mineral pada coccolith ini berasal dari senyawa kalsit, kemudian dengan adanya proses biokimia yang berjalan (kerja enzim) maka terbentuk gugusan coccolith (heterococcolith). Gambar 9.15 memperlihatkan pertumbuhan inti (nukleasi) sampai terwujud bentuk coccolith dengan struktur vertical dan radial (V-R). ~ 285 ~ Gambar 10.15. Bentuk coccosphere dan proses pertumbuhan “proto-coccolith” Sumber: Young dkk (1992). Prinsip dasar, sifat dari lingkaran nukleasi di heterococcolith dikontrol oleh c-axis dan a-axis yang ada di makromolekul, dimana pengendalian oleh c-axis akan berperan mengatur sistem biomineralnya. Adanya substrat dalam makromolekul maka inti akan berkembang menyusun kristal mineral. Bahan organik yang ada berintegrasi dengan kalsit maka terbentuk kalsium atau dapat juga pengikatan dengan ion karbonat sehingga memungkinkan terjadi kristal kalsit. Struktur coccolith berbentuk V dan R merupakan struktur paten walaupun terjadi evolusi pada inti Young dkk (1992). Holococcolith biomineralisasi, bentuk coccolith ini berasal dari haploid yang telah berkembang. Kajian tentang biomineral dari holococcolith relatif sedikit, seperti penelitian pada jenis Emiliania huxleyi dan Pleurochrysis carterae, ternyata produksi holococcolith tidak ada. Namun demikian, prinsip dasarnya dalam siklus hidup coccolithphore akan ~ 286 ~ mengikuti sistem fase haplo-diploid, tetapi bagi fase haploid tidak ada pembentukan kalsit. Pengamatan secara morfologi yang dilkakukan oleh ahli dari Norwegia, Halldal dan Markali yang disitir oleh Young dan Henriksen (2003) bentuk struktur holococcolith dapat dilihat pada gambar 9.16 berikut ini. Namun secara detail struktur penyusunan rangka holococcolith seperti yang ada pada kelompok heterococcolith sangat kurang risetnya. Coccosphere Organik mengelilingi coccolith Heksagonal kristal dari jenis Calyptrolithophora papillifera Detail coccolith Coccolith membentuk kristal rhombohedral Konstruksi kristal rhombohedral Gambar 10.16. Bentuk Holococcolith Sumber: Young dan Henriksen (2003) Secara morfologi bentuk holococcolith sangat unik bentuk strukturnya memanjang dan didominasi dengan “euhedral rhombohedra” rangka kristalnya berbentuk heksagonal. Kristalnya tidak saling menghambat atau tidak terjadi pertumbuhan didalam intinya. Kemudian kristal itu terlihat terbungkus dengan bahan organik sama seperti pada heteroccolith dibungkus dengan bahan polisakarida. ~ 287 ~ Foraminifera adalah amuba multi sel yang bisa menghasilkan kalsium, jenis ini termasuk kedalam bagian protista (Loeblich dan Tappan , 1987). Walaupun jenis organism ini sebagai organism laut, tetapi ada beberapa referens memperlihatkan di air tawar terdapat organisme seperti amuba namun tidak menghasilkan kalsit (Holzmann dan Pawlowski 2002; Holzmann dkk, 2003). Organisme ini telah menjadi perhatian beberapa dekade belakang ini, karena ada hubungannya dengan siklus karbon dioksida di udara, dimana bertalian dengan perubahan iklim global. Disamping itu rangka foraminifera di laut berperan juga dalam memberikan informasi “paleosenografi” dan siklus karbon dilaut secara global. Menurut Singh (2008) biostratigrafi di sedimen merupakan salah satu bagian yang diperlukan dalam dunia perminyakan yaitu menentukan satuan batuan berdasarkan kumpulan mikrofosil tertentu, khususnya foraminifera. Sehubungan dengan perubahan iklim tentang naiknya gas rumahkaca (CO2) dimana adanya kekuatiran lapisan es di bagian kutub bumi akan mencair sehingga akan menaikkan permukaan air, sehingga berdampak pada tenggelamnya pulau-pulau kecil. Sesungguhnya, samudera memiliki peran untuk menetralkan kandungan gas karbondioksida di udara, di perkirakan kemampuan menetralkan adalah 50-60 kali lebih besar dari atmosfer (Siegenthaler and Sarmiento, 1993). Halmana gelembung udara CO2 dipermukaan air berasal dari udara akan dinetralkan atau terikat dengan CaCO3 yang ada dilaut. Tetapi prosesnya sangat lambat bisa mencapai 1000 tahun, sehingga gas karbondioksida bertumpuk di udara. Oleh karena itu, banyak ahli biogeokimia memfokus kajiannya bagaimana ekosistem laut merespons konsentrasi CO2 di udara (Archer dan Maier-Reimer, 1994; Broecker, 1997; Sigman dan Boyle, 2000 serta Berger, 2002). ~ 288 ~ Foraminifera, karang dan coccolithphore berperan dalam siklus karbon secara global, halmana organismeorganisme itu menetralkan karbon dioksida di udara masuk ke dalam samudera, melalui empat proses, yakni: (1) pertukaran gas antara air dan udara melalui karbonat ion membentuk bikarbonat; (2) proses primer productivity; (3) produksi dan terlarut pada CaCO3 dan ke (4) sirkulasi samudera. Khusus foraminifera merupakan kelompok terbesar dalam pembentuk biomineral di laut, karena adanya pengendapan CaCO3 yang tinggi di laut. Kelompok organisme yang berperan dalam siklus karbon diudara mampu melakukan fotosintesis dan oksidasi bahan organik membentuk kalsium, aktifitas ini dikontrol dengan pH di laut dan tingkatan karbondioksida di atmosfer. Secara umum reaksi yang terjadia adalah sebagai berikut: Ca2+ + 2HCO3− → CaCO3 + H2O + CO2→ CaCO3 + CH2O + O2 (10.3) Pembentukan kalsium fotosintesis Ca2+ + 2HCO3− ← CaCO3 + H2O + CO2 ← CaCO3 + CH2O + O2 terlarut (10.4) respirasi Dalam dugaan Schiebel (2002) planktonik foraminifera mampu menghasilkan karbon 0.36–0.88 gross ton (Gt) per tahun dimana 32-80% terdeposit sebagai CaCO3 di dalam laut, dan diprediksi kalsium yang ada sama dengan 0,16 Gt di sedimen laut. Kalau didasarkan pada perhitungan Milliman (1993), endapan CaCO3 di dasar laut kurang lebih 40-50% adalah kalsium (Ca). Sedang di daerah pelagik akumulasi CaCO3 maksimal di perkirakan 0,09 Gt per tahun, kandungan itu ada pada coccolithphore ( diasumsikan foraminifera ada sebanyak 50%). Jumlah karbonat ini nantinya akan mengendap sebagai sedimen diperkirakan 0,045 Gt per tahun (kurang-lebih 50% akan tenggelam ke permukaan dasar laut), ~ 289 ~ beberapa foraminifera terlarut di sedimen itu, kemungkinan besar “lysocline” yang terlarut (Archer dkk, 1989). Produksi total CaCO3 oleh foraminifera di samudera terbuka diperkirakan oleh Schiebel (2001) ada sebanyak 3,24 Gt per tahun, sebanyak 65% dari jumlah itu akan terlarut di perairan. Dalam kaitan siklus karbon global, kemungkinan 10% akan menjadi karbon dioksida yang akan masuk ke atmosfer (Siegenthaler and Sarmiento 1993). Apabila konsentrasi karbondioksida di udara bertambah maka pH permukaan samudera akan menurun (Brewer dkk, 1997). Secara teoritis pembentukan kalsium oleh foraminifera di perairan berkaitan erat kondisi pH (derajat keasaman), halmana bila pH rendah maka pembentukan kalsium (calcification) dari foraminifera akan terhenti. Seandainya CO2 di atmosfer konstan maka bisa terbentuk sebanyak 0,4 gross ton karbon pertahun. Mekanisme kerja biomineral di foraminifera adalah sebagai berikut: sesungguhnya di endoplasma terdapat konsentrasi kalsium berlimpah, disamping itu terkandung juga magnesium (Mg), fosfat (P) dan kemungkinan sulfat (S). Sebagai organism hidup foraminifera mengandung matriks organik yang berfungsi membentuk granula mineral. Unsur kalsium merupakan cikal-bakal penyusunan kristal CaCO3, yang kemudian terendap sehingga terbentuk suatu gugus matriks organik. Pada saat itu kulit mulai terbentuk, dalam kerja penyusunan kulit ada dua tahapan yang terjadi yakni: pertama, magnesium yang ada pada kalsit yang halus akan melekat menyusun matriks organik; kedua, mulai terjadi pembentukan kalsium, dan secara massif terjadi pengendapan Mg yang rendah sehingga terbentuk kulit kalsit. Kalsit ini yang akan membentuk lapisan agregat kristal atau butiran yang agak lebih besar sehingga secara perlahan membentuk kerangka. . Proses biomineralisasi membentuk kalsit sekunder dalam gelembung air laut di sitoplasma dan modifikasinya mengurangi rasio unsur Mg dan Ca, disajikan pada gambar berikut. ~ 290 ~ Gambar 10.17. Skema Proses Pembentukan Kalsium di foraminifera. [V= vacuola; P=pseudopodia; S=simbiose alga; d= ruang batas biomineralisasi; IC= intralocullar sitoplasma; ec= extralocullar sitoplasma dan sw= seawater] Sumber: Erez J (2003) “The Source of Ions for Biomineralization in Foraminifera and Their Implications for Paleoceanographic Proxies” Selama sel memompa atau bergerak maka endositosis akan membentuk gelembung/rongga airlaut (vakuola) di dalam ~ 291 ~ sitoplasma, sehingga pH naik dan memungkinkan unsur Ca 2+ dan CT berada di gelembung udara itu. Kemudian gelembung itu didorong ke luar sampai di ruang batas biomineralisasi, yang akhirnya CaCO3 terendap di sel, dan kemungkinan kandungan Mg sangat rendah di airlaut dalam sel itu. Adanya difusi karbon dioksida di gelembung udara sebaliknya ion CO32- akan ditranspor melalui membrane sehingga terjadi penumpukan karbon (ter Kuile dkk. 1989a). Karena adanya proses fotosintesis tetap berlangsung, maka pH di sekitar gelembung airlaut itu tetap terjaga. Namun pada endoplasma terjadi kompetisi CO2 antara simbiose alga dan alkalinitas yang ada di gelembung air laut sehingga bisa terganggu pembentukan karbonat. Bagaimana hubungan antar Ca2+ dan CO32- dalam menyusun endapan kalsium karbonat, diuraikan sebagai berikut. Diketahui umum bahwa komponen utama air laut adalah unsur Ca2+ and CO32−, dimana konsentrasi Ca2+ ada sebanyak 10-11 mM sedang CO32− hanya 100−300 M artinya kandungan karbonat lebih rendah (50%) dari kalsium. Kedua unsur ini akan membentuk senyawa baru yang dikenal sebagai kalsium karbonat (CaCO3). Secara umum CaCO3 mengendap akan berpengaruh pada alkalinitas, halmana jumlah alkalinitas akan turun sehingga berakibat pula pada turunnya pH. Untuk menaikan kadar keasaman di perlukan sejumlah CO32− sehingga konsentrasi CT akan turun. Apabila derajat keasaman (pH) naik di gelembung, disana telah terjadi penguraian CO2(aq) sehingga terbentuk CT dan bila proses ini berjalan terus maka mulailah terjadi proses penyusunan kalsifikasi. Demikian pula di terumbu karang mekanisme ini juga terjadi Al Horani dkk (2003). Kalau di air laut konsentrasi CO32− ada sekitar 1 mM diperkirakan setengah dari konsentrasi adalah CT, kecuali bagi foraminifera pH di airlaut pada vakuola akan naik sehingga endoplasma sampai ruang pembentukan kalsium pHnya berkisar 9. Apabila vakuola itu diluar endoplasma ~ 292 ~ kemungkinan akan terjadi akumulasi sehingga konsentrasi C T akan tinggi sebab pH di sitosol ada sekitar 7,2 (kondisi normal bagi sel organisme laut). Foramininfera punya peran penting dalam siklus karbon global di laut, disamping itu kerangka foraminifera memberikan informasi yang berarti bagi paleoseanografi. Untuk proses biomineral pada foraminifera, mineralnya berawal dari gelembung air laut (vakuola) yang ada di sel , dimana tempat itu tersedia komponen dasar untuk kalsifikasi. Kemudian proses pengkapuran oleh kegiatan biologi akan membentuk matriks organik sehingga lapisan kulit terbentuk. Kristal yang terbentuk dalam bentuk tiga dimensi merupakan endapan matriks organik , di dalamnya terdapat pelbagai komposisi kimia maupun isotop. Sebagian besar proses kalsifikasi berjalan terus dengan adanya laminasi sekunder yang melibatkan kristal epitaxial. Biasanya kalsifikasi sekunder oleh pseudopodia terjadi dalam ruang yang dibatasi sedang ion utama untuk proses biomineralisasi berasal dari vakuola air laut. Gelembung airlaut di dalam organism peran terutama menaikan nilai pH sehingga karbon organik yang terlarut akan bertambah. Kalsit yang ada dalam ruang dibatasi itu memiliki fungsi rendahkan endapan Mg. Kalsium yang tersimpan akan membantu percepatan klasifikasi, biasanya Ca yang tersimpan ini ada dalam bentuk padat atau bentuk amorf. Pengurangan Mg di foraminifera terjadi di gelembung air laut. Mekanisme ini sama halnya untuk karbonat, dimana peningkatan CO32- biasanya dekat situs kalsifikasi, kalau pada foraminifera terjadi pada gelembung (vakuola) air laut sedang di karang terjadi proses Ca2+- ATPase. Organisme foraminifera dan karang mengandung pelbagai trace elemen seperti Sr, Ba, Cd, U dan sebagainya. Disamping itu oleh adanya fotosintesis maka memungkinkan terjadi struktur organik. ~ 293 ~ ⑪ KOMPOSISI DAN DISTRIBUSI KOBALT KAYA FERROMANGAN (Fe-Mn) DI KERAK SAMUDERA B atuan kobalt yang kaya akan Fe-Mn oksihidroksi atau sering disebut batuan Fe-Mn, banyak ditemui pada tumpukan tanah dasar laut, dataran tinggi di dasar laut , gunung dasar laut dan di dataran abisal. Bermula dari sedimen yang diangkut oleh arus pada jutaan tahun yang lalu, kemudian mengeras membentuk batuan di dasar samudera. Batuan ini sangat penting, karena berpotensi menghasilkan terutama kobalt, namun tidak hanya unsur itu, didalamnya banyak terdapat titanium, cerium, nikel, platina, mangan, thallium, tellurium dan unsur-unsur kimia lainnya. Lapisan batuan di dasar lautan itu bentuknya seperti aspal di jalan raya dengan ketebalan diatas 2,5 m atau seperti gumpalan kotoran yang telah mengeras di dasar laut. Halmana kerak Fe-Mn terbentuk sebagai endapan yang terjadi pada ambien suhu rendah di dasar perairan atau disebut sebagai “hidrogenetika”, dapat juga terjadi adanya kombinasi antar hidrogenetika dan hydrothermal (endapan berasal dari aktivitas vulkanik). Umumnya kerak Fe-Mn bersisikan sejumlah besi dan mangan yang memperkaya unsur di kerak kobalt, termasuk juga adanya unsur timah, bismuth dan platina, kemungkinan juga titanium serta bahan yang jarang ditemui seperti tellurium, thallium, fosfat dan sebagainya. Beberapa komponen dengan komposisinya di air laut, lithosfer dan batuan Fe-Mn di sajikan pada table 11.1. Endapan kobalt yang kaya kandungan “ferromanganese” merupakan sumber daya lam nir-hayati laut yang memiliki ~ 294 ~ nilai ekonomis yang tinggi, seperti prediksi ekonomi yang dikemukakan oleh Rompas dkk (2013) di Laut Nusantara ada sebesar 256 miliar $ US/tahun, nilai itu lebih tinggi dari minyak dan gas bumi (68 miliar $ US). Unsur kimia yang dikandung pada mineral seabed banyak digunakan untuk kepentingan teknologi tingkat tinggi atau “high-tech”, seperti bahan bakar peluncur satelit/roket, dan unsur besi, timah, tembaga dan tellurium menjadi bahan baku pembuatan badan roket, pesawat, alat-alat perang, armada transpor laut-darat, dan belakang ini berkembang sebagai bahan bagunan gedunggedung bertingkat. Begitu bernilai endapan di samudera, maka organisasi dunia, Perserikatan Bangsa-Bangsa (PBB) membentuk satu komisi khusus untuk mengurusi bidang ini, yaitu di beri nama “International Seabed Authority/ISA”. Kantor utama komisi ini berada di Kingston, Jamaica. Komisi bersidang dalam 4 tahun sekali, ditahun 2008, penulis pertama buku ini pernah menjadi sebagai anggota delegasi RI, dalam sidang itu sungguh besar minat negara-negara maju untuk menguasai kekayaan mineral yang tersimpan di dasar laut, terutama di kawasan Samudera Pasifik. Seperti pada sidang ISA tahun 2008, telah memutuskan beberapa negara maju : Cina, Amerika, korea dan costarica di beri kewenangan mengeksplorasi polimetalik nodul dan kerak kobalt yang ada di kawasan Pasifik berbatasan dengan negara Indonesia dan Papua new Guinea. Memang disaat itu komisi ISA dalam sidang telah mempersilahkan Indonesia untuk memanfaatkan area itu, karena negara yang terdekat. Tetapi Indonesia tidak memiliki teknologi dan dana yang cukup untuk melakukan eksplorasi dan eksploitasi mineral yang di dasar samudera, maka sidang memutuskan untuk diberi kesempatan negara-negara lain mengajukan permohonan kegiatan eksplorasi dan ekploitasi. ~ 295 ~ Tabel 11.1 Komponen Mn, Besi, Kobalt, Nikel, Platina, Cerium, Tembaga dan Tellurium (% berat) pada bebatuan Fe-Mn di Samudera. Fe/Mn Mangan Mn/air laut Mn/lithosfer Besi Fe/air Laut Fe/lithosfer Kobalt Co/air laut Co/lithosfer Nikel Ni/air laut Ni/lithosfer Platina Pt/air laut Pt/lithosfer Cerium Ce/air laut Ce/lithosfer Tembaga Cu/ air laut Cu/lithosfer Tellurium Te/airlaut Te/lithosfer Air Laut 1,2 5,0 X 10-9 6.0 X 10-9 1.0 X 10-10 5.0 X 10-8 2,4 X 10-11 2,8 X 10-10 2,5 X 10-8 1,66 X 10-11 - Lithosfer 57 0,095 1,9 X 107 54 9.0 X 10-8 2.5 X 10-3 2.5 X 106 8.0 X 10-3 1.6 X 105 4.0 X 10-7 1.7 X 104 7.0 X 10-3 2.5 X 107 5,0 X 10-3 2.0 X 105 1.0 X 10-6 0.6 X 10-5 - Batuan Fe-Mn 0,7 23 4,6 X 109 242 17 2,8 X 109 3,1 0,70 7,0 X 108 280 0,48 9,6 X 106 60 5 X 10-5 2,1 X 106 125 0,18 6,4 X 108 26 0,009 3,6 X 106 18 0,005 3,6 X 108 5000 Sumber : Hein (2004). Hakekatnya, mempelajari komposisi kandungan kimia yang ada di kobalt yang kaya akan Fe-Mn memiliki arti penting, selain sebagai sumber daya laut bernilai ekonomis tinggi (uraian diatas), tapi juga berguna bagi para ahli palaentologi, karena bahan endapan itu telah terbentuk sejak 60 juta tahun lalu, dan sekaligus merupakan rekaman sejarah iklim yang berlaku di daerah tersebut. ~ 296 ~ Para ilmuan di bidang geologi di tahun 1970-an mulai mendiskusikan tentang kandungan “ferromanganese” (Fe-Mn), bahwa ternyata Fe-Mn tidak hanya berasal dari bongkahan (nodul) dataran abisal saja, tetapi juga berasal dari kerak samudera yang disebut bongkahan gunung bawah laut ( seamount nodule). Morfologi kedua nodul tersebut berbeda. Dalam table 11.2. disajikan perbedaan “ferromangan oksida” di kedua lokasi itu. Prinsip dasar bongkahan yang ada disedimen ada dalam bentuk butiran kecil yang mengumpal dan mengeras berwujud bebatuan, padatan seperti tulang keras dan ada juga lapisan di atas permukaan sedimen. Mekanisme penyusunan sedimen atau pembentukan kerak kobalt yang kaya akan Fe-Mn melalui proses diagenetik, telah diuraikan secara rinci pada bagian (bab) sembilan. Untuk proses hidrogenetik umumnya melalui suatu interaksi kimia di perairan, halmana sedimen berasal dari daratan, atmosfer dan aliran sungai masuk ke laut, sementara dalam proses tenggelamnya material itu ke dasar perairan terjadilah interaksi kimia baik organik maupun anorganik, pada akhirnya bahanbahan itu mengendap (terdeposit) di dasar laut, kemudian lapisan endapan di atas permukaan dasar perairan maupun di dalam sedimen itu terjadi reaksi kimia yang sangat kompleks. Sedang proses pembentukan lewat hidrothermal, biasanya ada gerakan sentrifugal bumi, keluarkan magma yang menyuplai partikel ke dasar laut, disamping itu ada juga partikel dari luapan vulkanik masuk ke atmosfer yang akhirnya jatuh ke laut dan terdeposit di dasar perairan laut. Semua material tersebut yang masuk ke laut akan melewati suatu proses hidrogenetik dengan pelbagai bentuk reaksi kimia dan biokimia sehingga terjadi peleburan beberapa kimia yang akhirnya membentuk suatu ikatan kimia yang kompleks dan terendap didasar perairan (Hein dan Morgan, 1999). ~ 297 ~ Tabel 11.2 Klasifikasi Endapan Fe-Mn oksida didasarkan pada Bentuk, Proses dan lokasinya. Hidrogenetik Hidrothermal Diagenetik Nodul (Bongkahan) Abisal, Dataran tinggi laut, Seamount.1) Lapisan keras dan zona vulkanik Dataran abisal, permukaan dasar lautan Kerak (bebatuan) Lapisan tipis, pecahan vulkanik 2) aktif keluarkan pecahan, bahan vulkanik ---- Pecahan vulkanik, lapisan agak tebal Bahan vulkanik, Pecahan besar 5) Lembah, pusat tumpukan, Lingkungan vulkanik Diatas sedimen Sedimen keras pecahan vulkanik yang agak besar Gundukan tanah ------ Hidrogenetik & hidrothermal Pecahan bebatuan ukuran sedang Hidrogenetik & Diagenetik Dataran abisal, Permukaan dasar laut Lokasi Bahan aktif vulkanik, gunung didasar laut, zona bebatuan Kemiringan abisal Lapisan tipis (kerak dengan penuh bebatuan) ---- ------ Pecahan bebatuan vulkanik 4) Lapisan tipis pecahan vulanik Dekat daerah vulkanik ----- ------ ----- ------ ------- ------ Pinggiran kontinen 3) Sumber: Hein (2004) ~ 298 ~ Semua lokasi inti nodul. Tepi kontinen, Dekat vulkanik, Pecahan kecil Keterangan table 10.14 (diatas): 1) Biasanya berada di bukitan dasar laut, lereng kontinen dan pelataran (shelf). 2) Gunung dasar laut, guyot (seperti gunung tapi diatasnya datar) dan bukitan 3) Fe-Mn yang mengkilap (bercahaya) dan bentuk keras. 4) Kebanyakan terperangkap pada lembah berbentuk V, bentuk keras. 5) Lumur pasir, pasirbebatuan dank eras seperti semen. Umumnya morfologi kerak samudera dan bongkahan akan berbeda dan itu sangat tergantung pada lokasi tangkapan sedimen, seperti bentuk V (vernadite) dan yang lainnya “todorokite”. Demikian juga komposisi kimianya sangat berbeda, seperti ada lokasi tertentu tinggi kandungan kobalt dan ada juga yang tinggi kandungan tembaga, di tempat lain ada juga kandungan kobalt rendah tapi mangan tinggi. Umumnya perbedaan komposisi di pengaruhi juga faktor kedalaman dan daya sebaran komponen. Sebagaimana dalam table 11.2, proses hydrothermal yang terjadi di bawah dasar perairan, dapat menghasilkan elemen besi, Mn hidroksida dan oksihidroksida, dimana zat-zat itu akan membentuk lapisan mangan yang padat pada sedimen yang bersumber dari bahan vulkanik. Sedang jumlah dan komposisi besi dan Mn melalui proses hidrogenetik pada bongkahan Fe-Mn dapat dilihat pada table 11.1 diatas. Kalau dalam endapan hydrothermal ditemui kandungan besi/mangan sangat bervariasi yakni, dari 24000 (diatas 54% bebatuan besi) sampai 0,001 (diatas, 52% mangan oksida). Intinya sedimen di dasar laut banyak juga mineral besi dan mangan yang berasosiasi dengan pelbagai elemen membentuk kerak Fe-Mn (Hein, 2004). Kerak atau bebatuan Fe-Mn banyak terdapat di gunung bawah laut dan gundukan tanah di atas permukaan laut, secara global ~ 299 ~ terdapat di lekukan-lekukan di dasar perairan Pasifik dan Atlantik serta Samudera India. Namun demikian, penelitian di gunung bawah laut (seamount) banyak dilakukan di Pasifik bagian ekuator, lebih khusus di kawasan ZEE (Zona Economic Exclusive) negara federal Micronesia, kepulauan Marshall, Kiribati serta Samudera Pasifik bagian tengah ( Hein, 2004). Lebih kurang 50.000 gunung bawah laut di Samudera Pasifik, Atlantik dan India telah di ketahui kerak Fe-Mn relatif sedikit di gunung bawah laut tetapi jumlah yang banyak terdapat di gundukan tanah yang tersebar merata di atas permukaan dasar laut. Kemudian secara komposisi material yang ada di gundukan tanah itu umumnya berasal dari hidrothermal (bahan aktif vulkanik), sedang kerak yang terbentuk berasal sedimen asli di lokasi itu hanya berkisar <30% (Bury, 1989; Hein dkk, 2000). Sedang tipe hidrogenetik-hidrothermal yang ditemui di Pasifik bagian barat sebagian besar bersumber dari vulkanik aktif (Hein dkk, 1987). Gundukan tanah didasar perairan yang memanjang di kawasan barat dan selatan-barat Pasifik serta bagian tengah selatan dan timur Pasifik umumnya material itu berasal vulkanik. Kerak Fe-Mn biasanya berada di kedalaman 400-4000m, tetapi pada kedalam 1000 sampai 4000 meter lapisan kerak Fe-Mn lebih banyak dibandingkan dengan kedalaman lainnya. Kalau kandungannya kaya akan kobalt umumnya berada di kedalaman 800-2200 meter dimana daerah itu merupakan zona oksigen minimum (lihat gambar 11.1) Kalau di samudera Pasifik lapisan batuan Fe-Mn umumnya terbentuk di kedalaman 1500-2500 meter dimana kebanyakan berada di sekelilingi dan dilapisan atasnya gunung bawah laut. Dengan bertambahnya kedalaman maka kandungan kobalt bertambah, tetapi perairan di Pasifik selatan memperlihatkan kandungan kobalt lebih dominan di kedalaman rendah (tidak terlalu dalam), dimana wilayah ~ 300 ~ Gambar 11.1 Profil Kelarutan Mangan dan Fosfat Dalam Kaitannya dengan Kandungan Oksigen Perairan di atas Gunung Bawah Laut. Sumber : Hein (2004) zona oksigen minimum mulai berkurang banyak terjadi di Pasifik bagian selatan. Sesungguhnya kandungan kobalt maksimum dan pembentukan lapisan secara umum terjadi pada kedalaman 1000-1500 m (Cronan, 1984). Material yang ada di perairan (terapung dan melayang) akan tenggelam ke dasar jatuh di punggung gunung bawah laut, disamping itu juga bahan vulkanik jatuh di gundukan tanah di dasar laut atau di gunung bawah laut, dalam periode panjang material itu akan tersusun menjadi lapisan yang keras seperti batu padat. Menurut Hein dkk (2000) kandungan kerak FeMn ada di bagian tengah dan agak ke bagian bawah gunung. Dalam kenyataan sedimen pelagik di gunung bawah laut dan gundukan tanah tidak memberikan dukungan bagi pembentukan kerak. Tetapi debu vulkanik seperti karang batu ~ 301 ~ yang jatuh maupun yang keluar dari magma di dasar laut merupakan cikal-bakal kerak Fe-Mn. Prinsip dasar material vulkanik banyak tenggelam di kedalaman 3000 meter dekat dengan pulau bahkan membentuk gunung bawah laut berbentuk atol, bentuk seperti itu bisa menampung kotoran di perairan serta pelbagai komponen yang terdapat dimaterial vulkanik, yang pada akhirnya terjadilah interaksi kimia sehingga membentuk kerak samudera (Moore dkk, 1994). Perairan Pasifik tengah, sedimen yang terbentuk dari material yang melayang di perairan dan tenggelam ke dasar perairan umumnya memiliki ketebalan hanya 5-40 mm dan proses tersusunnya memakan waktu 10-30 jutaan tahun. Makin bertambah waktu lapisan itu makin menebal, disaat lapisan > 80 mm akan membentuk substrat batuan cretaceous. Intinya, kerak Fe-Mn di gunung bawah laut di Samudera Pasifik telah terbentuk sejak 65-95 juta tahun yang lalu, sedang sedimen yang menutupi dasar samudera Pasifik di perkirakan di mulai pada 25 juta tahun yang lalu. Kalau di Samudera Atlantik dan India jarang ditemui kerak Fe-Mn, kalau pun ada hanya terdapat di sekitar gunung bawah laut di new England (Atlantik bagian utara agak ke barat) dengan ketebalan diatas 125 mm. Untuk di Samudera India ada di bagian tengah Samudera India dengan ketebalan ± 72 mm. Secara umum gunung bawa laut puncaknya tidak datar diliputi lapisan keras bukan sedimen setebal 0-150 meter, dan ada juga permukaan yang datar (guyot) dengan ketebalan 0-500 meter. Bagian samping gunung itu berbentuk lapisan bukit kecil (± 10 meter tingginya) seperti “terasering” yang berlapis-lapis sampai ke bagian bawah gunung. Bukit di pinggiran gunung bawah laut itu ada yang membentuk kemiringan 20 derajat tetapi kebanyakan yang ditemui rata-rata kemiringan 40 derajat (Hein dkk, 2000). Kemiringan gunung kecil itu merupakan tempat akumulasi material sehingga terbentuklah lapisan keras dan disitulah kerak Fe-Mn terbentuk. Lapisan 2 ~ 302 ~ meter di bawah sedimen permukaan kandungan Fe-Mn berlimpah, menurut Yamazaki (1993) bahwa di lapisan itu ke arah lebih dalam lagi ditemui kandungan Fe-Mn dua kali lebih jumlahnya, maka di lapisan itu cocok untuk eksplorasi tambang. Karakteristik kerak Fe-Mn Hakekatnya, bebatuan di permukaan dasar laut disebut “botryoidal” dan ukurannya bervariasi ada yang berukuran millimeter (mikrobotryoidal) sampai dengan ukuran sentimeter. Oleh adanya gerakan (aliran) arus yang kuat, bebatuan ini akan berubah secara masif yang pada akhirnya membentuk granula dan keras dimana di dalam porosnya terdapat unsur kobalt yang tinggi. Perkembangan “botryoidal” menjadi lapisan padat dapat terjadi secara cepat tergantung pada kekuatan aliran arus, namun demikian penyusunan botryoidal ini sampai terwujud kerak di perlukan waktu yang sangat panjang. Profil bebatuan ini yaitu ketebalan dan strukturnya sangat tergantung pada kondisi oseanografi di lokasi itu. Umumnya butiran “botryoidal” yang menutupi batuan dengan ketebalan <40 mm adalah timah berwarna hitam. Lapisan pada ketebalan 40-80 mm berubah warna dari hitam ke warna coklatan dengan tanda garis titik-titik, biasanya mulai terjadinya pembentukan fosfat. Biasanya pada ketebalan > 80 mm akan terbentuk lapisan makroskopis di lapisan itu terdapat banyak fosfat. Dalam kenyataan kisaran pada lapisan 1 – 50 mm banyak terdapat batuan granit yang kaya akan detritus merupakan proses pembentukan kerak Fe-Mn, dan kecepatan pembentukannya tergantung pada pengendapan oksida (Hein dkk, 1992). Prinsip dasar kandungan bebatuan Fe-Mn berkembang tergantung juga pada substrat, apakah bahan vulaknik, batukapur, lumpur keras dengan kelimpahan fosforik ~ 303 ~ (sedimen) dan sebagainya, namun substrat dari bahan vulkanik lebih kuat menciptakan kerak/bebatuan Fe-Mn. Ketebalan lapisan bebatuan di perairan tergantung pada keadaan oseanografi dan substrat dimana unsur itu berkembang. Kandungan mineral Perbedaan ukuran kandungan mineral pada pebatuan Fe-Mn yang terbentuk oleh proses hydrothermal dan diagenetik tidak terlalu sulit, hanya dapat di lihat melalui kandungan besi dan mangan yang terendap (deposit). Dalam kenyataan pada fase kristal sesungghuhnya terkandung besi dan δ-MnO2 (ferruginous vernadite) yang berlimpah (Bolton dkk, 1990). Ukuran kristal dan kandungan mangan bisa diterah dengan menggunakan refleksi sinar X-ray pada 1,4 Å dan 2,4 Å. Halmana pada fase kristal umumnya terdapat δ-MnO2 diatas 95%, didalamnya terdapat butiran mineral seperti: kuarsa, plagioclase, kalium, pyrosen, phillipsite dan CFA (carbonat fluorapatite (Hein, 2004). Kandungan mineral pada kerak FeMn dari samudera Pasifik disajikan pada table 11.3. Tabel 11.3. Kandungan Mineral pada Kerak Fe-Mn di Samudera Pasifik. Dominan δ-MnO2 (besi-vernadit), besi-oksihidrksida (Ferroxyhite) Sebutan Lazim CFA, kuarsa, plagioclase, smectite Diluar kelaziman Phillipsite, goethite, todorokite, kalsit, K-fieldspar, pyrosen, opal-A, barite, amphibole, magnetite, amorf, aluminosilikat. Sebutan Lain Halida, illida, clinoptilolida, lepidocrosida, manjiroida, manganida, palygorskida, klorida, dolomida, stevesida, kutnahorida, hematida,modrnida, natrojarosida, manganosida, maghemida, lithiophorida, analsida CFA= Karbonat fluorapatit. Sumber: Hein (2004). Selain mineral tersebut ada juga bagian kerak dilapisi dengan kandungan fosfat dengan berisikan 30% karbonat ~ 304 ~ fluorapatit tetapi sesungguhnya ketebalan lapisan karbonat fluorapatit (CFA) di kerak Fe-Mn tidak melebihi 10%, namun disamping itu pula terdapat besi amorf oksihidrosida (δFeOOH, feroxyhyte) yang sebetulnya hasil perkembangan dari δ-MnO2 (Burns and Burns, 1977). Di samudera Pasifik kuarsa adalah bagian dari plagioclase sering disebut eolian yang umumnya menutupi bagian atas kerak, material ini berasal buangan gunung berapi. Kalau todorokite biasanya bongkahan Fe-Mn diagenetik sedang endapan mangan hydrothermal relatif sedikit. Di samudera Pasifik, khususnya di laut lepas California ditemui hanya 5% todorokite, mengapa demikian dikarenakan produktivitas biologi sangat tinggi sehingga potensi oksidasi adalah rendah, berbeda dengan wilayah pasifik tengah sampai ke bagian barat. Untuk karbonat fluorapatit (CFA) umumnya terdapat sebanyak 28% tetapi di Pasifik bagian barat dan tengah ditemui sebanyak 34%, sedang di laut lepas California sampai ke bagian utara Pasifik tidak ditemui kandungan karbonat fluorapatit. Tetapi kandungan CFA di samudera Atlantik dan India presentasinya kecil, umumnya lapisan itu belum lama terbentuk. Hasil riset membuktikan proses pembentukan lapisan fosfat pada Fe-Mn terjadi dalam dua periode, yaitu 24 juta tahun dan 34 juta tahun yang lalu (Hein dkk, 1993). Perkembangan pembentukan kerak/pebatuan Fe-Mn dengan proses hidrogenetik berjalan sangat lambat, yakni <1 11 mm per jutaan tahun, namun kebanyakan yang terjadi pada 1 - 6mm/jutaan tahun (lihat gambar 11.2). Dalam pembentukan pebatuan itu serapan elemen kecil melalui oksihidroksida berjalan sangat lambat, sehingga tidak bisa dipungkiri pertumbuhannya memakan waktu yang panjang sampai jutaan tahun. ~ 305 ~ Jumlah Sampel Rata-rata Pertumbuhan (mm/Jutaan tahun) Gambar 11.2. Kecepatan Perkembangan Bebatuan Fe-Mn secara Hidrogenetik Sumber: Hein dkk. (2000). Pengukuran umur dan kecepatan pembentukan pebatuan FeMn dapat dilakukan dengan metode radioaktif uranium dan beryllium hanya bisa terdeteksi pada bagian luar kerak setebal 2 – 20 mm. Atau dapat juga mempergunakan cara paleontologi yaitu memprediksi umur dengan memperhatikan substrat di pebatuan. Kedua metoda ini dapat menaksir umur, kecepatan perkembangan serta fase disaat tidak berkembang. Kalau menggunakan teknik pengukuran dengan isotop beryllium seharusnya ketebalan kerak lebih kurang 20 mm agar dapat terdeteksi umur pebatuan lebih baik, jika lebih dari itu bisa terjadi kesalahan. Hasil identifikasi kerak Fe-Mn dari Pasifik bagian ekuator ternyata lapisan kerak telah terbentuk sejak 60 juta tahun yang lalu (Hein, 2004). ~ 306 ~ Dapat juga dipergunakan metoda perbandingan isotop osmium, biasanya dengan cara ini digunakan pada pebatuan yang berumur 65 juta tahun lalu, dimana setiap lapisan pebatuan atau nanofosil biostratifikasi yang terbentuk memperlihatkan susunan lapisan tahunan. Dari data itu di perbandingankan sehingga dapat persentasenya, kemudian hasil kalkulasi itu di petakan kedalam grafik, cara ini disebut kurva Cenozoic air laut (Janin, 1985; Cowen dkk, 1993). Pada prinsipnya, untuk mengukur umur dan perkembangan pebatuan Fe-Mn dapat digunakan pelbagai metoda baik secara palaentologi maupun menggunakan radio isotop. Secara umum, umur lapisan pebatuan menentukan jumlah dan komposisi unsur kimia yang dikandungnya, artinya makin tua kerak/pebatuan itu, kelimpahan komposisi kimia yang dikandungnya makin bervariasi. Kerak Fe-Mn yang terbentuk dari proses hidrogenetika umumnya memiliki kandungan besi : mangan dengan perbandingan 0,4 dan 1,2, namun kebanyakan di temui adalah 0,7±0,2. Bagi pebatuan di pinggiran kontinen yang merupakan campuran antara proses hydrothermal dan hidrogenetika perbandingan komposisi Fe/Mn ada sekitar 1 dan 3, tetapi kebanyakan yang ditemui 1,3-1,8 (dapat dilihat pada table 11.4) Kobalt disuatu pebatuan sebagai logam yang memiliki nilai ekonomis tinggi (greatest economic potential) kandungannya berkisar 0,05% – 17% (500 – 17.000 ppm), tetapi jika pebatuan itu bersumber dari pelbagai jenis lapisan (baik di kerak maupun bongkahan abisal), maka nilai rata-rata kandung kobalt dipekirakan ada sekitar 0,19% - 0,74% (1900-7400 ppm) (lihat table 11.4). Sesungguhnya kobalt merupakan endapan logam yang terbentuk melalui proses hidrogenetika (Halbach dkk, 1982). Demikian juga, nikel dan platinum merupakan unsur kimia yang bernilai ekonomis penting. Pada pebatuan biasanya terkandung nikel sebesar 1,1% (11.000 ppm) dan platinum ada sekitar 1,3 ppm. Tetapi bongkahan (nodul) Fe-Mn di daerah ~ 307 ~ abisal banyak terkandung elemen seperti: besi, kobalt, platinum, timah, arsenik, bismut, bromida, vanadium, fosfat, kalsium, titanium, strontium, tellurium, aluminium, kalium dan kadmium. Sesungguhnya unsur kimia yang ada kerak FeMn lebih banyak dari yang dikandung oleh air laut, kecuali bromida, klorin dan natrium. Kelimpahan kandungan unsur kimia di pebatuan seperti: bismuth, kobalt, Mn, titanium,besi, tellurium, tembaga dan thorium bisa mencapai 108 sampai 1010 kali lebih banyak. Tetapi kalau unsur kimia seperti: tin, hafnium, zirconium, aluminium, yttrium, scandium, thallium, nikel, kalsium, niobium, indium, tembaga, germanium, zink, tungsten dan tantalum konsentrasinya 106 sampai 108 lebih banyak dari di air laut. Kalau kita bandingkan kandungan kimia yang ada di pebatuan Fe-Mn dengan yang ada di lithosfer, khususnya kimia tellurium umumnya di pebatuan lebih banyak 5000 kali dari yang terkandung di lithosfer, namun untuk kimia molybdenum, thallium, antimony, kobalt, Mn, bismuth, arsenik, selenium dan timah hanya 100 – 5000 kali lebih banyak. Kerak/pebatuan maupun bongkahan Fe-Mn sudah menjadi incaran petambang dunia, karena memiliki nilai ekonomi tinggi, tidak hanya kobalt, nikel, mangan dan platinum, tetapi juga unsure kimia titanium, cerium, tellurium, thallium, zirconium dan fosfat (Hein, 2004). ~ 308 ~ Tabel 11.4. Komposisi Kimia di Kerak Fe-Mn yang ada di Samudera Pasifik, India dan Atlantik serta bongkahan di Zona Clarion-Clipperton dan bongkahjan abisal lainnya. ~ 309 ~ Lanjutan Tabel 11.4 . ~ 310 ~ Sumber: data di Pasifik bagian barat-utara (Ku, 1977 disitasi oleh Hein, 2004); data di Hawai (De Carlo dan McMurttry, 1992); Data di Pasifik Selatan (Exon, 1977) dan Hein (2004). ~ 311 ~ Secara umum ahli geokimia berpendapat bahwa zat kimia yang berasosiasi membentuk kerak/pebatuan dapat dilalui dengan 5 fase, yaitu δ-MnO2, besi oksihidroksida, aluminiumsilika, CFA (carbonat fluorapatite) dan residu biogenik. Kalau zat kimia Mn, kobalt, nikel, kadmium dan molybdenum selalu bersenyawa dengan fase δ-MnO2. Namun demikian, lebih kurang 40% dari hasil kegiatan riset menunjukan jenis kimia timah, vadium, zink, natrium, kalsium, strontium, magnesium dan titanium juga bisa berasosiasi dengan fase δ-MnO2 (Hein, 2004). Zat kimia besi dan arsenik lebih mudah bersenyawa dengan besi oksihidroksida, walaupun juga elemen vanadium, tembaga, timah, yttrium, fosfat, chromium, beryllium, strontium, titanium dan cerium bisa bersenyawa dengan fase besi oksihidroksida. Untuk fase detrital (aluminiumsilika) yang sering bersenyawa adalah silikon, aluminium dan kalium, tetapi elemen kimia seperti: titanium, chromium, magnesium, besi, natrium dan tembaga mampu juga berasosiasi. Zat kimia yang punya sifat lebih mudah bersenyawa pada fase CFA adalah kalsium, fosfat dan CO2, tetapi kimia strontium, yttrium, molybdenum, barium, cerium dan zink mampu bersenyawa di fase CFA namun hanya di bagian tertentu saja atau tidak merata di semua pebatuan. Sedang fase residu biogenik zat kimia yang bisa bersenyawa meliputi barium, strontium, cerium, tembaga, vanadium, kalsium dan magnesium, namun zat besi, arsenik, natrium, molybdenum, yttrium, fosfat, karbon dioksida, timah, titanium dan nikel mampu juga berasosiasi tetapi hanya di bagian-bagian tertentu saja. Sesungguhnya zat besi memiliki kemampuan bersenyawa lebih kuat pada fase besi-oksihidroksida, namun demikian zat ini mudah bersenyawa melalui fase-fase lain termasuk fase campuran antar δ-MnO2 dan besioksihidroksida. Kalau pada fase detrital dan biogenik besi ~ 312 ~ ada dalam bentuk senyawa pyroxene, amphibole, smectite, magnetite dan spinel sebagai mineral. Kekuatan zat besi bersenyawa dengan unsur lain di kerak sangat tergantung pada kelimpahan ddisetiap fase (Hein dkk, 2000). Pada fase CFA biasanya berlangsung di pebatuan yang padat, dimana inti batuan itu banyak terdapat lapisan fosfat. Sedang bagian permukaan pebatuan keras jarang ditemui zat kalsium, fosfat dan CO2, kalaupun ada zat-zat itu bersenyawa dengan δ-MnO2 dan residu biogenik. Zat-zat seperti platinum, rhodium dan iridium yang bersenyawa dengan fase CFA akan makin bertambah dengan bertambahnya kepadatan kerak. Halini berlawanan dengan mekanisme pengikatan kobalt dan zat-zat lain melalui fase detrital, dimana jumlahnya makin berkurang dengan bertambahnya kepadatan (Halbach dkk, 1982). Dalam kerak Fe-Mn terdapat banyak zat-zat yang kandungannya relatif sedikit seperti lanthanum (La), lutetium (Lu), cerium (Ce), praseodymium (Pr), neodymium (Nd), samarium (Sm), europium (Eu), gadolinium (Gd), terbium (Tb), dysprosium (Dy), holmium (Ho), erbium (Er), thulium (Tm), ytterbium (Yb) diperkirakan ada ribuan ppm, sedang zat yttrium hanya ratusan ppm. Konsentrasi trivalent dari zat-zat yang jumlah sedikit (rare-earth element/REE), kecuali cerium, akan makin bertambah di kerak dengan bertambahnya kedalaman perairan (Aplin, 1984; De Carlo dan Fraley, 1990). Sesungguhnya pada kerak Fe-Mn di laut banyak ditemui zat-zat yang jumlahnya sedikit, tidak hanya REE. Seperti pada pecahan batu karang ukuran kecil terdapat sangat banyak kandungan REE, dan hampir semua samudera di dunia ditemui zat-zat itu. Umumnya zat-zat seperti lanthanum (La), Ce, Eu dan Gd hampir merata di semua samudera, kecuali zat yttrium terkadang tidak ada di tempat tertentu. Semua zat-zat itu berasal dari daratan yang masuk kelaut dihantar oleh aliran sungai sejak ribuan tahun lalu. Kecuali ada zat-zat yang mudah terjadi secara redoks ~ 313 ~ (reduksi-oksidasi), seperti cerium dan yttrium telah ada di air laut, yang kemudian diserap oleh Fe-Mn oksihidroksida. Cerium adalah satu-satunya REE yang memiliki iontrivalen, zat ini dilingkungan laut bersenyawa dengan mangan dan besi oksihidrooksida dalam ikatan oksidasi cerium dimana senyawa ini akan dikatalisis oleh mikroba di perairan (Moffett, 1990). Dalam kerak Fe-Mn terdapat juga zat kimia yang bernilai ekonomis tinggi, banyak di gunakan pada pelbagai industri tingkat tinggi (high-tech) di beberapa negara maju di dunia, zat-zat itu adalah platinum, palladium, rhodium, ruthenium dan iridium, kelompok zat-zat tersebut sering disebut sebagai grup kimia platinum (platinum group elements/PGEs). Sessungguhnya kelimpahan zat-zat tersebut di kerak bumi sangat tinggi, kecuali palladium relatif kurang (lihat table 11.4). Platinum jumlahnya sangat banyak di tambang kobalt, diperkirakan 0,8 ppm sampai dengan 3 ppm (Halbach dkk, 1984; Aplin and Cronan, 1985; Hein dkk, 1988). Sedang zat kimia rhodium, ruthenium dan iridium hanya ditemui 124 ppb, 32 ppb dan 54 ppb, kemudian palladium hanya 1-16 ppb saja. Intinya PGE memiliki hubungan positif dengan konsentrasi dan ketebalan kerak, artinya kosentrasi PGE makin tinggi akan memperlihatkan lapisan kerak makin tebal. Biasanya para ahli geologi dalam melakukan eksplorasi, salah satu indikator ekspetasi potensi ekonomi tinggi di daerah tambang hanya di dasarkan pada ketebalan kerak dan warna sampel pebatuan. Pembentukan lapisan fosfat di kerak Fe-Mn umumnya melalui hidrogenetik, kalau di samudera Pasifik, menurut Hein (2004) lapisan fosfat ada dua generasi, yakni generasi lapisan fosfat yang telah lama terbentuk dan lapisan generasi baru dengan relatif fosfatnya kurang. Umumnya tersebar luas di Pasifik bagian tengah dan selatan pada kedalaman >2800 meter. Pada dasarnya fosfat terbentuk melalui ikatan senyawa difase CFA (carbonat fluorapatite), dan pembentukannya ~ 314 ~ tidak di semua pinggiran kontinen, seperti dilingkungan laut ZEE Amerika bagian barat-utara tidak terbentuk lapisan fosfat di pebatuan. Pengendapan fosfat di laut telah berlangsung sejak 55 dan 25 juta tahun yang lalu, dimana zat itu bersenyawa dengan CFA yang kemudian terendap menutupi bagian atas pebatuan secara bertahap dengan berjalannya waktu lapisan itu makin menumpuk, dan akhirnya bagian tengah pebantuan terbentuk besi oksihidroksida. Umumnya lapisan fosfat yang terbentuk ada sekitar 12 cm, halmana kandungan kalsium diperkirakan 15% dari berat pebantuan, dan kandungan fosfat ada sekitar 5% dari berat. Menurut Hein dkk (1993) bahwa pembentuk fosfat di gunung dasar laut di samudera Pasifik bagian ekuator terjadi dua kali Cenozoic (major dan minor). Hal itu juga sama dengan pembentukan fosfat di Fe-Mn generasi lama. Kejadian major Cenozoic pada pembentuk fosfat di Fe-Mn terjadi pada ± 34 juta tahun lalu (Eocene-Oligocene) dan lapisan yang mengelilingi “Oligocene-Miocene” diperkirakan pada 24 juta tahun yang lalu. Sedang kejadian minor Cenozoic terjadi pada 15 juta tahun yang lalu (Miocene). Periode pembentukan fosfat di kerak Fe-Mn dapat terlihat jelas pada susunan lapisannya di pebatuan. Menurut Puteanus dan Halbach (1988), pembentukan lapisan fosfat pada kerak Fe-Mn dihubungkan dengan umur, berhubungan erat dengan komposisi kimia dan elemen mineral. Halmana penyusunan lapisan fosfat sampai pada lapisan bukan fosfat di kerak Fe-Mn dengan susunan sebagai berikut: silicon besi aluminium thorium > titanium kobalt> timah uranium. Sebaliknya zat nikel, tembaga, zink, yttrium, REE, strontium, platinum dan barium terdapat banyak di pebatuan fosfat. Sesungguhnya dalam kolom air dan daerah permukaan pebatuan di perairan laut miskin akan unsur kimia tetapi ~ 315 ~ oleh adanya masukan material ke lingkungan laut, berasal dari aliran sungai yang berlangsung ribuan tahun, aktifitas hidrothermal, material dari daratan serta adanya peleburan kimia di pebatuan oleh akibat sinar matahari (lihat uraian bab sebelumnya), maka material-material itu terjadi percampuran atau bersenyawa melalui media air (hidrogenetika) dan mengendap membentuk lapisan pebatuan, mekanisme ini memungkinkan terbentuknya kerak Fe-Mn. Dengan demikian di perairan laut telah terjadi interaksi pelbagai kimia yang kompleks baik organik maupun anorganik. Model reaksi yang terjadi seperti interaksi kimia dipermukaan air, thermodinamika dan kimia koloida memungkinkan terjadi endapan logam (Koeppenkastrop dan De Carlo, 1992; Koschinsky dan Halbach, 1995; Bau, 1996). Suatu hal yang menarik, zat kimia yang bersifat kation hidrat , seperti: kobalt, nikel, seng, timah, cadmium, thallium dan dan lain-lain agak kurang bersenyawa dengan Mn-oksihidroksida, sedang anion pada kimia yang bentuknya besar dan kompleks seperti: vanadium, arsenik, fosfat, zirconium, hafnium dan lain-lain mampu bersenyawa pada besi hidroksida walaupun kapasitas pengikatan adalah rendah. Pada pebatuan keras biasanya kurang kristalin atau sering dikatakan batuan amorf oksihidrosida, namun oleh adanya campuran antara besi dan mangan berbentuk koloid disertai bantuan kerja bakteri maka terbentuklah endapan logam. Kemudian endapan logam ini makin bertambah terjadilah penimbunan endapan sehingga terlihat adanya kisikisi kristal yang menutupi pebatuan Fe-Mn oksihidroksida. Kobalt yang ada di permukaan pebatuan merupakan hasil proses hidrogenetik, dimana kobalt (II) menjadi larutan kobalt (III), walaupun sesungguhnya reaksi yang terjadi bersifat tidak beraturan. Demikian pula, zat kimia timah, titanium, tellurium, thallium serta cerium terjadi mekanisme oksidasi yang relatif sama dengan kobalt (Koschinsky dan Halbach, 1995). ~ 316 ~ Sebetulnya kandungan kimia yang ada di perairan air laut merupakan refleksi dari kandungan kimia yang ada di pebatuan laut walaupun banyak faktor pembatasnya. Seperti keadaan zat kimia tembaga, nikel dan seng. Dimana di perairan, zat nikel lebih banyak dari pada tembaga dan seng. Tembaga yang di pebatuan bersifat larutan relatif kurang jumlahnya karena sebagian besar terbentuk dari zat organik di perairan laut dalam, halmana zat ini agak sulit bersenyawa dengan logam besi dan Mn-oksihidroksida (Takematsu dkk, 1989). Demikian juga dengan zat seng relatif lebih kurang dibandingkan dengan zat nikel di perairan, karena endapan seng di pebantuan juga sedikit. Hal itu berbeda dengan kandungan kobalt dan besi di laut dalam serta Fe-Mn di pebatuan (lihat table 11.1). Hakekatnya, jumlah zat dan konsentrasinya di pebantuan hidrogenetika sangat tergantung pada aktifitas partikel dan zat-zat yang ada di perairan, lamanya zat itu di laut, kelimpahan kandungan besi dan mangan di pebatuan, agen kimia koloid yang sangat kompleks di permukaan, jumlah bahan baik organik dan anorganik diperairan, aktifitas oksidasi MnO2 (oksigen/mangan) dan kemampuan reaksi kimia yang terkandung di perairan laut. Disamping itu material dari atmosfer dan daratan berpengaruh besar terhadap kecepatan pembentukan kerak Fe-Mn (Bau, 1996). ~ 317 ~ KEPUSTAKAAN ~ 318 ~ KEPUSTAKAAN Addadi L. and S. Weiner., 1992. Control and design principles in biological mineralization. Angew Chem Int Ed 31:153-169 Addadi L. and S. Weiner., 2001. Crystals, asymmetry and life. Nature 411:753-755 Addadi L.; S. Raz and S. Weiner., 2003. Taking advantage of disorder: amorphous calcium carbonate and its roles in biomineralization. Adv Mat 15:959-970 Ali S.Y., 1983. Calcification of cartilage. In: Cartilage, Structure, Function and Biochemistry. Hall BK (ed) Academic Press, New York, p 343-378 Andersen, N.R and A. Malahoff. 1977. The fate of fossil fuel CO 2 in the Ocean. Plenum Press. NY. 749 p Andreae, M.O. 1986. The Ocean as a Source of Atmospheric Sulfur Compounds. In the Role of Air-Sea Exchangge in Geochemical Cycling, P. Buat-Menarda (ed), 331-362. Drodrecht Reidel. Andreae, M.O., R.J., F. Bruynseels, H. Storm, R. Van Grieken and W. Maenhaut, 1986. Internal Mixtures of Sea Salt, Silicates, Excess Sulfate in Marine Aerosols. Science 232: 1620-1623 Aplin, A.C., 1984. Rare Earth Element Geochemistry of Central Pasific Ferromanganese Encrustation. Earth and Planetray Scien. Lett. 71: 13-22. Aplin, A.C and D.S. Cronan., 1985. Ferromanganese Oxide Deposits from the Central Pasific Ocean. I. Encrustation from the Line Island Archipelago. Geochimica et cosmochimica acta. 49: 427436. Archer D.E. ; S. Emerson and C. Reimers. 1989., Dissolution of calcite in deep-sea sediments: pH and O2 microelectrode results. Geochim Cosmochim Acta 53:2831-2845. Archer D and E. Maier-Reimer., 1994. Effect of deep-sea sedimentary calcite preservation on atmospheric CO2, concentration. Nature 367: 260-263 Archer, D.E., 1990. An Atlas of the Distribution of Calcium Carbonat in ~ 319 ~ Sediment of the deep Sea. Global Biochemical Cycles. 10: 159174. Balls, p.W., 1985. Copper, Lead and Cadmium in Coastal Waters of the Western North Sea. Marine Chem. 15, 363-378. Barnes, H. L., ed. 1997. Geochemistry of Hydrothermal Ore Deposits, 3rd ed. Wiley Interscience. New York. 561 p Bates, R. L., and Jackson, J. A. 1987. Glossary of Geology, third edition, American Geological Institute, p.598 Bau, M., 1996. Comparison of the Partitioning Behaviors of Yttrium, rare-earth elements, and Titanium between Hydrogenetik Marine Ferromanganese Crust and Seawater. Geochimca et Cosmochimica Acta, 60: 1709-1725. Bäuerlein E. (ed), 2000. Biomineralization. Wiley-VCH Verlag GmbH, Weinheim Germany. Bazylinski D.A., 1996. Controlled biomineralization of magnetic minerals by magnetotactic bacteria. Chem.Geo 132:191-198 Bazylinski D.A. and B.M. Moskowitz., 1997. Microbial biomineralization of magnetic iron minerals: Microbiology, magnetism and environmental significance. Rev Mineral 35:181-223 Bazylinski D.A. and R.B. Frankel., 2003. Biologically controlled mineralization in prokaryotes. Rev Mineral Geochem 54:217247 Belcher A.M; X.H. Wu; R.J. Christensen; P.K. Hansma; G.D. Stucky and D.E. Morse., 1996. Control of crystal phase switching and orientation by soluble mollusc-shell proteins. Nature 381(6577):56-58 Bender, M.L. and D.T. Heggie, 1984. Fate of organic carbon reaching the deep sea flow: a status report. Geochim. Cosmochim. Acta, 48, 977–986. Bengtson S. and M.S. Conway, 1992. Early radiation of biomineralizing phyla. In: Origin and Early Evolution of the Metazoa. Lipps JH, Signor PW (eds) Plenum, New York, p 447–481 ~ 320 ~ Beniash E.; J. Aizenberg; L. Addadi and S. Weiner., 1997. Amorphous calcium carbonate transforms into calcite during sea-urchin larval spicule growth. Proc R Soc London B Ser 264:461-465 Beniash E.; L. Addadi and S. Weiner., 1999. Cellular control over spicule formation in sea urchin embryos: a structural approach. J Struct Biol 125:50-62 Bennett, P. C. 1991. Quartz dissolution in organic-rich aqueous systems. Geochimica et Cosmochimica Acta 55:1781–1797. Berelson, W.M.; D.E. Hammond and G.A. Cutter., 1990. In situ measurements of calcium carbonate dissolution rates in deep sea sediments. Geochimica of Cosmoschimica Acta, 54: 30133020. Berger W.H., 2002. Climate history and the great geophysical experiment. In: Climate Development and the History of the North Atlantic Realm.Wefer G, Berger W, Behre KE, Jansen E (eds) Springer Verlag, p 1-16 Berner, R. A. 1980. Early Diagenesis: A Theoretical Approach. Princeton: Princeton University Press. 289 p Berner, R.A., 1981. A new geochemical classification of sedimentary environments. J. Sed. Petrol., 51, 359–365. Berner, B.A., 1982. Burial of organic carbon and pyrite sulfur in the modern ocean: its geochemical and environmental significance. Am J. Sci., 282, 451–473. Berner, R. A. 1989. Biogeochemical cycles of carbon and sulfur and their effect on atmospheric oxygen over Phanerozoic time. Palaeogeography, Palaeoclimatology, Palaecology 73: 97–122. Bettencourt V and A. Guerra., 2000. Growth increments and biomineralization process in cephalopod statoliths. J Exper Mar Biol Ecol 248:191-205 Bewen, J.M. and P.A. Yeats, 1980. Behaviour of Trace Metals During Estuarine Mixing. In River inputs to Oceans Systems, I.M. Martin, J.D. Burton and D. Eisma (eds), 103-115. Paris: UNEP/UNESCO. Billard C.. 1994. Life cycles. In: The Haptophyte Algae. Green J.C. and B.S.C. Leadbeater (eds) Clarendon Press, Oxford, p 167-186 ~ 321 ~ Blanchard, D.C. 1983. The Production, Distribution and Bacterial Enrichment of the Sea-Salt Aerosol. In Air-sea exchange of gases and particles. P.S. Liss & W.G.N. Slin (eds) pp. 407-454 Dondrecht; Reidel. Bolton, B.R.; N.F.Exon and J. Ostwald., 1990. Thick ferromanganese deposits from the Dampier Ridge and the Lord Howe Rise of eastern Australia. BMR journal of Auatralian Geology and Geophysics, 11: 421-427. Boogs, S. 1986. Petrology of Sedimentary Rocks, Mc Millan Publishing Company, New York, 707 p. Borowitzka M.A., 1982., Morphological and cytological aspects of algal calcification. Intl Rev Cytology.74:127-160. Bown P.R., 1998a. Calcareous Nannofossil Biostratigraphy. Chapman & Hall, London. Bown P.R., 1998b., Triassic. In: Calcareous Nannofossil Biostratigraphy. Bown PR (ed) Chapman & Hall, London, p 29-33. Bown P.R. and J.R. Young., 1998. Techniques. In: Calacareous Nannofossil Biostratigraphy. Bown PR (ed) Chapman & Hall, London, p 16-28 Brady, James E. Dan J. R. Holum, 1981. Fundamentals of Chemistry. Jhon Wiley & Sons. New York. Brasseur, Guy P.; Orlando, John J.; Tyndall, Geoffrey S., 1999. Atmospheric Chemistry and Global Change. Oxford University Press. Brewer P.G.; C. Goyet and G. Frienderich., 1997. Direct observation on the oceanic CO2 increase revisited. Geophys Proc Nat Acad Sci USA 94:8308-8313 Broecker, W. S., and T. H.Peng. 1974. Gas Exchange rates between Air and Sea. Tellus 26, 21-35. Broecker, W. S., and T. H.Peng. 1982. Tracers in the Sea. Eldigio Press, Columbia University. New York. 347 p ~ 322 ~ Burdige, D.J. and J.M. Gieskes, 1983. A pore water/solid phase diagenetic model for manganese in marine sediments. Am. J. Sci., 283, 29–47. Burdige, D.J., 2007. Preservation of organic matter in marine sediments: controls, mechanisms and an imbalance in sediment organic carbon budgets? Chem. Rev., 107, 467–485. Burke, C.M. and M.J. Atkinso. 1988. Measurement of total Alkalinity in Hypersaline Waters. Marine Chemistry, 25, 49-55. Burns R.G. and V.M. Burns., 1977. Mineralogy, in Marine Manganese Deposits. In Marine Manganese Deposits, G.P. Glasby (ed). Elsevier Amsterdam. Pp 185-248. Bury, S.J., 1989. The geochemistry of North Atlantic ferromanganese encrustation, Ph.D. Thesis, Cambridge University, 265 p. Calvert, S.E. and N. B. Price, 1970. Minor metal contents of Recent organic-rich sediments off South West Africa. Nature, 227, 593– 595. Cameron, M., and J. J. Papike. 1980. Crystal chemistry of silicate pyroxenes. Mineralogical Society of America Reviews in Mineralogy 7:5–92. Carlson, W. D., and J. L. Rosenfeld. 1981. Optical determination of topotactic aragonite -calcite growth kinetics: Metamorphic implications. Journal of Geology 89:615–638. Carmichael, I.S.E., and H. P. Eugster, eds. 1987. Thermodynamic Modeling of Geological Materials: Minerals, Fluids and Melts. Reviews in Mineralogy 17. Washington, D.C.: Mineralogical Society of America. Chester Roy. 1990. Marine Geochemistry Pub. Academic Division of UNWIN HYMAN. London. 698 h. Chester, R and T. Jickells, 2012. Marine Geochemistry (3rd Edt). Science Jhon Wiley & Sons Pub. London, 436 p. Childers, J.J. 1988. Hydrothermal Vents. A Case Study of the Biology and Chemistry of a Deep-sea hydrothermal vent of the Galapagos Rift. Deep-Sea Res. 35 p. 1673-1849. ~ 323 ~ Cohen A.L. and Ted A. McConnaughey., 2003. Geochemical Perspectives on Coral Mineralization. In Biomineralization by Jodi J. Rosso (Edt) on Review in Mineralogy and Geochemistry. Mineralogical Society of America, Geochemistry Society, Vol 54, 151-187 Colman, S. P., and D. P. Dethier, eds. 1986. Rates of Chemical Weathering of Rocks and Minerals. Academic Pres. New York. Constantz B.R., 1986. Coral skeleton construction: A physiochemically dominated process. Palaios 1:152- 157 Constantz B.R. and A. Meike., 1989. Calcite centers of calcification in Mussa Angulosa (Scleractinia). In: Origin, Evolution and Modern Aspects of Biomineralization in Plants and Animals. Crick RE (ed) Elsevier, Amsterdam, p 201-207 Cowen J.P.; E.H. De Carlo and D.L. McGee., 1993. Calcareous nannofossil biostratigraphie dating of a ferromanganese crust from Schumann Seamount. Marine Geology, 115: 289-306 Cronan, D.S., 1984. Criteria for the recognition of areas of potentially economic manganese nodules and encrustations in the CCOP/SOPAC region of the central and south-western tropical Pasific. South Pasific Marine Geological Notes, CCOP/SOPAC, 3:1-17. Cros L. and J.M. Fortuño, 2002. Atlas of northwestern Mediterranean coccolithophores. Scientia Marina 66: 1-186 Cros L.; A. Kleijne; A. Zeltner; C. Billard and J.R. Young. 2000. New examples of holococcolith-heterococcolith combination coccospheres and their implications for coccolithophorid biology. Mar Micropaleontol. 39:1-34. Darmono Djoko dkk., 2009. Mineral Dan Energi Kekayaan Bangsa. Sejarah Pertambangan dan Energi Indonesia. Dep. Energi dan Sumber Daya Mineral. Davies, T.A. and A.S. Laughton, 1972. Sedimentary Processes in the North Atlantic. Initial reports of the deep sea drilling project. Vol. 12. Pp 905-934. Washington DC. US Government Printing Office. Davies, T.A. and D.S. Gorsline. 1976. Oceanic Sediments and Sedimentary Processes. In Chemical Uceanography, J.P. Riley & R. Chester (eds). Vol, 5, p: 1-80. London Academic Press. ~ 324 ~ De Carlo, E.H. and G.M. McMurtry., 1992. Rare-earth element geochemistry of ferromanganese crust from Hawaiian Archipelago central Pasific. Chemical geology. 95: 235-250. De Carlo, E.H. and C.M. Fraley., 1990. Chemistry and Mineralogy of Ferromanganese Deposits from Equatorial Pacific Ocean. In Geology and Offshore Mineral Resources of the Central Pasific Basin. B.H. Kreating and B.R. Bolton (eds). Circum-Pasific Council for Energy and Mineral Resources. Houston, Texas. Earth Scien. Series. V: 5, pp 225-245. De Yoreo J.J and P.M. Dove., 2004. Shaping crystals with biomolecules. Science 306:1301-1302 De Vrind-de Jong E.W.; A.H. Borman; R. Thierry; P. Westbroek, M. Grüter and J.P. Kamerling., 1986. Calcification in the coccolithophorids Emiliania huxleyi and Pleurochrysis carterae II. Biochemical aspects. Syst. Assoc Spec Vol 30, p 205-217 De Vrind-de Jong E.W. and J.P.M. de Vrind., 1997. Algal deposition of carbonates and silicates. Rev Mineral 35:267-307 De Vrind-de Jong E.W.; P. van Emburg and J.P.M. de Vrind., 1994. Mechanisms of calcification: Emiliania huxleyi as a model system. In: The Haptophyte Algae. Green JC, Leadbeater BSC (eds) Syst Assoc Spec Vol 51, p 149-166 Drever, J. I., 1974. The magnesium problem. In E. D. Goldberg, ed. The Sea, vol. 5. New York: Wiley Interscience, pp. 337– 357. Drever, J. I., 1997. The Geochemistry of Natural Waters. New York: Simon and Schuster. Drever, J.I., 1982. The Geochemistry of Natural Waters. Englewood Cliffs, NJ: Prentice-Hall. Duda M. dan F. Pajak ., 2004. The issue of bioresorption of the Bio-Oss xenogeneic bone subtitue in bone defects. Ann UnivMariae Curie Sklodawska 59: 269277 Edvardsen B; W. Eikrem; J.C. Green; R.A. Andersen; S. Yeo Moon-van der Staay and L.K. Medlin., 2000. Phylogenetic reconstructions ~ 325 ~ of the Haptophyta inferred from 18S ribosomal DNA sequences and available morphological data. Phycologia 39:19-35 Elderfield, H., 1976. Hydrogenous Material In Marine Sediments: Excluding Manganese nodules. In Chemical Oceanography, J.P. Riley and R. Chester (eds) Vol. 5, 137-215 London Academic Press. Elderfield, H. (ed), 2006. The Oceans and Marine Geochemistry. Treatise on Geochemistry, Volume 6. Pergamon. New York. 664 p. Elgquist, B., and M. Wedborg. 1978. Stability constants of NaSO4 −, MgSO4, MgF+, MgCl+ ion pairs at the ionic strength of seawater by potentiometry. Marine Chemistry 6:243–252. El Wakeel, S.K. and J.P. Riley, 1961. Chemical and Mineralogical Studies of Deep Sea Sediment. Geochim Cosmochim. Acta 25, pp 110146. Engel, M. H., and S. A. Macko, eds. 1993. Organic Geochemistry: Principles and Applications. Plenum. New York. Erez J., 2003. The Source of Ions for Biomineralization in Foraminifera and Their Implications for Paleoceanographic Proxies In Biomineralization by Jodi J. Rosso (Edt) on Review in Mineralogy and Geochemistry. Mineralogical Society of America, Geochemistry Society, Vol 54, 115-149 Eugster, H. P., and D. R. Wones. 1962. Stability relations of the ferruginous biotite, annite. Journal of Petrology 3:82–125 Exon,N.F., 1997. Ferromanganese crust and nodule deposit from the continental margin south and west of Tasmania. Australian journal of Earth Sciences, 44: 701-710. Falini G; S. Albeck; S. Weiner and L. Addadi., 1996. Control of aragonite or calcite polymorphism by mollusk shell macromolecules. Science 271:67-69 Faure, G. 1991. Principles and Applications of Inorganic Geochemistry. New York: Macmillan. 369 p Ferry, J. M., ed. 1982. Characterization of Metamorphism through Mineral Equilibria. Reviews in Mineralogy 10. Washington, D.C.: Mineralogical Society of America. ~ 326 ~ Fichtinger-Schepman A.M.J.; J.P. Kamerling; C. Versluis and J.F.G. Vligenthart. 1981. Structural studies of the methylated, acidic polysaccharide associated with coccoliths of Emiliania huxleyi (Lohmann) Kamptner. Carbohydrate Research 93:105-123 Finlayson-Pitts, Barbara J.; Pitts, James N., Jr., 2000. Chemistry of the Upper and Lower Atmosphere. Academic Press. Fortin D, Ferris F.G and T.J. Beveridge., 1997. Surface-mediated mineral development by bacteria. Rev Mineral 35: 161-180 Fortin D and T.J.Beveridge., 2000. Mechanistic routes to biomineral surface development. In: Biomineralization. Baeuerlein E (ed) Wiley-VCH, Weinheim, Germany, p 7-24 Froelich, P.N., G.P. Klinkhammer and M.L. Bender., 1979. Early oxidation of organic matter in pelagic sediments of the eastern equatorial Atlantic: suboxic diagenesis. Geochim. Cosmochim. Acta, 43, 1075–1090. Fujiwara S; M. Tsuzuki; M. Kawachi; N. Minaka and I.Inouye., 2001. Molecular phylogeny of the haptophyta based on the rbcL gene and ssequence variation in the spacer region of the RUBISCO operon. J. Phycol 37:121-129 Fütterer D.K., 2006. The Solid Phase of Marine Sediments. In Marine Geochemistry, Horst D Schulz and Matthias Zabel (eds). Springer-Verlag Berlin Heidelberg. Germany. P 1-25. Galoway, F. and M. Bender., 1982. Diagenetic models of interstitial nitrate profiles in deep-sea suboxic sediments. Limnol. Oceanogr., 27, 624–638. Garrels, R.M. and F.T. Mackenzie. 1977. Rocks. New York: Norton. Evolution of Sedimentary Garrone R.; T.L. Simpson and J. Pottu-Boumendil., 1981. Ultrastructure and deposition of silica in sponges. In: Silicon and Siliceous Structures in Biological Systems. Simpson TL, Volcani BE (eds) Springer-Verlag, New York, p 495-525 Geisen M.; C. Billard; A.T.C. Broerse; L. Cros; I. Probert and J.R. Young . 2002. Life-cycle associations involving pairs of holococcolithophorid species: intraspecific variation or cryptic speciation? Eur J Phycol 37:531-550 ~ 327 ~ Gibbs, R.J. 1970. Mechanisms Controlling World River Water Chemistry. Science 170: 1088-1090. Gieskes, J.M., 1983. The chemistry of interstitial waters of deep sea sediments: interpretations of deep-sea drilling data, in Chemical Oceanography, J.P. Riley and R. Chester (eds), Vol. 8, pp.221–269. London: Academic Press Gilbert P.U.P.A., Mike Abrecht, Bradley H. Frazer, 2005. The OrganicMineral Interface in Biominerals. Reviews in Mineralogy & Geochemistry. Vol. 59, pp. 157-185, Mineralogical Society of America. Goldberg, E.D. and J.J. Griffin. 1964. Sedimentation Rates and Mineralogy in the south Atlantic. J. Geophys. Res 69 pp 42934309. Gotliv B.A; L. Addadi and S. Weiner., 2003. Mollusk shell acidic proteins: in search of individual functions. Chem Bio Chem 4:522-529 Gray, J. C., and J. C. G. Walker. 1990. Numerical Adventures with Geochemical Cycles. London: Oxford University Press. 456 p Haese, R.R. 2006 The Biogeochemistry of Iron. In Marine Geochemistry, Horst D Schulz and Matthias Zabel (eds). Springer-Verlag Berlin Heidelberg. Germany. pp 241-270. Harvie, C. E., N. Moller, and J. H. Weare. 1984. The prediction of mineral solubilities in natural waters: The Na-K-Mg-CaH-ClSO4-OH-HCO3-CO3-CO2-H2O system to high ionic strengths at 25°C. Geochimica et Cosmochimica Acta 48: 723–752 Hedges, J. I., and R. G. Keil. 1995. Sedimentary organic-matter preservation—an assessment and speculative synthesis. Marine Chemistry 492–493: 81–115 Hein, J.L.; A.Konschinsky; P.Halbach; F.T.Manheim, M.Bau; J.K. Kang and N. Lubicl., 1977. Iron and manganese oxide mineralization in the Pasific. In Manganese Mineralisation: Geochemistry and Mineralogy of Terrestrial and Marine Deposits, Hein et a (Eds). Geol. Sco. Special Pub, 119. 123-138. ~ 328 ~ Hein, J.R.; W.C. Schwab and A.S. David., 1988. Cobalt and Platium-rich ferromanganese Crust and Associated Substrate Rocks from the Marshall Island, Marine Geology, 78: 255-283. Hein J.R. and C.L. Morgan., 1999. Influence of substrate rocks on FeMn Crust Composition. Deep-sea research I, 46: 855-875. Hein J.R.; A. Koschinsky; M. Bau; F.T. Manheim; J.K. Kang and L. Roberts., 2000. Cobalt-rich ferromanganese crust in the Pacific. In Handbook of Marine Mineral Deposits, D.S. Cronan (ed), CRC Press, Boca Raton, Florida p. 239-279. Hein J.R., 2004. Cobalt-Rich Ferromanganese Crusts: Global Distribution, Composition, Origin and Research Activities. Dalam Prosiding workshop Tentang Minerals Other Than Polymetallic Nodules of The International Seabed Area (volume I), Dilaksanakan pada tanggal 26-30 Juni 2000 di Kingston Jamaica. pp 188-272 Helfinalis, 2005. Suspensi Dan Endapan Sedimen Di Perairan Laut Jawa. MAKARA SAINS, Vol. 9, No. 1, pp : 34-40 Hemleben C; O.R. Anderson; W. Berthold and M.Spindler., 1986. Calcification and chamber formation in foraminifera-a brief overview. In: Biomineralization in Lower Plants and Animals. Leadbeater BSC, Riding R (eds) Clarendon Press, Oxford, p 237249 Hess, P. C., 1989. Origins of Igneous Rocks. Cambridge: Harvard University Press. (Chapter 2 presents a thorough explanation of phase diagrams, although without reference to thermodynamics.) Hill, J.W., K. Koib dan S.W. Keller. 2004. Chemistry for Changing Times. (edition 10th). Pearson Prentice. Hall . USA. Holland, H. D. 1978. The Chemistry of the Atmosphere and Oceans. New York: Wiley Interscience. 339 p Holland, H. D. 1984. The Chemical Evolution of the Atmosphere and Oceans. Princeton: Princeton University Press. 365 p Holzmann M.; A. Habura; H. Giles; S.S. Bowser and J. Pawlowski., 2003. Freshwater foraminiferans revealed by analysis of environmental DNA samples. J Eukaryotic Microbiol 50(2):135139 ~ 329 ~ Holzmann M. and J. Pawlowski., 2002. Freshwater foraminiferans from Lake Geneva: Past and present. J. Foramin Res 32 (4):344-350 Hosokawa, I.O., F. Oshima and N. Kondo. 1970. On the Concentration of the Dissolved Chemical Elements in The Estuary of The Chikukogawa River. J. Oceanography. Soc. Jap. 26, 1-5. Horne, R. A., ed. 1972. Water and Aqueous Solutions: Structure, Thermodynamics, and Transport Properties. New York: Wiley Interscience. Honnerez, J., 1981. The Aging of the Oceanic Crust at Low Temperature. In The Sea. C. Emillani (ed). Vol. 7, 525-587. New York, Interscience. Indrani D.J., 2012. Komposit Hidroksiapatit Kalsinasi Suhu rendah dengan Alginat SARGASSUM DUPLICATUM atau SARGASSUM CRASSIFOLIUM Sebagai material Scaffold Untuk Pertumbuhan Sel Punca Mesenkimal. Disertasi Doktor dalam Bidang Ilmu Material FMIPA-UI. 168 h. Ittekkot, V. 1988. Global Trends in The Nature of Organic Matter in River Suspensions. Nature 332, 436-438. Isnaniawardhani V., Natsir dan Suhartati M., 2011. Tipe Sedimen Permukaan Dasar Laut Selatan Dan Utara Kepulauan Tambelan Perairan Natuna Selatan. Laporan Penelitian Pusat Penelitian Oseanografi (P2O) LIPI. Isnaniawardhani, V. , 2012. Karakteristik Sedimen dan Mikro Organisma Permukaan Dasar Laut Perairan Madura Bagian Utara. Bulletin of Scientific Contribution, Volume 10, Nomor 1, 18-30. Janin M.C., 1985. Biostratigraphie de concretions polymetallique de I’ Arhipel des Tuamotu, fondėe sur les nanofossiles calcaires., Bull. Soc. Geol. France. 8: 79-87. Jones, E.J.W. 1978. Sea-floor Spreading and the Evolution of the Ocean Basins. In Chemical Oceanography, J.P. Rilley and R. Chester (eds), vol 7, p 1-74. London. Academic Press. Jørgensen, B.B and S. Kasten, 2006. Sulfur Cycling and Methane Oxidation. In Marine Geochemistry, Horst D Schulz and ~ 330 ~ Matthias Zabel (eds). Springer-Verlag Germany. pp 271-309. Berlin Heidelberg. Katili, J.A. dan P. Marks, 1959. Geologi. Dep. Urusan Research Nasional Djakarta. 855 h. Kaul, L.W and P.N. Froelich. 1984. Modeling Estuarine Nutrient Geochemistry in A Simple System. Geochim. Cosmochim. Acta 48, 1417- 1433. Keil, R. G., E. Tsamakis, C. B. Fuh, C. Giddings, and J. I. Hedges. 1994. Mineralogical and textural controls on the organic composition of coastal marine sediments—hydrodynamic separation using SPLITT-fractionation. Geochimica et Cosmochimica Acta 582:879–893. Kerrick, D. M., and G. K. Jacobs. 1981. A modified RedlichKwong equation for H2O, CO2, and H2O-CO2 mixtures at elevated pressures and temperatures. American Journal of Science 281:735–767 Kerrick, D. M., ed. 1990. The Al2SiO5 polymorphs. Reviews of Mineralogy 22. Washington, D.C.: Mineralogical Society of America. Killops, S. D., and V. J. Killops. 1993. An Introduction to Organic Geochemistry. Wiley Pub.New York. 542 p Kirkpatrick, R. J. 1974. Kinetics of crystal growth in the system CaMgSi2O6-CaAl2SiO6. American Journal of Science 274: 215– 242. Kirkpatrick, R. J., G. R. Robinson, and J. F. Hays. 1976. Kinetics of crystal growth from silicate melts: Anorthite and diopside. Journal of Geophysical Research 81:5715–5720 Kirschvink J.L. and J.W.Hagadorn., 2000. A grand unified theory of biomineralization. In: Biomineralization. Bäuerlein E (ed) Wiley-VCH Verlag GmbH, Weinheim, Germany, p 139-149 Koeppenkastrop, D. and E.H. De Carlo., 1992., Sorption of Rare-earth elements from Seawater onto Synthetic Mineral Perticles: An experimental Approach. Chemical Geology. 95: 251-263. Konhauser K.O., 1998. Diversity of bacterial iron mineralization. EarthScience Rev 43:91-121 ~ 331 ~ Knoll A.H, 2003. Biomineralization and Evolutionary History. In Biomineralization by Jodi J. Rosso (Edt) on Review in Mineralogy and Geochemistry. Mineralogical Society of America, Geochemistry Society, Vol 54, 329-356. Konta, J. 1985. Mineralogy and Chemical Maturity of Suspended Matter in Major Rivers sampled Under the SCOPE?UNEP Project. In Transport of Carbon and Minerals in Major World Rivers, Part 3, E.T. Degens, S. Kempe and R. Herrera (eds), 569592. Mitt. Geol. Palont. Inst. Univ. Hamburg, SCOPE/UNEP, sonderband 58. Koning E.; J.M. van Iperen; W. van Raaphorst; W. Helder; G.J.A. Brummer and T.C.E. Weering., 2001. Selective preservation of upwelling-indicating diatoms in sediments off Somalia, NW Indian Ocean. Deep-Sea Research 48:2473-2495. Koschinsky, A. and P. Halbach., 1995. Sequential leaching of ferromanganese precipitates: Genetic implications. Geochimica et Cosmochimica Acta, 59: 5113-5132 Kretz, R. 1994. Metamorphic Crystallization.Wiley Pub. New York. 354 p Kröger N.; R. Deutzmann and Sumper M., 1999. Polycationic peptides from diatom biosilica that direct silica nanosphere formation. Science 286:1129-1132 Kröger N.; S. Lorenz; E. Brunner and M. Sumper., 2002. Self-assembly of highly phosphorylated silaffins and their function in biosilica morphogenesis. Science 298:584-586 Ku, T.L., W.S.Broecker and N. Opdyke. 1968. Comparison of Sedimentation rates measured by paleomagnetic and ionium methods of determination. Earth Planet Sci. Lett 4, 1-16. Lampitt, R.S. and A.N. Antia, 1997. Particle flux in deep sea: regional characteristics and temporal variability. Deep-Sea Res. I, 44, 1377–1403. Lampitt, R.S.; P.P. Newton ; T.D. Jickells; J. Thomson and P. King, 2000. Near bottom particle flux in the abyssal northeast Atlantic. Deep-Sea Res. II, 47, 2051–2071. ~ 332 ~ Langmuir, D. 1996. Aqueous Environmental Chemistry. Upper Saddle Brook: Prentice-Hall Lasaga, A. C. 1998. Kinetic Theory in the Earth Sciences. Princeton: Princeton University Press, 647 p. Lasaga, A. C., and H. Ohmoto. 2002. The oxygen geochemical cycle: Dynamics and stability. Geochimica et Cosmochimica Acta 66:361–38 1. Leadbeater B.S.C. and Riding R. (eds), 1986. Biomineraliza-tion in Lower Plants and Animals. The Systematics Association Special Volume. Clarendon Press, Oxford. Lee, C.; W. Wakeham and C. Arnosti, 2004. Particulate organic matter in the sea: the composition conundrum. Ambio, 33, 565–575. Levi-Kalisman .; L. Addadi and S. Weiner. 2001. Structure of the nacreous organic matrix of a bivalve mollusk shell examined in the hydrated state using cryo-TEM. J Struct Biol 135:8-17 Levi-Kalisman Y.; S. Raz; S. Weiner; L. Addadi and I. Sagi. 2002. Structural differences between biogenic amorphous calcium carbonate phases using x-ray absorption spectroscopy. Advanced Functional Mat 12(1):43-48 Li, Y.-H., and S. Gregory. 1975. Diffusion of ions in sea water and in deep-sea sediments. Geochimica et Cosmochimica Acta 38:703– 714. Li, Y.-H. 2000. A Compendium of Geochemistry. Princeton: Princeton University Press. 569 p. Liss, P.S., 1983. Gas Transfer: Experiments and geochemical implication. In Air-Sea Exchange of gases and particles, P.S. Liss & W.G. Slinn (eds), p 241-248> Dordrecht Reidel. Loeblich Ar. And H. Tappan ., 1987. Foraminifera genera and their classification. New York, Van Nostrand Reinhold Company Loeblich, A.R. dan H. Tappan. 1994. Foraminifera of the Sahul Shelf and Timor Sea. Cushman foundation for foraminifera research special publication. 31-661 pp. ~ 333 ~ Lowenstam H.A. and G.R. Rossman., 1975. Amorphous, hydrous, ferric phosphatic dermal granules in Molpadia (Holothurodidea): Physical and chemical characterization and ecologic implications of the bioinorganic fraction. Chem Geol 15:15-51. Lowenstam H.A. and L. Margulis., 1980. Calcium regulation and the appearance of calcareous skeletons in the fossil record. In: The Mechanisms of Biomineralization in Animals and Plants. Omori M, Watabe N (eds) Tokai University Press, Tokyo, p 289-300 Lowenstam HA and Weiner S., 1989. University Press, New York On Biomineralization. Oxford Lower S.K., M.F. Hochella Jr and T.J. Beveridge., 2001. Bacterial recognition of mineral surfaces: nanoscale interactions between Shewanella and -FeOOH. Science 292:1360-1363 Mackenzie, F.T. and R. L. Kump, 1995. Reverse weathering, clay mineral formation and oceanic element cycles. Science, 270, 586–587. Manheim, F.T.; R.M. Pratt and P.F. McFarlin., 1980. Composition and orgin of phosphorus deposits of the Blake Plateau. In Marine Phosphorus-Geochemistry, Occurrence, Genesis. Y.K. Bentor (ed). SEPM Special Publication 29: 117-137. Mann S., 2001. Biomineralization: Principles and Concepts in Bioinorganic Materials Chemistry. Oxford University Press, New York. Marsh M.E., 1994. Polyanion-mediated mineralization—assembly and reorganization of acidic polysaccharides in the Golgi system of a coccolithophorid alga during mineral deposition. Protoplasma 177:108-122 Marsh M.E., 2000. Polyanions in the CaCO3 mineralization of coccolithophores. In: Biomineralization: from Biology to Biotechnology and Medical Application. Bäuerlein E. (ed) WileyVCH, Weinheim, pp 251-268. Marsh M.E.; D. Chang and G.C. King., 1992. Isolation and characterization of a novel acidic polysaccharide containing tartrate and glyoxylate residues from the mineralized scales of a unicellular coccolithophorid alga Pleurochrysis carterae. J Biol Chem 267:20507-20512 ~ 334 ~ Marsh M.E.; A.L. Ridall; P. Azadi and P.J. Duke., 2002. Glacturonomannan and Golgi-derived membrane linked to growth and shaping of biogenic calcite. J Struct Biol 139: pp 3945 Maring, H.B and R.A. Duce, 1987. The Impact of Atmospheric Aerosol on Trace Metal Chemistry in Oipen Ocean Surface Waters. 1. Aluminium. Earth Planet. Sci. Latt. 84: 381-392. Martin R.E., 1995. Cyclic and secular variation in microfossil biomineralization: Clues to the biogeochemical evolution of Phanerozoic oceans. Global Planetary Change 11:1-23 Maybeck, M. 1978. Note on Dissolved Elemental Content of The Zaire River. Neth. Jur. Sea Res. 12 293-295. Maybeck, M. 1981. Pathway of Major Elements From Land to Ocean Through River. In River inputs to Ocean System. J. M. Martin, J.D. Burton and D.Eisma (Eds), p. 18 – 30. Paris UNEP/UNESCO. Mayer, L. M. 1994. Surface area control of organic carbon accumulation in continental shelf sediments. Geochimica et Cosmochimica Acta 114:347–363. McConnaughey T., 1989. 13C and 18O isotopic disequilibrium in biological carbonates: I. Patterns. Geochim Cosmochim Acta 53:151-162 McMurray, J. and R. C.Fay. 1995. Chemistry. Englewood Cliffs: PrenticeHall, 451 p. McSween, H.Y. Jr ; S. M. Richardson dan Maria E. Uhle. 2003. GEOCHEMISTRY Pathways and Processes (Edisi kedua). Columbia University Press. in the United States of America. 494 h. Meade, R.H., 1972. Transport and Deposition of Sediment in Estuaries. Geol. Soc. Am. Mem. 133 : 91-120 Medlin LK; W.H.C.F. Kooistra; D. Potter; J.B. Saunders and R.A. Andersen., 1997. Phylogenetic relationships of the "golden algae" (haptophytes, heterokont chromophytes) and their plastids. Pl Syst Evol Suppl 11: 187-219 ~ 335 ~ Middleburg, J.J. and L.A. Levin, 2009. Coastal hypoxia and sediment biogeochemistry. Biogeosciences, 6, 1273–1293. Milliman J.D., 1993. Production and accumulation of calcium carbonate in the ocean: budget of a non steady state. Global Biogeochem Cycles 7:927-957 Minkowyez, w.J., E.M. Sparrow, G.E. Schneider dan R.H. Pletcher (editor), 1988. Handbook of Nurerical Heat Transfer. John Wiley & Sons. New York. Moffett, J.W., 1990. Microbially Mediated Cerium Oxidation in Seawater. Nature, 345:421-423. Moore, J.; W.R. Normark and R.T. Holcomb., 1994. Giant Hawaiian underwater landslides. Science, 264: 46-47. Morel, F.M.M., 1983 , Principles of Aquatic Chemistry. A Wiley-Inter. Pub. Jhon Wiley & Sons. 446 p Morgenstein, M., 1992. Manganese accreation at the sediment water interface at 400-2400 meters depth, Hawaiian Achipelago. In ferromanganese Deposit on Ocean Floor. D.R. Horn (ed), Arden House, Harriman, New York, pp 131-138. Muller, P.J. and A. Mangini, 1980. Organic carbon decomposition ratio in sediments of the Pacific manganese nodule belt dated by 230Th and 231Pa. Earth Planet. Sci. Lett., 51, 96–114. Murton, B.J; L.M.Parson; P.J.Hunter and P.R. Miles, 2004. Evaluation of Non-living Resources of the Continental Shelf Beyond 200mile Limit of the World’s Margins. In Minerals other than Polymetallic Nodules of The International Seabed Area. Proceeding of a workshop, Kingston, Jamica : p 667-761. Natsir, S.M. 2010. Kelimpahan foraminifera resen pada sedimen permukaan di Teluk Ambon. J. Ilmu dan Teknologi Kelautan Tropis, 2(1):9-18. Natsir, S.M. dan Rubiman. 2010. Distribusi foraminifera bentik Resen di Laut Arafura. J. Ilmu dan Teknologi Kelautan, 2(2):74-82. Nriagu, J.O., 1979. Global Inventory of Natural and Antropogenic Emissions of Trace Metals to the Atmosphere. Nature 279, 409411. ~ 336 ~ Ohmoto, H., and R. O. Rye. 1979. Isotopes of sulfur and carbon. In H. L. Barnes ( ed.) Geochemistry of Hydrothermal Ore Deposits, 2nd ed. New York: Holt, Rinehart, and Winston, pp. 509–567. Olson, J. S., R. M. Garrels, et al. 1985. The Natural Carbon Cycle. Atmospheric Carbon Dioxide and the Global Carbon Cycle. J. R. Trabalka, ed. Washington, D.C.: U.S. Department of Energy, pp. 175–213. Open University, 1996. The Open University Courses Oceanography. Unit 1-12 (Milton Keynes). The Open Univesrsity Press. Oremland, R.S. and B.F.Taylor, 1978. Sulfate reduction and methanogenesis in marine sediments. Geochim. Cosmochim. Acta, 42, 209–214. Oxtoby, D.W., H.P. Gillis dan N.H. Nachtrieb. 2001. Prinsip-Prinsip Kimia Modern (Edisi ke 4). Alih bahasa, S.S. Achmadi. Editor Silverter L Sinarmata. Erlangga. Jakarta. Oxtoby, D.W., W.A. Freeman dan T.F. Block. 2003. Chemistry , Science of Change. (4th edition). Thomson Brooks/Cole. USA. Ozaki N; S. Sakuda and H. Nagasawa., 2001. Isolation and some characterization of an acidic polysaccharide with anticalcification activity from coccoliths of a marine alga, Pleurochrysis carterae. Biosci. Biotechnol Biochem 65:23302333 Parker, V. B., D. D. Wagman, and W. H. Evans. 1971. Selected Values of Chemical Thermodynamic Properties: Tables for the Alkaline Earth Elements (Elements 92 through 97 in the Standard Order of Arrangement). Technical Note 270-6. Washington, D.C.: U.S. National Bureau of Standards. Perry Carole C. 2003. Silicification: The Processes by Which Organisms Capture and Mineralize Silica. In Biomineralization by Jodi J. Rosso (Edt) on Review in Mineralogy and Geochemistry. Mineralogical Society of America, Geochemistry Society, Vol 54, 291- 327 Philpotts, A. R., 1990. Principles of Igneous and Metamorphic Rocks. Englewood Cliffs: Prentice-Hall. 476 p. ~ 337 ~ Pienaar R.N., 1994. Ultrastructure and calcification of coccolithophores. In: Coccolithophore. Winter A, Siesser WG (eds) Cambridge University Press, Cambridge, p 13-37 Pichocki, C. and M. Hoffert., 1987. Characteristic of Co-rich ferromanganese nodules and crust sampeled in French Polynesia. Marine Geology, 77: 109-119. Potsma, H., 1980. Sediment Transport and Sedimentation. In Chemistry and Biochemistry of Estuarie. E. Olausson and I. Cato (eds), 153-186. New York. Pytkowicz, R. M. 1983. Equilibria, Nonequilibria, and Natural Waters, vol. I. New York Prospero, J.M. 1981. Eolian Transport To The World Ocean. In The Sea C. Emiliani (ed) vol 7, 801 – 874. New York: interscience. Quimby-Hunt, M. S., and K. K. Turekian. 1983. Distribution of elements in sea water. EOS, Transactions of the American Geophysical Union 64:130–131. Raven J.A; H. Griffiths; S.M. Glidewell and T. Preston. 1982. The mechanism of oxalate biosynthesis in higher plants: Investigating with the stable isotopes 18O and 13C. Proc R Soc London B, Biol Sci 216:87-101 Remane J., 2000, International stratigraphic chart. International Union of Geosciences. IUGS Secretariat, Geological Survey of Norway, Trondheim, Norway Rifardi, 2012. Ekologi Sedimen Laut Moderen. UR PRESS Pekanbaru. 164 h. Rompas, R.M.; N.D.C. Rumampuk dan J.R. Rompas. 2006. Oseanografi Kimia. Dewan Kelautan Indonesia. Jakarta. 262 h. Rompas, R.M., 2010. Toksikologi Kelautan. Sekretariat Dewan Kelautan Indonesia. 338 h. Rompas. R.M.; Aryo Hanggono dan Gabriel A. Wagey. 2013. Tingkap Langit Taburi Laut Nusantara. Suatu Kekuatan Ekonomi Dan Ketahanan Bangsa. Balitbang Kementerian Kelautan dan Perikanan. 306 h. ~ 338 ~ Romano S.L. and S.D. Cairns, 2000. Molecular phylogenetic hypotheses for the evolution of scleractinian corals. Bull Mar Sci 67:1043–1068 Rona A.P., G.Klinkhammer, T.A. Nelson, J.H. Trefry and H. Elderfield., 1986. Black Smokers, Massive Sulphides and Vent Biota at the Mid-Atlantic Ridge. Nature 321, pp 33-37. Rona A. Peter. 2004. Metallogenesis of Marine Mineral Resouurces. Dalam Prosiding workshop Tentang Minerals Other Than Polymetallic Nodules of The International Seabed Area (volume I), Dilaksanakan pada tanggal 26-30 Juni 2000 di Kingston Jamaica. h 69-92 Saxena, S. K. 1973. Thermodynamics of Rock-Forming Crystalline Solutions. New York: Springer-Verlag. Schiebel R., 2002., Planktonic foraminiferal sedimentation and the marine calcite budget. Global Biogeochem Cycles 16(4):13-1–1321 Schnitzer, M. 1986. Reactions of humic substances with metals and minerals. In D. Carlisle, W. L. Berry, I. R. Kaplan, and J. R. Watterson, eds. Mineral Exploration: Biological Systems and Organic Matter. Englewood Cliffs: Prentice-Hall, pp. 408–427. Schneider, R. R.; Horst D. Schulz and Christian Hensen, 2006 Marine Carbonates: Their Formation and Destruction. In Marine Geochemistry, Horst D Schulz and Matthias Zabel (eds). Springer-Verlag Berlin Heidelberg. Germany. pp 311-337. Schüler D. and R.B. Frankel., 1999. Bacterial magnetosomes: Microbiology, biomineralization and biotechnological applications. Applied Microbiol Biotech 52:464-473 Seinfeld, John H.; Pandis, Spyros N., 2006. Atmospheric Chemistry and Physics - From Air Pollution to Climate Change (2nd Ed.). John Wiley and Sons, Inc. Seiter, K.; C. Hensen; J. Schröter and M. Zabel, 2004. Organic carbon content in surface sediments – defining regional provinces. Deep-Sea Res. I, 2001–2026. Siegenthaler U. and J.L. Sarmiento., 1993. Atmospheric carbon dioxide and the ocean. Nature 365(9):119-125 ~ 339 ~ Sigman D.M. and E.A. Boyle., 2000. Glacial/interglacial variations in atmospheric carbon dioxide. Nature 407(6806):859-869 Simkiss K., 1986. The processes of biomineralization in lower plants and animals-an overview. In: Biomineralization in Lower Plants and Animals. Vol 30. Leadbeater BSC, Riding R (eds) Oxford University Press, NY, p 19-37 Simkiss K. and K. Wilbur., 1989. Biomineralization. Cell Biology and Mineral Deposition. Academic Press, Inc., San Diego. Siswanto, A.D. 2011. Kajian Sebaran Substrat Sedimen Permukaan Dasar Di perairan Pantai Kabupaten Bangkalan. Embryo. Vol. 8. No.1. p 1-8. Smith, E. B. 1982. Basic Chemical Thermodynamics, 3rd ed. New York: Oxford University Press Skinner H.C.W. and J. Brian., 1976, Earth Resources. Prentice Hall, 643 p. USA. Skinner H.C.W. and A.H. Jahren ., 2003. Biomineralization. Biogeochemistry: Treatise on Geochemistry. W. H. Schlesinger, Elsevier Science. 8: 45-93. Soetart, K.; P.M.J. Herman and J.J. Middelburg, 1996. A model of diagenetic processes from the shelf to abyssal depths. Geochim. Cosmochim. Acta., 60, 1019–1040. Sri Saeni M. 2006. Kinetika Kimia. Diktat Kuliah Kimia (Edisi revisi) Dep. Kimia FMIPA IPB. P. 189-203. Stallard, R.F. and J.M. Edmond, 1981. Geochemistry of the Amazon 1. Precipitation Chemistry and the Marine Contribution to the Dissolved Load at the time of Peak Discharge. J. Geophys. Res. 86, 9844-9858. Stallard, R.F. and J.M. Edmond, 1983. Geochemistry of the Amazon 2, The Influence of Geology and Weathering Environment on the Dissolved load. J Geophys. Res. 88, 9671-9688. Stallard, R.F. and J.M. Edmond, 1987. Geochemistry of the Amazon 3, Weathering Chemistry and Linits to dissolved inputs. J Geophys. Res. 92: 8297-8307. ~ 340 ~ Stumm W., 1992. Chemistry of the Solid-Water Interface. John Wiley & Sons Inc, New York 346 p. Stumm, W., and J. J. Morgan. 1995. Aquatic Chemistry, Chemical Equilibria and Rates in Natural Waters, 3rd edt. New York: Wiley and sons, INC. 1021 h. Subroto E. Ariyono, 2011. Peran Geokimia Petrolium Dalam Usaha Ekploitasi Migas di Indonesia. Pidato pengukuhan guru besar di Institut Teknologi Bandung. 32 h. Sullivan B.K; C.B. Miller ; W.T. Peterson and A.H. Soeldner., 1975. A scanning electron microscope study of the mandibular morphology of boreal copepods. Marine Biol 30:175–182 Sumper M and Nils Kröger., 2004. Silica formation in diatoms: the function of long-chain polyamines and silaffins. Juornal Mater . Chem. Vol. 14, pp 2059-2065. The royal Society of Chemistry. Germany. Sundby, B.; N. Silverburg and R. Chesselet 1981. Pathways of Manganese in An Open Estuarine System. Geochim. Cosmochim Acta 45, 293-307 Sundquist, E. T. 1985. Geological perspectives on carbon dioxide and the carbon cycle. In E. T. Sundquist and W. S. Broecker, eds. The Carbon Cycle and Atmospheric CO2: Natural Variations Archean to Present. American Geophysical Union Monograph 32. Washington, D.C.: American Geophysical Union, pp. 5–60. Suradikusumah E. Dan H. Purwaningsih. 2006. Kesetimbang-an Kimia. Diktat Kuliah Kimia (Edisi revisi) Dep. Kimia FMIPA IPB. P. 136-153. Svedrup H.U. Martin W. Jhonson and Richard H. Fleming., 1962. The Oceans. Their Physics, Chemistry and General Biology. Pub. Prentice-Hall. Eleventh Printing, US. America. 1089 p. Swift D.M dan A.P. Wheeler., 1991. Some structural and functional properties of a possible organic matrix from the frustules of the freshwater diatom Cyclotella meneghiniana. In: Surface Reactive Peptides and Polymers. Vol 444. Sikes CS, A.P. Wheeler (eds) American Chemical Society, Washington, DC, p 340-353 ~ 341 ~ Swift D.M. dan A.P. Wheeler., 1992. Evidence of an organic matrix from diatom biosilica. J Phycol 28:202-209 Takematsu, N.; Y. Sato and S. Okabe., 1989. Factor Controling the Chemical Composition of Marine Manganese Nodules and Crusts: A review and synthesis. Marine Chemistry. 26: 41-46. Tebo B.M.; W.C. Ghiorse; L.G. van Waasbergen ; P.L. Siering and R. Caspi., 1997.. Bacterially mediated mineral formation: Insights into manganese(II) oxidation from molecular genetic and biochemical studies. Rev Mineral 35:225-266 Ter Kuile B. and J. Erez., 1984. In-situ growth rate experiments on the symbiont bearing foraminifera Amphistegina lobifera and Amphisorus hemrprichii. J Foramin Res 14(4)262-276 Ter Kuile B. and J. Erez., 1987. Uptake of inorganic carbon and internal carbon cycling in symbiont-bearing benthonic foraminifera. Mar Biol 94:499-510 Ter Kuile B. and J. Erez., 1988. The size and function of the internal inorganic carbon pool of the foraminifer Amphiseigina lobifera. Mar Biol 99:481-487 Ter Kuile B.; J. Erez and E. Padan., 1989a. Competition for inorganic carbon between photosynthesis and calcification in the symbiont-bearing foraminifer Amphistegina lobifera. Mar Biol 103:253-259 Ter Kuile B.; J. Erez and E. Padan. 1989b. Mechanisms for the uptake of inorganic carbon by two species of symbiont-bearing foraminifera. Mar Biol 103:241-251 Thomas L.C. 1992. Heat Transfer. Prentice hall, Englewood Cliffs, New Jersey. London. 804 h. Thompson, G. 1983. Hydrothermal Fluxes in the Ocean. In Chemical oceanography. J.P Riley & R. Chester (eds). Vol 8, 270-337. London. Academic Press. Thompson, J. B., J. Laird, and A. B. Thompson. 1982. Reactions in amphibolite, greenschist, and blueschist. Journal of Petrology 23:1–27. Tissot, B.P. and D.H. Welte, 1984. Petroleum Formation and Occurrence. Berlin: Springer-Verlag. ~ 342 ~ Tri Dewi K. dan Mustafa Hanafi., 2013. Karakteristik Komunitas Foraminifera Laut Dalam di teluk Tomini, Sulawesi. Jurnal Ilmu dan Teknologi Kelautan Tropis, Vol. 5, No. 1, Hlm. 17-25 Uematsu, M., R.A. Duce, J.M. Prospero, L.Chen, J.J. Merril and R.L. McDonald, 1983. Transport Mineral Aerosol From Asia over the North Pasific Ocean . J. Geophys. Res. 88: 5343-5352 Uematsu, M., R.A. Duce, T, Patterson and J.M. Prospero, 1985. Spatial Distribution of Mineral aerosol over the Southwest Pasific Ocean. SEAREX News 8, 34-38. Ujiie, H. and F. Shioya. 1980. Sedimen in Bay of Nago and Around the Island s of Sesoko. Sesoko. Mar. Sci. Lab., Tech. Rept. 7 : 1-17. Ujiie, H and Rifardi, 1993. Some Benthic Foraminifera from The Oura River Estuary and its Environs, Okinawa. Bull. Coll. Sci., Univ. Ryukyus, 56, 121-243. Ujiee, H. and Y. Oshiro, 1993. Surface Sediments of Coral Seas, West of miyako Island and its environs, Ryukyus Island Arc, Japan. Rep.Tech.Res.Center. Japan National Oil Corpseamount. Usui, A.; A. Nishimura and K. Lizasa., 1993. Submersible observations of manganese nodule and crust deposits on the Tenpo seamount north-western Pasific. Marine Georesources and Geotechnology, 11: 263-291. Van Cappellen P., 2003. Biomineralization and global biogeochemical cycles. Rev Mineral Geochem. 54:357-381 Veis Arthur, 2003. Mineralization in Organic Matrix Frameworks. In Biomineralization by Jodi J. Rosso (Edt) on Review in Mineralogy and Geochemistry. Mineralogical Society of America, Geochemistry Society, Vol 54, 249-289 Warneck, Peter, 2000. Chemistry of the Natural Atmosphere (2nd Ed.). Academic Press Watabe N. and R.J. Kingsley., 1989. Extra-, inter-, and intracellular mineralization in invertebrates and algae. In: Origin, Evolution, and Modern Aspects of Biomineralization in Plants and Animals. Crick RE (ed) Plenum, New York, p 209-223 ~ 343 ~ Wayne, Richard P. 2000. Chemistry of Atmospheres (3rd Ed.). Oxford University Press. Webb M.A., 1999. Cell-mediated crystallization of calcium oxalate in plants. Plant Cell 11:751-761 Weisel, C.P.; R.A. Duce; J.L. Fasching and R.W. Heaton, 1984. Estimates of the Transport of Trace Metals from the Ocean to the Atmosphere. J. Geophys. Res. 89: 11607-11618. Weiss, R.F. 1970. The Solubility of Nitrogen, Oxygen and Argon in Water and sea Water. Deep Sea Res. 17. 721-735. Weiss I.M.; N. Tuross; L. Addadi and S. Weiner., 2002. Mollusk larval shell formation: amorphous calcium carbonate is a precursor for aragonite. J Exp Zool 293:478-491. Weiner S, W. dan T. H.D. Wagner, 1999. Lamellar bone: structurefunction relations. Journal of Structural Biology 126: 241-255 Weiner S and L. Addadi., 2002. At the cutting edge. Perspectives. Science 298:375-376 Weiner S. and Patricia M. Dove, 2003. An Overview of Biomineralization Processes and the Problem of the Vital Effect. In Biomineralization by Jodi J. Rosso (Edt) on Review in Mineralogy and Geochemistry. Mineralogical Society of America, Geochemistry Society, Vol 54, 1-29. Weiner S. and J.J. Morgan. 1996. Aquatic Chemistry. Chemical Equilibria and rates in Natural Waters. Third Editions. WileyInterscience Pub. New York. Westbroek P.; J.R. Young and K. Linschooten., 1989. Coccolith production (Biomineralization) in the marine alga Emiliania huxleyi. J. Protozool 36:368-373 Williams A.; C. Luter and M. Cusack. 2001. The nature of siliceous mosaics forming the first shell of the brachiopod Discinisca. J Structur Biol 134:25–34. Wilson, T.R.S.; J. Thompson; S. Colley; D.J. Hydes and N.C. Higgs., 1985. Early organic diagenesis: the significance of progressive subsurface oxidation fronts in pelagic sediments. Geochim. Cosmochim. Acta, 49, 811–822. ~ 344 ~ Wilt F.H., 1999. Matrix and mineral in the sea urchin larval skeleton. J Struc Biol 126:216-226. Wilt F.H., 2002. Biomineralization of the spicules of sea urchin embryos. Zool Sci 19:253-261. Wolery, T.J and N.H. Sleep, 1976. Hydrothermal Circulation and Geochemical Flux at Mid-Oceanic Ridges. J. Geol. 84, pp 249276. Wood, B. J., and D. G. Fraser. 1977. Elementary Thermodynamics for Geologists. Oxford: Oxford University Press. Wood, W. W., and M. J. Petratis. 1984. Origin and distribution of carbon dioxide in the unsaturated zone of the southern high plains of Texas. Water Resources Research 20:1193–1208. Yamazaki, Y., 1993. A re-evalution of cobalt-rich crust abudance on the Pacific seamounts. International Journal of offshore and Polar engineering, 3:259-263. Yamazaki, T.; Y. Igarashi and K. Maeda., 1993. Buried cobalt rich manganese deposits on seamounts. Resource Geology Special Issue. 17: 76-82. Young J.R.; S.A. Davis ; P.R. Bown and S. Mann., 1999. Coccolith ultrastructure and biomineralization. J Struct Biol 126:195-215 Young J.R. and Karen Henriksen. 2003. Biomineralization Within Vesicles: The Calcite of Coccoliths. In Biomineralization by Jodi J. Rosso (Edt) on Review in Mineralogy and Geochemistry. Mineralogical Society of America, Geochemistry Society, Vol 54, 189-247. Zeebe R.E. and A. Sanyal., 2002. Comparison of two potential strategies of planktonic foraminifera for house building: Mg 2+ or H+ removal?. Geochim Cosmochim Acta 66(7):1159-1169 ~ 345 ~ Lampiran ~ 346 ~ Lampiran 1 Tabel Penjelasan Simbol Kimia yang terterah pada Tabel 11.4. Zat Kimia Fe Mn Si Na Al K Mg Ca Ti P S Cl CO2 Ag As B Ba Be Bi Br Cd Co Cr Cu Ga Hf Li Mo Nb Ni Pb Rb Sb Sc Nama umum Zat Kimia Besi Mangan Silikon Natrium Aluminium Kalium Magnesium Kalsium Titanium Fosfat Sulfur Klorida Karbon dioksida Perak Arsenik Boron Barium Beryllium Bismuth Bromida Kadmium Kobalt Khromium Tembaga Gallium Hafnium Lithium Molybdenum Niobium Nikel Timah Rubidium Antimony Scandium Se Sn Sr Te Tl Th U V W Y Zn Zr La Ce Pr Nd Sm Eu Gd Tb Dy Ho Er Tm Yb Lu Hg Au Ir Pd Pt Rh Ru Nama Selenium Tin Strontium Tellurium Thallium Thorium Uranium Vanadium Tungsten Yttrium Seng Zirconium Lanthanum Cerium Praseodymium Neodymium Samarium Europium Gadolinium Terbium Dysprosium Holmium Erbium Thulium Ytterbium Lutetium Merkuri Emas Iridium Palladium Platinum Rhodium Ruthenium Keterangan: Zat kimia La s/d Lu adalah elemen di bumi yang kandungnnya sangat sedikit (cetak tebal); zat kimia Ir s/d Ru adalah elemen grup platinum. Sumber: Hein (2004). ~ 347 ~ Lampiran 2 ~ 348 ~ Lampiran 3. Beberapa Unsur Kimia Penting Di Perairan Umum ~ 349 ~ Lampiran 4 Formula kimia dan Nama Umum Unsur-unsur yang ada dalam jaringan: H Hydrogen C Karbon N Nitrogen O Oksigen S Sulfur P fosfat Besi – Mangan (Fe-Mn)/ Kobalt kaya Ferromanganese di kerak bumi : Fe Besi Mn Mangan Cu Tembaga Co Kobalt Ion-ion Konservasi: Na+ Natrium ClKlorida K+ Kalium Ca2+ Kalsium Mg2+ Magnesium SO42+ Sulfat Radionukleotida di alam: U Th Pa Rn Ra Po Pb He 3H Uranium Thorium Protactinium Radon Radium Polonium Timah hitam Helium Tritium ~ 350 ~ Sistem Karbonat: CO2 H2CO3 HCO2CO32CaCO3 C(H2O) ∑CO2 C.A. Gas-Gas: Ne Ar O2 Kr N2 CO2 CH4 H2 H2 S N2O Karbon dioksida Asam karbonat Bikarbonat Karbonat Kalsium karbonat Bahan organik Total karbon anorganik terlarut Karbonat alkalinitas Neon Argon Oksigen Krypton Nitrogen Karbon dioksida Methan Hidrogen Asam sulfur Nitrooksida Komponen Nitrogen: N2 NO3NO2H2 O NH4+ NH3 Gas Nitrogen Nitrat Nitrit Nitrooksida Amonium Amonia Jenis kimia lainnya: PO43Fosfat H4SiO4 Asam Silisik SiO2 Silika Si Silikon ~ 351 ~ Lampiran 5 Simbol dan Cara Baca Alfabet Yunani Alpha A a Iota I I Rho P π Beta B β Kappa K κ Sigma ∑ σ Gamma Г γ Lambda Λ λ Tau Т τ Delta ∆ δ Mu М μ Upsilon Υ ν Epsilon Ε Є Nu И υ Phi Ф υ Zeta Ζ δ Xi Ξ ξ Chi Х א Eta Η ε Omicron Ο ο Psi Ψ ψ Theta Θ ζ Pi Π π Omega Ώ ω ~ 352 ~ Lampiran 6 Satuan Ukuran dan Konversi Satuan Besaran : atto ( a ) femto ( f ) pico ( p ) nano ( n ) micro ( μ ) milli ( m ) centi ( c ) deci ( d ) deca ( da ) hector ( h ) kilo ( k ) mega ( M ) giga ( G ) tera ( T ) Satuan Panjang : = 0,000000000000000001 = 0,000000000000001 = 0,0000000000001 = 0,000000001 = 0,000001 = 0,001 = 0,01 = 0,1 = 10 = 100 = 1000 = 1.000.000 = 1.000.000.000 = 1.000.000.000.000 1 ǻngström (Ǻ) 1 nanometer (nm) 1 mikron (μm) 1 millimeter (mm) 1 centimeter (cm) 1 inci 1 decimeter 1 meter (m) 1 kilometer (km) = 0,001 micron = 10-9 meter = 0,001 mm = 1000 mikron = 0,394 inci = 2,54 cm = 0,1 m = 39,37 inci = 1000 m = 0,62 mil darat = 10-10 m 1 mil darat = 5280 kaki = 0,87 mil laut = 6076 kaki = 1,15 mil darat = 2,54 cm = 0,3048 m = 0,9144 m = 1,83 m = 1,6 km 1 mil laut 1 inci 1 kaki 1 yard 1 fathom ~ 353 ~ = 10-6 = 10 Ǻ = 0,001 m = 3,281 kaki = 3280 kaki = 0,54 mil laut = 1,85 km = 12 inci = 3 kaki = 6 kaki = 10-18 = 10-15 = 10-12 = 10-9 = 10-6 = 10-3 = 10-2 = 10-1 = 101 = 102 = 103 = 106 = 109 = 1012 Luas : 1 cm2 1 m2 1 kaki2 1 inci2 1 are 1 km2 = 100 mm2 = 104 cm2 = 0,0929 m2 = 6,452 cm2 = 100 m2 = 106 m2 = 0,386 mil darat2 1 hektar (ha) = 10.000 m2 = 0,155 inci2 = 10,76 kaki2 = 144 inci2 = 247,1 acre = 0,292 mil laut2 Volume: 1 ml = 0,001 liter 1 liter = 1.000 cm3 1 gallon (gal) = 3,785 dm3 = 231 inci3 3 1m = 106 cm3 3 1 kaki = 1728 inci3 Fluida Amerika= 0,0353 kaki3 1 kaki3 = 7,481 gal = 2,832 X 10-2 m3 = 1 cm3 = 1 cc = 1,0576 kuart = 3,785 liter = 6,102 X 104 inci3 = 2,83 X 10-2 m3 = 28,32 liter Kecepatan: 1 knot = 1 mil laut/jam = 1,15 mil darat/jam = 1,85 km/jam = 0,515 m.S-1 atau 16.234 Km/tahun 1 mil darat/jam= 1,47 kaki/detik= 0,447 m/detik= 1,62 km/jam 1 m/detik = 100 cm/detik = 3,281 kaki/detik 1 mil darat/menit = 88 kaki/detik = 60 mil darat/jam Kecepatan suara di air laut salinitas 35% = 1507 m/detik Massa: 1 mg = 0,001 gram 1 kg = 1000 g 1 pound (lb) = 453,6 gram 1 ton (ton metrik) = 1000 kg 1 slug = 14,59 kg 1u = 1,66 X10-27 kg 1 ton panjang (Inggris) = 1.016 Mg 1 ton pendek (Amerika) = 0,907 Mg ~ 354 ~ = 2,2 pound = 106 g = 1 Mg Tekanan: 1 bar 1 atmosfir = 105 N/m2 = 14,50 lb/inci2 = 760 mm Hg = 76,0 cm Hg = 14,7 lb/inci2 = 1,013 X 105 N/m2 = 12,5 psi 1 Pa (Pascal) = 1 N/m2 = 1,45 X 10-4 lb/inci2 Temperatur: 0C 0K = 5/9 (0F-32) = 273.15 + 0C Energi: 1J = 0,738 kaki 1 lb = 107 erg 1 kal = 4,186 J 1 Btu = 252 kal = 1,054 X 103 J -19 1 eV = 1,6 X 10 J 931,5 MeV ekivalen dengan 1 u 1 kWh = 3,60 X 106 J Gaya: 1N = 105 dyne 1 lb = 4,448 N 1 dyne = 10-5 N = 0,2258 lb = 2,248 X 10-6 lb Daya: 1 tenaga kuda = 550 kaki*lb/detik = 0,746 kW 1W = 1 J/detik = 0,738 kaki*lb/detik 1 Btu/jam = 0,293 Unit Konsentrasi: M m μg-atom/L % (persen) ppt ppm ppb = 1 mole yang terlarut pada satu liter larutan = 1 mole yang terlarut dalam kg pelarut = μM = mg-atom/m3 = 1 g/100 mL = g/1000 ml = g/L = 10-3 g/1000 ml = mg/L = 10-6 g/1000 ml = μl/L ~ 355 ~ Lampiran 7. Siklus Karbon Dalam Kaitan Perubahan Iklim Global Sumber : Chester dan Jickells (2012). ~ 356 ~ Lampiran 8. CaCO3 di permukaan sedimen [%] Sebaran Karbonat di Laut Secara Umum Laut Sumber: Archer (1996) ~ 357 ~ Lampiran 9. SISTEM KARBONAT DI LAUT DALAM Sumber: Archer (1996) ~ 358 ~ Lampiran 10. Sumber Produksi Karbon Anorganik di Laut serta Kecepatan Akumulasi (satuan X 1012 mol per tahun) Sumber: Milliman dan Droxler, 1996). ~ 359 ~ PENJURUS IKHWAL A Abundant, 2, Aluminium, 2, 12,72,79, Astenosfer, 13 Abisal, 26, 170, Atmos, 27 Atmosfer, 27, 28, 35, 36, 43, 45, 46,60,63,64, 66,69,70,76,77, 144,157, 158, Argon, 27,60, 145,147, Amphiboles, 54, Aerosol, 60, 66,67,68,69,70,76,77, Antropogenik, 60, 62,65,73,74, 160,166, Asam arang, 61, Atlantik, 65,66, Anomalously enrich element, 72,75, Atmospheric interference factor, 73, Adiabatik, 93,95, Alotropi, 112, Aragonit, 134, Alkalinitas, 160, Arus di laut, 185, Air antara di sedimen, 214, Aktivitas electron, 216, Anaerob, 221, Anoksit, 223, Amorf, 232,264, Air interstitial, 236,239,241,243, 244,246, Archean, 256, Alveolate, 259, Asam silikik, 265, Aragonit, 275, B ~ 360 ~ Belerang,2, Besi, 3, 12, 23,79, 94,151,234,270,296, Basin modeling, 8, Biogeokimia, 10, Bikarbonat, 23,46,162,163, Bongkahan, 37, 79,82, 195,208,306 Bakteri, 37,77,163,217, 254, Biolimiting factor, 41,42, Bluegreen algae, 41, Bahan terlarut di sungai dan laut, 59, Biosfer, 64, Bioaktif, 236, BOD, 151, Biogeneuos, 175,210, Biogenic, 178,270, Bed load,188, Biomineralisasi, 253,259,271,279,282,286,290, Biomineral, 254,257,263,267,271,274, Biosilika, 261,266, C D Continental shelf, 26,168, Continental slope, 26,168, Continental rise, 26, 27,168,170, Continental margin, 167, Cerium, 39,80,296, Calcite, 55, COD, 151, Cyanophaecea, 156, Cosmogenous, 175, Calcareous oozes, 192,193,195,210, Calcareous, 278, Coccolith ooze, 192, Coccolith, 280, 281, 285, Carbonat ooze, 207, Cerozoan, 259, Coccolithophere, 283,284, Coccosphere, 286, Detritus, 183, Deposisi, 184, Diatom ooze, 193,262 Diagenesis, 214,217,226,232,234,237,250,251, Denitrification, 221, Deuterotome, 259, Demospongs, 260, Diploid, 282,283 E Delta, 52, Dolomit, 55, Debu di troposfer, 65, Debu, 66, 67, Derajat kespontanan, 101, Difusi, 120, 133, 240 Dekomposisi spinodal, 127, ~ 361 ~ Elemen kimia di laut, 38, Elemen utama di sungai, 49, Enrichment factor (EF), 71 Emisi partikel di atmosfer, 73, Emisi, 74, Energi, 85, 90,97,98, 105, Energi potensial, 90,91,119, Energi kinetic, 91,119, Entalpi, 98,99, Entropi, 100,101, 102, 103,104,111,112, Energi bebas, 107,108,125, Energi aktivasi, 117, Elnino, 157, Eoldiagenesis,181, Earlydiagenesis, 181, Erosi, 184,200, Effective diffusion coefficient, 239, Eukaryotik, 255,258, Era Mesoproterozoic, 256, F G Fe-Mn, 2, 18, 33, 39, 294,296, 298,299,303,306,308, Fosfat, 15, 33,41,164, Fluvial, 44, Feldspars, 54, Fosil, 72, Fluida, 85, 210, Fixed boundry, 93, Forsterit, 125, Feldspars, 126,127, Foraminifera, 199,275,291, Fragmen silikat, 200, Fragmen allochem, 200, Fungsi elektronegatif, 213, Fosfat, 267,270,301, Gradien konsentrasi, 129, Gas, 137,138,139,142,143,144,146,148,155,161, 162,166, Gas non-variabel di atmosfer, 137, Glaukonit, 174, Gravitasi arus, 185, Globigeina ooze, 192, H Geologi, 1, 14, 46, 256, Geochemical cycle, 3, Garam dapur, 24, Garam Inggris, 24, Guyot, 27, Glacial, 44, 45, Geothermal, 79, Gaya, 88, Grativitas, 97, Gibbs, 105, Hidrosfer, 19, Hg, 33,80, H2S, 39,144, 164, 165, Helium, 61, Hidrothermal, 77,79, 82,176, Hukum Newton ke2, 86, Hukum kekalan energi, 90,91,98, Hukum Fick, 238, Helmhltz function, 105, High nutrient-low chlorophyll, 165, Hemi-pelagik, 171,180,190,209,228,229, Hidrogenous, 175, 193, 195, 209, 210; Heterokont, 259, Haptophyte, 259, Holothurians, 269, Haploid, 282,283, Heteroccocolith, 284,285,287, Holoccocolith, 284,287, Hidrogenetik, 306, ~ 362 ~ I Inti Bumi, 1, 12, International Seabad Authority, 7, Ionosfer, 30, Igneous, 37, Ionic ratio, 47, Ion utama di sungai, 52, Isoterm, 87,101, Internal energik, 96, Interface, 141, 143,148,150, Ion karbonat, 159, Ion bikarbonat, 159, Interstitial water, 210, Inarticulate shell, 270, J Jesus Kristus, 14, James Joule, 94, K Kerak bumi, 1, 11, 12, Kerak Samudera, 11, 78,300, Kalsium, 2, 12, 15, 21, 22, 23, 30,46,47,207, 241,291, Kalsit, 134, 285, Kobalt, 2, 3, 18, 39, 294, 296,301, Katadoluminisen, 6, Kalium, 12, 22, 23, 245, Kambium, 14, Karbon, 15, 229,230, Klorida, 21, 33, 36,46,48, Kimia utama, 22, 40, Karbonat, 23, 51, 54, 162,163, 253,259,260, Karbondioksida, 28, 33, 39,60,145,147,157,158, 159,161,162, 164,278,288,292, Kimia konservatif, 31, Kalium klorida, 34, Kadmium, 42, Kristalisasi, 48, 113, Kuartz, 54, Koagulasi, 64, Kesetimbangan dinamika, 83, Kalor, 85, 87,91, 93,97,99,101,104, Kapasitas kalor, 92, Kinetika, 113, 116, 133,136, Kristal, 115,121, 129,131,132,133,269,270, Koefisien interdifusi, 120, Kelarutan oksigen di laut, 140,152, Koefisien difusi, 144, Kloroflorokarbon (CFC), 146, Korosi, 151, Kompaksi, 184,200, Kimia di sedimen laut, 199, Komposisi elemen di sedimen laut, 202,205, Katagenesis, 232, Karogen, 232, Kecepatan adveksi, 242, Karboksilat, 253, ~ 363 ~ L M Logos, 1 Litosfer, 13, Landas kontinen, 26, Lapisan Atmosfer, 29, Lapse rate, 29, 30, Limestone, 37, Logam mikro di atmosfer, 75, Listrik, 97, Laju reaksi, 114,115, Lapisan stagnan, 149, Lanina, 157, Lithougeneous, 175,193,195,209,210, Latelydiagenesis, 181, Lateral sea-bed, 186, Litifikasi, 200, Lateral, 235, Magnesium, 2, 12, 21, 33, 39,48,53, 242,243, Mesosfer, 13, 28, Manado, 21, Morfologi, 25, 26,167,297, Mid ocean ridge, 27, Mesopause, 28, Monovalen, 32, Mineral, 54,76, Micas, 54, Mortmorillonite, 54, Molar, 87, Movable boundry, 93, Magma, 132, Mineralisasi, 163,268,272,277,278, Mineral, 254, 258, 273,275, Methan, 165, Mid oceanic ridge, 171, 172, Mesodiagenesis, 181, Mikroorganisme, 197, Mangan, 223, 296, 301, Metagenesis,232 Moluska, 254, Mitosis, 283, N Nikel, 2, 12, 39, Natrium, 12, 21, 32, 46, 47,48, 49,53, 242, Nodul. 15,79, 208, Nitrogen, 27, 30, 33, 39,42, 144, 145,147,155, 156, 221, 242, Nenon, 61, Nir-adiabatik, 96, Nukleasi, 113,122, 123, 125,127, 135, Nacreous layer, 276, O Ontos, 1 Oksigen, 27, 30,60,84, 144,145,150,151, 223, 227,233,234,243, Ozon, 43, 84, Ocean basin floor, 170, ~ 364 ~ Oksidasi, 222,248,252, Opisthokont, 259, P Palaios, 1 Porositas, 6, Porewater, 247,249, Prakambium, 14,255, Petroleum, 16, 17, Polivalen, 32, Practical salinity scale, 34, 35, Platinum, 39, ppm, 43,151, Presipitasi, 47, 48,51, Pyroxenes, 54, 113,126, Phylogenetik, 255, 257,258,260 Partially stratified, 58, Planetarie grenslag, 61, Planetary boundry layer, 61, Partikel, 62,63,64,184, Partikel di atmosfer, 63,73, 76, Pasifik, 65,179,195, PCB, 146, Piston velocity, 147, Partikel di sungai, 179, Preropod ooze, 192, Proses daur-ulang sedimen di laut, 212, Proses diagenesis di sedimen, 220, Polysulfida pyrite (FeS2), 224, Prokaryotik, 255, Paleoproterozoic, 256, Proterozoic, 256,261, Poliamin, 263, Proto-coccolith, 286, R Redfield, 42, River particulate material, 54 Radiogenik, 80, Reaksi endoterm pada entalpi, 99,119, Reaksi eksoterm pada entalpi, 99,100,119, Reaksi unimolekuler, 115, Reaksi bimolekuler, 115, Reaksi termolekuler, 115, Rate limiting step, 134, Radiolaria ooze, 193, Red clay ooze, 193, Reaktivitas laut, 213, Redoks, 215,216,218,252, S Silika, 2, 15,242,261,264,266, Silikon, 2 Siliceous, 193, Seabed minerals, 9, Suhu, 11, 12, 30,64, 85,86, 87,95, 108,109,115, 124, 128,156, Selebung mantel, 12, Sulfur, 21, ~ 365 ~ Salinitas, 21, 22, 31, 34, 35,47, Samudera Pasifik, 22,68,164,171,179, Samudera Hindia, 22,67, 171,179, Samudera Atlantik, 22,171, 179, Semi-enclosed, 23, Spheira, 27, Seamount, 27, 39,171,173, Stratosfer, 28, 30 Stratopause, 28, Sulfat, 36,70,222,223,225,234,245, Sandstone, 37, Shales, 37, Scavenging, 38, Seng, 42, Senyawa inert, 43, Siklus karbon organik, 45, Saline, 49, Sungai-sungai di Indonesia, 50, Sedimen, 55, 167, 170,174,175,177,178,180, 190, 228, Solvus, 126, 127, Spinodal,126, 127, 128, Sistem albite-anorthite, 135, Submarine canyon, 169, 170, Sedimen di laut, 179,185,188, 209,231,235, Sedimentum, 182, Sedimen klasik, 183,184, Suspended load, 187, Saltation load, 188, Skala Wenworth, 189, Skala geologi, 256, Sedimen pelagik laut dalam, 191,192,228, Siliceous ooze, 193,207,210, Sebaran sedimen di laut, 193,196,198, Sedimen biogenic pelagis, 194, Sedimen terigen pelagik, 195, Skeletal, 254, Silaffin, 263, T ~ 366 ~ Thermodinamika, 3,85,87,89,96,100, 101,103, 111, Trench, 27, 171,172, Troposfer, 28, 29,43,60,64,69,70,83, Tropopause, 28,61, Termopause, 28, Termosfer, 30, Trace element, 39, 46,54,75,187, 206,207,217, Titanium, 39, Thallium, 39, Tellurium, 39,296, Topografi, 46, Termo, 84, Thermal equilibrium, 87, Tekanan, 89,98, 110,124, Tekanan parsial, 147,158,160, Termal, 97, Temperatur, 102,118,138, Tipologi Samudera, 168, Telodiagenesis,181, Tortuosity, 238, U UNCLOS, 8, Unsur utama, 23, Unsur kimia di Atmosfer, 43, Unsur kimia di bebatuan, 56,81, Unsur kimia, di tanah, 56, Unsur kimia terlarut di sungai, 56, Uap air laut, 69, Unsur kimia minor di dasar samudera, 81, Ukuran intensif, 94, Ukuran ekstensif, 94, Upwelling, 164,177, V Van’t Hoff, 5,115, Vulkanik, 44,71, 77,78,82, 137, Viskositas, 82, Vertikal, 235, W Weathering, 200, Z. Zona kedalaman laut, 24, Zona litoral, 25 Zona neritik, 25, Zona batial, 25, Zona abisal, 25, Zona diagenetik Mn, 247, Zat utama di sungai, 47, Zona reduksi, 249, ~ 367 ~