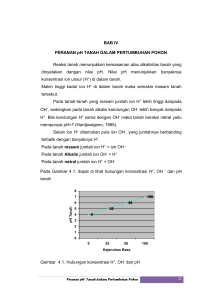
akifer dan berbagai parameter hidroliknya
advertisement

Week 9 AKIFER DAN BERBAGAI PARAMETER HIDROLIKNYA Reference: 1.Geological structures materials 2.Weight & Sonderegger, 2007, Manual of Applied Field Hydrogeology, McGraw-Hill online books 3.Mandel & Shiftan, 1981, Groundwater Resources: Investigation and Development, Academic Press PROPERTI FISIK DAN KIMIA AIRTANAH PROPERTI FISIKA AIRTANAH • Airtanah cenderung untuk mencapai kesetimbangan kimia-fisika dan hal ini akan dicapai setelah terjadi proses-proses di dalam airtanah yang berlangsung dari waktu ke waktu. • Properti Kimia/Fisika airtanah yang dapat dikenali di lapangan antara lain : Temperatur (oC), Derajat Keasaman (pH), Potensial Redoks (Eh) dan Daya Hantar Listrik (DHL). TEMPERATUR (OC) • Temperatur airtanah pada tempat dan waktu tertentu merupakan hasil dari bermacam proses pemanasan yang terjadi di bawah dan/atau di permukaan bumi (Matthess, 1982) • Dari perbandingan antara temperatur air pada tubuh air dengan temperatur rata‑rata udara lokal saat pengukuran akan diketahui adanya zonasi hipertermal, mesotermal, dan hipotermal. TEMPERATUR ( C) O • Zonasi Hipertermal : Zona dimana temperatur air pada tubuh air tersebut lebih tinggi dari temperatur rata-rata udara lokal. • Zonasi Mesotermal : Zona dimana temperatur air pada tubuh air sama dengan temperatur rata-rata udara lokal. • Zonasi Hipotermal : Zona dimana temperatur air pada tubuh air lebih rendah dari temperatur rata-rata udara lokal. Grafik Zonasi Temperatur Mataair pH • Karena kadar ion H+ sangat kecil, maka nilai konsentrasinya ditampilkan dalam bentuk pH yang mewakili nilai ‑log 9 konsentrasi ion hidrogen • Pada temperatur 25 oC keaktifan ion H+ dan ion OH- pada air adalah 9‑4, sehingga dengan asumsi konsentrasi H+ = OH- (1 X 9-7 mol/liter) maka nilai pH air murni = 7. • Faktor utama penentu keaktifan ion adalah jumlah reaksi kimia yang melibatkan ion hidrogen. pH • Reaksi kimia akan meningkat seiring dengan perubahan temperatur air. Perubahan temperatur menyebabkan pH air berubah dan perubahan pH air tersebut bergantung pada jenis endapan akifernya. • Metode paling sederhana untuk mengetahui nilai pH adalah menggunakan kertas indikator pH dengan kesalahan ± 0,9 unit. pH • Air yang bersifat asam (pH < 7) terdapat pada daerah‑daerah dengan endapan vulkanik, sedangkan air yang bersifat basa (pH > 7) terdapat pada daerah‑daerah dengan batuan Ultramafik (Hem, 1985). • Reaksi antara air dengan batuan ultramafik membentuk serpentinit. Reaksi ini mengikat ion H+ lebih besar daripada konsentrasi yang ada dalam sistem. Sedangkan pada kasus air panas, pH lebih rendah karena konsentrasi ion H+ yang di dalam sistem lebih besar dari yang diikat. POTENSIAL REDOKS (Eh) • Potensial redoks adalah ukuran kecenderungan (agresivitas) air untuk mengoksidasi atau mereduksi unsur yang terlarut dalam larutan. • Di dalam reaksi kimia hal ini terlihat dalam jumlah elektron yang dilepas dan elektron yang diikat. • Potensial redoks dinyatakan dalam satuan milivolt (mV). Besarnya Eh dapat diukur dan perbedaan potensial antara elektroda logam inert yang terbuat dari emas atau platinum dengan sebuah elektroda lain yang mempunyai nilai potensial konstan. POTENSIAL REDOKS (Eh) • Nilai potensial hidrogen dianggap sebagai nilai nol (baseline), sehingga jika nilai Eh air lebih besar dari nilai Eh hidrogen, maka potensial redoksnya positif. • Potensial redoks yang positif menunjukkan kondisi oksidasi, sedangkan nilai negatif menunjukkan kondisi reduksi. Diagram Eh – pH (Fetter, 1982) DAYA HANTAR LISTRIK (DHL) • Daya hantar listrik (spesific conductivity/konduktivitas) adalah ukuran kemampuan suatu zat menghantarkan arus listrik dalam temperatur tertentu yang dinyatakan dalam micromohs per centimeter oC. • Satuan yang lebih umum digunakan adalah mikroSiemens (S). Untuk menghantarkan arus listrik, ion‑ion bergerak dalam larutan memindahkan muatan listriknya (ionic mobility) yang bergantung pada ukuran dan interaksi antar ion dalam larutan. DAYA HANTAR LISTRIK (DHL) • Nilai daya hantar listrik untuk berbagai jenis air adalah sebagai berikut (Mandel, 1981) : - Air destilasi (aquades) : 0,5 – 50 S - Air hujan : 5,0 – 30 S - Airtanah segar : 30 – 2.000 S - Air laut : 45.000 – 55.000 S - Air garam (Brine) : > 90.000 S • Nilai konduktivitas merupakan fungsi antara temperatur, jenis ion‑ion terlarut, dan konsentrasi ion terlarut. Peningkatan ion‑ion yang terlarut menyebabkan nilai konduktivitas air juga meningkat. Sehingga dapat dikatakan nilai konduktivitas yang terukur merefleksikan konsentrasi ion yang terlarut pada air. PROPERTI KIMIA AIRTANAH • Unsur‑unsur kimiawi yang terkandung dalam airtanah dapat dibagi menjadi unsur mayor, unsur minor, dan unsur jarang. • Unsur utama (unsur mayor) terdiri dari ion‑ion Mg+, Ca2+, Na+, K+, Cl-, SO42-, dan HCO3-. Unsur utama ini selalu digunakan dalam penyajian data kimia airtanah, sedangkan unsur minor dan unsur jarang tidak selalu digunakan dan tergantung kepada aspek PROPERTI KIMIA AIRTANAH Penyajian Data Kimia Sampel Airtanah : • Penyajian Secara Numerik • Penyajian Secara Grafis Penyajian Secara Numerik • Data disiapkan dalam bentuk tabel dan dengan satuan konsentrasi mg/l. • Untuk mengetahui perbandingan jumlah masing‑masing ion dalam larutan, maka satuan mg/l dikonversi ke dalam satuan meq/l. • Konversi satuan dilakukan dengan membagi konsentrasi ion dalam mg/l dengan konsentrasi ion. Penyajian Secara Numerik • Konsentrasi ion dapat diketahui dengan membagi berat atom atau berat molekul dengan valensi ion. Prosedur perhitungan tersebut dapat dilihat dalam contoh berikut : a. Konversi 57 mg Ca/l ke dalam meq/l. Berat atom Ca = 40,08. Valensi +2. Jumlah ekivalen: 40,08 / 2 = 20,04 , maka : Ca = 57/20,04 = 2,84 meq/l. b. Konversi 154 mg HCO3-/l ke dalam meq/l - Berat atom H ~ 1,00 - Berat atom C ‑ 12,011 - Berat atom 0 ‑ 15,9994 - Berat molekul HC03 = 61,017 - valensi = 1 - Jumlah ekivalen = 61,017 - Maka HCO3- = 154/61,017 = 2,52 meq/l Penyajian Secara Numerik • Nilai Konversi untuk beberapa kation/anion yang penting : Na+ 22,9898 Fe2+ 27,9235 NO3- 62,005 K+ 39,92 Mn2+ 27,469 SO42- 48,031 Ca2+ 20,04 CO32- 30,005 Cl- 35,453 Mg2+ 12,156 HCO3- 61,017 Penyajian Secara Grafis • Pictorial Diagram a. Diagram Grafik Batang b. Diagram Lingkar/Radial • Multivarian Diagram a. Trilinier Diagram (Diagram Piper) b. Horizontal Diagram (Diagram Stiff dan Diagram Schoeller) Pictorial Diagram (Diagram Grafik Batang) Pictorial Diagram (Diagram Lingkar/Radial) Multivarian Diagram (Diagram Piper) Multivarian Diagram (Diagram Stiff) Multivarian Diagram (Diagram Schoeller TERIMA KASIH