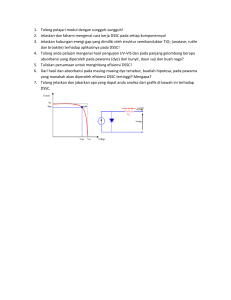
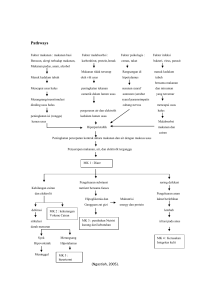
Pengaruh Penggunaan Elektrolit Gel Terhadap Arus
advertisement

JURNAL SAINS DAN SENI POMITS Vol. 3, No. 1, (2013) 1-6 1 Pengaruh Penggunaan Elektrolit Gel Terhadap Arus dan Tegangan DSSC Prototipe DSSC Ekstrak Kulit Manggis (Garcinia Mangostana L.) Sebagai Dye Sensitizer Iftihatur Rofi’ah, Gontjang Prajitno Jurusan Fisika, Fakultas IPA Institut Teknologi Sepuluh Nopember Jl. Arief Rahman Hakim, Surabaya 60111 E-mail:[email protected] Abstrak—Telah dilakukan fabrikasi DSSC dengan menggunakan dye kulit buah mannggis (Garcinia Mangostana L) dengan variasi elektrolit gel teknik pelapisan spin coating. Variasi elektrolit gel yang digunakan terdiri dari elektrolit A dan B. Elektrolit A dibuat dengan mencampurkan Kalium Iodide 3 gr dan 3 ml Iodine sebagai elektrolit cair, kemudian ditambahkan senyawa pembuat gel menggunakan 3 gr PEG 1000 yang dilarutkan kedalam 5 ml klorofom dan distirrer. Dibuat elektrolit B dengan komposisi berbeda dengan mencampurkan 3 gr KI kedalam 5 ml Iodine, kemudian dicampurkan senyawa pembuat gel menggunakan 6 ml PEG 1000 yang dilarutkan dalam 6 ml klorofom. Berdasarkan hasil pengujian menggunakan sumber cahaya lampu halogen. Diperoleh bahwa arus dan tegangan yang dihasilkan elektrolit gel cukup stabil. Arus tertinggi yang dihasilkan DSSC dengan elektrolit A sebesar 12,8 μA sedangkan pada DSSC dengan elektrolit B sebesar 21,4 μA. Pada penelitian ini jika semakin banyak Iodine yang digunakan maka arus yang dihasilkan semakin tinggi. Kata Kunci—DSSC, TiO 2 , Dye Ekstrak Kulit Manggis, Elektrolit Gel, Spin Coating. I. PENDAHULUAN el surya dalam perkembangannya telah banyak inovasi. Berdasarkan perkembangan teknologi saat ini dan bahan pembuatannya sel surya dibedakan menjadi dua yaitu pertama, sel surya konvensional yang berbasis silikon. Kedua, advance sel surya yang terbagi atas tiga macam yaitu Thin Film material, Multi junction (Tanden), Dye sensitized Solar Cell (DSSC). Diantara beberapa jenis sel surya tersebut yang mudah untuk difabrikasi dan membutuhkan biaya yang murah adala sel surya jenis DSSC. DSSC sebagai sel surya dengan dye sensitizer dari bahan organik dapat dikembangkan berbiaya murah serta fabrikasi mudah. Pada penelitian sebelumnya oleh Zamroni[1], fabrikasi DSSC masih menggunakan bahan semikonduktor TiO 2 yang berukuran mikro sebagai fotokatalisnya, dan menggunakan dye sensitizer kulit manggis dengan metode pelapisan TiO 2 pada kaca ITO yaitu metode Doctor Blade sehingga diperoleh nilai tegangan DSSC yang besar namun kestabilannya kurang. Penelitian Hidayat[2], mengunakan dye kulit manggis, bahan TiO 2 mikro dengan metode pelapisan Spin Coating dan membandingkan sel yang diberi spacer dan tidak diberi spacer. Hasil dari penelitian ini menunjukkan bahwa DSSC dengan spacer tegangan dan arus yang dihasilkan lebih stabil. Penelitian Romli[3], menggunakan dye yang sama dan metode yang sama dengan penelitian hidayat namun dibuat variasi kecepatan putar Spin Coating, hasilnya menunjukkan efisiensi yang lebih bagus. S Berdasarkan referensi di atas, masih perlu inovasi untuk mendapatkan optimalisasi dari fabrikasi DSSC. Maka dari itu diperlukan adanya penelitian yang lebih lanjut agar diperoleh efisiensi DSSC yang tinggi dan menghasilkan daya yang lebih besar. Pada penelitian ini akan digunakan metode Spin Coating untuk pelapisan TiO 2 . Bahan TiO 2 yang digunakan masih berukuran mikro dan berfasa anatase, bahan dye yang digunakan yaitu ekstrak kulit terluar buah manggis. Penelitian ini bertujuan untuk mengetahui bagaimana pengaruh elektrolit gel terhadap tegangan dan arus yang dihasilkan. Pada dasarnya prinsip kerja DSSC mengkonversi energi cahaya ke listrik dalam skala molekular dalam bentuk reaksi dari transfer elektron. Proses pertama dimulai dengan terjadinya eksitasi elektron pada dye akibat absorbsi foton. Dimana ini merupakan salah satu peran dari sifat TiO 2 . Ketika foton dari sinar matahari menimpa elektroda kerja pada DSSC, energi foton tersebut diserap oleh dye yang melekat pada permukaan TiO 2 . Sehingga dye mendapatkan energi untuk tereksitasi. Dye tereksitasi membawa energi dan diinjeksikan ke pita konduksi pada TiO 2 . TiO 2 berperan sebagai akseptor atau kolektor elektron. Molekul dye yang ditinggalkan kemudian dalam keadaan teroksidasi. Selanjutkan elektron akan ditransfer melewati rangkaian luar menuju elektroda pembanding ( elektroda yang mengandung lapisan karbon). Elektrolit (pasangan iodide dan triodide) yang bertindak sebagai mediator elektron sehingga dapat menghasilkan proses siklus dalam sel. Ion Triodide menangkap elektron yang berasal dari rangakaian luar dengan bantuan molekul karbon sebagai katalis. Elektron yang tereksitasi masuk kembali ke dalam sel dan dibantu oleh karbon sehingga dapat bereaksi dengan elektrolit yang menyebabkan penambahan ion iodide pada elektron. Kemudian satu ion iodide pada elektrolit mengantarkan elektron yang membawa energi menuju dye teroksidasi. Elektrolit menyediakan elektron pengganti untuk molekul dye teroksidasi. Sehingga dye kembali ke keadaan awal[2]. Secara umum, Gambar 1 menunjukan DSSC terdiri dari dye-sensitized yang terbuat dari bahan organik, lapisan TiO 2 nanokristal, larutan elektrolit yang mengandung pasangan redoks I-/I3- dan substrat kaca ITO sebagai elektoda kerja. Faktor luar area dan ketebalan lapisan semikonduktor yang mengatur peningkatan beban dye, kemudian kerapatan optis yang menghasilkan efisiensi penyerapan cahaya. Kerapatan optis menyatakan ukuran transmisi suatu elemen optik dengan panjang gelombang tertentu. Jika dihubungkan dengan pemberian radiasi pada suatu objek, maka kerapatan optisnya merupakan perbandingan antara intensitas awal dan intensitas transmisi. JURNAL SAINS DAN SENI POMITS Vol. 3, No. 1, (2013) 1-6 2 II. METODOLOGI Gambar 1 Skema DSSC DSSC berbentuk struktur sandwich, dimana dua elektroda yaitu elektroda TiO 2 dengan dye dan elektroda pembanding yang terbuat dari kaca ITO dilapisi karbon yang mengapit elektrolit membentuk sistem sel fotoelektrokimia. Elektroda pembanding terbuat dari kaca ITO yang dilapisi dengan karbon karena memiliki konduktivitas yang cukup dan resistansi panas dan aktivitas elektrokatalitik dari reduksi triiodide. TiO 2 adalah material fotokatalis yang memiliki daya oksidasi yang kuat, photostabilitas yang tinggi dan selektivitas redoks. Syarat penting untuk meningkatkan aktivitas katalis dari TiO 2 adalah meningkatkan luas permukaan dari TiO 2 yang bergantung pada ukuran kristalnya. Sifat fisis dan kimia dari TiO 2 bergantung pada ukuran, morfologi dan struktur kristalnya. TiO 2 memiliki tiga bentuk kristal yaitu anatase, rutile, dan brookite. Kristal TiO 2 fase anatase memiliki kemampuan yang lebih aktif daripada rutile. Anatase dianggap sebagai fase yang paling menguntungkan untuk fotokatalisis dan konversi solar energi. TiO 2 hanya mampu menyerap sinar ultraviolet (350-380 nm). Untuk meningkatkan serapan spektra TiO 2 di daerah tampak, dibutuhkan lapisan zat warna yang akan menyerap cahaya tampak. Zat warna tersebut berfungsi sebagai sensitizer. Buah manggis merupakan buah yang mempunyai banyak keunggulan dibandingkan buah lainnya. Bagian kulit buah manggis dapat dimanfaatkan sebagai penghasil zat warna alami yang dapat digunakan sebagai pewarna makanan, juga dapat dimanfaatkan sebagai antioksidan, antidiare dan antikanker. Pemanfaatan kulit buah manggis belum maksimal. Penampilan kulit buah manggis yang berwarna ungu menunjukkan ada pewarna alami yang terkandung didalamnya. Salah satu senyawa flavonoid yang terkandung dalam kulit buah manggis adalah antosianin[3]. Antosianin merupakan zat warna yang paling penting dan tersebar luas, pigmen memberikan warna pada tumbuhan tinggi dan mudah larut dalam air[4]. Pigmen ini berperan terhadap timbulnya warna pada bunga, daun, dan buah. Antosianin bersifat polar sehingga dapat dilarutkan pada pelarut polar seperti etanol, aseton, dan air. Berdasarkan tingkat polaritasnya antara antosiansin sebagai zat terlarut dan air sebagai pelarut tidak seimbang. Ekstraksi adalah kegiatan penarikan kandungan kimia yang dapat larut sehingga terpisah dari bahan yang tidak dapat larut dalam pelarut cair. Diketahuianya senyawa aktif yang dikandung oleh suatu bahan (simplisia) akan mempermudah pemilihan pelarut dan metode ekstraksi yang tepat[5]. A. Preparasi Elektroda Kerja Elektroda kerja terbuat dari kaca konduktif jenis FTO yang dilapisi dengan pasta TiO 2 . Cara membuat pasta TiO 2 yaitu dengan mencampurkan serbuk TiO 2 mikro sebanyak 4 gr dilarutkan dalam 15 ml Asam asetat, distirrer selama 30 menit. Kemudian ditambahkan 10 tetes Triton X-100 dan distirrer kembali selama 1 jam. Pasta TiO 2 yang sudah jadi dideposisikan pada kaca konduktif FTO dengan metode Spin Coating. Kecepatan putar Spin Coating 1000, 1500 dan 2000 masing-masing selama 40 menit. Agar didapatkan hasil deposisi yang baik maka hasil spin coating dikalsinasi pada temperatur 450ºC selama 30 menit dan didinginkan pada suhu 70 ºC agar pada pencelupan dye dapat menempel pada TiO 2. . B. Preparasi Dye Kulit Manggis sebagai fotosensitizer Pewarna yang digunakan dalam penelitian ini adalah ekstrak kulit manggis. Kulit manggis diekstrak dengan membuat bubuk dari kulit manggis yang telah dikeringkan, kemudian bubuk tersebut dilarutkan dengan menggunakan air. Dibuat 5 gr kulit manggis dan dilarutkan dalam 100 ml air. Untuk menguji daya serap dari ekstrak Jahe Merah yaitu dengan menggunakan UV-VIS spektrofotometer. C. Preparasi Larutan Elektrolit Larutan elektrolit yang akan digunakan dalam penelitian ini adalah pasangan redoks iodin dan Iodide (I-/I3-) dan akan ibuat gel dengan penambahan beberapa senyawa. Senyawa dalam pembuatan larutan elektrolit ini adalah Kalium Iodida (KI), Iodine, PEG 1000 dan Klorofom. Dibuat dua macam elektrolit gel dengan komposisi yang berbeda untuk melihat karakteristik dari masing-masing elektrolit. Prosedur awal pembuatan larutan elektrolit ini adalah untuk elektrolit A dibuat dengan mencampurkan 3gram Kalium Iodide ke dalam 3 ml Iodine dan distrirrer selama 15 menit. Kemudian disiapkan senyawa pembuat gelnya yaitu PEG 1000 sebanyak 3 gr dilarutkan dalam 5 ml klorofom, larutan tersebut kemudian dicampurkan apada elektrolit cair dan distirrer selama satu jam. Kemudian disimpan dalam wadah tertutup untuk menghindari penguapan. Elektrolit B dibuat dengan komposisi yang berbeda dari elektrolit A. elektrolit B dibuat dengan mencampurkan 3 gr KI kedalam 5 ml Iodine dan distirrer selama 15 menit dan merupakan elektrolit cair. Sedangkan senyawa pembuat gelnya dibuat dengan melarutkan 6 gr PEG 1000 kedalam 6 ml kloroform. Setelah itu dicampurkan pada larutan elektrolit cair dan distirrer selam 1 jam. D. Pembuatan Elektroda Pembanding Elektroda pembanding dibuat dengan kaca FTO yang dilapisi karbon. Pelapisan karbon pada kaca FTO yaitu dengan menggores-goreskan Pensil 8B pada bagian konduktif kaca FTO kemudian dipanaskan di atas nyali api lilin hingga terbentuk lapisan berwarna hitam seperti gambar 3. E. Pembuatan Sandwich DSSC Setelah masing-masing komponen DSSC tersebut siap langkah berikutnya adalah menyusun sandwich DSSC,berikut adalah prosesnya: JURNAL SAINS DAN SENI POMITS Vol. 3, No. 1, (2013) 1-6 1. Elektroda kerja yang telah disiapkan, direndam dalam larutan dye selama 1 hari agar dye dapat emenempel pada lapisan TiO 2 . 2. Disiapkan spacer dari selotip plastik dengan ukuran 2 mm dan disesuaikan dengan luasan elektroda TiO 2 yang tidak dilapisi pasta. 3. Kemudian larutan elektrolit dioleskan tepat di atas lapisan TiO 2 . Setelah itu diletakkan elektroda pembanding diatas substrat TiO 2 yang telah diberi spacer tadi, elektroda pembanding dipasang tidak sejajar untuk memudahkan pada saat pengujian. Setelah itu klip kertas dipasang untuk menguatkan kedua elektroda tersebut. 3 gelombang 330, 390, 460 dan 510 nm. Sinar matahari menghasilkan 5% spektra di daerah ultraviolet dan 45% di daerah cahaya tampak(380-780 nm). Dengan kemampuan absorbansi pada rentang panjang gelombang 280-520 maka kulit manggis memungkinkan untuk menyerap energi sinar matahari sehingga memaksimalakan daya kerja DSSC. F. Pengujian DSSC Pengujian DSSC meliputi tegangan dan arus, dilakukan di dalam ruangan dengan menggunakan cahaya lampu Halogen. Dan diguunakan voltmeter untuk menguukur arus dan tegangan serta rangkaian sebagai beban. Gambar 2 Absorbansi Kulit Manggis Gambar 1 Rangkaian Pengujian arus dan tegangan untuk DSSC III.HASIL DAN PEMBAHASAN G. Hasil Uji Spektrofotometer UV Vis pada Dye Kulit Manggis Semikonduktor TiO 2 hanya mampu menyerap sinar ultraviolet dengan panjang gelombang (350-380 nm). Untuk meningkatkan serapan spektra TiO 2 didaerah tampak, dibutuhkan zat warna yang akan menyerap cahaya tampak, Manggis adalah salah satu buah yang memiliki kandungan zat warna (antosianin). Dalam 100 gram kulit buah manggis terdapat 59,3 mg antosianin. Jika daya serapan dye kulit manggis tinggi maka kemampuan mengabsorb foton yang dipancarkan oleh sinar matahari juga besar sehingga mampu mengeksitasi elektron-elektron yang terdapat pada bahan semikonduktor yaitu TiO 2 dari pita konduksi dan arus yang dihasilkan cukup besar. Untuk mengetahui daya serap dye kulit manggis maka dilakukan uji UV-Vis. Alat yang digunakan untuk uji UV-Vis adalah spektrofotometrer UV-Vis. Prinsip kerja spektrofotometri UVVis yaitu interaksi yang terjadi antara energi yang berupa sinar monokromatis dari sumber sinar dengan materi yang berupa molekul. Besar energi yang diserap tertentu dan menyebabkan elektron tereksitasi dari keadaan dasar ke keadaaan tereksitasi yang memiliki energi lebih tinggi dari energi gap TiO 2 . Cahaya tampak berada pada panjang gelombang antara 380-780 nm, panjang gelombang tersebut divisualisasikan dengan beberapa macam spektrum warna. Dari hasil uji UV-Vis pada gambar 2 dye kulit manggis mengabsorb pada panjang gelombang cahaya dengan rentang antara 280-520 nm. Nilai absorbansi maksimum kulit manggis 5, sedangkan puncak absorbansi terjadi pada panjang H. Analisis Elektrolit Gel Pada penelitian-penelitian sebelumnya digunakan elektrolit cair sebagai media transfer elektron. Ketahanan arus dan tegangan yang diperoleh hanya bertahan dalam jangka waktu tertentu dan harus dilakukan penetesan ulang jika akan dilakukan pengujian lagi. Oleh karena itu penelitian kali ini elektrolit yang digunakan dibuat gel agar dalam penggunaannya DSSC mampu bertahan dalam jangka waktu yang lama tanpa fabrikasi ulang. Larutan elektrolit yang akan digunakan dalam penelitian ini adalah pasangan redoks iodin dan Iodide (I-/I3-) dibuat dengan dua macam variasi. Elektrolit A dibuat dengan mencampurkan 3 gram Kalium Iodide (KI) ke dalam 3 ml iodine dan distirrer selama 1 jam. Larutan yang sudah dibuat selanjutnya disimpan pada wadah/botol yang tertutup rapat (menghindari penguapan larutan). Disiapkan PEG 1000 sebanyak 3 gr dilarutkan kedalam 5 ml kloroform kemudian dicampurkan kedalam larutan elektrolit yang sebelumnya sudah dibuat dan distrirrer selama 1 jam dengan temperatur pemanasan 60ºC agar PEG 1000 cepat larut kedalam larutan tersebut. Untuk elektrolit B dibuat dengan komposisi berbeda dari elektrolit A, pada elektrolit B ini dibuat dengan mencampurkan 3 gr KI kedalam 5 ml Iodine, sebagai pembuat gelnya dicampurkan 6 gr PEG 1000 kedalam 6 ml kloroform dan dicampurkan kedalam larutan elektrolit yang sudah dibuat sebelumnya, distrirrer dengan waktu dan temperatur yang sama seperti elektrolit A. Digunakan polimer PEG sebagai senyawa pembuat gel. PEG disini dianalogikan hanya sebagai template dari elektrolit agar tidak mudah menguap sehingga arus dan tegangang yang dihasilkan stabil, jadi PEG tidak megikat senyawa-senyawa JURNAL SAINS DAN SENI POMITS Vol. 3, No. 1, (2013) 1-6 lain dari komposisi elektrolit. Dalam penggunaannya, PEG sering digunakan untuk sebagai campuran kosmetik maupun obat-obatan. Jenis PEG sendiri bervariasi sesuai dengan berat molekulnya. Untuk penelitian kali ini digunakan PEG 1000 yang berbentuk kristalin putih dan berminyak, dengan bentuk tersebut PEG perlu dilarutkan ke dalam senyawa lain agar mudah untuk dicampurkan pada pasangan larutan KI dan I. Pelarut yang digunakan adalah senyawa kloroform, dipilih senyawa tersebut karena sifat dari kloroform biasanya sangat baik digunakan sebagai pelarut organik, dan juga non polar, sebagai pelarut minyak dan lemak. Dari sifat-sifat tersebut maka dipilhlah kloroform sebagai pelarut PEG. Dari sintesis elektrolit yang dilakukan dapat disimpulkan bahwa pada penelitian kali ini berat molekul PEG yang digunakan untuk membuat gel mempunyai berat molekul minimal sebesar 1000 agar elektrolit dapat berubah menjadi gel dengan struktur yang lebih kental. Semakin banyak Iodine yang digunakan maka senyawa pembuat gelnya juga semakin banyak agar elektrolit dapat terbentuk gel. I. Pengujian DSSC Pengujian DSSC dilakukan di laboratorium optoelektronika fisika ITS Surabaya. Pengujian DSSC dilakukan dibawah sinar lampu halogen dengan jarak 3 cm dan intensitasnya 86400 lumen/m2. Permukaan sisi elektroda kerja TiO 2 berada dibagian yang disinari oleh halogen, data yang akan diambil adalah arus dan tegangan pada hambatan minimum sekitar 18 Ω dan hambatan maksimum 413 KΩ. Digunakan dua macam variasi elektrolit gel dengan 2 sampel DSSC yang berbeda. Pengujian dilakukan dengan menggunakan peralatan resistor jenis potensio Ω100 k sebanyak 4 buah yang dirangkai paralel, kabel penjepit buaya, PCB yang nantinya dibuat rangkaian sebagai beban pada DSSC, seperti yang terlihat pada gambar 3, multimeter 2 buah yang berfungsi untuk mengukur arus dan tegangan yang dihasilkan. Gambar 3 Proses Pengujian DSSC Pada pengujian DSSC, jika hambatan rangkaian yang dihasilkan potensiometer minimum maka akan timbul arus besar yang diperoleh dari DSSC, sesuai dengan hukum ohm yaitu tegangan diperoleh dari hasil perkalian arus dan hambatan, dari sini dapat diketahui bahwa hubungan antara hambatan dan tegangan adalah berbanding lurus, sedangkan arus sendiri merupakan hasil bagi antara tegangan dan 4 hambatan oleh karena itu jika hambatan yang diberikan minimum maka akan diperoleh arus yang besar. sedangkan jika hambatan yang diberikan pada rangkaian maksimum maka arus tidak terbaca, faktor tersebut dikarenakan arus yang dihasilkan sangat kecil sehingga alat ukur yang digunakan tidak mampu membaca besarnya arus yang dihasilkan. Untuk pengujian pada hambatan maksimum yaitu 413 KΩ akan terukur tegangan yang dihasilkan oleh DSSC, pada saat ini alat ukur berada pada rangkaian paralel dengan DSSC itu sendiri sehingga akan menghasilkan tegangan yang besar. J. Pengujian Arus yang Dihasilkan Oleh DSSC Ketika cahaya berupa foton yang berasal dari halogen menumbuk elektroda kerja, terjadi eksitasi elektron yang berasal dari dye akibat absorbsi foton. Elektron tereksitasi dari ground state ke excited state kemudian terinjeksi menuju band gap TiO 2 sehingga molekul dye teroksidasi. Dengan adanya donor elektron dari elektrolit (I-) maka molekul dye kembali ke keadaan awal dan mencegah penangkapan kembali elektron oleh dye teroksidasi. Setelah mencapai elektroda kerja elektron mengalir menuju elektroda karbon melalui rangkaian eksternal. Dengan adanya katalis pada elektroda karbon yaitu karbon itu sendiri, elektron diterima oleh elektrolit sehingga hole yang terbentuk pada elektrolit (I 3 -), akibat donor elektron pada proses sebelumnya berekombinasi dengan elektron sebelumnya membentuk Iodide (I-). Iodide ini digunakan untuk mendonor elektron kepada dye yang teroksidasi sehingga terbentuk siklus transport elektron dan menghasilkan arus. Arus yang dihasilkan oleh elektrolit gel ini berupa arus stabil, hal tersebut dapat dilihat pada gambar 4, gambar tersebut menunjukkan grafik yang dihasilkan oleh elektrolit A pada pengukuran dengan resistansi rangkaian sebesar 18Ω dan resistansi kaca sebesar 50K Ω. Pengambilan data dilakukan tiap menit untuk mengamati perubahan arus. Diperlihatkan bahwa kestabilan arus membutuhkan waktu sekitar 40 menit dari waktu awal pengukuran. Arus awal didapatkan 12,8 μA, perubahan saat menuju stabil dalam tiap menitnya mengalami penurunan drastis, hingga pada menit ke-40 arus menunjukkan perubahan yang stabil seiring berjalannya waktu. Pada penelitian ini arus yang dihasilkan tidak pernah nol, terbukti pada pengukuran setelah 2 jam arus stabil sekitar 4,2 μA sehingga dapat dipastikan arus tidak pernah hilang karena elektrolit yang digunakan tidak mudah menguap, sehingga proses siklus DSSC masih tetap berjalan untuk menghasilkan JURNAL SAINS DAN SENI POMITS Vol. 3, No. 1, (2013) 1-6 5 arus. 14 25 12 20 10 I(μA) Elktrolit A Arus (μA) Arus (μA) 15 8 I(μA) Elektrolit B 10 6 4 5 2 0 0 0 20 40 60 80 100 120 140 160 180 200 Waktu (menit) Gambar 4 Grafik hubungan Arus terhadap Waktu DSSC dengan elektrolit gel A pada hambatan 18 Ω dan resistansi kaca 50KΩ dengan waktu pengujian 2 jam Sampel berikutnya adalah sel DSSC dengan menggunakan elektrolit B. Pada pengujiannya dilakukan sama seperti sampel pada elektrolit A namun resistansi kaca konduktif pada sampel B ini lebih besar dari sampel A yaitu sekitar 380K Ω. Terlihat dari gambar 5 bahwa arus yang dihasilkan pun masih kecil. Arus ini mencapai keadaan stabil dalam waktu sekitar 50 menit. Berbeda dengan sampel A, pada sampel B didapatkan arus tertinggi 21,4 μA. Akan tetapi tegangan yang dihasilkan lebih kecil dari sampel DSSC elektrolit A. 25 20 Arus (μA) 15 10 5 0 0 50 100 150 Waktu (menit) Gambar 4.5 Grafik hubungan Arus terhadap Waktu DSSC dengan elektrolit B pada hambatan 18Ω dan resistansi kaca 380 KΩ dengan waktu pengukuran 2 jam 0 20 40 60 80 100 120 140 Waktu (menit) Gambar 6 Grafik perbandingan Arus pada DSSC elektrolit A dan B terhadap waktu pada hambatan 18Ω Dari sini dapat kita bandingkan kedua sampel tersebut. Dari grafik 6 diperlihatkan bahwa arus yang dihasilkan oleh elekrolit B lebih besar dari elektrolit A. Penggunaan Iodine sangat berpengaruh terhadap arus yang dihasilkan, pada penelitian ini semakin banyak Iodine yang digunakan maka arus yang dihasilkan semakin tinggi akan tetapi dalam kasus lain penggunaan Iodine yang terlalu banyak dapat mengurangi daya yang dihasilkan oleh DSSC. Selain itu kestabilan yang dihasilkan pun berbeda, semakin banyak kandungan Iodine maka waktu yang dibutuhkan menuju stabil pun semakin lama, karena pada penelitian ini stabil pada arus kecil. Jadi jika arus yang dihasilkan tinggi maka proses menuju stabil pun lama. Pada DSSC dengan elektrolit A pada menit ke-40 arus sudah mulai stabil. sedangkan pada DSSC dengan elektrolit B arus mulai stabil pada menit ke-60. K. Pengujian Tegangan yang dihasilkan DSSC Pengukuran tegangan dilakukan pada hambatan maksimum yang dihasilkan oleh potensiometer yaitu sekitar 413 Ω, K pada hambatan ini arus tidak terbaca dikarenakan alat ukur yang digunakan tidak mampu membaca arus yang sangat kecil. Berbeda dengan tegangan, hambatan berbanding lurus dengan tegangan sehingga jika hambatannya besar maka tegangan yang dihasilkan pun cukup besar. Tegangan yang dihasilkan DSSC berasal dari beda potensial antar energi fermi TiO 2 dengan potensial reduksi elektrolit. Jika ukuran partikel TiO 2 lebih kecil maka energi ferminya lebih besar sehingga tegangan yang dihasilkan juga lebih besar. JURNAL SAINS DAN SENI POMITS Vol. 3, No. 1, (2013) 1-6 300 6 tegangan dan arus tanpa fabrikasi lagi. Tegangan (mV) 250 DAFTAR PUSTAKA [1] 200 150 100 50 0 0 20 40 60 80 100 120 140 160 Waktu (menit) Gambar 4.7 Grafik hubungan Tegangan terhadap waktu DSSC dengan elektrolit A pada hambatan 413ΩK rsistansi kaca 50K Ω dengan waktu pengujian 2 jam Tegangan (mV) Pengukuran tegangan pada sampel B menunjukkan tegangan yang stabil pula. Pada sampel ini tegangan tidak lebih besar dari sampel A, hanya berkisar 102,1-147,9 mV. Perbedaan ini disebabkan oleh resistansi kaca yang digunakan. Untuk DSSC sampel resistansi kacanya sekitar 380 Ω. K Pengujian dilakukan selama 2 jam dan diamati tegangan yang dihasilkan setiap menitnya. Dapat dilihat dari gambar 4.8 bahwa tegangan yang dihasilkan awalnya mengalami kenaikan kemudian penurunan pada menit 10 dan mulai stabil pada menit ke 80. 160 140 120 100 80 60 40 20 0 0 20 40 60 80 100 120 140 160 Waktu (menit) Gambar 4.8 Grafik hubungan Tegangan terhadap Waktu DSSC dengan elektrolit B pada hambatan 413 ΩK resitansi kaca 380 KΩ dengan waktu pengukuran 2 jam IV. KESIMPULAN Telah berhasil dibuat sel surya tipe DSSC menggunakan variasi elektrolit gel dengan komposisi yang berbeda. Arus maksimum yang dihasilkan elektrolit A sebesar 12,8 μA sedangkan arus maksimum yang dihasilkan elektrolit B sebesar 21,4 μA. Dalam penggunaannya elektrolit gel mampu bertahan dalam jangka waktu yang lama untuk menghasilkan Zamroni, 2013, “Pembuatan dan Karakterisasi Prototipe Dye Sensitized Solar Cell (DSSC) Menggunakan Ekstraksi Kulit Buah Manggis Sebagai Dye Sensitizer Dengan Metode Ddoctor Blade”, Departemen FISIKA FMIPA, Institut Teknologi Sepuluh Nopember Surabaya, Surabaya. [2] Rahman, hidayat, 2013, “Pengaruh Pemberian Space (Bantalan) Untuk Mendapatkan Kestabilan Arus Dan Tegangan Prototipe Dssc Dengan Ekstraksi Kulit Buah Manggis (Garcinia Mangostana L.) Sebagai Dye Sensitizer”, Departemen FISIKA FMIPA, Institut Teknologi Sepuluh Nopember Surabaya, Surabaya. [3] Purwanto, Romli, 2013, “Variasi Kecepatan Putar Dan Waktu Pemutaran Spin Coating Dalam Pelapisan Tio 2 Untuk Pembuatan Dan Karakterisasi Prototipe Dssc Dengan Ekstraksi Kulit Buah Manggis (Garciniamangostana L.) Sebagai Dye Sensitizer”, Departemen FISIKA FMIPA, Institut Teknologi Sepuluh Nopember Surabaya, Surabaya. [4] Nasori, (2012), Pengembangan dan fabrikasi Dye Sensitized Solar Cell berbasis jahe Merah Dengan metode deposisi Spin Coating dan Docot Blade. Thesis, Jurusn Fisika Fakultas Matematika dan Ilmu Pengetahuan Alam, ITS Surabaya. [5] Durst, R. W., & Wrolstad, R. E., 2005. Unit F1.2: Characterization and Measurement of Anthocyanins by UV–visible Spectroscopy. In R. E. Wrolstad (Ed.), Handbook of analytical food chemistry (pp. 33– 45). NewYork: John Wiley & Sons. [6] Treyball, R.E., (1981), ―Mass-Transfer Operations‖, 3rd ed, Mc GrawHill, New York, hal. 717-723 [7] O’regan dan Gratzel, M.”A low –Cost, High Efficiency Solar Cell Based On Dye Sensitized Colloidal TiO 2 Films”. Nature Vol.353. Issue 6346, 737.1991 [8] http://www.chem-is-try.org/artikel kimia/kimia material/fotokatalis pada permukaan tio2/diakses 11 Januari 2013 [9] Sastrohamidjojo, H, 1991,Spektroskopi. Yogyakarta.: Liberty [10] H. Zhang, J.F. Banfield. “Understanding Polymorphic Phase Transformation Behavior during Growth of Nanocrystalline Aggregates: Insights from TiO2 “, J Phys Chem B, vol. 104, pp. 3481. 2000 [11] M. Hatta, Agus, dkk., 2005, Fabrikasi Devais Fotonik Berbasis Polimer PMMA dengan Metode Spin Coating, Jurnal Fisika dan aplikasinya, ITS Surabaya. [12] Spiro, M., Kandiah, M. and Price, W., (1990), ―Extraction of ginger rhizome: kinetic studies with dichloromethane, ethanol,2-propanol and acetone–water mixture‖, International Journal of Food Science and Technology, 25, hal. 157–167.