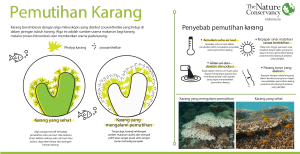
Pengaruhnya terhadap Komunitas Terumbu Karang Coral Bleaching
advertisement

Hayati, September 2001, hlm. 86-90 ISSN 0854-8587 Vol. 8, No.3 ULASAN Pemutihan Karang: Pengaruhnya terhadap Komunitas Terumbu Karang Coral Bleaching: Influences on the Coral Reef Communities CHAIR RANI lurusan Hmu Kelllutan, Fakultas Ilmu Kelllutan dan Perikanan, Universitas Hasanuddin lallln Perintis Kemerdekaan Km. 10 Tamalanrea, Makasar 90245, TeL +62-411-585189, E-mail: [email protected] Diterima 5 April 200lJDisetujui 26 Juli 2001 Coral reefs are among the most sensitive ecosystems to long-term climate change. In addition, between 50% and 70% of all corals reefs are directly threatened by human activities. One of the natural phenomena in coral reefs is bleaching, as a consequence of stress of climate changed (possibly due to the increase in temperature). Six major episodes of coral bleaching have occurred since 1979, with massive mortalities of coral affecting reefs in every part of the world. Entire reef systems have died following bleaching events. I would like to represent three important factors i.e. biological, physiological and ecological have significantly influenced the bleaching of coral reef communities. The biological influences were responsible in increasing coral mortality, decreasing of growth and calcification as well as reproduction capacity. The physiological influences involved decreasing photosynthesis and photosynthetic efficiency. The principal consequences of excess irradiance absorption are photoinhibitory damage to the photosystem n reaction center and generalized damage to membranes and proteins by singlet oxygen, superoxide and other free radicals. While, ecological influences include decreasing of coral reef condition, productivity and biodiversity, as well as the changes in communities structure. The reduced ability to grow and calcification may also translate into a reduced ability to compete space with other organisms. Terumbu karang adalah ekosistem laut yang paling spektakuler dan beragam di planet bumi. Terumbu karangjuga sangat kompleks dan produktif. Banyak spesiesnya sampai saat ini belum diketahui, diduga ada sekitar satu juta spesies, namun hanya sekitar 10% yang dapat digambarkan (ReakaKudla 1996). Terlepas dari hal tersebut di atas, terumbu karang diproyeksikan akan menjadi ekosistem yang lebih peka terhadap perubahan iklim dalam waktu yang panjang (IPCC 1988). Selain perubahan iklim, sekitar 50-70% terumbu karang juga secara potensial terancam oleh aktivitas manusia (Goreau 1992, Sebens 1994). Pemanfaatan dan pembangunan kawasan pesisir, praktik penangkapan ikan yang merusak, polusi laut, dan aliran air dari penggundulan hutan dan pertanian merupakan ancaman terbesar bagi terumbu karang. Fenomena alam lain yang berdampak besar terhadap" kondisi dan kerusakan terumbu karang ialah peristiwa """ pemutihan karang (coral bleaching). Pemutihan merupakan akibat dari cekaman (stress) sewaktu terjadi perubahan besar pada organisasi jaringan dan sitokimia dalam polip karang (Hayes & Goreau 1992). HasH akhir dari proses ini menyebabkan koloni karang menjadi putih, baik sebagian ataupun seluruh koloni. Beberapa contoh pemutihan terutama berhubungan dengan ;terdegradasinya pigmen-pigmen klorofil pada zooxantela yang disebabkan oleh pecahnya atau terjadinya foto-oksidasi klorofil (Asada & Takahashi 1987, Brown 1997). HasH pengamatan di Lautan PasifIk oleh Brown dan Ogden (1993) pada tahun 1982-1983 memperlihatkan adanya peningkatan suhu permukaan laut yang mengakibatkan keluarnya alga yang bersimbiosis dengan hewan terumbu. Hewan karang yang kehilangan simbionnya ini kemudian mati dan diperkirakan menurun dari 70% sampai 95%. Dengan demikian hewan ini masih menjadi faktor alam yang memberi kontribusi utama terhadap penurunan kondisi terumbu karang (Glynn 1993, Hoegh-Guldberg et al. 1997). Enam episode utama dari peristiwa pemutihan karang terjadi sejak tahun 1979 dan menyebabkan kematian massal populasi karang. Setelah peristiwa itu hampir seluruh sistem yang ada di terumbu karang menghilang (Hoegh-Guldberg 1999). Melihat besarnya pengaruh yang ditimbulkan oleh peristiwa pemutihan terhadap kerusakan karang dan sistem yang terkait pada terumbu karang maka tulisan ini mengulasnya ditinjau dari biologi, fisiologi, dan ekologinya. BIOLOGI Selama peristiwa pemutihan, karang kehilangan 60-90% darijumlah zooxantelanya dan zooxantela yang masih tersisa dapat kehilangan 50-80% pig men fotosintesisnya (Glynn 1996). Gangguan yang berkepanjangan dapat menyebabkan kematian, sebagian atau keseluruhan, tidak hanya pada individu koloni, tetapi juga terumbu karang secara luas. I I Vol. 8,2001 Pemutihan dapat pula terjadi pada organisme lain yang berasosiasi dengan terumbu karang seperti karang lunak, anemon, dan beberapa spesies kirna raksasa tertentu (Tridacna spp.), yang juga memiIiki alga simbiosis dalarn jaringannya (Hoegh-Guldberg & Jones 1999). Sarna seperti karang, organisme ini dapat juga mati apabila kondisi yang mengarah kepada pemutihan cukup parah. Pada beberapa spesies karang, pemutihan menyebabkan perturnbuhan jaringan dan pengendapan kapur (kalsifikasi) terhenti, demikian pula proses reproduksi secara seksual terharnbat. Karang dapat bertahan hidup jika tekanan hanya berlangsung dalam waktu yang singkat, tetapi akan mati jika dalam waktu yang lama. Meskipun demikian, peristiwa tekanan subletal dapat membuat karang sangat peka terhadap infeksi oleh berbagai penyakit. Ledakan penyakit (epizootik) yang terjadi dapat menyebabkan kematian karang secara nyata (Pomerance et al. 1999). Pendugaan kematian karang yang mengalami peristiwa pemutihan massal, mendekati nol pada kasus pemutihan yang ringan (Harriot 1985) sarnpai mendekati 100% seperti yang terlihat pada beberapa terurnbu perairan dangkal di Indonesia (Brown & Suharsono 1990) dan terurnbu di bagian barat Pasifik yang mengalarni peristiwa EI Nino pada tahun 19821983. Kematian yang meningkat pada peristiwa pemutihan ditentukan oleh peningkatan suhu dan larnanya suhu berada di atas suhu rata-rata maksimum musim panas. Kematian populasi karang dilaporkan setelah lima minggu peristiwa pemutihan di bag ian tengah Great Barrier Reef (Baird & Marshall 1998, Marshall & Baird 1999). Kematian ini didominasi oleh karang bercabang dari Acroporidae, yaitu Acropora hyacinthus dan A. gemmifera yang mencapai 7080%. Studi lain juga dilakukan untuk melihat pengaruh tekanan panas terhadap kemarnpuan reproduksi dari karang-karang pembangun terumbu. Dua ratus koloni karang yang tumbuh di rataan terumbu (reef flat) Pulau Heron telah dicobakan setelah terjadi peristiwa pemutihan pada tahun 1988, yaitu dengan membandingkan fekunditas antara koloni karang yang mengalarni pemutihan dan yang tidak. Hasil pengamatan tersebut menunjukkan bahwa pengaruh tekanan pemutihan pada karang, secara umum sangat mengurangi aktivitas reproduksi. Koloni Acropora humilis, Favia sp., Goniastrea sp., Montipora sp., Platygyra daedalea, dan Symphyllia sp. yang diarnati tidak mengandung telur, meskipun semuanya diduga melakukan reproduksi pada bulan berikutnya (HoeghGuldberg 1999). Pada pengarnatan yang dilakukan selarna priode pemijahan pada bulan November terlihat bahwa karang-karang yang mengalarni pemutihan tersebut telah pulih, tetapi tidak melakukan pemijahan. Pada spesies karang lain yang subur di rataan terumbu, jumlah telur dari spesies yang mengalami pemutihan sangat rendah dibandingkan dengan yang tidak mengalami pemutihan, seperti Acropora aspera, A. palifer, A. pulchra, dan Montipora digitata (Hoegh-Guldberg 1999). Rendahnya perkembangan reproduksi yang kemudian diikuti dengan kematian massal setelah peristiwa pemutihan berakibat terhadap lambatnya laju pemulihan pada populasi karang. ULASAN 87 Karang-karang pembangun terurnbu secara proporsiona) memberikan kontribusi mendasar terhadap produktivitas ekosistem terumbu karang (Muscatine 1980, 1990). Karang pembangun terumbu yang berada di bawah pengaruh pemutihan terlihat pertumbuhan dan kemampuan untuk pemulihannya berkur.mg. Pengaruh utarna pada peningkatan suhu menyebabkan hilangnya zooxantela pada karang pembangun terumbu dan invertebrata lainnya yang bersimbiosis dengan zooxantela. Secara prinsip, zooxantela adalah mesin produksi primer pada organisme tersebut. Oleh karen a itu, pemutihan menyebabkan laju produktivitas fotosintetik pada karang pembangun terumbu dan organisme simbiotik lainnya turun secara drarnatis (Coles & JokieI1977). Aktivitas fotosintesis dari zooxanthella adalah sumber energi utama dalarn proses pengapuran (Muscatine 1980, 1990). Pengurangan kemampuan tumbuh dan pengapuran dapat juga diterjemahkan ke dalam suatu pengurangan kemampuan untuk berkompetisi terhadap ruang dengan organisme lain, seperti rumput laut, dan akhirnya akan membatasi sebaran karang-karang pembangun terumbu. FISIOLOGI Suhu perairan akan mempengaruhi laju metabolisme pelbagai karang dan simbionnya. Pengaruh suhu terhadap produksi bergantung pada respons fotosintesis dan respirasi dari zooxantela dan hewan-hewan terhadap perubahan suhu yang terjadi. Kemampuan karang untuk mengadakan penyesuaian terhadap perubahan suhu dapat bervariasi menurut spesies dan tempat hidup karang. Sebagai contoh, karang laut dangkal dapat menyesuaikan diri pada suatu kisaran suhu yang luasjika dibandingkan dengan karang laut dalarn (Muller-Parker & D'Elia 1995). Suhu merupakan faktor penting yang mempengaruhi stabilitas dari simbiosis karang pada tingkat individu dan secara pasti dalarn Iingkup yang lebih luas, yaitu terurnbu karang (Glynn 1991). Meskipun batas toleransi karang terhadap suhu bervariasi antarspesies atau antardaerah pada spesies yang sarna, tetapi dapat dinyatakan bah wa karang dan organisme terumbu hidup pada suhu dekat dengan batas atas toleransinya (Johannes 1975), oleh karen a itu dapat disimpulkan bahwa hewan-hewan karang relatif sempit toleransinya terhadap suhu. Peningkatan suhu hanya beberapa derajat sedikit di atas arnbang batas (=:2-3OC) dapat mengurangi laju pertumbuhan atau kematian yang luas pada spesies karang secara umum (Neudecker 1987, Jokiel & Coles 1990). Dalarn kasus cekarnan suhu, kenaikan suhu mengganggu kemampuan zooxantela untuk berfotosintesis dan dapat memicu produksi senyawa kimia berbahaya yang akhirnya merusak sel-sel mereka (Jones et al. 1998, Hoegh-Guldberg & Jones 1999). Akibat dari kehilangan zooxantela dan penurunan pig men fotosintesis menyebabkan penurunan dan efisiensi fotosintesis padazooxantela (Brown 1997). Studijuga dibuat untuk mengidentifikasi tempat-tempat khusus yang mengalarni kerusakan pada peristiwaipemutihan oleh suhu tinggi. Warner et al. (1996) mempelajari zooxantela dari spesies yang hidup di belakang daerah terumbu, Siderastrea 88 ULASAN Hayati radians lebih tahan terhadap suhu dibandingkan karang Montastrea annularis dan Agaracia lamarkii yang hidup di bagian depan terumbu. Zooxantela pada M. annularis tampak lebih peka terhadap kerusakan yang disebabkan oleh suhu pada atau dekat pusat reaksi fotosistem II, sedangkan zooxantela pada S. radians tetap mampu menghilangkan energi yang dibangkitkan melaluijalur nonfotokimia, dengan demikian akan melindungi fotosistem kerusakan selama terjadi peningkatan suhu. Dalam peningkatan suhu tersebut, tampaknya zooxantela mempunyai kemampuan untuk mempertahankan diri dari peningkatan penyinaran dan suhu. Owens (1994) menggambarkan keterkaitan antara laju penyerapan foton dan laju penggunaan foton pada proses fotosintesis (Gambar 1). Respons jangka pendek pada organisme fotosintetik digambarkan oleh kurva fotosintesis penyinaran (F-P) dengan laju fotosintesis diplotkan terhadap intensitas penyinaran. Kurva F-P memperlihatkan kej~nuhan kinetik, jika peristiwa intensitas cahaya melebihi kisaran fisiologi karang maka laju penyerapan cahaya ialah linear terhadap intensitas cahaya tersebut. Perbedaan antara dua kurva (digambarkan dalam daerah yang diarsir) menunjukkan penyerapan energi cahaya yang melampaui kapasitas fotosintesis yang akan digunakan. Konsekuensi mendasar pada kelebihan cahaya yang diserap ialah kerusakan foto-inhibitor pada pusat reaksi fotosistem II dan secara umum merusak membran dan protein oleh adanya oksigen tunggal, superoksida, dan radikal bebas lainnya. Radikal bebas diketahui terlibat sebagai mediator dalam peristiwa pemutihan (Lesser et al. 1990). Suatu respons terhadap peningkatan suhu dan penyinaran telah dicobakan pada zoantid, Palythoa caribaeorum. Kerusakan yang ditimbulkan dari kelebihan cahaya yang diserap dapat disebabkan oleh perubahan pada faktor lingkungan lain, seperti beberapa gangguan (peningkatan suhu) yang menyebabkan suatu penurunan dalam laju fotosintesis dan selanjutnya kurva F-P akan menurun dan mengarah pada suatu penyerapan cahaya yang berlebih. Kerja terakhir terhadap karotenoid, diadinoxantin, dan diatoxantin dalam zooxantela karang menunjukkan bahwa terjadi perubahan atau pengaliran yang nyata selama suatu peristiwa pemutihan yang diakibatkan oleh radiasi matahari yang tinggi. Inter-conversion dari karotenoid pada zooxantela merupakan siklus xantofil yang bertanggung jawab terhadap Kejadian intensitas cahaya (W/m2) Gambar 1. Hubungan antara laju penyerapan foton (-----) dan laju pemanfaatan foton ( - ) dalam fotosintesis (Owens 1994). penghilangan suhu oleh pembangkitan energi yang berlebih pada organ fotokimia. Proses pembangkitan energi yang berlebih ini tidak dapat digunakan untuk fotosintesis dan akan dihilangkan dengan suatu cara yang aman dan terkontrol segera setelah penyerapan. Karotenoid lainnya yang teridentifikasi dalam karang, mungkin memiliki suatu peran fotoproteksi sebagai pengikat oksigen tunggal atau bebas dan sebagai pemecah rantai antioksidan (Shick et al. 1996). EKOLOGI Karang-karang pembangun terumbu tidak semuanya sarna dalam kepekaannya menerima pengaruh dari peningkatan suhu. Sebagai contoh, karang mas if (Porites spp.) relatiftahan terhadap tekanan suhu dan jika mengalami pemutihan cenderung pulih dengan sedikit atau tanpa peningkatan kematian. Sedangkan Acropora (karang bercabang) terlihat lebih peka oleh peningkatan suhu perairan. Dalam kasus ini bisa mencapai 95% dari koloni yang mengalami pemutihan dan mati dalam 3-6 bulan berikutnya (Gleason & Wellington 1993). Perubahan struktur komunitas juga dilaporkm oleh Brown (1997) di Pulau Pari yang rataan terumbunya didominasi oleh komunitas Acropora bercabang sebelum peristiwa pemutihan pada tahun 1983, namun pada tabun 1994 tempat tersebut telah didominasi oleh Porites bercabang dan masif. Salah satu dampak yang juga ditimbulkan oleh pemutihan ialah perubahan secara dramatis kekayaan spesies pada komunitas terumbu (Glynn 1988, 1990). Kepunahan lokal pada spesies karang telah dilaporkan dan pada satu kasus dari spesies hidrokoral telah mendekati kepunahan total di bagian timur Pasifik (de Weerdt & Glynn 1991). Bagaimana perubahan spesies akan mempengaruhi stabilitas dalamjangka panjang dari suatu terumbu karang sampai saat ini belum diketahui. Peristiwa pemutihan yang luas dan berlangsung lama juga dapat menurunkan produktivitas ekosistem terumbu karang. Penurunan produktivitas tersebut diperkirakan berpengaruh besar terhadap organisme lain, terutama burung dan mamalia laut, namun sedikit studi yang mengukur dampak tersebut. Beberapa kejadian EI Nino berhubungan kuat dengan kematian burung dan berkurangnya populasi penyu. Penurunan produktivitas terumbu karang selama awal tahun di Pulau Heron dan Pulau One Tree di bagian ujung selatan Great Barrier Reef tampaknya bertanggung jawab terhadap penurunan populasi ikan yang menjadi mangsa burung dan mamalia laut (Hoegh-Guldber 1999). Koloni karang yang memutih, apakah mereka mati seluruhnya atau hanya sebagian menjadi lebih rapuh terhadap perkembangan alga yang berlebihan, penyakit dan organisme pelubang (boring organism) yang menjangkiti karang akan melemahkan struktur terumbu (Rowan et al. 1997). Jika kematian tinggi, terumbu mati yang memutih berubah secara cepat menjadi abu-abu kecokelatan yang pupus seiring dengan perkembangan alga yang menutupi mereka. Bila dampak pemutihan yang terjadi sangat parah maka alga yang berkembang secara meluas dapat mencegah rekolonisasi , Vol. 8, 200} karang-karang baru dan secara dramatis mengubah pola keanekaragaman jenis karang dan menyebabkan restrukturisasi komunitas terumbu. Adapun dampak dari menurunnya pertumbuhan karang yang terkena pemutihan ialah mengurangi kemampuan karang untuk berkompetisi terhadap ruang dengan organisme bentik lainnya, seperti turf algae, alga koralin, makroalga, sepon, briozoa, dan tunicata. Hasil pengamatan di Costa Rica, Panama, Kepulauan Galapagos, dan Indonesia menunjukkan bahwa alga bentik dengan cepat turnbuh menutupi karang yang hampir mati atau mati pada terurnbu~terumbu yang rusak oleh peristiwa pemanasan EI Nino (Glynn 1993). Penurunan kapasitas reproduksi pada karang-karang yang mengalami pemutihanjuga diduga memberi dampak ekologi yang negatif dalam proses peremajaan karang dan terutama sangat kritis untuk menghasilkan spesies secara tahunan dan bahkan tidak dapat bereproduksi (Jokiel & Guinther 1978). Peristiwa pemutihan juga berdampak terhadap kelimpahan karang jika peristiwa tersebut mematikan karang-karang dewasa sebelum mereka matang dan bereproduksi. Sebagai contoh, karang-karang Acroporidae yang memerlukan waktu sekitar 4-5 tahun untuk matang (Harrison & Wallace 1990) apabila dikaitkan dengan peristiwa pemutihan yang terjttdi rata-rata setiap 3-4 tahun dan frekuensi ini terus meningkat, maka umumnya karang Acroporidae akan gagal untuk bereproduksi. Masalah yang lebih buruk bagi karang ialah lebih lamanya waktu yang dibutuhkan untuk matang dan murigkin pada akhimya yang terseleksi ialah karang-karang yang tergolong dalam r-strategist, yaitu karang yang mampu bereproduksi lebih awal dalam sejarah hidup mereka. Karang ini memiliki pertumbuhan yang cepat dengan bentuk pertumbuhan bercabang dan melebar seperti daun yang pada umumnya bersifat hermafrodit brooding dan bereproduksi secara bulanan sepanjang tahun. Karang-karang dengan strategi ini memiliki tingkat keberhasilan reproduksi yang tinggi dan menghasilkan planula dengan masa larva yang relatif singkat dan melekat di sekitar koloni induk sehingga spesies ini sering kali mendominasi suatu habitat di terumbu karang (Szmant 1986). Berlawanan dengan hal tersebut ialah karang-karang dengan k-strategist, yaitu karang yang berurnur panjang sebingga membutuhkan waktu yang lebih lama untuk bereproduksi (Hoegh-Guldberg 1999). Karang-karang dengan k-strategist ini memiliki bentuk pertumbuhan yang masif dan seperti tiang yang umumnya bereproduksi melalui pemijahan (Harriot 1983, Szmant 1986). Strategi reproduksi yang seperti ini memiliki tingkat keberhasilan reproduksi yang relatif lebih rendah jika dibandingkan dengan spesies-spesies r-strategist, namun menghasilkanjumlah telur yang lebih banyak. Spesies inijuga dikenal memiliki kemampuan fisik untuk hidup pada habitat yang ekstrem atau habitat yang mengalami gangguan fisik (Szmant 1986). Dampak pemutihan yang juga dapat memberikan pengaruh terhadap perubahan struktur komunitas karang ialah ledakan penyakit. Beberapa peristiwa pemutihan terjadi bersamaan atau sangat dekat dengan epizootik penyakit karang. Kemungkinannya ialah karang-karang yang sakit lebih mudah mengalami pemutihan atau karang-karang yang mengalami ULASAN 89 cekaman oleh peristiwa pemutihan menjadi lebih peka terhadap berbagai penyakit karang (Williams & Bunkley_ Williams 1990). Dampak peristiwa pemutihan terhadap struktur komunitas ikan mengikuti teori umum interaksi antara habitat ikan dan terumbu karang. Terlepas dari pemanfaatan itu sendiri, beberapa faktor yang memberi sumbangan terhadap komposisi komunitas ikan di terumbu semuanya berhubungan dengan struktur fisik dan kekompleksan terumbu karang. Pertama ialah kompetisi makanan yang menjadi faktor penting dalam menentukan keanekaragaman dan kelimpahan ikan. Pada terumbu karang sehat, keragaman dan kuantitas makanan tinggi dan berdampak positif langsung terbadap keragaman dan kelimpahan ikan. Sedangkan pada terumbu yang ~~g sehat atau karang mati akan cepat ditumbuhi oleh alga secara berlebihan, alga ini kemudian dirnakan oleh herbivora seperti ikan kakatua (Scarus spp.) dan akhirnya populasi dari jenis ikan ini akan meningkat. Pemangsaan alga dalam jumlah besar oleh ikan ini di satu sisi akan membatasi pertumbuhan alga, namun di sisi lain juga merusak struktur terumbu karena menyebabkan erosi pada kerangka kapur karang (Robertson & Gaines 1986). Dampak peristiwa pemutihan terhadap perubahan struktur komunitas ikan terumbu sangat sukar ditentukan (Ohman 1999). Secara umum ikan-ikan terumbu karang sangat terasosiasi dengan habitat terurnbu karena peristiwa pemutihan cenderung mematikan karang dan mengubah struktur terumbu. Pemutihan diduga mempengaruhi struktur komunitas ikan, namun karena populasi ikan-ikan terumbu memiliki karakter yang sangat kompleks maka berbagai faktor dapat mengontrol jumlah mereka dan pengaruhnya dapat bervariasi dari satu terumbu ke terumbu lainnya. Semuanya bergantung pada komposisi komunitas ikan, interaksi habitat sebelum dan sesudah dampak, dinamika peremajaan, serta struktur habitat sebelum dan sesudah gangguan. Jika spesies-spesies karang yang dominan terpengaruh oleh dampak pemutihan dan terdapat keterkaitan erat antara karang-karang dan populasi ikan yang ada, maka perubahan dalam komunitas mungkin dapat terjadi. Jika karang-karang mati menjadi pecahanpecahan karang (rubble), peluangnya ialah akan ada suatu penurunan besar terhadap kelirnpahan darrkeragaman ikan. DAFTAR PUSTAKA Asada K, Takahashi M. 1987. Production and scavenging of active oxygen in photosynthesis. Di dalam: Kyle OJ, Osmond CB, Arntzen CJ (cd). Photoinhibition. Amsterdam: Elsevier. hlm 228-287. Baird AH, Marshall PA. 1998. Mass bleaching of corals on the Great Barrier Reef. Coral Reefs 17:376. Brown BE. 1997. Coral bleaching: causes and consequences. Coral Reefs 16:S129-S138. Brown BE, Ogden JC. 1993. Coral bleaching. Sci Amer 268:64-70. Brown BE, Suharsono. 1990. Damage and recovery of coral reefs effected by El Nino related seawater warming in the Thousand lslands, Indonesia. Coral Reefs 8:163-170. Coles SL, Jokiel PL. 1977. Effects of temperature of photosynthesis and respiration in hermatypic corals. Mar Bioi 43:209-216. de Weerdt WH, Glynn PW. 1991. A new and presumably extinct species of Millepora (Hydrozoa) in the eastern Pacific. Med Leiden 65:267-276. j 90 ULASAN Gleason OF, Wellington GM. 1993. Ultraviolet radiation and coral bleaching. Nature 365:836-838. ' Glynn PW. 1988. EI Nino-Southern Oscillation 1982-83: nearshore population, community, and ecosystem responses. Ann Rev Ecol Systemat 19:309-345. Glynn PW. 1990. Cora1 mortality and disturbances to coral reefs in the tropical eastern Pacific: Di daIam: Proc Glob Ecol Conseq 1982-83 El Nino-Southern OsciL Amsterdam: Elsevier. him 55-126. Glynn PW. 1991. Coral reef bleaching in the 1980s and possible connections with global warming. Trends Ecol EvoI6:175-179. Glynn PW. 1993. Cora1 reefbleaching:ecological perspectives. Coral Reefs 12:1-17. Glynn PW. 1996. Coral bleaching: facts, hypotheses and implications. Glob Change Bioi 2:495-509. Goreau TI. 1992. Bleaching and reef community change in Iamaica: 19511991. Amer ZooI32:683-695. Harriot VI. 1983. Reproductive ecology of four scleractinian species at Lizard Island, Great Barrier Reef. Coral Reefs 2:9-18. Harriot VI. 1985. Mortality rates of scleractinian corals before and during a mass bleaching event Mar Ecol Prog Ser 21:81-88. Harrison PL, Wallace CC. 1990. Reproduction, dispersal and recruitment of scleractinian corals. Di daIam: Oubinsky Z (ed). Coral Reefs: Ecosystems of the World. Amsterdam: Elsevier. him 13-207. Hayes RI, Gareau TI. 1992. Histology of Caribbean and south Pacific bleached corals. Proc. 7* Int. Coral ReefSymp. Guam 1:71. Hoegh-Guldberg O. 1999. Climate change, coral bleaching and the future of the world's coral reefs. Mar Freshwat Res 50:839-866. Hoegh-Guldberg 0, Berkelmans R, Oliver 1. 1997. Coral bleaching: implications for the Great Barrier Reef Marine Park. Di daIam: Conference in Research and reefmanagement proceedings. Townsville, 24-26 Nov 1996. him 171-193. Hoegh-Guldberg O,Iones R. 1999. Photoinhibition and photoprotection in symbiotic dinoflagellates from reef-building corals. Mar Ecol Progr Ser 183:73-86. lPCC. 1988. The Regional1mpacts of Climate Change: An Assessment of Vulnerability. Oi daIam: Watson RT, Zinyowera MC, Moss RH (ed). Intergovernmental Panel on Climate Change. New York: Cambridge University Pr. Johannes RE. 1975. Pollution and degradation of coral reef communities. Di daIam: Wood ElF, Iohannes RE (ed). Trop Mar Pollut 12:13-50. Jokiel PL, Coles SL. 1990. Response of Hawaiian and other Indo-Pacific reef corals to elevated temperature. Coral Reefs 8:155-162. Jokiel PL, Guinther EB. 1978. Effects of temperature on reproduction in the hermatypic coral Pocillopora damicomis. Bull Mar Sci 28:786789. Jones R, Hoegh-Guldberg 0, Larkum AWL, Schreiber U. 1998. Temperature induced bleaching of corals begins with impairment of dark metabolism in zooxanthellae. Plant Cell Environ 21:1219-1230. Lesser MP, Stochaj WR, Tapley OW, Shick 1M. 1990. Bleaching in coral reef anthozoans: effects of irradiance, ultraviolet radiation, and temperature on the activities of protective enzymes against active oxygen. Coral Reefs 8:225-232. Hayati Marshall PA, Baird AH. 1999. Bleaching of coral in the Central Great Barrier Reef: variation in assemblage response and taxa susceptibilities. Mar Ecol Progr Ser 183:87-96. Muller-Parker G, O'Elia CF. 1995. Interaction between corals and their symbiotic algae. Di dalam: Birkeland C. Life and Death ofCoral Reefs. New York: International Thomson. him 96-113. Muscatine L. 1980. Productivity of Zooxanthellae. Di dalam: Falkowski PG (ed). Primary Productivity in the Sea. New York. Plenum. him 381402. Muscatine L. 1990. The role of symbiotic algae in carbon and energy flux in reef corals. Di dalam: Dubinsky Z (ed). Coral Reefs: Ecosystems of the World 25. Amsterdam: Elsevier. him 75-87. Neudecker S. 1987. Environment effects of power plants on coral reefs and ways to minimize them. Di dalam: Salvant B (ed). Human Impacts on Coral Reefs: Facts and Recommendations. Papetoai: Antenne de Tahiti Museum EPHE. him 103-118. Ohman MC. 1999. Coral bleaching effects on reef fish communities and fisheries. Di dalam: Jernelov A, Hewawasam I, Graulund A, Persson GA, Kristofersm L (ed). Coral reef degradation in the Indian Ocean: Status repons and project presentations. Stockholm: CORDIO. him 71-77. Owens TG. 1994. Excitation energy transfer between chlorophylls and carotenoids. A proposed molecular mechanism for non-photochemical quenching. Di dalam: Baker NR, Bowyer JR (ed). Photoinhibition of Photosynthesis from Molecular Mechanisms to the Field. Oxford: Bios. him 53-76. Pomerance R, Reaser JK, Thomas PO. 1999. Coral bleaching, coral mortality, and global climate change. The U.S. coral reef taskforce. http:// www.state.gov/www/globaUglobaCissues/coral_reefs/ 990305_ coralreeC rpthtrul. . Reaka-Kudla ML. 1996. The global biodiversity of coral reefs: a comparison with rainforest Di dalam: Reaka-Kudla ML, Wilson DE, Wilson EO. (ed). Biodiversity II: Understanding and protecting our natural resources. Washington DC: National Academy. him 83-108. Robertson DR, Gaines SO. 1986. Interference competition structures habitat use in a local assemblage of coral reef surgeonfishes. Ecology 67: 1372-1383. Rowan R, Knowlton N, Baker A,Iara J. 1997. Landscape ecology of algal symbionts creates variation within episodes of corla bleaching. Nature 388:265-269. Sebens KP. 1994. Biodiversity of coral reefs: What are we losing and why? Amer Zool 34:115-133. Shick 1M, Lesser MP, Jokiel PL. 1996. Ultraviolet radiation and coral stress. Glob Change Bioi 2:527-545. Szmant AM. 1986. Reproductive ecology of Caribbean reef corals. Coral Reefs 5:43-54. Warner ME, Fitt WK, Schmidt GW. 1996. The effects of elevated temperature on the photosynthetic efficiency of zooxanthellae in hospite from four different species of reef coral: a novel approach. Plant Cell Environ 19:291-299. Williams EH Ir, Bunkley-Williams L. 1990. The world-wide coral reef bleaching cycle and related sources of coral mortality. Atoll Res Bull 335:1-71.