STOIKIOMETRI
advertisement
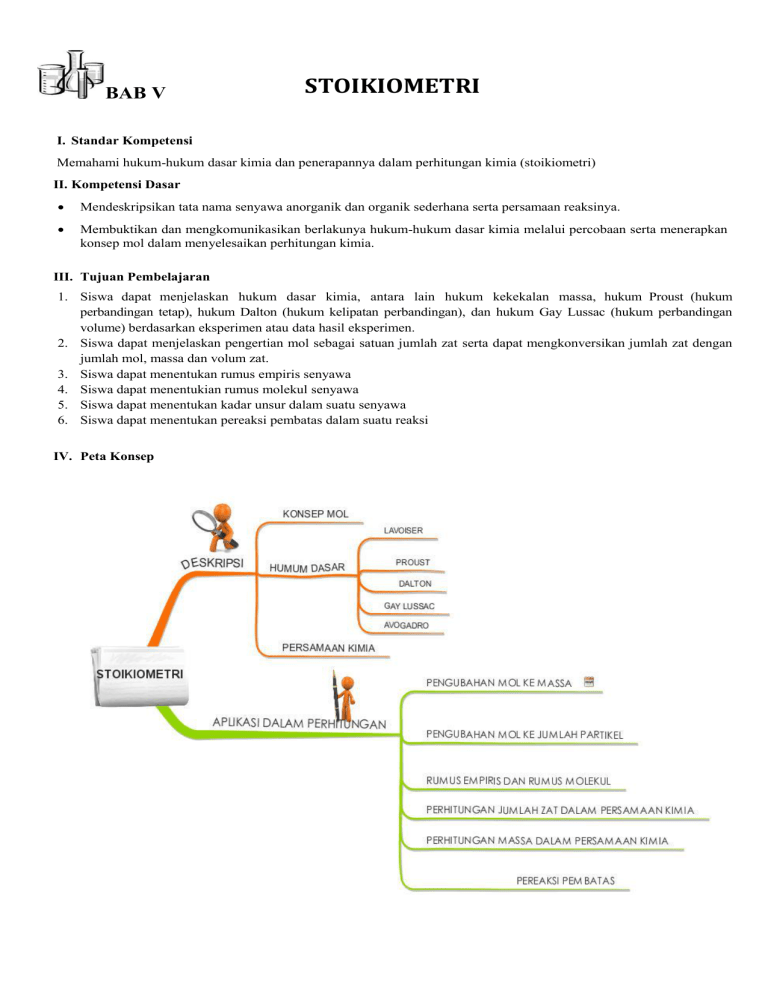
BAB V STOIKIOMETRI I. Standar Kompetensi Memahami hukum-hukum dasar kimia dan penerapannya dalam perhitungan kimia (stoikiometri) II. Kompetensi Dasar Mendeskripsikan tata nama senyawa anorganik dan organik sederhana serta persamaan reaksinya. Membuktikan dan mengkomunikasikan berlakunya hukum-hukum dasar kimia melalui percobaan serta menerapkan konsep mol dalam menyelesaikan perhitungan kimia. III. Tujuan Pembelajaran 1. Siswa dapat menjelaskan hukum dasar kimia, antara lain hukum kekekalan massa, hukum Proust (hukum perbandingan tetap), hukum Dalton (hukum kelipatan perbandingan), dan hukum Gay Lussac (hukum perbandingan volume) berdasarkan eksperimen atau data hasil eksperimen. 2. Siswa dapat menjelaskan pengertian mol sebagai satuan jumlah zat serta dapat mengkonversikan jumlah zat dengan jumlah mol, massa dan volum zat. 3. Siswa dapat menentukan rumus empiris senyawa 4. Siswa dapat menentukian rumus molekul senyawa 5. Siswa dapat menentukan kadar unsur dalam suatu senyawa 6. Siswa dapat menentukan pereaksi pembatas dalam suatu reaksi IV. Peta Konsep STOIKIOMETRI Dalam ilmu kimia, stoikiometri dibagi menjadi stoikiometri senyawa (komposisi) dan stoikiometri reaksi. Istilah stoikiometri berasal dari bahasa Yunani yaitu stoicheion yang berarti elemen atau unsur dan metron yang artinya mengukur. Jadi, stoikiometri dapat diartikan sebagai perhitungan kimia yaitu ilmu yang mempelajari dan menghitung hubungan kuantitatif dari reaktan dan produk dalam reaksi kimia (persamaan kimia). Konsep–konsep yang mendasari perhitungan kimia adalah massa atom relatif, rumus kimia, persamaan kimia, dan konsep mol . A. Hukum–Hukum Dasar Kimia Berikut ini akan dipelajari beberapa hukum yang mendasari perhitungan kimia, di antaranya hukum kekekalan massa (hukum Lavoisier), hukum perbandingan tetap (hukum Proust), hukum kelipatan perbandingan (hukum Dalton), dan hukum perbandingan volume (hukum Gay Lussac). 1. Hukum Lavoiser (Hukum Kekekalan Massa) Jika kita mengamati proses pembakaran kayu atau kertas, massa hasil reaksi seolah-olah berkurang karena kita hanya mendapatkan abu yang jumlahnya sedikit dari sisa pembakaran. Reaksi pembakaran yang kita lakukan berlangsung pada wadah yang terbuka, sedangkan sebagian besar hasil reaksi adalah gas sehingga massa zat yang tertinggal menjadi lebih sedikit. Tetapi, jika kita melakukan pembakaran tersebut pada ruang tertutup, maka massa zat sebelum dan sesudah reaksi akan sama. Gambar 1. Antoine Laurent Lavoisier/ Perancis (1743 – 1794) Antoine Laurent Lavoisier telah menyelidiki massa zat-zat sebelum dan sesudah reaksi. Lavoisier menimbang zat sebelum bereaksi, kemudianmenimbang hasil reaksinya. Ternyata massa zat sebelum dan sesudah reaksiselalu sama. Lavoisier menyimpulkan hasil penemuannya dalam suatu hukum yang disebut hukum kekekalan massa, yaitu: “Dalam sistem tertutup, massa zat sebelum dan sesudah reaksi adalah sama.” Contoh: Kawat tembaga (Cu) dibakar dalam pembakar bunsen sehingga terbentuk tembaga oksida (CuO), dengan persamaan: 2Cu(s) + O2(g)→2CuO(s) Jika berat Cu semula 32 g dan CuO yang terbentuk 40 g, berapa berat O2 yang bereaksi? Jawab: Menurut Hukum Kekekalan Massa, dalam reaksi kimia tidak terjadi perubahan massa. Oleh karena itu, berat O2 yang bereaksi adalah 40 g – 32 g = 8 g 32 g Cu(s) + 8 g O2(g) →40 g CuO(s) 2. Hukum Proust (Hukum Perbandingan Tetap) Pada tahun 1799, Joseph Louis proust dari Perancis melakukan eksperimen, yaitu mereaksikan gas hidrogen dan gas oksigen. Ia menemukan bahwa gas hidrogen dan gas oksigen selalu bereaksi membentuk senyawa air dengan perbandingan massa yang tetap, yaitu 1 : 8. Gambar 2. Joseph Louis Proust (1754-1826) Tabel 1. Data hasil eksperimen Proust Berdasarkan penelitian terhadap berbagai senyawa yang dilakukannya, Proust menyimpulkan bahwa “Perbandingan massa unsur-unsur dalam satu senyawa adalah tertentu dan tetap.” LATIHAN! 1. Perbandingan massa karbon (C) terhadap oksigen (O) dalam senyawa karbon dioksida(CO2) adalah 3 : 8. Berapa gram massa karbon dioksida yang terbentuk dan sisapereaksi, jika direaksikan: a. 6 gram karbon dengan 16 gram oksigen b. 6 gram karbon dengan 8 gram oksigen c. 3 gram karbon dengan 10 gram oksigen d. 12 gram karbon dengan 24 gram oksigen 2. Diketahui perbandingan massa kalsium dan oksigen dalam membentuk senyawa kalsium oksida adalah 5 : 2. Bila direaksikan 10 gram kalsium dan 12 gram oksigen, tentukanmassa kalsium oksida (CaO) yang terbentuk dan sisa pereaksi! 3. Perbandingan massa Fe : S dalam senyawa FeS adalah 7 : 4. Berapakah massa FeSyang terbentuk dan massa sisa pereaksi, jika direaksikan 35 gram besi dan 16 grambelerang? 4. Diketahui perbandingan massa tembaga dan oksigen dalam senyawa CuO adalah4 : 1. Tentukan massa CuO yang terbentuk dan sisa pereaksi, jika direaksikan: a. 8 gram tembaga dengan 2 gram oksigen b. 12 gram tembaga dengan 3 gram oksigen c. 20 gram tembaga dengan 10 gram oksigen d. 32 gram tembaga dengan 5 gram oksigen 5. Sampel zink sulfida dibuat dengan tiga cara yang berbeda, yaitu dalam 3,22 gram sampel pertama terdapat 1,06 gram zink, sedangkan dalam 5,38 gram sampel kedua terdapat 1,77 gram belerang. Dalam sampel ketiga, 0,93 gram zink bereaksi dengan 0,46 gram belerang. Apakah data ini memenuhi hukum perbandingan tetap (hukum Proust)? 3. Hukum Dalton (Hukum Kelipatan Berganda) Gambar 3. John Dalton (1766 – 1844) Hukum Proust dikembangkan lebih lanjut oleh ilmuwan lain untuk unsur-unsur yang dapat membentuk lebih dari satu senyawa. John Dalton (1766-1844) adalah ilmuan dari Inggris yang mengamati adanya suatu keteraturan yang terkait dengan perbandingan massa unsur-unsur dalam suatu senyawa. Untuk memahami hal ini, perhatikan tabel hasil percobaan reaksi antara nitrogen dengan oksigen berikut. Tabel 2. Data hasil eksperimen Dalton Dengan massa oksigen yang sama, ternyata perbandingan massa nitrogen dalam senyawa nitrogen dioksida dan senyawa nitrogen monoksida merupakan bilangan bulat dan sederhana. Dalam NO => Nitrogen : Oksigen = 0,875 : 1 Dalam NO2 => Nitrogen : Oksigen = 1,75 : 1 Perbandingan: Nitrogen (dalam NO) : Nitrogen (dalam NO2) = 0,875 : 1,75 = 1 : 2 Berdasarkan hasil percobaannya, Dalton merumuskan hukum kelipatan perbandingan(hukum Dalton) yang berbunyi: “Jika dua unsur membentuk dua senyawa atau lebih dan jika massa salah satu unsur dalam senyawa tersebut sama, maka perbandingan massa unsur lainnya dalam senyawa tersebut merupakan bilangan bulat sederhana.” Berikut adalah contoh penerapan hukum kelipatan perbandingan: LATIHAN! 1. Fosfor dan oksigen membentuk dua macam senyawa. Dalam 55 gram senyawa I terdapat 31 gram fosforus, sedangkan 71 gram senyawa II mengandung 40 gram oksigen. Tunjukkan bahwa kedua senyawa itu memenuhi hukum Dalton! 2. Unsur nitrogen dan oksigen dapat membentuk lebih dari satu senyawa, seperti NO,NO2, N2O3, dan N2O4.Pada kondisi tertentu, 1 g nitrogen tepat bereaksi dengan 1,14 g oksigen. Pada kondisiyang lain, 1 g nitrogen tepat bereaksi dengan 2,28 g oksigen.Jelaskan bahwa data ini sesuai dengan Hukum Perbandingan Berganda. Bagaimanarumus kimia kedua senyawa itu? 4. Hukum Gay Lussac (Hukum Perbandingan Volume) Joseph Louis Gay Lussac (1788-1850) dariPerancis tertarik pada penemuan Henry Cavendish (1731-1810) dari Inggris, yang menemukan perbandingan volume hidrogen yang bereaksi dengan oksigen membentuk air adalah 2 : 1, jika kedua gas itu diukur pada suhu (T) dan tekanan (P) yang sama. Gambar 4. Joseph Louis Gay Lussac (1778 – 1850) Kemudian, pada tahun 1808 Gay Lussac melakukan percobaan terhadap berbagai reaksi dan mengamati volume gas-gas yang terlibat dalam reaksi tersebut. Pengamatan menunjukkan bahwa reaksi pada temperatur (T) dan tekanan (P) yang sama diperoleh hasil sebagai berikut: 1) Pada volume tertentu gas hidrogen (H2) bereaksi dengan volume tertentu gas klorin (Cl2) menghasilkan gas hidrogen klorida (HCl), perbandingan volumenya adalah 1 : 1 : 2. H2(g) + Cl2(g)→ 2HCl(g) 2) Pada reaksi antara gas hidrogen dengan gas oksigen menghasilkan air, perbandingan volumenya adalah 2 : 1 : 2. 2H2(g) + O2(g)→ 2H2O(g) 3) Pada reaksi antara gas nitrogen dengan gas hidrogen membentuk amonia, perbandingan volumenya adalah 1 : 3 : 2. N2(g) + 3H2(g) → 2NH3(g) Dari data tersebut, Gay Lussac menyimpulkan penemuannya sebagai Hukum Perbandingan Volume, sebagai berikut: “Pada kondisi temperature (T) dan tekanan (P) yang sama, perbandingan volume gas-gas pereaksi dengan gas-gas hasil reaksi berbanding sebagai bilangan yang bulat dan sederhana.” Contoh: Amonia dibuat dari reaksi gas hidrogen dengan gas nitrogen menurut persamaan: 3H2(g) + N2(g)→ 2NH3(g) Jika 6 liter gas hidrogen bereaksi dengan gas nitrogen untuk membentuk amonia, hitunglah volume N2 yang bereaksi serta volume NH3 yang terbentuk jika diukur pada kondisi temperatur dan tekanan yang sama. Jawab: Perbandingan koefisien H2 : N2 : NH3 = 3 : 1 : 2. Jadi, jika H2 = 6 L Maka: Volume N2 = Volume NH3 = Jadi, volume N2 yang bereaksi = 2 L dan volume NH3 yang terbentuk = 4 L. LATIHAN! 1. Hitunglah volume gas metana dan karbon dioksida pada reaksi pembakaran metana berikut: gas metana + gas oksigen → karbondioksida + uap air volume gas oksigen yang bereaksi adala 15 mL dan perbandingan volumenya adalah 1 : 2 : 1 : 2 2. Perhatikan persamaan reaksi berikut: 2H2(g) + O2(g) → 2H2O(g) Hitung volume gas hidrogen dan gas oksigen yangdiperlukan untuk membuat 60 liter air! 3. Tiga liter gas propana (C3H8) dibakar sempurna dengan gas oksigen membentuk gaskarbon dioksida dan air, sesuai persamaan reaksi berikut. C3H8(g) + O2(g) → CO2(g) + H2O(l) a. Berapa liter gas oksigen yang diperlukan? b. Berapa liter gas karbon dioksida yang terbentuk? c. Berapa liter air yang terbentuk? 4. Lima liter gas N2O5 terurai sesuai reaksi berikut: N2O5(g) → N2(g) + O2(g) Pada suhu dan tekanan yang sama, tentukan volume gas nitrogen dan volume gasoksigen yang terbentuk! 5. 10 mL gas nitrogen (N2) dan 15 mL gas oksigen (O2) tepat habis bereaksi menjadi10 mL gas NaOb. Tentukan rumus kimia gas NaObtersebut! B. Hipotesis Avogadro Penemuan Gay Lussac dan hukum Dalton dikembangkan oleh seorang ahli fisika Italia, Amedeo Avogadro. Pada 1811, Avogadro menemukan bahwa gabungan dari atom-atom yang sama membentuk suatu molekul dengan kata lain Avogadro mengemukakan bahwa partikel unsur tidak harus berupa atom tunggal, tetapi dapat juga berupa molekul. Gambar 5. Amedeo Avogadro (1776–1856) Avogadro menjelaskan hukum perbandingan volume dengan mengajukan hipotesis sebagai berikut: “Pada suhu dan tekanan sama, gas-gas yang volumenya sama mengandung jumlah molekul yang sama.” Dengan kata lain, perbandingan volume gas-gas yang bereaksi sama dengan koefisien reaksinya. Salah satu contoh penerapan hipotesis Avogadro adalah pada reaksi pembakaran metana. 1 molekul CH4 2 molekul O2 1 molekul CO2 2 molekul H2O Gambar 6. Reaksi pembakaran metana Dengan persamaan reaksi: CH4(g) + 2O2(g) → CO2(g) + 2H2O(l) Maka perbandingan volume = perbandingan jumlah molekul = perbandingan koefisien Yaitu: 1 : 2 : 1 : 2 Contoh: Suatu senyawa hidrokarbon (CxHy) yang berwujud gas terbakar menurut reaksi: CxHy(g) + O2(g) → CO2(g) + H2O(g) (belum setara) Dari percobaan diketahui bahwa untuk membakar 2 liter gas CxHy(T, P) diperlukan 5liter gas oksigen (T, P) dan dihasilkan 4 liter gas karbon dioksida (T, P). Tentukanrumus molekul hidrokarbon tersebut! Jawab: Karena perbandingan volume sama dengan perbandingan koefisien reaksi, maka persamaan reaksinyamenjadi: 2CxHy(g) + 5O2(g) → 4CO2(g) + …. H2O(g) (belum setara) Jumlah atom oksigen disetarakan sehingga persamaan reaksi menjadi: 2CxHy(g) + 5O2(g) → 4CO2(g) + 2H2O(g) Untuk menyetarakan atom C dan H dengan cara sebagai berikut: Jadi, rumus molekul hidrokarbon tersebut adalah C2H2. LATIHAN! 1. Dua liter (T, P) gas nitrogen (N2) bereaksi dengan 4 liter (T, P) gas oksigen (O2) membentuk 4liter gas X. Tentukan rumus molekul gas X tersebut! 2. Pada penguraian sempurna 10 liter (T, P) suatu oksida nitrogen (NaOb) yang berupagas dihasilkan 20 liter (T, P) gas nitrogen dioksida dan 5 liter (T, P) gas oksigen.Tentukan rumus molekul NaOb! 3. Pada pembakaran sempurna 5 liter (T, P) gas CxHy diperlukan 15 liter (T, P) gasoksigen dan dihasilkan 10 liter (T, P) gas karbon dioksida sesuai persamaan reaksi berikut: CxHy(g) + O2(g) → CO2(g) + H2O(l) (belum setara) Tentukan rumus molekul CxHy tersebut! C. Stoikiometri Reaksi–Reaksi Gas Hukum Gay Lussac dan hipotesis Avogadro merupakan dasar bagi stoikiometri reaksi–reaksi gas. Jika pengukuran dilakukan pada temperatur dan tekanan yang sama, maka perbandingan volum gas yang terlibat dalam reaksi sama dengan koefisien reaksinya. Sehingga, jika salah satu volume komponen diketahui, maka volum komponen lainnya dapat ditentukan dengan cara berikut: Contoh 1: 5 liter gas butana (C4H10) dibakar sempurna menurut reaksi: C4H10(g) + O2(g) → CO2(g) + H2O(l)(belum setara) Hitunglah volume oksigen yang dibutuhkan dan volume gas karbon dioksida yang terbentuk! Jawab: 2C4H10(g) + 13O2(g) → 8CO2(g) + 10H2O(l) Contoh 2: Pada pembakaran sempurna 5 liter (T, P) campuran CH4 dan C2H6 dihasilkan 7 liter(T, P) karbon dioksida. Tentukan volume masing-masing gas dalam campuran tersebut! Jawab: Persamaan setara reaksi pembakaran CH4 dan C2H6 adalah: CH4(g) + 2O2(g)→ CO2(g) + 2H2O(l) 2C2H6+ 7O2(g)→ 4CO2(g) + 6H2O(l) Misal: volume C2H6 = x liter volume CH4 = (5 - x) liter 1) CH4(g) + 2O2(g) → CO2(g) + 2H2O(l) (5 - x) liter (5 - x) liter 2) 2C2H6 + 7O2(g) → 4CO2(g) + 6H2O(l) x liter x liter = 2x liter Dari persamaan 1 dan 2, maka: volum CO2 total = (5 - x) liter + 2x liter 7 liter = 5 + xliter x = 2 liter jadi, volume C2H6 = x liter = 2 liter volume CH4 = (5 - x) liter = 3 liter LATIHAN! 1. Gas belerang dioksida dibuat dengan reaksi antara gas belerang dan gas oksigen menurut persamaan reaksi: S(g) + O2(g) → SO2(g) Berapa volume gas belerang (T, P) dan gas oksigen (T, P) yang diperlukan untuk membuat 50 liter gas belerang dioksida (T, P)? 2. Pada pembakaran 5 liter (T, P) alkohol menurut reaksi: C2H5OH(g) + O2(g) → CO2(g) + H2O(l) tentukan volume oksigen yang bereaksi (T, P) dan volume gas karbon dioksida yang dihasilkan (T, P)! 3. Pada pembakaran sempurna 10 liter (T, P) campuran CH4 dan C2H4 dihasilkan 12 liter gas karbon dioksida sesuai reaksi: CH4(g) + O2(g) → CO2(g) + H2O(l) C2H4(g) + O2(g) → CO2(g) + H2O(l) tentukan susunan volume dalam campuran tersebut! 4. Pembakaran sempurna gas metana dan etana menghasilkan gas karbondioksida dan air. Jika volum gas CH4 dan C2H6 yang dibakar sama, reaksi pembakaran gas mana yang menghasilkan karbon dioksida terbanyak? UJI PEMAHAMAN 1. Berikut adalah hasil percobaan reaksi antara tembaga (Cu) dengan belerang (S)menghasilkan tembaga sulfida. Berdasarkan data hasil percobaan tersebut, berapakah perbandingan massa tembagadan belerang dalam senyawa CuS? 2. Dua liter suatu gas hidrokarbon (CxHy) dibakar sempurna memerlukan 6 liter gas oksigen dan menghasilkan 4 liter gas karbon dioksida dan uap air. Tuliskan persamaan reaksi dan tentukan rumus kimia gas hidrokarbon tersebut! 3. Pada reaksi pembakaran 8 liter campuran gas metana (CH4) dan propana (C3H8) diperlukan25 liter gas oksigen. Berapakah volume masing-masing gas tersebut? 4. Berapa liter gas H2dan gas O2 yang dibutuhkan untuk menghasilkan 15 liter uap air? Tuliskanpersamaan reaksinya! 5. Pada suhu dan tekanan tertentu, gas etanol (C2H5OH) dibakar sempurna dengan 60 liter udara yang mengandung 20% oksigen, menurut persamaan reaksi: C2H5OH + O2 → CO2+ H2O Bila diukur pada suhu dan tekanan yang sama, tentukan: a. volume etanol yang dibakar b. volume gas karbon dioksida yang dihasilkan 6. Suatu bahan bakar gas terdiri dari 80% volume metana (CH4) dan sisanya etana(C2H6). Hitunglah volume oksigen (T, P) yang diperlukan untuk membakar sempurna1 liter (T, P) bahan bakar tersebut! D. Konsep Mol Dalam kehidupan sehari-hari kita sering menggunakan satuan untuk menyebutkan bilangan yang besar untuk mempermudah perhitungan. Sebagai contoh satuan lusin, kilo, ons dan lain –lain. Satuan jumlah zat dalam ilmu kimia disebut mol. Satu mol zat mengandung jumlah partikel yang sama dengan jumlah partikel dalam 12 gram C–12, yaitu 6,02 × 1023 partikel. Jumlah partikel ini disebut sebagai bilangan Avogadro.Partikel zat dapat berupa atom, molekul, atau ion. Contoh: a. 1 mol besi (Fe) mengandung 6,02 × 1023atom besi (partikel unsur besi adalah atom). b. 1 mol air (H2O) mengandung 6,02 × 1023molekul air (partikel senyawa air adalah molekul). c. 1 mol Na+ mengandung 6,02 × 1023 ion Na+ (partikel ion Na+ adalah ion). Bilangan 6,02 × 1023 disebut tetapan Avogadro dan dinyatakan dengan lambang L. L = 6,02 × 1023 atom/molekul/ion 1) Hubungan Mol dengan Jumlah Partikel Hubungan antara jumlah mol (n) dengan jumlah partikel (X) dalam zat dapat dinyatakan sebagai berikut: 𝑋 𝑛 𝑋 𝑛 𝐿 𝑥 Contoh: 1. Tentukan jumlah partikel dalam 5 mol emas murni! Penyelesaian: = 3,01 × 1024 atom emas 2. Hitunglah jumlah partikel dalam 0,25 mol O2! Penyelesaian: = 1,505 × 1023molekul O2 LATIHAN! 1. Berapa jumlah atom karbon yang terkandung dalam 0,05 mol karbon? 2. Tentukan jumlah mol dari zat-zat berikut: a. 1,204 × 1024 atom Cu b. 3,01 × 1022 molekul CO2 c. 1.505 × 1024 ion Na+ 3. Tentukan jumlah partikel dari zat-zat berikut: a. 0,05 mol H2O b. 0,75 mol Fe c. 1,5 mol Cl4. Hitunglah jumlah mol NO2 di udara yang mengandung 0,7525 x 1023 molekul! 5. Berapakah jumlah molekul amonia yang terdapat dalam 500 mol NH3 2) Massa Molar Massa molar (mm) menyatakan massa yang dimiliki oleh 1 mol zat. Massa 1 mol zat sama dengan massa molekul relatif (Mr) zat tersebut dengan satuan gram/mol atau dengan kata lain, bilangan massa molar suatu zat sama dengan massa molekul relatifnya, yang membedakan hanya satuannya. Hubungan jumlah mol (n) dengan massa zat (m) adalah sebagai berikut: 𝑚 𝑛 𝑚𝑚 𝑛 𝑚 𝑚𝑚 dengan , m = massa zat (gram) n = jumlah mol (mol) mm = massa molar (gram/mol) Contoh: 1. Hitunglah massa dari 0,75 mol urea CO(NH2)2! (Ar C = 12, O = 16, N = 14, dan H = 1) Penyelesaian: mm CO(NH2)2= 60 g/mol LATIHAN! A. Hitunglah jumlah mol dari: a. 2,3 gram natrium (Ar Na = 23) b. 45 gram C6H12O6 (Ar C = 12, H = 1, dan O = 16) c. 35,1 gram NaCl (Ar Na = 23 dan Cl = 35,5) d. 196,5 gram seng (Ar Zn = 65,5) B. Hitunglah massa dari: a. 0,5 mol barium (Ar Ba = 137) b. 5 mol belerang (Ar S = 32) c. 2,5 mol K2SO4 (Ar K = 19, S = 32, dan O = 16) d. 0,3 mol CO2 (Ar C = 12 dan O = 16) e. 10 mol K2Cr2O7 (Ar K = 39, Cr = 52, dan O = 16) C. Tentukan Ar perak jika 5 mol perak massanya 540 gram! D. Hitunglah jumlah partikel gas O2 (ArO= 16) yang memiliki massa 16 gram! E. Hitunglah jumlah partikel gas Br2 (Mr =160) yang memiliki massa 1,6 g! F. Hitunglah massa 9,03 × 1023 molekul uap air (Ar H= 1; O = 16)! 3) Volume Molar Gas Hipotesis Avogadro menyebutkan bahwa pada suhu dan tekanan yang sama,semua gas dengan volume yang sama akan mengandung jumlah partikel yang sama pula. Oleh karena 1 mol setiap gas mempunyai jumlah molekul yang sama, maka pada suhu dan tekanan yang sama pula, 1 mol setiap gas mempunyai volume yang sama. Volume per mol gas disebut volume molar dan dilambangkanVm. Volume molar gas tidak tergantung pada jenisnya, tetapi hanya pada jumlah mol serta suhu dan tekanan pengukuran. Hubungan mol dengan volum gas dapat dinyatakan sebagai berikut: 𝑉 𝑛 𝑉𝑚 𝑛 𝑉 𝑉𝑚 Dengan, V = volume gas (liter) n = jumlah mol (mol) Vm = volume molar (liter/mol) Berikut merupakan beberapa keadaan yang dapat diadikan acuan dalam penentuan volume gas a) Keadaan Standar (STP) Keadaan standar dinyatakan dengan STP (Standard Temperature and Pressure) yaitu kondisi dengan suhu 0oC dan tekanan 1 atm. Pada keadaan STP, volume molar gas sama dengan 22,4 liter/mol. Pada keadaan STP:𝑉𝑚 𝑙𝑖𝑡𝑒𝑟 𝑚𝑜𝑙 − b) Keadaan Kamar (RTP) Keadaan kamar dinyatakan dengan RTP (Room Temperature and Pressure) yaitu kondisi dengan suhu 25oC dan tekanan 1 atm. Pada keadaan STP, volume molar gas sama dengan 24 liter/mol. Pada keadaan RTP:𝑉𝑚 𝑙𝑖𝑡𝑒𝑟 𝑚𝑜𝑙 − c) Persamaan Gas Ideal Volume gas pada suhu dan tekanan yang diketahui dapat dihitung dengan menggunakan persamaan gas yang disebut persamaan gas ideal berikut: dengan, P = tekanan gas (atm) 𝑛𝑅𝑇 V = volume gas (liter) 𝑃𝑉 𝑛𝑅𝑇 𝑉 𝑃 n = jumlah mol (mol) R = tetapan gas (0,082 L atm mol-1K-1) T = suhu mutlak gas (K) Contoh: Tentukan volume dari 2 mol gas nitrogen jika diukur pada: a. keadaan standar (STP) b. keadaan kamar (RTP) c. suhu 30 °C dan tekanan 1 atm penyelesaian: a. Pada keadaan standar (STP),Vm= 22,4 liter/mol b. c. V = 44,8 liter Pada keadaan kamar (RTP), Vm = 24 liter/mol V = 48 liter Pada suhu 30 °C dan tekanan 1 atm, dihitung dengan PV = nRT T = 273 + 30 = 303 K − − V = 49,692 liter d) Membandingkan Volume Gas Pada suhu dan tekanan yang sama, volume gas hanya bergantung padajumlah molnya. Misalkan gas pertama dengan jumlah mol n1 dan volumeV1 dan gas kedua dengan jumlah mol n2 dan volume V2, maka pada suhu dantekanan yang sama berlaku: 𝑛 𝑉 𝑛 𝑉 Contoh: Tentukan volume dari 2 mol gas nitrogen jika diukur pada suhu dan tekanan yang sama di mana 0,5 mol gas oksigen mempunyai volume 15 liter: Penyelesaian: 4) Kemolaran Larutan Kemolaran atau Molaritas (M) adalah salah satu cara menyatakan konsentrasi ataukepekatan larutan. Molaritas menyatakan jumlah mol zat terlarut dalam tiap liter larutan. Satuan molaritas (M) adalah mol/liter atau mmol/mL. 𝑴 𝒏 𝑽 dengan, M = kemolaran larutan (mol/lliter) n = jumlah mol (mol) V = volume larutan (liter) Contoh: Tentukan jumlah mol yang terdapat dalam 200 mL larutan urea 0,5 M! Penyelesaian: ⁄ LATIHAN! 1. Tentukan volume dari 0,25 mol gas oksigen pada suhu 27 °C dan tekanan 1 atm! 2. Tentukan volume dari 5 mol gas karbon dioksida pada keadaan standar (STP)! 3. Berapakah volume dari 0,75 mol gas belerang yang diukur pada suhu dan tekananyang sama pada saat 3 mol gas nitrogen volumenya 12 liter? 4. Berapakah volume dari 2,5 mol gas nitrogen dioksida pada keadaan kamar (RTP)? 5. Tentukan volume dari 0,2 mol gas hidrogen yang diukur pada: a. keadaan standar (STP) b. keadaan kamar (RTP) c. suhu 28 °C dan tekanan 1 atm d. suhu dan tekanan yang sama pada saat 2 mol gas karbon monoksida volumenya 25 liter 6. Berapakah molaritas larutan yang dibuat dengan melarutkan 5,85 gram NaCl (Ar Na= 23, Cl = 35,5) dalam 500 mL air? 7. Hitunglah massa NaOH (Ar Na = 23, O = 16, dan H = 1) yang harus dilarutkan untukmembuat 100 mL larutan NaOH 0,1 M! 8. Tentukan molaritas larutan dari: a. 0,8 mol dalam 250 mL larutan NaCl b. 0,5 mol dalam 1.000 mL larutanKOH 9. Tentukan molaritas larutan yang dibuat dengan melarutkan: a. 50 gram CaCO3 (Ar Ca = 40, C = 12, dan O = 16) dalam 250 mL air b. 11,6 gram Mg(OH)2 (Ar Mg = 24, O = 16, dan H = 1) dalam 2 liter air 10. Berapakah volume air yang dibutuhkan untuk melarutkan 2 mol KOH (Ar K = 39, O = 16, dan H = 1) untuk membuat larutan KOH 0,05 M? 11. Berapakah massa zat terlarut dalam 500 mL larutan Ca(OH)2 0,1 M (Ar Ca = 40, O = 16, dan H = 1)? 12. Berapa jumlah molekul N2yang terdapat dalam 5,6 L gas N2 diukur pada keadaanSTP? Tugas! Buatlah jembatan mol yang menggambarkan hubungan mol dengan jumlah partikel, massa, volume serta kemolaran zat! UJI PEMAHAMAN 1. Suatu senyawa massanya 22 g dan jumlah molnya 0,5 mol.Berapa Mr senyawa itu? 2. Suatu senyawa dengan massa 12 g dan jumlah molekul2,408 × 1023 molekul. Tentukan massa molekul relatif senyawa tersebut! 3. Berapa volume gas X yang diukur pada keadaan standar jika massa gas tersebut 34 g dan massa molar17 g mol–1? 4. Pada suhu dan tekanan sama, berapa volume gasCO2 yang diukur pada keadaan 1 liter gas NO yang massanya 14 g? 5. Diketahui massa atom relatif (Ar) C = 12, N = 14, O = 16, dan H = 1. Tentukan volumestandar (STP) dari: a. 4,4 gram gas CO2 b. 4 mol O2 c. 6,8 gram NH3 d. 1,806 × 1022 molekul H2 6. Diketahui Ar C = 12, N = 14, O = 16, S = 16, H = 1, dan Fe = 56. Tentukan massa dari: a. 4,48 liter gas dinitrogen pentaoksida (STP) b. 5 mol CO(NH2)2 c. 0,6 mol gas SO2 (RTP) d. 6,02 × 1021 atom besi 7. Tentukan jumlah partikel dari: a. 3 mol molekul H2O b. 2 liter gas oksigen pada 27 °C dan tekanan 1 atm c. 3,2 gram O2 (Ar O = 16) d. 40 gram CaCO3 (Ar Ca = 40, C = 12, dan O = 16) e. 6,72 liter gas NO2 (STP) 8. Tentukan molaritas larutan urea (CO(NH2)2) (Ar C = 12, O = 16, N = 14, dan H = 1) yang dibuat dengan melarutkan 24 gram dalam 500 mL air! 9. Pada suhu dan tekanan tertentu (T, P), 4,4 gram CO2 bervolume 10 liter. Pada suhudan tekanan yang sama, tentukan volume dari 19,2 gram gas SO2 (Ar C = 12, O = 16,dan S = 32)! 10. Berapakah volume dari 12,8 gram gas SO2 (Ar S = 32, O = 16) yang diukur pada suhu28 °C dan tekanan 1 atm? 11. Tentukan volume dari 0,5 mol gas CO yang diukur pada suhu 30 °C dan tekanan 1atm! 12. Berapakah massa C6H12O6 yang dibutuhkan untuk membuat 2 liter larutan C6H12O60,05 M (Ar C = 12, H = 1, O = 16)? E. Stoikiometri Senyawa 1) Kadar Unsur dalam Senyawa Dengan mengetahui jenis dan massa dari setiap komponen penyusun zat, kitadapat mengetahui komposisi zat tersebut. Komposisi zat dinyatakan dalam persen massa (% massa) atau disebut juga kadar. Perhitungan persen massa untuk setiap komponen dapat menggunakan persamaan berikut: 𝑃𝑒𝑟𝑠𝑒𝑛 𝑚𝑎𝑠𝑠𝑎 𝑘𝑜𝑚𝑝𝑜𝑛𝑒𝑛 𝑚𝑎𝑠𝑠𝑎 𝑘𝑜𝑚𝑝𝑜𝑛𝑒𝑛 𝑚𝑎𝑠𝑠𝑎 𝑧𝑎𝑡 X 100% Contoh: Seorang ahli kimia melakukan analisis terhadap sampel kimia dan dia menemukan bahwa sampel seberat 65 gram tersebut mengandung 48 gram karbon, 9 gram hidrogen,dan 8 gram oksigen. Nyatakan komposisi zat tersebut dalam persen massa! Penyelesaian: = 73, 85 % Kadar unsur atau komponen penyusun suatu senyawa juga dapat ditentukan melalui rumus kimia senyawanya, yaitu menggunakan massa atom relatif (Ar) unsur dan massa molekul relatif (Mr) senyawanya. Secara umum, untuk menghitung kadar atau persen massa unsur dalam suatu senyawa digunakan persamaan berikut: 𝑘𝑎𝑑𝑎𝑟 𝑈𝑛𝑠𝑢𝑟 𝑎𝑛𝑔𝑘𝑎 𝑖𝑛𝑑𝑒𝑘𝑠 𝑋 𝐴𝑟 𝑢𝑛𝑠𝑢𝑟 𝑋 𝑀𝑟 𝑠𝑒𝑛𝑦𝑎𝑤𝑎 Untuk menentukan massa unsur – unsur penyusun suatu senyawa, dan massa senyawa tersebut diketahui maka dapat digunakan persamaan berikut: 𝑚𝑎𝑠𝑠𝑎 𝑈𝑛𝑠𝑢𝑟 𝑎𝑛𝑔𝑘𝑎 𝑖𝑛𝑑𝑒𝑘𝑠 𝑋 𝐴𝑟 𝑢𝑛𝑠𝑢𝑟 𝑋 𝑚𝑎𝑠𝑠𝑎 𝑠𝑒𝑛𝑦𝑎𝑤𝑎 𝑀𝑟 𝑠𝑒𝑛𝑦𝑎𝑤𝑎 Contoh: Tentukan kadar unsur C, H, dan O dalam senyawa glukosa (C6H12O6)! (Ar C =12, H = 1, dan O = 16)! Penyelesaian: LATIHAN! 1. Satu sampel suatu zat mengandung 2,4 gram karbon, 3,2 gram oksigen, 5,6 gramnitrogen, dan 0,8 gram hidrogen. Nyatakan komposisi zat tersebut dalam persen massa! 2. Tentukan kadar C dan N dalam urea (CO(NH2)2)! (Ar C = 12, O = 16, N = 14, dan H = 1) 3. Berapakah massa oksigen yang diperlukan untuk membuat 500 kg air? (Ar H = 1 dan O = 16) 4. Berapakah massa kalsium yang terdapat dalam 250 kg CaCO3? (Ar Ca = 40, C = 12, dan O = 16) 5. Unsur nitrogen dan oksigen bereaksi, dan dapat membentuk lebih dari satu macam senyawa.Tentukan besarnya persentase unsur nitrogen dan oksigen dalam senyawaNO, NO2, N2O, N2O3, dan N2O5 (Ar N = 14 dan O = 16)! 6. Berapakah massa asam fosfat (H3PO4) yang dibuat dari 6,2 gram fosfat (Ar H = 1, P =31, dan O = 16)? 7. Analisis sampel menunjukkan terdapat 40% kalsium, 12 % karbon, dan 48% oksigen.Jika diketahui massa sample tersebut adalah 25 gram, tentukan massa setiap unsurdalam sampel tersebut! 2) 3) Menentukan Rumus Kimia Zat Rumus kimia menunjukkan jenis atom/unsur dan jumlah relatif masing – masing unsur yang terdapat dalam zat. Jumlah unsur yang terdapat dalam zat ditunjukkan dengan angka indeks. Rumus kimia zat dapat dibedakan menjadi rumus empiris dan rumus molekul. Rumus molekul menyatakan jenis dan jumlah atom – atom dalam satu molekul, sedangkan rumus empiris menyatakan perbandingan paling sederhana dari atom – atom dalam suatu molekul. Contoh: Tabel 1. Contoh Rumus Molekul dan Rumus Empiris Senyawa Senyawa Benzena Glukosa Propena Amonia Rumus Molekul C6H6 C6H12O6 C3H6 NH3 Rumus Empiris CH CH2O CH2 NH3 a. Menentukan Rumus Empiris Rumus empiris merupakan perbandingan paling sederhana dari atom–atom unsur penyusun suatu senyawa. Hal yang penting untuk menentukan rumus empiris suatu senyawa adalah menghitung jumlah mol yaitu perbandingan paling sederhana mol unsur–unsur penyusun senyawa. Contoh: Sebanyak 3 gram senyawa organik mengandung 1,2 gram karbon, 0,2 gram hidrogen dan sisanya adalah oksigen. Tentukan rumus empiris senyawa tersebut, jika diketahui Ar H = 1; C = 12; dan O = 16! Penyelesaian: i) Menentukan jumlah mol masing-masing unsur Jumlah mol C = Jumlah mol H = Jumlah mol O = ii) Menentukan perbandingan mol unsur - unsur Perbandingan mol C : mol H : mol O = 0,1 : 0,2 : 0,1 = 1 : 2 : 1 Sehingga, rumus empiris senyawa tersebut adalah CH2O. LATIHAN! 1. Tentukan rumus empiris dari asam asetat, pentena, propane, urea dan karbon dioksida! 2. Suatu senyawa mengandung 32,4 % natrium; 22,6 % belerang; dan sisanya oksigen(Ar Na = 23, S = 32, dan O =16). Tentukanlah rumus empiris senyawa tersebut! 3. Suatu senyawa nitrogen oksida terdiri dari 7 gram nitrogen dan 12 gram oksigen(Ar N = 14 dan O = 16).Tentukan rumus empiris nitrogen oksida tersebut! 4. Suatu senyawa mengandung 32,4 % natrium; 22,6 % belerang; dan sisanya oksigen(Ar Na = 23, S = 32, dan O =16). Tentukanlah rumus empiris senyawa tersebut! 5. Suatu senyawa mengandung 52,14% C; 13,03% H; dan 34,75% O. (Ar: C=12, H=1,O=16). Tentukan rumus perbandingan senyawa itu! b. Menentukan Rumus Molekul Rumus molekul rumus kimia yang menunjukkan jumlah atom dari masing–masing unsur dalam suatu senyawa. Pada dasarnya rumus molekul merupakan kelipatan-kelipatan dari rumus empirisnya. Sehingga, hubungan rumus empiris (RE) dan rumus molekul (RM) dapat dituliskan sebagai berikut: 𝑅𝑢𝑚𝑢𝑠 𝑒𝑚𝑝𝑖𝑟𝑖𝑠 𝑛 𝑅𝑢𝑚𝑢𝑠 𝑀𝑜𝑙𝑒𝑘𝑢𝑙 Nilai n dapat ditentukan jika rumus empiris dan massa molekul relatif(Mr) zat diketahui. 𝑀𝑟 𝑅𝑢𝑚𝑢𝑠 𝑚𝑜𝑙𝑒𝑘𝑢𝑙 𝑛 𝑥 𝑀𝑟 𝑅𝑢𝑚𝑢𝑠 𝐸𝑚𝑝𝑖𝑟𝑖𝑠 Contoh: Suatu senyawa dengan rumus empiris CH (Ar C = 12 dan H = 1) mempunyai Mr = 26. Tentukan rumus molekul senyawa tersebut! Penyelesaian: Mr = n × (Ar C + Ar H) 26 = n × (12 + 1) 26 = n × 13 n=2 Jadi, rumus molekul senyawa tersebut adalah (CH)2 = C2H2. LATIHAN! 1. Suatu senyawa memiliki rumus empiris C4H9 dan massa molekul relatif 114 g/mol.Tentukan rumus molekul senyawa tersebut! 2. Suatu senyawa memiliki rumus molekul CH3. Jikamolekul tersebut memiliki massa molekul relatif 30.Tentukan rumus molekulnya. 3. Suatu senyawa memiliki komposisi massa sebagaiberikut:54% C; 10% H; dan 36% O. Jika Mr senyawa tersebut 266 g/mol. Tentukan: a. rumus empiris; b. rumus molekul; dan c. massa C, H, dan O jika massa senyawa 28 gram. 4. Suatu hidrokarbon CxHy yang berbentuk gas terdiri dari 80% karbon dan sisanyahidrogen. Tentukan rumus empiris senyawa tersebut. Jika diketahui massa dari 1 litersenyawa itu (STP) adalah 1,34 gram, tentukan rumus molekul senyawa hidrokarbontersebut! 5. Senyawa CxHyOz tersusun dari 40% karbon, 6,67% hidrogen, dan sisanya oksigen.Jika Mr senyawa tersebut adalah 90, tentukan rumus molekul senyawa tersebut! 6. Suatu senyawa organik dengan Mr = 60 tersusun dari 40% karbon; 6,6% hidrogen; dansisanya oksigen (Ar C=12; H = 1; O = 16). Tentukan rumus molekul senyawa tersebut! 7. Senyawa hidrokarbon mengandung 90% C, sisanya H. Tentukan rumusempiris hidrokarbon tersebut, jika Mr hidrokarbon = 40. Bagaimana rumus molekulnya? F. Stoikiometri Reaksi 1) Koefisien Reaksi Koefisien reaksi merupakan perbandingan jumlah partikel dari zat yang terlibat dalam reaksi. Oleh karena 1 mol setiap zat mengandung jumlah partikel yang sama, maka perbandingan jumlah partikel sama dengan perbandingan jumlah mol. Jadi, koefisien reaksi merupakan perbandingan jumlah mol zat yang terlibat dalam reaksi. Dengan pengertian tersebut, maka banyaknya zat yang diperlukan atau dihasilkan dalam reaksi kimia dapat dihitung dengan menggunakan persamaan reaksi setara. Apabila jumlah mol salah satu zat yang bereaksi diketahui, maka jumlah mol zat yang lain dalam reaksi itu dapat ditentukan dengan menggunakan perbandingan koefisien reaksinya. Contoh: Aluminium larut dalam larutan asam sulfat menghasilkan larutan aluminium sulfat dan gas hidrogen. Persamaan reaksinya: 2Al(s) + 3H2SO4(aq) → Al2(SO4)3(aq) + 3H2(g) Berapa mol gas hidrogen dan mol larutan aluminium sulfat yang dihasilkan jika digunakan 0,5 mol aluminium? Penyelesaian: 2Al(s) + 3H2SO4(aq) → Al2(SO4)3(aq) + 3H2(g) 0,5 mol perbandingan koefisien Al : H2SO4 : Al2(SO4)3 : H2 adalah 2 : 3 : 1 : 3 Jumlah mol gas hidrogen = Jumlah mol larutan aluminium sulfat = LATIHAN! 1. 5,6 gram besi (Ar Fe = 56) dilarutkan dalam larutan asam klorida sesuai reaksi:Fe(s) + HCl(aq) → FeCl3(aq) + H2(g) Tentukan volume H2 yang dihasilkan pada keadaan standar (STP)! 2. Sebanyak 32 gram kalsium karbida (CaC2) dilarutkan dalam air menghasilkan gasasetilena (C2H2) menurut reaksi: CaC2(s) + H2O(l) → Ca(OH)2(s) + C2H2(g) Tentukan: a. mol CaC2 b. massa Ca(OH)2 yang dihasilkan c. volume gas asetilena yang dihasilkan pada keadaan standar (Ar Ca = 40, C = 12, O= 16, dan H = 1) 3. Diketahui persamaan reaksi: Mg(s) + HCl(aq) → MgCl2(aq) + H2(g) Jika Mg yang bereaksi adalah 2 mol, hitunglah: a. mol HCl yang bereaksi, b. volum gas H2 yang dihasilkan pada STP. 4. Gas propana C3H8 direaksikan dengan gas oksigen menghasilkan gas karbondioksida dan air. Jika C3H8 yang bereaksi adalah 4,4 gram, pada STP, tentukan: a. volum O2 yang bereaksi, b. volum CO2 yang dihasilkan, c. massa H2O yang dihasilkan. 5. Logam aluminium dapat bereaksi dengan larutan HCl menghasilkan larutan AlCl3 dan gas H2. Berapa gram gas H2 yang terbentuk dan jumlah molekul hidrogen dari 9 gram aluminium? ( Ar Al = 27, H = 1). 6. Pada saat korek api gas dinyalakan, reaksi yang terjadi adalah: C4H10(g) + O2(g) → CO2(g) + H2O(l) Jika pada reaksi itu dihasilkan 88 gram gas CO2, hitunglah massa C4H10 yangbereaksi! ( Ar C = 12, O = 16, H = 1) 2) Menentukan Rumus Kimia Hidrat Hidrat adalah zat padat yang mengikat beberapa molekul air sebagai bagian dari struktur kristalnya. Contoh: 1. Terusi (CuSO4.5 H2O): tembaga(II) sulfat pentahidrat 2. Gipsum (CaSO4.2 H2O): kalsium sulfat dihidrat 3. Garam inggris (MgSO4.7H2O): magnesium sulfat heptahidrat 4. Soda hablur (Na2CO3.10H2O): natrium karbonat dekahidrat Jika suatu senyawa hidrat dipanaskan, maka ada sebagian atau seluruh airkristalnya dapat dilepas (menguap). Jika suatu hidrat dilarutkan dalam air, maka air kristalnya akan lepas. Contoh: CuSO4.5H2O(s) → CuSO4(aq) + 5H2O(l) Gambar 7. CuSO4.5H2O (kiri) dan CuSO4 (kanan) Contoh: Sebanyak 5 gram hidrat dari tembaga(II) sulfat (CuSO4.xH2O) dipanaskan sampai semua air kristalnya menguap. Jika massa padatan tembaga (II) sulfat yang terbentuk adalah 3,2 gram, tentukan rumus hidrat tersebut! (Ar Cu = 63,5, S = 32, O = 16, dan H = 1). Penyelesaian: Massa H2O = 5 gram – 3,2 gram = 1,8 gram Mol CuSO4 = Mol H2O = = = Persamaan reaksi pemanasan CuSO4.xH2O: CuSO4.xH2O(s) → CuSO4(aq) + xH2O(l) 0,02 mol 0,1 mol Perbandingan mol CuSO4 : H2O = 0,02 mol : 0,1 mol = 1 : 5 Karena perbandingan mol = perbandingan koefisien, maka x = 5. Jadi, rumus hidrat tersebut adalah CuSO4.5H2O. LATIHAN! 1. Sebanyak 10 gram hidrat besi (II) sulfat dipanaskan sehingga diperoleh senyawa anhidratnya sebanyak 5,47 gram. Tentukan rumus hidrat senyawa tersebut! 2. 24,0 gram magnesium sulfat anhidrat bergabung dengan 25,2 gram airmembentuk senyawa magnesium sulfat hidrat. Tentukan rumus senyawa hidrattersebut. ( Mr MgSO4 = 120, H2O = 18) 3) Pereaksi Pembatas Di dalam suatu reaksi kimia, perbandingan mol zat-zat pereaksi yangditambahkan tidak selalu sama dengan perbandingan koefisien reaksinya. Halini menyebabkan ada zat pereaksi yang akan habis bereaksi lebih dahulu yang disebut sebagaipereaksi pembatas. Contoh: 1 mol larutan natrium hidroksida direaksikan dengan 1 mol larutan asam sulfat sesuai reaksi: 2NaOH(aq) + H2SO4(aq) → Na2SO4(aq) + 2H2O(l) Tentukan: a. pereaksi pembatas b. pereaksi yang sisa c. mol H2O yang dihasilkan Penyelesaian: 2NaOH(aq) + H2SO4(aq) → Na2SO4(aq) + 2H2O(l) m: 1 mol 1 mol r : 1 mol 0,5 mol 0,5 mol 1 mol s : 0,5 mol 0,5 mol 1 mol a. Pereaksi pembatasnya adalah NaOH b. Pereaksi sisanya adalah H2SO4 c. Mol H2O yang dihasilkan adalah 1 mol. LATIHAN! 1. 100 mL larutan Ca(OH)2 0,1 M direaksikan dengan 100 mL larutan HCl 0,1 M sesuaireaksi: Ca(OH)2(aq) + HCl(aq) → CaCl2(aq) + H2O(l) Tentukan pereaksi pembatas! 2. Perhatikan persamaan reaksi berikut: N2(g) + 3H2(g) → 2NH3(s) Jika 1 mol N2 direaksikan dengan 2 mol H2, tentukan: a. pereaksi pembatas! b. jumlah mol yang tersisa! c. jumlah mol NH3! 3. Di dalam bejana tertutup, 44,8 L gas NH3 direaksikan dengan 89,6 L gas O2 pada STP dengan reaksi: NH3(g) + O2(g) → N2(g) + H2O(g). a. Hitung volum gas N2 yang dihasilkan. b. Hitung volum H2O yang dihasilkan. c. Hitung volum gas yang tersisa. 4. 108 gram aluminium dibakar dengan 160 gram gas oksigen untuk membentuk aluminium oksida, Al2O3. Berapa gram Al2O3 terbentuk dan massa unsur yang tersisa? ( Ar Al = 27, O = 16) 5. 12 gram logam magnesium direaksikan dengan 0,5 mol asam sulfatmenghasilkan magnesium sulfat dan gas hidrogen. Hitung: a. massa magnesium sulfat yang dihasilkan, b. volum gas H2 yang dihasilkan pada STP, c. jumlah mol zat yang tersisa. Uji Kompetensi Bab 5 1. Persentase massa kalsium dalam batu kapur (CaCO3) adalah . . . . (ArCa = 40, C = 12, O =16) a. 12% c. 40% e. 60% b. 16% d. 48% a. Volum 2. 3 gram gas C2H6 pada STP adalah . . . . ( Ar C = 12, H = 1) a. 3,5 liter c.14 liter e. 28 liter b. 7 liter d. 2,24 liter 3. Pada suhu dan tekanan yang sama, 1 L gas berikut yang memiliki massapaling besar adalah . . . .( ArH = 1, C = 12, O = 16, S = 32 , N = 14) a. NH3 d. NO2 b. CO2 e.CH4 c. SO2 4. Jumlah apa yang sama di antara satu mol etanol C2H5OH dengan satu moletana C2H6 ? a. Massa c. Jumlah atom e. Jumlah molekul b. Volum pada STP d. Jumlah ikatan 5. Natrium hidrogen karbonat jika dipanaskan terurai dengan reaksi: 2NaHCO3(s) → Na2CO3(s)+ CO2(g)+ H2O(g). Jika 5 mol sampel NaHCO3dipanaskan, maka volum gas CO2 yang dihasilkan adalah (dik: Volum molar gas= 24 L) . . . . a. 24 L c. 36 L e. 48 L b. 60 L d. 72 L 6. 20 mL gas NH3 bereaksi dengan 20 mL gas oksigen (O2) pada STP dengan reaksi: 4NH3(g)+ 3O2(g) →2N2(g) + 6H2O(l).Volum oksigen yang bereaksiadalah . . . . a. 0 mL c. 5 mL e. 7,5 mL b. 15 mL d. 10 mL 7. Senyawa hidrida XH3 mengandung 90% unsur X. Ar dari X adalah . . . . a. 8 c. 27 e. 30 b. 90 d. 118 8. Reaksi besi(II) sulfida dengan gas oksigen berlangsung menurut reaksi: FeS(s) + O2(g) → Fe2O3(s) + SO2(g) Jikabereaksi 8,8 gram FeS murni (Ar Fe = 56, O= 16, S = 32), gas SO2 yang dihasilkan pada keadaan standar (STP) adalah a. 24,2 liter b. 2,24 liter c. 22,4 liter d. 1,12 liter e. 2,42 liter 9. Suatu senyawa organik terdiri dari 40% C, 6,67% H, dan sisanya oksigen. JikaAr C = 12, H = 1, O = 16 dan massa molekul senyawa tersebut 60, maka rumus molekul senyawa tersebut adalah … . a. CH4O c. C2H5OH e. CH3COH b. CH2O d. CH3COOH 10. Pada suhu dan tekanan yang sama, semua gas yang memiliki volume yang sama akan memiliki jumlah partikel yang sama. Pernyataan tersebut dikenal dengan hukum . . . . a. Gay Lussac c. Dalton e. Lavoisier b. Avogadro d. Proust 11. Jika dalam 8 liter gas CO2 (P, T) terdapat 6,02 × 1022 molekul gas tersebut, makapada suhu dan tekanan yang sama, 1,505 × 1021 molekul gas NO2 akan menempatiruang yang volumenya . . . . a. 0,2 liter c. 8 liter e. 20 liter b. 2 liter d. 16 liter 12. Massa yang terkandung dalam 3 mol urea (CO(NH2)2) (Ar C = 12, O = 16, N =14, dan H = 1) adalah . . . . a. 60 gram c. 150 gram e. 240 gram b. 120 gram d. 180 gram 13. Untuk membuat 500 mL larutan NaOH dengan konsentrasi 0,2 M diperlukan NaOH (Ar Na = 23, O = 16, dan H = 1) sebanyak . . . . a. 2 gram b. 10 gram c. 4 gram d. 16 gram e. 8 gram 14. Diketahui reaksi: Mg(s) + CuSO4(aq) → MgSO4(aq) + Cu(s) Bila 6 gram magnesium tepat habis bereaksi dengan larutan CuSO4 (Ar Mg = 24,Cu = 63,5), maka dihasilkan tembaga sebanyak ... . a. 7,94 gram c. 15,88 gram e. 31,75 gram b. 48 gram d. 63,5 gram 15.Berdasarkan reaksi: Pb(NO3)2(aq) + 2KI(aq) → PbI2(s) + 2KNO3(aq) bila 30 mL larutan Pb(NO3)2 0,1 M direaksikan dengan 20 mL larutan KI 0,4 M, maka massa endapan PbI2 (Ar Pb = 207, I = 127) yang terbentuk adalah ... a. 0,692 gram c. 1,383 gram e. 1,844 gram b. 2,766 gram d. 3,688 gram 16. Dalam kompor gas, 5 mol propana dibakar dengan 5mol gas oksigen menghasilkan CO2(g) sebanyak .... a. 3 mol b. 5 mol c. 10 mol d. 15 mol e. 30 17. Volume 0,5 mol gas oksigen yang diukur pada 25°Cdan 1 atm adalah .... a. 11,2 liter c. 24,44 liter b. 22,4 liter d. 28,25 liter e. 30,00 liter mol 18. Unsur-unsur yang membentuk dua atau lebih senyawaharus merupakan kelipatan bilangan bulat dansederhana. Pernyataan ini dikenal dengan Hukum a Lavoisier c Dalton e Gay–Lussac b Proust d Avogadro 19. Jika x mL gas H2 direaksikan dengan 3x mL gas Cl2maka gas HCl yang dibentuk sebanyak .... a. x mL b. 2x mL c. 3x mL d. 4x mL e. 3x2 mL 20. Volume O2 yang dibutuhkan untuk pembakarancampuran 5 liter CH4 dan 5 liter C2H4adalah . . . . a. 5 liter b. 20 liter c. 10 liter d. 25 liter 21. Hukum perbandingan tetap dikemukakan oleh . . . . a. Avogadro c. Dalton b. Proust d. Newton e. 15 liter e. Lavoisier 22. Pernyataan di bawah ini yang dikemukakan oleh Gay Lussac adalah . . . . a. energi tidak dapat diciptakan dan tidak dapat dimusnahkan b. massa zat sebelum dan sesudah reaksi adalah tetap c. perbandingan massa unsur-unsur dalam senyawa selalu tetap d. volume gas-gas yang bereaksi dan volume gas-gas hasil reaksi pada T dan Psama berbanding sebagai bilangan bulat dan sederhana e. pada T dan P sama, semua gas bervolume sama mengandung jumlah molekulyang sama 23. Pada suhu dan tekanan tertentu, m molekul H2S bervolume 0,25 liter. Pada suhudan tekanan yang sama, volume dari 4m molekul NH3 adalah . . . . a. 0,25 liter c. 0,5 liter e. 1 liter b. 1,5 liter d. 2 liter 24. Pada suhu dan tekanan tertentu, 2 liter gas nitrogen mengandung n molekul gasnitrogen. Pada suhu dan tekanan yang sama, jumlah molekul gas oksigen yang volumenya 10 liter adalah . . . . a. n molekul gas oksigen e. 5n molekul gas oksigen b. 2n molekul gas oksigen c. 3n molekul gas oksigen d. 4n molekul gas oksigen 25. Gas hidrokarbon (CxHy) bervolume 3 liter tepat dibakar sempurna dengan 18liter oksigen menghasilkan 12 liter gas karbon dioksida sesuai reaksi: CxHy+ O2 → CO2 + H2O (belum setara)Rumus molekul hidrokarbon tersebut adalah . . . . a. C5H12 b. C4H8 c. C5H10 d. C3H8 e. C4H6 26. Sebanyak 6 liter campuran gas metana (CH4) dan gas etana (C2H6) dapat dibakarsempurna dengan 19 liter gas oksigen pada suhu dan tekanan yang sama.Persamaan reaksinya: CH4 + 3O2 → CO2 + 2H2O 2C2H6 + 7O2→ 4CO2 + 6H2O Volume gas CH4 dan C2H6 berturut-turut adalah . . . . liter. a. 1 dan 5 b. 2 dan 4 c. 5 dan 1 d. 2 dan 3 e. 4 dan 2 27. Suatu campuran terdiri dari 60% volume gas N2 dan 40% volume gas O2.Perbandingan molekul gas N2 dan O2 dalam campuran itu adalah . . . . a. 3 : 2 b. 16 : 21 c. 4 : 3 d. 2 : 3 e. 21 : 16 28. Pada suhu dan tekanan tertentu, 10 liter gas NO bereaksi dengan 5 liter gas O2,sehingga menghasilkan 10 liter gas NxOypada suhu dan tekanan yang sama.Rumus molekul senyawa NxOyadalah . . . . a. NO2 b. N2O5 c. N2O4 d. N2O e. N2O3 29. Pada suhu 25 °C dan tekanan 1 atm diketahui kadar oksigen dalam udara adalah20%. Reaksi pembakaran karbon:C + O2 → CO2 Pada pembakaran karbon dengan 100 liter udara dihasilkan gas karbon dioksida sebanyak . . . a. 10 liter b. 80 liter c. 20 liter d. 100 liter e. 50 liter 30. Logam aluminium yang dapat dihasilkan dari 10.000 kg bauksit murni menurutreaksi: 2Al2O3(s) → 4Al(s) + 3O2(g)(Ar Al = 27 dan O = 16) adalah . . . . a. 8 000 kg c. 6.600 kg e. 5.300 kg b. 4.700 kg d. 1.900 kg 31. Sebanyak 11,2 gram serbuk besi (Fe) dipanaskan secara sempurna dengan 6,4gram serbuk belerang (S), sesuai reaksi:Fe + S → FeS Senyawa besi(II) sulfida (FeS) yang terbentuk sebanyak . . . . a. 6,4 g b. 17,6 g c. 11,2 g d. 22,4 g e. 12,8 g 32. Perbandingan massa magnesium dengan massa oksigen dalam senyawa magnesiumoksida adalah 3 : 2. Jika 12 gram magnesium direaksikan dengan 6 gramoksigen, maka massa magnesium oksida (MgO) yang terbentuk adalah . . . . a. 6 g21 g b. 10 g c. 30 g d. 15 g 33. Diketahui data percobaan pembentukan senyawa pirit sebagai berikut. Massa Besi (Fe) Massa Belerang (S) Massa pirit (FeS) 7 gram 8 gram 15 gram 14 gram 16 grm 40 gram 21 gram 24 gram 45 gram Perbandingan Fe : S adalah … . a. 1 : 2 b. 5 : 8 c. 2 : 3 d. 7 : 8 e. 4 : 3 34. Satu liter campuran gas terdiri dari 60% volume metana (CH4) dan sisanya gasetana (C2H6) dibakar sempurna sesuai reaksi: CH4 + 3O2 → 2CO2 + 2H2O 2C2H6 + 7O2 → 4CO2 + 6H2O Volume gas oksigen yang dibutuhkan adalah . . . . a. 2,4 l b. 3,0 l c. 2,6 l d. 3,2 l e. 2,8 l 35. Jika diketahui massa atom relatif H = 1, S = 32, O = 16 dan massa molekulrelatif (NH 4)2SO4 = 132, maka massa atom relatif N adalah … . a. 7 b. 20 c. 12 d. 28 e. 14 36. Diketahui Ar C = 12, O = 16, Na = 23, dan S = 32. Gas-gas berikut ini mempunyaimassa 32 gram, kecuali . . . . a. 0,4 mol SO3 c. 2 mol CH4 e. 0,5 mol SO2 b. 0,5 mol C4H10 d. 1 mol O2 37. Jumlah mol dari 29,8 gram amonium fosfat ((NH4)3PO4) (Ar N = 14, H = 1, dan P = 31) adalah . . . . a. 0,05 mol c. 0,15 mol e. b. 0,25 mol d. 1,10 mol f. 0,20 mol 38. Jika diketahui Ar Ca = 40, C = 12, O = 16 dan bilangan Avogadro = 6,02×1023,maka 50 gram CaCO3mempunyai jumlah molekul . . . . a. 3,01 × 1021 c. 6,02 × 1022 e. 1,204 × 1023 b. 3,01 × 1022 d. 3,10 × 1023 39. Pada senyawa K2Cr2O7 (Ar K = 39, Cr = 52, O = 16), kadar oksigen adalah a. 12% b. 42% c. 28% d. 62% 40. Dalam 1.500 kg urea (CO(NH2)2) terkandung unsur nitrogen sebesar . . . . a. 250 kg c. 300 kg b. 650 kg d. 700 kg e. 38% e. 500 kg 41. Sebanyak 305 kg pupuk ZA ((NH4)2SO4) (Ar N = 14, H = 1, S = 32, dan O = 16)disebar secara merata pada sawah seluas 1 hektar (10.000 m2). Massa nitrogenyang diperoleh setiap 10 m2tanah adalah . . . . a. 35 gram c. 65 gram e. 105 gram b. 140 gram d. 210 gram 42. Dalam 100 gram pupuk urea (CO(NH2)2) terdapat 22,4 gram nitrogen (Ar C = 12,O = 16, N = 14, H = 1). Kadar nitrogen dalam pupuk urea tersebut adalah . . . . a. 96% c. 48% e. 44,8% b. 23,3% d. 22,4% 43. Suatu senyawa mempunyai rumus empiris (CH2O)n dengan massa molekul relatif180 (Ar C = 12, H = 1, dan O = 16). Rumus molekul senyawa tersebut adalah . . . . a. CH2O c. C2H2O2 e. C3H6O3 b. C4H6O4 d. C6H12O6 44. Suatu senyawa hidrokarbon mempunyai rumus empiris CH2 (Ar C = 12 danH = 1). Jika 5,6 liter (STP) gas tersebut mempunyai massa 14 gram, maka rumus molekul gas tersebut adalah . . . . a. C2H4 b. C4H8 c. C2H6 d. C5H10 e. C3H8 45. Suatu senyawa oksida nitrogen NxOymengandung 63,16% nitrogen dan 36,84%oksigen (Ar N = 14 dan O = 16). Senyawa tersebut adalah . . . . a. NO b. N2O3 c. N2O d. N2O5 e. NO2 46. Sebanyak 0,37 gram senyawa organik CxHyOz(Ar C = 12, H = 1, dan O = 16)dibakar sempurna menghasilkan 0,88 gram CO2 dan 0,45 gram H2O sesuai reaksi:CxHyOz+ O2 → CO2 + H2O (belum setara) Rumus kimia senyawa organik tersebut adalah . . . . a. CH3OH c. C2H5OH e. C3H7OH b. C4H9OH d. CH3COOH 47. Pada kristalisasi 3,19 gram tembaga(II) sulfat (CuSO4) terbentuk 4,99 gram hidratCuSO4.xH2O (Ar Cu = 63,5, S = 32, O = 16, dan H = 1). Harga x adalah . . . . . a. 3 b. 6 c. 4 d. 7 e. 5 48. Apabila kristal BaCl2.x H2O (Ar Ba = 137, Cl = 35,5, H = 1, dan O = 16)mengandung 14,75% air kristal, maka rumus yang tepat untuk kristal tersebut adalah . . . . a. BaCl2.H2O b. BaCl2.4H2O c. BaCl2.2H2O d. BaCl2.5H2O e. BaCl2.3H2O 49. Pada pembakaran sempurna 6 gram C2H6 (Ar C = 12 dan O = 16) sesuai reaksi:2C2H6(g) + 7O2(g) → 4CO2(g) + 6H2O(l)gas CO2 yang dihasilkan pada keadaan standar (STP) adalah . . . . a. 2,24 liter b. 8,96 liter c. 4,48 liter d. 11,2 liter 50. 6,72 liter Reduksi besi(III) oksida dengan CO menghasilkan besi sesuai reaksi: Fe2O3+ 3CO → 2Fe + 3CO2Untuk menghasilkan 11,2 kg besi dibutuhkan Fe2O3 (Ar Fe = 56 dan O = 16) sebanyak . . a. 22 kg c. 20 kg e.18 kg b. 16 kg d. 15 kg GLOSARIUM Stoikiometri : Rumus Empiris : Rumus Kimia : Rumus Molekul : Pengukuran hubungan antara banyaknya reaksi dan hasil reaksi dari perubahan kimia yang ditunjukkan oleh persamaan reaksi kimia dalam rumus hanya ditunjuk macam–macam atom dan jumlah (relative)-nya tanpa ditunjuk pengugusan gabungan lambang kimia untuk menyatakan susunan molekul, senyawa, atau campuran rumus senyawa kimia yang mengandung lambing atom–atom atau radikal yang ada, yang diikuti dengan angka bawah yang menyatakan jumlah setiap jenis atom atau radikal dalam molekul. DAFTAR PUSTAKA Anderton, J. D., et al. (1996). Foundations Chemistry Second Edition. Australia: Longman. Brady, J. E. (1999). Kimia Universitas Asas dan Struktur Jilid 1 Edisi ke 5. Jakarta: Binarupa Aksara Briggs, J. G. R. 1998. For GCE O – Level. Singapore. Longman. Day, R. A. dan Underwood, A. L. (1992). Analisis Kimia Kuantitatif. Jakarta: Erlangga. Pujaatmaka, H. A. (1989). Kimia Universitas Azas dan Struktur Edisi ke-5. Jakarta: Erlangga Utami, Budi, dkk. (2009). Kimia 1untuk SMA/Ma Kelas X. Jakarta: Pusat Perbukuan Departemen Pendidikan Nasional 22 | m o d u l k i m i a k e l a s X STOIKIOMETRI 23 | m o d u l k i m i a k e l a s X STOIKIOMETRI